鲁教版化学九年级上册 5.2化学反应的表示 课后练习(含解析)
文档属性
| 名称 | 鲁教版化学九年级上册 5.2化学反应的表示 课后练习(含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 96.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-12-01 00:00:00 | ||
图片预览




文档简介
5.2 化学反应的表示
一、单选题(本大题共12小题,共24.0分)
1.下列关于2CO+O22CO2的说法中,不正确的是
A.表示一氧化碳与氧气在点燃条件下反应生成二氧化碳
B.反应前后碳元素的化合价不同
C.反应前后分子和原子的个数均不变
D.参加反应的氧气与生成的二氧化碳的分子个数比为1:2
2.通过化学方程式Fe + 2HCl = FeCl2 + H2↑,不能得出的结论是
A.该反应中的反应物和生成物 B.化学反应的快慢
C.反应发生所需的条件 D.各反应物和生成物的质量比
3.根据化学方程式不能获得该反应的信息是
A.反应物的种类 B.生成物的状态
C.化学反应的快慢 D.反应的条件
4.等质量的碳、镁,铁分别在足量的氧气中充分燃烧,消耗氧气的质量最多的是
A.碳 B.镁 C.铁 D.无法确定
5.下列关于化学方程式C+O2CO2的叙述中,正确的是
A.碳加氧气生成二氧化碳
B.碳在氧气中充分燃烧生成二氧化碳
C.12g碳加32g氧气等于44g二氧化碳
D.1个碳原子与2个氧原子反应生成1个二氧化碳分子
6.镁在空气中燃烧的化学方程式正确的是
A. B.
C. D.
7.下列关于化学方程式4P+5O2 2P2O5的读法,错误的是( )
A.磷和氧气在点燃的条件下反应生成五氧化二磷
B.在点燃的条件下,每4体积的磷和5体积的氧气完全反应,生成五氧化二磷
C.在点燃的条件下,每4个磷原子和5个氧气分子结合生成2个五氧化二磷分子
D.在点燃的条件下,每124份质量的磷和160份质量的氧气完全反应,生成284份质量的五氧化二磷
8.容器中物质X(用□表示)和物质Y(用○表示)的反应微粒之间的关系如下图所示,该反应的化学方程式表示为( )
A.3X+8Y=X3Y8
B.X+2Y=XY2
C.3X+6Y= X3Y6
D.3X+8Y=3XY2+2Y
9.将A、B、C三种物质各16g 混合加热,充分反应后混合物中有12g A、27g C和一定质量的D,已知B完全反应.若A、B、C、D的相对分子质量分别为16、32、44、18,则该反应的化学方程式可表示为
A.2A+B=C+2D B.A+2B=C+2D C.2A+B=2C+D D.A+B=C+D
10.对于方程式的下列说法正确的是
A.铝加氧气等于氧化铝
B.铝和氧气在点燃条件下反应生成氧化铝
C.4个铝原子加3个氧分子等于2个氧化铝分子
D.4份质量的铝和3份质量氧气反应生成2份质量的氧化铝
11.配平化学方程式时,所配化学计量数是否正确的依据是等号两边( )
A.化学式前化学计量数之和是否相等 B.各种元素的种类是否相同
C.各种物质的状态是否相同 D.各种元素的原子个数是否相等
12.下列化学方程式书写正确的是
A.氧化汞加热分解:HgOHg+O2↑
B.铁丝在氧气中燃烧:3Fe+2O2Fe3O4
C.铝和氧气反应生成氧化铝:2Al+O2=2AlO
D.碳在氧气中燃烧:C+O2=CO2
二、填空题(本大题共4小题,共32.0分)
13.某工厂废气中可能含有CO、CO2、N2中的一种或几种。为确定废气成分,同学们按如下流程进行实验。
(1)①中澄清石灰水变浑浊,写出该反应的化学方程式______
(2)将气体A通入浓NaOH溶液以除去CO2,其目的是______
(3)③中澄清石灰水变浑浊。请写出②中发生反应的化学方程式______
(4)原废气中一定含有的气体是______
(5)应将气体D进行如下处理(填序号)______
A 将气体D充分燃烧 B 将气体D直接排放到空气中 C 将气体D收集后再处理
14.如图是某反应的微观示意图,该反应化学方程式为______;生成物的质量比为______。
有限的元素可组成种类繁多的物质,请依据表中元素回答下列问题:
元素名称 氢 碳 氧 硫 铜
元素符号 H C O S Cu
(1)铜元素通常有+1、+2价,与氧元素可组成的物质有__15__、__16__(用化学式表示)。
(2)写出一个化合反应的化学方程式___17___。
(3)甲、乙、丙是初中常见物质,也是由上表中的一种或两种元素组成的。已知甲、丙的组成元素相同,丙是一种最常见的液体。甲、乙、丙存在如图所示的关系,“→”表示转化关系。
①丙是___18___(填名称)。
②写出甲转化成乙和丙的化学方程式___19___。
③写出丙转化成乙的化学方程式___20___。
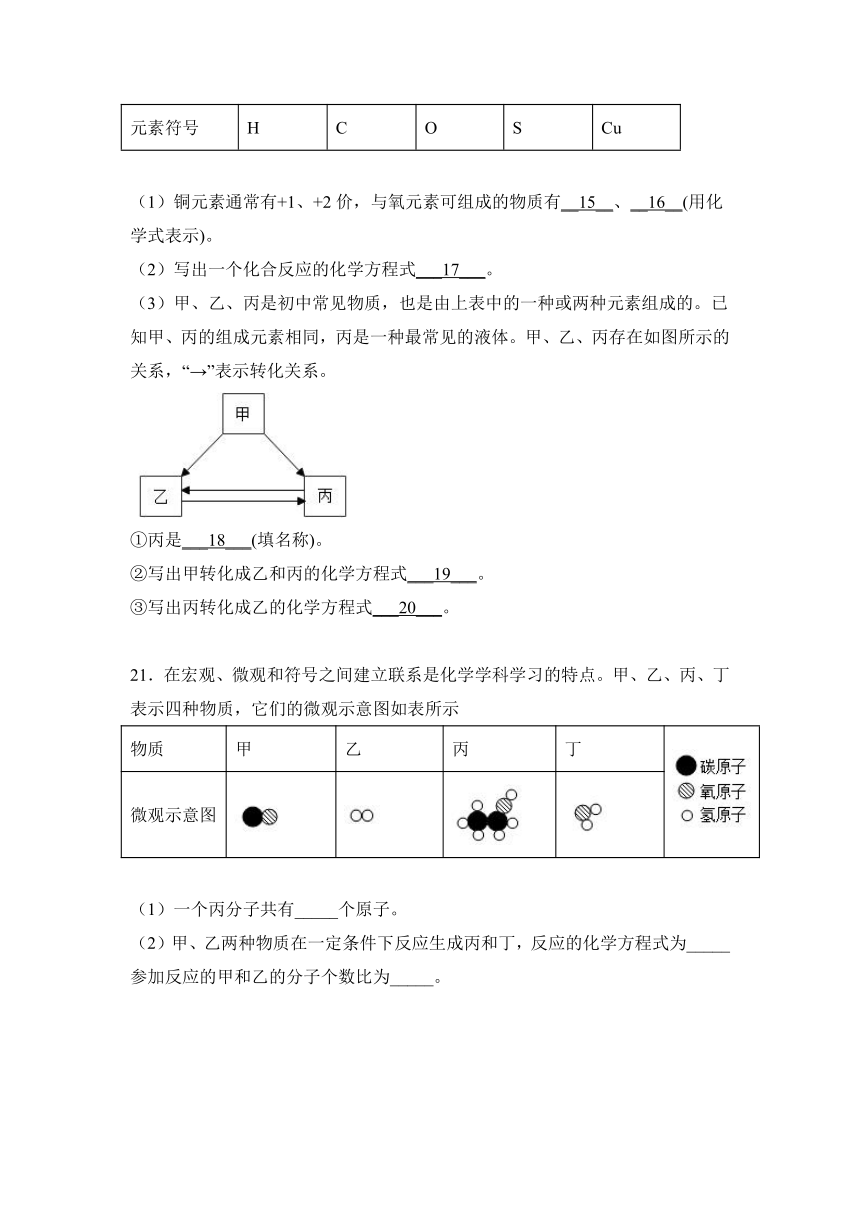
21.在宏观、微观和符号之间建立联系是化学学科学习的特点。甲、乙、丙、丁表示四种物质,它们的微观示意图如表所示
物质 甲 乙 丙 丁
微观示意图
(1)一个丙分子共有_____个原子。
(2)甲、乙两种物质在一定条件下反应生成丙和丁,反应的化学方程式为_____参加反应的甲和乙的分子个数比为_____。
参考答案
1.C
【详解】A. 从宏观的角度,该反应可读作:一氧化碳与氧气在点燃条件下反应生成二氧化碳,选项正确;
B. 反应前CO中碳元素的化合价为+2价,反应后CO2中碳元素的化合价为+4价,反应前后碳元素的化合价不同,选项正确;
C. 由化学方程式可知,反应前后分子的个数发生变化,原子的个数不变,选项错误;
D. 由化学方程式可知,参加反应的氧气与生成的二氧化碳的分子个数比为1:2,选项正确,故选C。
2.B
【详解】A.化学方程式Fe + 2HCl = FeCl2 + H2↑,可得出反应物是铁和稀盐酸,生成物是氯化亚铁和氢气,说法正确,不符合题意;
B.化学方程式Fe + 2HCl = FeCl2 + H2↑,无法确定化学反应的快慢,说法错误,不符合题意;
C.化学方程式Fe + 2HCl = FeCl2 + H2↑,可得出反应所需的条件是常温常压,说法正确,不符合题意;
D.通过化学方程式Fe + 2HCl = FeCl2 + H2↑,可得出每有56份质量的铁和73份质量的盐酸完全反应生成127份质量的氯化亚铁和2份质量的氢气,说法正确,不符合题意;
故选:B。
3.C
【详解】从化学方程式获得的信息主要有:反应物的种类、生成物的状态、反应条件、各物质间质量的关系,无法确定化学反应速率的快慢。
故选:C。
4.A
【详解】由于、、,即消耗32g氧气时,分别需要C、Mg、Fe的质量为12g、48g、,则等质量的碳、镁、铁燃烧,消耗氧气最多的是碳,故选A。
5.B
【详解】 A.碳和氧气在点燃条件下生成二氧化碳,A不正确;
B.碳在氧气中充分燃烧生成二氧化碳,B正确;
C.每12粉质量的碳和32份质量的氧气完全反应。生成44份质量的二氧化碳,C不正确;
D.每1个碳原子与1个氧分子反应生成1个二氧化碳分子,D不正确。
综上所述:选择B。
6.A
【详解】A.该化学方程式书写完全正确,故选项正确;
B.镁与氧气点燃生成氧化镁,正确的化学方程式应为,故选项错误;
C.氧气是反应物,不需要加气体符号,正确的化学方程式应为,故选项错误;
D.该化学方程式氧化镁的化学式书写错误,正确的化学方程式应为,故选项错误。
7.B
【详解】A.磷和氧气在点燃的条件下反应生成五氧化二磷,正确;
B.化学式前的计量数表示参加反应的微粒个数比,错误;
C.在点燃的条件下,每4个磷原子和5个氧气分子结合生成2个五氧化二磷分子,正确;
D.在点燃的条件下,每124份质量的磷和160份质量的氧气完全反应,生成284份质量的五氧化二磷,正确。
故选B。
8.B
【详解】根据反应容器中物质X和物质Y的反应微粒之间的关系图,图中的3个X物质的微粒全部参加反应,而8个物质Y的微粒有2个剩余未参加反应,反应生成的三个分子都是由1个X与2个Y构成的XY2型分子,因此该反应可表示为:X+2Y=XY2。故选B。
9.B
【详解】根据质量守恒定律,化学反应前后,物质的总质量不变,D的质量为:(16×3)-(12+27)=9g;
在此反应中,A质量减少16g-12g=4g;B完全反应,参加反应的质量为16g,C质量增加27g-16g=11g,D是生成的新物质,质量为9g。根据反应的数据可知,A、B为反应物,C、D为生成物.因为A、B的质量比为:4g:16g=1:4,它们的相对分子质量比为16:32=1:2,故B的系数应为2;C、D的质量比为:11g:9g=11:9,它们的相对分子质量比为:44:18=22:9,故D的系数应为2;故可判断反应的化学方程式为A+2B=C+2D。
故选B。
10.B
【详解】A.铝跟氧气在点燃的条件下,反应生成氧化铝,读化学方程式时,“+”和“=”应该读作“和”“生成”,而不能读铝加氧气点燃等于氧化铝,说法错误;
B.铝跟氧气在点燃的条件下,反应生成氧化铝,读化学方程式时,“+”和“=”应该读作“和”“生成”,说法正确;
C.由可知,4个铝原子和3个氧分子反应生成2个氧化铝分子,说法错误;
D.由可知,108份质量的铝和96份质量的氧气生成204份质量的氧化铝,说法错误。
故选:B。
11.D
【详解】由质量守恒定律,反应前后,原子种类、数目均不变,配平的实质是化学方程式两边的化学式前配上适当的化学计量数,使化学方程式两边各元素的原子总数相等。故选D。
【点睛】掌握化学反应前后各原子的数目不变、化学方程式的配平依据即可正确解答本题。
12.B
【详解】A.该方程式没有配平,正确的化学方程式为,故错误;
B.该化学方程式书写完全正确;
C.氧化铝的化学式书写错误,正确的化学方程式为,故错误;
D.该化学方程式缺少反应条件,正确的化学方程式为,故错误。
故选:B。
13. CO2+Ca(OH)2=CaCO3↓+H2O 以防干扰后面的实验 CuO+COCu+CO2 CO C
【分析】废气通入澄清石灰水,检验二氧化碳是否存在;若存在,利用氢氧化钠除去混合气体中的二氧化碳,以防干扰后面验证是否含有CO,因为CO还原氧化铜后也会产生二氧化碳气体,CO还原氧化铜后有CO2气体生成,CO还原氧化铜后的尾气CO有毒,不能直接排放于空气中,以防污染空气。
【详解】(1)二氧化碳能使澄清石灰水变浑浊的特性来检验二氧化碳的存在,其反应方程式为:CO2+Ca(OH)2═CaCO3↓+H2O。
(2)将气体A通入浓NaOH溶液以除去CO2,其目的是以防干扰后面的实验;
(3)若③中澄清石灰水变浑浊,则说明反应②中有二氧化碳气体产生,实验混合气体中含有CO,则CO与CuO反应的化学方程式为:CuO+COCu+CO2。
(4)由(1)、(2)、(3)可知,混合气体中一定含有CO气体。
(5)气体D是CO,有毒,需要将气体D收集后再处理。故选C。
14. 2CO+2NON2+2CO2 7:22
【详解】由微观示意图可知,该反应是一氧化碳和一氧化氮反应生成了氮气和二氧化碳,反应的方程式为:2CO+2NON2+2CO2;生成物的质量比为28:(44×2)=7:22。
15.Cu2O
16.CuO
17.
18.水
19.
20.
【解析】15.铜元素通常有+1、+2价,由正负化合价代数和为零可知,与氧元素可组成的物质有Cu2O、CuO;
16.铜元素通常有+1、+2价,由正负化合价代数和为零可知,与氧元素可组成的物质有Cu2O、CuO;
17.氢气与氧气在点燃条件下生成水,该反应是由两种物质生成一种物质的反应,属于化合反应,化学方程式为;
18.甲、乙、丙是初中常见物质,也是由上表中的一种或两种元素组成的。已知甲、丙的组成元素相同,丙是一种最常见的液体,丙是水,则甲是过氧化氢,过氧化氢在催化剂二氧化锰作用下生成水和氧气,则乙是氧气,氧气与水能相互转化,氢气在氧气中燃烧生成水,水在通电条件下生成氢气和氧气;代入框图进行验证,推断正确,故①丙是水;
19.甲、乙、丙是初中常见物质,也是由上表中的一种或两种元素组成的。已知甲、丙的组成元素相同,丙是一种最常见的液体,丙是水,则甲是过氧化氢,过氧化氢在催化剂二氧化锰作用下生成水和氧气,则乙是氧气,氧气与水能相互转化,氢气在氧气中燃烧生成水,水在通电条件下生成氢气和氧气;代入框图进行验证,推断正确,故②甲是过氧化氢溶液,转化成乙是氧气和丙是水的化学方程式为:;
20.甲、乙、丙是初中常见物质,也是由上表中的一种或两种元素组成的。已知甲、丙的组成元素相同,丙是一种最常见的液体,丙是水,则甲是过氧化氢,过氧化氢在催化剂二氧化锰作用下生成水和氧气,则乙是氧气,氧气与水能相互转化,氢气在氧气中燃烧生成水,水在通电条件下生成氢气和氧气;代入框图进行验证,推断正确,故③丙(水)转化成乙(氧气)的化学方程式为:。
21. 9 2CO+4H2C2H5OH+H2O 1:2
【详解】(1)由微粒的构成可知,一个丙分子是由9个原子构成的;
(2)由题意可知,一氧化碳和氢气在一定条件下反应生成了乙醇和水,反应的化学方程式是:2CO+4H2C2H5OH+H2O,由方程式可知,参加反应的甲和乙的分子个数比为2:4=1:2。
【点睛】根据变化微观示意图及粒子构成模拟图,根据分子由原子构成等特点,正确判断变化中的物质构成与粒子个数关系,是解答本题的基本方法。
一、单选题(本大题共12小题,共24.0分)
1.下列关于2CO+O22CO2的说法中,不正确的是
A.表示一氧化碳与氧气在点燃条件下反应生成二氧化碳
B.反应前后碳元素的化合价不同
C.反应前后分子和原子的个数均不变
D.参加反应的氧气与生成的二氧化碳的分子个数比为1:2
2.通过化学方程式Fe + 2HCl = FeCl2 + H2↑,不能得出的结论是
A.该反应中的反应物和生成物 B.化学反应的快慢
C.反应发生所需的条件 D.各反应物和生成物的质量比
3.根据化学方程式不能获得该反应的信息是
A.反应物的种类 B.生成物的状态
C.化学反应的快慢 D.反应的条件
4.等质量的碳、镁,铁分别在足量的氧气中充分燃烧,消耗氧气的质量最多的是
A.碳 B.镁 C.铁 D.无法确定
5.下列关于化学方程式C+O2CO2的叙述中,正确的是
A.碳加氧气生成二氧化碳
B.碳在氧气中充分燃烧生成二氧化碳
C.12g碳加32g氧气等于44g二氧化碳
D.1个碳原子与2个氧原子反应生成1个二氧化碳分子
6.镁在空气中燃烧的化学方程式正确的是
A. B.
C. D.
7.下列关于化学方程式4P+5O2 2P2O5的读法,错误的是( )
A.磷和氧气在点燃的条件下反应生成五氧化二磷
B.在点燃的条件下,每4体积的磷和5体积的氧气完全反应,生成五氧化二磷
C.在点燃的条件下,每4个磷原子和5个氧气分子结合生成2个五氧化二磷分子
D.在点燃的条件下,每124份质量的磷和160份质量的氧气完全反应,生成284份质量的五氧化二磷
8.容器中物质X(用□表示)和物质Y(用○表示)的反应微粒之间的关系如下图所示,该反应的化学方程式表示为( )
A.3X+8Y=X3Y8
B.X+2Y=XY2
C.3X+6Y= X3Y6
D.3X+8Y=3XY2+2Y
9.将A、B、C三种物质各16g 混合加热,充分反应后混合物中有12g A、27g C和一定质量的D,已知B完全反应.若A、B、C、D的相对分子质量分别为16、32、44、18,则该反应的化学方程式可表示为
A.2A+B=C+2D B.A+2B=C+2D C.2A+B=2C+D D.A+B=C+D
10.对于方程式的下列说法正确的是
A.铝加氧气等于氧化铝
B.铝和氧气在点燃条件下反应生成氧化铝
C.4个铝原子加3个氧分子等于2个氧化铝分子
D.4份质量的铝和3份质量氧气反应生成2份质量的氧化铝
11.配平化学方程式时,所配化学计量数是否正确的依据是等号两边( )
A.化学式前化学计量数之和是否相等 B.各种元素的种类是否相同
C.各种物质的状态是否相同 D.各种元素的原子个数是否相等
12.下列化学方程式书写正确的是
A.氧化汞加热分解:HgOHg+O2↑
B.铁丝在氧气中燃烧:3Fe+2O2Fe3O4
C.铝和氧气反应生成氧化铝:2Al+O2=2AlO
D.碳在氧气中燃烧:C+O2=CO2
二、填空题(本大题共4小题,共32.0分)
13.某工厂废气中可能含有CO、CO2、N2中的一种或几种。为确定废气成分,同学们按如下流程进行实验。
(1)①中澄清石灰水变浑浊,写出该反应的化学方程式______
(2)将气体A通入浓NaOH溶液以除去CO2,其目的是______
(3)③中澄清石灰水变浑浊。请写出②中发生反应的化学方程式______
(4)原废气中一定含有的气体是______
(5)应将气体D进行如下处理(填序号)______
A 将气体D充分燃烧 B 将气体D直接排放到空气中 C 将气体D收集后再处理
14.如图是某反应的微观示意图,该反应化学方程式为______;生成物的质量比为______。
有限的元素可组成种类繁多的物质,请依据表中元素回答下列问题:
元素名称 氢 碳 氧 硫 铜
元素符号 H C O S Cu
(1)铜元素通常有+1、+2价,与氧元素可组成的物质有__15__、__16__(用化学式表示)。
(2)写出一个化合反应的化学方程式___17___。
(3)甲、乙、丙是初中常见物质,也是由上表中的一种或两种元素组成的。已知甲、丙的组成元素相同,丙是一种最常见的液体。甲、乙、丙存在如图所示的关系,“→”表示转化关系。
①丙是___18___(填名称)。
②写出甲转化成乙和丙的化学方程式___19___。
③写出丙转化成乙的化学方程式___20___。
21.在宏观、微观和符号之间建立联系是化学学科学习的特点。甲、乙、丙、丁表示四种物质,它们的微观示意图如表所示
物质 甲 乙 丙 丁
微观示意图
(1)一个丙分子共有_____个原子。
(2)甲、乙两种物质在一定条件下反应生成丙和丁,反应的化学方程式为_____参加反应的甲和乙的分子个数比为_____。
参考答案
1.C
【详解】A. 从宏观的角度,该反应可读作:一氧化碳与氧气在点燃条件下反应生成二氧化碳,选项正确;
B. 反应前CO中碳元素的化合价为+2价,反应后CO2中碳元素的化合价为+4价,反应前后碳元素的化合价不同,选项正确;
C. 由化学方程式可知,反应前后分子的个数发生变化,原子的个数不变,选项错误;
D. 由化学方程式可知,参加反应的氧气与生成的二氧化碳的分子个数比为1:2,选项正确,故选C。
2.B
【详解】A.化学方程式Fe + 2HCl = FeCl2 + H2↑,可得出反应物是铁和稀盐酸,生成物是氯化亚铁和氢气,说法正确,不符合题意;
B.化学方程式Fe + 2HCl = FeCl2 + H2↑,无法确定化学反应的快慢,说法错误,不符合题意;
C.化学方程式Fe + 2HCl = FeCl2 + H2↑,可得出反应所需的条件是常温常压,说法正确,不符合题意;
D.通过化学方程式Fe + 2HCl = FeCl2 + H2↑,可得出每有56份质量的铁和73份质量的盐酸完全反应生成127份质量的氯化亚铁和2份质量的氢气,说法正确,不符合题意;
故选:B。
3.C
【详解】从化学方程式获得的信息主要有:反应物的种类、生成物的状态、反应条件、各物质间质量的关系,无法确定化学反应速率的快慢。
故选:C。
4.A
【详解】由于、、,即消耗32g氧气时,分别需要C、Mg、Fe的质量为12g、48g、,则等质量的碳、镁、铁燃烧,消耗氧气最多的是碳,故选A。
5.B
【详解】 A.碳和氧气在点燃条件下生成二氧化碳,A不正确;
B.碳在氧气中充分燃烧生成二氧化碳,B正确;
C.每12粉质量的碳和32份质量的氧气完全反应。生成44份质量的二氧化碳,C不正确;
D.每1个碳原子与1个氧分子反应生成1个二氧化碳分子,D不正确。
综上所述:选择B。
6.A
【详解】A.该化学方程式书写完全正确,故选项正确;
B.镁与氧气点燃生成氧化镁,正确的化学方程式应为,故选项错误;
C.氧气是反应物,不需要加气体符号,正确的化学方程式应为,故选项错误;
D.该化学方程式氧化镁的化学式书写错误,正确的化学方程式应为,故选项错误。
7.B
【详解】A.磷和氧气在点燃的条件下反应生成五氧化二磷,正确;
B.化学式前的计量数表示参加反应的微粒个数比,错误;
C.在点燃的条件下,每4个磷原子和5个氧气分子结合生成2个五氧化二磷分子,正确;
D.在点燃的条件下,每124份质量的磷和160份质量的氧气完全反应,生成284份质量的五氧化二磷,正确。
故选B。
8.B
【详解】根据反应容器中物质X和物质Y的反应微粒之间的关系图,图中的3个X物质的微粒全部参加反应,而8个物质Y的微粒有2个剩余未参加反应,反应生成的三个分子都是由1个X与2个Y构成的XY2型分子,因此该反应可表示为:X+2Y=XY2。故选B。
9.B
【详解】根据质量守恒定律,化学反应前后,物质的总质量不变,D的质量为:(16×3)-(12+27)=9g;
在此反应中,A质量减少16g-12g=4g;B完全反应,参加反应的质量为16g,C质量增加27g-16g=11g,D是生成的新物质,质量为9g。根据反应的数据可知,A、B为反应物,C、D为生成物.因为A、B的质量比为:4g:16g=1:4,它们的相对分子质量比为16:32=1:2,故B的系数应为2;C、D的质量比为:11g:9g=11:9,它们的相对分子质量比为:44:18=22:9,故D的系数应为2;故可判断反应的化学方程式为A+2B=C+2D。
故选B。
10.B
【详解】A.铝跟氧气在点燃的条件下,反应生成氧化铝,读化学方程式时,“+”和“=”应该读作“和”“生成”,而不能读铝加氧气点燃等于氧化铝,说法错误;
B.铝跟氧气在点燃的条件下,反应生成氧化铝,读化学方程式时,“+”和“=”应该读作“和”“生成”,说法正确;
C.由可知,4个铝原子和3个氧分子反应生成2个氧化铝分子,说法错误;
D.由可知,108份质量的铝和96份质量的氧气生成204份质量的氧化铝,说法错误。
故选:B。
11.D
【详解】由质量守恒定律,反应前后,原子种类、数目均不变,配平的实质是化学方程式两边的化学式前配上适当的化学计量数,使化学方程式两边各元素的原子总数相等。故选D。
【点睛】掌握化学反应前后各原子的数目不变、化学方程式的配平依据即可正确解答本题。
12.B
【详解】A.该方程式没有配平,正确的化学方程式为,故错误;
B.该化学方程式书写完全正确;
C.氧化铝的化学式书写错误,正确的化学方程式为,故错误;
D.该化学方程式缺少反应条件,正确的化学方程式为,故错误。
故选:B。
13. CO2+Ca(OH)2=CaCO3↓+H2O 以防干扰后面的实验 CuO+COCu+CO2 CO C
【分析】废气通入澄清石灰水,检验二氧化碳是否存在;若存在,利用氢氧化钠除去混合气体中的二氧化碳,以防干扰后面验证是否含有CO,因为CO还原氧化铜后也会产生二氧化碳气体,CO还原氧化铜后有CO2气体生成,CO还原氧化铜后的尾气CO有毒,不能直接排放于空气中,以防污染空气。
【详解】(1)二氧化碳能使澄清石灰水变浑浊的特性来检验二氧化碳的存在,其反应方程式为:CO2+Ca(OH)2═CaCO3↓+H2O。
(2)将气体A通入浓NaOH溶液以除去CO2,其目的是以防干扰后面的实验;
(3)若③中澄清石灰水变浑浊,则说明反应②中有二氧化碳气体产生,实验混合气体中含有CO,则CO与CuO反应的化学方程式为:CuO+COCu+CO2。
(4)由(1)、(2)、(3)可知,混合气体中一定含有CO气体。
(5)气体D是CO,有毒,需要将气体D收集后再处理。故选C。
14. 2CO+2NON2+2CO2 7:22
【详解】由微观示意图可知,该反应是一氧化碳和一氧化氮反应生成了氮气和二氧化碳,反应的方程式为:2CO+2NON2+2CO2;生成物的质量比为28:(44×2)=7:22。
15.Cu2O
16.CuO
17.
18.水
19.
20.
【解析】15.铜元素通常有+1、+2价,由正负化合价代数和为零可知,与氧元素可组成的物质有Cu2O、CuO;
16.铜元素通常有+1、+2价,由正负化合价代数和为零可知,与氧元素可组成的物质有Cu2O、CuO;
17.氢气与氧气在点燃条件下生成水,该反应是由两种物质生成一种物质的反应,属于化合反应,化学方程式为;
18.甲、乙、丙是初中常见物质,也是由上表中的一种或两种元素组成的。已知甲、丙的组成元素相同,丙是一种最常见的液体,丙是水,则甲是过氧化氢,过氧化氢在催化剂二氧化锰作用下生成水和氧气,则乙是氧气,氧气与水能相互转化,氢气在氧气中燃烧生成水,水在通电条件下生成氢气和氧气;代入框图进行验证,推断正确,故①丙是水;
19.甲、乙、丙是初中常见物质,也是由上表中的一种或两种元素组成的。已知甲、丙的组成元素相同,丙是一种最常见的液体,丙是水,则甲是过氧化氢,过氧化氢在催化剂二氧化锰作用下生成水和氧气,则乙是氧气,氧气与水能相互转化,氢气在氧气中燃烧生成水,水在通电条件下生成氢气和氧气;代入框图进行验证,推断正确,故②甲是过氧化氢溶液,转化成乙是氧气和丙是水的化学方程式为:;
20.甲、乙、丙是初中常见物质,也是由上表中的一种或两种元素组成的。已知甲、丙的组成元素相同,丙是一种最常见的液体,丙是水,则甲是过氧化氢,过氧化氢在催化剂二氧化锰作用下生成水和氧气,则乙是氧气,氧气与水能相互转化,氢气在氧气中燃烧生成水,水在通电条件下生成氢气和氧气;代入框图进行验证,推断正确,故③丙(水)转化成乙(氧气)的化学方程式为:。
21. 9 2CO+4H2C2H5OH+H2O 1:2
【详解】(1)由微粒的构成可知,一个丙分子是由9个原子构成的;
(2)由题意可知,一氧化碳和氢气在一定条件下反应生成了乙醇和水,反应的化学方程式是:2CO+4H2C2H5OH+H2O,由方程式可知,参加反应的甲和乙的分子个数比为2:4=1:2。
【点睛】根据变化微观示意图及粒子构成模拟图,根据分子由原子构成等特点,正确判断变化中的物质构成与粒子个数关系,是解答本题的基本方法。
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 水分子的变化
- 第三节 原子的构成
- 第四节 元素
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 溶液
- 第一节 溶液的形成
- 第二节 溶液组成的定量表示
- 到实验室去:配制一定溶质质量分数的溶液
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 物质组成的表示
- 第三节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去:二氧化碳的实验室制取与性质
