第12章盐复习题(含解析) 2023-2024学年九年级化学京改版(2013)下册
文档属性
| 名称 | 第12章盐复习题(含解析) 2023-2024学年九年级化学京改版(2013)下册 |

|
|
| 格式 | docx | ||
| 文件大小 | 118.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 北京课改版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-12-01 00:00:00 | ||
图片预览




文档简介
第12章 盐 复习题
一、单选题
1.下列说法中,正确的是
A.浓盐酸和浓硫酸露置在空气中,溶质的质量分数都会减小
B.用蒸馏水润湿的pH试纸测定10℅的盐酸溶液的pH,结果偏小
C.有盐参加和盐生成的反应一定是复分解反应
D.炼铁是把单质铁变成氧化铁的过程
2.下列各组离子在水中能大量共存的是
A.H+、Na+、Cl﹣、HCO3﹣
B.H+、K+、Cl﹣、OH﹣
C.Cu2+、Ba2+、Cl﹣、SO42﹣
D.K+、NH4+、Cl﹣、NO3﹣
3.康康发现农田里的小麦叶色发黄、易倒伏,需要到市场购买的一种化肥是
A.KCl B.CO(NH2)2
C.KNO3 D.NH4H2 PO4
4.分类是学习的一种重要方法。下列分类正确的是
A.橡皮、铅笔芯、食盐水都属于导体 B.冰、石蜡、玻璃都属于晶体
C.硝酸钾、硝酸铵、氯化钾都属于复合肥 D.水银、硫、氢气都属于单质
5.下列有关化学反应的说法中,正确的是
A.基本反应类型是置换反应 B.生成的不溶于稀盐酸
C.反应的实质是和生成 D.反应后所得溶液能使酚酞溶液变成红色
6.属于氮肥的是( )
A.NH4NO3 B.KCl C.K2SO4 D.Ca(H2PO4)2
7.通过一步化学反应实现如图所示的X、Y、Z三种物质间的转化,其中X、Y、Z对应的物质不合理的是
A.CuO、Cu(NO3)2、Cu(OH)2
B.Mg、MgO、MgCl2
C.HCl、BaCl2、NaCl
D.CO2、Na2CO3、CaCO3
8.下列有关化学方程式的书写正确的是
A.铁放入硝酸银溶液中:
B.正常雨水pH约为5.6的原因:
C.高炉炼铁的主要反应:
D.配制农药波尔多液:
9.下列物质的分类,正确的一组是
A.Cu、N、O2都属于单质 B.HNO3、H2SO4、NH4HCO3都属于酸
C.MgO、KIO3、Ca(HCO3)2都属于盐 D.CH4、C2H2、CH3CH2OH都属于有机物
10.下列化肥中属于复合肥料的是( )
A.KNO3 B.CO(NH2)2 C.Ca(H2PO4)2 D.NH4HCO3
11.下列物质若露置于空气中,会因发生物理变化而使质量增大的是( )
A.浓盐酸 B.生石灰 C.石灰石 D.浓硫酸
12.只用一种试剂就能把氢氧化钠溶液、稀盐酸和澄清石灰水鉴别开来,这种试剂是
A.氯化钡溶液 B.碳酸钠溶液 C.酚酞溶液 D.石蕊溶液
13.现有盐酸和CaCl2的混合溶液,向其中逐滴加入过量某物质X,溶液的pH随滴入X的量的变化关系如图所示。则X可能是( )
A.水 B.稀盐酸 C.饱和食盐水 D.纯碱溶液
二、填空题
14.以下除杂方法正确的是
①用足量的氢氧化钠溶液吸收CO气体中的CO2 ②除去 NH3中水蒸气气体选用浓硫酸
③除去N2中的少量O2:通过灼热的CuO 粉末 ④用点燃的方法除去CO2中混有的少量CO
⑤除去CaO中的少量CaCO3:加入足量稀盐酸,充分反应
⑥ 除去CO2中HCl气体选用浓氢氧化钠溶液
⑦除去Cu(NO3)2溶液中的少量AgNO3:加入足量铜粉,充分反应后过滤
⑧除去CO2中水蒸气选用氢氧化钠或生石灰固体
⑨为除去NaCl溶液中的Na2CO3,可向溶液中加入过量的氯化钙溶液
15.化学物质的多样性
物质名称 铜 氢气 生理盐水
化学式 / Ca(OH)2
构成物质的微粒符号 Na+,
物质所属具体类别
16.用化学符号或化学式填空:
(1)3个硫酸根离子 ;(2)醋酸分子 ;
(3)赤铁矿的主要成分 ;
(4)由三种元素组成的一种不稳定化合物,且能使紫色石蕊试液变红。该化合物的化学式 ;
(5)在蒸馒头时常加入一种名为“泡打粉”的膨松剂,其主要成分是 ;
(6)粮食发酵后可产生乙醇(C2H5OH)),乙醇是一种清洁能源,其燃烧的化学方程式为 。
17.泉上镇延祥村的“延祥贡茶”,是客家祖地宁化县的特产之一、
(1)茶树适宜生长在pH约4.5~6.5的土壤中,该土壤呈 性。
(2)科技特派员在茶园里套种大豆,通过大豆根瘤菌固氮来改良土壤,在此茶园中可以减少使用的化肥是________(填标号)。
A.KCl B.CO(NH2)2 C.Ca(H2PO4)2
(3)泡茶时需用热水,烧水壶使用一定时间后,内壁会出现一层水垢(主要成分为CaCO3与Mg(OH)2 ),可用厨房中的 (填名称)浸泡除去。
(4)泡茶时,若陶瓷茶杯破碎,从垃圾分类角度看,碎片应投入_______箱。(填字母)
A.可回收垃圾 B.有害垃圾 C.厨余垃圾 D.其他垃圾
18.铁锈的主要成分为Fe2O3,将生锈的铁钉投入盛稀盐酸的试管中,首先看到的现象是铁锈消失,溶液变成黄色,是因为发生下列反应: (用化学方程式表示),该反应 (填“是”或“不是”)复分解反应,过一会儿,看到固体表面产生气泡,是因为发生了下列反应: (用化学方程式表示),该反应属于 反应类型。
三、实验题
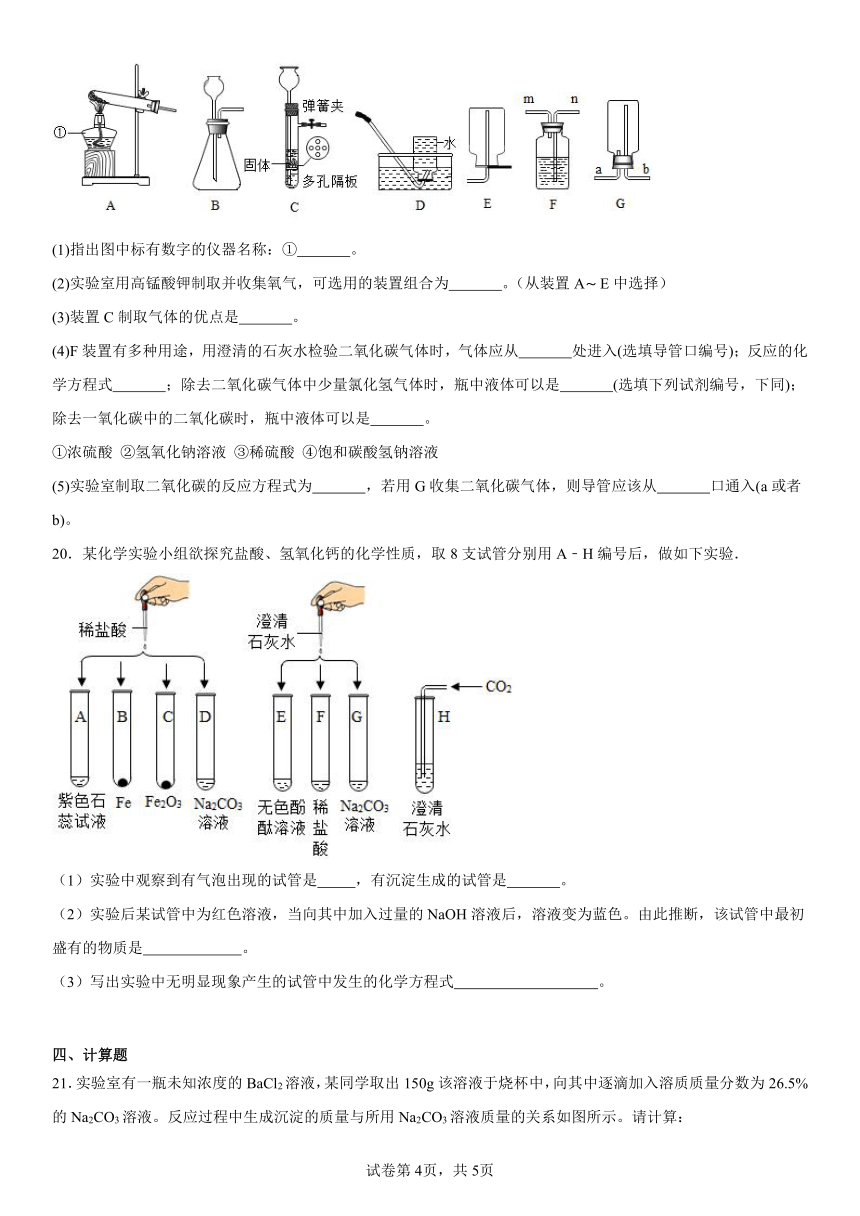
19.图A G是初中化学常见的仪器装置,回答下列问题:
(1)指出图中标有数字的仪器名称:① 。
(2)实验室用高锰酸钾制取并收集氧气,可选用的装置组合为 。(从装置A E中选择)
(3)装置C制取气体的优点是 。
(4)F装置有多种用途,用澄清的石灰水检验二氧化碳气体时,气体应从 处进入(选填导管口编号);反应的化学方程式 ;除去二氧化碳气体中少量氯化氢气体时,瓶中液体可以是 (选填下列试剂编号,下同);除去一氧化碳中的二氧化碳时,瓶中液体可以是 。
①浓硫酸 ②氢氧化钠溶液 ③稀硫酸 ④饱和碳酸氢钠溶液
(5)实验室制取二氧化碳的反应方程式为 ,若用G收集二氧化碳气体,则导管应该从 口通入(a或者b)。
20.某化学实验小组欲探究盐酸、氢氧化钙的化学性质,取8支试管分别用A﹣H编号后,做如下实验.
(1)实验中观察到有气泡出现的试管是 ,有沉淀生成的试管是 。
(2)实验后某试管中为红色溶液,当向其中加入过量的NaOH溶液后,溶液变为蓝色。由此推断,该试管中最初盛有的物质是 。
(3)写出实验中无明显现象产生的试管中发生的化学方程式 。
四、计算题
21.实验室有一瓶未知浓度的BaCl2溶液,某同学取出150g该溶液于烧杯中,向其中逐滴加入溶质质量分数为26.5%的Na2CO3溶液。反应过程中生成沉淀的质量与所用Na2CO3溶液质量的关系如图所示。请计算:
(1)配制26.5%的Na2CO3溶液80g,需要Na2CO3固体 g。
(2)图中A点对应的溶液中溶质有 (填化学式)
(3)BaCl2溶液的溶质质量分数是多少?(写出计算过程,结果保留到0.1%)
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.A
【详解】A、浓盐酸具有挥发性,氯化氢会挥发出去,导致溶质质量减小,溶质质量分数减小,浓硫酸具有吸水性,会吸收空气中的水分,溶液质量增加,溶质质量分数减小,符合题意;
B、pH试纸用蒸馏水润湿,会稀释原溶液,导致酸性减弱,pH偏大,不符合题意;
C、复分解反应是两种化合物互相交换成分生成另外两种化合物的反应,有盐参加和盐生成的反应不一定是复分解反应,如二氧化碳和氢氧化钠反应生成碳酸钠和水,碳酸钠是盐,有盐生成但不属于复分解反应,不符合题意;
D、炼铁是利用还原剂将氧化铁中的铁还原出来的过程,不符合题意。
故选A。
2.D
【详解】A、H+、HCO3﹣会生成二氧化碳气体和水,不能共存,故A错误;
B、H+、OH﹣两种离子能结合成水,不能大量共存,故B错误;
C、Ba2+、SO42﹣两种离子能结合成硫酸钡沉淀,不能大量共存,故C错误;
D、四种离子间不能结合成沉淀、气体或水,能大量共存,故D正确。故选D。
3.C
【分析】氮肥有促进植物茎、叶生长茂盛,叶色浓绿,提高植物蛋白质含量的作用,钾肥有促进植物生长,增强抗病虫害和抗倒伏能力等功能,故小麦叶色发黄,易倒伏、需要施加含氮和钾的化肥。
【详解】A、氯化钾只含钾一种营养元素,不符合题意;
B、尿素只含氮一种营养元素,不符合题意;
C、硝酸钾含K、N两种营养元素,符合题意;
D、磷酸二氢铵含N、P两种营养元素,不符合题意。
故选C。
4.D
【详解】A、食盐水、铅笔芯都属于导体,橡皮属于绝缘体,故选项分类错误;
B、冰有固定的熔点,属于晶体,玻璃和石蜡没有固定的熔点,属于非晶体,故选项分类错误;
C、硝酸钾中含有钾元素和氮元素,属于复合肥;硝酸铵中含有氮元素,属于氮肥;氯化钾中含有钾元素,属于钾肥;故选项分类错误;
D、水银是金属汞的俗称,是由汞元素组成的纯净物,属于单质;硫是由硫元素组成的纯净物,属于单质;氢气是由氢元素组成的纯净物,属于单质;故选项分类正确;
故选:D。
5.B
【详解】A、反应为两种化合物互相交换成分生成另外两种化合物的反应,故为复分解反应,置换反应的定义为单质和化合物生成单质和化合物的反应,故不为置换反应,故A错误,不符合题意;
B、硫酸钡沉淀既不溶于水也不溶于酸,故生成的 BaSO4 不溶于稀盐酸,故B正确,符合题意;
C、生成物中盐酸中仍有氢离子和氯离子,故反应的实质是钡离子和硫酸根离子生成硫酸钡沉淀,故C错误,不符合题意;
D、碱性溶液可以使无色酚酞溶液变成红色,该反应生成物为盐酸为酸性,故反应后所得溶液不能使酚酞溶液变成红色,故D错误,不符合题意。
故选:B。
6.A
【分析】本题主要考查化肥的分类方面的知识,解答时要分析化肥中含有哪种或哪几种营养元素,然后再根据化肥的分类方法确定化肥的种类。
【详解】A、NH4NO3中含有氮元素,属于氮肥,正确;B、KCl中含有钾元素,属于钾肥,错误;C、K2SO4中含有钾元素,属于钾肥,错误;D、Ca(H2PO4)2中含有磷元素,属于磷肥,错误。故选A。
【点睛】含有氮元素的肥料称为氮肥。含有磷元素的肥料称为磷肥。含有钾元素的肥料称为钾肥。同时含有氮、磷、钾三种元素中的两种或两种以上的肥料称为复合肥。
7.A
【分析】一步反应实现即原物质只发生一个反应即可转化为目标物质,根据所涉及物质的性质,分析能否只通过一个反应而实现即可。
【详解】A、氧化铜能与硝酸反应生成硝酸铜和水,Cu(NO3)2与氢氧化钠溶液反应生成氢氧化铜沉淀和硝酸钠,氧化铜难溶于水,不能与水反应,不能生成氢氧化铜,故X、Y、Z对应的物质不能实现这种转化;
B、Mg在氧气中燃烧生成氧化镁,镁与稀盐酸反应生成氯化镁和氢气,氧化镁与稀盐酸反应生成氯化镁和水,故X、Y、Z对应的物质能实现这种转化;
C、HCl与氢氧化钡反应生成氯化钡和水,氯化钡与碳酸钠反应生成碳酸钡沉淀和氯化钠,盐酸与氢氧化钠反应生成氯化钠和水,故X、Y、Z对应的物质能实现这种转化;
D、二氧化碳与氢氧化钠反应生成碳酸钠和水,碳酸钠与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水,故X、Y、Z对应的物质能实现这种转化。
故选:A。
【点睛】本题有一定难度,熟练掌握所涉及物质的性质、抓住关键词“能否一步实现”是解决此类问题的关键。
8.B
【详解】A、铁与硝酸银反应生成硝酸亚铁和银,该反应的化学方程式为:,不符合题意;
B、正常雨水的pH约为5.6,是因为二氧化碳与水反应生成碳酸,该反应的化学方程式为:,符合题意;
C、高炉炼铁是一氧化碳与氧化铁在高温下反应生成铁和二氧化碳,该反应的化学方程式为:,不符合题意;
D、配制农药波尔多液,是氢氧化钙与硫酸铜反应生成氢氧化铜和硫酸钙,该反应的化学方程式为:,不符合题意。
故选B。
9.D
【详解】A、铜是由铜元素组成的纯净物,属于单质,氧气是由氧元素组成的纯净物,属于单质,N可以表示氮元素,1个氮原子,不能表示单质,不符合题意;
B、硝酸、硫酸都是电离时产生的阳离子都是氢离子的化合物,都属于酸,碳酸氢铵是由铵根离子和碳酸氢根离子构成的化合物,属于盐,不符合题意;
C、氧化镁是由Mg、O两种元素组成的化合物,属于氧化物;碘酸钾是由钾离子和碘酸根离子构成的化合物,属于盐,碳酸氢钙是由钙离子和碳酸氢根离子构成的化合物,属于盐,不符合题意;
D、甲烷、乙炔、乙酸均含碳元素,属于有机物,符合题意。
故选D。
10.A
【详解】氮、磷、钾三种元素中至少含有两种的化肥是复合肥。A. KNO3含有钾、氮两种元素,属于复合肥,A选项符合题意;B. CO(NH2)2 属于氮肥,不属于复合肥,B选项不符合题意;C. Ca(H2PO4)2 属于磷肥,不属于复合肥,C选项不符合题意;D. NH4HCO3属于氮肥,不属于复合肥,D选项不符合题意。故选A。
11.D
【详解】A、浓盐酸容易挥发,挥发过程中没有新物质生成,属于物理变化,质量不断减小,不符合题意。
B、生石灰能与水反应生成氢氧化钙,物质的质量会增大,发生的是化学变化,不符合题意;
C、石灰石化学性质稳定,露置于空气中质量基本不变,不符合题意;
D、浓硫酸能够吸收空气中的水蒸气,质量增加,发生的是物理变化,符合题意;
故选:D。
12.B
【详解】只用一种试剂把氢氧化钠溶液、稀盐酸和澄清石灰水鉴别开来,则此种试剂与这三种物质混合要有明显的不同现象:
A、氯化钡溶液与这三种物质都不反应,故A不正确,不符合题意;
B、碳酸钠溶液和氢氧化钠溶液混合无现象,与盐酸混合产生气泡,与氢氧化钙溶液混合产生白色沉淀,能鉴别出来,故B正确,符合题意;
C、酚酞试液遇氢氧化钠溶液和氢氧化钙溶液都变红,无法鉴别,故C不正确,不符合题意;
D、石蕊遇氢氧化钠溶液和氢氧化钙溶液都变蓝,故无法鉴别,故D不正确,不符合题意。
故选B。
13.D
【详解】A、加水只能使溶液酸性变弱,不能变为碱性,A错误。
B、加稀盐酸溶液不会变为碱性,B错误。
C、饱和食盐水显中性,加饱和食盐水不会变为碱性,C错误。
D、纯碱溶液显碱性,它先和盐酸反应生成氯化钠二氧化碳和水,再和氯化钙反应生成碳酸钙沉淀和氯化钠,最后过量溶液显碱性,D正确。
故选:D。
14.①⑦
【详解】①除去CO气体中的CO2 :用足量的氢氧化钠溶液,氢氧化钠不与CO发生反应,与CO2反应生成碳酸钠和水,CO被除去且未引入新杂质,符合题意;
②除去 NH3中水蒸气气体选用浓硫酸:浓硫酸具有吸水性能除去水蒸气,但能与NH3发生反应,违背除杂原则,所选试剂只能与杂质反应,不能与原物质发生反应,不符合题意;
③除去N2中的少量O2:通过灼热的CuO 粉末 ,CuO不与O2反应,无法除去杂质,应该用灼热的铜网除去O2,不符合题意;
④用点燃的方法除去CO2中混有的少量CO,无法点燃,不能除去CO,不符合题意;
⑤除去CaO中的少量CaCO3:加入足量稀盐酸,充分反应,稀盐酸与CaCO3、CaO均发生反应,违背除杂原则所选试剂只能与杂质反应,不能与原物质发生反应,不符合题意;
⑥除去CO2中HCl气体选用浓氢氧化钠溶液:氢氧化钠与HCl与CO2均能发生反应,违背除杂原则所选试剂只能与杂质反应,不能与原物质发生反应,不符合题意;
⑦除去Cu(NO3)2溶液中的少量AgNO3:加入足量铜粉,铜粉不与Cu(NO3)2反应,与AgNO3反应生成硝酸铜和银,充分反应后过滤,除去生成的银和过量的铜粉,得到Cu(NO3)2溶液,少量AgNO3被除去且未引入新杂质,符合除杂原则,符合题意;
⑧除去CO2中水蒸气选用氢氧化钠或生石灰固体:氢氧化钠具有吸水性能吸收水蒸气,生石灰(CaO)能与水反应生成氢氧化钙,除去水蒸气,但氢氧化钠、氢氧化钙与CO2发生反应,违背除杂原则所选试剂只能与杂质反应,不能与原物质发生反应,不符合题意;
⑨除去NaCl溶液中的Na2CO3:向溶液中加入过量的氯化钙溶液,氯化钙与Na2CO3反应生成碳酸钙和氯化钠,Na2CO3被除去,所得溶液含有NaCl和过量的氯化钙,引入新杂质氯化钙,违背除杂原则不引入新杂质,不符合题意。
故选填:①⑦。
15. 碳酸钠 氢氧化钙 Cu H2 Na2CO3 Cu H2 Na+、Cl-、H2O Ca2+、OH- 单质 单质 混合物 盐 碱
【分析】本题考查化学术语的规范描述。
【详解】铜的化学式:Cu,是由铜原子构成,符号:Cu,属于单质;
氢气的化学式是:H2,是由氢气分子构成,符号:H2,属于单质;
生理盐水是混合物,里边含有氯化钠和水,氯化钠是由钠离子和氯离子构成:Na+、Cl-,水是由水分子构成:H2O;
碳酸钠化学式是:Na2CO3,属于盐;
氢氧化钙是由钙离子和氢氧根离子构成:Ca2+、OH-,属于碱。
【点睛】熟记常见物质的化学式和分类。
CH3COOH Fe2O3 H2CO3 NaHCO3
C2H5OH +3O22CO2+3H2O
【详解】(1)由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略,若表示多个该离子,就在其离子符号前加上相应的数字,故3个硫酸根离子可表示为:;
(2)由分子的表示方法,正确书写物质的化学式:CH3COOH;
(3)赤铁矿的主要成分为氧化铁,故答案为Fe2O3;
(4)使紫色石蕊试液变红的物质为酸,由三种元素组成的一种不稳定化合物,可以确定为碳酸,故答案为H2CO3
(5)泡打粉的主要成分为碳酸氢钠,其化学式为:NaHCO3;
(6)乙醇燃烧生成二氧化碳和水,所以化学方程式为:C2H5OH +3O2 2CO2+3H2O。
17.(1)酸
(2)B
(3)食醋或白醋
(4)D
【详解】(1)pH<7显酸性,所以pH约4.5~6.5的土壤中,该土壤呈酸性。
(2)通过大豆根瘤菌固氮来改良土壤,所以可以减少氮肥的使用。
A.KCl中含有钾元素,属于钾肥;
B.CO(NH2)2中含有氮元素,属于氮肥;
C.Ca(H2PO4)2中含有磷元素,属于磷肥。
故选:B。
(3)醋酸会与碳酸钙,氢氧化镁反应生成二氧化碳,所以水垢(主要成分为CaCO3与Mg(OH)2 ),可用厨房中的食醋或白醋浸泡除去。
(4)若陶瓷茶杯破碎,从垃圾分类角度看,碎片应投入其他垃圾箱。
故选:D。
18. Fe2O3+6HCl=2FeCl3+3H2O 是 Fe+2HCl==FeCl2+H2↑ 置换
【详解】铁锈的主要成分是氧化铁(Fe2O3),将生锈的铁钉放入稀盐酸中,先是表面的铁锈的主要成分氧化铁与盐酸反应生成氯化铁与水,反应现象为:铁锈逐渐消失,无色溶液变成黄色,反应的化学方程式为:Fe2O3+6HCl=2FeCl3+3H2O;该反应是两种化合物相互交换成分生成两种新的化合物的反应,属于复分解反应;当铁锈完全反应后,铁与稀盐酸发生反应,生成氯化亚铁与氢气,反应现象是有气泡产生,反应的化学方程式为:Fe+2HCl==FeCl2+H2↑,该反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,属于置换反应。
19.(1)酒精灯
(2)AD/DA
(3)可以随时控制反应的发生与停止
(4) n ④ ②
(5) CaCO3+2HCl=CaCl2+H2O+CO2↑ a
【详解】(1)图中标有数字①的仪器名称:酒精灯;
(2)高锰酸钾加热分解生成锰酸钾、二氧化锰和氧气,该反应的反应物是固体,反应条件是加热,属于固体加热型,氧气密度大于空气,不易溶于水,可用向上排空气法收集或排水法收集,实验室用高锰酸钾制取并收集氧气,可选用的装置组合为AD;
(3)在装置C中,固体药品放在多孔隔板上,液体药品从长颈漏斗中加入。反应开始后,关闭开关时,试管中的气体增多,压强增大,把液体压入长颈漏斗,固体和液体分离,反应停止,打开开关时,气体导出,试管中的气体减少,压强减小,液体和固体混合,反应进行。装置C的优点是可以随时控制反应的发生与停止。
(4)为了使气体与澄清石灰水充分接触,用澄清的石灰水检验二氧化碳气体时,气体应从n (长管)处进入;二氧化碳能与澄清石灰水中的氢氧化钙反应生成碳酸钙沉淀和水,反应的化学方程式为:;
氯化氢与水形成盐酸,碳酸氢钠与盐酸反应生成氯化钠、水和二氧化碳,二氧化碳不能与碳酸氢钠溶液反应,除去二氧化碳气体中少量氯化氢气体时,瓶中液体可以是碳酸氢钠溶液,故选④;
氢氧化钠与二氧化碳反应生成碳酸钠和水,一氧化碳不能与氢氧化钠反应,除去一氧化碳中的二氧化碳时,瓶中液体可以是氢氧化钠溶液,故选②;
(5)实验室制取二氧化碳,常用大理石或石灰石与盐酸反应,大理石或石灰石的主要成分是碳酸钙,碳酸钙与盐酸反应生成氯化钙、水和二氧化碳,反应的化学方程式是CaCO3+2HCl=CaCl2+H2O+CO2↑;二氧化碳密度大于空气,若用G收集二氧化碳气体,则导管应该从a口通入。
20. BD GH 紫色石蕊溶液 2HCl+Ca(OH)2═CaCl2+2H2O
【详解】(1)实验中观察到有气泡出现的试管是:BD,因为B中是铁和盐酸生成氯化亚铁和氢气,D中是碳酸钠和盐酸反应生成氯化钠和水和二氧化碳;有沉淀生成的试管是GH,因为G中碳酸钠与氢氧化钙反应生成碳酸钙白色沉淀和氢氧化钠,H中二氧化碳能使澄清的石灰水变浑浊;
(2)在A试管中盛有紫色石蕊试液,加入盐酸后,显酸性,酸能使紫色石蕊试液变红色,再向其中加入氢氧化钠溶液,当氢氧化钠把盐酸反应掉后,显碱性时,碱能使紫色石蕊试液变蓝色,由此可推断出该试管中最初盛有的物质是:紫色石蕊溶液;
(3)实验中无明显现象产生的试管是F,发生的是盐酸与氢氧化钙反应生成氯化钙和水,反应的方程式为:2HCl+Ca(OH)2═CaCl2+2H2O
21.(1)21.2g;
(2)NaCl、BaCl2;
(3)由图可知,恰好完全反应时,消耗碳酸钠溶质的质量为:40g×26.5%=10.6g;
BaCl2溶液的溶质质量分数是13.9%。
【详解】(1)需要Na2CO3固体的质量为:80g×26.5%=21.2g;
(2)氯化钡与碳酸钠反应生成碳酸钡和氯化钠,图中A点氯化钡未完全反应,则对应的溶液中溶质有:NaCl、BaCl2;
(3)见答案。
答案第1页,共2页
答案第1页,共2页
一、单选题
1.下列说法中,正确的是
A.浓盐酸和浓硫酸露置在空气中,溶质的质量分数都会减小
B.用蒸馏水润湿的pH试纸测定10℅的盐酸溶液的pH,结果偏小
C.有盐参加和盐生成的反应一定是复分解反应
D.炼铁是把单质铁变成氧化铁的过程
2.下列各组离子在水中能大量共存的是
A.H+、Na+、Cl﹣、HCO3﹣
B.H+、K+、Cl﹣、OH﹣
C.Cu2+、Ba2+、Cl﹣、SO42﹣
D.K+、NH4+、Cl﹣、NO3﹣
3.康康发现农田里的小麦叶色发黄、易倒伏,需要到市场购买的一种化肥是
A.KCl B.CO(NH2)2
C.KNO3 D.NH4H2 PO4
4.分类是学习的一种重要方法。下列分类正确的是
A.橡皮、铅笔芯、食盐水都属于导体 B.冰、石蜡、玻璃都属于晶体
C.硝酸钾、硝酸铵、氯化钾都属于复合肥 D.水银、硫、氢气都属于单质
5.下列有关化学反应的说法中,正确的是
A.基本反应类型是置换反应 B.生成的不溶于稀盐酸
C.反应的实质是和生成 D.反应后所得溶液能使酚酞溶液变成红色
6.属于氮肥的是( )
A.NH4NO3 B.KCl C.K2SO4 D.Ca(H2PO4)2
7.通过一步化学反应实现如图所示的X、Y、Z三种物质间的转化,其中X、Y、Z对应的物质不合理的是
A.CuO、Cu(NO3)2、Cu(OH)2
B.Mg、MgO、MgCl2
C.HCl、BaCl2、NaCl
D.CO2、Na2CO3、CaCO3
8.下列有关化学方程式的书写正确的是
A.铁放入硝酸银溶液中:
B.正常雨水pH约为5.6的原因:
C.高炉炼铁的主要反应:
D.配制农药波尔多液:
9.下列物质的分类,正确的一组是
A.Cu、N、O2都属于单质 B.HNO3、H2SO4、NH4HCO3都属于酸
C.MgO、KIO3、Ca(HCO3)2都属于盐 D.CH4、C2H2、CH3CH2OH都属于有机物
10.下列化肥中属于复合肥料的是( )
A.KNO3 B.CO(NH2)2 C.Ca(H2PO4)2 D.NH4HCO3
11.下列物质若露置于空气中,会因发生物理变化而使质量增大的是( )
A.浓盐酸 B.生石灰 C.石灰石 D.浓硫酸
12.只用一种试剂就能把氢氧化钠溶液、稀盐酸和澄清石灰水鉴别开来,这种试剂是
A.氯化钡溶液 B.碳酸钠溶液 C.酚酞溶液 D.石蕊溶液
13.现有盐酸和CaCl2的混合溶液,向其中逐滴加入过量某物质X,溶液的pH随滴入X的量的变化关系如图所示。则X可能是( )
A.水 B.稀盐酸 C.饱和食盐水 D.纯碱溶液
二、填空题
14.以下除杂方法正确的是
①用足量的氢氧化钠溶液吸收CO气体中的CO2 ②除去 NH3中水蒸气气体选用浓硫酸
③除去N2中的少量O2:通过灼热的CuO 粉末 ④用点燃的方法除去CO2中混有的少量CO
⑤除去CaO中的少量CaCO3:加入足量稀盐酸,充分反应
⑥ 除去CO2中HCl气体选用浓氢氧化钠溶液
⑦除去Cu(NO3)2溶液中的少量AgNO3:加入足量铜粉,充分反应后过滤
⑧除去CO2中水蒸气选用氢氧化钠或生石灰固体
⑨为除去NaCl溶液中的Na2CO3,可向溶液中加入过量的氯化钙溶液
15.化学物质的多样性
物质名称 铜 氢气 生理盐水
化学式 / Ca(OH)2
构成物质的微粒符号 Na+,
物质所属具体类别
16.用化学符号或化学式填空:
(1)3个硫酸根离子 ;(2)醋酸分子 ;
(3)赤铁矿的主要成分 ;
(4)由三种元素组成的一种不稳定化合物,且能使紫色石蕊试液变红。该化合物的化学式 ;
(5)在蒸馒头时常加入一种名为“泡打粉”的膨松剂,其主要成分是 ;
(6)粮食发酵后可产生乙醇(C2H5OH)),乙醇是一种清洁能源,其燃烧的化学方程式为 。
17.泉上镇延祥村的“延祥贡茶”,是客家祖地宁化县的特产之一、
(1)茶树适宜生长在pH约4.5~6.5的土壤中,该土壤呈 性。
(2)科技特派员在茶园里套种大豆,通过大豆根瘤菌固氮来改良土壤,在此茶园中可以减少使用的化肥是________(填标号)。
A.KCl B.CO(NH2)2 C.Ca(H2PO4)2
(3)泡茶时需用热水,烧水壶使用一定时间后,内壁会出现一层水垢(主要成分为CaCO3与Mg(OH)2 ),可用厨房中的 (填名称)浸泡除去。
(4)泡茶时,若陶瓷茶杯破碎,从垃圾分类角度看,碎片应投入_______箱。(填字母)
A.可回收垃圾 B.有害垃圾 C.厨余垃圾 D.其他垃圾
18.铁锈的主要成分为Fe2O3,将生锈的铁钉投入盛稀盐酸的试管中,首先看到的现象是铁锈消失,溶液变成黄色,是因为发生下列反应: (用化学方程式表示),该反应 (填“是”或“不是”)复分解反应,过一会儿,看到固体表面产生气泡,是因为发生了下列反应: (用化学方程式表示),该反应属于 反应类型。
三、实验题
19.图A G是初中化学常见的仪器装置,回答下列问题:
(1)指出图中标有数字的仪器名称:① 。
(2)实验室用高锰酸钾制取并收集氧气,可选用的装置组合为 。(从装置A E中选择)
(3)装置C制取气体的优点是 。
(4)F装置有多种用途,用澄清的石灰水检验二氧化碳气体时,气体应从 处进入(选填导管口编号);反应的化学方程式 ;除去二氧化碳气体中少量氯化氢气体时,瓶中液体可以是 (选填下列试剂编号,下同);除去一氧化碳中的二氧化碳时,瓶中液体可以是 。
①浓硫酸 ②氢氧化钠溶液 ③稀硫酸 ④饱和碳酸氢钠溶液
(5)实验室制取二氧化碳的反应方程式为 ,若用G收集二氧化碳气体,则导管应该从 口通入(a或者b)。
20.某化学实验小组欲探究盐酸、氢氧化钙的化学性质,取8支试管分别用A﹣H编号后,做如下实验.
(1)实验中观察到有气泡出现的试管是 ,有沉淀生成的试管是 。
(2)实验后某试管中为红色溶液,当向其中加入过量的NaOH溶液后,溶液变为蓝色。由此推断,该试管中最初盛有的物质是 。
(3)写出实验中无明显现象产生的试管中发生的化学方程式 。
四、计算题
21.实验室有一瓶未知浓度的BaCl2溶液,某同学取出150g该溶液于烧杯中,向其中逐滴加入溶质质量分数为26.5%的Na2CO3溶液。反应过程中生成沉淀的质量与所用Na2CO3溶液质量的关系如图所示。请计算:
(1)配制26.5%的Na2CO3溶液80g,需要Na2CO3固体 g。
(2)图中A点对应的溶液中溶质有 (填化学式)
(3)BaCl2溶液的溶质质量分数是多少?(写出计算过程,结果保留到0.1%)
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.A
【详解】A、浓盐酸具有挥发性,氯化氢会挥发出去,导致溶质质量减小,溶质质量分数减小,浓硫酸具有吸水性,会吸收空气中的水分,溶液质量增加,溶质质量分数减小,符合题意;
B、pH试纸用蒸馏水润湿,会稀释原溶液,导致酸性减弱,pH偏大,不符合题意;
C、复分解反应是两种化合物互相交换成分生成另外两种化合物的反应,有盐参加和盐生成的反应不一定是复分解反应,如二氧化碳和氢氧化钠反应生成碳酸钠和水,碳酸钠是盐,有盐生成但不属于复分解反应,不符合题意;
D、炼铁是利用还原剂将氧化铁中的铁还原出来的过程,不符合题意。
故选A。
2.D
【详解】A、H+、HCO3﹣会生成二氧化碳气体和水,不能共存,故A错误;
B、H+、OH﹣两种离子能结合成水,不能大量共存,故B错误;
C、Ba2+、SO42﹣两种离子能结合成硫酸钡沉淀,不能大量共存,故C错误;
D、四种离子间不能结合成沉淀、气体或水,能大量共存,故D正确。故选D。
3.C
【分析】氮肥有促进植物茎、叶生长茂盛,叶色浓绿,提高植物蛋白质含量的作用,钾肥有促进植物生长,增强抗病虫害和抗倒伏能力等功能,故小麦叶色发黄,易倒伏、需要施加含氮和钾的化肥。
【详解】A、氯化钾只含钾一种营养元素,不符合题意;
B、尿素只含氮一种营养元素,不符合题意;
C、硝酸钾含K、N两种营养元素,符合题意;
D、磷酸二氢铵含N、P两种营养元素,不符合题意。
故选C。
4.D
【详解】A、食盐水、铅笔芯都属于导体,橡皮属于绝缘体,故选项分类错误;
B、冰有固定的熔点,属于晶体,玻璃和石蜡没有固定的熔点,属于非晶体,故选项分类错误;
C、硝酸钾中含有钾元素和氮元素,属于复合肥;硝酸铵中含有氮元素,属于氮肥;氯化钾中含有钾元素,属于钾肥;故选项分类错误;
D、水银是金属汞的俗称,是由汞元素组成的纯净物,属于单质;硫是由硫元素组成的纯净物,属于单质;氢气是由氢元素组成的纯净物,属于单质;故选项分类正确;
故选:D。
5.B
【详解】A、反应为两种化合物互相交换成分生成另外两种化合物的反应,故为复分解反应,置换反应的定义为单质和化合物生成单质和化合物的反应,故不为置换反应,故A错误,不符合题意;
B、硫酸钡沉淀既不溶于水也不溶于酸,故生成的 BaSO4 不溶于稀盐酸,故B正确,符合题意;
C、生成物中盐酸中仍有氢离子和氯离子,故反应的实质是钡离子和硫酸根离子生成硫酸钡沉淀,故C错误,不符合题意;
D、碱性溶液可以使无色酚酞溶液变成红色,该反应生成物为盐酸为酸性,故反应后所得溶液不能使酚酞溶液变成红色,故D错误,不符合题意。
故选:B。
6.A
【分析】本题主要考查化肥的分类方面的知识,解答时要分析化肥中含有哪种或哪几种营养元素,然后再根据化肥的分类方法确定化肥的种类。
【详解】A、NH4NO3中含有氮元素,属于氮肥,正确;B、KCl中含有钾元素,属于钾肥,错误;C、K2SO4中含有钾元素,属于钾肥,错误;D、Ca(H2PO4)2中含有磷元素,属于磷肥,错误。故选A。
【点睛】含有氮元素的肥料称为氮肥。含有磷元素的肥料称为磷肥。含有钾元素的肥料称为钾肥。同时含有氮、磷、钾三种元素中的两种或两种以上的肥料称为复合肥。
7.A
【分析】一步反应实现即原物质只发生一个反应即可转化为目标物质,根据所涉及物质的性质,分析能否只通过一个反应而实现即可。
【详解】A、氧化铜能与硝酸反应生成硝酸铜和水,Cu(NO3)2与氢氧化钠溶液反应生成氢氧化铜沉淀和硝酸钠,氧化铜难溶于水,不能与水反应,不能生成氢氧化铜,故X、Y、Z对应的物质不能实现这种转化;
B、Mg在氧气中燃烧生成氧化镁,镁与稀盐酸反应生成氯化镁和氢气,氧化镁与稀盐酸反应生成氯化镁和水,故X、Y、Z对应的物质能实现这种转化;
C、HCl与氢氧化钡反应生成氯化钡和水,氯化钡与碳酸钠反应生成碳酸钡沉淀和氯化钠,盐酸与氢氧化钠反应生成氯化钠和水,故X、Y、Z对应的物质能实现这种转化;
D、二氧化碳与氢氧化钠反应生成碳酸钠和水,碳酸钠与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水,故X、Y、Z对应的物质能实现这种转化。
故选:A。
【点睛】本题有一定难度,熟练掌握所涉及物质的性质、抓住关键词“能否一步实现”是解决此类问题的关键。
8.B
【详解】A、铁与硝酸银反应生成硝酸亚铁和银,该反应的化学方程式为:,不符合题意;
B、正常雨水的pH约为5.6,是因为二氧化碳与水反应生成碳酸,该反应的化学方程式为:,符合题意;
C、高炉炼铁是一氧化碳与氧化铁在高温下反应生成铁和二氧化碳,该反应的化学方程式为:,不符合题意;
D、配制农药波尔多液,是氢氧化钙与硫酸铜反应生成氢氧化铜和硫酸钙,该反应的化学方程式为:,不符合题意。
故选B。
9.D
【详解】A、铜是由铜元素组成的纯净物,属于单质,氧气是由氧元素组成的纯净物,属于单质,N可以表示氮元素,1个氮原子,不能表示单质,不符合题意;
B、硝酸、硫酸都是电离时产生的阳离子都是氢离子的化合物,都属于酸,碳酸氢铵是由铵根离子和碳酸氢根离子构成的化合物,属于盐,不符合题意;
C、氧化镁是由Mg、O两种元素组成的化合物,属于氧化物;碘酸钾是由钾离子和碘酸根离子构成的化合物,属于盐,碳酸氢钙是由钙离子和碳酸氢根离子构成的化合物,属于盐,不符合题意;
D、甲烷、乙炔、乙酸均含碳元素,属于有机物,符合题意。
故选D。
10.A
【详解】氮、磷、钾三种元素中至少含有两种的化肥是复合肥。A. KNO3含有钾、氮两种元素,属于复合肥,A选项符合题意;B. CO(NH2)2 属于氮肥,不属于复合肥,B选项不符合题意;C. Ca(H2PO4)2 属于磷肥,不属于复合肥,C选项不符合题意;D. NH4HCO3属于氮肥,不属于复合肥,D选项不符合题意。故选A。
11.D
【详解】A、浓盐酸容易挥发,挥发过程中没有新物质生成,属于物理变化,质量不断减小,不符合题意。
B、生石灰能与水反应生成氢氧化钙,物质的质量会增大,发生的是化学变化,不符合题意;
C、石灰石化学性质稳定,露置于空气中质量基本不变,不符合题意;
D、浓硫酸能够吸收空气中的水蒸气,质量增加,发生的是物理变化,符合题意;
故选:D。
12.B
【详解】只用一种试剂把氢氧化钠溶液、稀盐酸和澄清石灰水鉴别开来,则此种试剂与这三种物质混合要有明显的不同现象:
A、氯化钡溶液与这三种物质都不反应,故A不正确,不符合题意;
B、碳酸钠溶液和氢氧化钠溶液混合无现象,与盐酸混合产生气泡,与氢氧化钙溶液混合产生白色沉淀,能鉴别出来,故B正确,符合题意;
C、酚酞试液遇氢氧化钠溶液和氢氧化钙溶液都变红,无法鉴别,故C不正确,不符合题意;
D、石蕊遇氢氧化钠溶液和氢氧化钙溶液都变蓝,故无法鉴别,故D不正确,不符合题意。
故选B。
13.D
【详解】A、加水只能使溶液酸性变弱,不能变为碱性,A错误。
B、加稀盐酸溶液不会变为碱性,B错误。
C、饱和食盐水显中性,加饱和食盐水不会变为碱性,C错误。
D、纯碱溶液显碱性,它先和盐酸反应生成氯化钠二氧化碳和水,再和氯化钙反应生成碳酸钙沉淀和氯化钠,最后过量溶液显碱性,D正确。
故选:D。
14.①⑦
【详解】①除去CO气体中的CO2 :用足量的氢氧化钠溶液,氢氧化钠不与CO发生反应,与CO2反应生成碳酸钠和水,CO被除去且未引入新杂质,符合题意;
②除去 NH3中水蒸气气体选用浓硫酸:浓硫酸具有吸水性能除去水蒸气,但能与NH3发生反应,违背除杂原则,所选试剂只能与杂质反应,不能与原物质发生反应,不符合题意;
③除去N2中的少量O2:通过灼热的CuO 粉末 ,CuO不与O2反应,无法除去杂质,应该用灼热的铜网除去O2,不符合题意;
④用点燃的方法除去CO2中混有的少量CO,无法点燃,不能除去CO,不符合题意;
⑤除去CaO中的少量CaCO3:加入足量稀盐酸,充分反应,稀盐酸与CaCO3、CaO均发生反应,违背除杂原则所选试剂只能与杂质反应,不能与原物质发生反应,不符合题意;
⑥除去CO2中HCl气体选用浓氢氧化钠溶液:氢氧化钠与HCl与CO2均能发生反应,违背除杂原则所选试剂只能与杂质反应,不能与原物质发生反应,不符合题意;
⑦除去Cu(NO3)2溶液中的少量AgNO3:加入足量铜粉,铜粉不与Cu(NO3)2反应,与AgNO3反应生成硝酸铜和银,充分反应后过滤,除去生成的银和过量的铜粉,得到Cu(NO3)2溶液,少量AgNO3被除去且未引入新杂质,符合除杂原则,符合题意;
⑧除去CO2中水蒸气选用氢氧化钠或生石灰固体:氢氧化钠具有吸水性能吸收水蒸气,生石灰(CaO)能与水反应生成氢氧化钙,除去水蒸气,但氢氧化钠、氢氧化钙与CO2发生反应,违背除杂原则所选试剂只能与杂质反应,不能与原物质发生反应,不符合题意;
⑨除去NaCl溶液中的Na2CO3:向溶液中加入过量的氯化钙溶液,氯化钙与Na2CO3反应生成碳酸钙和氯化钠,Na2CO3被除去,所得溶液含有NaCl和过量的氯化钙,引入新杂质氯化钙,违背除杂原则不引入新杂质,不符合题意。
故选填:①⑦。
15. 碳酸钠 氢氧化钙 Cu H2 Na2CO3 Cu H2 Na+、Cl-、H2O Ca2+、OH- 单质 单质 混合物 盐 碱
【分析】本题考查化学术语的规范描述。
【详解】铜的化学式:Cu,是由铜原子构成,符号:Cu,属于单质;
氢气的化学式是:H2,是由氢气分子构成,符号:H2,属于单质;
生理盐水是混合物,里边含有氯化钠和水,氯化钠是由钠离子和氯离子构成:Na+、Cl-,水是由水分子构成:H2O;
碳酸钠化学式是:Na2CO3,属于盐;
氢氧化钙是由钙离子和氢氧根离子构成:Ca2+、OH-,属于碱。
【点睛】熟记常见物质的化学式和分类。
CH3COOH Fe2O3 H2CO3 NaHCO3
C2H5OH +3O22CO2+3H2O
【详解】(1)由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略,若表示多个该离子,就在其离子符号前加上相应的数字,故3个硫酸根离子可表示为:;
(2)由分子的表示方法,正确书写物质的化学式:CH3COOH;
(3)赤铁矿的主要成分为氧化铁,故答案为Fe2O3;
(4)使紫色石蕊试液变红的物质为酸,由三种元素组成的一种不稳定化合物,可以确定为碳酸,故答案为H2CO3
(5)泡打粉的主要成分为碳酸氢钠,其化学式为:NaHCO3;
(6)乙醇燃烧生成二氧化碳和水,所以化学方程式为:C2H5OH +3O2 2CO2+3H2O。
17.(1)酸
(2)B
(3)食醋或白醋
(4)D
【详解】(1)pH<7显酸性,所以pH约4.5~6.5的土壤中,该土壤呈酸性。
(2)通过大豆根瘤菌固氮来改良土壤,所以可以减少氮肥的使用。
A.KCl中含有钾元素,属于钾肥;
B.CO(NH2)2中含有氮元素,属于氮肥;
C.Ca(H2PO4)2中含有磷元素,属于磷肥。
故选:B。
(3)醋酸会与碳酸钙,氢氧化镁反应生成二氧化碳,所以水垢(主要成分为CaCO3与Mg(OH)2 ),可用厨房中的食醋或白醋浸泡除去。
(4)若陶瓷茶杯破碎,从垃圾分类角度看,碎片应投入其他垃圾箱。
故选:D。
18. Fe2O3+6HCl=2FeCl3+3H2O 是 Fe+2HCl==FeCl2+H2↑ 置换
【详解】铁锈的主要成分是氧化铁(Fe2O3),将生锈的铁钉放入稀盐酸中,先是表面的铁锈的主要成分氧化铁与盐酸反应生成氯化铁与水,反应现象为:铁锈逐渐消失,无色溶液变成黄色,反应的化学方程式为:Fe2O3+6HCl=2FeCl3+3H2O;该反应是两种化合物相互交换成分生成两种新的化合物的反应,属于复分解反应;当铁锈完全反应后,铁与稀盐酸发生反应,生成氯化亚铁与氢气,反应现象是有气泡产生,反应的化学方程式为:Fe+2HCl==FeCl2+H2↑,该反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,属于置换反应。
19.(1)酒精灯
(2)AD/DA
(3)可以随时控制反应的发生与停止
(4) n ④ ②
(5) CaCO3+2HCl=CaCl2+H2O+CO2↑ a
【详解】(1)图中标有数字①的仪器名称:酒精灯;
(2)高锰酸钾加热分解生成锰酸钾、二氧化锰和氧气,该反应的反应物是固体,反应条件是加热,属于固体加热型,氧气密度大于空气,不易溶于水,可用向上排空气法收集或排水法收集,实验室用高锰酸钾制取并收集氧气,可选用的装置组合为AD;
(3)在装置C中,固体药品放在多孔隔板上,液体药品从长颈漏斗中加入。反应开始后,关闭开关时,试管中的气体增多,压强增大,把液体压入长颈漏斗,固体和液体分离,反应停止,打开开关时,气体导出,试管中的气体减少,压强减小,液体和固体混合,反应进行。装置C的优点是可以随时控制反应的发生与停止。
(4)为了使气体与澄清石灰水充分接触,用澄清的石灰水检验二氧化碳气体时,气体应从n (长管)处进入;二氧化碳能与澄清石灰水中的氢氧化钙反应生成碳酸钙沉淀和水,反应的化学方程式为:;
氯化氢与水形成盐酸,碳酸氢钠与盐酸反应生成氯化钠、水和二氧化碳,二氧化碳不能与碳酸氢钠溶液反应,除去二氧化碳气体中少量氯化氢气体时,瓶中液体可以是碳酸氢钠溶液,故选④;
氢氧化钠与二氧化碳反应生成碳酸钠和水,一氧化碳不能与氢氧化钠反应,除去一氧化碳中的二氧化碳时,瓶中液体可以是氢氧化钠溶液,故选②;
(5)实验室制取二氧化碳,常用大理石或石灰石与盐酸反应,大理石或石灰石的主要成分是碳酸钙,碳酸钙与盐酸反应生成氯化钙、水和二氧化碳,反应的化学方程式是CaCO3+2HCl=CaCl2+H2O+CO2↑;二氧化碳密度大于空气,若用G收集二氧化碳气体,则导管应该从a口通入。
20. BD GH 紫色石蕊溶液 2HCl+Ca(OH)2═CaCl2+2H2O
【详解】(1)实验中观察到有气泡出现的试管是:BD,因为B中是铁和盐酸生成氯化亚铁和氢气,D中是碳酸钠和盐酸反应生成氯化钠和水和二氧化碳;有沉淀生成的试管是GH,因为G中碳酸钠与氢氧化钙反应生成碳酸钙白色沉淀和氢氧化钠,H中二氧化碳能使澄清的石灰水变浑浊;
(2)在A试管中盛有紫色石蕊试液,加入盐酸后,显酸性,酸能使紫色石蕊试液变红色,再向其中加入氢氧化钠溶液,当氢氧化钠把盐酸反应掉后,显碱性时,碱能使紫色石蕊试液变蓝色,由此可推断出该试管中最初盛有的物质是:紫色石蕊溶液;
(3)实验中无明显现象产生的试管是F,发生的是盐酸与氢氧化钙反应生成氯化钙和水,反应的方程式为:2HCl+Ca(OH)2═CaCl2+2H2O
21.(1)21.2g;
(2)NaCl、BaCl2;
(3)由图可知,恰好完全反应时,消耗碳酸钠溶质的质量为:40g×26.5%=10.6g;
BaCl2溶液的溶质质量分数是13.9%。
【详解】(1)需要Na2CO3固体的质量为:80g×26.5%=21.2g;
(2)氯化钡与碳酸钠反应生成碳酸钡和氯化钠,图中A点氯化钡未完全反应,则对应的溶液中溶质有:NaCl、BaCl2;
(3)见答案。
答案第1页,共2页
答案第1页,共2页
