重庆市西南大学附高2023-2024学年高一上学期11月检测(二)化学试题(含答案)
文档属性
| 名称 | 重庆市西南大学附高2023-2024学年高一上学期11月检测(二)化学试题(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 440.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-12-03 00:00:00 | ||
图片预览


文档简介
重庆市西南大学附高2023-2024学年高一上学期11月检测(二)
化学试题
(满分:100分;考试时间:60分钟)
2023年11月
注意事项:
1.答题前,考生先将自己的姓名、班级、考场/座位号、准考证号填写在答题卡上。
2.答选择题时,必须使用2B铅笔填涂:答非选择题时,必须使用0.5毫米的黑色签字笔书写;必须在题号对应的答题区域内作答,超出答题区域书写无效;保持答卷清洁、完整。
3.考试结束后,将答题卡交回(试题卷学生保管,以备评讲)。
可能用到的相对原子质量:H1 C12 O16 Na23
一、选择题:本题共14小题,每小题4分,共56分。在每小题给出的四个选项中,只有一项符合题目要求。
1.我国传统文化源远流长。对下列古文或诗词的解读错误的是( )
A.“野火烧不尽”涉及氧化还原反应
B.“曾青得铁则为铜”过程发生了复分解反应
C.“日照澄洲江雾开,淘金女伴满江隈”涉及丁达尔效应
D.“方以类聚,物以群分”表达了对于世界体系的分类概念
2.下列物质中,属于电解质,且在水溶液中和熔融状态下都能导电的是( )
A.HCl B. C.Na D.KCl
3.下列分类错误的是( )
A.氧化物:、干冰 B.碱:、烧碱
C.盐:AgCl、纯碱 D.酸:、氯水
4.下列说法正确的是( )
A.新制氯水应保存在棕色细口瓶中
B.在空气中长期放置,最终生成NaOH
C.酒精、钠等着火,可以用二氧化碳灭火器扑灭
D.发生氯气泄漏,可用沾NaOH溶液的湿毛巾捂住口鼻,向上风口或地势高的地方逃生
5.下列物质,既能由金属与氯气直接化合得到,也能由金属与盐酸反应得到的是( )
A. B. C. D.
6.根据反应:,,。下列物质的氧化性强弱判断正确的是( )
A. B.
C. D.
7.下列各组离子在指定溶液中能大量共存的是( )
A.在碳酸钠溶液中:、、、
B.强碱性溶液:、、、
C.强酸性溶液:、、、
D.无色溶液中:、、、
8.下列离子方程式书写错误的是( )
A.Na与水反应:
B.向澄清石灰水中通入过量:
C.与水反应:
D.溶液中加入少量NaOH溶液:
9.下列说法正确的是( )
A.在溶液中逐滴滴入稀HCl溶液,立即产生气泡
B.将加入滴有酚酞的水中,溶液先变红后褪色
C.将洁厕灵(含HCl)与84消毒液(含NaClO)混合使用可增强消毒效果
D.工业上将通入澄清石灰水制漂白粉,其有效成分是和
10.为除去括号内的杂质,下列所选用的试剂或方法错误的是( )
A.溶液(HCl):加入过量固体后过滤
B.:将混合气体通过足量的饱和溶液
C.溶液():向溶液中通入足量的气体
D.固体粉末():加热到固体质量不再减轻为止
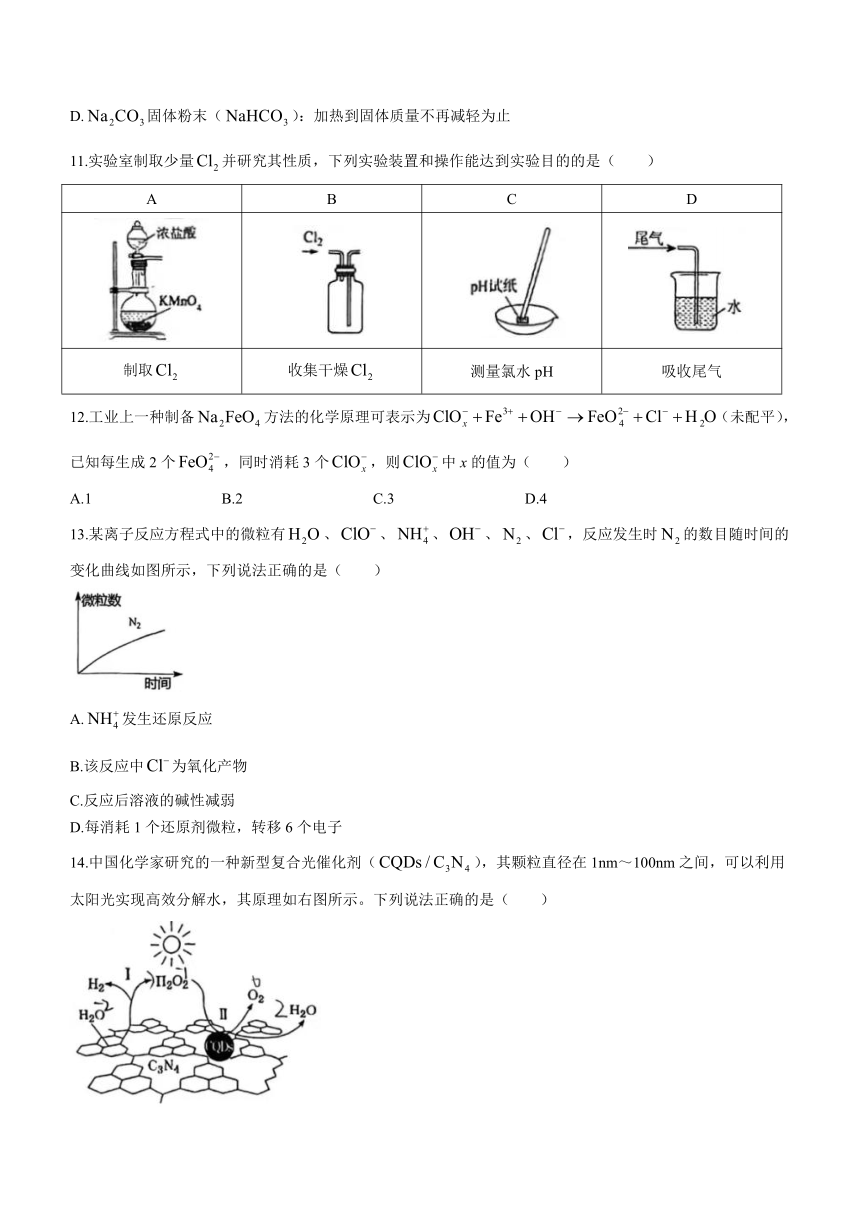
11.实验室制取少量并研究其性质,下列实验装置和操作能达到实验目的的是( )
A B C D
制取 收集干燥 测量氯水pH 吸收尾气
12.工业上一种制备方法的化学原理可表示为(未配平),已知每生成2个,同时消耗3个,则中x的值为( )
A.1 B.2 C.3 D.4
13.某离子反应方程式中的微粒有、、、、、,反应发生时的数目随时间的变化曲线如图所示,下列说法正确的是( )
A.发生还原反应
B.该反应中为氧化产物
C.反应后溶液的碱性减弱
D.每消耗1个还原剂微粒,转移6个电子
14.中国化学家研究的一种新型复合光催化剂(),其颗粒直径在1nm~100nm之间,可以利用太阳光实现高效分解水,其原理如右图所示。下列说法正确的是( )
A.该种复合光催化剂是胶体
B.两个阶段的总反应:
C.阶段Ⅰ的反应中,是还原产物,是氧化产物
D.阶段Ⅱ的反应中,每消耗2个,转移4个
二、填空题:本大题共3小题,共44分。
15.(14分)某无色透明的溶液中可能大量含有以下离子中的几种:、、、、、、、、、,且每种离子的数目相等。为确定其组成,分别取原溶液进行了如下四组实验:
①取少量溶液于试管中,滴入石蕊试液,溶液变红;
②取少量溶液做焰色试验,透过蓝色钴玻璃片观察,焰色为紫色;
③取少量溶液于试管中,滴入硝酸钡溶液,产生白色沉淀;
④取少量溶液于试管中,滴入过量氢氧化钠溶液,产生白色沉淀;
(1)由步骤①可以判断溶液中存在的离子为________(填离子符号,下同),由步骤②可以判断溶液中存在的离子为________。
(2)写出步骤③发生反应的离子方程式________;
写出步骤④产生白色沉淀的离子方程式________;
(3)综合以上实验分析,该溶液中一定存在的阴离子是________(填离子符号)。
(4)取一定量的原溶液,逐滴滴入溶液,恰好使溶液中的沉淀量达到最大值,此时溶液呈________性(填“酸”、“中”、“碱”),此时溶液中还大量存在的阳离子为________(填离子符号)。
(5)取一定量的原溶液,加入铜片,观察到铜片溶解,同时产生气泡(经测定该气体为NO),溶液最终变为蓝色。写出该反应的离子方程式________。
16.(15分)钠及其化合物在生活和生产中有重要用途。
(1)因外观和食盐相似,有咸味,容易使人误食中毒。已知能发生如下反应:。请回答:
①上述反应中,氧化产物是________(填化学式),其中HI在反应中体现出的性质为________(填字母)。
A.酸性 B.氧化性 C.碱性 D.还原性
②某厂废液中含有3%~6%的,直接排放会造成污染,下列试剂能使转化为不引起二次污染的的是________(填字母)。
A.NaClO B. C. D.
(2)是实验室常用的试剂,也常作呼吸面具和潜水艇里的供氧剂。
①写出与反应的化学方程式________.
②将二氧化碳和水蒸气组成的混合气体8.0g通过足量的粉末,完全吸收后固体质量增重3.2g,则该混合气体中水蒸气的质量为________。
③将一定量的固体投入到含有下列离子的溶液中:、、、,完全反应后,溶液中上述离子数目几乎不变的是________(填离子符号)。
(3)是实验室中常用的物质。侯德榜“联合制碱法”将制碱技术发展到一个新的水平。该工艺以氯化钠为原料制取纯碱,主要流程如图所示(部分物质已略去)。
①上述流程中,物质X是________(填化学式)。
②写出沉淀池的化学反应方程式________。
③下列关于侯德榜“联合制碱法”说法错误的是________(填字母).
A.上述流程中滤液中可分离得到一种氮肥
B.上述流程应在饱和NaCl溶液中先通,再通
C.沉淀池中析出晶体利用了相同条件下物质溶解度的差异
D.该工艺的碳原子利用率理论上为100%
17.(15分)一氧化二氯()是国际公认的高效安全灭菌消毒剂,其部分性质如下:现用如图所示装置制备少量。
已知:常温下,是棕黄色、有刺激性气味的气体,易溶于水,且与水反应生成HClO;熔点:-120.6℃:沸点2.0℃。
(1)盛有浓盐酸的仪器的名称是________。
(2)装置A中发生反应的离子方程式为________。
(3)装置B中的试剂是________(填名称)。
(4)装置C 中固体产物中有和另一种常见的钠盐,写出该反应的化学方程式________。
(5)为进一步探究的性质,甲同学取E中滴到湿润的有色布条上,观察到有色布条________(填“能”或“不能”)褪色;乙同学取少量滴入到淀粉-KI的酸性溶液中,观察到溶液变蓝,写出该反应的离子方程式________。
(6)装置G的作用是吸收氯气,查阅资料可知,氯气与NaOH溶液能发生如下反应:,(未配平)。实验结束后测得G溶液中数目为8a,则上述两个反应共转移电子数为________;若还测得溶液中的数目为a,则溶液中的数目为________。
重庆市西南大学附高2023-2024学年高一上学期11月检测(二)
化学答案
1-5 BDDAC 6-10 AACBB 11-14 AACB
15.(1)
(2)
(3) 、
(4)中 、
(5)
16.(1)① AD
②B
(2)①
②3.6g
③
(3)①
②
③B
17.(1)分液漏斗
(2)
(3)饱和食盐水
(4)
(5)能
(6)8a 3a
化学试题
(满分:100分;考试时间:60分钟)
2023年11月
注意事项:
1.答题前,考生先将自己的姓名、班级、考场/座位号、准考证号填写在答题卡上。
2.答选择题时,必须使用2B铅笔填涂:答非选择题时,必须使用0.5毫米的黑色签字笔书写;必须在题号对应的答题区域内作答,超出答题区域书写无效;保持答卷清洁、完整。
3.考试结束后,将答题卡交回(试题卷学生保管,以备评讲)。
可能用到的相对原子质量:H1 C12 O16 Na23
一、选择题:本题共14小题,每小题4分,共56分。在每小题给出的四个选项中,只有一项符合题目要求。
1.我国传统文化源远流长。对下列古文或诗词的解读错误的是( )
A.“野火烧不尽”涉及氧化还原反应
B.“曾青得铁则为铜”过程发生了复分解反应
C.“日照澄洲江雾开,淘金女伴满江隈”涉及丁达尔效应
D.“方以类聚,物以群分”表达了对于世界体系的分类概念
2.下列物质中,属于电解质,且在水溶液中和熔融状态下都能导电的是( )
A.HCl B. C.Na D.KCl
3.下列分类错误的是( )
A.氧化物:、干冰 B.碱:、烧碱
C.盐:AgCl、纯碱 D.酸:、氯水
4.下列说法正确的是( )
A.新制氯水应保存在棕色细口瓶中
B.在空气中长期放置,最终生成NaOH
C.酒精、钠等着火,可以用二氧化碳灭火器扑灭
D.发生氯气泄漏,可用沾NaOH溶液的湿毛巾捂住口鼻,向上风口或地势高的地方逃生
5.下列物质,既能由金属与氯气直接化合得到,也能由金属与盐酸反应得到的是( )
A. B. C. D.
6.根据反应:,,。下列物质的氧化性强弱判断正确的是( )
A. B.
C. D.
7.下列各组离子在指定溶液中能大量共存的是( )
A.在碳酸钠溶液中:、、、
B.强碱性溶液:、、、
C.强酸性溶液:、、、
D.无色溶液中:、、、
8.下列离子方程式书写错误的是( )
A.Na与水反应:
B.向澄清石灰水中通入过量:
C.与水反应:
D.溶液中加入少量NaOH溶液:
9.下列说法正确的是( )
A.在溶液中逐滴滴入稀HCl溶液,立即产生气泡
B.将加入滴有酚酞的水中,溶液先变红后褪色
C.将洁厕灵(含HCl)与84消毒液(含NaClO)混合使用可增强消毒效果
D.工业上将通入澄清石灰水制漂白粉,其有效成分是和
10.为除去括号内的杂质,下列所选用的试剂或方法错误的是( )
A.溶液(HCl):加入过量固体后过滤
B.:将混合气体通过足量的饱和溶液
C.溶液():向溶液中通入足量的气体
D.固体粉末():加热到固体质量不再减轻为止
11.实验室制取少量并研究其性质,下列实验装置和操作能达到实验目的的是( )
A B C D
制取 收集干燥 测量氯水pH 吸收尾气
12.工业上一种制备方法的化学原理可表示为(未配平),已知每生成2个,同时消耗3个,则中x的值为( )
A.1 B.2 C.3 D.4
13.某离子反应方程式中的微粒有、、、、、,反应发生时的数目随时间的变化曲线如图所示,下列说法正确的是( )
A.发生还原反应
B.该反应中为氧化产物
C.反应后溶液的碱性减弱
D.每消耗1个还原剂微粒,转移6个电子
14.中国化学家研究的一种新型复合光催化剂(),其颗粒直径在1nm~100nm之间,可以利用太阳光实现高效分解水,其原理如右图所示。下列说法正确的是( )
A.该种复合光催化剂是胶体
B.两个阶段的总反应:
C.阶段Ⅰ的反应中,是还原产物,是氧化产物
D.阶段Ⅱ的反应中,每消耗2个,转移4个
二、填空题:本大题共3小题,共44分。
15.(14分)某无色透明的溶液中可能大量含有以下离子中的几种:、、、、、、、、、,且每种离子的数目相等。为确定其组成,分别取原溶液进行了如下四组实验:
①取少量溶液于试管中,滴入石蕊试液,溶液变红;
②取少量溶液做焰色试验,透过蓝色钴玻璃片观察,焰色为紫色;
③取少量溶液于试管中,滴入硝酸钡溶液,产生白色沉淀;
④取少量溶液于试管中,滴入过量氢氧化钠溶液,产生白色沉淀;
(1)由步骤①可以判断溶液中存在的离子为________(填离子符号,下同),由步骤②可以判断溶液中存在的离子为________。
(2)写出步骤③发生反应的离子方程式________;
写出步骤④产生白色沉淀的离子方程式________;
(3)综合以上实验分析,该溶液中一定存在的阴离子是________(填离子符号)。
(4)取一定量的原溶液,逐滴滴入溶液,恰好使溶液中的沉淀量达到最大值,此时溶液呈________性(填“酸”、“中”、“碱”),此时溶液中还大量存在的阳离子为________(填离子符号)。
(5)取一定量的原溶液,加入铜片,观察到铜片溶解,同时产生气泡(经测定该气体为NO),溶液最终变为蓝色。写出该反应的离子方程式________。
16.(15分)钠及其化合物在生活和生产中有重要用途。
(1)因外观和食盐相似,有咸味,容易使人误食中毒。已知能发生如下反应:。请回答:
①上述反应中,氧化产物是________(填化学式),其中HI在反应中体现出的性质为________(填字母)。
A.酸性 B.氧化性 C.碱性 D.还原性
②某厂废液中含有3%~6%的,直接排放会造成污染,下列试剂能使转化为不引起二次污染的的是________(填字母)。
A.NaClO B. C. D.
(2)是实验室常用的试剂,也常作呼吸面具和潜水艇里的供氧剂。
①写出与反应的化学方程式________.
②将二氧化碳和水蒸气组成的混合气体8.0g通过足量的粉末,完全吸收后固体质量增重3.2g,则该混合气体中水蒸气的质量为________。
③将一定量的固体投入到含有下列离子的溶液中:、、、,完全反应后,溶液中上述离子数目几乎不变的是________(填离子符号)。
(3)是实验室中常用的物质。侯德榜“联合制碱法”将制碱技术发展到一个新的水平。该工艺以氯化钠为原料制取纯碱,主要流程如图所示(部分物质已略去)。
①上述流程中,物质X是________(填化学式)。
②写出沉淀池的化学反应方程式________。
③下列关于侯德榜“联合制碱法”说法错误的是________(填字母).
A.上述流程中滤液中可分离得到一种氮肥
B.上述流程应在饱和NaCl溶液中先通,再通
C.沉淀池中析出晶体利用了相同条件下物质溶解度的差异
D.该工艺的碳原子利用率理论上为100%
17.(15分)一氧化二氯()是国际公认的高效安全灭菌消毒剂,其部分性质如下:现用如图所示装置制备少量。
已知:常温下,是棕黄色、有刺激性气味的气体,易溶于水,且与水反应生成HClO;熔点:-120.6℃:沸点2.0℃。
(1)盛有浓盐酸的仪器的名称是________。
(2)装置A中发生反应的离子方程式为________。
(3)装置B中的试剂是________(填名称)。
(4)装置C 中固体产物中有和另一种常见的钠盐,写出该反应的化学方程式________。
(5)为进一步探究的性质,甲同学取E中滴到湿润的有色布条上,观察到有色布条________(填“能”或“不能”)褪色;乙同学取少量滴入到淀粉-KI的酸性溶液中,观察到溶液变蓝,写出该反应的离子方程式________。
(6)装置G的作用是吸收氯气,查阅资料可知,氯气与NaOH溶液能发生如下反应:,(未配平)。实验结束后测得G溶液中数目为8a,则上述两个反应共转移电子数为________;若还测得溶液中的数目为a,则溶液中的数目为________。
重庆市西南大学附高2023-2024学年高一上学期11月检测(二)
化学答案
1-5 BDDAC 6-10 AACBB 11-14 AACB
15.(1)
(2)
(3) 、
(4)中 、
(5)
16.(1)① AD
②B
(2)①
②3.6g
③
(3)①
②
③B
17.(1)分液漏斗
(2)
(3)饱和食盐水
(4)
(5)能
(6)8a 3a
同课章节目录
