6.2二氧化碳制取的研究点评卷(含答案)2023-2024学年九年级化学人教版上册
文档属性
| 名称 | 6.2二氧化碳制取的研究点评卷(含答案)2023-2024学年九年级化学人教版上册 |

|
|
| 格式 | docx | ||
| 文件大小 | 132.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-12-04 00:00:00 | ||
图片预览


文档简介
6.2二氧化碳制取的研究点评卷---2023-2024学年九年级化学人教版上册
一、单选题
1.下列叙述正确的是( )
A.烧杯加热时应放置在石棉网上
B.剩余的药品放回原试剂瓶中,不能随意丢弃
C.用嘴吹灭燃着的酒精灯
D.制取气体时,先装药品,再检查装置的气密性
2.常用于检验二氧化碳的物质是( )
A.水 B.食盐水 C.澄清石灰水 D.糖水
3.某气体只能用排水法收集(下图),下列说法正确的是( )
A.当导管口开始有气泡冒出时立即收集
B.当集气瓶口冒出大量气泡时停止收集,取出,再用玻璃片粗糙面盖上
C.当集气瓶口冒出大量气泡时停止收集,在水下用玻璃片光滑面盖上, 取出
D.该气体具有的性质是:不易(或难溶于水);密度与空气接近或与空气中的成分反应
4.下列关于二氧化碳(CO2),说法正确的是( )
A.二氧化碳分子是由碳原子和氧分子构成的
B.保持二氧化碳化学性质的最小粒子是碳原子和氧原子
C.向一定量石灰水中持续通空气,石灰水会变浑浊
D.二氧化碳是由碳原子和氧分子构成的
5.下图装置中哪些可以控制反应的发生和停止 ( )
A.①③ B.②③ C.①④ D.②④
6.实验室里用向上排空气法收集CO2,依据的CO2性质是( )
A.密度 B.颜色 C.气味 D.熔点
7.下列实验操作能达到预期目的是( )
A.用75mL酒精和25mL水配制100mL消毒酒精
B.用托盘天平称取10.58g碳酸钠粉末
C.用向上排空气法收集纯净的氢气
D.用10mL的量筒量取9.0mL水
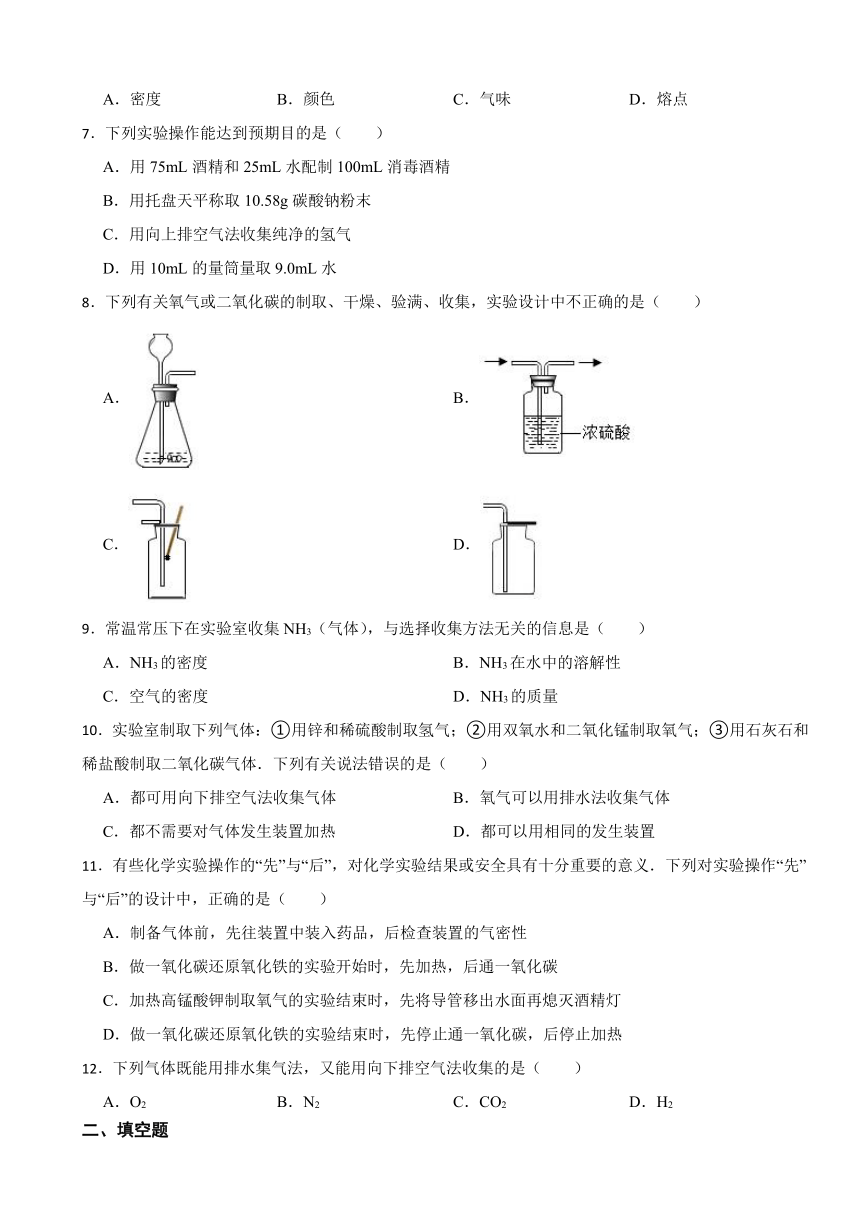
8.下列有关氧气或二氧化碳的制取、干燥、验满、收集,实验设计中不正确的是( )
A. B.
C. D.
9.常温常压下在实验室收集NH3(气体),与选择收集方法无关的信息是( )
A.NH3的密度 B.NH3在水中的溶解性
C.空气的密度 D.NH3的质量
10.实验室制取下列气体:①用锌和稀硫酸制取氢气;②用双氧水和二氧化锰制取氧气;③用石灰石和稀盐酸制取二氧化碳气体.下列有关说法错误的是( )
A.都可用向下排空气法收集气体 B.氧气可以用排水法收集气体
C.都不需要对气体发生装置加热 D.都可以用相同的发生装置
11.有些化学实验操作的“先”与“后”,对化学实验结果或安全具有十分重要的意义.下列对实验操作“先”与“后”的设计中,正确的是( )
A.制备气体前,先往装置中装入药品,后检查装置的气密性
B.做一氧化碳还原氧化铁的实验开始时,先加热,后通一氧化碳
C.加热高锰酸钾制取氧气的实验结束时,先将导管移出水面再熄灭酒精灯
D.做一氧化碳还原氧化铁的实验结束时,先停止通一氧化碳,后停止加热
12.下列气体既能用排水集气法,又能用向下排空气法收集的是( )
A.O2 B.N2 C.CO2 D.H2
二、填空题
13.如图为常见的气体发生和收集装置,B装置的优点为 ,请写出一个用A装置制取气体的化学方程式 ,该气体可用 装置收集.
14. 生活中处处有化学。
(1) 漂白粉的有效成分是次氯酸钙[Ca(ClO)2],次氯酸钙中氯元素的化合价为 。
(2)干冰可用于人工降雨,主要是因为 。
(3)①右表为“新盖中盖”产品的部分说明。
①该产品的保健功能是“补钙”,这里的“钙”是指 (填字母序号)。
A.钙原子 B.钙元素 C.碳酸钙 D.钙单质
②根据说明计算,每片高钙片中含碳酸钙的质量分数是 。
(4)热水壶中沉积的水垢主要成分为氢氧化镁和碳酸钙,用食醋(含醋酸CH3COOH)可以除去水垢,其中与氢氧化镁反应的化学方程式为:2CH3COOH+Mg(OH)2 =(CH3COO)2 Mg +2 H2O,则醋酸与碳酸钙反应的化学方程式为 。
三、计算题
15.鸡蛋壳的主要成分是碳酸钙。为了测定鸡蛋壳中钙元素的质量分数,小华同学进行了如下实验:将鸡蛋壳洗净、干燥并捣碎后,称取10g放在烧杯里,然后往烧杯中滴加足量的稀盐酸,加入稀盐酸的量与生成气体的量如图所示.试求该鸡蛋壳中钙元素的质量分数.(假设鸡蛋壳中其他物质不与盐酸反应)
四、实验探究题
16.下图是实验室制取气体常用的装置,请根据装置回答下列问题。
(1)写出标号仪器名称:① ;② 。
(2)实验室用装置A制取氧气,发生反应的化学方程式是 ,要得到比较纯净的氧气通常选用 (填字母)装置收集。
(3)实验室常用石灰石和稀盐酸在常温下反应制取二氧化碳,应选择的发生装置是 ,如图F所示,将二氧化碳气体慢慢倒入烧杯中,观察到蜡烛由低到高依次熄灭,说明二氧化碳具有的性质是:①不支持燃烧;② ;③ 。
17.有如图所示的仪器和KClO3、MnO2、稀H2SO4、石灰石、稀盐酸等药品供选择,若在实验室完成下列实验,请填写下列空白处:
(1)制取并收集CO2气体,你选择的仪器是 (填仪器序号);
(2)若再补充一种药品,也可用上述制CO2的装置来制O2,你补充的药品是 ;
(3)再补充一种仪器,并选择上述原有仪器和药品制取并收集O2,反应的化学方程式是 .
五、综合题
18.化学实验和化学计算都是化学学习的重要内容.
(1)(一)通过学习,我们已经掌握了一些气体的制备方法,如制取氧气的方法有:
甲.分离液体空气;乙.加热分解高锰酸钾;丙.分解过氧化氢;丁.加热分解氯酸钾等;也初步认识了一些气体的制取和收集装置,例如:
仪器a的名称是 .
(2)以上制取氧气的方法中,属于物理方法的是 ;
(3)若用方法丙制取氧气,应选用的装置组合为 (填字母序号)
(4)(二)在现代生活中,人们越来越注重微量元素的摄取.碘元素对人体有着至关重要的作用.
如图是某地市场销售的一种“加碘食盐”包装袋上的部分说明,请回答下列问题:
食用“碘盐”属于 ;(纯净物或混合物)
(5)根据碘盐的食用方法和贮存指南,可推知碘酸钾的化学性质之一是:
(6)碘酸钾(KIO3)中钾元素、碘元素的质量比是 ,碘酸钾(KIO3)中碘元素的质量分数的计算式是 .
答案解析部分
1.【答案】A
2.【答案】C
3.【答案】D
4.【答案】C
5.【答案】D
6.【答案】A
7.【答案】D
8.【答案】C
9.【答案】D
10.【答案】A
11.【答案】C
12.【答案】D
13.【答案】控制反应速率;2KClO3 2KCl+3O2↑;C 或 E
14.【答案】+1;易升华、吸热;B;50%;2CH3COOH + CaCO3 =(CH3COO)2 Ca + H2O + CO2↑
15.【答案】解:根据图示可知,完全反应时生成的CO2质量为2.2g.
设所取鸡蛋壳中碳酸钙的质量为x,
CaCO3+ 2HCl═ CaCl2+H2O+ CO2↑
100
44
x
2.2g
x=5g
碳酸钙中Ca的质量分数=
所取鸡蛋壳中钙的质量分数=
答:该鸡蛋壳中钙元素的质量分数为20%.
16.【答案】(1)长颈漏斗;集气瓶
(2);C
(3)B;不燃烧;密度比空气大
17.【答案】(1)①②⑦⑧
(2)过氧化氢溶液
(3)2KClO3 2KCl+3O2↑
18.【答案】(1)集气瓶
(2)甲
(3)BC(BE)
(4)混合物
(5)受热易分解
(6)39:127; ×100%
一、单选题
1.下列叙述正确的是( )
A.烧杯加热时应放置在石棉网上
B.剩余的药品放回原试剂瓶中,不能随意丢弃
C.用嘴吹灭燃着的酒精灯
D.制取气体时,先装药品,再检查装置的气密性
2.常用于检验二氧化碳的物质是( )
A.水 B.食盐水 C.澄清石灰水 D.糖水
3.某气体只能用排水法收集(下图),下列说法正确的是( )
A.当导管口开始有气泡冒出时立即收集
B.当集气瓶口冒出大量气泡时停止收集,取出,再用玻璃片粗糙面盖上
C.当集气瓶口冒出大量气泡时停止收集,在水下用玻璃片光滑面盖上, 取出
D.该气体具有的性质是:不易(或难溶于水);密度与空气接近或与空气中的成分反应
4.下列关于二氧化碳(CO2),说法正确的是( )
A.二氧化碳分子是由碳原子和氧分子构成的
B.保持二氧化碳化学性质的最小粒子是碳原子和氧原子
C.向一定量石灰水中持续通空气,石灰水会变浑浊
D.二氧化碳是由碳原子和氧分子构成的
5.下图装置中哪些可以控制反应的发生和停止 ( )
A.①③ B.②③ C.①④ D.②④
6.实验室里用向上排空气法收集CO2,依据的CO2性质是( )
A.密度 B.颜色 C.气味 D.熔点
7.下列实验操作能达到预期目的是( )
A.用75mL酒精和25mL水配制100mL消毒酒精
B.用托盘天平称取10.58g碳酸钠粉末
C.用向上排空气法收集纯净的氢气
D.用10mL的量筒量取9.0mL水
8.下列有关氧气或二氧化碳的制取、干燥、验满、收集,实验设计中不正确的是( )
A. B.
C. D.
9.常温常压下在实验室收集NH3(气体),与选择收集方法无关的信息是( )
A.NH3的密度 B.NH3在水中的溶解性
C.空气的密度 D.NH3的质量
10.实验室制取下列气体:①用锌和稀硫酸制取氢气;②用双氧水和二氧化锰制取氧气;③用石灰石和稀盐酸制取二氧化碳气体.下列有关说法错误的是( )
A.都可用向下排空气法收集气体 B.氧气可以用排水法收集气体
C.都不需要对气体发生装置加热 D.都可以用相同的发生装置
11.有些化学实验操作的“先”与“后”,对化学实验结果或安全具有十分重要的意义.下列对实验操作“先”与“后”的设计中,正确的是( )
A.制备气体前,先往装置中装入药品,后检查装置的气密性
B.做一氧化碳还原氧化铁的实验开始时,先加热,后通一氧化碳
C.加热高锰酸钾制取氧气的实验结束时,先将导管移出水面再熄灭酒精灯
D.做一氧化碳还原氧化铁的实验结束时,先停止通一氧化碳,后停止加热
12.下列气体既能用排水集气法,又能用向下排空气法收集的是( )
A.O2 B.N2 C.CO2 D.H2
二、填空题
13.如图为常见的气体发生和收集装置,B装置的优点为 ,请写出一个用A装置制取气体的化学方程式 ,该气体可用 装置收集.
14. 生活中处处有化学。
(1) 漂白粉的有效成分是次氯酸钙[Ca(ClO)2],次氯酸钙中氯元素的化合价为 。
(2)干冰可用于人工降雨,主要是因为 。
(3)①右表为“新盖中盖”产品的部分说明。
①该产品的保健功能是“补钙”,这里的“钙”是指 (填字母序号)。
A.钙原子 B.钙元素 C.碳酸钙 D.钙单质
②根据说明计算,每片高钙片中含碳酸钙的质量分数是 。
(4)热水壶中沉积的水垢主要成分为氢氧化镁和碳酸钙,用食醋(含醋酸CH3COOH)可以除去水垢,其中与氢氧化镁反应的化学方程式为:2CH3COOH+Mg(OH)2 =(CH3COO)2 Mg +2 H2O,则醋酸与碳酸钙反应的化学方程式为 。
三、计算题
15.鸡蛋壳的主要成分是碳酸钙。为了测定鸡蛋壳中钙元素的质量分数,小华同学进行了如下实验:将鸡蛋壳洗净、干燥并捣碎后,称取10g放在烧杯里,然后往烧杯中滴加足量的稀盐酸,加入稀盐酸的量与生成气体的量如图所示.试求该鸡蛋壳中钙元素的质量分数.(假设鸡蛋壳中其他物质不与盐酸反应)
四、实验探究题
16.下图是实验室制取气体常用的装置,请根据装置回答下列问题。
(1)写出标号仪器名称:① ;② 。
(2)实验室用装置A制取氧气,发生反应的化学方程式是 ,要得到比较纯净的氧气通常选用 (填字母)装置收集。
(3)实验室常用石灰石和稀盐酸在常温下反应制取二氧化碳,应选择的发生装置是 ,如图F所示,将二氧化碳气体慢慢倒入烧杯中,观察到蜡烛由低到高依次熄灭,说明二氧化碳具有的性质是:①不支持燃烧;② ;③ 。
17.有如图所示的仪器和KClO3、MnO2、稀H2SO4、石灰石、稀盐酸等药品供选择,若在实验室完成下列实验,请填写下列空白处:
(1)制取并收集CO2气体,你选择的仪器是 (填仪器序号);
(2)若再补充一种药品,也可用上述制CO2的装置来制O2,你补充的药品是 ;
(3)再补充一种仪器,并选择上述原有仪器和药品制取并收集O2,反应的化学方程式是 .
五、综合题
18.化学实验和化学计算都是化学学习的重要内容.
(1)(一)通过学习,我们已经掌握了一些气体的制备方法,如制取氧气的方法有:
甲.分离液体空气;乙.加热分解高锰酸钾;丙.分解过氧化氢;丁.加热分解氯酸钾等;也初步认识了一些气体的制取和收集装置,例如:
仪器a的名称是 .
(2)以上制取氧气的方法中,属于物理方法的是 ;
(3)若用方法丙制取氧气,应选用的装置组合为 (填字母序号)
(4)(二)在现代生活中,人们越来越注重微量元素的摄取.碘元素对人体有着至关重要的作用.
如图是某地市场销售的一种“加碘食盐”包装袋上的部分说明,请回答下列问题:
食用“碘盐”属于 ;(纯净物或混合物)
(5)根据碘盐的食用方法和贮存指南,可推知碘酸钾的化学性质之一是:
(6)碘酸钾(KIO3)中钾元素、碘元素的质量比是 ,碘酸钾(KIO3)中碘元素的质量分数的计算式是 .
答案解析部分
1.【答案】A
2.【答案】C
3.【答案】D
4.【答案】C
5.【答案】D
6.【答案】A
7.【答案】D
8.【答案】C
9.【答案】D
10.【答案】A
11.【答案】C
12.【答案】D
13.【答案】控制反应速率;2KClO3 2KCl+3O2↑;C 或 E
14.【答案】+1;易升华、吸热;B;50%;2CH3COOH + CaCO3 =(CH3COO)2 Ca + H2O + CO2↑
15.【答案】解:根据图示可知,完全反应时生成的CO2质量为2.2g.
设所取鸡蛋壳中碳酸钙的质量为x,
CaCO3+ 2HCl═ CaCl2+H2O+ CO2↑
100
44
x
2.2g
x=5g
碳酸钙中Ca的质量分数=
所取鸡蛋壳中钙的质量分数=
答:该鸡蛋壳中钙元素的质量分数为20%.
16.【答案】(1)长颈漏斗;集气瓶
(2);C
(3)B;不燃烧;密度比空气大
17.【答案】(1)①②⑦⑧
(2)过氧化氢溶液
(3)2KClO3 2KCl+3O2↑
18.【答案】(1)集气瓶
(2)甲
(3)BC(BE)
(4)混合物
(5)受热易分解
(6)39:127; ×100%
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
