2.2 化学反应的限度 同步测试题(含解析) 2023-2024学年高二上学期化学鲁科版(2019)选择性必修1
文档属性
| 名称 | 2.2 化学反应的限度 同步测试题(含解析) 2023-2024学年高二上学期化学鲁科版(2019)选择性必修1 |  | |
| 格式 | docx | ||
| 文件大小 | 614.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-12-05 12:16:22 | ||
图片预览




文档简介
2.2 化学反应的限度 同步测试题
一、单选题
1.改变下列哪个条件,一定会引起平衡的移动( )
A.温度 B.浓度 C.压强 D.催化剂
2.合成氨工业中采用循环操作,主要是为了( )
A.增大化学反应速率 B.提高平衡混合物中氨的含量
C.降低氨的沸点 D.提高氮气和氢气的利用率
3.在一定条件下,反应2HI(g) H2(g)+I2(g)△H>0达到平衡时,要使混合气体的颜色变浅,可采取的措施是( )
①增大氢气的浓度 ②升高温度 ③降低温度 ④增大压强 ⑤增大HI的浓度 ⑥扩大体积 ⑦加催化剂.
A.①③⑥ B.③⑤⑥ C.①③⑤ D.②④⑤
4.下列化学反应中:Ag++Fe2+ Ag(固)+Fe3+(正反应放热)为使平衡体系析出更多的银,可采取的措施是( )
A.常温下加压 B.增加Fe3+的浓度
C.增加Fe2+的浓度 D.移去一些析出的银
5.为了探究外界条件对反应aX(g)+bY(g) cZ(g)的影响,以X和Y物质的量比为a∶b开始反应,通过实验得到不同条件下达到平衡时Z的物质的量分数,实验结果如下图所示。以下判断正确的是( )
A.ΔH>0,a+b>c B.ΔH>0,a+bC.ΔH<0,a+b>c D.ΔH<0,a+b6.反应2A(g) + B(g) C(g) + 3D(g),达到平衡时,下列说法正确的是( )
A.A、B全部变成了C和D
B.A,B,C,D四种物质的浓度一定相等
C.反应速率为零
D.单位时间内B消耗的物质的量和B生成的物质的量相等
7.温度为T℃时,向容积为2L的恒容密闭容器中充入一定量和,发生反应:,有关数据如下表所示。下列说法正确的是( )
反应物 CO
起始时的物质的量/mol 1.2 0.6
平衡时的物质的量/mol 0.9 0.3
A.平衡时,CO和的转化率相等
B.平衡时,反应放出的热量为
C.平衡时,CO的浓度是CO2浓度的3倍
D.T℃时。该反应的平衡常数
8.在一定条件下,反应:2NO+O2 NO2在定容容器中发生,对该反应达到平衡的标志的描述中,错误的是( )
A.混合气体的总分子数不再变化 B.混合气体的颜色不再变化
C.容器的总压强不再变化 D.混合气体的总质量不再变化
9.硫酸是一种重要的化工产品,硫酸的消耗量常被视为一个国家工业发展水平的一种标志.目前的重要生产方法是“接触法”,有关接触氧化反应2SO2+O2 2SO3,的说法不正确的是( )
A.该反应为可逆反应,故在一定条件下二氧化硫和氧气不可能全部转化为三氧化硫
B.达到平衡后,反应就停止了,故此时正、逆反应速率相等且均为零
C.一定条件下,向某密闭容器中加入2molSO2和1molO2,则从反应开始到达到平衡的过程中,正反应速率不断减小,逆反应速率不断增大,某一时刻,正、逆反应速率相等
D.在利用上述反应生产三氧化硫时,要同时考虑反应所能达到的限度和化学反应速率两方面的问题
10.下列事实中,不能用勒夏特列原理解释的有几项( )
①Fe(SCN)3溶液中加入固体KSCN后颜色变深
②将混合气体中的氨液化有利于合成氨反应
③实验室常用排饱和食盐水的方法收集氯气
④红棕色NO2气体加压后颜色先变深后变浅
⑤加入催化剂有利于合成氨的反应
⑥由H2(g)、I2(g)和HI(g)组成的平衡体系加压后颜色变深
⑦500 ℃时比室温更有利于合成氨的反应
A.三项 B.四项 C.五项 D.六项
11.一定温度下,在容积为2L的恒容密闭容器中发生反应,加入1molA和1molB,经5s反应达平衡,此时容器内的压强与起始时压强比为6:5,同时生成0.4molD,下列叙述中不正确的是( )
A.
B.5s内B的平均反应速率
C.当混合气体的密度不再改变时,该反应已达到平衡状态
D.当时,标志着该反应达到平衡状态
12.对于反应2HI(g) H2(g) +I2(g),下列叙述能够说明己达平衡状态的是( )
A.混合气体的颜色不再变化
B.温度和体积一定时,容器内压强不再变化
C.1molH-H键生成的同时有2molH-I键断裂
D.各物质的物质的量浓度之比为2:1:1
13.在一个不传热的固定容积的密闭容器中发生可逆反应:
mA(g)+nB(g) pC(g)+qD(g)(m、n、p、q为任意整数)。下列不能作为达到平衡状态的标志的是( )
A.单位时间内有m mol A消耗,同时有p mol C生成
B.体系的温度不再改变
C.各组分的浓度不再改变
D.各组分的质量分数不再改变
14.在一定温度下的恒容容器中,当下列物理量不再发生变化时,表明反应: A(s)+3B(g) 2C(g)+D(g)已达平衡状态的是( )
A.混合气体的压强 B.混合气体的密度
C.体系的温度 D.气体的总物质的量
15.在恒定的某温度下,三个容积均为2.0 L的恒容密闭容器中发生如下反应:,各容器中起始物质的量浓度与反应温度(已知)如表所示:
容器 温度/℃ 起始物质的量浓度
甲 0.10 0.10 0 0
乙 0 0 0.10 0.20
丙 0.10 0.10 0 0
反应过程中甲、丙容器中的物质的量随时间变化关系如图所示。下列说法错误的是( )
A.该反应的正反应为放热反应,平衡常数
B.达到平衡时,乙容器中的压强一定小于甲容器的2倍
C.乙容器中反应达到平衡时,的转化率大于40%
D.丙容器中反应达到平衡后,再充入0.10 mol NO和0.10 mol ,此时v(正)>v(逆)
16.下列说法正确的是( )
A.增加水的量或升高温度,可以加快镁跟水的反应速率
B.增大硫酸的浓度,一定可以加快锌与硫酸反应制取氢气的速率
C.在反应2H++S2O32﹣=S↓+SO2+H2O中,增大压强,可以加快硫析出的速率
D.煅烧硫铁矿时,把硫铁矿粉碎或通入纯O2可加快反应的速率
二、综合题
17.2021年国务院政府工作报告明确提出要制定2030年前碳排放达峰行动方案。如何实现碳的氧化物的资源化利用解决温室效应问题是当前科学家亟待解决的问题。请回答下列问题:
(1)一定温度下,测得、和的燃烧热分别为、和,由
可知 。
(2)在恒温恒容条件下,下列不能说明反应达到平衡状态的是 (填序号)。
a.
b.混合气体的密度不变
c.混合气体的平均摩尔质量不变
d.化学平衡常数不变
e.混合气体的压强不变
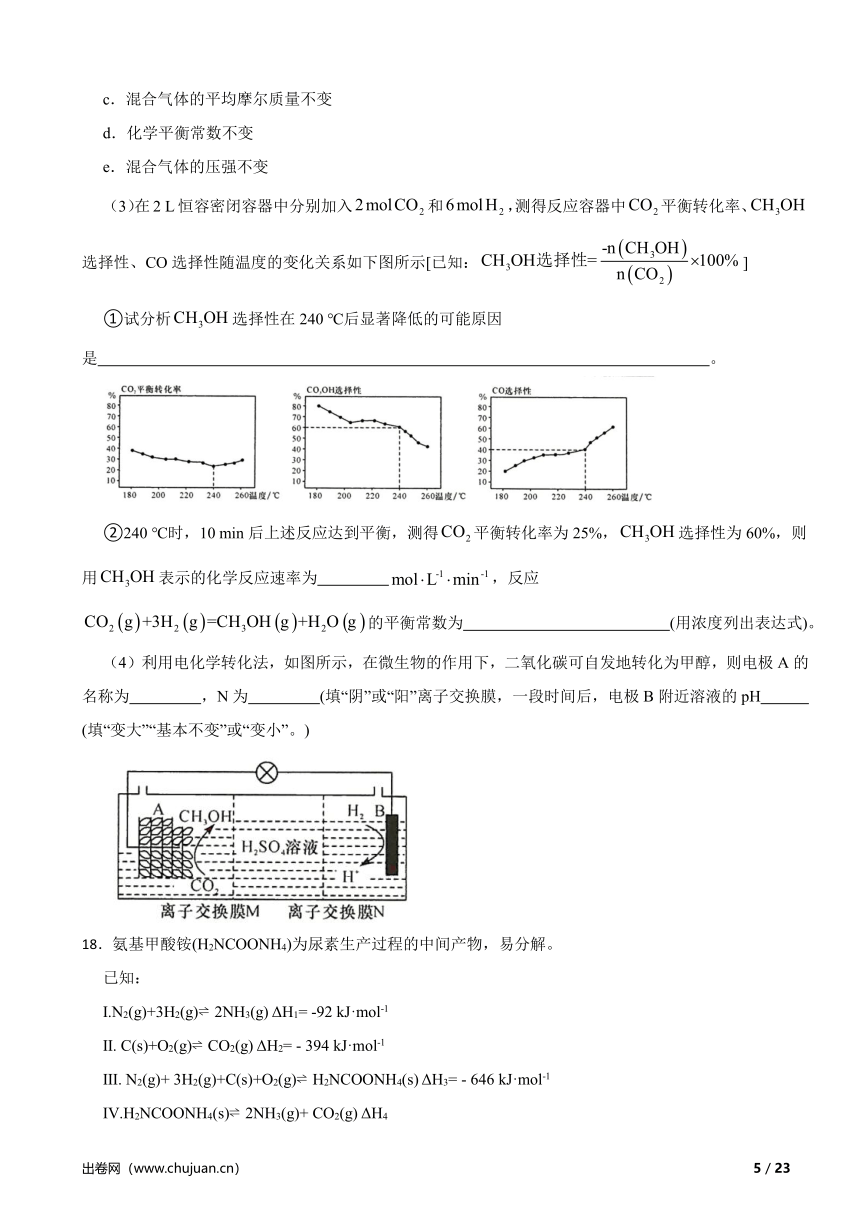
(3)在2 L恒容密闭容器中分别加入和,测得反应容器中平衡转化率、选择性、CO选择性随温度的变化关系如下图所示[已知:]
①试分析选择性在240 ℃后显著降低的可能原因是 。
②240 ℃时,10 min后上述反应达到平衡,测得平衡转化率为25%,选择性为60%,则用表示的化学反应速率为 ,反应的平衡常数为 (用浓度列出表达式)。
(4)利用电化学转化法,如图所示,在微生物的作用下,二氧化碳可自发地转化为甲醇,则电极A的名称为 ,N为 (填“阴”或“阳”离子交换膜,一段时间后,电极B附近溶液的pH (填“变大”“基本不变”或“变小”。)
18.氨基甲酸铵(H2NCOONH4)为尿素生产过程的中间产物,易分解。
已知:
Ⅰ.N2(g)+3H2(g) 2NH3(g) ΔH1= -92 kJ·mol-1
Ⅱ. C(s)+O2(g) CO2(g) ΔH2= - 394 kJ·mol-1
Ⅲ. N2(g)+ 3H2(g)+C(s)+O2(g) H2NCOONH4(s) ΔH3= - 646 kJ·mol-1
Ⅳ.H2NCOONH4(s) 2NH3(g)+ CO2(g) ΔH4
回答下列问题:
(1)NH3的空间构型为 。NH3的键角大于PH3, 分析原因: 。
(2)ΔH4= 。 T℃下在某密闭容器中加入H2NCOONH4(s),假设只发生反应Ⅳ,达平衡时测得NH3的浓度为c1;保持温度不变,加压(缩小容器的体积),测得新的平衡条件下NH3的浓度为c2,则c1 c 2(填“>” “<”或“=”)。反应Ⅳ在 (填“高温” “低温”或“任意温度”)条件下能够自发进行。
(3)某温度下在一刚性的密闭容器中,充入等物质的量N2和H2发生反应Ⅰ,起始压强为1MPa, 10min 末达平衡,测得平衡时压强为0.8MPa,则10min内v(N2)= MPa/min。此时平衡常数Kp= 。对于该条件下的反应,下列说法错误的是 。
A.当N2的体积分数不变时,说明反应已经达到化学平衡状态
B.温度升高化学反应速率加快,化学平衡常数增大
C.其他条件不变时,若适当增加N2的用量,可以提高H2的平衡转化率
D.使用合适的催化剂可以加快化学反应速率,但ΔH1不变
(4)在一定的条件 下,将AmolN2和BmolH2充入某体积固定的密闭容器中合成NH3,在不同的催化剂(甲或乙)下发生反应,反应相同时间后H2的转化率与温度的关系如图:
某学习小组的同学通过讨论得出结论: 200℃时, a点对应的转化率(5%)不是使用催化剂甲下H2的平衡转化率。判断依据是: 。
19.研究脱除烟气中的NO是环境保护、促进社会可持续发展的重要课题。选择性催化还原技术是利用还原剂氨或尿素,把烟气中的NO还原成和。相关反应方程式如下:
(1)① 。
②有氧条件下,在Fe基催化剂表面,还原NO的反应机理如图所示,该过程可描述为 。
(2)近年来,低温等离子体(NTP)技术是在高压放电下,产生自由基(O*),自由基将NO氧化为后,再用溶液吸收,便达到消除NO的目的。实验室将模拟气(、、NO)以一定流速通入低温等离子体装置,实验装置如图所示。
①等离子体技术在低温条件下可提高NO的转化率,原因是 。
②若4.6g被含0.05mol 溶液充分吸收,转移电子数为0.05mol,则此反应的离子方程式为 。
③其他条件相同,等离子体的功率与NO的转化率关系如图所示,当功率大于30W时,NO转化率下降的原因可能是 。
20.在容积为2L的密闭容器中进行如下反应:A(g)+2B(g) 3C(g)+nD(g),开始时A为4mol,B为6mol;5min末时测得C的物质的量为6mol,用D表示的化学反应速率v(D)为0.4mol/(L min).请回答下列有关问题:
(1)5min末A的物质的量浓度为 .
(2)前5min内用B表示的化学反应速率v(B)为 .
(3)化学方程式中n值为 .
(4)此反应在四种不同情况下的反应速率分别为:
①v(A )=5mol/( L min ) ②v( B )=6mol/( L min )
③v(C)=4.5mol/( L min ) ④v(D )=8mol/( L min )
其中反应速率最快的是 (填编号).
21.有甲、乙两容器,甲的容积固定,乙的容积可变.在一定温度下,向甲中通入3molN2和4molH2,反应达到平衡时,生成NH3物质的量为amol.
(1)①相同温度下,若乙中通入6molN2和8molH2,且保持压强与甲相同,反应达到平衡时,生成NH3物质的量为bmol,则b与a的关系可表示为 ,两容器中氮气的转化率甲 乙(填“>”、“<”或“=”)
②若①中乙与甲的容积始终相等,达到平衡时,生成NH3物质的量为Cmol,则C与a的关系可表示为
(2)如图左表示在密闭容器中反应:2SO2+O2 2SO3+Q达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,
a 时刻改变的条件可能是 ;
b 时刻改变的条件可能是 .
答案解析部分
1.【答案】A
【解析】【解答】催化剂只影响化学反应速率,不一定引起平衡的移动;当一个反应的前后化学计量数之和相等时,压强也不一定引起平衡的移动;当反应中各物质的浓度均按照化学计量数变化时,也不一定引起平衡的移动;故B、C、D选项错误;当温度改变时,反应的平衡常数改变,化学反应重新达到新的状态,一定会引起平衡的移动。故A项正确。
【分析】增大反应物或减少生成物浓度,平衡朝正反应移动
增大生成物或减少反应物浓度,平衡朝逆反应移动
升高温度,平衡朝吸热方向移动
降低温度,平衡朝放热方向移动
左右两边气体系数不相同
增大压强,缩小体积,平衡朝气体体积缩小的方向移动
减小压强,增大体积,平衡朝气体体积增大的方向移动
恒压下,充入不反应气体则增大体积,往体积增大移动
恒容下,充入不反应气体,速率不变,平衡不移动
左右两边气体系数相同,改变压强平衡不移动
加入催化剂,速率增大,平衡不移动
2.【答案】D
【解析】【解答】合成氨工业中氢气和氮气在催化剂作用下生成氨气的反应为可逆反应,反应后的混合气分离出氨气后还含有氢气和氮气,进行循环操作可以提高氮气和氢气的利用率,降低成本;与增大化学反应速率、提高平衡混合物中氨的含量、降低氨的沸点无必然关系;
故答案为:D。
【分析】由于合成氨反应为可逆反应,且转化率很低,原料不能很好地利用,采用循环操作目的为提高原料转化率。
3.【答案】A
【解析】【解答】解:①增大氢气的浓度,平衡逆向移动,混合气体的颜色变浅,故正确;
②升高温度,平衡正向移动,混合气体的颜色加深,故错误;
③降低温度,平衡逆向移动,混合气体的颜色变浅,故正确;
④增大压强,相当于缩小体积,各种气体的浓度都增大,混合气体的颜色加深,故错误;
⑤增大HI浓度,平衡正向移动,碘浓度增大,混合气体的颜色加深,故错误;
⑥减小压强,各气体浓度减小,混合气体的颜色变浅,故正确;
⑦加催化剂,平衡不移动,混合气体的颜色不变,故错误;
故选A.
【分析】要使混合气体的颜色变浅,即减小碘的浓度,平衡逆向移动,从影响平衡移动的因素角度考虑.
4.【答案】C
【解析】【解答】A. 常温下加压对此反应无影响,A不符合题意;
B. 增加Fe3+的浓度,平衡逆向移动,不能析出更多的银,B不符合题意;
C. 增加Fe2+的浓度,平衡正向移动,能析出更多的银,C符合题意;
D. Ag为固体,移去一些析出的银,平衡不移动,D不符合题意。
故答案为:C。
【分析】A.该反应中没有气体参加,改变压强不能使平衡发生移动;
B.增大生成物浓度平衡逆向移动;
C.增大反应物浓度平衡正向移动;
D.银为固体,减少银的量,平衡不移动。
5.【答案】C
【解析】【解答】根据图像可知压强相同时升高温度Z的含量降低,所以正反应是放热反应;温度相同时增大压强Z的含量升高,这说明正反应是体积减小的,则有△H<0,a+b>c,
故答案为:C。
【分析】根据勒夏特列原理,温度升高,反应逆向移动,为放热反应
压强增大,正向移动,则a+b>c
6.【答案】D
【解析】【解答】A.反应2A(g) + B(g) C(g) + 3D(g),达到平衡时,各组成含量保持不变,反应是可逆反应不能进行彻底,故A不符合题意;
B. 物质浓度和起始量、变化量有关,平衡状态下A、B、C、D四种物质的浓度不一定相等,故B不符合题意;
C.平衡状态是动态平衡,V正=V逆 0,反应仍在进行,反应未停止,故C不符合题意;
D. 单位时间内B消耗的物质的量和B生成的物质的量相等说明反应达到平衡状态,故D符合题意;
故答案为:D
【分析】根据化学平衡状态的特征进行解答。当反应达到平衡状态时,正逆反应速率相等(且不为0),达到一种动态的平衡;各物质的溶度、百分含量不变,以及由此衍生的一些量也不发生改变;对于反应前后气体分子数不同的反应,如果气体的压强不变,则其达到了平衡状态;由此即可得出答案。
7.【答案】C
【解析】【解答】A.起始时CO和物质的量不相等,平衡时两者消耗的物质的量相等,因此平衡时,CO和的转化率不相等,故A不符合题意;
B.根据方程式分析消耗1molCO,反应放出41kJ的热量,平衡时,消耗0.3molCO,则反应放出的热量为12.3kJ,故B不符合题意;
C.根据改变量之比等于计量系数之比,消耗CO物质的量为0.3mol,因此生成二氧化碳物质的量为0.3mol,则平衡时CO物质的量是CO2物质的量的3倍,因此平衡时CO浓度是CO2浓度的3倍,故C符合题意;
D.T℃时,平衡时CO和物质的量分别为0.9mol、0.3mol,生成的二氧化碳和氢气物质的量都为0.3mol,则反应的平衡常数,故D不符合题意。
故答案为:C。
【分析】A、转化率=变化量/起始量;
B、结合热化学方程式给出的焓变计算;
C、结合三段式判断;
D、平衡常数=生成物浓度幂之积/反应物浓度幂之积。
8.【答案】D
【解析】【解答】解:A、混合气体的总分子数不再变化,说明各物质的量不变,反应达平衡状态,故A错误;
B、混合气体的颜色不再变化,说明二氧化氮的浓度不变,反应达平衡状态,故B错误;
C、容器的总压强不再变化,说明气体的物质的量不变,反应达平衡状态,故C错误;
D、混合气体的总质量一直不随时间的变化而变化,所以不一定平衡,故D正确;
故选D.
【分析】根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
9.【答案】B
【解析】【解答】解:A、可逆反应是在一定条件下不能进行彻底的反应,正反应和逆反应同时进行,该反应为可逆反应,故在一定条件下SO2和O2不可能全部转化为SO3 ,故A正确;
B、达到平衡后,正反应速率和逆反应速率相同,是动态平衡,速率不能为0,故B错误;
C、一定条件下,向某密闭容器中加入2 mol SO2和1mol O2,则从反应开始到平衡的过程中,正反应速率不断减小,逆反应速率不断增大,某一时刻,正、逆反应速率相等达到平衡,故C正确;
D、反应是放热反应,但为了反应速率需要一定温度,催化剂活性最大,压强在常温下,二氧化硫的转化率已经横高改变压强对转化率影响不大,故D正确;
故选B.
【分析】A、依据可逆反应的特征分析判断;
B、化学平衡是动态平衡,正反应速率和逆反应速率相同;
C、依据平衡建立的过程分析;
D、合成需要考虑温度压强对平衡的影响和经济效益.
10.【答案】A
【解析】【解答】①Fe(SCN)3溶液中加入固体KSCN固体,溶液中c(SCN-)增大,平衡向着生成Fe(SCN)3的方向进行,使得溶液颜色变深,可用勒夏特列原理解释,①不符合题意;
②合成氨反应中,将NH3液化,使得混合气体中c(NH3)减小,平衡正向移动,有利于合成氨反应,可用勒夏特列原理解释,②不符合题意;
③Cl2与H2O的反应为可逆反应Cl2+H2O HCl+HClO,由于饱和食盐水中c(Cl-)达到最大值,因此可抑制Cl2与H2O的反应,故可用排饱和食盐水的方法收集Cl3,可用勒夏特列原理解释,③不符合题意;
④NO2转化为N2O4的反应为2NO2(g) N2O4(g),加压后,体积减小,浓度增大,溶液的颜色变深;由于增大压强,平衡正向移动,因此气体的颜色又变浅,可用勒夏特列原理解释,④不符合题意;
⑤加入催化剂只能改变反应速率,不能改变平衡移动,因此加入催化剂有利于合成氨的反应,不能用勒夏特列原理解释,⑤符合题意;
⑥平衡体系中发生的反应为:H2(g)+I2(g) 2HI(g),由于反应前后气体分子数不变,因此加压对平衡移动无影响,颜色变深,是由于c(I2)增大引起,不能用勒夏特列原理解释,⑥符合题意;
⑦合成氨的反应为放热反应,升高温度不利于NH3的产生;而采用500℃是因为在该温度下催化剂的活性高,不可用勒夏特列原理解释,⑦符合题意;
综上,不能用勒夏特列原理解释的有⑤⑥⑦,共三项,A符合题意;
故答案为:A
【分析】能用勒夏特列原理解释,则过程中涉及可逆反应的平衡移动,据此分析。
11.【答案】B
【解析】【解答】A、反应前后,物质的量之比等于压强之比,则有,解得a=0.8,则,解得x=4,故A正确;
B、5s内B的平均反应速率 ,故B错误;
C、随着反应的进行,混合气体的密度发生变化,当当混合气体的密度不再改变时,该反应已达到平衡状态,故C正确;
D、 当时,正逆反应速率相等,该反应达到平衡状态,故D正确;
故答案为:B。
【分析】达到平衡时,生成0.4molD,设同时生成amolC,则有三段式:
。
12.【答案】A
【解析】【解答】A.混合气体的颜色不再变化,说明碘蒸气的浓度不变,达平衡状态,故A符合题意;
B.气体两边的计量数相等,所以温度和体积一定时,容器内压强一直不变化,故B不符合题意;
C.1molH-H键生成的同时有2molH-I键断裂,都体现正反应方向,未体现正与逆的关系,故C不符合题意;
D.当体系达平衡状态时,各物质的物质的量浓度之比可能为2:1:1,也可能不是2:1:1,与各物质的初始浓度及转化率有关,故D不符合题意;
故答案为:A。
【分析】化学平衡状态的判断方法
1、达到化学平衡状态的本质标志
化学平衡状态的本质标志是:正反应速率等于逆反应速率,但不等于零,v正=v逆是对同一反应物或同一生成物而言。对某一反应物来说,正反应消耗掉反应物的速度等于逆反应生成该反应物的速度。
2、达到化学平衡状态的等价标志
所谓“等价标志”是指可以间接衡量某一可逆反应是否达到化学平衡状态的标志。
(1)与v正=v逆等价的标志
①同一物质:该物质的生成速率等于它的消耗速率,如:v正生成=v逆消耗。
②不同的物质:速率之比等于化学方程式中的化学计量数之比,但必须是不同方向的速率,如:v正生成:v逆消耗=m:n。
③可逆反应的正、逆反应速率不再随时间发生变化。
④化学键断裂情况=化学键生成情况。对同一物质而言,断裂化学键的物质的量与形成化学键的物质的量相等。对不同物质而言,与各物质的化学计量数和分子内的化学键多少有关。
(2)反应混合物中各组成成分的含量保持不变
①质量不再改变:各组成成分的质量不再改变,各反应物或生成物的总质量不再改变(不是指反应物的生成物的总质量不变),各组分的质量分数不再改变。
②物质的量不再改变:各组分的物质的量不再改变,各组分的物质的量分数不再改变,各反应物或生成物的总物质的量不再改变。
③对气体物质:若反应前后的物质都是气体,且化学计量数不等,总物质的量、总压强(恒温、恒容)、平均摩尔质量、混合气体的密度(恒温、恒压)保持不变。
④反应物的转化率、产物的产率保持不变。
⑤有颜色变化的体系颜色不再发生变化。
⑥物质的量浓度不再改变。当各组分(不包括固体或纯液体)的物质的量浓度不再改变时,则达到了化学平衡状态。
13.【答案】A
【解析】【解答】A.单位时间内物质的变化量之比与化学计量系数之比相等不能说明其达到平衡,故A符合题意;
B.该反应温度不变可说明反应得到平衡,故B不符合题意;
C.各组分的浓度不变可说明达到平衡,故C不符合题意;
D.各组分的质量分数不变也可说明其平衡,故D不符合题意;
故答案为:A
【分析】根据 在一个不传热的固定容积的密闭容器中发生可逆反应: 判断达到平衡可以根据,温度不变,浓度不变,组分不变等,结合选项判断即可。
14.【答案】B
【解析】【解答】A、可逆反应: A(s)+3B(g) 2C(g)+D(g),反应前后,气体的物质的量不发生变化,体积恒定,反应自开始到平衡,压强都是一定值,故A不符合题意;
B、A是固体,随着反应进行,气体的质量在增加而体积不变,故气体的密度是变量。当气体的总质量不发生变化时,气体的密度也不再变化,说明到达平衡状态,故B符合题意;
C、该反应是在一定温度下的恒容容器中进行的,所以无论该反应是否达到平衡状态, 体系的温度保持不变,不能判定反应达到平衡状态,故C不符合题意;
D.该反应是一个反应前后气体体积不变的化学反应,无论该反应是否达到平衡状态,气体的总物质的量始终不变,故D不符合题意;
故答案为:B。
【分析】A.该反应是一个反应前后气体体积不变的反应,压强始终不变;
B.A是固体,反映进行过程中气体质量会变化;
C.温度是确定的,始终不变;
D.该反应是一个反应前后气体体积不变的反应。
15.【答案】C
【解析】【解答】A.先拐先平温度高,甲平衡状态二氧化碳物质的量小,说明温度越高平衡逆向进行,逆反应为吸热反应,正反应为放热反应,温度T1>T2,平衡常数K(T1)B.温度T1>T2,反应为放热反应,温度降低平衡正向进行,气体物质的量减小,气体压强减小,乙气体物质的量为甲的2倍,相当于增大压强,平衡正向移动,气体物质的量减小,达到平衡时,乙容器中的压强一定小于甲容器的2倍,故B不符合题意;
C.由图象可知,丙中达到平衡状态二氧化碳0.12mol,
乙若达到相同平衡状态,体积增大一倍,浓度变为原来的二分之一,
此时氮气转化率,但相同体积条件下,相当于体积缩小压强增大平衡正向进行,氮气转化率小于40%,故C符合题意;
D.结合表格中丙的相关数据,列“三段式”:
平衡常数,丙容器中反应达到平衡后,再充0.10 mol NO和0.10 mol CO2,浓度商Qc=,平衡正向进行,此时v(正)>v(逆),故D不符合题意;
故答案为:C。
【分析】A.温度越高反应速率越快,达到平衡的时间越短,升温甲平衡状态二氧化碳物质的量小,说明升温平衡逆向移动,正反应为放热反应;
B.乙中生成物物质的量转化为反应物的物质的量时恰好是甲的2倍,若甲乙温度相同且甲乙中反应物转化率相同时,乙容器中压强是甲的2倍,但温度:T1>T2,即甲>乙,降低温度,平衡正向移动,故达到平衡时,乙容器中的压强小于甲容器的2倍;
D.计算此时的浓度熵,与平衡常数比较两者相对大小,确定平衡进行的方向。
16.【答案】D
【解析】【解答】A.增加水的量,浓度不变,则反应速率不变,故A错误;
B.浓硫酸与锌反应不生成氢气,故B错误;
C.反应在溶液中进行,增大压强,溶液浓度不变,则速率不变,故C错误;
D.增大固体表面积或增大反应物浓度,反应速率增大,故D正确.
故选D.
【分析】A.增加水的量,反应速率不变;
B.浓硫酸与锌反应不生成氢气;
C.反应在溶液中进行,增大压强,速率不变;
D.增大固体表面积或增大反应物浓度,反应速率增大.
17.【答案】(1)﹣87.6
(2)bd
(3)催化剂活性降低(合成甲醇为放热反应,温度升高,平衡逆向移动等合理答案都行);0.015;
(4)正极;阴;变小
【解析】【解答】(1)一定温度下,测得、和的燃烧热分别为、和,
则①
②
③
④
根据盖斯定律①+②×2+④-③得-283-285.8×2+40.9+726.1=-87.6;
(2)a.,正逆反应速率相等,反应一定达到平衡状态,故不选a;
b.反应前后气体总质量不变,容器体积不变,密度是恒量,混合气体的密度不变,反应不一定平衡,
故答案为:b;
c.反应前后气体物质的量改变,气体总质量不变,所以平均摩尔质量是变量,混合气体的平均摩尔质量不变,反应一定达到平衡状态,故不选c;
d.恒温条件下,平衡常数是恒量,化学平衡常数不变,反应不一定平衡,
故答案为:d;
e.反应前后气体物质的量改变,容器体积不变,压强是变量,混合气体的压强不变,反应一定达到平衡状态,故不选e;
选bd;
(3)①催化剂能够改变反应的活化能,但催化剂受温度影响较大,温度升高,催化剂活性可能降低,造成选择性降低;或者根据两个反应,第一个反应生成CO为吸热反应,温度升高,平衡正向移动,而合成甲醇为放热反应,温度升高,转化率降低;所以选择性在240 ℃后显著降低。
②240 ℃时,10 min后上述反应达到平衡,测得平衡转化率为25%,选择性为60%,则生成甲醇的物质的量是2mol×25%×60%=0.3mol;反应消耗二氧化碳2mol×25%-0.3mol=0.2mol,消耗氢气0.2mol,生成水0.2mol;反应消耗二氧化碳0.3mol、消耗氢气0.9mol、生成水0.3mol,则容器中二氧化碳的物质的量是1.5mol、氢气的物质的量是6mol-0.2mol-0.9mol=4.9mol、甲醇的物质的量是0.3mol、水的物质的量是0.5mol,
用表示的化学反应速率为,反应的平衡常数为。
(4)根据图示可知,二氧化碳在电极A得电子发生还原反应生成甲醇,A为正极;负极氢气失电子变成氢离子,中间的硫酸根离子经过阴离子交换膜N进入右侧形成硫酸,故离子交换膜N为阴离子交换膜,电极B附近溶液的pH降低。
【分析】(1)根据盖斯定律计算;
(2)依据化学平衡的特征“等”和“定”进行分析判断;
(3)①催化剂有高效性和选择性;
②利用“三段式”法计算。
(4)根据正极得电子发生还原反应;负极失电子,阴离子经过阴离子交换膜分析。
18.【答案】(1)三角锥形;中心原子均为sp3杂化,且都只有一对孤电子对,电负性N>P,NH3中的键合电子(共用电子对)离中心原子更近,排斥力更大,键角越大
(2)+160kJ·mol-l;=;高温
(3)0.01;12.5( MPa)-2;B
(4)催化剂不能使平衡发生移动,该反应为放热反应,温度升高平衡逆向移动,则a点为200℃时使用催化剂甲下的平衡转化率应高于b点的转化率
【解析】【分析】(1)NH3中心原子氮原子形成3个共价键且含有1对孤电子对,为sp3杂化,空间构型为三角锥形;NH3的键角大于PH3,原因为:中心原子均为sp3杂化,且都只有一对孤电子对,电负性N>P,NH3 中的键合电子(共用电子对)离中心原子更近,排斥力更大,键角越大;
(2)已知:
Ⅰ.N2(g)+3H2(g) 2NH3(g) ΔH1= -92 kJ·mol-1
Ⅱ. C(s)+O2(g) CO2(g)|ΔH2= - 394 kJ·mol-1
Ⅲ. N2(g)+ 3H2(g)+C(s)+O2(g) H2NCOONH4(s) ΔH3= - 646 kJ·mol-1
由盖斯定律可知,Ⅰ+Ⅱ-Ⅲ得到反应Ⅳ.H2NCOONH4(s) 2NH3(g)+ CO2(g),故ΔH4=ΔH1+ΔH2-ΔH3=+160 kJ·mol-1;
反应Ⅳ的平衡常数为:K=c2(NH3)c(CO2),密闭容器中加入H2NCOONH4(s),保持温度不变,加压平衡常数不变,则新的平衡条件下NH3的浓度为c2=c1;反应Ⅳ为吸热的熵增反应,故在高温条件下能够自发进行;
(3)刚性的密闭容器中,充入等物质的量N2和H2发生反应Ⅰ,假设投料均为1mol,起始压强为1MPa;10min 末达平衡,测得平衡时压强为0.8MPa,则总的物质的量为1.6mol,总的物质的量减小0.4mol,根据N2(g)+3H2(g) 2NH3(g)可知生成氨气0.4mol、消耗氮气、氢气分别为0.2mol、0.6mol,平衡时氮气、氢气、氨气分别为0.8mol、0.4mol、0.4mol,则10min内v(N2)=MPa/min。此时平衡常数Kp=。
A.当N2的体积分数不变时,说明正逆反应速率相等,平衡不再移动,反应已经达到化学平衡状态,A正确;
B.反应为放热反应,温度升高化学反应速率加快,平衡逆向移动,化学平衡常数减小,B不正确;
C.其他条件不变时,若适当增加N2的用量,平衡正向移动,可以提高H2的平衡转化率,C正确;
D.使用合适的催化剂可以加快化学反应速率,但不该反应的焓变,故ΔH1不变,D正确;
故答案为:B;
(4)催化剂不能使平衡发生移动,该反应为放热反应,温度升高平衡逆向移动,则a点为200℃时使用催化剂甲下的平衡转化率应高于b点的转化率,与图像不符,故200℃时, a点对应的转化率(5%)不是使用催化剂甲下H2的平衡转化率。
【分析】(1)依据价层电子对数=σ键数+孤电子对数,由价层电子对数确定VSEPR模型,再确定空间立体构型;依据孤对电子之间排斥作用>孤对电子与成键电子对之间排斥>成键电子对之间排斥分析;
(2)依据盖斯定律分析;依据ΔG=ΔH-TΔS<0分析;
(3)利用三段式法计算;利用“变者不变即平衡”;
(4)依据影响反应速率和化学平衡的因素分析。
19.【答案】(1);在Fe基催化剂表面,吸附在的酸性配位点上形成,NO与吸附在配位点上形成,而后与结合生成的与NO反应生成、,并从催化剂表面逸出
(2)NO与反应生成是放热反应,低温时有利于反应的正向进行;;功率增大时,会产生更多的O*自由基,NO更易被氧化为;功率增大,和在放电时会生成NO;相比而言后者产生的NO更多
【解析】【解答】(1)①由已知③
④ ,
⑤
则①=×⑤+×④-×③,则×(-2780KJ/mol)+×(-112mol/mol)-×180.5/mol=;
②由图可知该过程可描述为在Fe基催化剂表面,吸附在的酸性配位点上形成,NO与吸附在配位点上形成,而后与结合生成的与NO反应生成、,并从催化剂表面逸出;
(2)①由题干信息可知一氧化氮和氧气的反应是放热反应,从平衡移动的角度分析,低温有利于平衡正向移动,故答案为:NO与反应生成是放热反应,低温时有利于反应的正向进行;
②4.6g的物质的量为0.1mol,此时转移0.05mol电子,说明该反应为歧化反应,即+4价氮反应后变为+3价和+5价,用碳酸根离子配平电荷即可,离子方程式为:;
③由图可知在高压放电下,产生自由基(O*),功率越大产生的自由基越多,自由基将NO氧化为的量也越多,但是在放电条件下氮气也可以和氧气反应生成一氧化氮,功率越大产生的一氧化氮越多,故答案为:功率增大时,会产生更多的O*自由基,NO更易被氧化为;功率增大,和在放电时会生成NO;相比而言后者产生的NO更多。
【分析】(1)利用盖斯定律进行运算,在进行方程式加减运算是,焓变也要相应进行运算,注意焓变的“+和-”号;
(2)①低温条件下可提高NO的转化率 ,说明低温使该反应平衡正向移动,所以要从温度对平衡移动角度分析;②分析可知,该离子反应为氧化还原反应,NO2反应歧化反应,利用化合价升降相等配平;③题目信息给出,高温条件下O2会产生O自由基,自由基会与NO氧化为NO2,所以从高压条件下会使NO转化率降低。
20.【答案】(1)1mol/L
(2)0.4mol/(L min)
(3)2
(4)①
【解析】【解答】解:5min末时测得C的物质的量为6mol,v(C)= =0.6mol/(L min),用D表示的化学反应速率v(D)为0.4mol/(L min),由速率之比等于化学计量数之比可知, ,解得x=2,则
A(g)+ 2B(g) 3C(g)+ 2D(g)
开始 4 6 0 0
转化 2 4 6 4
平衡 2 2 6 4
;(1)5min末A的物质的量浓度为 =1mo1/L,故答案为:1mol/L; (2)前5min内用B表示的化学反应速率v(B)为 =0.4mol/( L min ),故答案为:0.4mol/( L min );(3)由上述分析可知,n=2,故答案为:2;(4)反应速率与化学计量数的比值越大,反应速率越快,则①中 =5,②中 =3,③中 =1.5,④中 =4,显然①中比值最大,反应速率最快,故答案为:①.
【分析】5min末时测得C的物质的量为6mol,v(C)= =0.6mol/(L min),用D表示的化学反应速率v(D)为0.4mol/(L min),由速率之比等于化学计量数之比可知, ,解得x=2,则
A(g)+ 2B(g) 3C(g)+ 2D(g)
开始 4 6 0 0
转化 2 4 6 4
平衡 2 2 6 4
结合v= 、c= 及反应速率与化学计量数的比值越大,反应速率越快来解答.
21.【答案】(1)b=2a;=;c>2a
(2)升温;减小SO3浓度
【解析】【解答】解:(1)①相同温度下,若乙中通入6molN2和8molH2,且保持压强与甲相同,反应达到平衡时,平衡和甲中的平衡是等效的,所以生成NH3物质的量为bmol原投料时的2倍,即b=2a,物质的转化率是相等的,故答案为:b=2a;=;②若①中乙与甲的容积始终相等,达到平衡时,相当于在原来的基础上加压,使得合成氨的反应正向进行,此时c>2a,故答案为:c>2a;(2)①a时逆反应速率大于正反应速率,且正逆反应速率都增大,说明平衡应向逆反应方向移动,该反应的正反应放热,应为升高温度的结果,故答案为:升温;②b时正反应速率不变,逆反应速率减小,在此基础上逐渐减小,应为减小生成物的原因,若增大压强时,平衡向正反应方向移动,则正逆反应速率都增大,且正反应速率大于逆反应速率,图象应为
,
故答案为:减小SO3浓度.
【分析】(1)①根据恒温恒压下,所投进的物质等比即等效来回答;②根据压强对化学平衡移动的影响知识来回答判断;(2)根据正逆反应速率的变化结合温度、压强对反应速率和化学平衡的影响判断,a时逆反应速率大于正反应速率,且正逆反应速率都增大,b时正反应速率大于逆反应速率,注意逆反应速率突然减小的特点.
出卷网(www.chujuan.cn) 1 / 1
一、单选题
1.改变下列哪个条件,一定会引起平衡的移动( )
A.温度 B.浓度 C.压强 D.催化剂
2.合成氨工业中采用循环操作,主要是为了( )
A.增大化学反应速率 B.提高平衡混合物中氨的含量
C.降低氨的沸点 D.提高氮气和氢气的利用率
3.在一定条件下,反应2HI(g) H2(g)+I2(g)△H>0达到平衡时,要使混合气体的颜色变浅,可采取的措施是( )
①增大氢气的浓度 ②升高温度 ③降低温度 ④增大压强 ⑤增大HI的浓度 ⑥扩大体积 ⑦加催化剂.
A.①③⑥ B.③⑤⑥ C.①③⑤ D.②④⑤
4.下列化学反应中:Ag++Fe2+ Ag(固)+Fe3+(正反应放热)为使平衡体系析出更多的银,可采取的措施是( )
A.常温下加压 B.增加Fe3+的浓度
C.增加Fe2+的浓度 D.移去一些析出的银
5.为了探究外界条件对反应aX(g)+bY(g) cZ(g)的影响,以X和Y物质的量比为a∶b开始反应,通过实验得到不同条件下达到平衡时Z的物质的量分数,实验结果如下图所示。以下判断正确的是( )
A.ΔH>0,a+b>c B.ΔH>0,a+b
A.A、B全部变成了C和D
B.A,B,C,D四种物质的浓度一定相等
C.反应速率为零
D.单位时间内B消耗的物质的量和B生成的物质的量相等
7.温度为T℃时,向容积为2L的恒容密闭容器中充入一定量和,发生反应:,有关数据如下表所示。下列说法正确的是( )
反应物 CO
起始时的物质的量/mol 1.2 0.6
平衡时的物质的量/mol 0.9 0.3
A.平衡时,CO和的转化率相等
B.平衡时,反应放出的热量为
C.平衡时,CO的浓度是CO2浓度的3倍
D.T℃时。该反应的平衡常数
8.在一定条件下,反应:2NO+O2 NO2在定容容器中发生,对该反应达到平衡的标志的描述中,错误的是( )
A.混合气体的总分子数不再变化 B.混合气体的颜色不再变化
C.容器的总压强不再变化 D.混合气体的总质量不再变化
9.硫酸是一种重要的化工产品,硫酸的消耗量常被视为一个国家工业发展水平的一种标志.目前的重要生产方法是“接触法”,有关接触氧化反应2SO2+O2 2SO3,的说法不正确的是( )
A.该反应为可逆反应,故在一定条件下二氧化硫和氧气不可能全部转化为三氧化硫
B.达到平衡后,反应就停止了,故此时正、逆反应速率相等且均为零
C.一定条件下,向某密闭容器中加入2molSO2和1molO2,则从反应开始到达到平衡的过程中,正反应速率不断减小,逆反应速率不断增大,某一时刻,正、逆反应速率相等
D.在利用上述反应生产三氧化硫时,要同时考虑反应所能达到的限度和化学反应速率两方面的问题
10.下列事实中,不能用勒夏特列原理解释的有几项( )
①Fe(SCN)3溶液中加入固体KSCN后颜色变深
②将混合气体中的氨液化有利于合成氨反应
③实验室常用排饱和食盐水的方法收集氯气
④红棕色NO2气体加压后颜色先变深后变浅
⑤加入催化剂有利于合成氨的反应
⑥由H2(g)、I2(g)和HI(g)组成的平衡体系加压后颜色变深
⑦500 ℃时比室温更有利于合成氨的反应
A.三项 B.四项 C.五项 D.六项
11.一定温度下,在容积为2L的恒容密闭容器中发生反应,加入1molA和1molB,经5s反应达平衡,此时容器内的压强与起始时压强比为6:5,同时生成0.4molD,下列叙述中不正确的是( )
A.
B.5s内B的平均反应速率
C.当混合气体的密度不再改变时,该反应已达到平衡状态
D.当时,标志着该反应达到平衡状态
12.对于反应2HI(g) H2(g) +I2(g),下列叙述能够说明己达平衡状态的是( )
A.混合气体的颜色不再变化
B.温度和体积一定时,容器内压强不再变化
C.1molH-H键生成的同时有2molH-I键断裂
D.各物质的物质的量浓度之比为2:1:1
13.在一个不传热的固定容积的密闭容器中发生可逆反应:
mA(g)+nB(g) pC(g)+qD(g)(m、n、p、q为任意整数)。下列不能作为达到平衡状态的标志的是( )
A.单位时间内有m mol A消耗,同时有p mol C生成
B.体系的温度不再改变
C.各组分的浓度不再改变
D.各组分的质量分数不再改变
14.在一定温度下的恒容容器中,当下列物理量不再发生变化时,表明反应: A(s)+3B(g) 2C(g)+D(g)已达平衡状态的是( )
A.混合气体的压强 B.混合气体的密度
C.体系的温度 D.气体的总物质的量
15.在恒定的某温度下,三个容积均为2.0 L的恒容密闭容器中发生如下反应:,各容器中起始物质的量浓度与反应温度(已知)如表所示:
容器 温度/℃ 起始物质的量浓度
甲 0.10 0.10 0 0
乙 0 0 0.10 0.20
丙 0.10 0.10 0 0
反应过程中甲、丙容器中的物质的量随时间变化关系如图所示。下列说法错误的是( )
A.该反应的正反应为放热反应,平衡常数
B.达到平衡时,乙容器中的压强一定小于甲容器的2倍
C.乙容器中反应达到平衡时,的转化率大于40%
D.丙容器中反应达到平衡后,再充入0.10 mol NO和0.10 mol ,此时v(正)>v(逆)
16.下列说法正确的是( )
A.增加水的量或升高温度,可以加快镁跟水的反应速率
B.增大硫酸的浓度,一定可以加快锌与硫酸反应制取氢气的速率
C.在反应2H++S2O32﹣=S↓+SO2+H2O中,增大压强,可以加快硫析出的速率
D.煅烧硫铁矿时,把硫铁矿粉碎或通入纯O2可加快反应的速率
二、综合题
17.2021年国务院政府工作报告明确提出要制定2030年前碳排放达峰行动方案。如何实现碳的氧化物的资源化利用解决温室效应问题是当前科学家亟待解决的问题。请回答下列问题:
(1)一定温度下,测得、和的燃烧热分别为、和,由
可知 。
(2)在恒温恒容条件下,下列不能说明反应达到平衡状态的是 (填序号)。
a.
b.混合气体的密度不变
c.混合气体的平均摩尔质量不变
d.化学平衡常数不变
e.混合气体的压强不变
(3)在2 L恒容密闭容器中分别加入和,测得反应容器中平衡转化率、选择性、CO选择性随温度的变化关系如下图所示[已知:]
①试分析选择性在240 ℃后显著降低的可能原因是 。
②240 ℃时,10 min后上述反应达到平衡,测得平衡转化率为25%,选择性为60%,则用表示的化学反应速率为 ,反应的平衡常数为 (用浓度列出表达式)。
(4)利用电化学转化法,如图所示,在微生物的作用下,二氧化碳可自发地转化为甲醇,则电极A的名称为 ,N为 (填“阴”或“阳”离子交换膜,一段时间后,电极B附近溶液的pH (填“变大”“基本不变”或“变小”。)
18.氨基甲酸铵(H2NCOONH4)为尿素生产过程的中间产物,易分解。
已知:
Ⅰ.N2(g)+3H2(g) 2NH3(g) ΔH1= -92 kJ·mol-1
Ⅱ. C(s)+O2(g) CO2(g) ΔH2= - 394 kJ·mol-1
Ⅲ. N2(g)+ 3H2(g)+C(s)+O2(g) H2NCOONH4(s) ΔH3= - 646 kJ·mol-1
Ⅳ.H2NCOONH4(s) 2NH3(g)+ CO2(g) ΔH4
回答下列问题:
(1)NH3的空间构型为 。NH3的键角大于PH3, 分析原因: 。
(2)ΔH4= 。 T℃下在某密闭容器中加入H2NCOONH4(s),假设只发生反应Ⅳ,达平衡时测得NH3的浓度为c1;保持温度不变,加压(缩小容器的体积),测得新的平衡条件下NH3的浓度为c2,则c1 c 2(填“>” “<”或“=”)。反应Ⅳ在 (填“高温” “低温”或“任意温度”)条件下能够自发进行。
(3)某温度下在一刚性的密闭容器中,充入等物质的量N2和H2发生反应Ⅰ,起始压强为1MPa, 10min 末达平衡,测得平衡时压强为0.8MPa,则10min内v(N2)= MPa/min。此时平衡常数Kp= 。对于该条件下的反应,下列说法错误的是 。
A.当N2的体积分数不变时,说明反应已经达到化学平衡状态
B.温度升高化学反应速率加快,化学平衡常数增大
C.其他条件不变时,若适当增加N2的用量,可以提高H2的平衡转化率
D.使用合适的催化剂可以加快化学反应速率,但ΔH1不变
(4)在一定的条件 下,将AmolN2和BmolH2充入某体积固定的密闭容器中合成NH3,在不同的催化剂(甲或乙)下发生反应,反应相同时间后H2的转化率与温度的关系如图:
某学习小组的同学通过讨论得出结论: 200℃时, a点对应的转化率(5%)不是使用催化剂甲下H2的平衡转化率。判断依据是: 。
19.研究脱除烟气中的NO是环境保护、促进社会可持续发展的重要课题。选择性催化还原技术是利用还原剂氨或尿素,把烟气中的NO还原成和。相关反应方程式如下:
(1)① 。
②有氧条件下,在Fe基催化剂表面,还原NO的反应机理如图所示,该过程可描述为 。
(2)近年来,低温等离子体(NTP)技术是在高压放电下,产生自由基(O*),自由基将NO氧化为后,再用溶液吸收,便达到消除NO的目的。实验室将模拟气(、、NO)以一定流速通入低温等离子体装置,实验装置如图所示。
①等离子体技术在低温条件下可提高NO的转化率,原因是 。
②若4.6g被含0.05mol 溶液充分吸收,转移电子数为0.05mol,则此反应的离子方程式为 。
③其他条件相同,等离子体的功率与NO的转化率关系如图所示,当功率大于30W时,NO转化率下降的原因可能是 。
20.在容积为2L的密闭容器中进行如下反应:A(g)+2B(g) 3C(g)+nD(g),开始时A为4mol,B为6mol;5min末时测得C的物质的量为6mol,用D表示的化学反应速率v(D)为0.4mol/(L min).请回答下列有关问题:
(1)5min末A的物质的量浓度为 .
(2)前5min内用B表示的化学反应速率v(B)为 .
(3)化学方程式中n值为 .
(4)此反应在四种不同情况下的反应速率分别为:
①v(A )=5mol/( L min ) ②v( B )=6mol/( L min )
③v(C)=4.5mol/( L min ) ④v(D )=8mol/( L min )
其中反应速率最快的是 (填编号).
21.有甲、乙两容器,甲的容积固定,乙的容积可变.在一定温度下,向甲中通入3molN2和4molH2,反应达到平衡时,生成NH3物质的量为amol.
(1)①相同温度下,若乙中通入6molN2和8molH2,且保持压强与甲相同,反应达到平衡时,生成NH3物质的量为bmol,则b与a的关系可表示为 ,两容器中氮气的转化率甲 乙(填“>”、“<”或“=”)
②若①中乙与甲的容积始终相等,达到平衡时,生成NH3物质的量为Cmol,则C与a的关系可表示为
(2)如图左表示在密闭容器中反应:2SO2+O2 2SO3+Q达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,
a 时刻改变的条件可能是 ;
b 时刻改变的条件可能是 .
答案解析部分
1.【答案】A
【解析】【解答】催化剂只影响化学反应速率,不一定引起平衡的移动;当一个反应的前后化学计量数之和相等时,压强也不一定引起平衡的移动;当反应中各物质的浓度均按照化学计量数变化时,也不一定引起平衡的移动;故B、C、D选项错误;当温度改变时,反应的平衡常数改变,化学反应重新达到新的状态,一定会引起平衡的移动。故A项正确。
【分析】增大反应物或减少生成物浓度,平衡朝正反应移动
增大生成物或减少反应物浓度,平衡朝逆反应移动
升高温度,平衡朝吸热方向移动
降低温度,平衡朝放热方向移动
左右两边气体系数不相同
增大压强,缩小体积,平衡朝气体体积缩小的方向移动
减小压强,增大体积,平衡朝气体体积增大的方向移动
恒压下,充入不反应气体则增大体积,往体积增大移动
恒容下,充入不反应气体,速率不变,平衡不移动
左右两边气体系数相同,改变压强平衡不移动
加入催化剂,速率增大,平衡不移动
2.【答案】D
【解析】【解答】合成氨工业中氢气和氮气在催化剂作用下生成氨气的反应为可逆反应,反应后的混合气分离出氨气后还含有氢气和氮气,进行循环操作可以提高氮气和氢气的利用率,降低成本;与增大化学反应速率、提高平衡混合物中氨的含量、降低氨的沸点无必然关系;
故答案为:D。
【分析】由于合成氨反应为可逆反应,且转化率很低,原料不能很好地利用,采用循环操作目的为提高原料转化率。
3.【答案】A
【解析】【解答】解:①增大氢气的浓度,平衡逆向移动,混合气体的颜色变浅,故正确;
②升高温度,平衡正向移动,混合气体的颜色加深,故错误;
③降低温度,平衡逆向移动,混合气体的颜色变浅,故正确;
④增大压强,相当于缩小体积,各种气体的浓度都增大,混合气体的颜色加深,故错误;
⑤增大HI浓度,平衡正向移动,碘浓度增大,混合气体的颜色加深,故错误;
⑥减小压强,各气体浓度减小,混合气体的颜色变浅,故正确;
⑦加催化剂,平衡不移动,混合气体的颜色不变,故错误;
故选A.
【分析】要使混合气体的颜色变浅,即减小碘的浓度,平衡逆向移动,从影响平衡移动的因素角度考虑.
4.【答案】C
【解析】【解答】A. 常温下加压对此反应无影响,A不符合题意;
B. 增加Fe3+的浓度,平衡逆向移动,不能析出更多的银,B不符合题意;
C. 增加Fe2+的浓度,平衡正向移动,能析出更多的银,C符合题意;
D. Ag为固体,移去一些析出的银,平衡不移动,D不符合题意。
故答案为:C。
【分析】A.该反应中没有气体参加,改变压强不能使平衡发生移动;
B.增大生成物浓度平衡逆向移动;
C.增大反应物浓度平衡正向移动;
D.银为固体,减少银的量,平衡不移动。
5.【答案】C
【解析】【解答】根据图像可知压强相同时升高温度Z的含量降低,所以正反应是放热反应;温度相同时增大压强Z的含量升高,这说明正反应是体积减小的,则有△H<0,a+b>c,
故答案为:C。
【分析】根据勒夏特列原理,温度升高,反应逆向移动,为放热反应
压强增大,正向移动,则a+b>c
6.【答案】D
【解析】【解答】A.反应2A(g) + B(g) C(g) + 3D(g),达到平衡时,各组成含量保持不变,反应是可逆反应不能进行彻底,故A不符合题意;
B. 物质浓度和起始量、变化量有关,平衡状态下A、B、C、D四种物质的浓度不一定相等,故B不符合题意;
C.平衡状态是动态平衡,V正=V逆 0,反应仍在进行,反应未停止,故C不符合题意;
D. 单位时间内B消耗的物质的量和B生成的物质的量相等说明反应达到平衡状态,故D符合题意;
故答案为:D
【分析】根据化学平衡状态的特征进行解答。当反应达到平衡状态时,正逆反应速率相等(且不为0),达到一种动态的平衡;各物质的溶度、百分含量不变,以及由此衍生的一些量也不发生改变;对于反应前后气体分子数不同的反应,如果气体的压强不变,则其达到了平衡状态;由此即可得出答案。
7.【答案】C
【解析】【解答】A.起始时CO和物质的量不相等,平衡时两者消耗的物质的量相等,因此平衡时,CO和的转化率不相等,故A不符合题意;
B.根据方程式分析消耗1molCO,反应放出41kJ的热量,平衡时,消耗0.3molCO,则反应放出的热量为12.3kJ,故B不符合题意;
C.根据改变量之比等于计量系数之比,消耗CO物质的量为0.3mol,因此生成二氧化碳物质的量为0.3mol,则平衡时CO物质的量是CO2物质的量的3倍,因此平衡时CO浓度是CO2浓度的3倍,故C符合题意;
D.T℃时,平衡时CO和物质的量分别为0.9mol、0.3mol,生成的二氧化碳和氢气物质的量都为0.3mol,则反应的平衡常数,故D不符合题意。
故答案为:C。
【分析】A、转化率=变化量/起始量;
B、结合热化学方程式给出的焓变计算;
C、结合三段式判断;
D、平衡常数=生成物浓度幂之积/反应物浓度幂之积。
8.【答案】D
【解析】【解答】解:A、混合气体的总分子数不再变化,说明各物质的量不变,反应达平衡状态,故A错误;
B、混合气体的颜色不再变化,说明二氧化氮的浓度不变,反应达平衡状态,故B错误;
C、容器的总压强不再变化,说明气体的物质的量不变,反应达平衡状态,故C错误;
D、混合气体的总质量一直不随时间的变化而变化,所以不一定平衡,故D正确;
故选D.
【分析】根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
9.【答案】B
【解析】【解答】解:A、可逆反应是在一定条件下不能进行彻底的反应,正反应和逆反应同时进行,该反应为可逆反应,故在一定条件下SO2和O2不可能全部转化为SO3 ,故A正确;
B、达到平衡后,正反应速率和逆反应速率相同,是动态平衡,速率不能为0,故B错误;
C、一定条件下,向某密闭容器中加入2 mol SO2和1mol O2,则从反应开始到平衡的过程中,正反应速率不断减小,逆反应速率不断增大,某一时刻,正、逆反应速率相等达到平衡,故C正确;
D、反应是放热反应,但为了反应速率需要一定温度,催化剂活性最大,压强在常温下,二氧化硫的转化率已经横高改变压强对转化率影响不大,故D正确;
故选B.
【分析】A、依据可逆反应的特征分析判断;
B、化学平衡是动态平衡,正反应速率和逆反应速率相同;
C、依据平衡建立的过程分析;
D、合成需要考虑温度压强对平衡的影响和经济效益.
10.【答案】A
【解析】【解答】①Fe(SCN)3溶液中加入固体KSCN固体,溶液中c(SCN-)增大,平衡向着生成Fe(SCN)3的方向进行,使得溶液颜色变深,可用勒夏特列原理解释,①不符合题意;
②合成氨反应中,将NH3液化,使得混合气体中c(NH3)减小,平衡正向移动,有利于合成氨反应,可用勒夏特列原理解释,②不符合题意;
③Cl2与H2O的反应为可逆反应Cl2+H2O HCl+HClO,由于饱和食盐水中c(Cl-)达到最大值,因此可抑制Cl2与H2O的反应,故可用排饱和食盐水的方法收集Cl3,可用勒夏特列原理解释,③不符合题意;
④NO2转化为N2O4的反应为2NO2(g) N2O4(g),加压后,体积减小,浓度增大,溶液的颜色变深;由于增大压强,平衡正向移动,因此气体的颜色又变浅,可用勒夏特列原理解释,④不符合题意;
⑤加入催化剂只能改变反应速率,不能改变平衡移动,因此加入催化剂有利于合成氨的反应,不能用勒夏特列原理解释,⑤符合题意;
⑥平衡体系中发生的反应为:H2(g)+I2(g) 2HI(g),由于反应前后气体分子数不变,因此加压对平衡移动无影响,颜色变深,是由于c(I2)增大引起,不能用勒夏特列原理解释,⑥符合题意;
⑦合成氨的反应为放热反应,升高温度不利于NH3的产生;而采用500℃是因为在该温度下催化剂的活性高,不可用勒夏特列原理解释,⑦符合题意;
综上,不能用勒夏特列原理解释的有⑤⑥⑦,共三项,A符合题意;
故答案为:A
【分析】能用勒夏特列原理解释,则过程中涉及可逆反应的平衡移动,据此分析。
11.【答案】B
【解析】【解答】A、反应前后,物质的量之比等于压强之比,则有,解得a=0.8,则,解得x=4,故A正确;
B、5s内B的平均反应速率 ,故B错误;
C、随着反应的进行,混合气体的密度发生变化,当当混合气体的密度不再改变时,该反应已达到平衡状态,故C正确;
D、 当时,正逆反应速率相等,该反应达到平衡状态,故D正确;
故答案为:B。
【分析】达到平衡时,生成0.4molD,设同时生成amolC,则有三段式:
。
12.【答案】A
【解析】【解答】A.混合气体的颜色不再变化,说明碘蒸气的浓度不变,达平衡状态,故A符合题意;
B.气体两边的计量数相等,所以温度和体积一定时,容器内压强一直不变化,故B不符合题意;
C.1molH-H键生成的同时有2molH-I键断裂,都体现正反应方向,未体现正与逆的关系,故C不符合题意;
D.当体系达平衡状态时,各物质的物质的量浓度之比可能为2:1:1,也可能不是2:1:1,与各物质的初始浓度及转化率有关,故D不符合题意;
故答案为:A。
【分析】化学平衡状态的判断方法
1、达到化学平衡状态的本质标志
化学平衡状态的本质标志是:正反应速率等于逆反应速率,但不等于零,v正=v逆是对同一反应物或同一生成物而言。对某一反应物来说,正反应消耗掉反应物的速度等于逆反应生成该反应物的速度。
2、达到化学平衡状态的等价标志
所谓“等价标志”是指可以间接衡量某一可逆反应是否达到化学平衡状态的标志。
(1)与v正=v逆等价的标志
①同一物质:该物质的生成速率等于它的消耗速率,如:v正生成=v逆消耗。
②不同的物质:速率之比等于化学方程式中的化学计量数之比,但必须是不同方向的速率,如:v正生成:v逆消耗=m:n。
③可逆反应的正、逆反应速率不再随时间发生变化。
④化学键断裂情况=化学键生成情况。对同一物质而言,断裂化学键的物质的量与形成化学键的物质的量相等。对不同物质而言,与各物质的化学计量数和分子内的化学键多少有关。
(2)反应混合物中各组成成分的含量保持不变
①质量不再改变:各组成成分的质量不再改变,各反应物或生成物的总质量不再改变(不是指反应物的生成物的总质量不变),各组分的质量分数不再改变。
②物质的量不再改变:各组分的物质的量不再改变,各组分的物质的量分数不再改变,各反应物或生成物的总物质的量不再改变。
③对气体物质:若反应前后的物质都是气体,且化学计量数不等,总物质的量、总压强(恒温、恒容)、平均摩尔质量、混合气体的密度(恒温、恒压)保持不变。
④反应物的转化率、产物的产率保持不变。
⑤有颜色变化的体系颜色不再发生变化。
⑥物质的量浓度不再改变。当各组分(不包括固体或纯液体)的物质的量浓度不再改变时,则达到了化学平衡状态。
13.【答案】A
【解析】【解答】A.单位时间内物质的变化量之比与化学计量系数之比相等不能说明其达到平衡,故A符合题意;
B.该反应温度不变可说明反应得到平衡,故B不符合题意;
C.各组分的浓度不变可说明达到平衡,故C不符合题意;
D.各组分的质量分数不变也可说明其平衡,故D不符合题意;
故答案为:A
【分析】根据 在一个不传热的固定容积的密闭容器中发生可逆反应: 判断达到平衡可以根据,温度不变,浓度不变,组分不变等,结合选项判断即可。
14.【答案】B
【解析】【解答】A、可逆反应: A(s)+3B(g) 2C(g)+D(g),反应前后,气体的物质的量不发生变化,体积恒定,反应自开始到平衡,压强都是一定值,故A不符合题意;
B、A是固体,随着反应进行,气体的质量在增加而体积不变,故气体的密度是变量。当气体的总质量不发生变化时,气体的密度也不再变化,说明到达平衡状态,故B符合题意;
C、该反应是在一定温度下的恒容容器中进行的,所以无论该反应是否达到平衡状态, 体系的温度保持不变,不能判定反应达到平衡状态,故C不符合题意;
D.该反应是一个反应前后气体体积不变的化学反应,无论该反应是否达到平衡状态,气体的总物质的量始终不变,故D不符合题意;
故答案为:B。
【分析】A.该反应是一个反应前后气体体积不变的反应,压强始终不变;
B.A是固体,反映进行过程中气体质量会变化;
C.温度是确定的,始终不变;
D.该反应是一个反应前后气体体积不变的反应。
15.【答案】C
【解析】【解答】A.先拐先平温度高,甲平衡状态二氧化碳物质的量小,说明温度越高平衡逆向进行,逆反应为吸热反应,正反应为放热反应,温度T1>T2,平衡常数K(T1)
C.由图象可知,丙中达到平衡状态二氧化碳0.12mol,
乙若达到相同平衡状态,体积增大一倍,浓度变为原来的二分之一,
此时氮气转化率,但相同体积条件下,相当于体积缩小压强增大平衡正向进行,氮气转化率小于40%,故C符合题意;
D.结合表格中丙的相关数据,列“三段式”:
平衡常数,丙容器中反应达到平衡后,再充0.10 mol NO和0.10 mol CO2,浓度商Qc=,平衡正向进行,此时v(正)>v(逆),故D不符合题意;
故答案为:C。
【分析】A.温度越高反应速率越快,达到平衡的时间越短,升温甲平衡状态二氧化碳物质的量小,说明升温平衡逆向移动,正反应为放热反应;
B.乙中生成物物质的量转化为反应物的物质的量时恰好是甲的2倍,若甲乙温度相同且甲乙中反应物转化率相同时,乙容器中压强是甲的2倍,但温度:T1>T2,即甲>乙,降低温度,平衡正向移动,故达到平衡时,乙容器中的压强小于甲容器的2倍;
D.计算此时的浓度熵,与平衡常数比较两者相对大小,确定平衡进行的方向。
16.【答案】D
【解析】【解答】A.增加水的量,浓度不变,则反应速率不变,故A错误;
B.浓硫酸与锌反应不生成氢气,故B错误;
C.反应在溶液中进行,增大压强,溶液浓度不变,则速率不变,故C错误;
D.增大固体表面积或增大反应物浓度,反应速率增大,故D正确.
故选D.
【分析】A.增加水的量,反应速率不变;
B.浓硫酸与锌反应不生成氢气;
C.反应在溶液中进行,增大压强,速率不变;
D.增大固体表面积或增大反应物浓度,反应速率增大.
17.【答案】(1)﹣87.6
(2)bd
(3)催化剂活性降低(合成甲醇为放热反应,温度升高,平衡逆向移动等合理答案都行);0.015;
(4)正极;阴;变小
【解析】【解答】(1)一定温度下,测得、和的燃烧热分别为、和,
则①
②
③
④
根据盖斯定律①+②×2+④-③得-283-285.8×2+40.9+726.1=-87.6;
(2)a.,正逆反应速率相等,反应一定达到平衡状态,故不选a;
b.反应前后气体总质量不变,容器体积不变,密度是恒量,混合气体的密度不变,反应不一定平衡,
故答案为:b;
c.反应前后气体物质的量改变,气体总质量不变,所以平均摩尔质量是变量,混合气体的平均摩尔质量不变,反应一定达到平衡状态,故不选c;
d.恒温条件下,平衡常数是恒量,化学平衡常数不变,反应不一定平衡,
故答案为:d;
e.反应前后气体物质的量改变,容器体积不变,压强是变量,混合气体的压强不变,反应一定达到平衡状态,故不选e;
选bd;
(3)①催化剂能够改变反应的活化能,但催化剂受温度影响较大,温度升高,催化剂活性可能降低,造成选择性降低;或者根据两个反应,第一个反应生成CO为吸热反应,温度升高,平衡正向移动,而合成甲醇为放热反应,温度升高,转化率降低;所以选择性在240 ℃后显著降低。
②240 ℃时,10 min后上述反应达到平衡,测得平衡转化率为25%,选择性为60%,则生成甲醇的物质的量是2mol×25%×60%=0.3mol;反应消耗二氧化碳2mol×25%-0.3mol=0.2mol,消耗氢气0.2mol,生成水0.2mol;反应消耗二氧化碳0.3mol、消耗氢气0.9mol、生成水0.3mol,则容器中二氧化碳的物质的量是1.5mol、氢气的物质的量是6mol-0.2mol-0.9mol=4.9mol、甲醇的物质的量是0.3mol、水的物质的量是0.5mol,
用表示的化学反应速率为,反应的平衡常数为。
(4)根据图示可知,二氧化碳在电极A得电子发生还原反应生成甲醇,A为正极;负极氢气失电子变成氢离子,中间的硫酸根离子经过阴离子交换膜N进入右侧形成硫酸,故离子交换膜N为阴离子交换膜,电极B附近溶液的pH降低。
【分析】(1)根据盖斯定律计算;
(2)依据化学平衡的特征“等”和“定”进行分析判断;
(3)①催化剂有高效性和选择性;
②利用“三段式”法计算。
(4)根据正极得电子发生还原反应;负极失电子,阴离子经过阴离子交换膜分析。
18.【答案】(1)三角锥形;中心原子均为sp3杂化,且都只有一对孤电子对,电负性N>P,NH3中的键合电子(共用电子对)离中心原子更近,排斥力更大,键角越大
(2)+160kJ·mol-l;=;高温
(3)0.01;12.5( MPa)-2;B
(4)催化剂不能使平衡发生移动,该反应为放热反应,温度升高平衡逆向移动,则a点为200℃时使用催化剂甲下的平衡转化率应高于b点的转化率
【解析】【分析】(1)NH3中心原子氮原子形成3个共价键且含有1对孤电子对,为sp3杂化,空间构型为三角锥形;NH3的键角大于PH3,原因为:中心原子均为sp3杂化,且都只有一对孤电子对,电负性N>P,NH3 中的键合电子(共用电子对)离中心原子更近,排斥力更大,键角越大;
(2)已知:
Ⅰ.N2(g)+3H2(g) 2NH3(g) ΔH1= -92 kJ·mol-1
Ⅱ. C(s)+O2(g) CO2(g)|ΔH2= - 394 kJ·mol-1
Ⅲ. N2(g)+ 3H2(g)+C(s)+O2(g) H2NCOONH4(s) ΔH3= - 646 kJ·mol-1
由盖斯定律可知,Ⅰ+Ⅱ-Ⅲ得到反应Ⅳ.H2NCOONH4(s) 2NH3(g)+ CO2(g),故ΔH4=ΔH1+ΔH2-ΔH3=+160 kJ·mol-1;
反应Ⅳ的平衡常数为:K=c2(NH3)c(CO2),密闭容器中加入H2NCOONH4(s),保持温度不变,加压平衡常数不变,则新的平衡条件下NH3的浓度为c2=c1;反应Ⅳ为吸热的熵增反应,故在高温条件下能够自发进行;
(3)刚性的密闭容器中,充入等物质的量N2和H2发生反应Ⅰ,假设投料均为1mol,起始压强为1MPa;10min 末达平衡,测得平衡时压强为0.8MPa,则总的物质的量为1.6mol,总的物质的量减小0.4mol,根据N2(g)+3H2(g) 2NH3(g)可知生成氨气0.4mol、消耗氮气、氢气分别为0.2mol、0.6mol,平衡时氮气、氢气、氨气分别为0.8mol、0.4mol、0.4mol,则10min内v(N2)=MPa/min。此时平衡常数Kp=。
A.当N2的体积分数不变时,说明正逆反应速率相等,平衡不再移动,反应已经达到化学平衡状态,A正确;
B.反应为放热反应,温度升高化学反应速率加快,平衡逆向移动,化学平衡常数减小,B不正确;
C.其他条件不变时,若适当增加N2的用量,平衡正向移动,可以提高H2的平衡转化率,C正确;
D.使用合适的催化剂可以加快化学反应速率,但不该反应的焓变,故ΔH1不变,D正确;
故答案为:B;
(4)催化剂不能使平衡发生移动,该反应为放热反应,温度升高平衡逆向移动,则a点为200℃时使用催化剂甲下的平衡转化率应高于b点的转化率,与图像不符,故200℃时, a点对应的转化率(5%)不是使用催化剂甲下H2的平衡转化率。
【分析】(1)依据价层电子对数=σ键数+孤电子对数,由价层电子对数确定VSEPR模型,再确定空间立体构型;依据孤对电子之间排斥作用>孤对电子与成键电子对之间排斥>成键电子对之间排斥分析;
(2)依据盖斯定律分析;依据ΔG=ΔH-TΔS<0分析;
(3)利用三段式法计算;利用“变者不变即平衡”;
(4)依据影响反应速率和化学平衡的因素分析。
19.【答案】(1);在Fe基催化剂表面,吸附在的酸性配位点上形成,NO与吸附在配位点上形成,而后与结合生成的与NO反应生成、,并从催化剂表面逸出
(2)NO与反应生成是放热反应,低温时有利于反应的正向进行;;功率增大时,会产生更多的O*自由基,NO更易被氧化为;功率增大,和在放电时会生成NO;相比而言后者产生的NO更多
【解析】【解答】(1)①由已知③
④ ,
⑤
则①=×⑤+×④-×③,则×(-2780KJ/mol)+×(-112mol/mol)-×180.5/mol=;
②由图可知该过程可描述为在Fe基催化剂表面,吸附在的酸性配位点上形成,NO与吸附在配位点上形成,而后与结合生成的与NO反应生成、,并从催化剂表面逸出;
(2)①由题干信息可知一氧化氮和氧气的反应是放热反应,从平衡移动的角度分析,低温有利于平衡正向移动,故答案为:NO与反应生成是放热反应,低温时有利于反应的正向进行;
②4.6g的物质的量为0.1mol,此时转移0.05mol电子,说明该反应为歧化反应,即+4价氮反应后变为+3价和+5价,用碳酸根离子配平电荷即可,离子方程式为:;
③由图可知在高压放电下,产生自由基(O*),功率越大产生的自由基越多,自由基将NO氧化为的量也越多,但是在放电条件下氮气也可以和氧气反应生成一氧化氮,功率越大产生的一氧化氮越多,故答案为:功率增大时,会产生更多的O*自由基,NO更易被氧化为;功率增大,和在放电时会生成NO;相比而言后者产生的NO更多。
【分析】(1)利用盖斯定律进行运算,在进行方程式加减运算是,焓变也要相应进行运算,注意焓变的“+和-”号;
(2)①低温条件下可提高NO的转化率 ,说明低温使该反应平衡正向移动,所以要从温度对平衡移动角度分析;②分析可知,该离子反应为氧化还原反应,NO2反应歧化反应,利用化合价升降相等配平;③题目信息给出,高温条件下O2会产生O自由基,自由基会与NO氧化为NO2,所以从高压条件下会使NO转化率降低。
20.【答案】(1)1mol/L
(2)0.4mol/(L min)
(3)2
(4)①
【解析】【解答】解:5min末时测得C的物质的量为6mol,v(C)= =0.6mol/(L min),用D表示的化学反应速率v(D)为0.4mol/(L min),由速率之比等于化学计量数之比可知, ,解得x=2,则
A(g)+ 2B(g) 3C(g)+ 2D(g)
开始 4 6 0 0
转化 2 4 6 4
平衡 2 2 6 4
;(1)5min末A的物质的量浓度为 =1mo1/L,故答案为:1mol/L; (2)前5min内用B表示的化学反应速率v(B)为 =0.4mol/( L min ),故答案为:0.4mol/( L min );(3)由上述分析可知,n=2,故答案为:2;(4)反应速率与化学计量数的比值越大,反应速率越快,则①中 =5,②中 =3,③中 =1.5,④中 =4,显然①中比值最大,反应速率最快,故答案为:①.
【分析】5min末时测得C的物质的量为6mol,v(C)= =0.6mol/(L min),用D表示的化学反应速率v(D)为0.4mol/(L min),由速率之比等于化学计量数之比可知, ,解得x=2,则
A(g)+ 2B(g) 3C(g)+ 2D(g)
开始 4 6 0 0
转化 2 4 6 4
平衡 2 2 6 4
结合v= 、c= 及反应速率与化学计量数的比值越大,反应速率越快来解答.
21.【答案】(1)b=2a;=;c>2a
(2)升温;减小SO3浓度
【解析】【解答】解:(1)①相同温度下,若乙中通入6molN2和8molH2,且保持压强与甲相同,反应达到平衡时,平衡和甲中的平衡是等效的,所以生成NH3物质的量为bmol原投料时的2倍,即b=2a,物质的转化率是相等的,故答案为:b=2a;=;②若①中乙与甲的容积始终相等,达到平衡时,相当于在原来的基础上加压,使得合成氨的反应正向进行,此时c>2a,故答案为:c>2a;(2)①a时逆反应速率大于正反应速率,且正逆反应速率都增大,说明平衡应向逆反应方向移动,该反应的正反应放热,应为升高温度的结果,故答案为:升温;②b时正反应速率不变,逆反应速率减小,在此基础上逐渐减小,应为减小生成物的原因,若增大压强时,平衡向正反应方向移动,则正逆反应速率都增大,且正反应速率大于逆反应速率,图象应为
,
故答案为:减小SO3浓度.
【分析】(1)①根据恒温恒压下,所投进的物质等比即等效来回答;②根据压强对化学平衡移动的影响知识来回答判断;(2)根据正逆反应速率的变化结合温度、压强对反应速率和化学平衡的影响判断,a时逆反应速率大于正反应速率,且正逆反应速率都增大,b时正反应速率大于逆反应速率,注意逆反应速率突然减小的特点.
出卷网(www.chujuan.cn) 1 / 1
同课章节目录
- 第1章 化学反应与能量转化
- 第1节 化学反应的热效应
- 第2节 化学能转化为电能——电池
- 第3节 电能转化为化学能——电解
- 第4节 金属的腐蚀与防护
- 微项目 设计载人航天器用化学电池与氧气再生方案——化学反应中能量及物质的转化利用
- 第2章 化学反应的方向、 限度与速率
- 第1节 化学反应的方向
- 第2节 化学反应的限度
- 第3节 化学反应的速率
- 第4节 化学反应条件的优化——工业合成氨
- 微项目 探讨如何利用工业废气中的二氧化碳合成甲醇——化学反应选择与反应条件优化
- 第3章 物质在水溶液中的行为
- 第1节 水与水溶液
- 第2节 弱电解质的电离 盐类的水解
- 第3节 沉淀溶解平衡
- 第4节 离子反应
- 微项目 揭秘索尔维制碱法和侯氏制碱法——化学平衡思想的创造性应用
