1.3 烃 同步测试题(含解析) 2023-2024学年高二下学期化学鲁科版(2019)选择性必修3
文档属性
| 名称 | 1.3 烃 同步测试题(含解析) 2023-2024学年高二下学期化学鲁科版(2019)选择性必修3 |

|
|
| 格式 | docx | ||
| 文件大小 | 268.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-12-05 12:17:57 | ||
图片预览


文档简介
1.3 烃 同步测试题
一、单选题
1.由乙烯推测丙烯(CH2=CH—CH3)的结构或性质正确的是( )
A.不能使酸性高锰酸钾溶液褪色
B.不能在空气中燃烧
C.能使溴水褪色
D.与HCl在一定条件下能加成只得到一种产物
2.下列反应中,属于加成反应的是( )
A.CH3CH=CH2+Br2 CH3CHBrCH2Br
B.CH3CH2OH CH2=CH2↑+H2O
C.CH3COOH+CH3OH CH3COOCH3+H2O
D. +HNO3 -NO2+H2O
3.等物质的量的乙烯和甲烷,完全燃烧消耗氧气的物质的量的关系是( )
A.前者大 B.后者大 C.相等 D.不能确定
4.下列有关甲烷的叙述不正确的是( )
A.甲烷的二氯代物只有一种
B.甲烷性质稳定,通常情况下不与强酸、强碱、氧化剂反应
C.烷烃跟卤素单质在光照条件下能发生取代反应,烷烃燃烧时生成和
D.甲烷在光照条件下最多可以和发生取代反应
5.化学与生产、生活、社会密切相关。下列有关说法正确的是()
A.用浸泡过酸性高锰酸钾溶液的硅藻土吸收水果释放的乙烯,可达到水果保鲜的目的。
B.为了提高酒精的杀菌消毒效果,医院常用体积分数为100%的酒精。
C.氯仿是良好的溶剂,可广泛用于有机化工,对环境无影响。
D.石墨烯是一种从石墨材料中用“撕裂”方法“剥离”出的单层碳原子面材料,石墨烯和乙烯都属于烯烃。
6.下列关于实验室制取乙炔及其性质的说法正确的是
A.乙炔在空气中点燃,伴有明亮的火焰和浓黑烟
B.为了加快反应速率可用饱和食盐水代替水
C.实验室制取乙炔的反应为
D.用溴水除去乙炔中的杂质
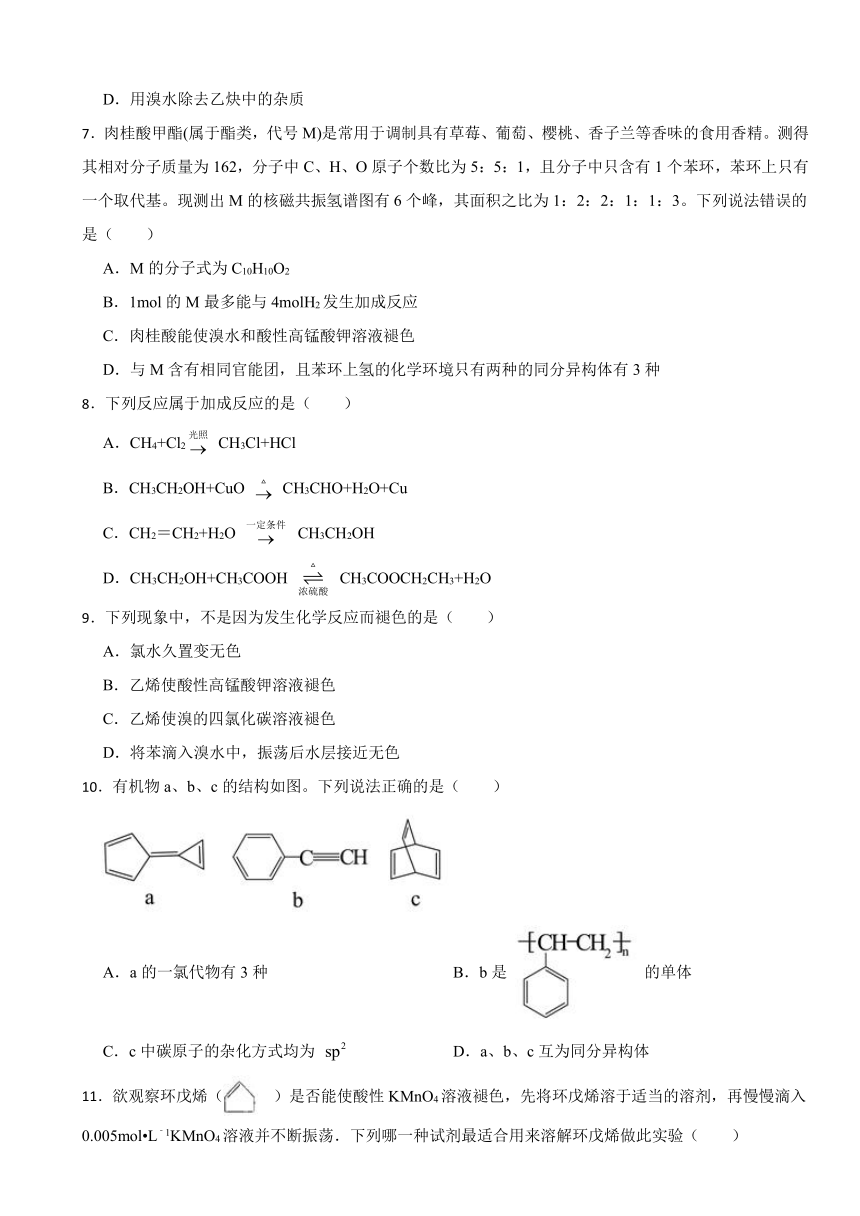
7.肉桂酸甲酯(属于酯类,代号M)是常用于调制具有草莓、葡萄、樱桃、香子兰等香味的食用香精。测得其相对分子质量为162,分子中C、H、O原子个数比为5:5:1,且分子中只含有1个苯环,苯环上只有一个取代基。现测出M的核磁共振氢谱图有6个峰,其面积之比为1:2:2:1:1:3。下列说法错误的是( )
A.M的分子式为C10H10O2
B.1mol的M最多能与4molH2发生加成反应
C.肉桂酸能使溴水和酸性高锰酸钾溶液褪色
D.与M含有相同官能团,且苯环上氢的化学环境只有两种的同分异构体有3种
8.下列反应属于加成反应的是( )
A.CH4+Cl2 CH3Cl+HCl
B.CH3CH2OH+CuO CH3CHO+H2O+Cu
C.CH2=CH2+H2O CH3CH2OH
D.CH3CH2OH+CH3COOH CH3COOCH2CH3+H2O
9.下列现象中,不是因为发生化学反应而褪色的是( )
A.氯水久置变无色
B.乙烯使酸性高锰酸钾溶液褪色
C.乙烯使溴的四氯化碳溶液褪色
D.将苯滴入溴水中,振荡后水层接近无色
10.有机物a、b、c的结构如图。下列说法正确的是( )
A.a的一氯代物有3种 B.b是 的单体
C.c中碳原子的杂化方式均为 D.a、b、c互为同分异构体
11.欲观察环戊烯( )是否能使酸性KMnO4溶液褪色,先将环戊烯溶于适当的溶剂,再慢慢滴入0.005mol L﹣1KMnO4溶液并不断振荡.下列哪一种试剂最适合用来溶解环戊烯做此实验( )
A.四氯化碳 B.裂化汽油 C.甲苯 D.水
12.关于化合物2-苯基丙烯( ),下列说法错误的是( )
A.能使稀高锰酸钾溶液褪色 B.可以发生加成聚合反应
C.分子中所有原子共平面 D.易溶于甲苯等有机溶剂
13.下列关于烯烃的化学性质的叙述正确的是( )
A.烯烃能使溴的CCl4溶液褪色,是因为烯烃与溴发生了取代反应
B.烯烃不能使酸性KMnO4溶液褪色
C.在一定条件下,烯烃能与H2、H2O、HX(卤化氢)发生加成反应
D.可用酸性高锰酸钾溶液除去甲烷中少量的乙烯
14.X、Y两种有机物的分子式不同,但均含有C、H或C、H、O,将X、Y以任意比例混合,只要物质的量之和不变,完全燃烧时所消耗的氧气量和生成水的物质的量也分别不变。则下列有关判断正确的是( )
A.X、Y分子式中氢原子数一定要相同,碳原子数必定相同
B.若X为CH4,则相对分子质量最小的Y是甲醇
C.若X为CH4,则相对分子质量最小的Y是乙二醇
D.X、Y的化学式应含有相同的氢原子数,且相差n个碳原子,同时相差2n个氧原子(n为正整数)
15.下列实验中,对应的现象以及结论都正确的是( )
选项 实验 现象 结论
A 铝丝用砂纸打磨后,放在冷的浓硝酸中浸泡一段时间后,放入CuSO4溶液中 铝丝表面变红色 铝可从铜盐溶液中置换出铜
B 溶有SO2的BaCl2溶液中通入气体X 有白色沉淀生成 X一定是Cl2
C 将盐酸与石灰石反应产生的气体通入硅酸钠溶液 硅酸钠溶液变浑浊 证明非金属性:Cl>C>Si
D 将乙烯通入溴的四氯化碳溶液 四氯化碳溶液最终变为无色 产物为无色且溶于四氯化碳
A.A B.B C.C D.D
16.下列属于加成反应的是( )
A.CH2=CH2 + H2O CH3CH2OH
B.CH4 + Cl2CH3Cl + HCl
C.2CH3CH2OH + O2CH3COOH + H2O
D.2CH3CH2OH+2Na 2CH3CH2ONa + H2↑
二、综合题
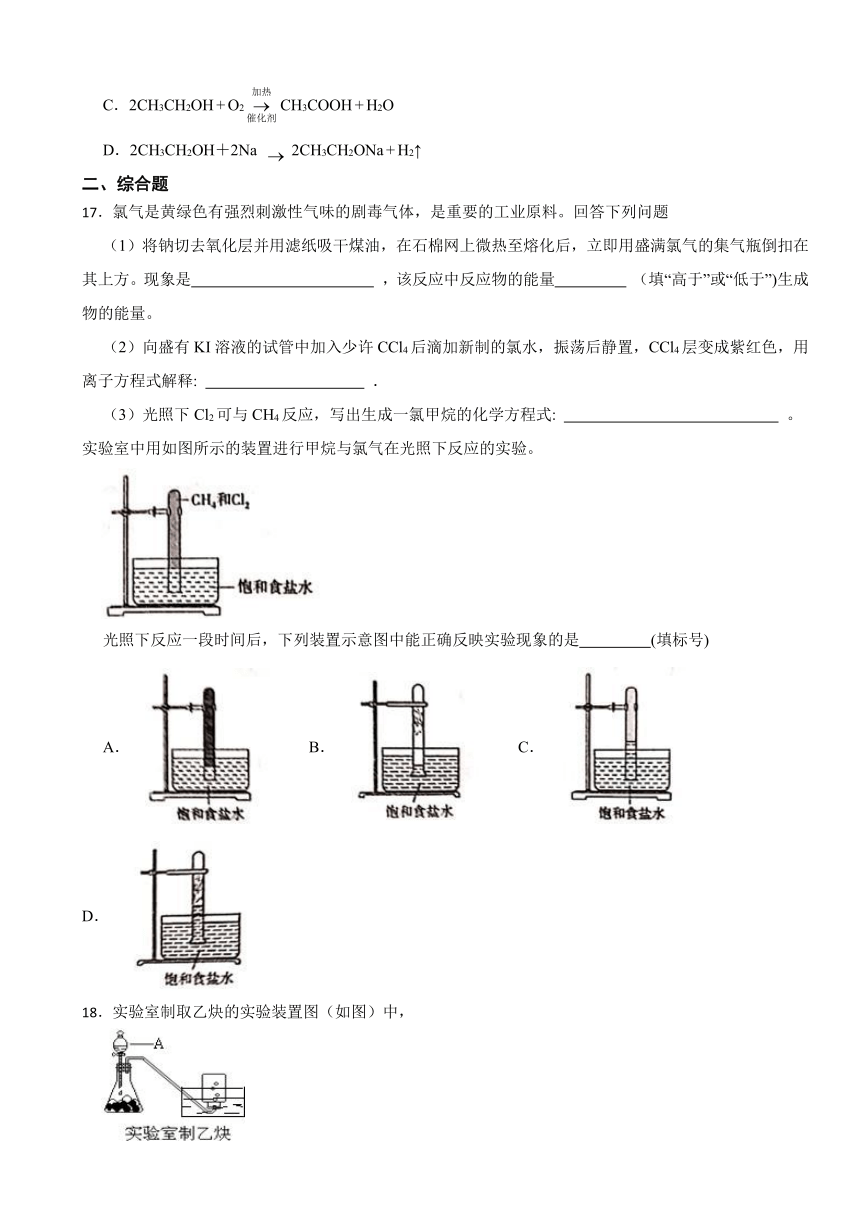
17.氯气是黄绿色有强烈刺激性气味的剧毒气体,是重要的工业原料。回答下列问题
(1)将钠切去氧化层并用滤纸吸干煤油,在石棉网上微热至熔化后,立即用盛满氯气的集气瓶倒扣在其上方。现象是 ,该反应中反应物的能量 (填“高于”或“低于”)生成物的能量。
(2)向盛有KI溶液的试管中加入少许CCl4后滴加新制的氯水,振荡后静置,CCl4层变成紫红色,用离子方程式解释: .
(3)光照下Cl2可与CH4反应,写出生成一氯甲烷的化学方程式: 。实验室中用如图所示的装置进行甲烷与氯气在光照下反应的实验。
光照下反应一段时间后,下列装置示意图中能正确反映实验现象的是 (填标号)
A. B. C. D.
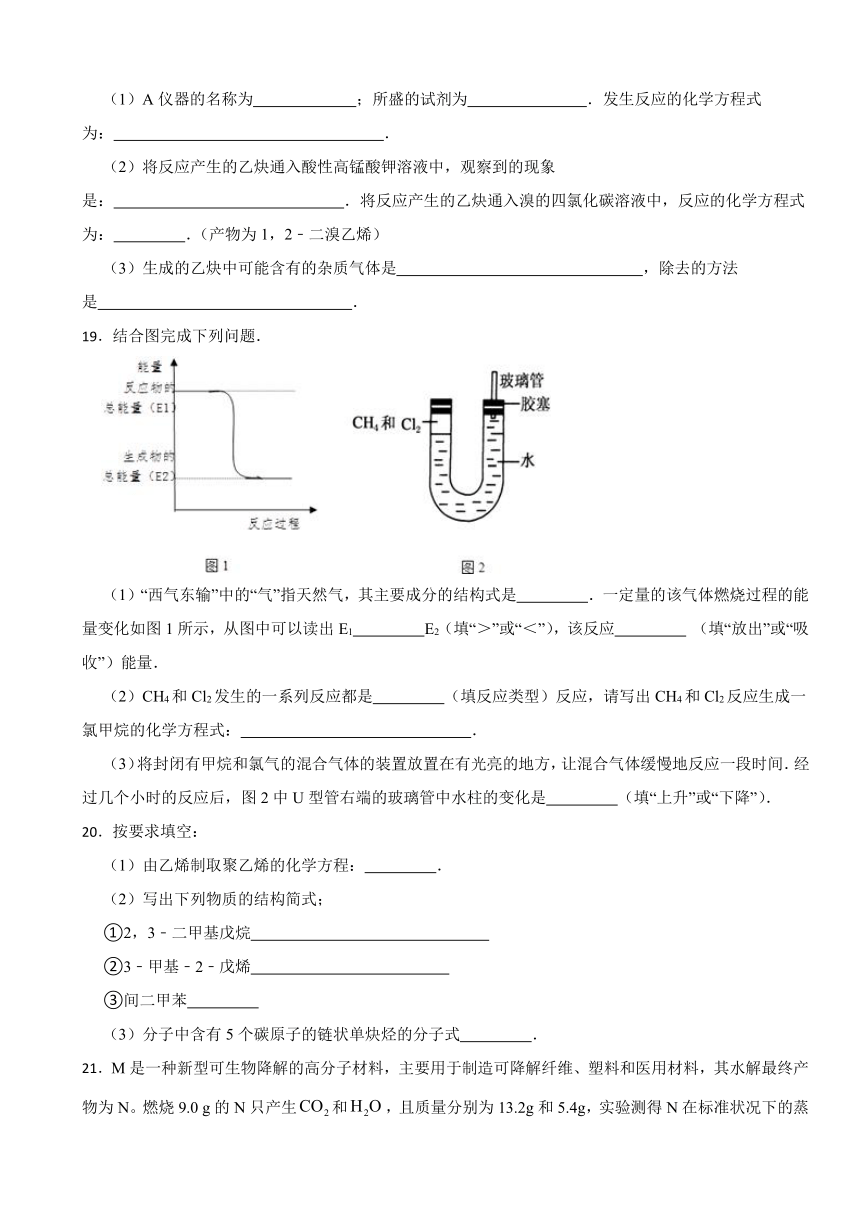
18.实验室制取乙炔的实验装置图(如图)中,
(1)A仪器的名称为 ;所盛的试剂为 .发生反应的化学方程式为: .
(2)将反应产生的乙炔通入酸性高锰酸钾溶液中,观察到的现象是: .将反应产生的乙炔通入溴的四氯化碳溶液中,反应的化学方程式为: .(产物为1,2﹣二溴乙烯)
(3)生成的乙炔中可能含有的杂质气体是 ,除去的方法是 .
19.结合图完成下列问题.
(1)“西气东输”中的“气”指天然气,其主要成分的结构式是 .一定量的该气体燃烧过程的能量变化如图1所示,从图中可以读出E1 E2(填“>”或“<”),该反应 (填“放出”或“吸收”)能量.
(2)CH4和Cl2发生的一系列反应都是 (填反应类型)反应,请写出CH4和Cl2反应生成一氯甲烷的化学方程式: .
(3)将封闭有甲烷和氯气的混合气体的装置放置在有光亮的地方,让混合气体缓慢地反应一段时间.经过几个小时的反应后,图2中U型管右端的玻璃管中水柱的变化是 (填“上升”或“下降”).
20.按要求填空:
(1)由乙烯制取聚乙烯的化学方程: .
(2)写出下列物质的结构简式;
①2,3﹣二甲基戊烷
②3﹣甲基﹣2﹣戊烯
③间二甲苯
(3)分子中含有5个碳原子的链状单炔烃的分子式 .
21.M是一种新型可生物降解的高分子材料,主要用于制造可降解纤维、塑料和医用材料,其水解最终产物为N。燃烧9.0 g的N只产生和,且质量分别为13.2g和5.4g,实验测得N在标准状况下的蒸气密度为;N分子中四种氢原子的个数比为1:1:1:3。
(1)写出N的分子式: 。
(2)写出N的结构简式: ,写出N在催化剂条件下发生缩聚反应合成M的化学方程式: 。
答案解析部分
1.【答案】C
【解析】【解答】根据丙烯的结构简式可知分子中含有碳碳双键,化学性质类似于乙烯,能使酸性高锰酸钾溶液褪色、能使溴水褪色、可以燃烧,与HCl在一定条件下能加成得到两种产物,即CH3CH2CH2Cl或CH3CHClCH3,
故答案为:C。
【分析】本题考查官能团(碳碳双键)的结构、特点。根据碳碳双键的特点进行分析解答即可。
2.【答案】A
【解析】【解答】A. 碳碳双键断裂,两个碳原子分别结合了1个溴原子,属于加成反应,A项符合题意;
B. CH3CH2OH CH2=CH2↑+H2O,属于消去反应,B项不符合题意;
C. CH3COOH+CH3OH CH3COOCH3+H2O,为酸与醇的酯化反应,属于取代反应,C项不符合题意;
D. +HNO3 -NO2+H2O,为苯的硝化反应,属于取代反应,D项不符合题意;
故答案为:A。
【分析】加成反应是有机物分子中的不饱和键断裂,断键原子与其他原子或原子团相结合,生成新的化合物的反应,据此判断。
3.【答案】A
【解析】【解答】乙烯分子式为C2H4,1mol乙烯完全燃烧消耗3mol氧气,甲烷分子式为CH4,1mol甲烷完全燃烧消耗2mol氧气,完全燃烧消耗氧气的物质的量的关系是前者大,
故答案为:A。
【分析】可根据甲烷和乙烯的燃烧方程式判断等物质的量的两种物质耗氧量的多少;也可根据等物质的量的甲烷和乙烯,乙烯比甲烷的碳原子的物质的量多来进行判断。
4.【答案】D
【解析】【解答】A、甲烷为正四面体结构,其二氯代物只有一种,A不符合题意。
B、甲烷的性质稳定,通常情况下不与强酸、强碱、氧化剂反应,B不符合题意。
C、烷烃在光照条件下能与卤素单质发生取代反应,完全燃烧时生成CO2和H2O,C不符合题意。
D、1molCH4能与4molCl2发生取代反应,D符合题意。
故答案为:D
【分析】A、甲烷的二氯代物只有一种。
B、甲烷性质稳定,不与强酸、强碱、氧化剂反应。
C、烷烃完全燃烧生成H2O和CO2。
D、1molCH4光照条件下可与4molCl2发生取代反应。
5.【答案】A
【解析】【解答】A.乙烯具有催熟作用,能被KMnO4溶液吸收,可用浸泡过酸性高锰酸钾溶液的硅藻土吸收水果释放的乙烯,起到水果保鲜的作用,A符合题意;
B.医用酒精的浓度为78%,用100%的酒精易造成酒精中毒,B不符合题意;
C.氯仿散发到空气中,易造成空气污染,C不符合题意;
D.石墨烯是碳的一种单质,不属于有机物,D不符合题意;
故答案为:A
【分析】A.乙烯能被KMnO4氧化;
B.医用酒精的浓度为78%;
C.氯仿会对环境造成污染;
D.石墨烯是碳的一种单质;
6.【答案】A
【解析】【解答】A.乙炔中含碳量高,则乙炔在空气中点燃,有明亮的火焰和浓黑烟,故A符合题意;
B.与水反应剧烈,选饱和食盐水代替水使反应平稳,故B不符合题意;
C.反应生成乙炔和氢氧化钙,则实验室制取乙炔的反应为:CaC2+2H2O→C2H2↑+Ca(OH)2,故C不符合题意;
D.乙炔含碳碳三键,与溴水发生加成反应,故D不符合题意;
故答案为:A。
【分析】 A.乙炔中含碳量较高;
B.用饱和食盐水代替水可减小反应速率;
C.实验室制取乙炔的反应为CaC2+2H2O→C2H2↑+Ca(OH)2;
D.乙炔会与溴水反应。
7.【答案】D
【解析】【解答】A.根据上述分析可知M的分子式为:C10H10O2,A不符合题意;
B.M的结构简式为:,碳碳双键和苯环可以和氢气发生加成反应,1mol的M最多能与4molH2发生加成反应,B不符合题意;
C.肉桂酸种含有碳碳双键,所以能使溴水和酸性高锰酸钾溶液褪色,C不符合题意;
D.与M含有相同官能团,则含有碳碳双键和酯基,且苯环上氢的化学环境只有两种,说明苯环有两个取代基,且位于对位,则对应的同分异构体有以下几种情况,①和、、-COOCH3,共3种,②和,共2种,③和-OOCH ,共2种,加一起一共7种,D符合题意;
故答案为:D。
【分析】M分子中C、H、O原子个数比为5:5:1,设分子式为(C5H5O)n,则81n=162,解得n=2,则M的分子式为C10H10O2,分子中只含有1个苯环,苯环上只有一个取代基。现测出M的核磁共振氢谱图有6个峰,其面积之比为1:2:2:1:1:3 ,则M的结构简式为。
8.【答案】C
【解析】【解答】A. CH4+Cl2 CH3Cl+HCl属于取代反应,故A不符合题意;
B. CH3CH2OH+CuO CH3CHO+H2O+Cu属于氧化反应,故B不符合题意;
C. CH2=CH2+H2O CH3CH2OH属于加成反应,故C符合题意;
D. CH3CH2OH+CH3COOH CH3COOCH2CH3+H2O属于酯化反应,故D不符合题意。
故答案为C。
【分析】加氢去氧是还原,加氧去氢是氧化,或则从化合价升降来分析反应。
9.【答案】D
【解析】【解答】A.氯水中存在可逆反应,次氯酸见光易分解生成HCl和氧气,次氯酸浓度减小,可逆反应平衡正向移动,氯气浓度减小,故久置变无色,故A不符合;
B.乙烯含有碳碳双键,能被酸性高锰酸钾溶液氧化从而使其褪色,故B不符合;
C.乙烯含有碳碳双键,能与溴的四氯化碳溶液发生加成反应从而使其褪色,故C不符合;
D. 溴单质易溶于苯中,将苯滴入溴水中振荡,苯将溴单质萃取,故水层接近无色,发生物理变化,故D符合;
故答案为:D。
【分析】A.氯气溶于水生成盐酸和次氯酸,次氯酸见光分解生成盐酸和氧气;
B.乙烯与酸性高锰酸钾发生氧化还原反应;
C.乙烯与溴的四氯化碳发生加成反应。
10.【答案】A
【解析】【解答】A.根据等效氢原理可知,a的一氯代物有3种如图所示: ,A符合题意;
B.b的加聚产物是: , 的单体是苯乙烯不是b,B不符合题意;
C.c中碳原子的杂化方式由6个 ,2个sp3,C不符合题意;
D.a、b、c的分子式分别为:C8H6,C8H6,C8H8,故c与a、b不互为同分异构体,D不符合题意;
故答案为:A。
【分析】
A.根据等效氢分析,含3种等效氢;
B.单体应是含碳碳双键;
C.杂化类型 、sp3两种;
D.分子式均不同,不属于同分异构。
11.【答案】A
【解析】【解答】A、四氯化碳不能够与高锰酸钾溶液反应,能够溶解该有机物,故A正确;
B、由于裂解汽油含有不饱和烃,能够使高锰酸钾溶液褪色,对实验带来干扰,故B错误;
C、由于甲苯能够使高锰酸钾溶液发生氧化反应,使高锰酸钾溶液褪色,对实验带来干扰,故C错误;
D、由于水不能够溶解该有机物,故D错误;
故选A.
【分析】A、四氯化碳是常用的有机溶剂,不能够与高锰酸钾溶液反应;
B、裂解汽油含有不饱和烃,能够使高锰酸钾溶液褪色;
C、甲苯能够使高锰酸钾溶液褪色;
D、水是无机溶剂,不能够溶剂该有机物.
12.【答案】C
【解析】【解答】A.该有机物中含有碳碳双键,可被酸性高锰酸钾氧化,故A不符合题意;
B.该有机物中含有碳碳双键,可发生加成聚合反应,故B不符合题意;
C.苯分子中所有原子共平面、乙烯分子中所有原子共平面,甲烷分子为正四面体结构,有3个原子共平面,该分子中甲基具有甲烷结构特点,所以该分子中所有原子不能共平面,故C符合题意;
D.该有机物中含有碳碳双键,没有亲水基团,故难溶于水,易溶于有机溶剂,故D不符合题意;
故答案为:C。
【分析】根据有机物结构式确定官能团,是双键,可发生加成反应和苯环上加成反应。结合碳原子的成键方式可判断原子是否共面
13.【答案】C
【解析】【解答】A.烯烃都含有碳碳双键,因此烯烃能使溴的CCl4溶液褪色,是因为烯烃与溴发生了加成反应,故A不符合题意;
B.烯烃都含有碳碳双键,能使酸性KMnO4溶液褪色,故B不符合题意;
C.在催化剂作用下,烯烃能与H2、H2O、HX(卤化氢)发生加成反应,故C符合题意;
D.不能用酸性高锰酸钾溶液除去甲烷中少量的乙烯,乙烯和酸性高锰酸钾反应生成二氧化碳,引入新的杂质,故D不符合题意。
故答案为:C。
【分析】A.烯烃中含有碳碳双键,能与溴发生了加成反应而使溴的CCl4溶液褪色;
B.烯烃中含有碳碳双键,能被KMnO4氧化而使酸性KMnO4溶液褪色;
C.烯烃中含有碳碳双键,能与H2、H2O、HX(卤化氢)发生加成反应;
D.乙烯和酸性高锰酸钾反应生成二氧化碳。
14.【答案】D
【解析】【解答】总物质的量一定时有机物完全燃烧时,生成水的质量和消耗O2的质量不变,则化学式中的氢原子个数相同,且在CxHyOz中(x+ )相同,如果X、Y的化学式应含有相同的氢原子数,且相差n个碳原子,同时相差2n个氧原子(n为正整数)。
A.X、Y分子式中氢原子数一定相同,碳原子数可能相同,A不符合题意;
B.若X为甲烷,另一种有机物分子中一定含有4个H,且耗氧量与甲烷相同,相对分子质量最小的Y为:C2H4O2,可能为甲酸甲酯,也可能是乙酸;甲醇和甲烷的耗氧量不同,故不可能为甲醇,B不符合题意;
C.乙二醇分子中含有6个H原子,与甲烷含有氢原子数不相同,不可能为乙二醇,C不符合题意;
D.X、Y的化学式应含有相同的氢原子数,则物质的量一定时生成水的量相同;若相差n个碳原子,同时相差2n个氧原子(n为正整数),则消耗氧气的量相同,D符合题意;
故合理选项是D。
【分析】根据总物质的量一定时有机物完全燃烧时,生成水的质量和消耗O2的质量不变,则化学式中的氢原子个数相同,且在CxHyOz中(x+ )相同,若X、Y的化学式应含有相同的氢原子数,且相差n个碳原子,同时相差2n个氧原子(n为正整数),据此对各选项进行判断。
15.【答案】D
【解析】【解答】A.铝丝用砂纸打磨后,放在冷的浓硝酸中浸泡一段时间后,发生钝化形成致密氧化膜,因为Al2O3与CuSO4不反应,所以放入CuSO4溶液中,铝丝表面不会生成铜,A不符合题意;
B.向溶有SO2的BaCl2溶液中通入气体X,产生的白色沉淀可能为亚硫酸钡或硫酸钡,则X可能为氨气或者氧化性气体(如氯气、臭氧等),B不符合题意;
C.比较元素的非金属性强弱,要看元素的最高价氧化物对应水化物的酸性强弱,所以不应该使用盐酸与石灰石反应,应该用高氯酸与石灰石反应,C不符合题意;
D.乙烯与溴单质发生加成反应生成无色1,2-二溴乙烷且溶于四氯化碳,所以将乙烯通入溴的四氯化碳溶液中,溶液最终变为无色,D符合题意;
故答案为:D
【分析】A.常温下,浓硝酸能使铝钝化;
B.产生的白色沉淀为BaSO4,则通入的气体具有氧化性,能将SO2氧化成SO42-;
C.证明非金属性的强弱,应用其最高价含氧酸的酸性强弱比较得出;
D.乙烯能与Br2发生加成反应,有机液体一般可互溶;
16.【答案】A
【解析】【解答】加成反应的特点是碳碳双键断开,断键位置各自加上1个原子或1个基团;
A、该反应为乙烯的加成反应,A正确;
B、该反应为甲烷的取代反应,B错误;
C、该反应为乙醇的催化氧化反应,C错误;
D、该反应为乙醇的取代反应,D错误;
故答案为:A
【分析】加成反应的特点是碳碳双键断开,断键位置各自加上1个原子或1个基团;取代反应的特点是两个分子发生反应,彼此交换原子或基团。
17.【答案】(1)剧烈燃烧,产生白烟;高于
(2)Cl2+2I-=I2+2Cl-
(3)Cl2+CH4 CH3Cl+HCl;D
【解析】【解答】(1)金属钠在氯气中剧烈燃烧,产生白烟;该反应过程中放出大量热,因此反应物的能量高于生成物的能量;
(2)CCl4层变成紫红色,说明有碘单质生成,该反应的化学方程式为:Cl2+2I-=I2+2Cl-;
(3)光照条件下, CH4与Cl2发生取代反应生成CH3Cl和HCl,该反应的化学方程式为: Cl2+CH4 CH3Cl+HCl;
CH4与Cl2的取代反应为多步同时进行的反应,生成物中CH3Cl为气体,CH2Cl2、CHCl3、CCl4都为有机液体,不溶于水,同时反应生成的HCl能溶于水;故反应后试管内有部分水进入,同时试管内液体出现分层、试管内有部分气体剩余,D符合题意;
【分析】(1)根据钠在氯气中燃烧的现象分析;
(2)CCl4层变成紫红色,说明有碘单质生成,结合氯气的氧化性强于碘单质的氧化性,书写反应的离子方程式;
(3)光照条件下, CH4与Cl2发生取代反应生成CH3Cl和HCl,据此写出反应的化学方程式;
CH4与Cl2的取代反应为多步同时进行的反应,根据生成物的性质分析;
18.【答案】(1)分液漏斗;饱和食盐水;CaC2+2H2O→Ca(OH)2+CH≡CH↑
(2)酸性高锰酸钾溶液紫色褪去;
(3)硫化氢、磷化氢(H2S、PH3);将混合气体通过CuSO4溶液洗气
【解析】【解答】解:(1)A仪器的名称为,碳化钙与水反应生成乙炔,反应非常剧烈,为了减慢反应的速率,通常用饱和食盐水与碳化钙反应,发生的反应方程式为:CaC2+2H2O→Ca(OH)2+CH≡CH↑,故答案为:分液漏斗;饱和食盐水; CaC2+2H2O→Ca(OH)2+CH≡CH↑;(2)乙炔中含有碳碳三键,具有还原性,能被酸性的高锰酸钾氧化而使高锰酸钾褪色,乙炔为不饱和烃与溴能1:1加成生成1,2﹣二溴乙烯,化学方程式为: ,故答案为:酸性高锰酸钾溶液紫色褪去; ;(3)电石主要成分是CaC2 ,还有杂质CaS Ca3P2等,这些杂质CaS、Ca3P2也能和水反应,生成H2S,PH3等杂质,H2S,PH3都与硫酸铜溶液发生反应而除去,故可以用硫酸铜溶液除去杂质;
故答案为:硫化氢、磷化氢(H2S、PH3);将混合气体通过CuSO4溶液洗气.
【分析】(1)熟悉常见仪器的名称,碳化钙与水反应生成乙炔;(2)依据乙炔中含有碳碳三键,能发生与溴发生加成反应,具有还原性,能使高锰酸钾褪色解答;(3)电石主要成分是CaC2,还有杂质CaS Ca3P2等,这些杂质CaS Ca3P2也能和水反应,生成H2S,PH3等杂质,可以用硫酸铜溶液除去.
19.【答案】(1);>;放出
(2)取代;CH4+Cl2 CH3Cl+HCl
(3)下降
【解析】【解答】解:(1)天然气主要成分为甲烷,是一个碳原子和四个氢原子形成的正四面体结构,故结构式为 ;从图像可知,E1>E2,而当反应物能量高于生成物能量时,反应放热,故答案为: ;>;放出;(2)甲烷和氯气在光照条件下发生取代反应,反应的化学方程式:CH4+Cl2 CH3Cl+HCl,故答案为:取代;CH4+Cl2 CH3Cl+HCl;(3)经过几个小时的反应后,消耗氯气,反应中气体的物质的量减少,所以压强减小,且生成的HCl能够溶解于水,U型管右端的玻璃管中水柱降低,故答案为:下降.
【分析】(1)天然气主要成分为甲烷,是一个碳原子和四个氢原子形成的正四面体结构,图像中反应物能量高于生成物为放热反应;(2)甲烷和氯气在光照条件下发生取代反应;(3)根据大气压强原理来判断U型管右端的玻璃管中水柱变化.
20.【答案】(1)
(2)(CH3)2CHCH(CH3)CH2CH3;CH3CH=C(CH3)CH2CH3;
(3)C5H8
【解析】【解答】解:(1)乙烯中含有碳碳双键,在适当的温度、压强、催化剂条件下,乙烯能发生加聚反应生成聚乙烯,反应方程式为: ,故答案为: ;(2)①2,3﹣二甲基戊烷,最长碳链为5,在2、3号碳上分别含有1个甲基,故结构简式为:(CH3)2CHCH(CH3)CH2CH3;故答案为:(CH3)2CHCH(CH3)CH2CH3;②依据系统命名方法,结合名称写出结构简式,3﹣甲基﹣2﹣戊烯的结构简式是:CH3CH=C(CH3)CH2CH3,故答案为:CH3CH=C(CH3)CH2CH3;③间二甲苯中苯环连接2个甲基且处于间位位置,起结构简式为: ,
故答案为: ;(3)链状单炔烃的通式CnH2n﹣2,5个碳原子的链状单炔烃的分子式为C5H8,故答案为:C5H8.
【分析】(1)乙烯含有碳碳双键,可发生加聚反应生成聚乙烯;(2)根据有机物的命名原则写出各有机物的结构简式:①遵循碳链最长,支链最多,该烷烃最长碳链为5,在2、3号碳上分别含有1个甲基,补齐氢原子;②给主链编号时从距离碳碳双键最近的一端开始,侧链视为取代基;③苯环连接2个甲基且处于间位位置;(3)可依据链状单炔烃的通式CnH2n﹣2书写.
21.【答案】(1)
(2);+(n-1)H2O
【解析】【解答】(1)N的摩尔质量,,N中:,,,则N的分子式为;
(2)N在催化剂的作用下发生缩聚反应生成M,由N的分子中四种氢原子的个数比为1∶1∶1∶3,可知N的结构简式为,缩聚反应的化学方程式为+(n-1)H2O。
【分析】(1)根据给出的数据即可计算出N的相对分子质量,结合氢原子的种类即可写出分子式
(2)根据要求即可写出结构简式,结合反应物即可写出方程式
一、单选题
1.由乙烯推测丙烯(CH2=CH—CH3)的结构或性质正确的是( )
A.不能使酸性高锰酸钾溶液褪色
B.不能在空气中燃烧
C.能使溴水褪色
D.与HCl在一定条件下能加成只得到一种产物
2.下列反应中,属于加成反应的是( )
A.CH3CH=CH2+Br2 CH3CHBrCH2Br
B.CH3CH2OH CH2=CH2↑+H2O
C.CH3COOH+CH3OH CH3COOCH3+H2O
D. +HNO3 -NO2+H2O
3.等物质的量的乙烯和甲烷,完全燃烧消耗氧气的物质的量的关系是( )
A.前者大 B.后者大 C.相等 D.不能确定
4.下列有关甲烷的叙述不正确的是( )
A.甲烷的二氯代物只有一种
B.甲烷性质稳定,通常情况下不与强酸、强碱、氧化剂反应
C.烷烃跟卤素单质在光照条件下能发生取代反应,烷烃燃烧时生成和
D.甲烷在光照条件下最多可以和发生取代反应
5.化学与生产、生活、社会密切相关。下列有关说法正确的是()
A.用浸泡过酸性高锰酸钾溶液的硅藻土吸收水果释放的乙烯,可达到水果保鲜的目的。
B.为了提高酒精的杀菌消毒效果,医院常用体积分数为100%的酒精。
C.氯仿是良好的溶剂,可广泛用于有机化工,对环境无影响。
D.石墨烯是一种从石墨材料中用“撕裂”方法“剥离”出的单层碳原子面材料,石墨烯和乙烯都属于烯烃。
6.下列关于实验室制取乙炔及其性质的说法正确的是
A.乙炔在空气中点燃,伴有明亮的火焰和浓黑烟
B.为了加快反应速率可用饱和食盐水代替水
C.实验室制取乙炔的反应为
D.用溴水除去乙炔中的杂质
7.肉桂酸甲酯(属于酯类,代号M)是常用于调制具有草莓、葡萄、樱桃、香子兰等香味的食用香精。测得其相对分子质量为162,分子中C、H、O原子个数比为5:5:1,且分子中只含有1个苯环,苯环上只有一个取代基。现测出M的核磁共振氢谱图有6个峰,其面积之比为1:2:2:1:1:3。下列说法错误的是( )
A.M的分子式为C10H10O2
B.1mol的M最多能与4molH2发生加成反应
C.肉桂酸能使溴水和酸性高锰酸钾溶液褪色
D.与M含有相同官能团,且苯环上氢的化学环境只有两种的同分异构体有3种
8.下列反应属于加成反应的是( )
A.CH4+Cl2 CH3Cl+HCl
B.CH3CH2OH+CuO CH3CHO+H2O+Cu
C.CH2=CH2+H2O CH3CH2OH
D.CH3CH2OH+CH3COOH CH3COOCH2CH3+H2O
9.下列现象中,不是因为发生化学反应而褪色的是( )
A.氯水久置变无色
B.乙烯使酸性高锰酸钾溶液褪色
C.乙烯使溴的四氯化碳溶液褪色
D.将苯滴入溴水中,振荡后水层接近无色
10.有机物a、b、c的结构如图。下列说法正确的是( )
A.a的一氯代物有3种 B.b是 的单体
C.c中碳原子的杂化方式均为 D.a、b、c互为同分异构体
11.欲观察环戊烯( )是否能使酸性KMnO4溶液褪色,先将环戊烯溶于适当的溶剂,再慢慢滴入0.005mol L﹣1KMnO4溶液并不断振荡.下列哪一种试剂最适合用来溶解环戊烯做此实验( )
A.四氯化碳 B.裂化汽油 C.甲苯 D.水
12.关于化合物2-苯基丙烯( ),下列说法错误的是( )
A.能使稀高锰酸钾溶液褪色 B.可以发生加成聚合反应
C.分子中所有原子共平面 D.易溶于甲苯等有机溶剂
13.下列关于烯烃的化学性质的叙述正确的是( )
A.烯烃能使溴的CCl4溶液褪色,是因为烯烃与溴发生了取代反应
B.烯烃不能使酸性KMnO4溶液褪色
C.在一定条件下,烯烃能与H2、H2O、HX(卤化氢)发生加成反应
D.可用酸性高锰酸钾溶液除去甲烷中少量的乙烯
14.X、Y两种有机物的分子式不同,但均含有C、H或C、H、O,将X、Y以任意比例混合,只要物质的量之和不变,完全燃烧时所消耗的氧气量和生成水的物质的量也分别不变。则下列有关判断正确的是( )
A.X、Y分子式中氢原子数一定要相同,碳原子数必定相同
B.若X为CH4,则相对分子质量最小的Y是甲醇
C.若X为CH4,则相对分子质量最小的Y是乙二醇
D.X、Y的化学式应含有相同的氢原子数,且相差n个碳原子,同时相差2n个氧原子(n为正整数)
15.下列实验中,对应的现象以及结论都正确的是( )
选项 实验 现象 结论
A 铝丝用砂纸打磨后,放在冷的浓硝酸中浸泡一段时间后,放入CuSO4溶液中 铝丝表面变红色 铝可从铜盐溶液中置换出铜
B 溶有SO2的BaCl2溶液中通入气体X 有白色沉淀生成 X一定是Cl2
C 将盐酸与石灰石反应产生的气体通入硅酸钠溶液 硅酸钠溶液变浑浊 证明非金属性:Cl>C>Si
D 将乙烯通入溴的四氯化碳溶液 四氯化碳溶液最终变为无色 产物为无色且溶于四氯化碳
A.A B.B C.C D.D
16.下列属于加成反应的是( )
A.CH2=CH2 + H2O CH3CH2OH
B.CH4 + Cl2CH3Cl + HCl
C.2CH3CH2OH + O2CH3COOH + H2O
D.2CH3CH2OH+2Na 2CH3CH2ONa + H2↑
二、综合题
17.氯气是黄绿色有强烈刺激性气味的剧毒气体,是重要的工业原料。回答下列问题
(1)将钠切去氧化层并用滤纸吸干煤油,在石棉网上微热至熔化后,立即用盛满氯气的集气瓶倒扣在其上方。现象是 ,该反应中反应物的能量 (填“高于”或“低于”)生成物的能量。
(2)向盛有KI溶液的试管中加入少许CCl4后滴加新制的氯水,振荡后静置,CCl4层变成紫红色,用离子方程式解释: .
(3)光照下Cl2可与CH4反应,写出生成一氯甲烷的化学方程式: 。实验室中用如图所示的装置进行甲烷与氯气在光照下反应的实验。
光照下反应一段时间后,下列装置示意图中能正确反映实验现象的是 (填标号)
A. B. C. D.
18.实验室制取乙炔的实验装置图(如图)中,
(1)A仪器的名称为 ;所盛的试剂为 .发生反应的化学方程式为: .
(2)将反应产生的乙炔通入酸性高锰酸钾溶液中,观察到的现象是: .将反应产生的乙炔通入溴的四氯化碳溶液中,反应的化学方程式为: .(产物为1,2﹣二溴乙烯)
(3)生成的乙炔中可能含有的杂质气体是 ,除去的方法是 .
19.结合图完成下列问题.
(1)“西气东输”中的“气”指天然气,其主要成分的结构式是 .一定量的该气体燃烧过程的能量变化如图1所示,从图中可以读出E1 E2(填“>”或“<”),该反应 (填“放出”或“吸收”)能量.
(2)CH4和Cl2发生的一系列反应都是 (填反应类型)反应,请写出CH4和Cl2反应生成一氯甲烷的化学方程式: .
(3)将封闭有甲烷和氯气的混合气体的装置放置在有光亮的地方,让混合气体缓慢地反应一段时间.经过几个小时的反应后,图2中U型管右端的玻璃管中水柱的变化是 (填“上升”或“下降”).
20.按要求填空:
(1)由乙烯制取聚乙烯的化学方程: .
(2)写出下列物质的结构简式;
①2,3﹣二甲基戊烷
②3﹣甲基﹣2﹣戊烯
③间二甲苯
(3)分子中含有5个碳原子的链状单炔烃的分子式 .
21.M是一种新型可生物降解的高分子材料,主要用于制造可降解纤维、塑料和医用材料,其水解最终产物为N。燃烧9.0 g的N只产生和,且质量分别为13.2g和5.4g,实验测得N在标准状况下的蒸气密度为;N分子中四种氢原子的个数比为1:1:1:3。
(1)写出N的分子式: 。
(2)写出N的结构简式: ,写出N在催化剂条件下发生缩聚反应合成M的化学方程式: 。
答案解析部分
1.【答案】C
【解析】【解答】根据丙烯的结构简式可知分子中含有碳碳双键,化学性质类似于乙烯,能使酸性高锰酸钾溶液褪色、能使溴水褪色、可以燃烧,与HCl在一定条件下能加成得到两种产物,即CH3CH2CH2Cl或CH3CHClCH3,
故答案为:C。
【分析】本题考查官能团(碳碳双键)的结构、特点。根据碳碳双键的特点进行分析解答即可。
2.【答案】A
【解析】【解答】A. 碳碳双键断裂,两个碳原子分别结合了1个溴原子,属于加成反应,A项符合题意;
B. CH3CH2OH CH2=CH2↑+H2O,属于消去反应,B项不符合题意;
C. CH3COOH+CH3OH CH3COOCH3+H2O,为酸与醇的酯化反应,属于取代反应,C项不符合题意;
D. +HNO3 -NO2+H2O,为苯的硝化反应,属于取代反应,D项不符合题意;
故答案为:A。
【分析】加成反应是有机物分子中的不饱和键断裂,断键原子与其他原子或原子团相结合,生成新的化合物的反应,据此判断。
3.【答案】A
【解析】【解答】乙烯分子式为C2H4,1mol乙烯完全燃烧消耗3mol氧气,甲烷分子式为CH4,1mol甲烷完全燃烧消耗2mol氧气,完全燃烧消耗氧气的物质的量的关系是前者大,
故答案为:A。
【分析】可根据甲烷和乙烯的燃烧方程式判断等物质的量的两种物质耗氧量的多少;也可根据等物质的量的甲烷和乙烯,乙烯比甲烷的碳原子的物质的量多来进行判断。
4.【答案】D
【解析】【解答】A、甲烷为正四面体结构,其二氯代物只有一种,A不符合题意。
B、甲烷的性质稳定,通常情况下不与强酸、强碱、氧化剂反应,B不符合题意。
C、烷烃在光照条件下能与卤素单质发生取代反应,完全燃烧时生成CO2和H2O,C不符合题意。
D、1molCH4能与4molCl2发生取代反应,D符合题意。
故答案为:D
【分析】A、甲烷的二氯代物只有一种。
B、甲烷性质稳定,不与强酸、强碱、氧化剂反应。
C、烷烃完全燃烧生成H2O和CO2。
D、1molCH4光照条件下可与4molCl2发生取代反应。
5.【答案】A
【解析】【解答】A.乙烯具有催熟作用,能被KMnO4溶液吸收,可用浸泡过酸性高锰酸钾溶液的硅藻土吸收水果释放的乙烯,起到水果保鲜的作用,A符合题意;
B.医用酒精的浓度为78%,用100%的酒精易造成酒精中毒,B不符合题意;
C.氯仿散发到空气中,易造成空气污染,C不符合题意;
D.石墨烯是碳的一种单质,不属于有机物,D不符合题意;
故答案为:A
【分析】A.乙烯能被KMnO4氧化;
B.医用酒精的浓度为78%;
C.氯仿会对环境造成污染;
D.石墨烯是碳的一种单质;
6.【答案】A
【解析】【解答】A.乙炔中含碳量高,则乙炔在空气中点燃,有明亮的火焰和浓黑烟,故A符合题意;
B.与水反应剧烈,选饱和食盐水代替水使反应平稳,故B不符合题意;
C.反应生成乙炔和氢氧化钙,则实验室制取乙炔的反应为:CaC2+2H2O→C2H2↑+Ca(OH)2,故C不符合题意;
D.乙炔含碳碳三键,与溴水发生加成反应,故D不符合题意;
故答案为:A。
【分析】 A.乙炔中含碳量较高;
B.用饱和食盐水代替水可减小反应速率;
C.实验室制取乙炔的反应为CaC2+2H2O→C2H2↑+Ca(OH)2;
D.乙炔会与溴水反应。
7.【答案】D
【解析】【解答】A.根据上述分析可知M的分子式为:C10H10O2,A不符合题意;
B.M的结构简式为:,碳碳双键和苯环可以和氢气发生加成反应,1mol的M最多能与4molH2发生加成反应,B不符合题意;
C.肉桂酸种含有碳碳双键,所以能使溴水和酸性高锰酸钾溶液褪色,C不符合题意;
D.与M含有相同官能团,则含有碳碳双键和酯基,且苯环上氢的化学环境只有两种,说明苯环有两个取代基,且位于对位,则对应的同分异构体有以下几种情况,①和、、-COOCH3,共3种,②和,共2种,③和-OOCH ,共2种,加一起一共7种,D符合题意;
故答案为:D。
【分析】M分子中C、H、O原子个数比为5:5:1,设分子式为(C5H5O)n,则81n=162,解得n=2,则M的分子式为C10H10O2,分子中只含有1个苯环,苯环上只有一个取代基。现测出M的核磁共振氢谱图有6个峰,其面积之比为1:2:2:1:1:3 ,则M的结构简式为。
8.【答案】C
【解析】【解答】A. CH4+Cl2 CH3Cl+HCl属于取代反应,故A不符合题意;
B. CH3CH2OH+CuO CH3CHO+H2O+Cu属于氧化反应,故B不符合题意;
C. CH2=CH2+H2O CH3CH2OH属于加成反应,故C符合题意;
D. CH3CH2OH+CH3COOH CH3COOCH2CH3+H2O属于酯化反应,故D不符合题意。
故答案为C。
【分析】加氢去氧是还原,加氧去氢是氧化,或则从化合价升降来分析反应。
9.【答案】D
【解析】【解答】A.氯水中存在可逆反应,次氯酸见光易分解生成HCl和氧气,次氯酸浓度减小,可逆反应平衡正向移动,氯气浓度减小,故久置变无色,故A不符合;
B.乙烯含有碳碳双键,能被酸性高锰酸钾溶液氧化从而使其褪色,故B不符合;
C.乙烯含有碳碳双键,能与溴的四氯化碳溶液发生加成反应从而使其褪色,故C不符合;
D. 溴单质易溶于苯中,将苯滴入溴水中振荡,苯将溴单质萃取,故水层接近无色,发生物理变化,故D符合;
故答案为:D。
【分析】A.氯气溶于水生成盐酸和次氯酸,次氯酸见光分解生成盐酸和氧气;
B.乙烯与酸性高锰酸钾发生氧化还原反应;
C.乙烯与溴的四氯化碳发生加成反应。
10.【答案】A
【解析】【解答】A.根据等效氢原理可知,a的一氯代物有3种如图所示: ,A符合题意;
B.b的加聚产物是: , 的单体是苯乙烯不是b,B不符合题意;
C.c中碳原子的杂化方式由6个 ,2个sp3,C不符合题意;
D.a、b、c的分子式分别为:C8H6,C8H6,C8H8,故c与a、b不互为同分异构体,D不符合题意;
故答案为:A。
【分析】
A.根据等效氢分析,含3种等效氢;
B.单体应是含碳碳双键;
C.杂化类型 、sp3两种;
D.分子式均不同,不属于同分异构。
11.【答案】A
【解析】【解答】A、四氯化碳不能够与高锰酸钾溶液反应,能够溶解该有机物,故A正确;
B、由于裂解汽油含有不饱和烃,能够使高锰酸钾溶液褪色,对实验带来干扰,故B错误;
C、由于甲苯能够使高锰酸钾溶液发生氧化反应,使高锰酸钾溶液褪色,对实验带来干扰,故C错误;
D、由于水不能够溶解该有机物,故D错误;
故选A.
【分析】A、四氯化碳是常用的有机溶剂,不能够与高锰酸钾溶液反应;
B、裂解汽油含有不饱和烃,能够使高锰酸钾溶液褪色;
C、甲苯能够使高锰酸钾溶液褪色;
D、水是无机溶剂,不能够溶剂该有机物.
12.【答案】C
【解析】【解答】A.该有机物中含有碳碳双键,可被酸性高锰酸钾氧化,故A不符合题意;
B.该有机物中含有碳碳双键,可发生加成聚合反应,故B不符合题意;
C.苯分子中所有原子共平面、乙烯分子中所有原子共平面,甲烷分子为正四面体结构,有3个原子共平面,该分子中甲基具有甲烷结构特点,所以该分子中所有原子不能共平面,故C符合题意;
D.该有机物中含有碳碳双键,没有亲水基团,故难溶于水,易溶于有机溶剂,故D不符合题意;
故答案为:C。
【分析】根据有机物结构式确定官能团,是双键,可发生加成反应和苯环上加成反应。结合碳原子的成键方式可判断原子是否共面
13.【答案】C
【解析】【解答】A.烯烃都含有碳碳双键,因此烯烃能使溴的CCl4溶液褪色,是因为烯烃与溴发生了加成反应,故A不符合题意;
B.烯烃都含有碳碳双键,能使酸性KMnO4溶液褪色,故B不符合题意;
C.在催化剂作用下,烯烃能与H2、H2O、HX(卤化氢)发生加成反应,故C符合题意;
D.不能用酸性高锰酸钾溶液除去甲烷中少量的乙烯,乙烯和酸性高锰酸钾反应生成二氧化碳,引入新的杂质,故D不符合题意。
故答案为:C。
【分析】A.烯烃中含有碳碳双键,能与溴发生了加成反应而使溴的CCl4溶液褪色;
B.烯烃中含有碳碳双键,能被KMnO4氧化而使酸性KMnO4溶液褪色;
C.烯烃中含有碳碳双键,能与H2、H2O、HX(卤化氢)发生加成反应;
D.乙烯和酸性高锰酸钾反应生成二氧化碳。
14.【答案】D
【解析】【解答】总物质的量一定时有机物完全燃烧时,生成水的质量和消耗O2的质量不变,则化学式中的氢原子个数相同,且在CxHyOz中(x+ )相同,如果X、Y的化学式应含有相同的氢原子数,且相差n个碳原子,同时相差2n个氧原子(n为正整数)。
A.X、Y分子式中氢原子数一定相同,碳原子数可能相同,A不符合题意;
B.若X为甲烷,另一种有机物分子中一定含有4个H,且耗氧量与甲烷相同,相对分子质量最小的Y为:C2H4O2,可能为甲酸甲酯,也可能是乙酸;甲醇和甲烷的耗氧量不同,故不可能为甲醇,B不符合题意;
C.乙二醇分子中含有6个H原子,与甲烷含有氢原子数不相同,不可能为乙二醇,C不符合题意;
D.X、Y的化学式应含有相同的氢原子数,则物质的量一定时生成水的量相同;若相差n个碳原子,同时相差2n个氧原子(n为正整数),则消耗氧气的量相同,D符合题意;
故合理选项是D。
【分析】根据总物质的量一定时有机物完全燃烧时,生成水的质量和消耗O2的质量不变,则化学式中的氢原子个数相同,且在CxHyOz中(x+ )相同,若X、Y的化学式应含有相同的氢原子数,且相差n个碳原子,同时相差2n个氧原子(n为正整数),据此对各选项进行判断。
15.【答案】D
【解析】【解答】A.铝丝用砂纸打磨后,放在冷的浓硝酸中浸泡一段时间后,发生钝化形成致密氧化膜,因为Al2O3与CuSO4不反应,所以放入CuSO4溶液中,铝丝表面不会生成铜,A不符合题意;
B.向溶有SO2的BaCl2溶液中通入气体X,产生的白色沉淀可能为亚硫酸钡或硫酸钡,则X可能为氨气或者氧化性气体(如氯气、臭氧等),B不符合题意;
C.比较元素的非金属性强弱,要看元素的最高价氧化物对应水化物的酸性强弱,所以不应该使用盐酸与石灰石反应,应该用高氯酸与石灰石反应,C不符合题意;
D.乙烯与溴单质发生加成反应生成无色1,2-二溴乙烷且溶于四氯化碳,所以将乙烯通入溴的四氯化碳溶液中,溶液最终变为无色,D符合题意;
故答案为:D
【分析】A.常温下,浓硝酸能使铝钝化;
B.产生的白色沉淀为BaSO4,则通入的气体具有氧化性,能将SO2氧化成SO42-;
C.证明非金属性的强弱,应用其最高价含氧酸的酸性强弱比较得出;
D.乙烯能与Br2发生加成反应,有机液体一般可互溶;
16.【答案】A
【解析】【解答】加成反应的特点是碳碳双键断开,断键位置各自加上1个原子或1个基团;
A、该反应为乙烯的加成反应,A正确;
B、该反应为甲烷的取代反应,B错误;
C、该反应为乙醇的催化氧化反应,C错误;
D、该反应为乙醇的取代反应,D错误;
故答案为:A
【分析】加成反应的特点是碳碳双键断开,断键位置各自加上1个原子或1个基团;取代反应的特点是两个分子发生反应,彼此交换原子或基团。
17.【答案】(1)剧烈燃烧,产生白烟;高于
(2)Cl2+2I-=I2+2Cl-
(3)Cl2+CH4 CH3Cl+HCl;D
【解析】【解答】(1)金属钠在氯气中剧烈燃烧,产生白烟;该反应过程中放出大量热,因此反应物的能量高于生成物的能量;
(2)CCl4层变成紫红色,说明有碘单质生成,该反应的化学方程式为:Cl2+2I-=I2+2Cl-;
(3)光照条件下, CH4与Cl2发生取代反应生成CH3Cl和HCl,该反应的化学方程式为: Cl2+CH4 CH3Cl+HCl;
CH4与Cl2的取代反应为多步同时进行的反应,生成物中CH3Cl为气体,CH2Cl2、CHCl3、CCl4都为有机液体,不溶于水,同时反应生成的HCl能溶于水;故反应后试管内有部分水进入,同时试管内液体出现分层、试管内有部分气体剩余,D符合题意;
【分析】(1)根据钠在氯气中燃烧的现象分析;
(2)CCl4层变成紫红色,说明有碘单质生成,结合氯气的氧化性强于碘单质的氧化性,书写反应的离子方程式;
(3)光照条件下, CH4与Cl2发生取代反应生成CH3Cl和HCl,据此写出反应的化学方程式;
CH4与Cl2的取代反应为多步同时进行的反应,根据生成物的性质分析;
18.【答案】(1)分液漏斗;饱和食盐水;CaC2+2H2O→Ca(OH)2+CH≡CH↑
(2)酸性高锰酸钾溶液紫色褪去;
(3)硫化氢、磷化氢(H2S、PH3);将混合气体通过CuSO4溶液洗气
【解析】【解答】解:(1)A仪器的名称为,碳化钙与水反应生成乙炔,反应非常剧烈,为了减慢反应的速率,通常用饱和食盐水与碳化钙反应,发生的反应方程式为:CaC2+2H2O→Ca(OH)2+CH≡CH↑,故答案为:分液漏斗;饱和食盐水; CaC2+2H2O→Ca(OH)2+CH≡CH↑;(2)乙炔中含有碳碳三键,具有还原性,能被酸性的高锰酸钾氧化而使高锰酸钾褪色,乙炔为不饱和烃与溴能1:1加成生成1,2﹣二溴乙烯,化学方程式为: ,故答案为:酸性高锰酸钾溶液紫色褪去; ;(3)电石主要成分是CaC2 ,还有杂质CaS Ca3P2等,这些杂质CaS、Ca3P2也能和水反应,生成H2S,PH3等杂质,H2S,PH3都与硫酸铜溶液发生反应而除去,故可以用硫酸铜溶液除去杂质;
故答案为:硫化氢、磷化氢(H2S、PH3);将混合气体通过CuSO4溶液洗气.
【分析】(1)熟悉常见仪器的名称,碳化钙与水反应生成乙炔;(2)依据乙炔中含有碳碳三键,能发生与溴发生加成反应,具有还原性,能使高锰酸钾褪色解答;(3)电石主要成分是CaC2,还有杂质CaS Ca3P2等,这些杂质CaS Ca3P2也能和水反应,生成H2S,PH3等杂质,可以用硫酸铜溶液除去.
19.【答案】(1);>;放出
(2)取代;CH4+Cl2 CH3Cl+HCl
(3)下降
【解析】【解答】解:(1)天然气主要成分为甲烷,是一个碳原子和四个氢原子形成的正四面体结构,故结构式为 ;从图像可知,E1>E2,而当反应物能量高于生成物能量时,反应放热,故答案为: ;>;放出;(2)甲烷和氯气在光照条件下发生取代反应,反应的化学方程式:CH4+Cl2 CH3Cl+HCl,故答案为:取代;CH4+Cl2 CH3Cl+HCl;(3)经过几个小时的反应后,消耗氯气,反应中气体的物质的量减少,所以压强减小,且生成的HCl能够溶解于水,U型管右端的玻璃管中水柱降低,故答案为:下降.
【分析】(1)天然气主要成分为甲烷,是一个碳原子和四个氢原子形成的正四面体结构,图像中反应物能量高于生成物为放热反应;(2)甲烷和氯气在光照条件下发生取代反应;(3)根据大气压强原理来判断U型管右端的玻璃管中水柱变化.
20.【答案】(1)
(2)(CH3)2CHCH(CH3)CH2CH3;CH3CH=C(CH3)CH2CH3;
(3)C5H8
【解析】【解答】解:(1)乙烯中含有碳碳双键,在适当的温度、压强、催化剂条件下,乙烯能发生加聚反应生成聚乙烯,反应方程式为: ,故答案为: ;(2)①2,3﹣二甲基戊烷,最长碳链为5,在2、3号碳上分别含有1个甲基,故结构简式为:(CH3)2CHCH(CH3)CH2CH3;故答案为:(CH3)2CHCH(CH3)CH2CH3;②依据系统命名方法,结合名称写出结构简式,3﹣甲基﹣2﹣戊烯的结构简式是:CH3CH=C(CH3)CH2CH3,故答案为:CH3CH=C(CH3)CH2CH3;③间二甲苯中苯环连接2个甲基且处于间位位置,起结构简式为: ,
故答案为: ;(3)链状单炔烃的通式CnH2n﹣2,5个碳原子的链状单炔烃的分子式为C5H8,故答案为:C5H8.
【分析】(1)乙烯含有碳碳双键,可发生加聚反应生成聚乙烯;(2)根据有机物的命名原则写出各有机物的结构简式:①遵循碳链最长,支链最多,该烷烃最长碳链为5,在2、3号碳上分别含有1个甲基,补齐氢原子;②给主链编号时从距离碳碳双键最近的一端开始,侧链视为取代基;③苯环连接2个甲基且处于间位位置;(3)可依据链状单炔烃的通式CnH2n﹣2书写.
21.【答案】(1)
(2);+(n-1)H2O
【解析】【解答】(1)N的摩尔质量,,N中:,,,则N的分子式为;
(2)N在催化剂的作用下发生缩聚反应生成M,由N的分子中四种氢原子的个数比为1∶1∶1∶3,可知N的结构简式为,缩聚反应的化学方程式为+(n-1)H2O。
【分析】(1)根据给出的数据即可计算出N的相对分子质量,结合氢原子的种类即可写出分子式
(2)根据要求即可写出结构简式,结合反应物即可写出方程式
