第3章 第1节 第2课时 水溶液的酸碱性与ph 课件(共32张PPT)2023-2024学年高二化学鲁科版(2019)选择性必修第一册
文档属性
| 名称 | 第3章 第1节 第2课时 水溶液的酸碱性与ph 课件(共32张PPT)2023-2024学年高二化学鲁科版(2019)选择性必修第一册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 4.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-12-05 00:00:00 | ||
图片预览








文档简介
(共32张PPT)
第3章 第1节
第2课时 水溶液的酸碱性与pH
学习目标
1.掌握溶液的酸碱性与pH的关系,掌握检测溶液pH的方法(重点)。
2.了解溶液pH调控的意义。
3.能正确计算酸碱溶液的pH(难点)。
(已整理)李丽娟
由于水的电离,在水溶液中始终存在着H+和OH-,而且稀水溶液中Kw=c平(H+)·c平(OH-)。那么,水溶液中H+、OH-的浓度与溶液的酸碱性有什么关系呢 水溶液的酸碱度又如何量度呢
酸性 ? 碱性
联想质疑
溶液的酸碱性与pH
一
室温下,某酸溶液中的 c平(H+) 为 1.0×10-5 mol·L-1 ,该溶液中c平(OH-) 是多少?
根据Kw=c平(H+)·c平(OH-) = 1.0× 10-14 mol2·L-2
得c平(OH-)= =
Kw
c平(H+)
1.0×10-14 mol2·L-2
1.0×10-5 mol·L-1
=1.0×10-9 mol·L-1
交流研讨
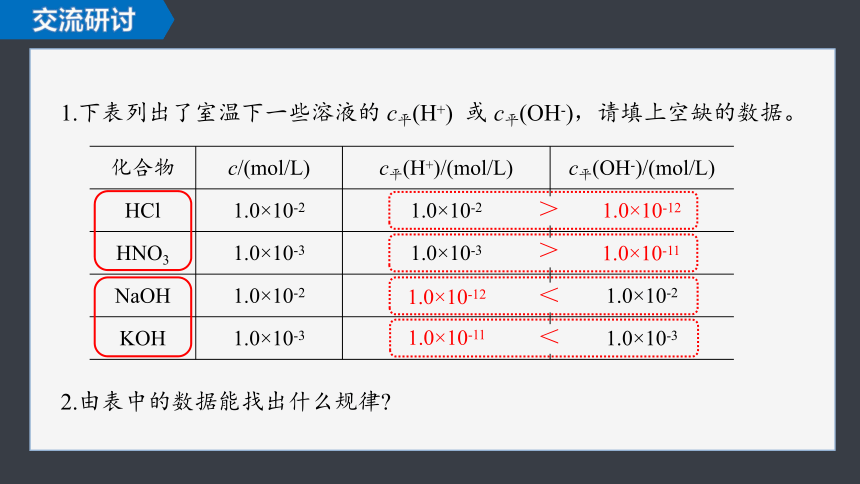
1.下表列出了室温下一些溶液的 c平(H+) 或 c平(OH-),请填上空缺的数据。
化合物 c/(mol/L) c平(H+)/(mol/L) c平(OH-)/(mol/L)
HCl 1.0×10-2 1.0×10-2
HNO3 1.0×10-3 1.0×10-3
NaOH 1.0×10-2 1.0×10-2
KOH 1.0×10-3 1.0×10-3
1.0×10-12
1.0×10-11
1.0×10-12
1.0×10-11
2.由表中的数据能找出什么规律
>
>
<
<
交流研讨
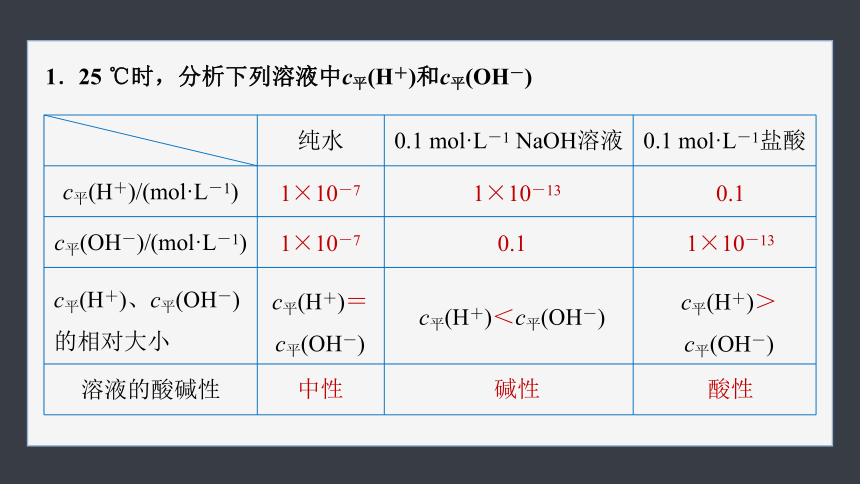
1.25 ℃时,分析下列溶液中c平(H+)和c平(OH-)
纯水 0.1 mol·L-1 NaOH溶液 0.1 mol·L-1盐酸
c平(H+)/(mol·L-1)
c平(OH-)/(mol·L-1)
c平(H+)、c平(OH-)的相对大小
溶液的酸碱性
1×10-7
1×10-13
0.1
1×10-7
0.1
1×10-13
c平(H+)=
c平(OH-)
c平(H+)<c平(OH-)
c平(H+)>
c平(OH-)
中性
碱性
酸性
2.溶液的酸碱性与c平(H+)、c平(OH-)的关系
(1)任何水溶液中都有H+和OH-。
(2)溶液的酸碱性取决于溶液中c平(H+)、c平(OH-)的相对大小。
酸性溶液:c平(H+)>c平(OH-)
中性溶液:c平(H+)=平(OH-)
碱性溶液:c平(H+)常温
c平(H+)>1×10-7 mol·L-1
=1×10-7 mol·L-1
c平(H+)<1×10-7 mol·L-1
c平(H+)越大,酸性越强
c平(OH-)越大,碱性越强
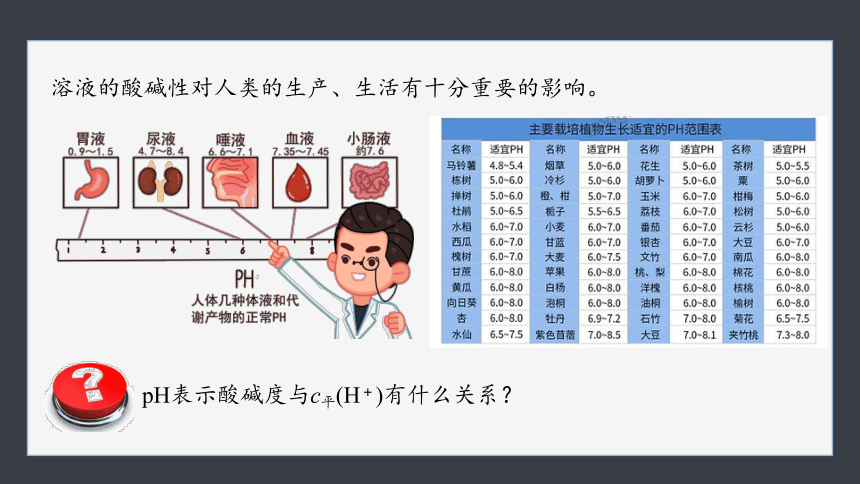
pH表示酸碱度与c平(H+)有什么关系?
溶液的酸碱性对人类的生产、生活有十分重要的影响。
3.溶液的pH
概念:c平(H+)的负对数,pH=-lg c平(H+)
适用范围: c平(H+)、 c平(OH-)小于1 mol·L-1的稀溶液,
pH范围在“0~14”
(1) pH
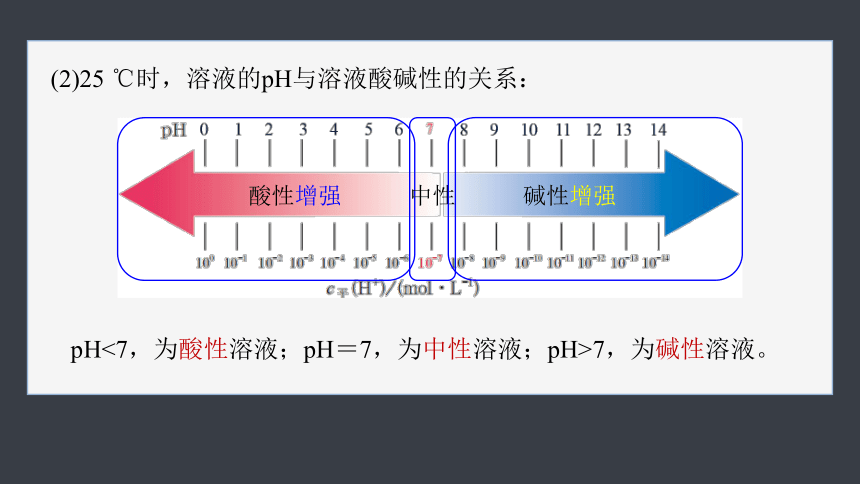
(2)25 ℃时,溶液的pH与溶液酸碱性的关系:
pH<7,为酸性溶液;pH=7,为中性溶液;pH>7,为碱性溶液。
中性
碱性增强
酸性增强
思考交流
1.根据公式计算下列溶液的pH(常温),并比较其酸碱性的强弱。
(1)①c平(H+)=1×10-5 mol·L-1的溶液pH=____;
②0.001 mol·L-1的稀盐酸pH=____;
③0.005 mol·L-1的稀硫酸pH=____;
上述三种溶液酸性由强到弱的顺序:_________(填序号)。
5
3
2
③>②>①
思考交流
(2)①c平(H+)=1×10-9 mol·L-1的溶液pH=____;
②c平(OH-)=1×10-4的溶液pH=____;
③0.001 mol·L-1的稀NaOH溶液pH=____;
上述三种溶液碱性由强到弱的顺序为__________(填序号)。
9
10
11
③>②>①
思考交流
2.pH=7的溶液一定呈中性吗?用pH判断溶液酸碱性时,要注意什么?
答案 pH=7的溶液不一定呈中性。如100 ℃时,pH=6为中性。只有在室温下才能用pH与7的相对大小来判断溶液的酸碱性。
3.常温下pH=1的盐酸和pH=11的NaOH溶液由水电离出的c(H+)分别是多少?
答案 1×10-13 mol·L-1、1×10-11 mol·L-1
思考交流
4.25 ℃时,某溶液中由水电离出的c(H+)=1×10-12 mol·L-1,请探究该溶液的pH可能为多少?
答案 2或12
归纳总结
返回
计算酸碱溶液的pH
酸性:先求c平(H+)—→pH(注意元数)
碱性:先求c平(OH-) c平(H+)—→pH
pH的测定和调控的意义
二
如何测定溶液的酸碱度?
酸碱指示剂,可检验溶液的酸碱性
在生活、生产和科学研究中,需要更精确的表示溶液的酸碱性的强弱程度,
酸碱指示剂就不能胜任了,那我们应如何测定溶液的酸碱度呢?
交流·研讨
1.pH的测定
(1) pH试纸
①广泛pH试纸:范围1~ 14,可识别的pH差约为1
②精密pH试纸:范围较窄,可识别的pH差约为0.2或0.3
(2)酸度计
可精密测量pH,测得的pH可以是整数或小数,
量程为0~14
思考交流
(1)某盐酸由于长期放置,标签脱落,为确定其pH,用pH试纸测量的具体操作为__________________________________________________
_______________________________________________________________________________________________。若使用时将试纸湿润,则测定结果如何变化?_____。用湿润的pH试纸测量任何溶液一定有误差吗?_________________________________。
用镊子取一小片pH试纸放在干燥、洁净的玻璃片(或表面
皿)上,用干净的玻璃棒蘸取待测液滴在试纸的中部,试纸变色后,与标准比色卡对照比色,确定溶液的pH
偏高
不一定,溶液为中性时测定结果不变
思考交流
(2)用广泛pH试纸测量溶液的pH时,记录的数据有何特点?
答案 读出的pH只能是1~14的整数。
(3)是否可用pH试纸测定氯水的pH?简述理由。
答案 不能,因为氯水具有漂白性。
2.测定和调控溶液pH的应用
人体健康
人体各种体液都有一定的pH。可以利用检测血液的pH来诊断疾病
生活应用
护发素保护头发,就是调节头发pH使之达到适宜的酸碱度
环保领域
酸性或碱性废水的处理,可利用中和反应调节pH
农业生产
土壤pH影响植物对养分的吸收,不同作物生长对土壤pH范围有不同要求
科学实验
工业生产
溶液的pH控制是影响实验结果或产品质量、产量的一个重要因素
返回
酸碱溶液稀释或混合时pH计算
三
1.下列溶液被稀释后,计算所得溶液的pH(常温)
溶液稀释 pH
pH=3的稀盐酸加水稀释100倍
pH=2的稀硫酸加水稀释100倍
pH=11的NaOH溶液加水稀释10倍
pH=12的Ba(OH)2溶液加水稀释10倍
pH=5的稀盐酸加水稀释1 000倍
pH=9的NaOH溶液加水稀释1 000倍
5
4
10
11
约为7,略小于7
约为7,略大于7
2.(1)pH=3的醋酸加水稀释到原来的10倍,溶液的pH范围:
___________。
(2)pH=12的氨水加水稀释到原来的10倍,溶液的pH范围:
___________。
311酸碱溶液稀释时pH变化规律(常温)
(1)强酸(或强碱)每稀释10倍,pH向7靠拢1个单位。
(2)弱酸(或弱碱)每稀释10倍,pH向7靠拢不到1个单位。
(3)酸碱溶液无限稀释,pH只能接近7。
归纳总结
3.常温下,计算下列溶液混合后的pH。
(1)pH=3的盐酸与pH=5的硫酸溶液等体积混合后溶液的pH为_____。
3.3
(2)pH=2的盐酸与pH=4的硫酸,若按1∶10的体积比混合(溶液体积变化忽略不计)。混合后溶液的pH为________。
3
(3)pH=10和pH=12的两种NaOH溶液等体积混合后溶液的pH为_____。
11.7
pH=-lg(2×10-12)=12-lg 2≈11.7
4.0.015 mol·L-1的硫酸与0.01 mol·L-1的NaOH溶液等体积混合后溶液的pH是____。
2
酸过量,设混合前两溶液的体积均为V L
5.常温下,pH=12的NaOH溶液和pH=4的盐酸等体积混合后溶液的pH为________。
11.7
pH=-lg (2×10-12)=12-lg 2≈11.7
c(OH-)=10-2 mol·L-1
c(H+)=10-4 mol·L-1
碱过量
酸碱中和反应后pH计算的一般思路(常温)
归纳总结
恰好完全反应呈中性 pH=7
酸过量
碱过量
第3章 第1节
第2课时 水溶液的酸碱性与pH
学习目标
1.掌握溶液的酸碱性与pH的关系,掌握检测溶液pH的方法(重点)。
2.了解溶液pH调控的意义。
3.能正确计算酸碱溶液的pH(难点)。
(已整理)李丽娟
由于水的电离,在水溶液中始终存在着H+和OH-,而且稀水溶液中Kw=c平(H+)·c平(OH-)。那么,水溶液中H+、OH-的浓度与溶液的酸碱性有什么关系呢 水溶液的酸碱度又如何量度呢
酸性 ? 碱性
联想质疑
溶液的酸碱性与pH
一
室温下,某酸溶液中的 c平(H+) 为 1.0×10-5 mol·L-1 ,该溶液中c平(OH-) 是多少?
根据Kw=c平(H+)·c平(OH-) = 1.0× 10-14 mol2·L-2
得c平(OH-)= =
Kw
c平(H+)
1.0×10-14 mol2·L-2
1.0×10-5 mol·L-1
=1.0×10-9 mol·L-1
交流研讨
1.下表列出了室温下一些溶液的 c平(H+) 或 c平(OH-),请填上空缺的数据。
化合物 c/(mol/L) c平(H+)/(mol/L) c平(OH-)/(mol/L)
HCl 1.0×10-2 1.0×10-2
HNO3 1.0×10-3 1.0×10-3
NaOH 1.0×10-2 1.0×10-2
KOH 1.0×10-3 1.0×10-3
1.0×10-12
1.0×10-11
1.0×10-12
1.0×10-11
2.由表中的数据能找出什么规律
>
>
<
<
交流研讨
1.25 ℃时,分析下列溶液中c平(H+)和c平(OH-)
纯水 0.1 mol·L-1 NaOH溶液 0.1 mol·L-1盐酸
c平(H+)/(mol·L-1)
c平(OH-)/(mol·L-1)
c平(H+)、c平(OH-)的相对大小
溶液的酸碱性
1×10-7
1×10-13
0.1
1×10-7
0.1
1×10-13
c平(H+)=
c平(OH-)
c平(H+)<c平(OH-)
c平(H+)>
c平(OH-)
中性
碱性
酸性
2.溶液的酸碱性与c平(H+)、c平(OH-)的关系
(1)任何水溶液中都有H+和OH-。
(2)溶液的酸碱性取决于溶液中c平(H+)、c平(OH-)的相对大小。
酸性溶液:c平(H+)>c平(OH-)
中性溶液:c平(H+)=平(OH-)
碱性溶液:c平(H+)
c平(H+)>1×10-7 mol·L-1
=1×10-7 mol·L-1
c平(H+)<1×10-7 mol·L-1
c平(H+)越大,酸性越强
c平(OH-)越大,碱性越强
pH表示酸碱度与c平(H+)有什么关系?
溶液的酸碱性对人类的生产、生活有十分重要的影响。
3.溶液的pH
概念:c平(H+)的负对数,pH=-lg c平(H+)
适用范围: c平(H+)、 c平(OH-)小于1 mol·L-1的稀溶液,
pH范围在“0~14”
(1) pH
(2)25 ℃时,溶液的pH与溶液酸碱性的关系:
pH<7,为酸性溶液;pH=7,为中性溶液;pH>7,为碱性溶液。
中性
碱性增强
酸性增强
思考交流
1.根据公式计算下列溶液的pH(常温),并比较其酸碱性的强弱。
(1)①c平(H+)=1×10-5 mol·L-1的溶液pH=____;
②0.001 mol·L-1的稀盐酸pH=____;
③0.005 mol·L-1的稀硫酸pH=____;
上述三种溶液酸性由强到弱的顺序:_________(填序号)。
5
3
2
③>②>①
思考交流
(2)①c平(H+)=1×10-9 mol·L-1的溶液pH=____;
②c平(OH-)=1×10-4的溶液pH=____;
③0.001 mol·L-1的稀NaOH溶液pH=____;
上述三种溶液碱性由强到弱的顺序为__________(填序号)。
9
10
11
③>②>①
思考交流
2.pH=7的溶液一定呈中性吗?用pH判断溶液酸碱性时,要注意什么?
答案 pH=7的溶液不一定呈中性。如100 ℃时,pH=6为中性。只有在室温下才能用pH与7的相对大小来判断溶液的酸碱性。
3.常温下pH=1的盐酸和pH=11的NaOH溶液由水电离出的c(H+)分别是多少?
答案 1×10-13 mol·L-1、1×10-11 mol·L-1
思考交流
4.25 ℃时,某溶液中由水电离出的c(H+)=1×10-12 mol·L-1,请探究该溶液的pH可能为多少?
答案 2或12
归纳总结
返回
计算酸碱溶液的pH
酸性:先求c平(H+)—→pH(注意元数)
碱性:先求c平(OH-) c平(H+)—→pH
pH的测定和调控的意义
二
如何测定溶液的酸碱度?
酸碱指示剂,可检验溶液的酸碱性
在生活、生产和科学研究中,需要更精确的表示溶液的酸碱性的强弱程度,
酸碱指示剂就不能胜任了,那我们应如何测定溶液的酸碱度呢?
交流·研讨
1.pH的测定
(1) pH试纸
①广泛pH试纸:范围1~ 14,可识别的pH差约为1
②精密pH试纸:范围较窄,可识别的pH差约为0.2或0.3
(2)酸度计
可精密测量pH,测得的pH可以是整数或小数,
量程为0~14
思考交流
(1)某盐酸由于长期放置,标签脱落,为确定其pH,用pH试纸测量的具体操作为__________________________________________________
_______________________________________________________________________________________________。若使用时将试纸湿润,则测定结果如何变化?_____。用湿润的pH试纸测量任何溶液一定有误差吗?_________________________________。
用镊子取一小片pH试纸放在干燥、洁净的玻璃片(或表面
皿)上,用干净的玻璃棒蘸取待测液滴在试纸的中部,试纸变色后,与标准比色卡对照比色,确定溶液的pH
偏高
不一定,溶液为中性时测定结果不变
思考交流
(2)用广泛pH试纸测量溶液的pH时,记录的数据有何特点?
答案 读出的pH只能是1~14的整数。
(3)是否可用pH试纸测定氯水的pH?简述理由。
答案 不能,因为氯水具有漂白性。
2.测定和调控溶液pH的应用
人体健康
人体各种体液都有一定的pH。可以利用检测血液的pH来诊断疾病
生活应用
护发素保护头发,就是调节头发pH使之达到适宜的酸碱度
环保领域
酸性或碱性废水的处理,可利用中和反应调节pH
农业生产
土壤pH影响植物对养分的吸收,不同作物生长对土壤pH范围有不同要求
科学实验
工业生产
溶液的pH控制是影响实验结果或产品质量、产量的一个重要因素
返回
酸碱溶液稀释或混合时pH计算
三
1.下列溶液被稀释后,计算所得溶液的pH(常温)
溶液稀释 pH
pH=3的稀盐酸加水稀释100倍
pH=2的稀硫酸加水稀释100倍
pH=11的NaOH溶液加水稀释10倍
pH=12的Ba(OH)2溶液加水稀释10倍
pH=5的稀盐酸加水稀释1 000倍
pH=9的NaOH溶液加水稀释1 000倍
5
4
10
11
约为7,略小于7
约为7,略大于7
2.(1)pH=3的醋酸加水稀释到原来的10倍,溶液的pH范围:
___________。
(2)pH=12的氨水加水稀释到原来的10倍,溶液的pH范围:
___________。
3
(1)强酸(或强碱)每稀释10倍,pH向7靠拢1个单位。
(2)弱酸(或弱碱)每稀释10倍,pH向7靠拢不到1个单位。
(3)酸碱溶液无限稀释,pH只能接近7。
归纳总结
3.常温下,计算下列溶液混合后的pH。
(1)pH=3的盐酸与pH=5的硫酸溶液等体积混合后溶液的pH为_____。
3.3
(2)pH=2的盐酸与pH=4的硫酸,若按1∶10的体积比混合(溶液体积变化忽略不计)。混合后溶液的pH为________。
3
(3)pH=10和pH=12的两种NaOH溶液等体积混合后溶液的pH为_____。
11.7
pH=-lg(2×10-12)=12-lg 2≈11.7
4.0.015 mol·L-1的硫酸与0.01 mol·L-1的NaOH溶液等体积混合后溶液的pH是____。
2
酸过量,设混合前两溶液的体积均为V L
5.常温下,pH=12的NaOH溶液和pH=4的盐酸等体积混合后溶液的pH为________。
11.7
pH=-lg (2×10-12)=12-lg 2≈11.7
c(OH-)=10-2 mol·L-1
c(H+)=10-4 mol·L-1
碱过量
酸碱中和反应后pH计算的一般思路(常温)
归纳总结
恰好完全反应呈中性 pH=7
酸过量
碱过量
同课章节目录
- 第1章 化学反应与能量转化
- 第1节 化学反应的热效应
- 第2节 化学能转化为电能——电池
- 第3节 电能转化为化学能——电解
- 第4节 金属的腐蚀与防护
- 微项目 设计载人航天器用化学电池与氧气再生方案——化学反应中能量及物质的转化利用
- 第2章 化学反应的方向、 限度与速率
- 第1节 化学反应的方向
- 第2节 化学反应的限度
- 第3节 化学反应的速率
- 第4节 化学反应条件的优化——工业合成氨
- 微项目 探讨如何利用工业废气中的二氧化碳合成甲醇——化学反应选择与反应条件优化
- 第3章 物质在水溶液中的行为
- 第1节 水与水溶液
- 第2节 弱电解质的电离 盐类的水解
- 第3节 沉淀溶解平衡
- 第4节 离子反应
- 微项目 揭秘索尔维制碱法和侯氏制碱法——化学平衡思想的创造性应用
