【人教版】初中化学九下11.1 生活中常见的盐 同步测试题 (含答案)
文档属性
| 名称 | 【人教版】初中化学九下11.1 生活中常见的盐 同步测试题 (含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 395.9KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-12-06 00:00:00 | ||
图片预览



文档简介
中小学教育资源及组卷应用平台
课题一 生活中常见的盐 同步测试题
一、单选题(共10题;共20分)
1.“84消毒液”是宾馆、医院、学校等一些公共场所常备的消毒剂,适用于环境和物体表面消毒,其有效成分主要是次氯酸钠(化学式为NaClO)。次氯酸钠属于( )
A. 酸 B. 碱 C. 盐 D. 氧化物
2.在发酵面团中加入含下列某种物质的溶液揉和,既能除去面团中的酸,又能使蒸出的馒头疏松多孔。这种物质是( )
A. Na2CO3 B. Ca(OH)2 C. CaO D. NaCl
3.泉州是海上丝绸之路的起点,古代的染坊常用某种“碱剂”来精炼丝绸,其主要成分是一种盐,水溶液呈碱性,它能使促进蚕丝表面的丝胶蛋白质水解而除去,从而使丝绸颜色洁白、质感柔软、色泽光亮,这种“碱剂”可能是( )
A. 食盐 B. 烧碱 C. 草木灰 D. 熟石灰
4.四瓶失去标签的溶液分别为:①NaOH、②CuSO4、③MgCl2、④Na2SO4 , 不用其它任何试剂而要将它们一一鉴别出来的正确顺序是( )
A. ③①②④ B. ②③④① C. ②①③④ D. ①③②④
5.某一无色溶液具有下列性质:①使无色酚酞试液变红;②与CuSO4溶液反应可产生蓝色沉淀;③与纯碱溶液反应产生白色沉淀。此溶液是( )
A. 氢氧化钠溶液 B. 澄清石灰水 C. 氯化钙溶液 D. 盐酸
6.氨碱法生产纯碱的主要反应原理如下: ;2NaHCO3 Na2CO3+CO2↑+H2O,下列有关“侯氏制碱法”的叙述中,错误的是( )
A. 加热时的稳定性:碳酸钠 碳酸氢钠
B. 用食盐制纯碱还需要要含碳、氧元素的物质
C. 配制饱和食盐水时,可通过搅拌来提高食盐的溶解度
D. 向饱和食盐中先通入氨气的作用是使溶液呈碱性,促进二氧化碳的吸收
7.贝壳的主要成分是碳酸钙,小强设计了如图的实验进行探究,以下关于此实验现象的描述中,错误的是( )
A. 有气泡产生 B. 表面皿内壁有浑浊出现
C. 贝壳逐渐溶解 D. 烧杯中溶液的质量不变
8.某中学化学兴趣小组四名学生,对某厂排放的污水进行检测,先取废液观察,呈无色、均一、透明状,然后用pH试纸测得污水的pH=1.下表为四名学生对该厂废水成分初步检测的分析结果,可能正确的是()
A. NaOH、KNO3、CuSO4、NaCl B. KNO3、NaCl、Na2SO4、HCl
C. HCl、Na2CO3、Na2SO4 D. HCl、H2SO4、KNO3、BaCl2
9.为除去粗盐中的泥沙、Ca2+、Mg2+、SO42-等杂质,可将粗盐溶于水,再进行下列五步操作:①过滤②加过量的氢氧化钠溶液③加适量盐酸④加过量的碳酸钠溶液⑤加过量的氯化钡溶液。正确的操作顺序是()
A. ④⑤②①③ B. ②④⑤①③
C. ②⑤④①③ D. ⑤②④③①
10.甲、乙、丙、丁是初中化学常见的物质,它们的转化关系如图所示(反应条件已省略)。下列说法正确的是( )
A. 若丁是水,则该反应一定属于中和反应
B. 若丙为沉淀,则甲、乙中一定有一种物质是盐
C. 若甲、丁均为单质,则该反应一定属于置换反应
D. 若乙是一种碱、丁是一种盐,则该反应一定属于复分解反应
二、综合题(共7题;共31分)
11.有下列几种物质,请选择合适的标号(a~f)填空(不得重复)
a.稀盐酸 b.稀硫酸 c.熟石灰
d.硫酸铜 e.食盐 f.生石灰
(1)少量存于胃液中帮助消化的是________
(2)常用降低土壤酸性的是________
(3)常用于食品干燥剂的是________
(4)用来清除铁锈的物质________
(5)医学上用于配制生理盐水的是 ________
(6)农业上用于配制波尔多液的是 ________
12.晓红同学为同学们表演了一组化学魔术,在三支盛有液体的玻璃杯中,分 别倒入用酒瓶装的一种液体,同学们看到下列奇特现象:A 杯中变成了“红葡萄酒”(变为红色);B 杯变成了“汽水”(产生大量的气泡);C 杯中变成了“牛奶”(有 白色沉淀)。请你揭开魔术秘密:
(1)酒瓶中的液体可能是________;
(2)B 杯中产生的气体是________;
(3)写出 C 杯中发生的化学方程式________。
13.下表列出了部分酸、碱、盐在20℃时的溶解性.
阴离子/阳离子 氢氧根离子 硝酸根离子 氯离子 硫酸根离子 碳酸根离子
H+ 溶、挥 溶、挥 溶 溶、挥
Na+ 溶 溶 溶 溶 溶
Ba2+ 溶 溶 溶 不 不
Cu2+ 不 溶 溶 溶 —
请依据上表,按要求回答下列问题:
(1)写出氢氧根离子的符号________.
(2)写出一种不溶性碱的化学式________,写出一种可溶性盐的化学式________。
(3)氯化钙溶液与硝酸钠溶液________(填“能”或“不能”)发生反应,原因是________。
(4)碱和盐反应时,反应物一般都须是可溶的.请写出一个碱和盐反应的化学方程式:________。
(5)NaOH和Ca(OH)2是两种可溶性碱,其溶液均为无色.请写出一种能鉴别这两种物质的试剂名称________.
14.现有一包白色固体粉末,可能含有CuSO4、Na2SO4、CaCO3、NaCl、NH4HCO3中的一种或几种。现做如下实验:
(1)取少量白色固体加热,无氨味,则原固体中一定不含________。
(2)另取少量白色固体加足量的水溶解,得到无色澄清溶液,则此白色固体粉末中一定没有________、________。
(3)取上述溶液适量,滴加过量的BaCl2溶液,出现白色沉淀,再加入足量稀硝酸,沉淀不消失。则此白色固体粉末中一定含有________,可能含有________,写出产生白色沉淀的化学方程式________。
15.氯碱工业以粗盐(主要成分是NaCl,含少量泥沙、CaCl2、MgCl2)为原料,生产氯气和氢氧化钠,模拟流程如下:
(1)试剂A与试剂B的组合为________(填序号)
①KOH ② NaOH ③K2CO3 ④Na2CO3
(2)操作A需使用玻璃棒,玻璃棒的作用是________
(3)流程中Mg元素必须转化成________(填化学式)才能完全除去
(4)写出电解NaCl溶液的化学方程式________
(5)该工业副产品H2目前还不能作为燃料被广泛应用,其理由________(答一条即可)
16.A~G为初中化学常见物质。已知A属于盐,是重要的建筑材料,G是赤铁矿石的主要成分,F可用于中和硫酸厂的废水。它们的转化关系如图所示(反应条件未完全标出)。
(1)写出G的化学式:________;
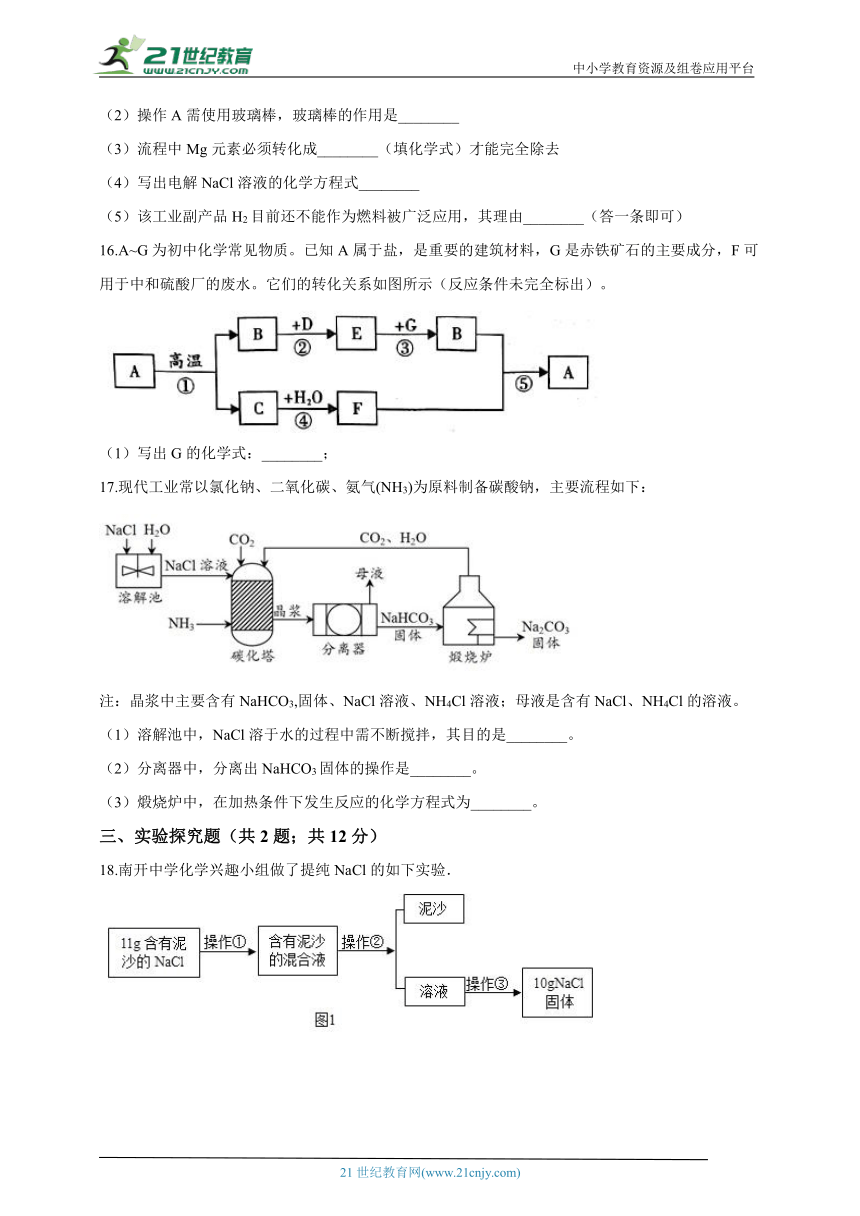
17.现代工业常以氯化钠、二氧化碳、氨气(NH3)为原料制备碳酸钠,主要流程如下:
注:晶浆中主要含有NaHCO3,固体、NaCl溶液、NH4Cl溶液;母液是含有NaCl、NH4Cl的溶液。
(1)溶解池中,NaCl溶于水的过程中需不断搅拌,其目的是________。
(2)分离器中,分离出NaHCO3固体的操作是________。
(3)煅烧炉中,在加热条件下发生反应的化学方程式为________。
三、实验探究题(共2题;共12分)
18.南开中学化学兴趣小组做了提纯NaCl的如下实验.
请根据实验回答下列问题:
(1)操作①、②、③依次为图中的(填序号)________.
(2)操作③中玻璃棒的作用是________.
(3)如图A操作,当蒸发皿中出现________时,应停止加热.
(4)若得到NaCl的产率比实际值偏低,则可能的原因是(填序号)_____.
A.过滤时滤纸有破损
B.蒸发时有固体溅出
C.把固体从蒸发皿转移到天平上称量时,有较多固体粘在了蒸发皿上
D.溶解11g含有泥沙的NaCl时,加入的水量不足
(5)用上述实验所得的氯化钠配制溶质质量分数为5%的氯化钠溶液50g,不需要的仪器为(填序号)________.
A量筒 B天平 C烧杯 D漏斗 E蒸发皿 F玻璃棒 G酒精灯
19.某校化学兴趣小组的同学学习了酸、碱、盐的知识后,对课本中“酸、碱、盐之间并不是都能发生复分解反应”这句话产生了兴趣,展开了探究性学习。
(提出问题)发生复分解反应应具备哪些条件?
(1)(活动探究)该小组同学进行以下四组实验,发现均能反应,写出④的化学方程式:________。
①硝酸钡溶液与稀硫酸
②稀硫酸与碳酸钾溶液
③稀盐酸与氢氧化钠溶液
④硝酸钡溶液与碳酸钾
(2)(理论分析)上述反应为什么能够发生?是因为在这些反应物的溶液中有特殊的阴、阳离子,它们两两结合生成了沉淀或气体或水。如:
①中有 ;
②中有 ;
③中有 ;
④中有________两种离子,所以才发生化学反应。
(3)(得出结论)经过分析,该小组同学得出以下结论:生成物中是否有沉淀或气体或________,是判断酸、碱、盐之间能否发生复分解反应的主要条件。
(4)(形成网络)按照一定的顺序排列某些离子,就可以形成一种知识网络。在网络中,用“-”相连接的阴、阳离子间能两两结合生成沉淀或气体或水。现有 、 两种离子,请将它们填入下面合适的“ ”内,使其形成一个更为完整的复分解反应的知识网络。
________ ________
四、计算题(共1题;共7分)
20.纯碱是一种重要的工业原料,盐湖中的纯碱常常会含有少量的氯化钠(其它杂质忽略不计)。取6g纯碱样品放在烧杯中并不断滴入稀盐酸,当稀盐酸滴加至35g时,烧杯内溶液的总质量为38.8g(假设产生的气体全部逸出),产生气体的质量与滴入稀盐酸的质量关系如下图所示。请计算:
(1)A点产生气体的质量m是________g。
(2)B点时,烧杯内溶液中的溶质是________(写化学式)。
(3)纯碱样品中碳酸钠的质量分数。(精确到0.1%)
课题一 生活中常见的盐 同步测试题参考答案
一、单选题
1. C 2. A 3. C 4. C 5. B 6. C 7. D 8. B 9. C 10. C
二、综合题
11. (1)a(2)c(3)f(4)b(5)e(6)d
12. (1)碳酸钠(2)二氧化碳
(3)Na2CO3+Ca(OH) 2=CaCO3↓+2NaOH
13. (1)OH-
(2)Cu(OH)2;CuSO4
(3)不能;不符合复分解反应的条件
(4)CuSO4+2NaOH═Cu(OH)2↓+Na2SO4
(5)二氧化碳或者碳酸钠溶液
14. (1)NH4HCO3
(2)CuSO4或CaCO3;CaCO3或CuSO4
(3)Na2SO4 ;NaCl;BaCl2 + Na2SO4=2NaCl + BaSO4↓
15. (1)②④
(2)引流
(3)Mg(OH)2
(4)2NaCl+2H2O H2↑+Cl2↑+2NaOH
(5)H2不易储存和运输或生产H2的成本高
16. (1)Fe2O3
17. (1)加速溶解
(2)过滤
(3)2NaHCO3 Na2CO3+H2O+CO2↑
三、实验探究题
18. (1)C、B、A
(2)加快氯化钠的溶解速率
(3)较多固体
(4)B,C,D
(5)DEG
19. (1)Ba(NO3)2+K2CO3==BaCO3↓+2KNO3
(2)Ba2++CO32-==BaCO3↓
(3)水
(4);
四、计算题
20. (1)2.2
(2)NaCl、HCl
(3)设样品中碳酸钠的质量为x,
Na2CO3+2HCl=2NaCl+ H2O+CO2↑
106 44
X 2.2g
x=5.3g,
纯碱样品中碳酸钠的质量分数为
答:纯碱样品中碳酸钠的质量分数88.3%。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
课题一 生活中常见的盐 同步测试题
一、单选题(共10题;共20分)
1.“84消毒液”是宾馆、医院、学校等一些公共场所常备的消毒剂,适用于环境和物体表面消毒,其有效成分主要是次氯酸钠(化学式为NaClO)。次氯酸钠属于( )
A. 酸 B. 碱 C. 盐 D. 氧化物
2.在发酵面团中加入含下列某种物质的溶液揉和,既能除去面团中的酸,又能使蒸出的馒头疏松多孔。这种物质是( )
A. Na2CO3 B. Ca(OH)2 C. CaO D. NaCl
3.泉州是海上丝绸之路的起点,古代的染坊常用某种“碱剂”来精炼丝绸,其主要成分是一种盐,水溶液呈碱性,它能使促进蚕丝表面的丝胶蛋白质水解而除去,从而使丝绸颜色洁白、质感柔软、色泽光亮,这种“碱剂”可能是( )
A. 食盐 B. 烧碱 C. 草木灰 D. 熟石灰
4.四瓶失去标签的溶液分别为:①NaOH、②CuSO4、③MgCl2、④Na2SO4 , 不用其它任何试剂而要将它们一一鉴别出来的正确顺序是( )
A. ③①②④ B. ②③④① C. ②①③④ D. ①③②④
5.某一无色溶液具有下列性质:①使无色酚酞试液变红;②与CuSO4溶液反应可产生蓝色沉淀;③与纯碱溶液反应产生白色沉淀。此溶液是( )
A. 氢氧化钠溶液 B. 澄清石灰水 C. 氯化钙溶液 D. 盐酸
6.氨碱法生产纯碱的主要反应原理如下: ;2NaHCO3 Na2CO3+CO2↑+H2O,下列有关“侯氏制碱法”的叙述中,错误的是( )
A. 加热时的稳定性:碳酸钠 碳酸氢钠
B. 用食盐制纯碱还需要要含碳、氧元素的物质
C. 配制饱和食盐水时,可通过搅拌来提高食盐的溶解度
D. 向饱和食盐中先通入氨气的作用是使溶液呈碱性,促进二氧化碳的吸收
7.贝壳的主要成分是碳酸钙,小强设计了如图的实验进行探究,以下关于此实验现象的描述中,错误的是( )
A. 有气泡产生 B. 表面皿内壁有浑浊出现
C. 贝壳逐渐溶解 D. 烧杯中溶液的质量不变
8.某中学化学兴趣小组四名学生,对某厂排放的污水进行检测,先取废液观察,呈无色、均一、透明状,然后用pH试纸测得污水的pH=1.下表为四名学生对该厂废水成分初步检测的分析结果,可能正确的是()
A. NaOH、KNO3、CuSO4、NaCl B. KNO3、NaCl、Na2SO4、HCl
C. HCl、Na2CO3、Na2SO4 D. HCl、H2SO4、KNO3、BaCl2
9.为除去粗盐中的泥沙、Ca2+、Mg2+、SO42-等杂质,可将粗盐溶于水,再进行下列五步操作:①过滤②加过量的氢氧化钠溶液③加适量盐酸④加过量的碳酸钠溶液⑤加过量的氯化钡溶液。正确的操作顺序是()
A. ④⑤②①③ B. ②④⑤①③
C. ②⑤④①③ D. ⑤②④③①
10.甲、乙、丙、丁是初中化学常见的物质,它们的转化关系如图所示(反应条件已省略)。下列说法正确的是( )
A. 若丁是水,则该反应一定属于中和反应
B. 若丙为沉淀,则甲、乙中一定有一种物质是盐
C. 若甲、丁均为单质,则该反应一定属于置换反应
D. 若乙是一种碱、丁是一种盐,则该反应一定属于复分解反应
二、综合题(共7题;共31分)
11.有下列几种物质,请选择合适的标号(a~f)填空(不得重复)
a.稀盐酸 b.稀硫酸 c.熟石灰
d.硫酸铜 e.食盐 f.生石灰
(1)少量存于胃液中帮助消化的是________
(2)常用降低土壤酸性的是________
(3)常用于食品干燥剂的是________
(4)用来清除铁锈的物质________
(5)医学上用于配制生理盐水的是 ________
(6)农业上用于配制波尔多液的是 ________
12.晓红同学为同学们表演了一组化学魔术,在三支盛有液体的玻璃杯中,分 别倒入用酒瓶装的一种液体,同学们看到下列奇特现象:A 杯中变成了“红葡萄酒”(变为红色);B 杯变成了“汽水”(产生大量的气泡);C 杯中变成了“牛奶”(有 白色沉淀)。请你揭开魔术秘密:
(1)酒瓶中的液体可能是________;
(2)B 杯中产生的气体是________;
(3)写出 C 杯中发生的化学方程式________。
13.下表列出了部分酸、碱、盐在20℃时的溶解性.
阴离子/阳离子 氢氧根离子 硝酸根离子 氯离子 硫酸根离子 碳酸根离子
H+ 溶、挥 溶、挥 溶 溶、挥
Na+ 溶 溶 溶 溶 溶
Ba2+ 溶 溶 溶 不 不
Cu2+ 不 溶 溶 溶 —
请依据上表,按要求回答下列问题:
(1)写出氢氧根离子的符号________.
(2)写出一种不溶性碱的化学式________,写出一种可溶性盐的化学式________。
(3)氯化钙溶液与硝酸钠溶液________(填“能”或“不能”)发生反应,原因是________。
(4)碱和盐反应时,反应物一般都须是可溶的.请写出一个碱和盐反应的化学方程式:________。
(5)NaOH和Ca(OH)2是两种可溶性碱,其溶液均为无色.请写出一种能鉴别这两种物质的试剂名称________.
14.现有一包白色固体粉末,可能含有CuSO4、Na2SO4、CaCO3、NaCl、NH4HCO3中的一种或几种。现做如下实验:
(1)取少量白色固体加热,无氨味,则原固体中一定不含________。
(2)另取少量白色固体加足量的水溶解,得到无色澄清溶液,则此白色固体粉末中一定没有________、________。
(3)取上述溶液适量,滴加过量的BaCl2溶液,出现白色沉淀,再加入足量稀硝酸,沉淀不消失。则此白色固体粉末中一定含有________,可能含有________,写出产生白色沉淀的化学方程式________。
15.氯碱工业以粗盐(主要成分是NaCl,含少量泥沙、CaCl2、MgCl2)为原料,生产氯气和氢氧化钠,模拟流程如下:
(1)试剂A与试剂B的组合为________(填序号)
①KOH ② NaOH ③K2CO3 ④Na2CO3
(2)操作A需使用玻璃棒,玻璃棒的作用是________
(3)流程中Mg元素必须转化成________(填化学式)才能完全除去
(4)写出电解NaCl溶液的化学方程式________
(5)该工业副产品H2目前还不能作为燃料被广泛应用,其理由________(答一条即可)
16.A~G为初中化学常见物质。已知A属于盐,是重要的建筑材料,G是赤铁矿石的主要成分,F可用于中和硫酸厂的废水。它们的转化关系如图所示(反应条件未完全标出)。
(1)写出G的化学式:________;
17.现代工业常以氯化钠、二氧化碳、氨气(NH3)为原料制备碳酸钠,主要流程如下:
注:晶浆中主要含有NaHCO3,固体、NaCl溶液、NH4Cl溶液;母液是含有NaCl、NH4Cl的溶液。
(1)溶解池中,NaCl溶于水的过程中需不断搅拌,其目的是________。
(2)分离器中,分离出NaHCO3固体的操作是________。
(3)煅烧炉中,在加热条件下发生反应的化学方程式为________。
三、实验探究题(共2题;共12分)
18.南开中学化学兴趣小组做了提纯NaCl的如下实验.
请根据实验回答下列问题:
(1)操作①、②、③依次为图中的(填序号)________.
(2)操作③中玻璃棒的作用是________.
(3)如图A操作,当蒸发皿中出现________时,应停止加热.
(4)若得到NaCl的产率比实际值偏低,则可能的原因是(填序号)_____.
A.过滤时滤纸有破损
B.蒸发时有固体溅出
C.把固体从蒸发皿转移到天平上称量时,有较多固体粘在了蒸发皿上
D.溶解11g含有泥沙的NaCl时,加入的水量不足
(5)用上述实验所得的氯化钠配制溶质质量分数为5%的氯化钠溶液50g,不需要的仪器为(填序号)________.
A量筒 B天平 C烧杯 D漏斗 E蒸发皿 F玻璃棒 G酒精灯
19.某校化学兴趣小组的同学学习了酸、碱、盐的知识后,对课本中“酸、碱、盐之间并不是都能发生复分解反应”这句话产生了兴趣,展开了探究性学习。
(提出问题)发生复分解反应应具备哪些条件?
(1)(活动探究)该小组同学进行以下四组实验,发现均能反应,写出④的化学方程式:________。
①硝酸钡溶液与稀硫酸
②稀硫酸与碳酸钾溶液
③稀盐酸与氢氧化钠溶液
④硝酸钡溶液与碳酸钾
(2)(理论分析)上述反应为什么能够发生?是因为在这些反应物的溶液中有特殊的阴、阳离子,它们两两结合生成了沉淀或气体或水。如:
①中有 ;
②中有 ;
③中有 ;
④中有________两种离子,所以才发生化学反应。
(3)(得出结论)经过分析,该小组同学得出以下结论:生成物中是否有沉淀或气体或________,是判断酸、碱、盐之间能否发生复分解反应的主要条件。
(4)(形成网络)按照一定的顺序排列某些离子,就可以形成一种知识网络。在网络中,用“-”相连接的阴、阳离子间能两两结合生成沉淀或气体或水。现有 、 两种离子,请将它们填入下面合适的“ ”内,使其形成一个更为完整的复分解反应的知识网络。
________ ________
四、计算题(共1题;共7分)
20.纯碱是一种重要的工业原料,盐湖中的纯碱常常会含有少量的氯化钠(其它杂质忽略不计)。取6g纯碱样品放在烧杯中并不断滴入稀盐酸,当稀盐酸滴加至35g时,烧杯内溶液的总质量为38.8g(假设产生的气体全部逸出),产生气体的质量与滴入稀盐酸的质量关系如下图所示。请计算:
(1)A点产生气体的质量m是________g。
(2)B点时,烧杯内溶液中的溶质是________(写化学式)。
(3)纯碱样品中碳酸钠的质量分数。(精确到0.1%)
课题一 生活中常见的盐 同步测试题参考答案
一、单选题
1. C 2. A 3. C 4. C 5. B 6. C 7. D 8. B 9. C 10. C
二、综合题
11. (1)a(2)c(3)f(4)b(5)e(6)d
12. (1)碳酸钠(2)二氧化碳
(3)Na2CO3+Ca(OH) 2=CaCO3↓+2NaOH
13. (1)OH-
(2)Cu(OH)2;CuSO4
(3)不能;不符合复分解反应的条件
(4)CuSO4+2NaOH═Cu(OH)2↓+Na2SO4
(5)二氧化碳或者碳酸钠溶液
14. (1)NH4HCO3
(2)CuSO4或CaCO3;CaCO3或CuSO4
(3)Na2SO4 ;NaCl;BaCl2 + Na2SO4=2NaCl + BaSO4↓
15. (1)②④
(2)引流
(3)Mg(OH)2
(4)2NaCl+2H2O H2↑+Cl2↑+2NaOH
(5)H2不易储存和运输或生产H2的成本高
16. (1)Fe2O3
17. (1)加速溶解
(2)过滤
(3)2NaHCO3 Na2CO3+H2O+CO2↑
三、实验探究题
18. (1)C、B、A
(2)加快氯化钠的溶解速率
(3)较多固体
(4)B,C,D
(5)DEG
19. (1)Ba(NO3)2+K2CO3==BaCO3↓+2KNO3
(2)Ba2++CO32-==BaCO3↓
(3)水
(4);
四、计算题
20. (1)2.2
(2)NaCl、HCl
(3)设样品中碳酸钠的质量为x,
Na2CO3+2HCl=2NaCl+ H2O+CO2↑
106 44
X 2.2g
x=5.3g,
纯碱样品中碳酸钠的质量分数为
答:纯碱样品中碳酸钠的质量分数88.3%。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
同课章节目录
