第三章 烃的衍生物 单元测试(含解析) 2022-2023学年下学期高二化学人教版(2019)选择性必修3
文档属性
| 名称 | 第三章 烃的衍生物 单元测试(含解析) 2022-2023学年下学期高二化学人教版(2019)选择性必修3 |

|
|
| 格式 | docx | ||
| 文件大小 | 703.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-12-09 00:00:00 | ||
图片预览



文档简介
第三章《烃的衍生物》单元测试
一、单选题(共14题)
1.下列推理结果正确的是
A.目前芯片用硅基材料,未来可能用碳基材料
B.金属钠在空气中燃烧生成,则金属锂在空气燃烧生成
C.通入溶液中至过量,没有明显现象,则通入溶液中至过量,也没明显现象
D.1乙醛和足量的银氨溶液反应可得2金属银,则1甲醛和足量的银氨溶液反应也可得2银
2.下列除去杂质的方法正确的是
①除去乙烷中少量的乙烯:光照条件下通入Cl2,气液分离;
②除去乙酸乙酯中少量的乙酸:用饱和碳酸钠溶液洗涤,分液;
③除去苯中混有的少量苯酚:加入浓溴水后过滤取滤液;
④除去乙醇中少量的乙酸:加足量生石灰,蒸馏。
⑤除去硝基苯中混有的浓硝酸和浓硫酸,加入NaOH溶液,静置,分液
⑥溴苯中混有溴,加入KI溶液,振荡,再用汽油萃取
A.①②⑥ B.②④⑤ C.③④⑥ D.②③④⑤
3.二羟基甲戊酸是合成青蒿素的原料之一,其结构如图a所示。下列有关二羟基甲戊酸的说法错误的是
A.二嵯基甲戊酸的分子式为
B.与乳酸(结构如图b)互为同系物
C.与乙醇、乙酸均能发生酯化反应,能使酸性溶液褪色
D.等量的二羟基甲戊酸消耗Na和的物质的量之比为3∶1
4.下列过程对应的离子反应方程式书写正确的是
A.乙酰胺与NaOH溶液混合共热:
B.NaHCO3溶液与过量澄清石灰水混合:
C.苯酚钠溶液中通入CO2出现浑浊:2 +CO2+H2O→2 +CO
D.以镁作电极电解MgCl2水溶液:
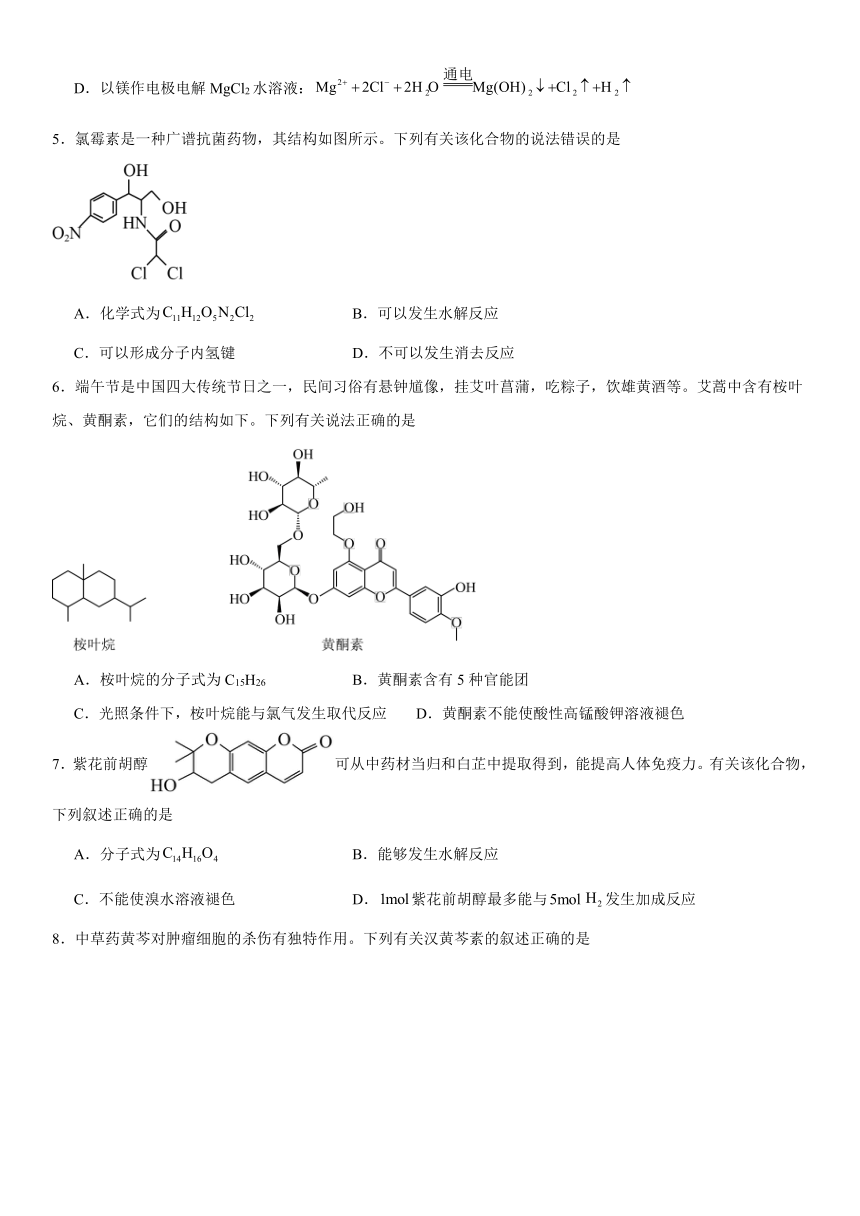
5.氯霉素是一种广谱抗菌药物,其结构如图所示。下列有关该化合物的说法错误的是
A.化学式为 B.可以发生水解反应
C.可以形成分子内氢键 D.不可以发生消去反应
6.端午节是中国四大传统节日之一,民间习俗有悬钟馗像,挂艾叶菖蒲,吃粽子,饮雄黄酒等。艾蒿中含有桉叶烷、黄酮素,它们的结构如下。下列有关说法正确的是
A.桉叶烷的分子式为C15H26 B.黄酮素含有5种官能团
C.光照条件下,桉叶烷能与氯气发生取代反应 D.黄酮素不能使酸性高锰酸钾溶液褪色
7.紫花前胡醇可从中药材当归和白芷中提取得到,能提高人体免疫力。有关该化合物,下列叙述正确的是
A.分子式为 B.能够发生水解反应
C.不能使溴水溶液褪色 D.紫花前胡醇最多能与发生加成反应
8.中草药黄芩对肿瘤细胞的杀伤有独特作用。下列有关汉黄芩素的叙述正确的是
A.汉黄芩素有4种含氧官能团
B.该物质遇溶液能显色
C.该物质分子式为
D.与足量发生完全加成反应,1该物质最多消耗7
9.下列实验操作正确且能达到预期目的的是
编号 实验目的 操作
A 欲证明 CH2=CHCHO 中含有碳碳双键 滴入酸性 KMnO4 溶液,看紫红色是否褪去
B 欲除去苯中混有的苯酚 向混合液中加入浓溴水,充分反应后,过滤
C 比较铜和镁的金属活动性强弱 用石墨作电极电解等浓度 Mg(NO3)2、Cu(NO3)2 的混合液
D 确定碳和氯两元素非金属性强弱 测同温同浓度 NaHCO3 和 NaClO 水溶液的 pH
A.A B.B C.C D.D
10.下列有关高级脂肪酸甘油酯的说法正确的是
A.高级脂肪酸甘油酯是高分子化合物
B.天然的不饱和高级脂肪酸甘油酯都是简单甘油酯
C.植物油可以使酸性高锰酸钾溶液褪色
D.高级脂肪酸和乙酸互为同系物
11.乙醇催化氧化制取乙醛(沸点为20.8℃,能与水混溶)的装置(夹持装置已略) 如图所示。下列说法错误的是
A.①中用胶管连接其作用是平衡气压,便于液体顺利流下
B.实验过程中铜丝会出现红黑交替变化
C.实验开始时需先加热②,再通O2,然后加热③
D.实验结束时需先将④中的导管移出,再停止加热。
12.下列有关乙酸性质的叙述错误的是
A.乙酸是有强烈刺激性气味的无色液体,易溶于水和乙醇
B.乙酸的沸点比乙醇高
C.乙酸的酸性比碳酸强,它是一元酸,能与碳酸盐反应
D.在发生酯化反应时,乙酸分子羧基中的氢原子跟醇分子中的羟基结合成水
13.下列各组中的反应,属于同一反应类型的是
A.由2-溴丙烷水解制2-丙醇;由丙烯与水反应制1-丙醇
B.由甲苯硝化制对硝基甲苯;由甲苯与酸性高锰酸钾溶液反应制苯甲酸
C.由氯代环己烷制环己烯;由丙烯与溴水反应制1,2-二溴丙烷
D.由苯与液溴反应制溴苯;乙醇在浓硫酸作用下加热至140℃时生成乙醚
14.下列方案设计、现象和结论都正确的是
目的 方案设计 现象和结论
A 检验某无色溶液中是否含有 取少量该溶液于试管中,加稀硝酸酸化,再加入硝酸钡溶液 若有白色沉淀生成,则该溶液中一定含有
B 探究不同金属离于对分解速率的影响 取2支试管,向2支试管中各加入5 mL 6%溶液,分别向试管中各加入溶液和溶液 相同时间内产生气泡多的,则催化效果好
C 判断某有机物是否为醛类 取2mL样品溶液于试管中,加入5~6滴新制氢氧化铜,加热 若产生砖红色沉淀,则该有机物属于醛类
D 检验某无色气体是否为 将气体通入品红溶液中,再加热 若通入气体后品红溶液褪色,加热该褪色溶液能恢复红色,则一定为
A.A B.B C.C D.D
二、填空题(共8题)
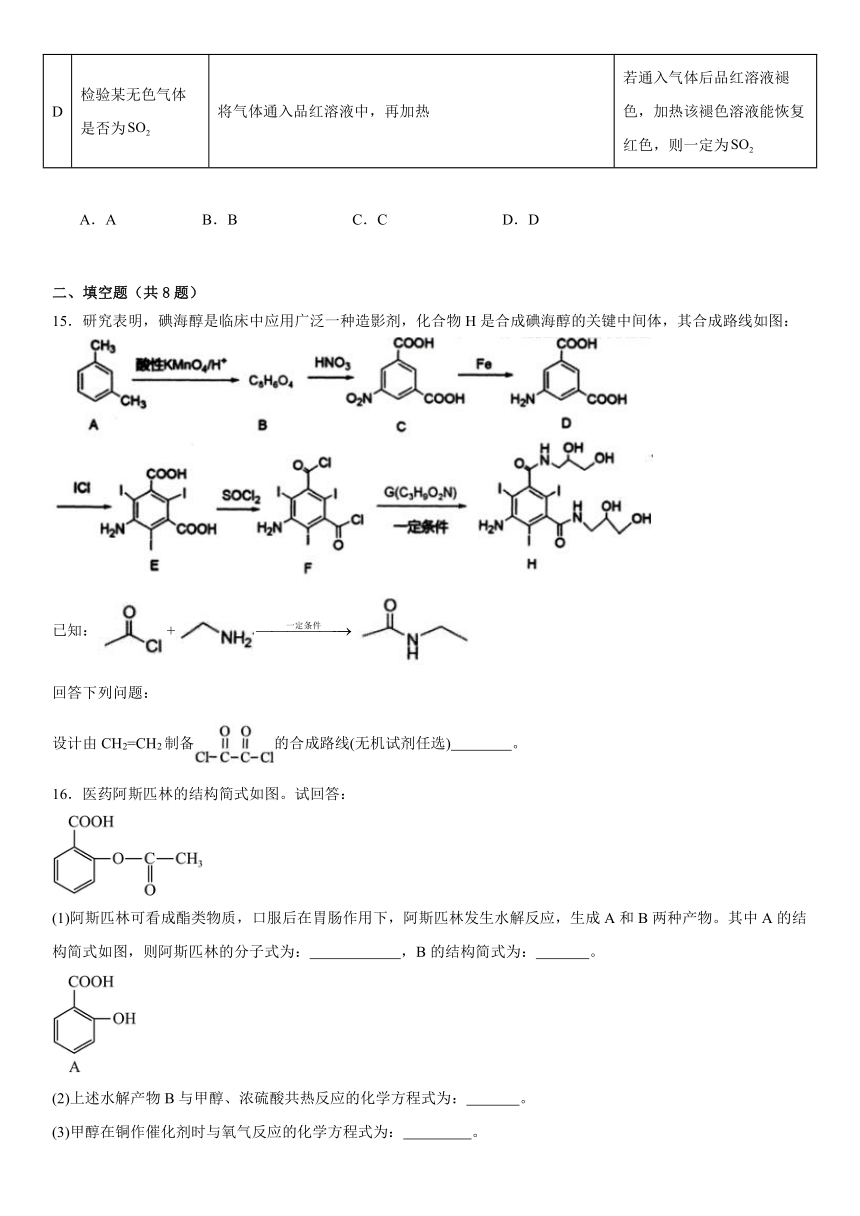
15.研究表明,碘海醇是临床中应用广泛一种造影剂,化合物H是合成碘海醇的关键中间体,其合成路线如图:
已知:+
回答下列问题:
设计由CH2=CH2制备的合成路线(无机试剂任选) 。
16.医药阿斯匹林的结构简式如图。试回答:
(1)阿斯匹林可看成酯类物质,口服后在胃肠作用下,阿斯匹林发生水解反应,生成A和B两种产物。其中A的结构简式如图,则阿斯匹林的分子式为: ,B的结构简式为: 。
(2)上述水解产物B与甲醇、浓硫酸共热反应的化学方程式为: 。
(3)甲醇在铜作催化剂时与氧气反应的化学方程式为: 。
17.回答下列问题
(1)现有下列4种重要的有机物:
a.CH3CH2CHO b.CH3CH2CH3 c. d.
①与新制氢氧化铜反应的方程式 。
②能与浓硝酸反应生成TNT的方程式是 。
③滴浓溴水产生白色沉淀的方程式是: 。
④能发生消去反应的化学方程式: 。
(2)在潜水艇和消防员呼吸面具中,Na2O2所发生的化学反应方程式 , 。
(3)氯化亚铁溶液中滴加氢氧化钠溶液,产生白色沉底,最后变成红褐色 , 。
18.已知一个碳原子连两个—OH的结构不稳定,会很快脱去一分子水,其变化如下:
→ + H2O
下图中B和、等都是A和Cl2发生反应生成的产物,E是一种高分子化合物,透光性能好,常用作一些灯饰外壳。过程中一些小分子都已经略去。
(1)A的化学名称为
(2)第④步的化学方程式为 ,该反应类型为 ;
(3)第⑦步的化学方程式为 ,该反应类型为 ;
(4)E的结构简式为 ;
(5)符合下列条件:苯环上有两个取代基且苯环上只有两种不同化学环境的氢的C的同分异构体的结构简式分别是 、 、 。
19.有机物A可以通过不同化学反应分别制得B、C和D三种物质,结构简式如图所示:
(1)A的分子式是 ;B中的含氧官能团名称是 。
(2)A→B的反应类型是 ;A~D中互为同分异构体的是 (填代号)。
(3)D在酸性条件下水解的化学方程式是 。
(4)检验B中醛基的方法 。
20.烃A可以发生下列过程所示的变化:
(1)烃A的结构简式是 ;
(2)反应①属 反应;
(3)反应②的化学方程式是 ,属 反应;反应③的化学方程式是 ,属 反应。
21.某实验兴趣小组用李比希法、现代仪器等测定有机物X的组成和结构。实验测得0.300 g样品X完全燃烧,产物气体先通过干燥剂高氯酸镁,高氯酸镁质量增加0.180 g,再通过碱石灰,碱石灰质量增加0.440 g。
(1)由实验数据分析计算可得X的实验式(最简式)为 。
(2)若红外光谱测得X中含有“C=O”和“C—O—C”的结构,质谱法测得X的相对分子质量是60,则X的名称为 。
(3)若质谱法测得X的相对分子质量是90,两分子X能通过酯化反应形成六元环状结构的有机物Y,Y的结构简式为 。
22.有机物的性质与其所具有的官能团直接相关,辨析有机物的官能团,运用官能团的性质分析、理解有机物发生的反应是掌握有机物的金钥匙。某有机化合物A的结构简式为,回答下列问题:
(1)A中含有的官能团名称分别有 ,下列反应中①加成;②水解;③酯化;④氧化;⑤中和;⑥消去;⑦还原,其中A可以发生的有 填字母序号)
a.①②③④⑤⑥⑦ b.①③④⑤⑦ c.①③④⑤⑥⑦ d.②③④⑤⑥
(2)取一定量Na、NaOH、NaHCO3分别与等物质的量A充分反应,则消耗Na、NaOH、NaHCO3三种物质的物质的量之比为
(3)A与足量Na2CO3反应所得有机产物的结构简式是 。
某种兴奋剂的结构简式如图所示,回答下列问题:
。
(4)该兴奋剂与FeCl3溶液混合,现象是 。
(5)滴入KMnO4酸性溶液,振荡,紫色褪去,并不能证明其结构中含有碳碳双键,理由是 ,下列证明其结构中含有碳碳双键的方法中,合理且简单易行的是 。
A.加入浓溴水,溴水褪色
B.先加入足量NaOH溶液再加入浓溴水,溴水褪色
C.先加入足量NaOH溶液再加入酸性KMnO4溶液,溶液褪色
D.先滴加NaOH溶液到刚好反应,再加入溴水,溴水褪色
(6)1mol该物质分别与浓溴水和H2反应时,最多消耗Br2和H2的物质的量分别为 mol和 mol。
EPA(二十碳五烯酸)、DPA(二十二碳五烯酸)、DHA(二十二碳六烯酸,常称脑黄金)是不饱和程度大的长链脂肪酸(即高级脂肪酸),属于ω-3不饱和脂肪酸,是人体大脑发育、成长的重要物质,结构简式如下图。它们与甘油形成的酯是油脂的成分之一:
回答下列问题:
(7)关于EPA、DPA、DHA的下列说法中,错误的是_______。
A.EPA与DPA互为同系物 B.DPA与DHA互为同分异构体
C.EPA的分子式为C20H30O2 D.DHA的甘油酯常温下为液态
(8)油脂在人体新陈代谢中发挥着重要的作用。有关油脂的说法错误的是_______。
A.油脂的水解叫皂化反应
B.天然油脂大多为混甘油酯
C.硬脂酸(C17H35COOH)甘油酯沸点可能比DPA甘油酯高
D.油脂的主要成分是高级脂肪酸的甘油酯,属于酯类
(9)“深海鱼油”含较丰富的DHA甘油酯,请结合结构解释“深海鱼油”为什么一般做成胶囊状 。
试卷第1页,共3页
参考答案:
1.A
【详解】A.目前芯片都是使用硅基半导体材料制造的,被称为硅基芯片,未来碳基芯片将成为芯片发展的主流,故A正确;
B.Na的金属性强于Li,金属钠在空气中燃烧生成,金属锂在空气燃烧生成,故B错误;
C.硝酸的酸性比碳酸强,则通入溶液中至过量,没有明显现象,但通入溶液中至过量,由于硝酸根在酸性条件下具有强的氧化性,二氧化硫被氧化成硫酸根,硫酸根与钡离子生成硫酸钡白色沉淀,故C错误;
D.1乙醛分子中含有1mol醛基,与足量的银氨溶液反应可得2金属银,而1mol甲醛分子中可以看成有2mol醛基,则与足量的银氨溶液反应可得4银,故D错误;
答案选A。
2.B
【详解】①光照条件下通入Cl2 ,氯气会和乙烷之间发生取代反应,和乙烯之间发生加成反应,虽然将杂质除去,但是将要留的物质反应了,不符合除杂的原则,故①错误;
②饱和碳酸钠溶液可以和乙酸之间发生中和反应,但是和乙酸乙酯是互不相溶的,分液即可实现分离,故②正确;
③溴易溶于苯,用溴水除杂会引入新的杂质,则除去苯中的少量苯酚,向混合物中加入NaOH溶液后分液,故③错误;
④乙酸与生石灰反应,而乙醇不能,且乙醇易挥发,而乙酸钙为离子型化合物,沸点高,故除去乙醇中少量的乙酸可以加足量生石灰后蒸馏,故④正确;
⑤硝基苯中混有浓硝酸和浓硫酸,加入NaOH溶液,浓硝酸和浓硫酸都可与NaOH反应,而硝基苯不反应且不溶于水,所以可用NaOH溶液除杂,故⑤正确;
⑥溴苯中混有溴,加入KI溶液,Br2能与KI溶液反应生成I2单质,I2与溴苯互溶,不能分离,再加入汽油,I2单质与溴苯汽油互溶,无法用汽油萃取,故⑥错误;
综上所述②④⑤正确,故选B。
3.B
【详解】A.根据结构简式可知,二甲戊酸的分子式为C6H12O4,A正确;
B.两者结构不相似,故不为同系物,B错误;
C.由图a可知,二羟基甲戊酸含有两个羟基和1个羧基,羟基能与乙酸发生酯化反应,其中-CH2OH中的羟基能使酸性高锰酸钾溶液褪色,羧基能与乙醇发生酯化反应,C正确;
D.羟基羧基均能与钠反应,与碳酸氢钠反应的只能是羧基,等量的二羟基甲戊酸消耗Na和的物质的量之比为3∶1,D正确;
答案选B。
4.A
【详解】A.乙酰胺与NaOH溶液混合共热发生水解反应生成乙酸钠和氨气,反应的离子方程式是,故A正确;
B.NaHCO3溶液与过量澄清石灰水混合,生成氢氧化钠、碳酸钙、水,反应的离子方程式是,故B错误;
C.苯酚钠溶液中通入CO2生成碳酸氢钠、苯酚,反应的离子方程式是 +CO2+H2O→ +HCO,故C错误;
D.以镁作电极电解MgCl2水溶液,阳极镁失电子生成镁离子,阴极氢离子得电子生成氢气,电解方程式为,故D错误;
选A。
5.D
【详解】A.由结构简式可知氯霉素的化学式为,故A正确;
B.酰胺基、氯原子的存在使氯霉素可以发生水解反应,故B正确;
C.羟基上的H原子和另一个羟基上的氧原子、亚氨基的N形成分子内氢键,氮原子上的H可以和羟基山的氧形成分子间氢键,故C正确;
D.羟基相连C原子邻位的C原子上连有H原子,则该化合物可发生消去反应,故D错误;
故选:D。
6.C
【详解】A.根据桉叶烷的结构简式可知其分子式为C15H28,A错误;
B.根据黄酮素的结构简式可知,含有羟基,醚键,羰基,碳碳双键,4种官能团,B错误;
C.桉叶烷中碳原子上的氢原子光照条件下,可以和氯气发生取代反应,C正确;
D.黄酮素结构中含有碳碳双键和羟基,都可以被酸性高锰酸钾氧化,使其褪色,D错误;
故选C。
7.B
【详解】A.根据紫花前胡醇的结构简式可知,其分子式为,A项错误;
B.分子中含有酯基,能够发生水解反应,B项正确;
C.分子中含有碳碳双键,使溴水溶液褪色,C项错误;
D.分子中含有1个苯环和1个碳碳双键,故紫花前胡醇最多能与4mol发生加成反应,D项错误;
答案选B。
8.B
【详解】A.汉黄芩素有羟基、醚键、羰基3种含氧官能团,故A错误;
B.汉黄芩素有酚羟基,所以遇溶液能显色,故B正确;
C.根据汉黄芩素的结构简式,可知分子式为,故C错误;
D.苯环、碳碳双键、羰基都能与氢气发生加成反应,与足量发生完全加成反应,1该物质最多消耗8,故D错误;
选B。
9.C
【详解】A.碳碳双键和醛基都能被高锰酸钾氧化,不能用酸性高锰酸钾鉴别,A错误;
B.苯酚与浓溴水反应产生的三溴苯酚白色物质能够溶解在有机物苯中,不能通过过滤除去,B错误;
C.用石墨作电极电解混合溶液,阴极上铜离子放电,可以比较铜和镁的金属活动性强弱,C正确;
D.元素的非金属性越强,其最高价氧化物对应的水化物的酸性就越强。C的最高价含氧酸为H2CO3,对应的钠盐为NaHCO3,Cl的最高价含氧酸为HClO4,对应的钠盐为NaClO4,所以通过测同温同浓度 NaHCO3 和 NaClO 水溶液的 pH,无法确定C和Cl的非金属性强弱,D错误;
故答案为:C。
10.C
【详解】A.高分子化合物的相对分子质量一般为几万到几十万,高级脂肪酸甘油酯不是高分子化合物,A错;
B.天然的不饱和高级脂肪酸甘油酯一般为混合甘油酯,B错;
C.植物油中烃基部分含有不饱和键,所以可以使酸性高锰酸钾溶液褪色,C正确;
D.高级脂肪酸包括硬脂酸、软脂酸、油酸等,油酸分子中含有碳碳双键,不是乙酸的同系物,D错;
答案选C。
11.C
【详解】A.装置中若关闭K时向烧瓶中加入液体,会使烧瓶中压强增大,双氧水不能顺利流下,①中用胶管连接,打开K时,可以平衡气压,便于液体顺利流下,A选项正确;
B.实验中Cu作催化剂,但在过渡反应中,红色的Cu会被氧化成黑色的CuO,CuO又会被还原为红色的Cu,故会出现红黑交替的现象,B选项正确;
C.实验开始时应该先加热③,防止乙醇通入③时冷凝,C选项错误;
D.为防止倒吸,实验结束时需先将④中的导管移出,再停止加热,D选项正确;
答案选C。
12.D
【详解】乙酸是有强烈刺激性气味的无色液体,易溶于水和乙醇,沸点高于乙醇,含有一个羧基属于一元酸,酸性强于碳酸,能和碳酸盐反应,发生酯化反应时乙酸分子脱羟基,故选D。
13.D
【详解】A.由2-溴丙烷水解制2-丙醇是取代反应;由丙烯与水反应制1-丙醇是加成反应,A不符合题意;
B.由甲苯硝化制对硝基甲苯是取代反应;由甲苯与酸性高锰酸钾溶液反应制苯甲酸是氧化反应,B不符合题意;
C.由氯代环己烷制环己烯是消去反应;由丙烯与溴水反应制1,2-二溴丙烷是加成反应,C不符合题意;
D.由苯与液溴反应制溴苯是取代反应;乙醇在浓硫酸作用下加热至140℃时生成乙醚是取代反应,D符合题意;
故选D。
14.D
【详解】A.检验应用盐酸酸化,再加氯化钡溶液检验,故A错误;
B.探究不同金属离于对分解速率的影响应选用相同阴离子的金属盐,该方案中盐中的阴离子不同,无法排除阴离子的干扰,故B错误;
C.与氢氧化铜加热产生砖红色沉淀的可能是醛类,也可能是甲酸类物质,故C错误;
D.二氧化硫能使品红褪色,且加热能恢复,因此可用品红检验二氧化硫,故D正确;
故选:D。
15.CH2=CH2BrCH2CH2Br
【详解】利用题中信息,由CH2=CH2与溴发生加成反应生成1,2-二溴乙烷,1,2-二溴乙烷在氢氧化钠的水溶液中加热发生水解反应生成乙二醇,乙二醇被酸性高锰酸钾氧化生成乙二酸,乙二酸与SOCl2发生取代反应生成,故合成路线流程图为:CH2=CH2BrCH2CH2Br
故答案为:CH2=CH2BrCH2CH2Br。
16. C9H8O4 CH3COOH CH3COOH+CH3OHCH3COOCH3+H2O 2CH3OH+O22HCHO+2H2O
【分析】(1)由结构可知分子式,由图可知生成A为邻羟基苯甲酸,根据酯水解规律可知B为CH3COOH;
(2)乙酸与甲醇在浓硫酸存在条件下发生酯化反应生成乙酸甲酯;
(3)甲醇在铜作催化剂时与氧气反应生成HCHO。
【详解】(1)由结构可知阿斯匹林的分子式为C9H8O4,其中酯基-COOC-可发生水解反应生成A和B,生成A为邻羟基苯甲酸,则B为CH3COOH;
(2)阿司匹林水解产生A是邻羟基苯甲酸,B是乙酸,乙酸与甲醇、浓硫酸共热反应的化学方程式为CH3COOH+CH3OHCH3COOCH3+H2O;
(3)甲醇分子中羟基连接的C原子上有2个H原子,在铜作催化剂时与氧气发生氧化反应,产生甲醛和水,反应的化学方程式为2CH3OH+O22HCHO+2H2O。
【点睛】本题考查有机物的结构与性质,把握有机物的结构、官能团及性质为解答的关键,注意酯、羧酸、醇的性质和转化关系,侧重考查学生的分析与应用能力。
17.(1) CH3CH2CHO 2Cu(OH)2 CH3CH2COOH + Cu2O↓+ 2H2O +3HNO3+3H2O +3Br2↓+3HBr CH3CHClCH3+NaOHCH3CH=CH2↑+NaCl+H2O
(2) 2Na2O2+2CO2=2Na2CO3+O2↑ 2Na2O2+2H2O=4NaOH+O2↑
(3) FeCl2+2NaOH= Fe(OH)2+2NaCl 4Fe(OH)2+O2+2H2O= 4Fe(OH)3
【详解】(1)①醛类物质与新制氢氧化铜反应,相应的方程式应为a与新制氢氧化铜反应:CH3CH2CHO+ 2Cu(OH)2 CH3CH2COOH + Cu2O↓+ 2H2O。
②d能与浓硝酸反应生成TNT(三硝基甲苯)的方程式是:+3HNO3+3H2O。
③c与浓溴水反应产生白色沉淀(2,4,6-三溴苯酚)和氢溴酸,方程式是:+3Br2↓+3HBr。
④b能与氢氧化钠的乙醇溶液发生消去反应,化学方程式:CH3CHClCH3+NaOHCH3CH=CH2↑+NaCl+H2O。
(2)呼吸生成二氧化碳,则Na2O2所发生的化学反应方程式包括:2Na2O2+2CO2=2Na2CO3+O2↑;2Na2O2+2H2O=4NaOH+O2↑。
(3)氯化亚铁溶液中滴加氢氧化钠溶液,产生白色沉底(Fe(OH)2),Fe(OH)2氧化最后变成红褐色(Fe(OH)3),方程式包括FeCl2+2NaOH= Fe(OH)2+2NaCl; 4Fe(OH)2+O2+2H2O= 4Fe(OH)3。
18. 乙苯 氧化反应 加成反应
【详解】(1)A和氯气发生取代反应生成,所以A是乙苯,结构简式为。
(2)是卤代烃,可以发生水解反应,所以C的结构简式为。C中含有羟基,能发生催化氧化,方程式为:。
(3)C中含有羟基,也能发生消去反应,生成D,所以D的结构简式为。D中含有碳碳双键,能发生加成反应,方程式为:。
(4)D中含有碳碳双键,能发生加聚反应,生成高分子化合物E,所以E的结构简式为:。
(5)苯环上有两个取代基且苯环上只有两种不同化学环境的氢,说明两个取代基是对位的,所以根据C的分子式可知,如果取代基其中之一是乙基,则对位就是酚羟基;如果是甲基,则对位就是-CH2OH或-OCH3,所以可能的结构简式为。
19. C9H10O3 醛基、羧基 氧化反应 C和D +H2O 取少量B于试管中,加适量NaOH使溶液为碱性,再与新制氢氧化铜悬浊液混合加热,有红色沉淀生成,则证明有醛基
【详解】(1)根据A的结构简式得出A的分子式是C9H10O3,B中的含氧官能团名称是醛基、羧基;
(2)A→B是醇变醛的反应,因此反应类型是氧化反应;A—D中,C、D分子式相同,均为C9H8O2,结构式不同,因此互为同分异构体的是C与D;
(3)D在酸性条件下水解的化学方程式是+H2O;
(4)检验B中醛基的方法为取少量B于试管中,加适量NaOH使溶液为碱性,再与新制氢氧化铜悬浊液混合加热,有红色沉淀生成,则证明有醛基。
20. CH3CH=CH2 加成 CH3CHBrCH2Br+2NaOHCH3CH(OH)CH2OH+2NaBr; 水解(取代) CH3CH(OH)CH2OH+O2CH3COCHO+2H2O 氧化
【分析】用逆推法分析烃A的转化过程,C物质能在浓硫酸存在的条件下发生脱去水分子反应,说明C物质中应含有羟基,C在浓硫酸的作用下发生分子间的消去反应,根据的结构简式,可知C应为。根据B→C的反应条件可知,B为卤代烃,结合烃A→B的过程,可知B的结构简式为:CH3CHBrCH2Br。烃A→B为烃A与Br2发生加成反应生成CH3CHBrCH2Br 的过程,由此可知烃A为CH3CH=CH2。C→E为醇被催化氧化生成醛的过程,C中有一个与羟基直接相连的碳原子上只有一个氢原子。结合醇的催化氧化规律可知E的结构简式。据此分析。
【详解】(1)由分析可知,烃A的结构简式为CH3CH=CH2。答案为:CH3CH=CH2;
(2)反应①为CH3CH=CH2与Br2反应生成CH3CHBrCH2Br,反应类型为加成反应。答案为:加成;
(3)根据反应②的反应条件可知为卤代烃与NaOH水溶液共热发生水解(取代)反应的过程,反应方程式为:CH3CHBrCH2Br+2NaOHCH3CH(OH)CH2OH+2NaBr;反应③为CH3CH(OH)CH2OH被催化氧化生成醛的过程,根据醇被催化氧化的规律可知,CH3CH(OH)CH2OH被催化氧化生成CH3COCHO。反应方程式为:CH3CH(OH)CH2OH+O2CH3COCHO+2H2O,故答案为:CH3CHBrCH2Br+2NaOHCH3CH(OH)CH2OH+2NaBr;水解(取代);CH3CH(OH)CH2OH+O2CH3COCHO+2H2O;氧化。
【点睛】注意C的结构为,存在和,根据醇的催化氧化规律,被氧化为-CHO,被氧化成。
21. CH2O 甲酸甲酯
【分析】将有机物燃烧,其中的C转化为CO2,其中的H转化为H2O,根据高氯酸镁质量增加确定H2O的质量,根据碱石灰增加质量确定CO2的质量,由H2O、CO2的质量计算H、C元素的质量,根据C、H元素的质量和与有机物的质量关系确定其中O元素的质量,根据C、H、O的质量计算它们的最简整数比,得到最简式;然后根据物质含有的官能团及相对分子质量确定物质X的结构简式及物质名称。
【详解】(1)0.300 g样品X完全燃烧,反应产生的气体先通过干燥剂高氯酸镁,高氯酸镁质量增加0.180 g就是水的质量,n(H2O)==0.01 mol;再通过碱石灰,碱石灰质量增加0.440 g为CO2的质量,则n(CO2)==0.01 mol,所以0.300 g样品X中含有O元素的质量是m(O)=0.300 g-0.01 mol×2×1 g/mol-0.01 mol×12 g/mol=0.16 g,则n(O)==0.01 mol,所以n(C):n(H):n(O)=0.01 mol:0.01 mol×2:0.01 mol=1:2:1,故该物质的最简式是CH2O;
(2)物质X的最简式CH2O的式量是30,质谱法测得X的相对分子质量是60,则X的分子式是C2H4O2,若红外光谱测得X中含有“C=O”和“C—O—C”的结构,则X含有酯基,X的结构简式是HCOOCH3,该物质的名称为甲酸甲酯;
(3)若质谱法测得X的相对分子质量是90,说明X分子中含有3个CH2O基团,X的分子式是C3H6O3,两分子X能通过酯化反应形成六元环状结构的有机物Y,则X是2-羟基丙酸,X的结构简式是,2个X通过酯化反应形成六元环状结构的有机物Y结构简式是:。
22.(1) 羟基、醛基、羧基 c
(2)3:2:1
(3)
(4)溶液变紫色
(5) 碳碳双键、酚羟基、苯环上甲基都可以被酸性高锰酸钾溶液氧化 D
(6) 4 7
(7)B
(8)A
(9)含有碳碳不饱和键,容易被空气中氧气氧化
【详解】(1)由图可知,A中含有的官能团名称分别有羟基、醛基、羧基;
①含有苯环,能加成;②酚羟基、醛基、羧基、羟基均不能水解;③含有羧基、羟基,能酯化;④分子中支链上的羟基能被氧化;⑤含有羧基具有酸的通性,能中和;⑥支链上的羟基能消去;⑦支链上的醛基能被还原为羟基;故A可以发生的有c;
(2)钠能和酚羟基、羧基、羟基反应,氢氧化钠能和酚羟基、羧基反应,碳酸氢钠能和羧基反应,故一定量Na、NaOH、NaHCO3分别与等物质的量A充分反应,则消耗Na、NaOH、NaHCO3三种物质的物质的量之比为3:2:1;
(3)A中酚羟基、羧基可与足量Na2CO3反应,反应所得有机产物的结构简式是;
(4)该兴奋剂中含有酚羟基,与FeCl3溶液混合,现象是溶液变紫色;
(5)分子中碳碳双键、酚羟基、苯环上甲基都可以被酸性高锰酸钾溶液氧化,故紫色褪去,并不能证明其结构中含有碳碳双键;
A.酚羟基的邻对位的氢能和溴水发生取代反应,加入浓溴水,溴水褪色,不能说明含有碳碳双键,A不符合题意;
B.先加入足量NaOH溶液,氢氧化钠和溴反应能使溴水褪色,不能说明含有碳碳双键,B不符合题意;
C.苯环上甲基可以被酸性高锰酸钾溶液氧化,溶液褪色,不能说明含有碳碳双键,C不符合题意;
D.先滴加NaOH溶液到刚好反应,酚羟基恰好被反应,再加入溴水,溴水褪色,说明溴和碳碳双键发生反应,D符合题意;
故选D;
(6)酚羟基的邻对位的氢能和溴水发生取代反应,碳碳双键能和溴发生加成反应1mol该物质最多消耗Br2为4mol;苯环、碳碳双键能和溴加成,故1mol该物质最多消耗Br2为7mol;
(7)A.同系物是指结构相似、分子组成相差若干个“CH2”原子团的有机化合物;EPA与DPA互为同系物,A正确;
B.同分异构体是分子式相同、结构不同的化合物;DPA与DHA两者的分子式不同,不互为同分异构体,B错误;
C.由图可知,EPA的分子式为C20H30O2,C正确;
D.DHA的甘油酯是油脂的成分之一,常温下为液态,D正确;
故选B;
(8)A.油脂在碱性条件下的水解为皂化反应,A错误;
B.天然油脂大多为多种高级脂肪酸形成的混甘油酯,B正确;
C.硬脂酸(C17H35COOH)甘油酯为饱和脂肪酸甘油酯,通常沸点较高,C正确;
D.油脂的主要成分是高级脂肪酸的甘油酯,含有酯基,属于酯类,D正确;
故选A;
(9)DHA甘油酯中含有碳碳不饱和键,容易被空气中氧气氧化,故一般做成胶囊状
一、单选题(共14题)
1.下列推理结果正确的是
A.目前芯片用硅基材料,未来可能用碳基材料
B.金属钠在空气中燃烧生成,则金属锂在空气燃烧生成
C.通入溶液中至过量,没有明显现象,则通入溶液中至过量,也没明显现象
D.1乙醛和足量的银氨溶液反应可得2金属银,则1甲醛和足量的银氨溶液反应也可得2银
2.下列除去杂质的方法正确的是
①除去乙烷中少量的乙烯:光照条件下通入Cl2,气液分离;
②除去乙酸乙酯中少量的乙酸:用饱和碳酸钠溶液洗涤,分液;
③除去苯中混有的少量苯酚:加入浓溴水后过滤取滤液;
④除去乙醇中少量的乙酸:加足量生石灰,蒸馏。
⑤除去硝基苯中混有的浓硝酸和浓硫酸,加入NaOH溶液,静置,分液
⑥溴苯中混有溴,加入KI溶液,振荡,再用汽油萃取
A.①②⑥ B.②④⑤ C.③④⑥ D.②③④⑤
3.二羟基甲戊酸是合成青蒿素的原料之一,其结构如图a所示。下列有关二羟基甲戊酸的说法错误的是
A.二嵯基甲戊酸的分子式为
B.与乳酸(结构如图b)互为同系物
C.与乙醇、乙酸均能发生酯化反应,能使酸性溶液褪色
D.等量的二羟基甲戊酸消耗Na和的物质的量之比为3∶1
4.下列过程对应的离子反应方程式书写正确的是
A.乙酰胺与NaOH溶液混合共热:
B.NaHCO3溶液与过量澄清石灰水混合:
C.苯酚钠溶液中通入CO2出现浑浊:2 +CO2+H2O→2 +CO
D.以镁作电极电解MgCl2水溶液:
5.氯霉素是一种广谱抗菌药物,其结构如图所示。下列有关该化合物的说法错误的是
A.化学式为 B.可以发生水解反应
C.可以形成分子内氢键 D.不可以发生消去反应
6.端午节是中国四大传统节日之一,民间习俗有悬钟馗像,挂艾叶菖蒲,吃粽子,饮雄黄酒等。艾蒿中含有桉叶烷、黄酮素,它们的结构如下。下列有关说法正确的是
A.桉叶烷的分子式为C15H26 B.黄酮素含有5种官能团
C.光照条件下,桉叶烷能与氯气发生取代反应 D.黄酮素不能使酸性高锰酸钾溶液褪色
7.紫花前胡醇可从中药材当归和白芷中提取得到,能提高人体免疫力。有关该化合物,下列叙述正确的是
A.分子式为 B.能够发生水解反应
C.不能使溴水溶液褪色 D.紫花前胡醇最多能与发生加成反应
8.中草药黄芩对肿瘤细胞的杀伤有独特作用。下列有关汉黄芩素的叙述正确的是
A.汉黄芩素有4种含氧官能团
B.该物质遇溶液能显色
C.该物质分子式为
D.与足量发生完全加成反应,1该物质最多消耗7
9.下列实验操作正确且能达到预期目的的是
编号 实验目的 操作
A 欲证明 CH2=CHCHO 中含有碳碳双键 滴入酸性 KMnO4 溶液,看紫红色是否褪去
B 欲除去苯中混有的苯酚 向混合液中加入浓溴水,充分反应后,过滤
C 比较铜和镁的金属活动性强弱 用石墨作电极电解等浓度 Mg(NO3)2、Cu(NO3)2 的混合液
D 确定碳和氯两元素非金属性强弱 测同温同浓度 NaHCO3 和 NaClO 水溶液的 pH
A.A B.B C.C D.D
10.下列有关高级脂肪酸甘油酯的说法正确的是
A.高级脂肪酸甘油酯是高分子化合物
B.天然的不饱和高级脂肪酸甘油酯都是简单甘油酯
C.植物油可以使酸性高锰酸钾溶液褪色
D.高级脂肪酸和乙酸互为同系物
11.乙醇催化氧化制取乙醛(沸点为20.8℃,能与水混溶)的装置(夹持装置已略) 如图所示。下列说法错误的是
A.①中用胶管连接其作用是平衡气压,便于液体顺利流下
B.实验过程中铜丝会出现红黑交替变化
C.实验开始时需先加热②,再通O2,然后加热③
D.实验结束时需先将④中的导管移出,再停止加热。
12.下列有关乙酸性质的叙述错误的是
A.乙酸是有强烈刺激性气味的无色液体,易溶于水和乙醇
B.乙酸的沸点比乙醇高
C.乙酸的酸性比碳酸强,它是一元酸,能与碳酸盐反应
D.在发生酯化反应时,乙酸分子羧基中的氢原子跟醇分子中的羟基结合成水
13.下列各组中的反应,属于同一反应类型的是
A.由2-溴丙烷水解制2-丙醇;由丙烯与水反应制1-丙醇
B.由甲苯硝化制对硝基甲苯;由甲苯与酸性高锰酸钾溶液反应制苯甲酸
C.由氯代环己烷制环己烯;由丙烯与溴水反应制1,2-二溴丙烷
D.由苯与液溴反应制溴苯;乙醇在浓硫酸作用下加热至140℃时生成乙醚
14.下列方案设计、现象和结论都正确的是
目的 方案设计 现象和结论
A 检验某无色溶液中是否含有 取少量该溶液于试管中,加稀硝酸酸化,再加入硝酸钡溶液 若有白色沉淀生成,则该溶液中一定含有
B 探究不同金属离于对分解速率的影响 取2支试管,向2支试管中各加入5 mL 6%溶液,分别向试管中各加入溶液和溶液 相同时间内产生气泡多的,则催化效果好
C 判断某有机物是否为醛类 取2mL样品溶液于试管中,加入5~6滴新制氢氧化铜,加热 若产生砖红色沉淀,则该有机物属于醛类
D 检验某无色气体是否为 将气体通入品红溶液中,再加热 若通入气体后品红溶液褪色,加热该褪色溶液能恢复红色,则一定为
A.A B.B C.C D.D
二、填空题(共8题)
15.研究表明,碘海醇是临床中应用广泛一种造影剂,化合物H是合成碘海醇的关键中间体,其合成路线如图:
已知:+
回答下列问题:
设计由CH2=CH2制备的合成路线(无机试剂任选) 。
16.医药阿斯匹林的结构简式如图。试回答:
(1)阿斯匹林可看成酯类物质,口服后在胃肠作用下,阿斯匹林发生水解反应,生成A和B两种产物。其中A的结构简式如图,则阿斯匹林的分子式为: ,B的结构简式为: 。
(2)上述水解产物B与甲醇、浓硫酸共热反应的化学方程式为: 。
(3)甲醇在铜作催化剂时与氧气反应的化学方程式为: 。
17.回答下列问题
(1)现有下列4种重要的有机物:
a.CH3CH2CHO b.CH3CH2CH3 c. d.
①与新制氢氧化铜反应的方程式 。
②能与浓硝酸反应生成TNT的方程式是 。
③滴浓溴水产生白色沉淀的方程式是: 。
④能发生消去反应的化学方程式: 。
(2)在潜水艇和消防员呼吸面具中,Na2O2所发生的化学反应方程式 , 。
(3)氯化亚铁溶液中滴加氢氧化钠溶液,产生白色沉底,最后变成红褐色 , 。
18.已知一个碳原子连两个—OH的结构不稳定,会很快脱去一分子水,其变化如下:
→ + H2O
下图中B和、等都是A和Cl2发生反应生成的产物,E是一种高分子化合物,透光性能好,常用作一些灯饰外壳。过程中一些小分子都已经略去。
(1)A的化学名称为
(2)第④步的化学方程式为 ,该反应类型为 ;
(3)第⑦步的化学方程式为 ,该反应类型为 ;
(4)E的结构简式为 ;
(5)符合下列条件:苯环上有两个取代基且苯环上只有两种不同化学环境的氢的C的同分异构体的结构简式分别是 、 、 。
19.有机物A可以通过不同化学反应分别制得B、C和D三种物质,结构简式如图所示:
(1)A的分子式是 ;B中的含氧官能团名称是 。
(2)A→B的反应类型是 ;A~D中互为同分异构体的是 (填代号)。
(3)D在酸性条件下水解的化学方程式是 。
(4)检验B中醛基的方法 。
20.烃A可以发生下列过程所示的变化:
(1)烃A的结构简式是 ;
(2)反应①属 反应;
(3)反应②的化学方程式是 ,属 反应;反应③的化学方程式是 ,属 反应。
21.某实验兴趣小组用李比希法、现代仪器等测定有机物X的组成和结构。实验测得0.300 g样品X完全燃烧,产物气体先通过干燥剂高氯酸镁,高氯酸镁质量增加0.180 g,再通过碱石灰,碱石灰质量增加0.440 g。
(1)由实验数据分析计算可得X的实验式(最简式)为 。
(2)若红外光谱测得X中含有“C=O”和“C—O—C”的结构,质谱法测得X的相对分子质量是60,则X的名称为 。
(3)若质谱法测得X的相对分子质量是90,两分子X能通过酯化反应形成六元环状结构的有机物Y,Y的结构简式为 。
22.有机物的性质与其所具有的官能团直接相关,辨析有机物的官能团,运用官能团的性质分析、理解有机物发生的反应是掌握有机物的金钥匙。某有机化合物A的结构简式为,回答下列问题:
(1)A中含有的官能团名称分别有 ,下列反应中①加成;②水解;③酯化;④氧化;⑤中和;⑥消去;⑦还原,其中A可以发生的有 填字母序号)
a.①②③④⑤⑥⑦ b.①③④⑤⑦ c.①③④⑤⑥⑦ d.②③④⑤⑥
(2)取一定量Na、NaOH、NaHCO3分别与等物质的量A充分反应,则消耗Na、NaOH、NaHCO3三种物质的物质的量之比为
(3)A与足量Na2CO3反应所得有机产物的结构简式是 。
某种兴奋剂的结构简式如图所示,回答下列问题:
。
(4)该兴奋剂与FeCl3溶液混合,现象是 。
(5)滴入KMnO4酸性溶液,振荡,紫色褪去,并不能证明其结构中含有碳碳双键,理由是 ,下列证明其结构中含有碳碳双键的方法中,合理且简单易行的是 。
A.加入浓溴水,溴水褪色
B.先加入足量NaOH溶液再加入浓溴水,溴水褪色
C.先加入足量NaOH溶液再加入酸性KMnO4溶液,溶液褪色
D.先滴加NaOH溶液到刚好反应,再加入溴水,溴水褪色
(6)1mol该物质分别与浓溴水和H2反应时,最多消耗Br2和H2的物质的量分别为 mol和 mol。
EPA(二十碳五烯酸)、DPA(二十二碳五烯酸)、DHA(二十二碳六烯酸,常称脑黄金)是不饱和程度大的长链脂肪酸(即高级脂肪酸),属于ω-3不饱和脂肪酸,是人体大脑发育、成长的重要物质,结构简式如下图。它们与甘油形成的酯是油脂的成分之一:
回答下列问题:
(7)关于EPA、DPA、DHA的下列说法中,错误的是_______。
A.EPA与DPA互为同系物 B.DPA与DHA互为同分异构体
C.EPA的分子式为C20H30O2 D.DHA的甘油酯常温下为液态
(8)油脂在人体新陈代谢中发挥着重要的作用。有关油脂的说法错误的是_______。
A.油脂的水解叫皂化反应
B.天然油脂大多为混甘油酯
C.硬脂酸(C17H35COOH)甘油酯沸点可能比DPA甘油酯高
D.油脂的主要成分是高级脂肪酸的甘油酯,属于酯类
(9)“深海鱼油”含较丰富的DHA甘油酯,请结合结构解释“深海鱼油”为什么一般做成胶囊状 。
试卷第1页,共3页
参考答案:
1.A
【详解】A.目前芯片都是使用硅基半导体材料制造的,被称为硅基芯片,未来碳基芯片将成为芯片发展的主流,故A正确;
B.Na的金属性强于Li,金属钠在空气中燃烧生成,金属锂在空气燃烧生成,故B错误;
C.硝酸的酸性比碳酸强,则通入溶液中至过量,没有明显现象,但通入溶液中至过量,由于硝酸根在酸性条件下具有强的氧化性,二氧化硫被氧化成硫酸根,硫酸根与钡离子生成硫酸钡白色沉淀,故C错误;
D.1乙醛分子中含有1mol醛基,与足量的银氨溶液反应可得2金属银,而1mol甲醛分子中可以看成有2mol醛基,则与足量的银氨溶液反应可得4银,故D错误;
答案选A。
2.B
【详解】①光照条件下通入Cl2 ,氯气会和乙烷之间发生取代反应,和乙烯之间发生加成反应,虽然将杂质除去,但是将要留的物质反应了,不符合除杂的原则,故①错误;
②饱和碳酸钠溶液可以和乙酸之间发生中和反应,但是和乙酸乙酯是互不相溶的,分液即可实现分离,故②正确;
③溴易溶于苯,用溴水除杂会引入新的杂质,则除去苯中的少量苯酚,向混合物中加入NaOH溶液后分液,故③错误;
④乙酸与生石灰反应,而乙醇不能,且乙醇易挥发,而乙酸钙为离子型化合物,沸点高,故除去乙醇中少量的乙酸可以加足量生石灰后蒸馏,故④正确;
⑤硝基苯中混有浓硝酸和浓硫酸,加入NaOH溶液,浓硝酸和浓硫酸都可与NaOH反应,而硝基苯不反应且不溶于水,所以可用NaOH溶液除杂,故⑤正确;
⑥溴苯中混有溴,加入KI溶液,Br2能与KI溶液反应生成I2单质,I2与溴苯互溶,不能分离,再加入汽油,I2单质与溴苯汽油互溶,无法用汽油萃取,故⑥错误;
综上所述②④⑤正确,故选B。
3.B
【详解】A.根据结构简式可知,二甲戊酸的分子式为C6H12O4,A正确;
B.两者结构不相似,故不为同系物,B错误;
C.由图a可知,二羟基甲戊酸含有两个羟基和1个羧基,羟基能与乙酸发生酯化反应,其中-CH2OH中的羟基能使酸性高锰酸钾溶液褪色,羧基能与乙醇发生酯化反应,C正确;
D.羟基羧基均能与钠反应,与碳酸氢钠反应的只能是羧基,等量的二羟基甲戊酸消耗Na和的物质的量之比为3∶1,D正确;
答案选B。
4.A
【详解】A.乙酰胺与NaOH溶液混合共热发生水解反应生成乙酸钠和氨气,反应的离子方程式是,故A正确;
B.NaHCO3溶液与过量澄清石灰水混合,生成氢氧化钠、碳酸钙、水,反应的离子方程式是,故B错误;
C.苯酚钠溶液中通入CO2生成碳酸氢钠、苯酚,反应的离子方程式是 +CO2+H2O→ +HCO,故C错误;
D.以镁作电极电解MgCl2水溶液,阳极镁失电子生成镁离子,阴极氢离子得电子生成氢气,电解方程式为,故D错误;
选A。
5.D
【详解】A.由结构简式可知氯霉素的化学式为,故A正确;
B.酰胺基、氯原子的存在使氯霉素可以发生水解反应,故B正确;
C.羟基上的H原子和另一个羟基上的氧原子、亚氨基的N形成分子内氢键,氮原子上的H可以和羟基山的氧形成分子间氢键,故C正确;
D.羟基相连C原子邻位的C原子上连有H原子,则该化合物可发生消去反应,故D错误;
故选:D。
6.C
【详解】A.根据桉叶烷的结构简式可知其分子式为C15H28,A错误;
B.根据黄酮素的结构简式可知,含有羟基,醚键,羰基,碳碳双键,4种官能团,B错误;
C.桉叶烷中碳原子上的氢原子光照条件下,可以和氯气发生取代反应,C正确;
D.黄酮素结构中含有碳碳双键和羟基,都可以被酸性高锰酸钾氧化,使其褪色,D错误;
故选C。
7.B
【详解】A.根据紫花前胡醇的结构简式可知,其分子式为,A项错误;
B.分子中含有酯基,能够发生水解反应,B项正确;
C.分子中含有碳碳双键,使溴水溶液褪色,C项错误;
D.分子中含有1个苯环和1个碳碳双键,故紫花前胡醇最多能与4mol发生加成反应,D项错误;
答案选B。
8.B
【详解】A.汉黄芩素有羟基、醚键、羰基3种含氧官能团,故A错误;
B.汉黄芩素有酚羟基,所以遇溶液能显色,故B正确;
C.根据汉黄芩素的结构简式,可知分子式为,故C错误;
D.苯环、碳碳双键、羰基都能与氢气发生加成反应,与足量发生完全加成反应,1该物质最多消耗8,故D错误;
选B。
9.C
【详解】A.碳碳双键和醛基都能被高锰酸钾氧化,不能用酸性高锰酸钾鉴别,A错误;
B.苯酚与浓溴水反应产生的三溴苯酚白色物质能够溶解在有机物苯中,不能通过过滤除去,B错误;
C.用石墨作电极电解混合溶液,阴极上铜离子放电,可以比较铜和镁的金属活动性强弱,C正确;
D.元素的非金属性越强,其最高价氧化物对应的水化物的酸性就越强。C的最高价含氧酸为H2CO3,对应的钠盐为NaHCO3,Cl的最高价含氧酸为HClO4,对应的钠盐为NaClO4,所以通过测同温同浓度 NaHCO3 和 NaClO 水溶液的 pH,无法确定C和Cl的非金属性强弱,D错误;
故答案为:C。
10.C
【详解】A.高分子化合物的相对分子质量一般为几万到几十万,高级脂肪酸甘油酯不是高分子化合物,A错;
B.天然的不饱和高级脂肪酸甘油酯一般为混合甘油酯,B错;
C.植物油中烃基部分含有不饱和键,所以可以使酸性高锰酸钾溶液褪色,C正确;
D.高级脂肪酸包括硬脂酸、软脂酸、油酸等,油酸分子中含有碳碳双键,不是乙酸的同系物,D错;
答案选C。
11.C
【详解】A.装置中若关闭K时向烧瓶中加入液体,会使烧瓶中压强增大,双氧水不能顺利流下,①中用胶管连接,打开K时,可以平衡气压,便于液体顺利流下,A选项正确;
B.实验中Cu作催化剂,但在过渡反应中,红色的Cu会被氧化成黑色的CuO,CuO又会被还原为红色的Cu,故会出现红黑交替的现象,B选项正确;
C.实验开始时应该先加热③,防止乙醇通入③时冷凝,C选项错误;
D.为防止倒吸,实验结束时需先将④中的导管移出,再停止加热,D选项正确;
答案选C。
12.D
【详解】乙酸是有强烈刺激性气味的无色液体,易溶于水和乙醇,沸点高于乙醇,含有一个羧基属于一元酸,酸性强于碳酸,能和碳酸盐反应,发生酯化反应时乙酸分子脱羟基,故选D。
13.D
【详解】A.由2-溴丙烷水解制2-丙醇是取代反应;由丙烯与水反应制1-丙醇是加成反应,A不符合题意;
B.由甲苯硝化制对硝基甲苯是取代反应;由甲苯与酸性高锰酸钾溶液反应制苯甲酸是氧化反应,B不符合题意;
C.由氯代环己烷制环己烯是消去反应;由丙烯与溴水反应制1,2-二溴丙烷是加成反应,C不符合题意;
D.由苯与液溴反应制溴苯是取代反应;乙醇在浓硫酸作用下加热至140℃时生成乙醚是取代反应,D符合题意;
故选D。
14.D
【详解】A.检验应用盐酸酸化,再加氯化钡溶液检验,故A错误;
B.探究不同金属离于对分解速率的影响应选用相同阴离子的金属盐,该方案中盐中的阴离子不同,无法排除阴离子的干扰,故B错误;
C.与氢氧化铜加热产生砖红色沉淀的可能是醛类,也可能是甲酸类物质,故C错误;
D.二氧化硫能使品红褪色,且加热能恢复,因此可用品红检验二氧化硫,故D正确;
故选:D。
15.CH2=CH2BrCH2CH2Br
【详解】利用题中信息,由CH2=CH2与溴发生加成反应生成1,2-二溴乙烷,1,2-二溴乙烷在氢氧化钠的水溶液中加热发生水解反应生成乙二醇,乙二醇被酸性高锰酸钾氧化生成乙二酸,乙二酸与SOCl2发生取代反应生成,故合成路线流程图为:CH2=CH2BrCH2CH2Br
故答案为:CH2=CH2BrCH2CH2Br。
16. C9H8O4 CH3COOH CH3COOH+CH3OHCH3COOCH3+H2O 2CH3OH+O22HCHO+2H2O
【分析】(1)由结构可知分子式,由图可知生成A为邻羟基苯甲酸,根据酯水解规律可知B为CH3COOH;
(2)乙酸与甲醇在浓硫酸存在条件下发生酯化反应生成乙酸甲酯;
(3)甲醇在铜作催化剂时与氧气反应生成HCHO。
【详解】(1)由结构可知阿斯匹林的分子式为C9H8O4,其中酯基-COOC-可发生水解反应生成A和B,生成A为邻羟基苯甲酸,则B为CH3COOH;
(2)阿司匹林水解产生A是邻羟基苯甲酸,B是乙酸,乙酸与甲醇、浓硫酸共热反应的化学方程式为CH3COOH+CH3OHCH3COOCH3+H2O;
(3)甲醇分子中羟基连接的C原子上有2个H原子,在铜作催化剂时与氧气发生氧化反应,产生甲醛和水,反应的化学方程式为2CH3OH+O22HCHO+2H2O。
【点睛】本题考查有机物的结构与性质,把握有机物的结构、官能团及性质为解答的关键,注意酯、羧酸、醇的性质和转化关系,侧重考查学生的分析与应用能力。
17.(1) CH3CH2CHO 2Cu(OH)2 CH3CH2COOH + Cu2O↓+ 2H2O +3HNO3+3H2O +3Br2↓+3HBr CH3CHClCH3+NaOHCH3CH=CH2↑+NaCl+H2O
(2) 2Na2O2+2CO2=2Na2CO3+O2↑ 2Na2O2+2H2O=4NaOH+O2↑
(3) FeCl2+2NaOH= Fe(OH)2+2NaCl 4Fe(OH)2+O2+2H2O= 4Fe(OH)3
【详解】(1)①醛类物质与新制氢氧化铜反应,相应的方程式应为a与新制氢氧化铜反应:CH3CH2CHO+ 2Cu(OH)2 CH3CH2COOH + Cu2O↓+ 2H2O。
②d能与浓硝酸反应生成TNT(三硝基甲苯)的方程式是:+3HNO3+3H2O。
③c与浓溴水反应产生白色沉淀(2,4,6-三溴苯酚)和氢溴酸,方程式是:+3Br2↓+3HBr。
④b能与氢氧化钠的乙醇溶液发生消去反应,化学方程式:CH3CHClCH3+NaOHCH3CH=CH2↑+NaCl+H2O。
(2)呼吸生成二氧化碳,则Na2O2所发生的化学反应方程式包括:2Na2O2+2CO2=2Na2CO3+O2↑;2Na2O2+2H2O=4NaOH+O2↑。
(3)氯化亚铁溶液中滴加氢氧化钠溶液,产生白色沉底(Fe(OH)2),Fe(OH)2氧化最后变成红褐色(Fe(OH)3),方程式包括FeCl2+2NaOH= Fe(OH)2+2NaCl; 4Fe(OH)2+O2+2H2O= 4Fe(OH)3。
18. 乙苯 氧化反应 加成反应
【详解】(1)A和氯气发生取代反应生成,所以A是乙苯,结构简式为。
(2)是卤代烃,可以发生水解反应,所以C的结构简式为。C中含有羟基,能发生催化氧化,方程式为:。
(3)C中含有羟基,也能发生消去反应,生成D,所以D的结构简式为。D中含有碳碳双键,能发生加成反应,方程式为:。
(4)D中含有碳碳双键,能发生加聚反应,生成高分子化合物E,所以E的结构简式为:。
(5)苯环上有两个取代基且苯环上只有两种不同化学环境的氢,说明两个取代基是对位的,所以根据C的分子式可知,如果取代基其中之一是乙基,则对位就是酚羟基;如果是甲基,则对位就是-CH2OH或-OCH3,所以可能的结构简式为。
19. C9H10O3 醛基、羧基 氧化反应 C和D +H2O 取少量B于试管中,加适量NaOH使溶液为碱性,再与新制氢氧化铜悬浊液混合加热,有红色沉淀生成,则证明有醛基
【详解】(1)根据A的结构简式得出A的分子式是C9H10O3,B中的含氧官能团名称是醛基、羧基;
(2)A→B是醇变醛的反应,因此反应类型是氧化反应;A—D中,C、D分子式相同,均为C9H8O2,结构式不同,因此互为同分异构体的是C与D;
(3)D在酸性条件下水解的化学方程式是+H2O;
(4)检验B中醛基的方法为取少量B于试管中,加适量NaOH使溶液为碱性,再与新制氢氧化铜悬浊液混合加热,有红色沉淀生成,则证明有醛基。
20. CH3CH=CH2 加成 CH3CHBrCH2Br+2NaOHCH3CH(OH)CH2OH+2NaBr; 水解(取代) CH3CH(OH)CH2OH+O2CH3COCHO+2H2O 氧化
【分析】用逆推法分析烃A的转化过程,C物质能在浓硫酸存在的条件下发生脱去水分子反应,说明C物质中应含有羟基,C在浓硫酸的作用下发生分子间的消去反应,根据的结构简式,可知C应为。根据B→C的反应条件可知,B为卤代烃,结合烃A→B的过程,可知B的结构简式为:CH3CHBrCH2Br。烃A→B为烃A与Br2发生加成反应生成CH3CHBrCH2Br 的过程,由此可知烃A为CH3CH=CH2。C→E为醇被催化氧化生成醛的过程,C中有一个与羟基直接相连的碳原子上只有一个氢原子。结合醇的催化氧化规律可知E的结构简式。据此分析。
【详解】(1)由分析可知,烃A的结构简式为CH3CH=CH2。答案为:CH3CH=CH2;
(2)反应①为CH3CH=CH2与Br2反应生成CH3CHBrCH2Br,反应类型为加成反应。答案为:加成;
(3)根据反应②的反应条件可知为卤代烃与NaOH水溶液共热发生水解(取代)反应的过程,反应方程式为:CH3CHBrCH2Br+2NaOHCH3CH(OH)CH2OH+2NaBr;反应③为CH3CH(OH)CH2OH被催化氧化生成醛的过程,根据醇被催化氧化的规律可知,CH3CH(OH)CH2OH被催化氧化生成CH3COCHO。反应方程式为:CH3CH(OH)CH2OH+O2CH3COCHO+2H2O,故答案为:CH3CHBrCH2Br+2NaOHCH3CH(OH)CH2OH+2NaBr;水解(取代);CH3CH(OH)CH2OH+O2CH3COCHO+2H2O;氧化。
【点睛】注意C的结构为,存在和,根据醇的催化氧化规律,被氧化为-CHO,被氧化成。
21. CH2O 甲酸甲酯
【分析】将有机物燃烧,其中的C转化为CO2,其中的H转化为H2O,根据高氯酸镁质量增加确定H2O的质量,根据碱石灰增加质量确定CO2的质量,由H2O、CO2的质量计算H、C元素的质量,根据C、H元素的质量和与有机物的质量关系确定其中O元素的质量,根据C、H、O的质量计算它们的最简整数比,得到最简式;然后根据物质含有的官能团及相对分子质量确定物质X的结构简式及物质名称。
【详解】(1)0.300 g样品X完全燃烧,反应产生的气体先通过干燥剂高氯酸镁,高氯酸镁质量增加0.180 g就是水的质量,n(H2O)==0.01 mol;再通过碱石灰,碱石灰质量增加0.440 g为CO2的质量,则n(CO2)==0.01 mol,所以0.300 g样品X中含有O元素的质量是m(O)=0.300 g-0.01 mol×2×1 g/mol-0.01 mol×12 g/mol=0.16 g,则n(O)==0.01 mol,所以n(C):n(H):n(O)=0.01 mol:0.01 mol×2:0.01 mol=1:2:1,故该物质的最简式是CH2O;
(2)物质X的最简式CH2O的式量是30,质谱法测得X的相对分子质量是60,则X的分子式是C2H4O2,若红外光谱测得X中含有“C=O”和“C—O—C”的结构,则X含有酯基,X的结构简式是HCOOCH3,该物质的名称为甲酸甲酯;
(3)若质谱法测得X的相对分子质量是90,说明X分子中含有3个CH2O基团,X的分子式是C3H6O3,两分子X能通过酯化反应形成六元环状结构的有机物Y,则X是2-羟基丙酸,X的结构简式是,2个X通过酯化反应形成六元环状结构的有机物Y结构简式是:。
22.(1) 羟基、醛基、羧基 c
(2)3:2:1
(3)
(4)溶液变紫色
(5) 碳碳双键、酚羟基、苯环上甲基都可以被酸性高锰酸钾溶液氧化 D
(6) 4 7
(7)B
(8)A
(9)含有碳碳不饱和键,容易被空气中氧气氧化
【详解】(1)由图可知,A中含有的官能团名称分别有羟基、醛基、羧基;
①含有苯环,能加成;②酚羟基、醛基、羧基、羟基均不能水解;③含有羧基、羟基,能酯化;④分子中支链上的羟基能被氧化;⑤含有羧基具有酸的通性,能中和;⑥支链上的羟基能消去;⑦支链上的醛基能被还原为羟基;故A可以发生的有c;
(2)钠能和酚羟基、羧基、羟基反应,氢氧化钠能和酚羟基、羧基反应,碳酸氢钠能和羧基反应,故一定量Na、NaOH、NaHCO3分别与等物质的量A充分反应,则消耗Na、NaOH、NaHCO3三种物质的物质的量之比为3:2:1;
(3)A中酚羟基、羧基可与足量Na2CO3反应,反应所得有机产物的结构简式是;
(4)该兴奋剂中含有酚羟基,与FeCl3溶液混合,现象是溶液变紫色;
(5)分子中碳碳双键、酚羟基、苯环上甲基都可以被酸性高锰酸钾溶液氧化,故紫色褪去,并不能证明其结构中含有碳碳双键;
A.酚羟基的邻对位的氢能和溴水发生取代反应,加入浓溴水,溴水褪色,不能说明含有碳碳双键,A不符合题意;
B.先加入足量NaOH溶液,氢氧化钠和溴反应能使溴水褪色,不能说明含有碳碳双键,B不符合题意;
C.苯环上甲基可以被酸性高锰酸钾溶液氧化,溶液褪色,不能说明含有碳碳双键,C不符合题意;
D.先滴加NaOH溶液到刚好反应,酚羟基恰好被反应,再加入溴水,溴水褪色,说明溴和碳碳双键发生反应,D符合题意;
故选D;
(6)酚羟基的邻对位的氢能和溴水发生取代反应,碳碳双键能和溴发生加成反应1mol该物质最多消耗Br2为4mol;苯环、碳碳双键能和溴加成,故1mol该物质最多消耗Br2为7mol;
(7)A.同系物是指结构相似、分子组成相差若干个“CH2”原子团的有机化合物;EPA与DPA互为同系物,A正确;
B.同分异构体是分子式相同、结构不同的化合物;DPA与DHA两者的分子式不同,不互为同分异构体,B错误;
C.由图可知,EPA的分子式为C20H30O2,C正确;
D.DHA的甘油酯是油脂的成分之一,常温下为液态,D正确;
故选B;
(8)A.油脂在碱性条件下的水解为皂化反应,A错误;
B.天然油脂大多为多种高级脂肪酸形成的混甘油酯,B正确;
C.硬脂酸(C17H35COOH)甘油酯为饱和脂肪酸甘油酯,通常沸点较高,C正确;
D.油脂的主要成分是高级脂肪酸的甘油酯,含有酯基,属于酯类,D正确;
故选A;
(9)DHA甘油酯中含有碳碳不饱和键,容易被空气中氧气氧化,故一般做成胶囊状
