1.1.1反应热焓变 同步练习 (含答案)2023-2024学年高二上学期化学人教版(2019)选择性必修1
文档属性
| 名称 | 1.1.1反应热焓变 同步练习 (含答案)2023-2024学年高二上学期化学人教版(2019)选择性必修1 |

|
|
| 格式 | docx | ||
| 文件大小 | 503.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-12-10 00:00:00 | ||
图片预览

文档简介
1.1.1反应热 焓变
一、单选题
1.下列关于能量变化的说法正确的是
A.化学反应遵循质量守恒的同时,也遵循能量守恒
B.已知C(石墨,s) = C(金刚石,s) △H>0,则金刚石比石墨稳定
C.古文说 “冰,水为之,而寒于水” 说明等量的水和冰相比,冰的能量更高
D.化学反应在物质变化的同时,伴随着能量变化,其表现形式只有吸热和放热两种
2.下列说法中正确的是
A.化学反应中的能量变化都是以热量形式体现的
B.化学键的断裂一定会伴随着化学变化
C.加入催化剂可以改变化学反应的反应热
D.原电池原理的本质是发生氧化还原反应
3.下列有关热化学方程式的叙述中,正确的是( )
A.含20.0gNaOH的稀溶液与足量的稀硫酸完全中和,放出28.7kJ的热量,则表示中和热的热化学方程式为2NaOH(aq)+H2SO4(aq)=Na2SO4(aq)+2H2O(l) △H=-114.8kJ·mol-1
B.已知热化学方程式:SO2(g)+O2(g)SO3(g) △H=-98.32kJ·mol-1,在容器中充入2molSO2和1molO2充分反应,最终放出的热量为196.64kJ
C.已知2H2(g)+O2(g)=2H2O(g) △H=-483.6kJ·mol-1,则H2的燃烧热为241.8kJ·mol-1
D.已知石墨转化为金刚石为吸热,那么石墨比金刚石稳定
4.最新报道:科学家首次用X射线激光技术观察到CO与O在催化剂表面形成化学键的过程。反应过程的示意图如下:
下列说法正确的是
A.状态I→状态Ⅲ表示CO与O2反应生成CO2的过程
B.CO和O生成CO2是吸热反应
C.状态I→状态Ⅲ表示CO与O反应生成CO2的过程
D.在该过程中,CO断键形成C和O
5.某同学设计如图所示实验,探究化学反应中的能量变化
下列判断正确的是
A.由实验可知,Ⅰ、Ⅱ、Ⅲ所涉及的反应都是放热反应
B.将实验Ⅰ中的镁片更换为等质量的镁粉后释放出的热量增多
C.实验Ⅲ中将玻璃搅拌器改为铜质搅拌器对实验结果没有影响
D.实验Ⅲ中若用浓硫酸测定中和反应的反应热,则测定的ΔH偏低
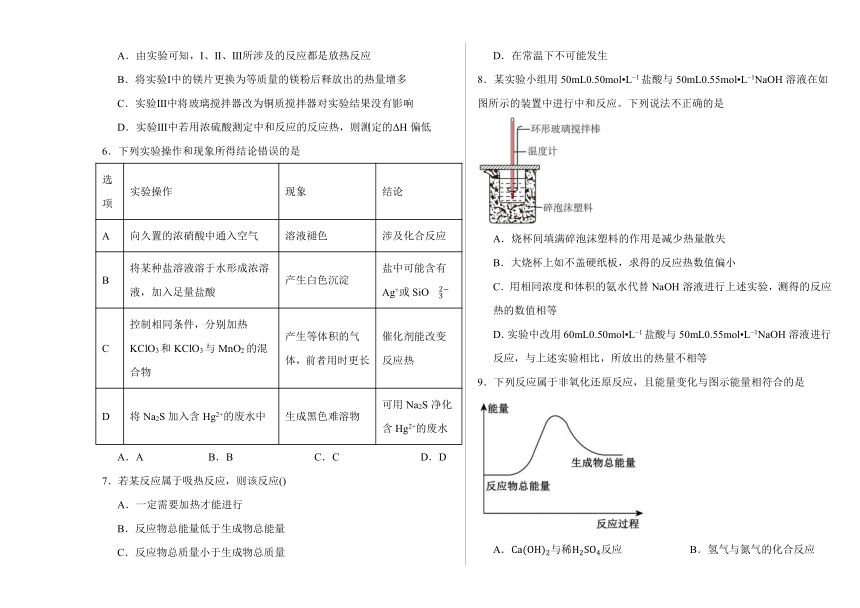
6.下列实验操作和现象所得结论错误的是
选项 实验操作 现象 结论
A 向久置的浓硝酸中通入空气 溶液褪色 涉及化合反应
B 将某种盐溶液溶于水形成浓溶液,加入足量盐酸 产生白色沉淀 盐中可能含有Ag+或SiO
C 控制相同条件,分别加热KClO3和KClO3与MnO2的混合物 产生等体积的气体,前者用时更长 催化剂能改变反应热
D 将Na2S加入含Hg2+的废水中 生成黑色难溶物 可用Na2S净化含Hg2+的废水
A.A B.B C.C D.D
7.若某反应属于吸热反应,则该反应()
A.一定需要加热才能进行
B.反应物总能量低于生成物总能量
C.反应物总质量小于生成物总质量
D.在常温下不可能发生
8.某实验小组用50mL0.50mol L 1盐酸与50mL0.55mol L 1NaOH溶液在如图所示的装置中进行中和反应。下列说法不正确的是
A.烧杯间填满碎泡沫塑料的作用是减少热量散失
B.大烧杯上如不盖硬纸板,求得的反应热数值偏小
C.用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的反应热的数值相等
D.实验中改用60mL0.50mol L 1盐酸与50mL0.55mol L 1NaOH溶液进行反应,与上述实验相比,所放出的热量不相等
9.下列反应属于非氧化还原反应,且能量变化与图示能量相符合的是
A.与稀反应 B.氢气与氮气的化合反应
C.灼热的炭与反应 D.晶体与晶体反应
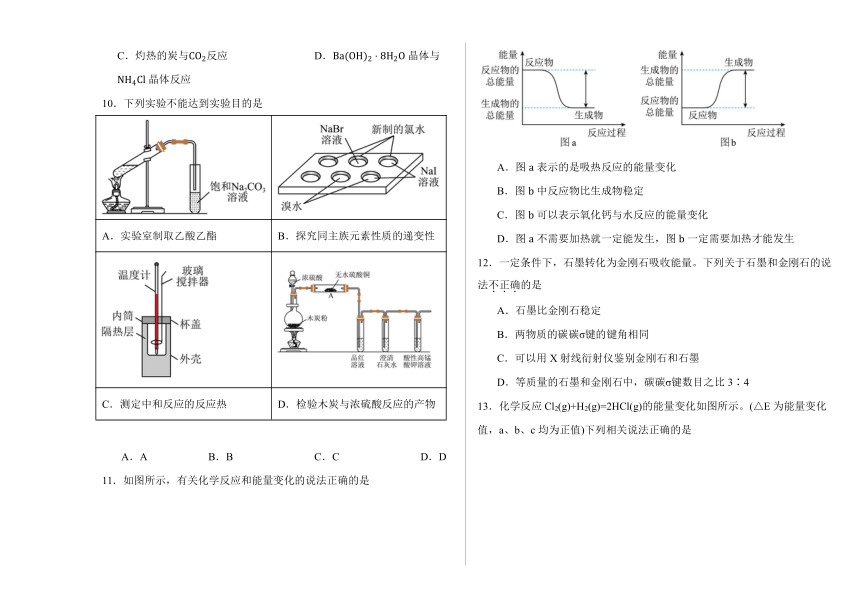
10.下列实验不能达到实验目的是
A.实验室制取乙酸乙酯 B.探究同主族元素性质的递变性
C.测定中和反应的反应热 D.检验木炭与浓硫酸反应的产物
A.A B.B C.C D.D
11.如图所示,有关化学反应和能量变化的说法正确的是
A.图表示的是吸热反应的能量变化
B.图中反应物比生成物稳定
C.图可以表示氧化钙与水反应的能量变化
D.图不需要加热就一定能发生,图一定需要加热才能发生
12.一定条件下,石墨转化为金刚石吸收能量。下列关于石墨和金刚石的说法不正确的是
A.石墨比金刚石稳定
B.两物质的碳碳σ键的键角相同
C.可以用X射线衍射仪鉴别金刚石和石墨
D.等质量的石墨和金刚石中,碳碳σ键数目之比3∶4
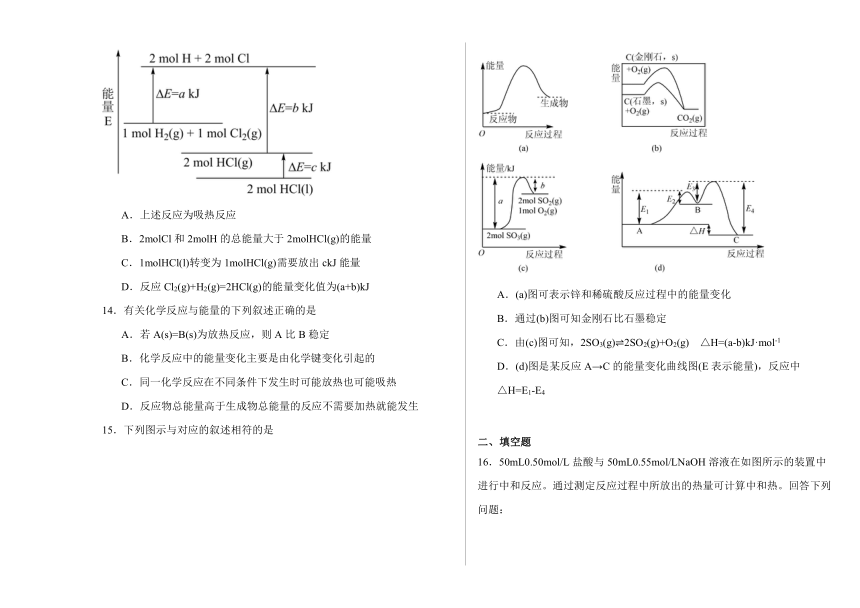
13.化学反应Cl2(g)+H2(g)=2HCl(g)的能量变化如图所示。(△E为能量变化值,a、b、c均为正值)下列相关说法正确的是
A.上述反应为吸热反应
B.2molCl和2molH的总能量大于2molHCl(g)的能量
C.1molHCl(l)转变为1molHCl(g)需要放出ckJ能量
D.反应Cl2(g)+H2(g)=2HCl(g)的能量变化值为(a+b)kJ
14.有关化学反应与能量的下列叙述正确的是
A.若A(s)=B(s)为放热反应,则A比B稳定
B.化学反应中的能量变化主要是由化学键变化引起的
C.同一化学反应在不同条件下发生时可能放热也可能吸热
D.反应物总能量高于生成物总能量的反应不需要加热就能发生
15.下列图示与对应的叙述相符的是
A.(a)图可表示锌和稀硫酸反应过程中的能量变化
B.通过(b)图可知金刚石比石墨稳定
C.由(c)图可知,2SO3(g)2SO2(g)+O2(g) △H=(a-b)kJ·mol-1
D.(d)图是某反应A→C的能量变化曲线图(E表示能量),反应中△H=E1-E4
二、填空题
16.50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
(1)从实验装置看,图中尚缺少的一种玻璃仪器是 。
(2)烧杯间填满碎纸条的作用是 。
(3)实验中改用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比较,所放出的热量 (填“相等”或“不相等”),中和热 (填“相等”或“不相等”),理由是 。
(4)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得中和热的数值与57.3kJ/mol相比较会 。(填“偏大”、“偏小”或“无影响”)。
(5)完整地做一次这样的实验,需测定 次温度。
(6)大烧杯上如不盖硬纸板,求得的中和热数值 (填“偏大”、“偏小”或“无影响”
17.氨在国民经济中占有重要地位。合成氨工业中,合成塔中每产生2mol NH3,放出92.2kJ热量。
(1)工业合成氨的热化学方程式是: 。
(2)已知:
1mol N-H键断裂吸收的能量约等于 kJ。
18.等质量的碳酸钠、碳酸氢钠粉末分别与足量的盐酸发生反应时,产生CO2较多的是 (填化学式)。实验过程中,同学们感受到碳酸钠与盐酸的反应是放热反应,而碳酸氢钠与盐酸的反应是吸热反应,下图中代表碳酸钠与盐酸反应的是 (填字母)。
19.Ⅰ.燃料电池电动汽车是利用氢气、甲醇、天然气(主要成分为甲烷)、汽油等燃料和空气中的氧在催化剂的作用下在燃料电池中经电化学反应产生的电能,并作为主要动力源驱动的汽车。
(1)汽车行驶的过程中,能量的转化形式为 。
Ⅱ.利用下表数据回答下列问题:
燃料 燃烧热/(kJ·mol-1) 燃料 燃烧热/(kJ·mol-1)
氢气 285.8 甲醇(CH3OH) 726.51
甲烷(CH4) 890.3 正丁烷(CH3CH2CH2CH3) 2878.0
乙烷(C2H6) 1559.8 2869.6
丙烷(C3H8) 2219.9
(2)表示乙烷燃烧热的热化学方程式为 。
(3)稳定性:正丁烷 异丁烷(填“>”“<”或“=”);原因 。
(4)相同质量的燃料, (填“C”或“H”)的质量分数越大,燃烧放出的热量越多。
(5)二氧化碳是重要的温室气体,从环保角度分析,放出相同的热量时选择 (填“乙烷”或“甲醇”)作为燃料产生的CO2较少。
(6)现有氢气和丙烷混合气体3 mol,完全燃烧共产生2791.5 kJ的热量,则氢气和丙烷的物质的量之比为 。
20.在寒冷的冬季,我们可以通过取暖器、电热炉,暖宝宝等来取暖。请查阅资料,设计一个通过化学反应产生热量的暖手袋的制作方案 。
三、实验题
21.I.中和热测定:
(1)中和热测定的实验中,用到的玻璃仪器有烧杯、温度计、 、 。
(2)量取反应物时,取50 mL 0.50 mol·Lˉ1的盐酸,还需加入的试剂是 (填序号)。
a.50 mL 0.50 mol·Lˉ1NaOH溶液
b.50 mL 0.55 mol·Lˉ1NaOH溶液
c.1.0 g NaOH固体
II.现用中和滴定测定某盐酸的浓度,有关数据记录如下:
滴定序号 待测液体积(mL) 所消耗烧碱标准液的体积(mL)
滴定前 滴定后 消耗的体积
1 25.00 0.50 25.12 24.62
2 25.00 / / /
3 25.00 5.00 29.58 24.58
(3)应用 式滴定管盛装0.2500 mol/L烧碱标准液,锥形瓶中装有25.00mL待测盐酸溶液。
(4)如图表示第二次滴定时50 mL滴定管中前后液面的位置。该次滴定所用标准烧碱溶液体积为 mL。
(5)根据所给数据,计算出该盐酸的物质的量浓度(注意保留合适的有效数字),c (HCl) = 。
(6)读数时,若滴定前仰视,滴定后俯视,则会使最终测定结果 (填“无影响”、“偏高”、“偏低”。下同);若装标准液的滴定管在装液前未用标准NaOH溶液润洗,会使最终测定结果 。
参考答案:
1.A2.D3.D4.C5.D6.C7.B8.C9.D10.D11.B12.B13.B14.B15.C
16. 环形玻璃搅拌棒 减少实验过程中热量损失 不相等 相等 因为中和热是指在稀溶液中,酸跟碱发生中和反应生成1molH2O所放出的能量,与酸碱用量无关 偏小 3 偏小
17.(1)
(2)391
18. NaHCO3 a
19.(1)化学能转化为电能,电能转化为动能
(2)C2H6(g)+O2(g)=2CO2(g)+3H2O(l) ΔH=-1559.8 kJ·mol-1
(3) < 由表格中的数据可知,异丁烷的燃烧热比正丁烷的燃烧热小,则异丁烷的能量低,即稳定性:正丁烷<异丁烷
(4)H
(5)乙烷
(6)2∶1
20.原理:铁粉在水存在下能跟空气里的氧气反应,放出热量。
4Fe+2H2O+3O2=2Fe2O3·H2O+Q
准备:取一只约80×120mm(的自封式塑料袋),另用无纺布缝制一只略大于上塑料袋的布袋。
操作:
(1)用大头针在自封式塑料袋上扎几十个针眼(袋的两层同时扎穿)。
(2)称取15g 小颗粒状活性炭、40g 还原铁粉、5g 细木屑,都放在一只烧杯中,再加入15mL 15%的食盐水,用玻璃棒搅拌均匀。
(3)把烧杯里的混合物全部加入扎过孔的塑料袋内,封上袋口。把这塑料袋放入自制的布袋中,扎住袋口。
(4)反复搓擦这袋5~8分钟,能感觉布袋的温度明显上升。
21. 玻璃棒 环形玻璃搅拌棒 b 碱 24.60 0.2460mol/L 偏低 偏高
一、单选题
1.下列关于能量变化的说法正确的是
A.化学反应遵循质量守恒的同时,也遵循能量守恒
B.已知C(石墨,s) = C(金刚石,s) △H>0,则金刚石比石墨稳定
C.古文说 “冰,水为之,而寒于水” 说明等量的水和冰相比,冰的能量更高
D.化学反应在物质变化的同时,伴随着能量变化,其表现形式只有吸热和放热两种
2.下列说法中正确的是
A.化学反应中的能量变化都是以热量形式体现的
B.化学键的断裂一定会伴随着化学变化
C.加入催化剂可以改变化学反应的反应热
D.原电池原理的本质是发生氧化还原反应
3.下列有关热化学方程式的叙述中,正确的是( )
A.含20.0gNaOH的稀溶液与足量的稀硫酸完全中和,放出28.7kJ的热量,则表示中和热的热化学方程式为2NaOH(aq)+H2SO4(aq)=Na2SO4(aq)+2H2O(l) △H=-114.8kJ·mol-1
B.已知热化学方程式:SO2(g)+O2(g)SO3(g) △H=-98.32kJ·mol-1,在容器中充入2molSO2和1molO2充分反应,最终放出的热量为196.64kJ
C.已知2H2(g)+O2(g)=2H2O(g) △H=-483.6kJ·mol-1,则H2的燃烧热为241.8kJ·mol-1
D.已知石墨转化为金刚石为吸热,那么石墨比金刚石稳定
4.最新报道:科学家首次用X射线激光技术观察到CO与O在催化剂表面形成化学键的过程。反应过程的示意图如下:
下列说法正确的是
A.状态I→状态Ⅲ表示CO与O2反应生成CO2的过程
B.CO和O生成CO2是吸热反应
C.状态I→状态Ⅲ表示CO与O反应生成CO2的过程
D.在该过程中,CO断键形成C和O
5.某同学设计如图所示实验,探究化学反应中的能量变化
下列判断正确的是
A.由实验可知,Ⅰ、Ⅱ、Ⅲ所涉及的反应都是放热反应
B.将实验Ⅰ中的镁片更换为等质量的镁粉后释放出的热量增多
C.实验Ⅲ中将玻璃搅拌器改为铜质搅拌器对实验结果没有影响
D.实验Ⅲ中若用浓硫酸测定中和反应的反应热,则测定的ΔH偏低
6.下列实验操作和现象所得结论错误的是
选项 实验操作 现象 结论
A 向久置的浓硝酸中通入空气 溶液褪色 涉及化合反应
B 将某种盐溶液溶于水形成浓溶液,加入足量盐酸 产生白色沉淀 盐中可能含有Ag+或SiO
C 控制相同条件,分别加热KClO3和KClO3与MnO2的混合物 产生等体积的气体,前者用时更长 催化剂能改变反应热
D 将Na2S加入含Hg2+的废水中 生成黑色难溶物 可用Na2S净化含Hg2+的废水
A.A B.B C.C D.D
7.若某反应属于吸热反应,则该反应()
A.一定需要加热才能进行
B.反应物总能量低于生成物总能量
C.反应物总质量小于生成物总质量
D.在常温下不可能发生
8.某实验小组用50mL0.50mol L 1盐酸与50mL0.55mol L 1NaOH溶液在如图所示的装置中进行中和反应。下列说法不正确的是
A.烧杯间填满碎泡沫塑料的作用是减少热量散失
B.大烧杯上如不盖硬纸板,求得的反应热数值偏小
C.用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的反应热的数值相等
D.实验中改用60mL0.50mol L 1盐酸与50mL0.55mol L 1NaOH溶液进行反应,与上述实验相比,所放出的热量不相等
9.下列反应属于非氧化还原反应,且能量变化与图示能量相符合的是
A.与稀反应 B.氢气与氮气的化合反应
C.灼热的炭与反应 D.晶体与晶体反应
10.下列实验不能达到实验目的是
A.实验室制取乙酸乙酯 B.探究同主族元素性质的递变性
C.测定中和反应的反应热 D.检验木炭与浓硫酸反应的产物
A.A B.B C.C D.D
11.如图所示,有关化学反应和能量变化的说法正确的是
A.图表示的是吸热反应的能量变化
B.图中反应物比生成物稳定
C.图可以表示氧化钙与水反应的能量变化
D.图不需要加热就一定能发生,图一定需要加热才能发生
12.一定条件下,石墨转化为金刚石吸收能量。下列关于石墨和金刚石的说法不正确的是
A.石墨比金刚石稳定
B.两物质的碳碳σ键的键角相同
C.可以用X射线衍射仪鉴别金刚石和石墨
D.等质量的石墨和金刚石中,碳碳σ键数目之比3∶4
13.化学反应Cl2(g)+H2(g)=2HCl(g)的能量变化如图所示。(△E为能量变化值,a、b、c均为正值)下列相关说法正确的是
A.上述反应为吸热反应
B.2molCl和2molH的总能量大于2molHCl(g)的能量
C.1molHCl(l)转变为1molHCl(g)需要放出ckJ能量
D.反应Cl2(g)+H2(g)=2HCl(g)的能量变化值为(a+b)kJ
14.有关化学反应与能量的下列叙述正确的是
A.若A(s)=B(s)为放热反应,则A比B稳定
B.化学反应中的能量变化主要是由化学键变化引起的
C.同一化学反应在不同条件下发生时可能放热也可能吸热
D.反应物总能量高于生成物总能量的反应不需要加热就能发生
15.下列图示与对应的叙述相符的是
A.(a)图可表示锌和稀硫酸反应过程中的能量变化
B.通过(b)图可知金刚石比石墨稳定
C.由(c)图可知,2SO3(g)2SO2(g)+O2(g) △H=(a-b)kJ·mol-1
D.(d)图是某反应A→C的能量变化曲线图(E表示能量),反应中△H=E1-E4
二、填空题
16.50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
(1)从实验装置看,图中尚缺少的一种玻璃仪器是 。
(2)烧杯间填满碎纸条的作用是 。
(3)实验中改用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比较,所放出的热量 (填“相等”或“不相等”),中和热 (填“相等”或“不相等”),理由是 。
(4)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得中和热的数值与57.3kJ/mol相比较会 。(填“偏大”、“偏小”或“无影响”)。
(5)完整地做一次这样的实验,需测定 次温度。
(6)大烧杯上如不盖硬纸板,求得的中和热数值 (填“偏大”、“偏小”或“无影响”
17.氨在国民经济中占有重要地位。合成氨工业中,合成塔中每产生2mol NH3,放出92.2kJ热量。
(1)工业合成氨的热化学方程式是: 。
(2)已知:
1mol N-H键断裂吸收的能量约等于 kJ。
18.等质量的碳酸钠、碳酸氢钠粉末分别与足量的盐酸发生反应时,产生CO2较多的是 (填化学式)。实验过程中,同学们感受到碳酸钠与盐酸的反应是放热反应,而碳酸氢钠与盐酸的反应是吸热反应,下图中代表碳酸钠与盐酸反应的是 (填字母)。
19.Ⅰ.燃料电池电动汽车是利用氢气、甲醇、天然气(主要成分为甲烷)、汽油等燃料和空气中的氧在催化剂的作用下在燃料电池中经电化学反应产生的电能,并作为主要动力源驱动的汽车。
(1)汽车行驶的过程中,能量的转化形式为 。
Ⅱ.利用下表数据回答下列问题:
燃料 燃烧热/(kJ·mol-1) 燃料 燃烧热/(kJ·mol-1)
氢气 285.8 甲醇(CH3OH) 726.51
甲烷(CH4) 890.3 正丁烷(CH3CH2CH2CH3) 2878.0
乙烷(C2H6) 1559.8 2869.6
丙烷(C3H8) 2219.9
(2)表示乙烷燃烧热的热化学方程式为 。
(3)稳定性:正丁烷 异丁烷(填“>”“<”或“=”);原因 。
(4)相同质量的燃料, (填“C”或“H”)的质量分数越大,燃烧放出的热量越多。
(5)二氧化碳是重要的温室气体,从环保角度分析,放出相同的热量时选择 (填“乙烷”或“甲醇”)作为燃料产生的CO2较少。
(6)现有氢气和丙烷混合气体3 mol,完全燃烧共产生2791.5 kJ的热量,则氢气和丙烷的物质的量之比为 。
20.在寒冷的冬季,我们可以通过取暖器、电热炉,暖宝宝等来取暖。请查阅资料,设计一个通过化学反应产生热量的暖手袋的制作方案 。
三、实验题
21.I.中和热测定:
(1)中和热测定的实验中,用到的玻璃仪器有烧杯、温度计、 、 。
(2)量取反应物时,取50 mL 0.50 mol·Lˉ1的盐酸,还需加入的试剂是 (填序号)。
a.50 mL 0.50 mol·Lˉ1NaOH溶液
b.50 mL 0.55 mol·Lˉ1NaOH溶液
c.1.0 g NaOH固体
II.现用中和滴定测定某盐酸的浓度,有关数据记录如下:
滴定序号 待测液体积(mL) 所消耗烧碱标准液的体积(mL)
滴定前 滴定后 消耗的体积
1 25.00 0.50 25.12 24.62
2 25.00 / / /
3 25.00 5.00 29.58 24.58
(3)应用 式滴定管盛装0.2500 mol/L烧碱标准液,锥形瓶中装有25.00mL待测盐酸溶液。
(4)如图表示第二次滴定时50 mL滴定管中前后液面的位置。该次滴定所用标准烧碱溶液体积为 mL。
(5)根据所给数据,计算出该盐酸的物质的量浓度(注意保留合适的有效数字),c (HCl) = 。
(6)读数时,若滴定前仰视,滴定后俯视,则会使最终测定结果 (填“无影响”、“偏高”、“偏低”。下同);若装标准液的滴定管在装液前未用标准NaOH溶液润洗,会使最终测定结果 。
参考答案:
1.A2.D3.D4.C5.D6.C7.B8.C9.D10.D11.B12.B13.B14.B15.C
16. 环形玻璃搅拌棒 减少实验过程中热量损失 不相等 相等 因为中和热是指在稀溶液中,酸跟碱发生中和反应生成1molH2O所放出的能量,与酸碱用量无关 偏小 3 偏小
17.(1)
(2)391
18. NaHCO3 a
19.(1)化学能转化为电能,电能转化为动能
(2)C2H6(g)+O2(g)=2CO2(g)+3H2O(l) ΔH=-1559.8 kJ·mol-1
(3) < 由表格中的数据可知,异丁烷的燃烧热比正丁烷的燃烧热小,则异丁烷的能量低,即稳定性:正丁烷<异丁烷
(4)H
(5)乙烷
(6)2∶1
20.原理:铁粉在水存在下能跟空气里的氧气反应,放出热量。
4Fe+2H2O+3O2=2Fe2O3·H2O+Q
准备:取一只约80×120mm(的自封式塑料袋),另用无纺布缝制一只略大于上塑料袋的布袋。
操作:
(1)用大头针在自封式塑料袋上扎几十个针眼(袋的两层同时扎穿)。
(2)称取15g 小颗粒状活性炭、40g 还原铁粉、5g 细木屑,都放在一只烧杯中,再加入15mL 15%的食盐水,用玻璃棒搅拌均匀。
(3)把烧杯里的混合物全部加入扎过孔的塑料袋内,封上袋口。把这塑料袋放入自制的布袋中,扎住袋口。
(4)反复搓擦这袋5~8分钟,能感觉布袋的温度明显上升。
21. 玻璃棒 环形玻璃搅拌棒 b 碱 24.60 0.2460mol/L 偏低 偏高
