第3章 有机合成及其应用合成高分子化合物 练习卷(含解析)2022-2023学年下学期高二化学鲁科版(2019)选择性必修3
文档属性
| 名称 | 第3章 有机合成及其应用合成高分子化合物 练习卷(含解析)2022-2023学年下学期高二化学鲁科版(2019)选择性必修3 |

|
|
| 格式 | docx | ||
| 文件大小 | 1.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-12-11 00:00:00 | ||
图片预览




文档简介
第3章 有机合成及其应用 合成高分子化合物 练习卷
一、单选题(共14题)
1.化学是材料学的基础。下列说法不正确的是
A.可降解聚乳酸塑料的推广应用可减少“白色污染”
B.制造特种防护服的芳纶纤维属于有机高分子材料
C.北京冬奥会火炬使用的碳纤维不属于有机高分子材料
D.制作电器开关用的脲醛树脂属于热塑性塑料
2.维生素C是重要的营养素,其分子结构如图所示,下列关于维生素C的说法正确的是
A.维生素C的分子式为
B.维生素C的含氧官能团有羟基、羧基
C.维生素C易溶于水
D.维生素C不能使酸性高锰酸钾溶液褪色
3.下列叙述正确的是
A.中共面的碳原子最多有13个
B.的一氯代物有4种
C.乙二酸二乙酯与二乙酸乙二酯互为同分异构体
D.由2种单体经过加聚反应合成
4.下列有关高分子材料制备的说法错误的是
A.己二酸和己二胺发生缩聚反应生成尼龙66
B.一定条件下,乙烯和丙烯发生加聚反应合成塑料
C.苯酚和甲醛在一定条件下发生缩聚反应生成酚醛树脂
D.乳酸[CH3CH(OH)COOH]发生加聚反应合成可降解高分子材料
5.下列说法不正确的是
A.己烷共有4种同分异构体,它们的熔点、沸点各不相同
B.在一定条件下,苯分别与液溴、浓硝酸、浓硫酸作用生成溴苯、硝基苯、苯磺酸的反应都属于取代反应
C.的一氯代物有5种
D.聚合物()可由单体CH3CH=CH2和CH2=CH2加聚制得
6.某有机物的结构如图所示,1mol该有机物
A.最多可以与反应
B.最多可以与1molNaOH反应
C.可用酸性检验结构中的碳碳双键
D.与发生加成反应产物有4种
7.下列有关的说法不正确的是
A.该有机物的分子式为,1mol该有机物完全燃烧需消耗4molO2
B.该有机物能发生取代反应、加成反应、氧化反应、中和反应
C.该有机物分别与足量Na、NaOH、反应,生成物均为
D.该有机物分子内和分子间都能发生酯化反应
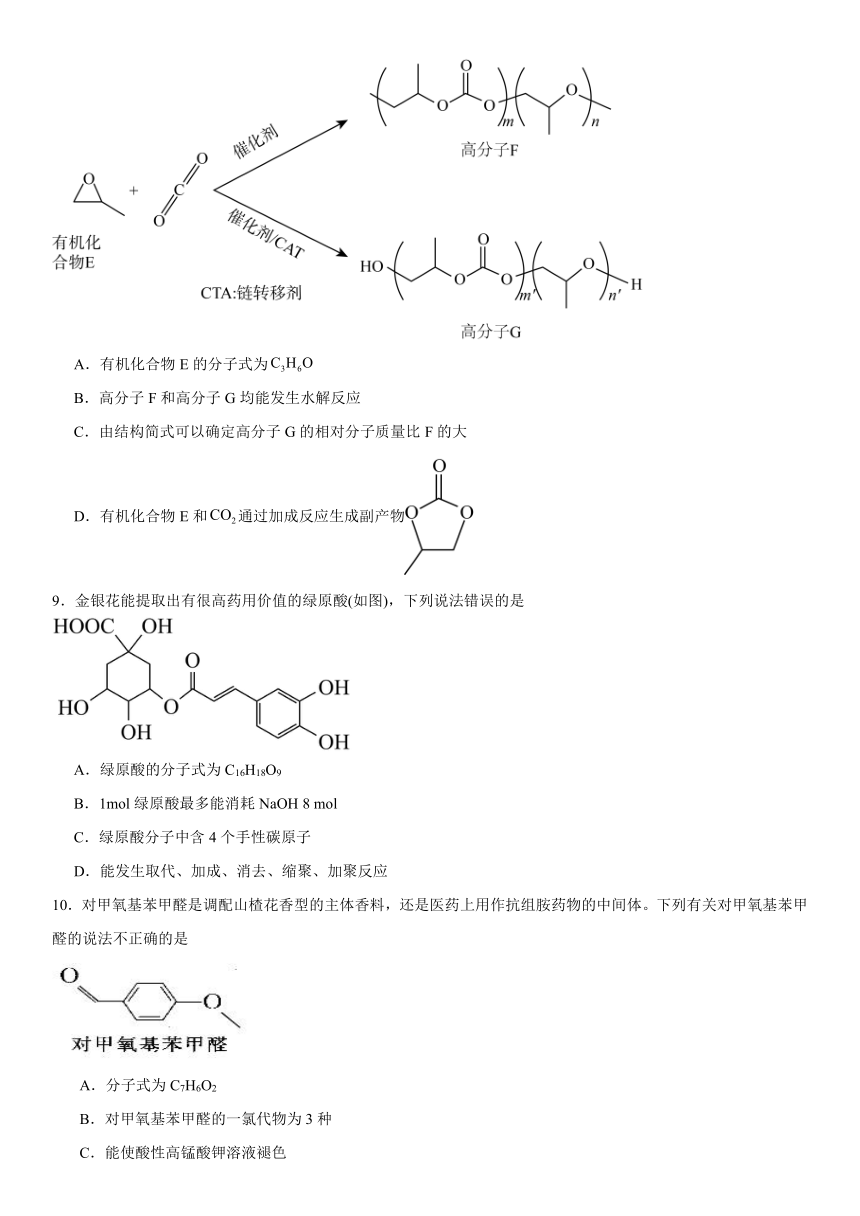
8.环氧化物与开环共聚反应是合成高附加值化学品的一种有效途径,两类共聚物的合成路线如下(副产物为环状碳酸酯)。下列说法不合理的是
A.有机化合物E的分子式为
B.高分子F和高分子G均能发生水解反应
C.由结构简式可以确定高分子G的相对分子质量比F的大
D.有机化合物E和通过加成反应生成副产物
9.金银花能提取出有很高药用价值的绿原酸(如图),下列说法错误的是
A.绿原酸的分子式为C16H18O9
B.1mol绿原酸最多能消耗NaOH 8 mol
C.绿原酸分子中含4个手性碳原子
D.能发生取代、加成、消去、缩聚、加聚反应
10.对甲氧基苯甲醛是调配山楂花香型的主体香料,还是医药上用作抗组胺药物的中间体。下列有关对甲氧基苯甲醛的说法不正确的是
A.分子式为C7H6O2
B.对甲氧基苯甲醛的一氯代物为3种
C.能使酸性高锰酸钾溶液褪色
D.1mol对甲氧基苯甲醛能和4mol氢气发生加成反应
11.化学与科学、技术、社会、环境密切相关。下列有关说法不正确的是
A.乙烯与氧气在银催化作用下生成环氧乙烷符合绿色化学的原子经济性要求
B.草莓棚中使用的“吊袋式二氧化碳气肥”的主要成分可以是碳酸钙
C.水暖器材中的PVC管常用作进水管,而PE管常用作出水管
D.用 CO2 合成聚碳酸酯可降解塑料,实现“碳”的循环利用
12.近年来我国取得了很多令世界瞩目的科技成果,化学功不可没。下列说法正确的是
A.神舟十三号载人飞船返回舱逃逸系统复合材料中的酚醛树脂属于天然高分子化合物
B.“北斗系统”组网成功,其芯片的主要成分为二氧化硅
C.“嫦娥五号”运载火箭用液氧、液氢做推进剂,产物对环境无污染
D.T-碳(T-Carbon)是中科院预言的一种三维碳结构晶体,其与C60互为同位素
13.某金属有机多孔材料(MOFA)在常温常压下对CO2具有超高的吸附能力,并能高效催化CO2与环氧乙烷衍生物的反应,其工作原理如图所示。下列说法错误的是
A.该材料的吸附作用具有选择性 B.若R为H,分子不可能为平面形结构
C.在生成的过程中,有键形成 D.CO2可用于有机物碳骨架的增长与构建
14.下列各组中两个变化所发生的反应,属于同一类型的是
①由甲苯制甲基环己烷与由乙烷制溴乙烷
②乙烯使溴水褪色与乙炔使酸性高锰酸钾水溶液褪色
③由乙烯制聚乙烯与由乙炔制聚乙炔
④由苯制硝基苯与由利用甲烷制备氯仿
A.只有①③ B.只有①④ C.只有②③ D.只有③④
二、填空题(共8题)
15.按要求回答下列问题:
(1)按系统命名法,的名称是 。
(2)与化合物互为同分异构体且一氯代物有两种的烃的结构简式为 。
(3)某烷烃分子的碳骨架结构为,若此烷烃为炔烃加氢制得,则此炔烃的结构简式为 。
(4)有机化合物A常用于食品行业。已知9.0gA在足量中充分燃烧,将生成的混合气体依次通过足量的浓硫酸和碱石灰,分别增加5.4g和13.2g,经检验剩余气体为。
①A分子的质谱图如图所示,则A的分子式是 。
②经红外光谱测定,已知A分子中含有羧基,A分子的核磁共振氢谱有4组吸收峰,且峰面积之比是1:1:1:3,则A的结构简式是 。
16.(1)根据核磁共振氢谱图可以确定有机物分子中氢原子的种类和数目。例如:乙醚的结构式为,其核磁共振氢谱中有2个信号(如下图)。
①下列分子中,其核磁共振氢谱中只有一种峰(信号)的物质是 (填字母)。
A.CH3-CH3 B.CH3COOH C.CH3COOCH3 D.CH3COCH3
②化合物A和B的分子式都是C2H4Br2,A的核磁共振氢谱如下图所示,则A的结构简式为 ,请预测B的核磁共振氢谱上有 个峰(信号)。
③用核磁共振氢谱的方法来研究C2H6O的结构,请简要说明根据核磁共振氢谱的结果来确定C2H6O分子结构的方法是 。
(2)有机物C常用于食品行业。已知9.0gC在足量O2中充分燃烧,将生成的混合气体依次通过足量的浓硫酸和碱石灰,分别增重5.4g和13.2g,经检验剩余气体为O2。
①C分子的质谱图如图所示,从图中可知其相对分子质量是 ,则C的分子式是 。
②C能与NaHCO3溶液发生反应,C一定含有的官能团名称是 。
③C分子的核磁共振氢谱有4个峰,峰面积之比是1:1:1:3,则C的结构简式是 。
17.香豆素—3—羧酸丹皮酚酯具有多种生物活性,结构简式为,用M表示,合成路线如图:
已知:丹皮酚的结构简式为。
已知:++R2OH。
请根据已学知识,写出以CH3OH和为原料(其它试剂任选)合成的路线 。
18.化学概念和用语是化学学科发展的基础,回答下列问题:
(1)有下列几组物质,请将序号填入下列空格内:
A.和油酸
B.和石墨
C.和
D.和
E.乙醇和乙二醇
①互为同位素的是 ;
②互为同系物的是 ;
③互为同素异形体的是 ;
④互为同分异构体的是 ;
⑤既不是同系物,又不是同分异体,也不是同素异形体,但可看成是同一类物质的是 。
(2)完成下列反应的化学方程式:
①乙醛与银氨溶液发生银镜反应: ;
②淀粉水解生成葡萄糖 ;
③向对甲基苯酚溶液中滴加饱和溴水: ;
④由丙烯制取聚丙烯: ;
⑤由己二酸和己二胺合成尼龙66(聚己二酰己二胺): 。
19.请填写下列空白:
(1)请写出支链只有一个乙基且式量最小的烷烃的结构简式: 在沥青中存在一系列结构相似的稠环芳香烃。这一系列化合物中的前三个同系物的结构简式如图所示。
(2)芘的分子式是
(3)这一系列有机物的通式可用含x的代数式来表示(x为自然数1,2,3,4…),则该通式为 。
(4)随着x值的增大,这一系列化合物含碳的质量分数的极限数值为 。(保留三位有效数字)
(5)环蕃A(cyclophane)和超蕃B(superphane)是一种光电信息材料,都属于烃(B中氢原子未画出),它们的结构如图所示。
下列有关说法正确的是 。
A.环蕃和超蕃互为同系物
B.环蕃能使酸性高锰酸钾溶液褪色
C.环蕃能与液溴、硝酸发生取代反应
超蕃的一氯取代物只有1种,二氯取代物有3种
20.按要求回答下列问题
(1)某烯烃在同温同压下蒸气的密度是密度42倍的烯烃,分子中所有碳原子一定在同一平面上,该烯烃的结构简式 该烯烃在一定条件下生成高分子化合物的化学方程式 ;
(2)系统命名为三甲基戊烯的结构简式 ;
(3)按系统命名法填写有机物的名称是
(4)的同分异构体数目为 种;
(5)乙烯使溴的四氯化碳溶液褪色的化学方程式为
(6)相对分子质量为的某烃的分子式
(7)1升乙炔和气态烯烃混合物与11升氧气混合后点燃,充分反应后,气体的体积为12升,(反应前后均为、),求:
①原1升混合气体中烯烃的可能的分子式
②乙炔和烯烃的物质的量之比
21.某烃经李比希元素分析实验测得碳的质量分数为85.71%,该烃的质谱图显示:分子离子峰的质荷比为70,该烃的核磁共振氢谱如下图所示。请确定该烃的
(1)实验式 ;
(2)分子式 ;
(3)结构简式 。
22.自20世纪90年代以来,稠环化合物的研究开发工作十分迅速,这一类物质在高科技领域有着十分广泛的应用前景。下面是苯和一系列稠环芳香烃的结构简式:
试解答下列问题:
(1)写出化合物②⑤的分子式:② ;⑤ ;
(2)这组化合物分子式的通式是:
(3)某课外兴趣小组,做了系列实验,他们将该系列的前5种芳香烃逐一加到浓的酸性高锰酸钾溶液中加热。结果发现,只有苯无明显变化,其余4种物质都能使酸性高锰钾溶
液褪色。经分析知后4种稠环芳烃的氧化产物是:、
或者两者都有。由此你能得出的结论是: ,
(4)甲、乙、丙三同学同做酸性高锰酸钾溶液氧化并五苯的实验。甲将氧化后的混合液酸化分离得到一种无色晶体X,称取0.2540g X,用热水配成100mL溶液中和滴定,取出25.00mL,用0.1000mol·L-1NaOH溶液中和滴定,滴到10.00mL时达到终点;丙用酸性高锰酸钾氧化并五苯,将氧化后的混合液酸化分离得到无色晶体Y,中和测定知Y的中和能力只有X的中和能力的一半;乙用酸性高锰钾溶液氧化并五苯,将氧化后的混合液酸化分离得无色晶体,经分析其中包含了甲与丙得的两种成分,通过计算推理确定X的结构简式 。
(5)在Y的同分异构体中与Y同属芳香族化合物既可看作羧酸类,又可看作酯类的同分异构体的结构简式有: ,
在Y的同分异构体中既不属于羧酸类,又不属于酯类,但可看作常见芳香烃的衍生物的同分异构体的结构简式有 (写一种)
试卷第1页,共3页
参考答案:
1.D
【详解】A.“白色污染”是指塑料污染,因此可降解聚乳酸塑料的推广应用可减少“白色污染”,故A说法正确;
B.有机高分子材料包括塑料、合成纤维、合成橡胶,芳纶纤维属于合成纤维,即属于有机高分子材料,故B说法正确;
C.碳纤维是碳单质,不属于有机物,故C说法正确;
D.脲醛树脂制成的塑料制品不能加热熔融,只能一次成型,是热固性,故D说法错误;
答案为D。
2.C
【详解】A.维生素C的分子式为,选项A错误;
B.维生素C的含氧官能团有羟基、酯基,选项B错误;
C.维生素C分子中含有大量的羟基,故易溶于水,选项C正确;
D.维生素C的碳碳双键和羟基能使酸性高锰酸钾溶液褪色,选项D错误。
答案选C。
3.C
【详解】A.中苯环和乙烯为平面型结构,而乙炔为直线形结构,则所有的碳原子有可能都在同一平面上,乙基中碳碳单键发生旋转,该分子中所有C原子都可以共面,即共平面的碳原子共14个。故A错误;
B.分子内等效氢为3种,则一氯代物有3种,故B错误;
C.乙二酸二乙酯与二乙酸乙二酯的分子式均为C6H10O4,且结构不同,互为同分异构体,故C正确;
D.高分子化合物是由3种单体经过加聚反应合成,故D错误;
答案为C。
4.D
【详解】A.工业上己二酸和已二胺以等摩尔比进行反应缩聚得到尼龙66 ,A正确;
B.乙烯、丙烯相互反应生成乙烯一丙烯共聚物塑料,是加聚反应,B正确;
C.苯酚在一定条件下能与甲醛发生缩聚反应生成酚醛树脂,C正确;
D.聚乳酸是一种新型绿色环保可降解的高分子材料,但乳酸生成聚乳酸是缩聚反应,D错误;
故答案为:D。
5.A
【详解】A.己烷共有5种同分异构体,即、、、、,故A错误;
B.在一定条件下,苯与液溴生成、苯与浓硝酸,在浓硫酸作用下反应生成硝基苯、苯与浓硫酸反应生成苯磺酸,都属于取代反应,故B正确;
C.有5种位置的氢即,其一氯代物有5种,故C正确;
D.聚合物()从左边第二个碳与第三个碳原子断碳碳键即,第一个碳和第二个碳形成双键,第三个和第四个碳形成双键,因此可由单体CH3CH=CH2和CH2=CH2加聚制得,故D正确。
综上所述,答案为A。
6.D
【详解】A.能与氢气发生反应的官能团为碳碳双键、醛基,1mol碳碳双键需要1mol氢气,1mol醛基需要1mol氢气,则1mol该有机物最多可与3molH2反应,A项错误;
B.能与NaOH溶液反应的官能团为酯基和羧基,则1mol该有机物最多与2molNaOH反应,B项错误;
C.该有机物能被酸性高锰酸钾氧化的官能团为醛基、羟基、碳碳双键,故不可用酸性高锰酸钾检验结构中的碳碳双键,C项错误;
D.与发生加成反应产物为、、、,反应产物有4种,D项正确;
答案选D。
7.C
【详解】A.该有机物的分子式为,1mol该有机物完全燃烧消耗的物质的量为4mol,选项A正确;
B.因该有机物含碳碳双键,能发生加成反应、氧化反应,含有羧基,能发生取代反应(酯化反应)和中和反应,选项B正确;
C.因该有机物同时含有羧基和羟基,该有机物与足量Na反应的产物应为,选项C错误;
D.因该有机物同时含有羧基和羟基,则该有机物分子内与分子间均能发生酯化反应,选项D正确。
答案选C。
8.C
【详解】A.有机化合物E的分子式为,A合理;
B.高分子F和高分子G均含有酯基,都能发生水解反应,B合理;
C.高分子F中的和高分子G中的的相对大小不确定,因此两者的相对分子质量不能比较大小,C不合理;
D.对比化合物E与环状碳酸酯的结构简式,可以确定化合物E与CO2是通过加成反应生成环状碳酸酯,D合理;
故选C。
9.B
【详解】A.根据绿原酸结构简式,结合C原子最外层有4个电子,可以形成4个共价键,可知其分子式为C16H18O9,A正确;
B.根据绿原酸结构简式可知:1个绿原酸分子中含有1个羧基、1个酯基和2个酚羟基可以与NaOH发生反应;酯基水解产生的羧基可以与NaOH反应,产生的醇羟基不能与NaOH反应,故1mol绿原酸最多能消耗4 mol 的NaOH,B错误;
C.结合4个不同原子或原子团的碳原子为手性碳原子,则与3个醇-OH相连的C及与酯基直接相连的六元环上的C为手性碳原子,因此物质分子中共有4个手性碳原子,C正确;
D.绿原酸分子中含有羟基和羧基及酯基,所以能发生取代反应;含有不饱和的碳碳双键,能够发生加成反应;由于与醇羟基连接的C原子的邻位C原子上含有H原子,能够发生消去反应;分子中含有羧基和羟基,能够发生缩聚反应;含有不饱和的碳碳双键,能够发生加聚反应,D正确;
故合理选项是B。
10.A
【详解】A.由图示结构简式可知,分子式为C8H8O2, A错误;
B.对甲氧基苯甲醛分子内有2种氢,故一氯代物为3种,B正确;
C.对甲氧基苯甲醛中含有醛基,能与新制氢氧化铜悬浊液、银氨溶液等反应,故能发生氧化反应,使酸性高锰酸钾溶液褪色,C正确;
D.1 mol对甲氧基苯甲醛含有1mol苯环能与3molH2加成,1mol醛基能与1molH2加成,故一共能和4 mol氢气发生加成反应,D正确;
答案为A。
11.B
【详解】A.乙烯与氧气在银催化作用下生成环氧乙烷,反应物全部转化为生成物,从理论、经济、环保以及操作等方面都很好,符合绿色化学的原子经济性要求,故A不选;
B.碳酸钙需要在高温下煅烧分解得到二氧化碳,草莓棚中不能使用碳酸钙来产生二氧化碳,故选B;
C.PVC是聚氯乙烯的简称,PVC中含有Cl在受热时会产生有毒有害的物质,所以常用作热水器的进水管,PE是聚乙烯的简称,PE无臭,无毒,具有优良的耐低温性能(最低使用温度可达-100~-70°C),化学稳定性好,能耐大多数酸碱的侵蚀(不耐具有氧化性质的酸),所以常用作热水器的出水管,故C不选;
D.用 CO2合成聚碳酸酯可降解塑料,节约资源,减少碳的排放,符合低碳经济要求,同时该塑料在讲解过程中又生成二氧化碳,能实现“碳”的循环利用,故D不选。
答案选B。
12.C
【详解】A.酚醛树脂是由人工合称的高分子材料,A错误;
B.芯片的主要成分为硅单质,二氧化硅主要用于制作光导纤维,B错误;
C.液氧、液氢反应可以放出大量的热,产物为水,对环境无污染,C正确;
D.T-碳(T-Carbon)和C60为碳元素形成的不同单质,互为同素异形体,不是同位素,D错误;
综上所述答案为C。
13.C
【详解】A.某金属有机多孔材料(MOFA)在常温常压下对CO2具有超高的吸附能力,该材料的吸附作用具有选择性,A正确;
B.该物质分子中含有的C原子为饱和C原子,具有甲烷的四面体结构,因此分子不可能是平面结构,B正确;
C.在由a生成b的过程中,需断裂CO2分子中的C=O中较活泼的键及a中的C-O键,同时形成新的C-O键,并没有键形成,C错误;
D.根据选项C分析可知:CO2在有机合成中,可用于有机物碳骨架的增长与构建,D正确;
故合理选项是C。
14.D
【详解】①由甲苯制甲基环己烷的反应为加成反应,由乙烷制溴乙烷的反应为取代反应,反应类型不相同,故不符合题意;
②乙烯使溴水褪色的反应为加成反应,乙炔使酸性高锰酸钾水溶液褪色的反应为氧化反应,反应类型不相同,故不符合题意;
③由乙烯制聚乙烯和由乙炔制聚乙炔的反应都为加聚反应,反应类型相同,故符合题意;
④由苯制硝基苯和由利用甲烷制备氯仿的反应都为取代反应,反应类型相同,故符合题意;
只有③④符合题意,故选D。
15.(1)3,4-二甲基己烷
(2)
(3)
(4)
【解析】(1)
主链有6个碳原子,第3、4号碳原子各有1个甲基,名称是3,4-二甲基己烷;
(2)
与化合物互为同分异构体且一氯代物有两种,说明分子中有2种等效氢,结构对称,符合条件的结构简式为。
(3)
某烷烃分子的碳骨架结构为,若此烷烃为炔烃加氢制得,根据C原子能形成4个共价键,此炔烃的结构简式为;
(4)
9.0gA在足量中充分燃烧,将生成的混合气体依次通过足量的浓硫酸和碱石灰,分别增加5.4g和13.2g ,说明反应生成5.4g水、13.2g二氧化碳,则9gA中含有H原子0.6mol、含有C原子0.3mol,含有氧原子,则A分子的实验式为CH2O,根据A分子的质谱图可知,A的相对分子质量为90,A的分子式是C3H6O3。
②经红外光谱测定,已知A分子中含有羧基,A分子的核磁共振氢谱有4组吸收峰,且峰面积之比是1:1:1:3,则A的结构简式是。
16. AD BrCH2CH2Br 2 通过其核磁共振氢谱中的峰信号可以判断有3个信号时,分子结构为CH3CH2OH;1个信号时分子结构为CH3-O-CH3 90 C3H6O3 羧基
【详解】(1)①核磁共振氢谱中只有一种峰,说明该分子中的H原子都是等效的,只有1种H原子,
A. CH3-CH3中6个H原子都是等效的,核磁共振氢谱中只有一种峰,故A选;
B. CH3COOH中甲基中的H原子与羧基中的H原子所处化学环境不同,CH3COOH有2种H原子,核磁共振氢谱中有2个峰,故B不选;
C. CH3COOCH3中甲基所处化学环境不同,甲基H原子不同,有2种H原子,核磁共振氢谱中有2个峰,故C不选;
D. CH3COCH3中2个甲基连在同一个羰基上,6个H原子都是等效的,核磁共振氢谱中只有一种峰,故D选;
故选AD;
②)由A的核磁共振氢谱可知,分子中只有一种H原子,A分子中2个Br原子连接不同的碳原子,故A的结构简式为BrCH2CH2Br,B与A互为同分异构体,B分子中2个Br原子连接在同一碳原子上,B为CH3CHBr2,分子中有2种H原子,故核磁共振氢谱图有2个峰;
③通过其核磁共振氢谱中的峰信号可以判断有3个信号时,分子结构为CH3CH2OH;1个信号时,分子结构为CH3-O-CH3;
(2)①由C分子的质谱图,可知C的相对分子质量为90,9g C的物质的量为,燃烧生成二氧化碳为,生成水为,则1个有机物分子中N(C)=、N(H)=,则分子中N(O)=,故有机物C的分子式为C3H6O3;
②C能与NaHCO3溶液发生反应,C一定含有羧基;
③有机物C的分子式为C3H6O3,含有羧基,C分子的核磁共振氢谱有4个吸收峰,说明含有4种H原子,峰面积之比是1:1:1:3,则4种H原子数目为1、1、1、3,则A的结构简式为:CH3CH(OH)COOH。
17.
【详解】被酸性高锰酸钾溶液氧化生成,和甲醇发生酯化反应生成,和反应生成,合成路线为:。
18.(1) D A B C E
(2)
【详解】(1)①质子数相同,中子数不同的原子互为同位素,互为同位素的是D.和;
②结构相似,组成上相差n个CH2原子团的有机物互为同系物,互为同系物的是A.和油酸;
③同种元素的不同单质互为同素异形体,互为同素异形体的是B.和石墨;
④分子式相同,结构不同的物质互为同分异构体,互为同分异构体的是C.和 ;
⑤既不是同系物,又不是同分异体,也不是同素异形体,但可看成是同一类物质的是E.乙醇和乙二醇,两者均为醇。
(2)①乙醛与银氨溶液发生银镜反应的化学方程式:;
②淀粉水解生成葡萄糖的化学方程式;
③向对甲基苯酚溶液中滴加饱和溴水的化学方程式:;
④由丙烯制取聚丙烯的化学方程式:;
⑤由己二酸和己二胺合成尼龙66(聚己二酰己二胺) 的化学方程式:。
19.(1)CH3CH2CH
(2)C16H10
(3)C(6x+4)H(2x+6)
(4)97.3%
(5)B、C
【详解】(1)支链只有一个乙基且式量最小的烷烃是3—乙基戊烷,结构简式为CH3CH2CH(CH2CH3)2。
(2)根据有机物的结构简式可知芘的分子式是C16H10。
(3)根据有机物的结构简式可知萘的分子式为C10H8,与芘的分子式相比少1个C6H2,所以这一系列有机物的通式如果用含x的代数式来表示,则该通式可表示为C(6x+4)H(2x+6)。
(4)随着x值的增大,这一系列化合物含碳的质量分数为 ,则其极限数值为 。
(5)A.根据二者的结构简式可知二者的结构不相似,且含有相同的碳原子数,因此环蕃和超蕃不能互为同系物,A错误;
B.环蕃分子中与苯环相连的碳原子含有氢原子,因此能使酸性高锰酸钾溶液褪色,B正确;
C.含有苯环,因此环蕃能与液溴、硝酸发生取代反应,C正确;
D.超蕃的一氯取代物只有2种,D错误;
答案选BC。
20.(1) n
(2)
(3)3-甲基-4-乙基辛烷
(4)5
(5)CH2=CH2+Br2→CH2Br-CH2Br
(6)C13H26
(7) C3H6 (或C4H8) 1:1 (或2:1)
【解析】(1)
某烯烃在同温同压下蒸气的密度是H2密度42倍,则烯烃相对分子质量为42×2=84,由,故烯烃分子式为C6H12,分子中所有碳原子一定在同一平面上,则烯烃为,该烯烃在一定条件下生成高分子化合物的化学方程式n;
(2)
2,3,3-三甲基-1-戊烯的结构简式为;
(3)
最长主链有8个碳原子,从距离甲基近的一定编碳号,甲基处于3号、乙基在4号碳原子上,编号为,其名称为3-甲基-4-乙基辛烷;
(4)
C6H14属于烷烃,其同分异构体有CH3(CH2)4CH3、CH3CH2CH2CH(CH3)2、CH3CH2CH(CH3)CH2CH3、、共5种;
(5)
乙烯与溴发生加成反应生成1,2-二溴乙烷,反应方程式为CH2=CH2+Br2→CH2Br-CH2Br;
(6)
分子中最大碳原子数目=,该烃的分子式为C13H26;
(7)
设该混合烃的平均分子组成为CxHy,则:
CxHy+(x+)O2 xCO2+H2O,△V=1+ x+-x-=-1,由△V=0,则-1=0,解得y=4,C2H2分子中氢原子个数为2,而混合烃的平均组成中氢原子个数为4,所以,烯烃中氢原子个数必大于4,又因为是气态烯烃,碳原子个数必小于或等于4,所以烯烃只能是C3H6或C4H8,若是C2H2、C3H6,设二者物质的量分别为xmol、ymol,则=4,整理可得x:y=1:1,若是C2H2、C4H8,设二者物质的量分别为amol、bmol,则=4,整理可得a:b=2:1,
①原1升混合气体中烯烃的可能的分子式:C3H6 (或C4H8);
②乙炔和烯烃的物质的量之比:1:1 (或2:1)。
21. CH2 C5H10
【详解】因分子离子峰的质荷比为70,则有该有机物的相对分子质量为70,分子中的碳原子数:=5,氢原子个数:=10,则其分子式为C5H10,实验式为CH2,由核磁共振氢谱图可得出该烃分子中只有一种化学环境下的氢原子,从而其结构简式为:,故答案为CH2、C5H10、 。
【点睛】本题主要展示了科学家确定有机物结构的一般流程,先确定有机物的元素组成,然后由相对分子质量确定有机物的分子式,最后通过核磁共振氢谱图等方法来确定有机物的结构。该烃的分子式为C5H10,而分子中只有一种氢原子,故分子中应该含有5个CH2原子团,从而推断该烃为环戊烷。
22.(1)
(2)
(3)苯很稳定,不能被高锰酸钾氧化
(4)
(5)
【分析】(1)根据有机物的结构简式可以写出各物质的分子式;
(2)根据以上五种有机物的分子式找出碳、氢原子数目的变化规律,从而找出通式;
(3)根据信息即可得出苯很稳定的结论;
(4)根据题给信息可知,后4种稠环芳烃的氧化产物是:、;甲将氧化后的混合液酸化分离得到一种无色晶体X的中和碱的能力是丙将氧化混合液酸化分离得到无色晶体Y中和碱的能力的2倍,且乙将氧化后的混合液酸化分离得无色晶体,经分析其中包含了甲与丙的两种成分,所以X的结构简式为,Y的结构简式为;
(5)根据Y的结构简式为;结合与Y互为同分异构体的条件,进行分析。
【详解】(1)根据有机物的结构简式可知,①② ③ ④ ⑤;答案:②;⑤;
(2)根据以上五种有机物的分子式可知,碳原子数相差4,氢原子数相差2个,因此这组化合物分子式的通式是:;答案:;
(3)前5种芳香烃逐一加到浓的酸性高锰酸钾溶液中加热,结果发现,只有苯无明显变化,其余4种物质都能使酸性高锰钾溶液褪色,这说明苯的结构很稳定,不能被高锰酸钾氧化;答案:苯很稳定,不能被高锰酸钾氧化;
(4)根据题给信息可知,后4种稠环芳烃的氧化产物是:、;甲将氧化后的混合液酸化分离得到一种无色晶体X的中和碱的能力是丙将氧化混合液酸化分离得到无色晶体Y中和碱的能力的2倍,且乙将氧化后的混合液酸化分离得无色晶体,经分析其中包含了甲与丙的两种成分,所以X的结构简式为,Y的结构简式为;甲实验中消耗氢氧化钠的量为;而X( )分子量为254;所以0.2540g X的物质的量为;1molX中含有,所以0.001molX消耗碱液0.004mol;符合题意转化关系。
答案:;
(5)结合以上分析可知,Y的结构简式为;与Y同属芳香族化合物既可看作羧酸类,又可看作酯类的同分异构体的结构简式有:,,;在Y的同分异构体中既不属于羧酸类,又不属于酯类,但可看作常见芳香烃的衍生物的同分异构体的结构简式有等;
答案:,,;
一、单选题(共14题)
1.化学是材料学的基础。下列说法不正确的是
A.可降解聚乳酸塑料的推广应用可减少“白色污染”
B.制造特种防护服的芳纶纤维属于有机高分子材料
C.北京冬奥会火炬使用的碳纤维不属于有机高分子材料
D.制作电器开关用的脲醛树脂属于热塑性塑料
2.维生素C是重要的营养素,其分子结构如图所示,下列关于维生素C的说法正确的是
A.维生素C的分子式为
B.维生素C的含氧官能团有羟基、羧基
C.维生素C易溶于水
D.维生素C不能使酸性高锰酸钾溶液褪色
3.下列叙述正确的是
A.中共面的碳原子最多有13个
B.的一氯代物有4种
C.乙二酸二乙酯与二乙酸乙二酯互为同分异构体
D.由2种单体经过加聚反应合成
4.下列有关高分子材料制备的说法错误的是
A.己二酸和己二胺发生缩聚反应生成尼龙66
B.一定条件下,乙烯和丙烯发生加聚反应合成塑料
C.苯酚和甲醛在一定条件下发生缩聚反应生成酚醛树脂
D.乳酸[CH3CH(OH)COOH]发生加聚反应合成可降解高分子材料
5.下列说法不正确的是
A.己烷共有4种同分异构体,它们的熔点、沸点各不相同
B.在一定条件下,苯分别与液溴、浓硝酸、浓硫酸作用生成溴苯、硝基苯、苯磺酸的反应都属于取代反应
C.的一氯代物有5种
D.聚合物()可由单体CH3CH=CH2和CH2=CH2加聚制得
6.某有机物的结构如图所示,1mol该有机物
A.最多可以与反应
B.最多可以与1molNaOH反应
C.可用酸性检验结构中的碳碳双键
D.与发生加成反应产物有4种
7.下列有关的说法不正确的是
A.该有机物的分子式为,1mol该有机物完全燃烧需消耗4molO2
B.该有机物能发生取代反应、加成反应、氧化反应、中和反应
C.该有机物分别与足量Na、NaOH、反应,生成物均为
D.该有机物分子内和分子间都能发生酯化反应
8.环氧化物与开环共聚反应是合成高附加值化学品的一种有效途径,两类共聚物的合成路线如下(副产物为环状碳酸酯)。下列说法不合理的是
A.有机化合物E的分子式为
B.高分子F和高分子G均能发生水解反应
C.由结构简式可以确定高分子G的相对分子质量比F的大
D.有机化合物E和通过加成反应生成副产物
9.金银花能提取出有很高药用价值的绿原酸(如图),下列说法错误的是
A.绿原酸的分子式为C16H18O9
B.1mol绿原酸最多能消耗NaOH 8 mol
C.绿原酸分子中含4个手性碳原子
D.能发生取代、加成、消去、缩聚、加聚反应
10.对甲氧基苯甲醛是调配山楂花香型的主体香料,还是医药上用作抗组胺药物的中间体。下列有关对甲氧基苯甲醛的说法不正确的是
A.分子式为C7H6O2
B.对甲氧基苯甲醛的一氯代物为3种
C.能使酸性高锰酸钾溶液褪色
D.1mol对甲氧基苯甲醛能和4mol氢气发生加成反应
11.化学与科学、技术、社会、环境密切相关。下列有关说法不正确的是
A.乙烯与氧气在银催化作用下生成环氧乙烷符合绿色化学的原子经济性要求
B.草莓棚中使用的“吊袋式二氧化碳气肥”的主要成分可以是碳酸钙
C.水暖器材中的PVC管常用作进水管,而PE管常用作出水管
D.用 CO2 合成聚碳酸酯可降解塑料,实现“碳”的循环利用
12.近年来我国取得了很多令世界瞩目的科技成果,化学功不可没。下列说法正确的是
A.神舟十三号载人飞船返回舱逃逸系统复合材料中的酚醛树脂属于天然高分子化合物
B.“北斗系统”组网成功,其芯片的主要成分为二氧化硅
C.“嫦娥五号”运载火箭用液氧、液氢做推进剂,产物对环境无污染
D.T-碳(T-Carbon)是中科院预言的一种三维碳结构晶体,其与C60互为同位素
13.某金属有机多孔材料(MOFA)在常温常压下对CO2具有超高的吸附能力,并能高效催化CO2与环氧乙烷衍生物的反应,其工作原理如图所示。下列说法错误的是
A.该材料的吸附作用具有选择性 B.若R为H,分子不可能为平面形结构
C.在生成的过程中,有键形成 D.CO2可用于有机物碳骨架的增长与构建
14.下列各组中两个变化所发生的反应,属于同一类型的是
①由甲苯制甲基环己烷与由乙烷制溴乙烷
②乙烯使溴水褪色与乙炔使酸性高锰酸钾水溶液褪色
③由乙烯制聚乙烯与由乙炔制聚乙炔
④由苯制硝基苯与由利用甲烷制备氯仿
A.只有①③ B.只有①④ C.只有②③ D.只有③④
二、填空题(共8题)
15.按要求回答下列问题:
(1)按系统命名法,的名称是 。
(2)与化合物互为同分异构体且一氯代物有两种的烃的结构简式为 。
(3)某烷烃分子的碳骨架结构为,若此烷烃为炔烃加氢制得,则此炔烃的结构简式为 。
(4)有机化合物A常用于食品行业。已知9.0gA在足量中充分燃烧,将生成的混合气体依次通过足量的浓硫酸和碱石灰,分别增加5.4g和13.2g,经检验剩余气体为。
①A分子的质谱图如图所示,则A的分子式是 。
②经红外光谱测定,已知A分子中含有羧基,A分子的核磁共振氢谱有4组吸收峰,且峰面积之比是1:1:1:3,则A的结构简式是 。
16.(1)根据核磁共振氢谱图可以确定有机物分子中氢原子的种类和数目。例如:乙醚的结构式为,其核磁共振氢谱中有2个信号(如下图)。
①下列分子中,其核磁共振氢谱中只有一种峰(信号)的物质是 (填字母)。
A.CH3-CH3 B.CH3COOH C.CH3COOCH3 D.CH3COCH3
②化合物A和B的分子式都是C2H4Br2,A的核磁共振氢谱如下图所示,则A的结构简式为 ,请预测B的核磁共振氢谱上有 个峰(信号)。
③用核磁共振氢谱的方法来研究C2H6O的结构,请简要说明根据核磁共振氢谱的结果来确定C2H6O分子结构的方法是 。
(2)有机物C常用于食品行业。已知9.0gC在足量O2中充分燃烧,将生成的混合气体依次通过足量的浓硫酸和碱石灰,分别增重5.4g和13.2g,经检验剩余气体为O2。
①C分子的质谱图如图所示,从图中可知其相对分子质量是 ,则C的分子式是 。
②C能与NaHCO3溶液发生反应,C一定含有的官能团名称是 。
③C分子的核磁共振氢谱有4个峰,峰面积之比是1:1:1:3,则C的结构简式是 。
17.香豆素—3—羧酸丹皮酚酯具有多种生物活性,结构简式为,用M表示,合成路线如图:
已知:丹皮酚的结构简式为。
已知:++R2OH。
请根据已学知识,写出以CH3OH和为原料(其它试剂任选)合成的路线 。
18.化学概念和用语是化学学科发展的基础,回答下列问题:
(1)有下列几组物质,请将序号填入下列空格内:
A.和油酸
B.和石墨
C.和
D.和
E.乙醇和乙二醇
①互为同位素的是 ;
②互为同系物的是 ;
③互为同素异形体的是 ;
④互为同分异构体的是 ;
⑤既不是同系物,又不是同分异体,也不是同素异形体,但可看成是同一类物质的是 。
(2)完成下列反应的化学方程式:
①乙醛与银氨溶液发生银镜反应: ;
②淀粉水解生成葡萄糖 ;
③向对甲基苯酚溶液中滴加饱和溴水: ;
④由丙烯制取聚丙烯: ;
⑤由己二酸和己二胺合成尼龙66(聚己二酰己二胺): 。
19.请填写下列空白:
(1)请写出支链只有一个乙基且式量最小的烷烃的结构简式: 在沥青中存在一系列结构相似的稠环芳香烃。这一系列化合物中的前三个同系物的结构简式如图所示。
(2)芘的分子式是
(3)这一系列有机物的通式可用含x的代数式来表示(x为自然数1,2,3,4…),则该通式为 。
(4)随着x值的增大,这一系列化合物含碳的质量分数的极限数值为 。(保留三位有效数字)
(5)环蕃A(cyclophane)和超蕃B(superphane)是一种光电信息材料,都属于烃(B中氢原子未画出),它们的结构如图所示。
下列有关说法正确的是 。
A.环蕃和超蕃互为同系物
B.环蕃能使酸性高锰酸钾溶液褪色
C.环蕃能与液溴、硝酸发生取代反应
超蕃的一氯取代物只有1种,二氯取代物有3种
20.按要求回答下列问题
(1)某烯烃在同温同压下蒸气的密度是密度42倍的烯烃,分子中所有碳原子一定在同一平面上,该烯烃的结构简式 该烯烃在一定条件下生成高分子化合物的化学方程式 ;
(2)系统命名为三甲基戊烯的结构简式 ;
(3)按系统命名法填写有机物的名称是
(4)的同分异构体数目为 种;
(5)乙烯使溴的四氯化碳溶液褪色的化学方程式为
(6)相对分子质量为的某烃的分子式
(7)1升乙炔和气态烯烃混合物与11升氧气混合后点燃,充分反应后,气体的体积为12升,(反应前后均为、),求:
①原1升混合气体中烯烃的可能的分子式
②乙炔和烯烃的物质的量之比
21.某烃经李比希元素分析实验测得碳的质量分数为85.71%,该烃的质谱图显示:分子离子峰的质荷比为70,该烃的核磁共振氢谱如下图所示。请确定该烃的
(1)实验式 ;
(2)分子式 ;
(3)结构简式 。
22.自20世纪90年代以来,稠环化合物的研究开发工作十分迅速,这一类物质在高科技领域有着十分广泛的应用前景。下面是苯和一系列稠环芳香烃的结构简式:
试解答下列问题:
(1)写出化合物②⑤的分子式:② ;⑤ ;
(2)这组化合物分子式的通式是:
(3)某课外兴趣小组,做了系列实验,他们将该系列的前5种芳香烃逐一加到浓的酸性高锰酸钾溶液中加热。结果发现,只有苯无明显变化,其余4种物质都能使酸性高锰钾溶
液褪色。经分析知后4种稠环芳烃的氧化产物是:、
或者两者都有。由此你能得出的结论是: ,
(4)甲、乙、丙三同学同做酸性高锰酸钾溶液氧化并五苯的实验。甲将氧化后的混合液酸化分离得到一种无色晶体X,称取0.2540g X,用热水配成100mL溶液中和滴定,取出25.00mL,用0.1000mol·L-1NaOH溶液中和滴定,滴到10.00mL时达到终点;丙用酸性高锰酸钾氧化并五苯,将氧化后的混合液酸化分离得到无色晶体Y,中和测定知Y的中和能力只有X的中和能力的一半;乙用酸性高锰钾溶液氧化并五苯,将氧化后的混合液酸化分离得无色晶体,经分析其中包含了甲与丙得的两种成分,通过计算推理确定X的结构简式 。
(5)在Y的同分异构体中与Y同属芳香族化合物既可看作羧酸类,又可看作酯类的同分异构体的结构简式有: ,
在Y的同分异构体中既不属于羧酸类,又不属于酯类,但可看作常见芳香烃的衍生物的同分异构体的结构简式有 (写一种)
试卷第1页,共3页
参考答案:
1.D
【详解】A.“白色污染”是指塑料污染,因此可降解聚乳酸塑料的推广应用可减少“白色污染”,故A说法正确;
B.有机高分子材料包括塑料、合成纤维、合成橡胶,芳纶纤维属于合成纤维,即属于有机高分子材料,故B说法正确;
C.碳纤维是碳单质,不属于有机物,故C说法正确;
D.脲醛树脂制成的塑料制品不能加热熔融,只能一次成型,是热固性,故D说法错误;
答案为D。
2.C
【详解】A.维生素C的分子式为,选项A错误;
B.维生素C的含氧官能团有羟基、酯基,选项B错误;
C.维生素C分子中含有大量的羟基,故易溶于水,选项C正确;
D.维生素C的碳碳双键和羟基能使酸性高锰酸钾溶液褪色,选项D错误。
答案选C。
3.C
【详解】A.中苯环和乙烯为平面型结构,而乙炔为直线形结构,则所有的碳原子有可能都在同一平面上,乙基中碳碳单键发生旋转,该分子中所有C原子都可以共面,即共平面的碳原子共14个。故A错误;
B.分子内等效氢为3种,则一氯代物有3种,故B错误;
C.乙二酸二乙酯与二乙酸乙二酯的分子式均为C6H10O4,且结构不同,互为同分异构体,故C正确;
D.高分子化合物是由3种单体经过加聚反应合成,故D错误;
答案为C。
4.D
【详解】A.工业上己二酸和已二胺以等摩尔比进行反应缩聚得到尼龙66 ,A正确;
B.乙烯、丙烯相互反应生成乙烯一丙烯共聚物塑料,是加聚反应,B正确;
C.苯酚在一定条件下能与甲醛发生缩聚反应生成酚醛树脂,C正确;
D.聚乳酸是一种新型绿色环保可降解的高分子材料,但乳酸生成聚乳酸是缩聚反应,D错误;
故答案为:D。
5.A
【详解】A.己烷共有5种同分异构体,即、、、、,故A错误;
B.在一定条件下,苯与液溴生成、苯与浓硝酸,在浓硫酸作用下反应生成硝基苯、苯与浓硫酸反应生成苯磺酸,都属于取代反应,故B正确;
C.有5种位置的氢即,其一氯代物有5种,故C正确;
D.聚合物()从左边第二个碳与第三个碳原子断碳碳键即,第一个碳和第二个碳形成双键,第三个和第四个碳形成双键,因此可由单体CH3CH=CH2和CH2=CH2加聚制得,故D正确。
综上所述,答案为A。
6.D
【详解】A.能与氢气发生反应的官能团为碳碳双键、醛基,1mol碳碳双键需要1mol氢气,1mol醛基需要1mol氢气,则1mol该有机物最多可与3molH2反应,A项错误;
B.能与NaOH溶液反应的官能团为酯基和羧基,则1mol该有机物最多与2molNaOH反应,B项错误;
C.该有机物能被酸性高锰酸钾氧化的官能团为醛基、羟基、碳碳双键,故不可用酸性高锰酸钾检验结构中的碳碳双键,C项错误;
D.与发生加成反应产物为、、、,反应产物有4种,D项正确;
答案选D。
7.C
【详解】A.该有机物的分子式为,1mol该有机物完全燃烧消耗的物质的量为4mol,选项A正确;
B.因该有机物含碳碳双键,能发生加成反应、氧化反应,含有羧基,能发生取代反应(酯化反应)和中和反应,选项B正确;
C.因该有机物同时含有羧基和羟基,该有机物与足量Na反应的产物应为,选项C错误;
D.因该有机物同时含有羧基和羟基,则该有机物分子内与分子间均能发生酯化反应,选项D正确。
答案选C。
8.C
【详解】A.有机化合物E的分子式为,A合理;
B.高分子F和高分子G均含有酯基,都能发生水解反应,B合理;
C.高分子F中的和高分子G中的的相对大小不确定,因此两者的相对分子质量不能比较大小,C不合理;
D.对比化合物E与环状碳酸酯的结构简式,可以确定化合物E与CO2是通过加成反应生成环状碳酸酯,D合理;
故选C。
9.B
【详解】A.根据绿原酸结构简式,结合C原子最外层有4个电子,可以形成4个共价键,可知其分子式为C16H18O9,A正确;
B.根据绿原酸结构简式可知:1个绿原酸分子中含有1个羧基、1个酯基和2个酚羟基可以与NaOH发生反应;酯基水解产生的羧基可以与NaOH反应,产生的醇羟基不能与NaOH反应,故1mol绿原酸最多能消耗4 mol 的NaOH,B错误;
C.结合4个不同原子或原子团的碳原子为手性碳原子,则与3个醇-OH相连的C及与酯基直接相连的六元环上的C为手性碳原子,因此物质分子中共有4个手性碳原子,C正确;
D.绿原酸分子中含有羟基和羧基及酯基,所以能发生取代反应;含有不饱和的碳碳双键,能够发生加成反应;由于与醇羟基连接的C原子的邻位C原子上含有H原子,能够发生消去反应;分子中含有羧基和羟基,能够发生缩聚反应;含有不饱和的碳碳双键,能够发生加聚反应,D正确;
故合理选项是B。
10.A
【详解】A.由图示结构简式可知,分子式为C8H8O2, A错误;
B.对甲氧基苯甲醛分子内有2种氢,故一氯代物为3种,B正确;
C.对甲氧基苯甲醛中含有醛基,能与新制氢氧化铜悬浊液、银氨溶液等反应,故能发生氧化反应,使酸性高锰酸钾溶液褪色,C正确;
D.1 mol对甲氧基苯甲醛含有1mol苯环能与3molH2加成,1mol醛基能与1molH2加成,故一共能和4 mol氢气发生加成反应,D正确;
答案为A。
11.B
【详解】A.乙烯与氧气在银催化作用下生成环氧乙烷,反应物全部转化为生成物,从理论、经济、环保以及操作等方面都很好,符合绿色化学的原子经济性要求,故A不选;
B.碳酸钙需要在高温下煅烧分解得到二氧化碳,草莓棚中不能使用碳酸钙来产生二氧化碳,故选B;
C.PVC是聚氯乙烯的简称,PVC中含有Cl在受热时会产生有毒有害的物质,所以常用作热水器的进水管,PE是聚乙烯的简称,PE无臭,无毒,具有优良的耐低温性能(最低使用温度可达-100~-70°C),化学稳定性好,能耐大多数酸碱的侵蚀(不耐具有氧化性质的酸),所以常用作热水器的出水管,故C不选;
D.用 CO2合成聚碳酸酯可降解塑料,节约资源,减少碳的排放,符合低碳经济要求,同时该塑料在讲解过程中又生成二氧化碳,能实现“碳”的循环利用,故D不选。
答案选B。
12.C
【详解】A.酚醛树脂是由人工合称的高分子材料,A错误;
B.芯片的主要成分为硅单质,二氧化硅主要用于制作光导纤维,B错误;
C.液氧、液氢反应可以放出大量的热,产物为水,对环境无污染,C正确;
D.T-碳(T-Carbon)和C60为碳元素形成的不同单质,互为同素异形体,不是同位素,D错误;
综上所述答案为C。
13.C
【详解】A.某金属有机多孔材料(MOFA)在常温常压下对CO2具有超高的吸附能力,该材料的吸附作用具有选择性,A正确;
B.该物质分子中含有的C原子为饱和C原子,具有甲烷的四面体结构,因此分子不可能是平面结构,B正确;
C.在由a生成b的过程中,需断裂CO2分子中的C=O中较活泼的键及a中的C-O键,同时形成新的C-O键,并没有键形成,C错误;
D.根据选项C分析可知:CO2在有机合成中,可用于有机物碳骨架的增长与构建,D正确;
故合理选项是C。
14.D
【详解】①由甲苯制甲基环己烷的反应为加成反应,由乙烷制溴乙烷的反应为取代反应,反应类型不相同,故不符合题意;
②乙烯使溴水褪色的反应为加成反应,乙炔使酸性高锰酸钾水溶液褪色的反应为氧化反应,反应类型不相同,故不符合题意;
③由乙烯制聚乙烯和由乙炔制聚乙炔的反应都为加聚反应,反应类型相同,故符合题意;
④由苯制硝基苯和由利用甲烷制备氯仿的反应都为取代反应,反应类型相同,故符合题意;
只有③④符合题意,故选D。
15.(1)3,4-二甲基己烷
(2)
(3)
(4)
【解析】(1)
主链有6个碳原子,第3、4号碳原子各有1个甲基,名称是3,4-二甲基己烷;
(2)
与化合物互为同分异构体且一氯代物有两种,说明分子中有2种等效氢,结构对称,符合条件的结构简式为。
(3)
某烷烃分子的碳骨架结构为,若此烷烃为炔烃加氢制得,根据C原子能形成4个共价键,此炔烃的结构简式为;
(4)
9.0gA在足量中充分燃烧,将生成的混合气体依次通过足量的浓硫酸和碱石灰,分别增加5.4g和13.2g ,说明反应生成5.4g水、13.2g二氧化碳,则9gA中含有H原子0.6mol、含有C原子0.3mol,含有氧原子,则A分子的实验式为CH2O,根据A分子的质谱图可知,A的相对分子质量为90,A的分子式是C3H6O3。
②经红外光谱测定,已知A分子中含有羧基,A分子的核磁共振氢谱有4组吸收峰,且峰面积之比是1:1:1:3,则A的结构简式是。
16. AD BrCH2CH2Br 2 通过其核磁共振氢谱中的峰信号可以判断有3个信号时,分子结构为CH3CH2OH;1个信号时分子结构为CH3-O-CH3 90 C3H6O3 羧基
【详解】(1)①核磁共振氢谱中只有一种峰,说明该分子中的H原子都是等效的,只有1种H原子,
A. CH3-CH3中6个H原子都是等效的,核磁共振氢谱中只有一种峰,故A选;
B. CH3COOH中甲基中的H原子与羧基中的H原子所处化学环境不同,CH3COOH有2种H原子,核磁共振氢谱中有2个峰,故B不选;
C. CH3COOCH3中甲基所处化学环境不同,甲基H原子不同,有2种H原子,核磁共振氢谱中有2个峰,故C不选;
D. CH3COCH3中2个甲基连在同一个羰基上,6个H原子都是等效的,核磁共振氢谱中只有一种峰,故D选;
故选AD;
②)由A的核磁共振氢谱可知,分子中只有一种H原子,A分子中2个Br原子连接不同的碳原子,故A的结构简式为BrCH2CH2Br,B与A互为同分异构体,B分子中2个Br原子连接在同一碳原子上,B为CH3CHBr2,分子中有2种H原子,故核磁共振氢谱图有2个峰;
③通过其核磁共振氢谱中的峰信号可以判断有3个信号时,分子结构为CH3CH2OH;1个信号时,分子结构为CH3-O-CH3;
(2)①由C分子的质谱图,可知C的相对分子质量为90,9g C的物质的量为,燃烧生成二氧化碳为,生成水为,则1个有机物分子中N(C)=、N(H)=,则分子中N(O)=,故有机物C的分子式为C3H6O3;
②C能与NaHCO3溶液发生反应,C一定含有羧基;
③有机物C的分子式为C3H6O3,含有羧基,C分子的核磁共振氢谱有4个吸收峰,说明含有4种H原子,峰面积之比是1:1:1:3,则4种H原子数目为1、1、1、3,则A的结构简式为:CH3CH(OH)COOH。
17.
【详解】被酸性高锰酸钾溶液氧化生成,和甲醇发生酯化反应生成,和反应生成,合成路线为:。
18.(1) D A B C E
(2)
【详解】(1)①质子数相同,中子数不同的原子互为同位素,互为同位素的是D.和;
②结构相似,组成上相差n个CH2原子团的有机物互为同系物,互为同系物的是A.和油酸;
③同种元素的不同单质互为同素异形体,互为同素异形体的是B.和石墨;
④分子式相同,结构不同的物质互为同分异构体,互为同分异构体的是C.和 ;
⑤既不是同系物,又不是同分异体,也不是同素异形体,但可看成是同一类物质的是E.乙醇和乙二醇,两者均为醇。
(2)①乙醛与银氨溶液发生银镜反应的化学方程式:;
②淀粉水解生成葡萄糖的化学方程式;
③向对甲基苯酚溶液中滴加饱和溴水的化学方程式:;
④由丙烯制取聚丙烯的化学方程式:;
⑤由己二酸和己二胺合成尼龙66(聚己二酰己二胺) 的化学方程式:。
19.(1)CH3CH2CH
(2)C16H10
(3)C(6x+4)H(2x+6)
(4)97.3%
(5)B、C
【详解】(1)支链只有一个乙基且式量最小的烷烃是3—乙基戊烷,结构简式为CH3CH2CH(CH2CH3)2。
(2)根据有机物的结构简式可知芘的分子式是C16H10。
(3)根据有机物的结构简式可知萘的分子式为C10H8,与芘的分子式相比少1个C6H2,所以这一系列有机物的通式如果用含x的代数式来表示,则该通式可表示为C(6x+4)H(2x+6)。
(4)随着x值的增大,这一系列化合物含碳的质量分数为 ,则其极限数值为 。
(5)A.根据二者的结构简式可知二者的结构不相似,且含有相同的碳原子数,因此环蕃和超蕃不能互为同系物,A错误;
B.环蕃分子中与苯环相连的碳原子含有氢原子,因此能使酸性高锰酸钾溶液褪色,B正确;
C.含有苯环,因此环蕃能与液溴、硝酸发生取代反应,C正确;
D.超蕃的一氯取代物只有2种,D错误;
答案选BC。
20.(1) n
(2)
(3)3-甲基-4-乙基辛烷
(4)5
(5)CH2=CH2+Br2→CH2Br-CH2Br
(6)C13H26
(7) C3H6 (或C4H8) 1:1 (或2:1)
【解析】(1)
某烯烃在同温同压下蒸气的密度是H2密度42倍,则烯烃相对分子质量为42×2=84,由,故烯烃分子式为C6H12,分子中所有碳原子一定在同一平面上,则烯烃为,该烯烃在一定条件下生成高分子化合物的化学方程式n;
(2)
2,3,3-三甲基-1-戊烯的结构简式为;
(3)
最长主链有8个碳原子,从距离甲基近的一定编碳号,甲基处于3号、乙基在4号碳原子上,编号为,其名称为3-甲基-4-乙基辛烷;
(4)
C6H14属于烷烃,其同分异构体有CH3(CH2)4CH3、CH3CH2CH2CH(CH3)2、CH3CH2CH(CH3)CH2CH3、、共5种;
(5)
乙烯与溴发生加成反应生成1,2-二溴乙烷,反应方程式为CH2=CH2+Br2→CH2Br-CH2Br;
(6)
分子中最大碳原子数目=,该烃的分子式为C13H26;
(7)
设该混合烃的平均分子组成为CxHy,则:
CxHy+(x+)O2 xCO2+H2O,△V=1+ x+-x-=-1,由△V=0,则-1=0,解得y=4,C2H2分子中氢原子个数为2,而混合烃的平均组成中氢原子个数为4,所以,烯烃中氢原子个数必大于4,又因为是气态烯烃,碳原子个数必小于或等于4,所以烯烃只能是C3H6或C4H8,若是C2H2、C3H6,设二者物质的量分别为xmol、ymol,则=4,整理可得x:y=1:1,若是C2H2、C4H8,设二者物质的量分别为amol、bmol,则=4,整理可得a:b=2:1,
①原1升混合气体中烯烃的可能的分子式:C3H6 (或C4H8);
②乙炔和烯烃的物质的量之比:1:1 (或2:1)。
21. CH2 C5H10
【详解】因分子离子峰的质荷比为70,则有该有机物的相对分子质量为70,分子中的碳原子数:=5,氢原子个数:=10,则其分子式为C5H10,实验式为CH2,由核磁共振氢谱图可得出该烃分子中只有一种化学环境下的氢原子,从而其结构简式为:,故答案为CH2、C5H10、 。
【点睛】本题主要展示了科学家确定有机物结构的一般流程,先确定有机物的元素组成,然后由相对分子质量确定有机物的分子式,最后通过核磁共振氢谱图等方法来确定有机物的结构。该烃的分子式为C5H10,而分子中只有一种氢原子,故分子中应该含有5个CH2原子团,从而推断该烃为环戊烷。
22.(1)
(2)
(3)苯很稳定,不能被高锰酸钾氧化
(4)
(5)
【分析】(1)根据有机物的结构简式可以写出各物质的分子式;
(2)根据以上五种有机物的分子式找出碳、氢原子数目的变化规律,从而找出通式;
(3)根据信息即可得出苯很稳定的结论;
(4)根据题给信息可知,后4种稠环芳烃的氧化产物是:、;甲将氧化后的混合液酸化分离得到一种无色晶体X的中和碱的能力是丙将氧化混合液酸化分离得到无色晶体Y中和碱的能力的2倍,且乙将氧化后的混合液酸化分离得无色晶体,经分析其中包含了甲与丙的两种成分,所以X的结构简式为,Y的结构简式为;
(5)根据Y的结构简式为;结合与Y互为同分异构体的条件,进行分析。
【详解】(1)根据有机物的结构简式可知,①② ③ ④ ⑤;答案:②;⑤;
(2)根据以上五种有机物的分子式可知,碳原子数相差4,氢原子数相差2个,因此这组化合物分子式的通式是:;答案:;
(3)前5种芳香烃逐一加到浓的酸性高锰酸钾溶液中加热,结果发现,只有苯无明显变化,其余4种物质都能使酸性高锰钾溶液褪色,这说明苯的结构很稳定,不能被高锰酸钾氧化;答案:苯很稳定,不能被高锰酸钾氧化;
(4)根据题给信息可知,后4种稠环芳烃的氧化产物是:、;甲将氧化后的混合液酸化分离得到一种无色晶体X的中和碱的能力是丙将氧化混合液酸化分离得到无色晶体Y中和碱的能力的2倍,且乙将氧化后的混合液酸化分离得无色晶体,经分析其中包含了甲与丙的两种成分,所以X的结构简式为,Y的结构简式为;甲实验中消耗氢氧化钠的量为;而X( )分子量为254;所以0.2540g X的物质的量为;1molX中含有,所以0.001molX消耗碱液0.004mol;符合题意转化关系。
答案:;
(5)结合以上分析可知,Y的结构简式为;与Y同属芳香族化合物既可看作羧酸类,又可看作酯类的同分异构体的结构简式有:,,;在Y的同分异构体中既不属于羧酸类,又不属于酯类,但可看作常见芳香烃的衍生物的同分异构体的结构简式有等;
答案:,,;
