第三章 物质在水溶液中的行为 (含答案)检测题 2023-2024学年上学期高二化学鲁科版(2019)选择性必修1
文档属性
| 名称 | 第三章 物质在水溶液中的行为 (含答案)检测题 2023-2024学年上学期高二化学鲁科版(2019)选择性必修1 |  | |
| 格式 | docx | ||
| 文件大小 | 597.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-12-11 08:23:29 | ||
图片预览



文档简介
第三章《物质在水溶液中的行为》检测题
一、单选题(共20题)
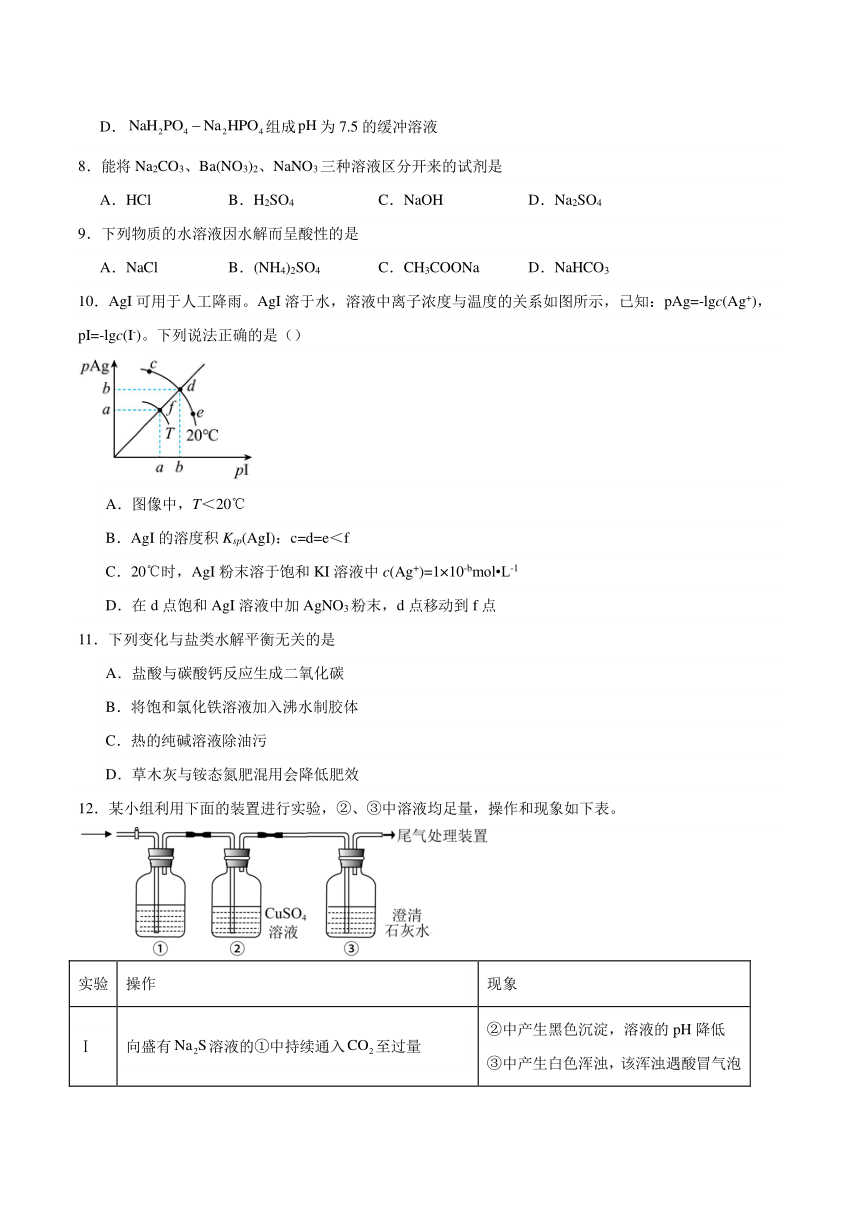
1.将打磨后的镁条放入盛有50 mL蒸馏水的烧杯后,用pH传感器和浊度传感器监测溶液中pH和溶液浊度随时间的变化如图。下列有关描述错误的是
A.该实验进行的温度高于常温
B.实线表示溶液浊度随时间的变化
C.150 s时向溶液中滴入酚酞试液,溶液变浅红色
D.150 s~250 s溶液浊度下降是因为生成的Mg(OH)2沉降
2.某研究小组利用电位滴定法研究盐酸滴加亚磷酸钠溶液过程中的化学变化,得到电极电位U和溶液pH随盐酸滴加的体积变化曲线如图所示。下列说法不正确的是
[已知:①电位滴定法的原理:在化学计量点附近,被测离子浓度发生突跃,指示电极电位也发生了突跃,进而确定滴定终点。②亚磷酸是二元弱酸,其电离常数分别是,]
A.a点对应溶液的溶质为和,
B.第二次电极电位突跃发生的化学反应为:
C.c点对应的溶液中可能存在:
D.水的电离程度:a>b
3.室温下,用0.5mol·L-1Na2CO3溶液浸泡CaSO4粉末,一段时间后过滤,向滤渣中加稀醋酸,产生气泡。已知Ksp(CaSO4)=5×10-5,Ksp(CaCO3)=3×10-9。下列说法正确的是
A.0.5mol·L-1Na2CO3溶液中存在c(Na+)=c(CO)+c(HCO)+c(H2CO3)
B.反应CaSO4+COCaCO3+SO正向进行,需满足>×104
C.过滤后所得清液中一定存在c(Ca2+)=且c(Ca2+)≤
D.滤渣中加入稀醋酸发生反应的离子方程式为CaCO3+2H+=Ca2++CO2↑+H2O
4.时水的电离达到平衡:,下列叙述不正确的是
A.将水加热,增大,减小
B.向水中加入少量硫酸氢钠固体,增大
C.某溶液中由水电离出的氢离子浓度为,则该溶液一定显碱性
D.向水中滴入少量溶液,平衡逆向移动,降低
5.25℃时,下列各组离子能大量共存的是
A.的水溶液中:、、、
B.能使紫色石蕊试剂变红的水溶液中:、、、
C.水电离出的的水溶液中:、、、
D.的水溶液中:、、、
6.将0.1mol明矾溶于水形成100mL溶液,以下说法正确的是( )
A.明矾净水是利用了明矾的强氧化性
B.溶液的焰色反应为紫色,这是化学性质
C.加入Ba(OH)2溶液至沉淀物质的量达到最大,消耗Ba(OH)2溶液0.2mol
D.加入Ba(OH)2溶液至SO42-恰好完全沉淀,Al3+全部转化为AlO2-
7.下列物质的应用过程中不涉及盐类水解的是
A.小苏打用作食品膨松剂
B.硫酸铝钾作净水剂
C.热碱水清洗厨房里的油污
D.组成为7.5的缓冲溶液
8.能将Na2CO3、Ba(NO3)2、NaNO3三种溶液区分开来的试剂是
A.HCl B.H2SO4 C.NaOH D.Na2SO4
9.下列物质的水溶液因水解而呈酸性的是
A.NaCl B.(NH4)2SO4 C.CH3COONa D.NaHCO3
10.AgI可用于人工降雨。AgI溶于水,溶液中离子浓度与温度的关系如图所示,已知:pAg=-lgc(Ag+),pI=-lgc(I-)。下列说法正确的是()
A.图像中,T<20℃
B.AgI的溶度积Ksp(AgI):c=d=e<f
C.20℃时,AgI粉末溶于饱和KI溶液中c(Ag+)=1×10-bmol L-1
D.在d点饱和AgI溶液中加AgNO3粉末,d点移动到f点
11.下列变化与盐类水解平衡无关的是
A.盐酸与碳酸钙反应生成二氧化碳
B.将饱和氯化铁溶液加入沸水制胶体
C.热的纯碱溶液除油污
D.草木灰与铵态氮肥混用会降低肥效
12.某小组利用下面的装置进行实验,②、③中溶液均足量,操作和现象如下表。
实验 操作 现象
Ⅰ 向盛有溶液的①中持续通入至过量 ②中产生黑色沉淀,溶液的pH降低 ③中产生白色浑浊,该浑浊遇酸冒气泡
Ⅱ 向盛有溶液的①中持续通入气体至过量 现象同实验Ⅰ
资料:CaS遇水完全水解
由上述实验得出的结论不正确的是
A.③中白色浑浊不可能是CaS
B.②中由于酸性,发生反应:
C.实验Ⅱ的①中过量发生的反应是:
D.由实验Ⅰ和Ⅱ不能比较和酸性的强弱
13.下列表述正确的个数是
①碳纳米管(具有纳米尺度的直径)、氢氧化铁胶体、淀粉溶液均为胶体
②只能表示强酸强碱稀溶液生成可溶性盐和水的反应
③强电解质的导电能力比弱电解质强
④金属原子失电子数越多,还原性越强,故还原性
⑤是碱性氧化物,因此可以和水反应生成对应的碱
⑥长期置于空气中,最终产物是
⑦燃烧一定是氧化还原反应
A.1个 B.2个 C.3个 D.4个
14.常温下,0.1mol L-1一元酸HA溶液中c(OH-)/c(H+)=1×10-6,下列叙述正确的是( )
A.该溶液中水的离子积常数为1×10 12
B.该一元酸溶液的pH=1
C.该溶液中由水电离出的c(H+)=1×10 6mol L-1
D.向该溶液中加入一定量NaA晶体或加水稀释,溶液中c(OH-)均增大
15.已知25℃时,几种弱酸的电离平衡常数如下:
:,
:,
:,,
则以下反应不能自发进行的是
A.
B.
C.
D.
16.下列物质中,属于强电解质的是
A.硫酸钠 B.盐酸 C.二氧化硫 D.一水合氨
17.向吸收液中通入过量的制备无水的主要流程如下,通入所引起的溶液体积变化和挥发可忽略,下列说法不正确的是
A.母液中:
B.中和后的溶液中:
C.吸收过程中有气体产生
D.溶液中:
18.下列各组气体在通常情况下既能用浓硫酸干燥又能用碱石灰干燥的是( )
A.、、 B.HCl、、
C.、、CO D.、、
19.对于下列实验,其离子方程式描述错误的是
A.稀硝酸中加入少量铁粉:
B.将足量溶液滴入浊液中:
C.通入冷的KOH溶液中:
D.溶液中加入少量溶液:
20.如图是用于干燥、收集并吸收多余气体的装置,下列方案正确的是
选项 X 收集气体 Y
A 碱石灰 氯化氢 水
B 浓硫酸 氯化氢 氢氧化钠
C 碱石灰 氯气 水
D 无水氯化钙 氯气 氢氧化钠
A.A B.B C.C D.D
二、非选择题(共5题)
21.和都是重要的化工产品,均可应用于造纸业。
(1)溶液的,用离子方程式表示原因 。
(2)某小组同学用如图所示装置探究饱和和溶液混合反应的实验。打开分液漏斗活塞向烧瓶中加入饱和溶液,产生大量的白色胶状沉淀。反应的离子方程式是 。
(3)已知在常温下测得浓度均为的下列5种溶液的:
溶质
8.8 9.7 11.6 10.3 11.1
判断下列反应不能成立的是 (填编号)。
A.
B.
C.
D.
(4)亚磷酸()是中强酸,它与足量的溶液反应生成。试回答下列问题:
①中元素在周期表中的位置为 。
②是 (填“正盐”或者“酸式盐”)。
22.在NH4Cl溶液中加入稀HNO3,能抑制NH水解。(_______)
23.I.某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选择甲基橙作指示剂。请填写下列空白:
(1)在中和滴定的过程中有如下操作:①用标准盐酸润洗滴定管 ②往滴定管内注入标准盐酸溶液 ③检查滴定管是否漏水 ④滴定,则在操作过程中正确的顺序是 (写序号)
(2)在滴定时,左手把握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视 ;滴定终点的判定依据是 。
(3)下列操作中可能使所测氢氧化钠溶液的浓度数值偏低的是 。
A.酸式滴定管未用标准盐酸溶液润洗就直接注入标准盐酸溶液
B.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
II.[Cu(NH3)4]2+在实验室中制备方法如下:向盛有硫酸铜水溶液的试管里加入氨水,首先形成蓝色沉淀,继续添加氨水,沉淀溶解,得到深蓝色的透明溶液。
(4)请写出蓝色沉淀溶解得到深蓝色溶液的离子方程式 。
(5)[Cu(NH3)4]2+中的配体为 ,提供孤电子对的配位原子是 。
24.A、B、C、D是短周期元素形成的四种气体单质,甲、乙、丙、丁是化合物,其中化合物乙是离子晶体,D元素的原子最外层电子数是次外层的3倍,C的氧化性比D强,它们的转化关系如图所示(它们的生成物均给出,反应条件略去)。
(1)写出分子式:A 、B 、
C 、D ;
(2)写出乙的阴离子水解的离子方程式: ;
(3)写出反应①、②化学方程式:① 、② ;
(4)举出实例说明单质C比D氧化性强(用化学方程式表示): 。
(5)A、C、D与B反应生成的氢化物的沸点由高到低的顺序是 。
25.某强酸性溶液X中仅含有NH、Al3+、Ba2+、Fe2+、Fe3+、CO、SO、SO、Cl-、NO中的一种或几种,取该溶液进行连续实验,实验过程如下:
下列有关推断合理的是
A.根据上述连续实验不能确定溶液X中是否含有Fe3+
B.沉淀H为Al(OH)3、BaCO3的混合物
C.溶液中一定含有H+、Al3+、NH、Fe2+、SO、Cl-
D.若溶液X为100 mL,产生的气体A为112 mL(标况),则X中c(Fe2+)=0.05 mol·L-1
参考答案:
1.B 2.C 3.C 4.C 5.B 6.D 7.A 8.B 9.B 10.B 11.A 12.B 13.B 14.D 15.B 16.A 17.B 18.C 19.A 20.D
21. ClO-+H2OHClO+OH- Al3++3ClO-+3H2O=Al(OH)3↓+3HClO A 第三周期第ⅤA族 正盐
22.正确
23. ③①②④ 锥形瓶内溶液颜色变化 滴最后一滴盐酸时,溶液由黄色变成橙色且30秒内不变色 D Cu(OH)2+4NH3·H2O=[Cu(NH3)4]2++2OH-+4H2O NH3 N
24. N2 H2 F2 O2 F+H2OHF+OH 8NH3+3F2= 6NH4F+N2 4NH3+5O24NO+6H2O 2F2+2H2O = 4HF+O2 H2O>HF>NH3
25.A
一、单选题(共20题)
1.将打磨后的镁条放入盛有50 mL蒸馏水的烧杯后,用pH传感器和浊度传感器监测溶液中pH和溶液浊度随时间的变化如图。下列有关描述错误的是
A.该实验进行的温度高于常温
B.实线表示溶液浊度随时间的变化
C.150 s时向溶液中滴入酚酞试液,溶液变浅红色
D.150 s~250 s溶液浊度下降是因为生成的Mg(OH)2沉降
2.某研究小组利用电位滴定法研究盐酸滴加亚磷酸钠溶液过程中的化学变化,得到电极电位U和溶液pH随盐酸滴加的体积变化曲线如图所示。下列说法不正确的是
[已知:①电位滴定法的原理:在化学计量点附近,被测离子浓度发生突跃,指示电极电位也发生了突跃,进而确定滴定终点。②亚磷酸是二元弱酸,其电离常数分别是,]
A.a点对应溶液的溶质为和,
B.第二次电极电位突跃发生的化学反应为:
C.c点对应的溶液中可能存在:
D.水的电离程度:a>b
3.室温下,用0.5mol·L-1Na2CO3溶液浸泡CaSO4粉末,一段时间后过滤,向滤渣中加稀醋酸,产生气泡。已知Ksp(CaSO4)=5×10-5,Ksp(CaCO3)=3×10-9。下列说法正确的是
A.0.5mol·L-1Na2CO3溶液中存在c(Na+)=c(CO)+c(HCO)+c(H2CO3)
B.反应CaSO4+COCaCO3+SO正向进行,需满足>×104
C.过滤后所得清液中一定存在c(Ca2+)=且c(Ca2+)≤
D.滤渣中加入稀醋酸发生反应的离子方程式为CaCO3+2H+=Ca2++CO2↑+H2O
4.时水的电离达到平衡:,下列叙述不正确的是
A.将水加热,增大,减小
B.向水中加入少量硫酸氢钠固体,增大
C.某溶液中由水电离出的氢离子浓度为,则该溶液一定显碱性
D.向水中滴入少量溶液,平衡逆向移动,降低
5.25℃时,下列各组离子能大量共存的是
A.的水溶液中:、、、
B.能使紫色石蕊试剂变红的水溶液中:、、、
C.水电离出的的水溶液中:、、、
D.的水溶液中:、、、
6.将0.1mol明矾溶于水形成100mL溶液,以下说法正确的是( )
A.明矾净水是利用了明矾的强氧化性
B.溶液的焰色反应为紫色,这是化学性质
C.加入Ba(OH)2溶液至沉淀物质的量达到最大,消耗Ba(OH)2溶液0.2mol
D.加入Ba(OH)2溶液至SO42-恰好完全沉淀,Al3+全部转化为AlO2-
7.下列物质的应用过程中不涉及盐类水解的是
A.小苏打用作食品膨松剂
B.硫酸铝钾作净水剂
C.热碱水清洗厨房里的油污
D.组成为7.5的缓冲溶液
8.能将Na2CO3、Ba(NO3)2、NaNO3三种溶液区分开来的试剂是
A.HCl B.H2SO4 C.NaOH D.Na2SO4
9.下列物质的水溶液因水解而呈酸性的是
A.NaCl B.(NH4)2SO4 C.CH3COONa D.NaHCO3
10.AgI可用于人工降雨。AgI溶于水,溶液中离子浓度与温度的关系如图所示,已知:pAg=-lgc(Ag+),pI=-lgc(I-)。下列说法正确的是()
A.图像中,T<20℃
B.AgI的溶度积Ksp(AgI):c=d=e<f
C.20℃时,AgI粉末溶于饱和KI溶液中c(Ag+)=1×10-bmol L-1
D.在d点饱和AgI溶液中加AgNO3粉末,d点移动到f点
11.下列变化与盐类水解平衡无关的是
A.盐酸与碳酸钙反应生成二氧化碳
B.将饱和氯化铁溶液加入沸水制胶体
C.热的纯碱溶液除油污
D.草木灰与铵态氮肥混用会降低肥效
12.某小组利用下面的装置进行实验,②、③中溶液均足量,操作和现象如下表。
实验 操作 现象
Ⅰ 向盛有溶液的①中持续通入至过量 ②中产生黑色沉淀,溶液的pH降低 ③中产生白色浑浊,该浑浊遇酸冒气泡
Ⅱ 向盛有溶液的①中持续通入气体至过量 现象同实验Ⅰ
资料:CaS遇水完全水解
由上述实验得出的结论不正确的是
A.③中白色浑浊不可能是CaS
B.②中由于酸性,发生反应:
C.实验Ⅱ的①中过量发生的反应是:
D.由实验Ⅰ和Ⅱ不能比较和酸性的强弱
13.下列表述正确的个数是
①碳纳米管(具有纳米尺度的直径)、氢氧化铁胶体、淀粉溶液均为胶体
②只能表示强酸强碱稀溶液生成可溶性盐和水的反应
③强电解质的导电能力比弱电解质强
④金属原子失电子数越多,还原性越强,故还原性
⑤是碱性氧化物,因此可以和水反应生成对应的碱
⑥长期置于空气中,最终产物是
⑦燃烧一定是氧化还原反应
A.1个 B.2个 C.3个 D.4个
14.常温下,0.1mol L-1一元酸HA溶液中c(OH-)/c(H+)=1×10-6,下列叙述正确的是( )
A.该溶液中水的离子积常数为1×10 12
B.该一元酸溶液的pH=1
C.该溶液中由水电离出的c(H+)=1×10 6mol L-1
D.向该溶液中加入一定量NaA晶体或加水稀释,溶液中c(OH-)均增大
15.已知25℃时,几种弱酸的电离平衡常数如下:
:,
:,
:,,
则以下反应不能自发进行的是
A.
B.
C.
D.
16.下列物质中,属于强电解质的是
A.硫酸钠 B.盐酸 C.二氧化硫 D.一水合氨
17.向吸收液中通入过量的制备无水的主要流程如下,通入所引起的溶液体积变化和挥发可忽略,下列说法不正确的是
A.母液中:
B.中和后的溶液中:
C.吸收过程中有气体产生
D.溶液中:
18.下列各组气体在通常情况下既能用浓硫酸干燥又能用碱石灰干燥的是( )
A.、、 B.HCl、、
C.、、CO D.、、
19.对于下列实验,其离子方程式描述错误的是
A.稀硝酸中加入少量铁粉:
B.将足量溶液滴入浊液中:
C.通入冷的KOH溶液中:
D.溶液中加入少量溶液:
20.如图是用于干燥、收集并吸收多余气体的装置,下列方案正确的是
选项 X 收集气体 Y
A 碱石灰 氯化氢 水
B 浓硫酸 氯化氢 氢氧化钠
C 碱石灰 氯气 水
D 无水氯化钙 氯气 氢氧化钠
A.A B.B C.C D.D
二、非选择题(共5题)
21.和都是重要的化工产品,均可应用于造纸业。
(1)溶液的,用离子方程式表示原因 。
(2)某小组同学用如图所示装置探究饱和和溶液混合反应的实验。打开分液漏斗活塞向烧瓶中加入饱和溶液,产生大量的白色胶状沉淀。反应的离子方程式是 。
(3)已知在常温下测得浓度均为的下列5种溶液的:
溶质
8.8 9.7 11.6 10.3 11.1
判断下列反应不能成立的是 (填编号)。
A.
B.
C.
D.
(4)亚磷酸()是中强酸,它与足量的溶液反应生成。试回答下列问题:
①中元素在周期表中的位置为 。
②是 (填“正盐”或者“酸式盐”)。
22.在NH4Cl溶液中加入稀HNO3,能抑制NH水解。(_______)
23.I.某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选择甲基橙作指示剂。请填写下列空白:
(1)在中和滴定的过程中有如下操作:①用标准盐酸润洗滴定管 ②往滴定管内注入标准盐酸溶液 ③检查滴定管是否漏水 ④滴定,则在操作过程中正确的顺序是 (写序号)
(2)在滴定时,左手把握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视 ;滴定终点的判定依据是 。
(3)下列操作中可能使所测氢氧化钠溶液的浓度数值偏低的是 。
A.酸式滴定管未用标准盐酸溶液润洗就直接注入标准盐酸溶液
B.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
II.[Cu(NH3)4]2+在实验室中制备方法如下:向盛有硫酸铜水溶液的试管里加入氨水,首先形成蓝色沉淀,继续添加氨水,沉淀溶解,得到深蓝色的透明溶液。
(4)请写出蓝色沉淀溶解得到深蓝色溶液的离子方程式 。
(5)[Cu(NH3)4]2+中的配体为 ,提供孤电子对的配位原子是 。
24.A、B、C、D是短周期元素形成的四种气体单质,甲、乙、丙、丁是化合物,其中化合物乙是离子晶体,D元素的原子最外层电子数是次外层的3倍,C的氧化性比D强,它们的转化关系如图所示(它们的生成物均给出,反应条件略去)。
(1)写出分子式:A 、B 、
C 、D ;
(2)写出乙的阴离子水解的离子方程式: ;
(3)写出反应①、②化学方程式:① 、② ;
(4)举出实例说明单质C比D氧化性强(用化学方程式表示): 。
(5)A、C、D与B反应生成的氢化物的沸点由高到低的顺序是 。
25.某强酸性溶液X中仅含有NH、Al3+、Ba2+、Fe2+、Fe3+、CO、SO、SO、Cl-、NO中的一种或几种,取该溶液进行连续实验,实验过程如下:
下列有关推断合理的是
A.根据上述连续实验不能确定溶液X中是否含有Fe3+
B.沉淀H为Al(OH)3、BaCO3的混合物
C.溶液中一定含有H+、Al3+、NH、Fe2+、SO、Cl-
D.若溶液X为100 mL,产生的气体A为112 mL(标况),则X中c(Fe2+)=0.05 mol·L-1
参考答案:
1.B 2.C 3.C 4.C 5.B 6.D 7.A 8.B 9.B 10.B 11.A 12.B 13.B 14.D 15.B 16.A 17.B 18.C 19.A 20.D
21. ClO-+H2OHClO+OH- Al3++3ClO-+3H2O=Al(OH)3↓+3HClO A 第三周期第ⅤA族 正盐
22.正确
23. ③①②④ 锥形瓶内溶液颜色变化 滴最后一滴盐酸时,溶液由黄色变成橙色且30秒内不变色 D Cu(OH)2+4NH3·H2O=[Cu(NH3)4]2++2OH-+4H2O NH3 N
24. N2 H2 F2 O2 F+H2OHF+OH 8NH3+3F2= 6NH4F+N2 4NH3+5O24NO+6H2O 2F2+2H2O = 4HF+O2 H2O>HF>NH3
25.A
同课章节目录
- 第1章 化学反应与能量转化
- 第1节 化学反应的热效应
- 第2节 化学能转化为电能——电池
- 第3节 电能转化为化学能——电解
- 第4节 金属的腐蚀与防护
- 微项目 设计载人航天器用化学电池与氧气再生方案——化学反应中能量及物质的转化利用
- 第2章 化学反应的方向、 限度与速率
- 第1节 化学反应的方向
- 第2节 化学反应的限度
- 第3节 化学反应的速率
- 第4节 化学反应条件的优化——工业合成氨
- 微项目 探讨如何利用工业废气中的二氧化碳合成甲醇——化学反应选择与反应条件优化
- 第3章 物质在水溶液中的行为
- 第1节 水与水溶液
- 第2节 弱电解质的电离 盐类的水解
- 第3节 沉淀溶解平衡
- 第4节 离子反应
- 微项目 揭秘索尔维制碱法和侯氏制碱法——化学平衡思想的创造性应用
