3.1 课时1 铁的单质 课件(共22张PPT) 2023-2024学年高一化学人教版(2019)必修一
文档属性
| 名称 | 3.1 课时1 铁的单质 课件(共22张PPT) 2023-2024学年高一化学人教版(2019)必修一 |  | |
| 格式 | pptx | ||
| 文件大小 | 21.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-12-11 11:07:44 | ||
图片预览







文档简介
(共22张PPT)
埃菲尔铁塔
港珠澳大桥
地铁管道
第一节 铁及其化合物 课时1
第三章 铁 金属材料
1.了解铁元素在自然界中的存在形态、与人体健康的关系,体会化学对人类生活的重要意义。
2.能用氧化还原反应原理进一步认识铁的化学性质。
3.基于实验事实写出铁与水蒸气反应的化学方程式,并用于解释生产中简单的化学问题,培养安全意识。
知识点一:铁在自然界中的存在形态
人类最早使用的铁,是来自太空的陨铁。铁在自然界中可以像陨铁中的铁那样以单质形态存在,但主要是以+2价和+3价化合物的形态存在于矿石中。
陨铁
赤铁矿Fe2O3
磁铁矿Fe3O4
自然界有金属钠单质吗?
没有,钠的金属活动性强
为什么自然界有铁单质?
铁的金属活动性弱
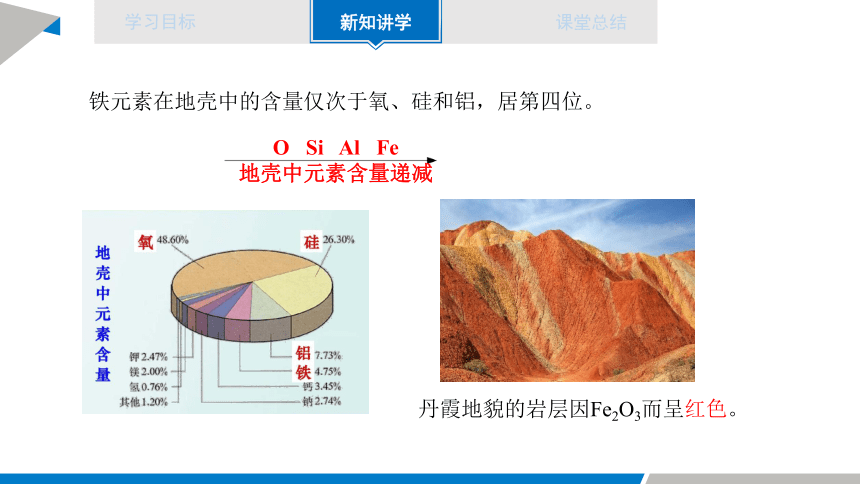
铁元素在地壳中的含量仅次于氧、硅和铝,居第四位。
O Si Al Fe
地壳中元素含量递减
丹霞地貌的岩层因Fe2O3而呈红色。
战国铁剑
打铁炉
战国铁炉
我国从很早之前就掌握了冶铁技术
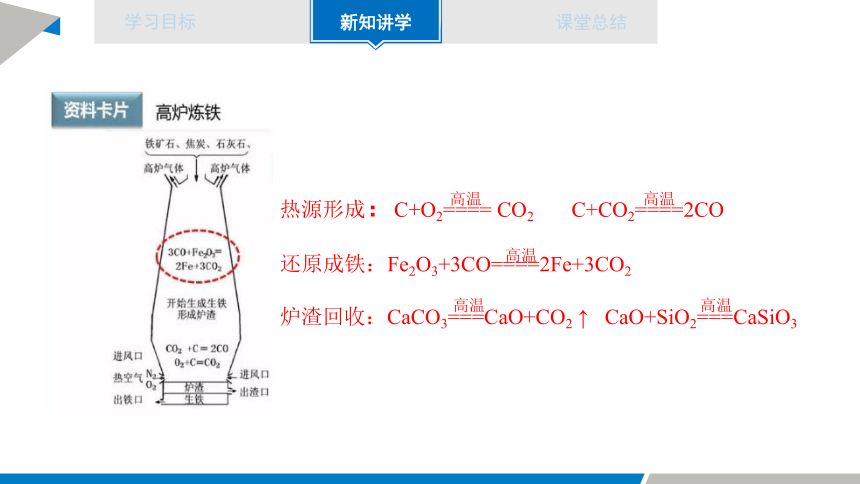
你还记得高炉炼铁的化学反应吗?
还原成铁:Fe2O3+3CO====2Fe+3CO2
高温
高温
高温
热源形成:C+O2==== CO2 C+CO2====2CO
高温
高温
炉渣回收:CaCO3===CaO+CO2 ↑ CaO+SiO2===CaSiO3
知识点二:铁的单质
1.铁的物理性质
颜色 状态 金属通性 熔点 沸点 密度 特性
银白色,有金属光泽 固体 导电性、导热性、延展性 1535℃ 2750℃ 7.86g/cm3 易被磁铁吸引
铁块(银白色)
铁粉(黑色)
2.铁的化学性质
想一想我们学过铁与哪些物质的反应?写出这些反应的化学方程式。
(2)非氧化性酸的反应(如:HCl等)
Fe+2H+=Fe2++H2↑
(3)与盐溶液的反应(如:CuSO4等)
Fe+Cu2+=Fe2++Cu
【思考·讨论】上述反应中,铁化合价有什么异同?为什么有这样的异同?
(1) 与非金属单质的反应(如:O2、Cl2等)
2Fe+3Cl2 2FeCl3
3Fe+4O2 Fe3O4
Fe+S FeS
加热
Fe
FeCl3
化合价升高
0
+3
铁与氯气的反应:
铁与盐酸溶液的反应:
Fe
FeCl2
化合价升高
0
+2
铁与硫酸铜溶液的反应:
Fe
FeSO4
化合价升高
0
+2
Fe - 2e- = Fe2+
Fe - 3e- = Fe3+
Fe与弱氧化剂(如盐酸、硫酸铜等)的反应,铁失去两个电子,生成Fe2+
Fe与强氧化剂(氯气等)的反应,铁失去三个电子,生成Fe3+
下列物质反应后一定有+3价铁生成的是( )
①过量的Fe与Cl2反应
②Fe与过量稀硫酸反应
③ FeCl2溶液中通入少量Cl2
④ Fe和Fe2O3的混合物溶于盐酸中
A.只有① B.①③ C.①②③ D.全部
练一练
B
炽热的铁水倒入模具中
在钢铁厂的生产中,炽热的钢水或者铁水注入模具之前,模具必须进行充分的干燥处理,不得留有水。这是为什么呢?
因为铁会在高温下与水发生反应
反应生成了什么?
3.铁与水蒸气反应
视频
(1)实验现象:
(2)反应方程式:
铁粉逐渐红热,生成黑色固体
气泡破裂,气体燃烧,发出轻微爆鸣声
3Fe+4H2O(g)==== Fe3O4+4H2
高温
(3)装置分析
棉花的作用是什么?
肥皂泡的作用是什么?
棉花的作用是在受热时提供反应所需的水蒸气。
肥皂泡的作用是为了储存气体,方便检验产物。
可以提高加热温度。
为什么酒精灯的火焰用防风罩罩住?
①试管口略向下倾斜;
④结束时,先撤导管,再移酒精灯。
②酒精灯先加热湿棉花,有水蒸气后,再点燃酒精灯加热还原铁粉;
③加热一会后再将导管插入到肥皂水中;
(4)实验注意事项
4.金属与水反应的一般规律
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
金属性越强,常温下与水反应越剧烈
(1)活泼金属K、Na等可与冷水迅速剧烈反应(放热),生成可溶性碱与H2。
(2)Mg与冷水反应缓慢,但在加热条件(或沸水),Mg与水的反应加快。
(3)Fe、Zn等可以与水蒸气反应生成金属氧化物和H2。
(4)Cu、Hg、Ag、Pt、Au不与水反应。
1.下列关于铁与水蒸气反应的说法中不正确的是( )
A.反应中有氢气产生
B.此反应需在高温下才能发生
C.生成的铁的化合物中铁全部呈+3价
D.该反应中水作氧化剂
练一练
C
2.在玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气。用试管收集产生的经过干燥的气体,并靠近火焰点燃。
a.实验现象是红热的铁与水蒸气反应,
放出气体,这种气体点燃时能燃烧
且发出爆鸣声,有关反应的化学
方程式是_____________________________。
b.干燥管内可装入的试剂是____________________________,
其作用是 ,使收集的氢气易点燃。
c.玻璃管中石棉绒是作为铁粉的载体,其目的是__ ________ ____;
实验开始时应先点燃 处酒精灯,实验结束时应先熄灭 处酒精灯。
3Fe+4H2O(g) ====Fe3O4+4H2
高温
碱石灰(或无水CaCl2、硅胶等)
吸收水蒸气
增大铁粉与水蒸气的接触面积
A
B
缺铁性贫血(IDA)
红细胞中含有血红蛋白,而血红蛋白的作用是运输氧气,亚铁离子是血红蛋白的组成成分之一。
01
缺铁性贫血比较明显的表现就是口唇、眼结膜、甲床等颜色发白,同时会有心慌、乏力、头晕、注意力不集中、食欲减退、耳鸣、心悸、气促等症状。
03
人体对铁的摄入量不足,便会影响到血红蛋白的合成,从而使红细胞中血红蛋白的含量显著减少,随之红细胞数目就减少。会使人体内的各细胞、组织供氧不足,将导致缺铁性贫血症。
02
知识扩展
生活中的铁元素
动物内脏、红肉(猪肉、牛肉、羊肉等)、鱼类和蛋类食物
01
必要时可服用补铁剂来达到铁元素的适宜摄入量
03
铁强化酱油也可以补充日常所需的铁元素
02
补铁剂
目前常用的铁剂有硫酸亚铁、富马酸亚铁、乳酸亚铁等,乳酸亚铁属于有机铁剂,吸收不消耗胃酸,不会对肠胃有刺激性。
01
铁剂不能与咖啡、浓茶同服。服用铁剂期间,那是因为茶和咖啡里含有丰富的鞣酸,这种物质和铁会生成一种不溶性的铁质沉淀,从而阻碍铁的吸收。
03
铁剂不能和抗酸药一起服用。不能同时服用铁剂和抗酸药,因为抗酸药属于碱性药物,同时服用会影响铁质吸收。
02
铁单质
物理性质
化学性质
银白色固体、有延展性
熔、沸点高;导电、导热
与氯气反应:2Fe+3Cl2 ======2FeCl3
与水蒸汽反应:3Fe+4H2O(g)==== Fe3O4+4H2
能被磁铁吸引
高温
与硫反应:Fe+S ======FeS
埃菲尔铁塔
港珠澳大桥
地铁管道
第一节 铁及其化合物 课时1
第三章 铁 金属材料
1.了解铁元素在自然界中的存在形态、与人体健康的关系,体会化学对人类生活的重要意义。
2.能用氧化还原反应原理进一步认识铁的化学性质。
3.基于实验事实写出铁与水蒸气反应的化学方程式,并用于解释生产中简单的化学问题,培养安全意识。
知识点一:铁在自然界中的存在形态
人类最早使用的铁,是来自太空的陨铁。铁在自然界中可以像陨铁中的铁那样以单质形态存在,但主要是以+2价和+3价化合物的形态存在于矿石中。
陨铁
赤铁矿Fe2O3
磁铁矿Fe3O4
自然界有金属钠单质吗?
没有,钠的金属活动性强
为什么自然界有铁单质?
铁的金属活动性弱
铁元素在地壳中的含量仅次于氧、硅和铝,居第四位。
O Si Al Fe
地壳中元素含量递减
丹霞地貌的岩层因Fe2O3而呈红色。
战国铁剑
打铁炉
战国铁炉
我国从很早之前就掌握了冶铁技术
你还记得高炉炼铁的化学反应吗?
还原成铁:Fe2O3+3CO====2Fe+3CO2
高温
高温
高温
热源形成:C+O2==== CO2 C+CO2====2CO
高温
高温
炉渣回收:CaCO3===CaO+CO2 ↑ CaO+SiO2===CaSiO3
知识点二:铁的单质
1.铁的物理性质
颜色 状态 金属通性 熔点 沸点 密度 特性
银白色,有金属光泽 固体 导电性、导热性、延展性 1535℃ 2750℃ 7.86g/cm3 易被磁铁吸引
铁块(银白色)
铁粉(黑色)
2.铁的化学性质
想一想我们学过铁与哪些物质的反应?写出这些反应的化学方程式。
(2)非氧化性酸的反应(如:HCl等)
Fe+2H+=Fe2++H2↑
(3)与盐溶液的反应(如:CuSO4等)
Fe+Cu2+=Fe2++Cu
【思考·讨论】上述反应中,铁化合价有什么异同?为什么有这样的异同?
(1) 与非金属单质的反应(如:O2、Cl2等)
2Fe+3Cl2 2FeCl3
3Fe+4O2 Fe3O4
Fe+S FeS
加热
Fe
FeCl3
化合价升高
0
+3
铁与氯气的反应:
铁与盐酸溶液的反应:
Fe
FeCl2
化合价升高
0
+2
铁与硫酸铜溶液的反应:
Fe
FeSO4
化合价升高
0
+2
Fe - 2e- = Fe2+
Fe - 3e- = Fe3+
Fe与弱氧化剂(如盐酸、硫酸铜等)的反应,铁失去两个电子,生成Fe2+
Fe与强氧化剂(氯气等)的反应,铁失去三个电子,生成Fe3+
下列物质反应后一定有+3价铁生成的是( )
①过量的Fe与Cl2反应
②Fe与过量稀硫酸反应
③ FeCl2溶液中通入少量Cl2
④ Fe和Fe2O3的混合物溶于盐酸中
A.只有① B.①③ C.①②③ D.全部
练一练
B
炽热的铁水倒入模具中
在钢铁厂的生产中,炽热的钢水或者铁水注入模具之前,模具必须进行充分的干燥处理,不得留有水。这是为什么呢?
因为铁会在高温下与水发生反应
反应生成了什么?
3.铁与水蒸气反应
视频
(1)实验现象:
(2)反应方程式:
铁粉逐渐红热,生成黑色固体
气泡破裂,气体燃烧,发出轻微爆鸣声
3Fe+4H2O(g)==== Fe3O4+4H2
高温
(3)装置分析
棉花的作用是什么?
肥皂泡的作用是什么?
棉花的作用是在受热时提供反应所需的水蒸气。
肥皂泡的作用是为了储存气体,方便检验产物。
可以提高加热温度。
为什么酒精灯的火焰用防风罩罩住?
①试管口略向下倾斜;
④结束时,先撤导管,再移酒精灯。
②酒精灯先加热湿棉花,有水蒸气后,再点燃酒精灯加热还原铁粉;
③加热一会后再将导管插入到肥皂水中;
(4)实验注意事项
4.金属与水反应的一般规律
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
金属性越强,常温下与水反应越剧烈
(1)活泼金属K、Na等可与冷水迅速剧烈反应(放热),生成可溶性碱与H2。
(2)Mg与冷水反应缓慢,但在加热条件(或沸水),Mg与水的反应加快。
(3)Fe、Zn等可以与水蒸气反应生成金属氧化物和H2。
(4)Cu、Hg、Ag、Pt、Au不与水反应。
1.下列关于铁与水蒸气反应的说法中不正确的是( )
A.反应中有氢气产生
B.此反应需在高温下才能发生
C.生成的铁的化合物中铁全部呈+3价
D.该反应中水作氧化剂
练一练
C
2.在玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气。用试管收集产生的经过干燥的气体,并靠近火焰点燃。
a.实验现象是红热的铁与水蒸气反应,
放出气体,这种气体点燃时能燃烧
且发出爆鸣声,有关反应的化学
方程式是_____________________________。
b.干燥管内可装入的试剂是____________________________,
其作用是 ,使收集的氢气易点燃。
c.玻璃管中石棉绒是作为铁粉的载体,其目的是__ ________ ____;
实验开始时应先点燃 处酒精灯,实验结束时应先熄灭 处酒精灯。
3Fe+4H2O(g) ====Fe3O4+4H2
高温
碱石灰(或无水CaCl2、硅胶等)
吸收水蒸气
增大铁粉与水蒸气的接触面积
A
B
缺铁性贫血(IDA)
红细胞中含有血红蛋白,而血红蛋白的作用是运输氧气,亚铁离子是血红蛋白的组成成分之一。
01
缺铁性贫血比较明显的表现就是口唇、眼结膜、甲床等颜色发白,同时会有心慌、乏力、头晕、注意力不集中、食欲减退、耳鸣、心悸、气促等症状。
03
人体对铁的摄入量不足,便会影响到血红蛋白的合成,从而使红细胞中血红蛋白的含量显著减少,随之红细胞数目就减少。会使人体内的各细胞、组织供氧不足,将导致缺铁性贫血症。
02
知识扩展
生活中的铁元素
动物内脏、红肉(猪肉、牛肉、羊肉等)、鱼类和蛋类食物
01
必要时可服用补铁剂来达到铁元素的适宜摄入量
03
铁强化酱油也可以补充日常所需的铁元素
02
补铁剂
目前常用的铁剂有硫酸亚铁、富马酸亚铁、乳酸亚铁等,乳酸亚铁属于有机铁剂,吸收不消耗胃酸,不会对肠胃有刺激性。
01
铁剂不能与咖啡、浓茶同服。服用铁剂期间,那是因为茶和咖啡里含有丰富的鞣酸,这种物质和铁会生成一种不溶性的铁质沉淀,从而阻碍铁的吸收。
03
铁剂不能和抗酸药一起服用。不能同时服用铁剂和抗酸药,因为抗酸药属于碱性药物,同时服用会影响铁质吸收。
02
铁单质
物理性质
化学性质
银白色固体、有延展性
熔、沸点高;导电、导热
与氯气反应:2Fe+3Cl2 ======2FeCl3
与水蒸汽反应:3Fe+4H2O(g)==== Fe3O4+4H2
能被磁铁吸引
高温
与硫反应:Fe+S ======FeS
