4.1 课时1 原子结构 课件(共23张PPT) 2023-2024学年高一化学人教版(2019)必修一
文档属性
| 名称 | 4.1 课时1 原子结构 课件(共23张PPT) 2023-2024学年高一化学人教版(2019)必修一 |  | |
| 格式 | pptx | ||
| 文件大小 | 994.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-12-11 11:10:31 | ||
图片预览






文档简介
(共23张PPT)
同学们,我们初中学习过原子结构的构成,回忆一下原子是由什么构成的。
原子核
质子
中子
核外电子
原子
第一节 原子结构与元素周期表 课时1
第四章 物质结构 元素周期律
1.了解原子结构模型的演变过程,从而认识原子的结构特点。
2.能归纳多电子原子中核外电子排布的规律,能用原子结构示意图表示1~20号元素原子的核外电子排布。
3.知道质量数和 X的含义。
A
Z
知识点一:原子结构
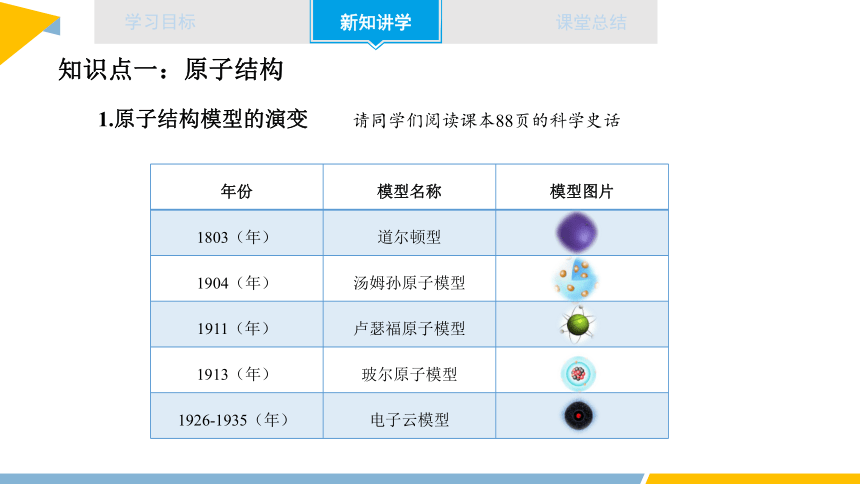
1.原子结构模型的演变
年份 模型名称 模型图片
1803(年) 道尔顿型
1904(年) 汤姆孙原子模型
1911(年) 卢瑟福原子模型
1913(年) 玻尔原子模型
1926-1935(年) 电子云模型
请同学们阅读课本88页的科学史话
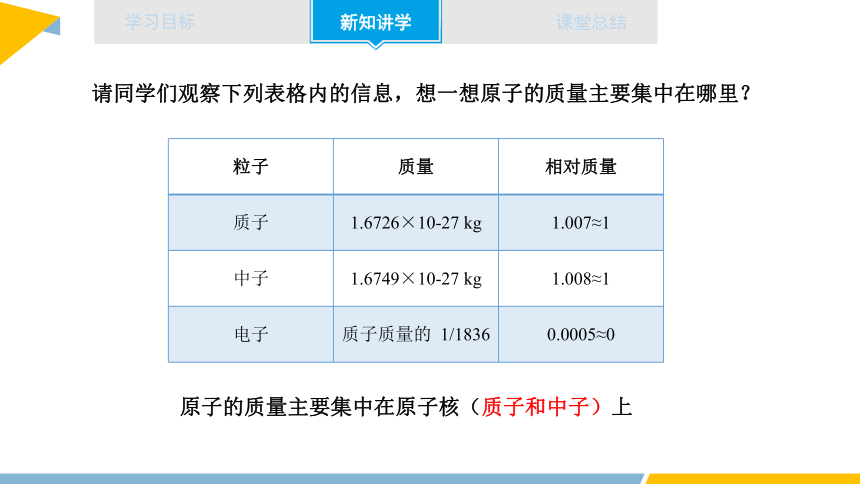
粒子 质量 相对质量
质子 1.6726×10-27 kg 1.007≈1
中子 1.6749×10-27 kg 1.008≈1
电子 质子质量的 1/1836 0.0005≈0
请同学们观察下列表格内的信息,想一想原子的质量主要集中在哪里?
原子的质量主要集中在原子核(质子和中子)上
2.质量数
原子的质量主要集中在原子核上,质子和中子的相对质量都近似为1,如果忽略电子的质量,将核内所有质子和中子的相对质量取近似整数值相加,所得的数值叫做质量数,用符号 A 表示。
等式关系:质量数(A)=质子数(Z)+中子数(N)
质量数
质子数
Z个质子,Z个电子和(A-Z)个中子的X原子
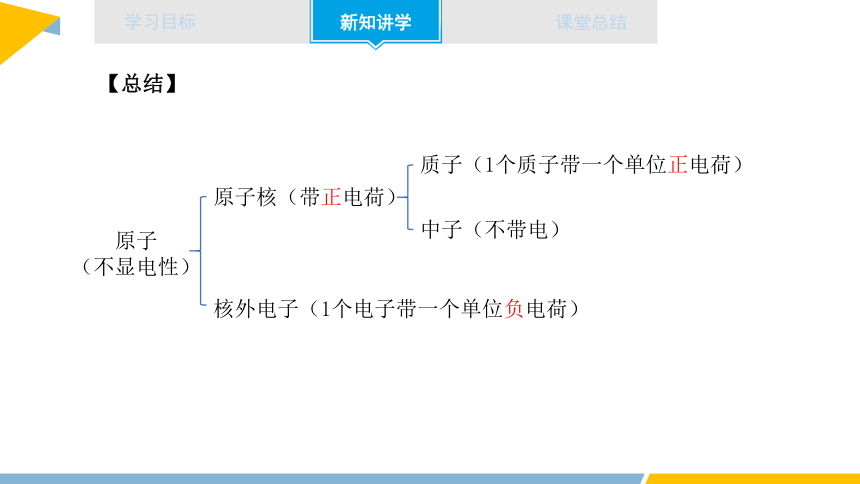
原子核(带正电荷)
质子(1个质子带一个单位正电荷)
中子(不带电)
核外电子(1个电子带一个单位负电荷)
原子(不显电性)
【总结】
练一练
1.判断正误,正确的打“√”,错误的打“×”。
(1)34S 原子核内中子数为16
(2)2H核外电子数为2
(3)13C 和15N 核内中子数相差1
(4)含有8个质子,8个中子的原子的化学符号是16O
( )
( )
( )
( )
×
×
√
√
2.已知Mg2+核外有10个电子,Mg原子有12个中子,下列表述Mg原子符号正确的是( )。
A. Mg B. Mg
C. Mg D. Mg
12
10
22
12
24
12
22
8
C
3.下列关于核电池燃料 Pu的说法中正确的是( )。
238
94
A.中子数为94 B.电子数为94
C.质子数为238 D.质量数为144
B
知识点二:原子核外电子排布的规律
1.电子层
在含有多个电子的原子里,电子分别在能量不同的区域内运动。我们把不同的区域简化为不连续的壳层,称作电子层。
电子层模型示意图
把这种电子层模型比拟为洋葱式结构
电子层 (n) 1 2 3 4 5 6 7
或 K L M N O P Q
一般总是先从能量低的排起,当一层充满之后再填充下一层
离核由近到远,电子能量由低到高
【思考】每个电子层最多可以容纳多少个电子呢?
稀有气体元素原子的电子排布
①当K层为最外层时,最多能容纳的电子数是多少?
②除了K层,其他各层为最外层时,最多能容纳的电子数是多少?
③次外层最多容纳的电子数是多少?
④倒数第三层最多容纳的电子数是多少?
⑤你能归纳出第n层最多能容纳的电子数吗?
下表是稀有气体元素原子的电子层排布,从中你能发现什么规律?请思考并回答下列问题。
思考与讨论
稀有气体元素原子的电子排布
①当K层为最外层时,最多能容纳的电子数是多少?
K层为最外层时,最多能容纳的电子数为2个
下表是稀有气体元素原子的电子层排布,从中你能发现什么规律?请思考并回答下列问题。
思考与讨论
稀有气体元素原子的电子排布
②除了K层,其他各层为最外层时,最多能容纳的电子数是多少?
其他各层为最外层时,最多容纳电子数为8个
下表是稀有气体元素原子的电子层排布,从中你能发现什么规律?请思考并回答下列问题。
思考与讨论
稀有气体元素原子的电子排布
③次外层最多容纳的电子数是多少?
次外层最多能容纳电子数为18个
下表是稀有气体元素原子的电子层排布,从中你能发现什么规律?请思考并回答下列问题。
思考与讨论
稀有气体元素原子的电子排布
④倒数第三层最多容纳的电子数是多少?
倒数第三层最多容纳的电子数为32个
下表是稀有气体元素原子的电子层排布,从中你能发现什么规律?请思考并回答下列问题。
思考与讨论
稀有气体元素原子的电子排布
⑤你能归纳出第n层最多能容纳的电子数吗?
2×12、2×22、2×32、2×42......
原子核外每一层最多能容纳的电子数为2n2
下表是稀有气体元素原子的电子层排布,从中你能发现什么规律?请思考并回答下列问题。
思考与讨论
①电子一般先从能量低的排起,当一层充满后再填充下一层
②K层为最外层时,最多能容纳的电子数为2个
③其他各层为最外层时,最多容纳电子数为8个(K层为2个)
④次外层最多能容纳电子数为18个
⑤倒数第三层最多容纳的电子数为32个
⑥2×12、2×22、2×32、2×42......原子核外每一层最多能容纳的电子数为2n2
【结论】
【注意】这些规律是相互联系,相互制约,不可分割。
3.原子结构示意图
元素符号
原子核
核内质子数
M层电子数
电子层
钠原子的原子结构示意图
1. 请你根据所归纳的电子排布规律,用原子结构示意图表示核电荷数为1~20号元素原子的核外电子排布。
练一练
H He Li Be B
C N O F Ne
Na Mg Al Si P
S Cl Ar K Ca
2.某元素原子的核外有三个电子层,最外层电子数是7。该原子核内的质子数是( )。
A.14 B.15
C.16 D.17
D
3.下面关于多电子原子的核外电子运动规律的叙述正确的是( )。
A.①④ B.②③
C.①③ D.②④
①核外电子是分层运动的 ②所有电子在同一区域里运动
③能量高的电子在离核近的区域内运动 ④能量低的电子在离核近的区域内运动
A
4.判断正误,正确的打“ √ ”,错误的打“ × ”。
(1)原子呈电中性是因为中子不带电。( )
(2)粒子中的质子数与核外电子数一定相等。( )
(3)某种氯原子的中子数是18,则其质量数是35,核外电子数是17。( )
(4)核外电子排布相同的粒子化学性质一定相同。( )
×
×
√
×
原子结构
原子结构模型演变
核外电子的排布规律
质量数
最外层最多能容纳8个电子(K层为2个)
次外层最多能容纳18个电子(L层为8个)
倒数第三层最多能容纳32个电子
每个电子层最多能容纳的电子数为2n2
多电子遵循能量最低原理
质量数=质子数+中子数
同学们,我们初中学习过原子结构的构成,回忆一下原子是由什么构成的。
原子核
质子
中子
核外电子
原子
第一节 原子结构与元素周期表 课时1
第四章 物质结构 元素周期律
1.了解原子结构模型的演变过程,从而认识原子的结构特点。
2.能归纳多电子原子中核外电子排布的规律,能用原子结构示意图表示1~20号元素原子的核外电子排布。
3.知道质量数和 X的含义。
A
Z
知识点一:原子结构
1.原子结构模型的演变
年份 模型名称 模型图片
1803(年) 道尔顿型
1904(年) 汤姆孙原子模型
1911(年) 卢瑟福原子模型
1913(年) 玻尔原子模型
1926-1935(年) 电子云模型
请同学们阅读课本88页的科学史话
粒子 质量 相对质量
质子 1.6726×10-27 kg 1.007≈1
中子 1.6749×10-27 kg 1.008≈1
电子 质子质量的 1/1836 0.0005≈0
请同学们观察下列表格内的信息,想一想原子的质量主要集中在哪里?
原子的质量主要集中在原子核(质子和中子)上
2.质量数
原子的质量主要集中在原子核上,质子和中子的相对质量都近似为1,如果忽略电子的质量,将核内所有质子和中子的相对质量取近似整数值相加,所得的数值叫做质量数,用符号 A 表示。
等式关系:质量数(A)=质子数(Z)+中子数(N)
质量数
质子数
Z个质子,Z个电子和(A-Z)个中子的X原子
原子核(带正电荷)
质子(1个质子带一个单位正电荷)
中子(不带电)
核外电子(1个电子带一个单位负电荷)
原子(不显电性)
【总结】
练一练
1.判断正误,正确的打“√”,错误的打“×”。
(1)34S 原子核内中子数为16
(2)2H核外电子数为2
(3)13C 和15N 核内中子数相差1
(4)含有8个质子,8个中子的原子的化学符号是16O
( )
( )
( )
( )
×
×
√
√
2.已知Mg2+核外有10个电子,Mg原子有12个中子,下列表述Mg原子符号正确的是( )。
A. Mg B. Mg
C. Mg D. Mg
12
10
22
12
24
12
22
8
C
3.下列关于核电池燃料 Pu的说法中正确的是( )。
238
94
A.中子数为94 B.电子数为94
C.质子数为238 D.质量数为144
B
知识点二:原子核外电子排布的规律
1.电子层
在含有多个电子的原子里,电子分别在能量不同的区域内运动。我们把不同的区域简化为不连续的壳层,称作电子层。
电子层模型示意图
把这种电子层模型比拟为洋葱式结构
电子层 (n) 1 2 3 4 5 6 7
或 K L M N O P Q
一般总是先从能量低的排起,当一层充满之后再填充下一层
离核由近到远,电子能量由低到高
【思考】每个电子层最多可以容纳多少个电子呢?
稀有气体元素原子的电子排布
①当K层为最外层时,最多能容纳的电子数是多少?
②除了K层,其他各层为最外层时,最多能容纳的电子数是多少?
③次外层最多容纳的电子数是多少?
④倒数第三层最多容纳的电子数是多少?
⑤你能归纳出第n层最多能容纳的电子数吗?
下表是稀有气体元素原子的电子层排布,从中你能发现什么规律?请思考并回答下列问题。
思考与讨论
稀有气体元素原子的电子排布
①当K层为最外层时,最多能容纳的电子数是多少?
K层为最外层时,最多能容纳的电子数为2个
下表是稀有气体元素原子的电子层排布,从中你能发现什么规律?请思考并回答下列问题。
思考与讨论
稀有气体元素原子的电子排布
②除了K层,其他各层为最外层时,最多能容纳的电子数是多少?
其他各层为最外层时,最多容纳电子数为8个
下表是稀有气体元素原子的电子层排布,从中你能发现什么规律?请思考并回答下列问题。
思考与讨论
稀有气体元素原子的电子排布
③次外层最多容纳的电子数是多少?
次外层最多能容纳电子数为18个
下表是稀有气体元素原子的电子层排布,从中你能发现什么规律?请思考并回答下列问题。
思考与讨论
稀有气体元素原子的电子排布
④倒数第三层最多容纳的电子数是多少?
倒数第三层最多容纳的电子数为32个
下表是稀有气体元素原子的电子层排布,从中你能发现什么规律?请思考并回答下列问题。
思考与讨论
稀有气体元素原子的电子排布
⑤你能归纳出第n层最多能容纳的电子数吗?
2×12、2×22、2×32、2×42......
原子核外每一层最多能容纳的电子数为2n2
下表是稀有气体元素原子的电子层排布,从中你能发现什么规律?请思考并回答下列问题。
思考与讨论
①电子一般先从能量低的排起,当一层充满后再填充下一层
②K层为最外层时,最多能容纳的电子数为2个
③其他各层为最外层时,最多容纳电子数为8个(K层为2个)
④次外层最多能容纳电子数为18个
⑤倒数第三层最多容纳的电子数为32个
⑥2×12、2×22、2×32、2×42......原子核外每一层最多能容纳的电子数为2n2
【结论】
【注意】这些规律是相互联系,相互制约,不可分割。
3.原子结构示意图
元素符号
原子核
核内质子数
M层电子数
电子层
钠原子的原子结构示意图
1. 请你根据所归纳的电子排布规律,用原子结构示意图表示核电荷数为1~20号元素原子的核外电子排布。
练一练
H He Li Be B
C N O F Ne
Na Mg Al Si P
S Cl Ar K Ca
2.某元素原子的核外有三个电子层,最外层电子数是7。该原子核内的质子数是( )。
A.14 B.15
C.16 D.17
D
3.下面关于多电子原子的核外电子运动规律的叙述正确的是( )。
A.①④ B.②③
C.①③ D.②④
①核外电子是分层运动的 ②所有电子在同一区域里运动
③能量高的电子在离核近的区域内运动 ④能量低的电子在离核近的区域内运动
A
4.判断正误,正确的打“ √ ”,错误的打“ × ”。
(1)原子呈电中性是因为中子不带电。( )
(2)粒子中的质子数与核外电子数一定相等。( )
(3)某种氯原子的中子数是18,则其质量数是35,核外电子数是17。( )
(4)核外电子排布相同的粒子化学性质一定相同。( )
×
×
√
×
原子结构
原子结构模型演变
核外电子的排布规律
质量数
最外层最多能容纳8个电子(K层为2个)
次外层最多能容纳18个电子(L层为8个)
倒数第三层最多能容纳32个电子
每个电子层最多能容纳的电子数为2n2
多电子遵循能量最低原理
质量数=质子数+中子数
