4.3防治二氧化硫对环境的污染(教案)(表格式)——高一上学期化学苏教版(2019)必修第一册
文档属性
| 名称 | 4.3防治二氧化硫对环境的污染(教案)(表格式)——高一上学期化学苏教版(2019)必修第一册 |
|
|
| 格式 | docx | ||
| 文件大小 | 684.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-12-11 00:00:00 | ||
图片预览


文档简介
课题: 防治二氧化硫对环境的污染
教学目的要求: 1.了解自然界中硫元素的循环。2.了解酸雨的成因、危害及防治方法,形成环保意识。3.了解雾霾的形成及防治办法和空气质量评价。
教学重点: 酸雨的成因、硫酸雨的防治方法; 雾霾的防治和空气质量评价
教学难点:硫酸雨的防治方法; 雾霾的防治和空气质量评价
教 学 过 程 教师活动 学生活动
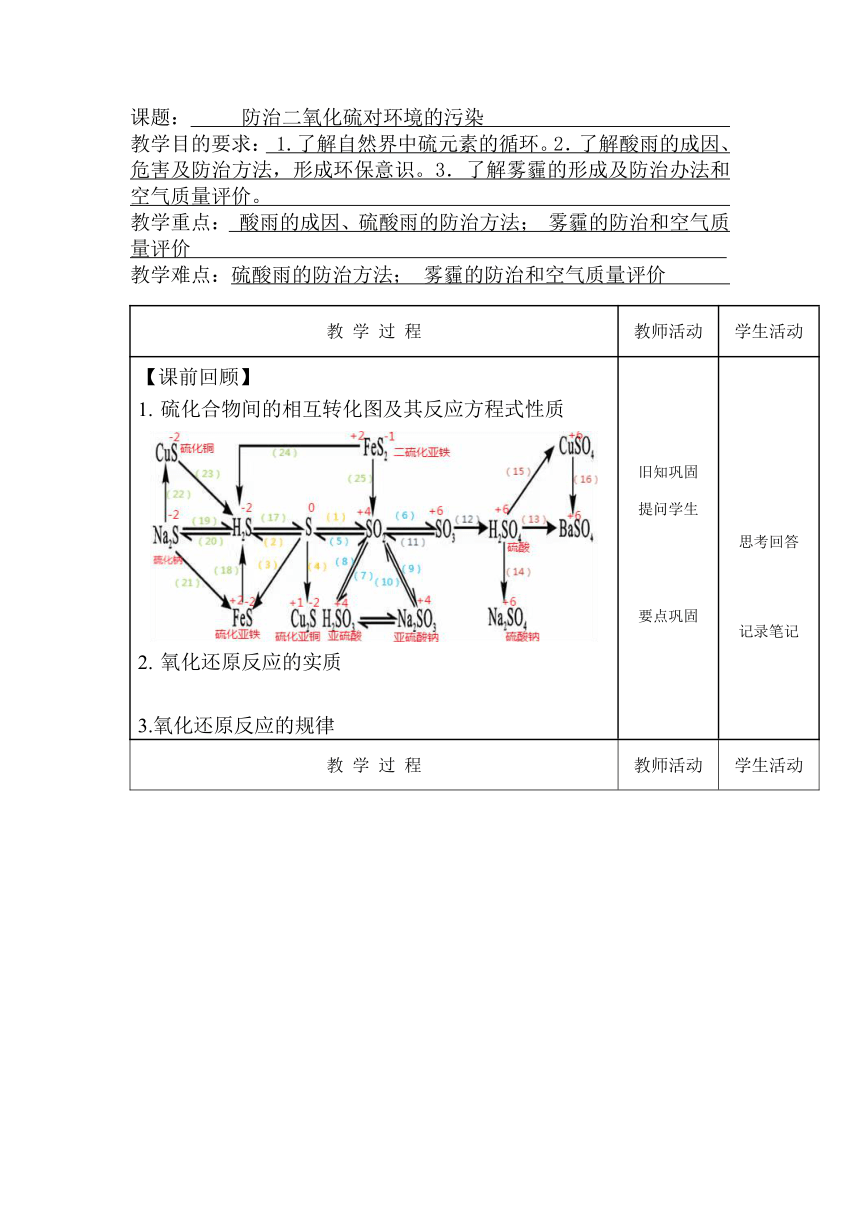
【课前回顾】 硫化合物间的相互转化图及其反应方程式性质 氧化还原反应的实质 3.氧化还原反应的规律 旧知巩固 提问学生 要点巩固 思考回答 记录笔记
教 学 过 程 教师活动 学生活动
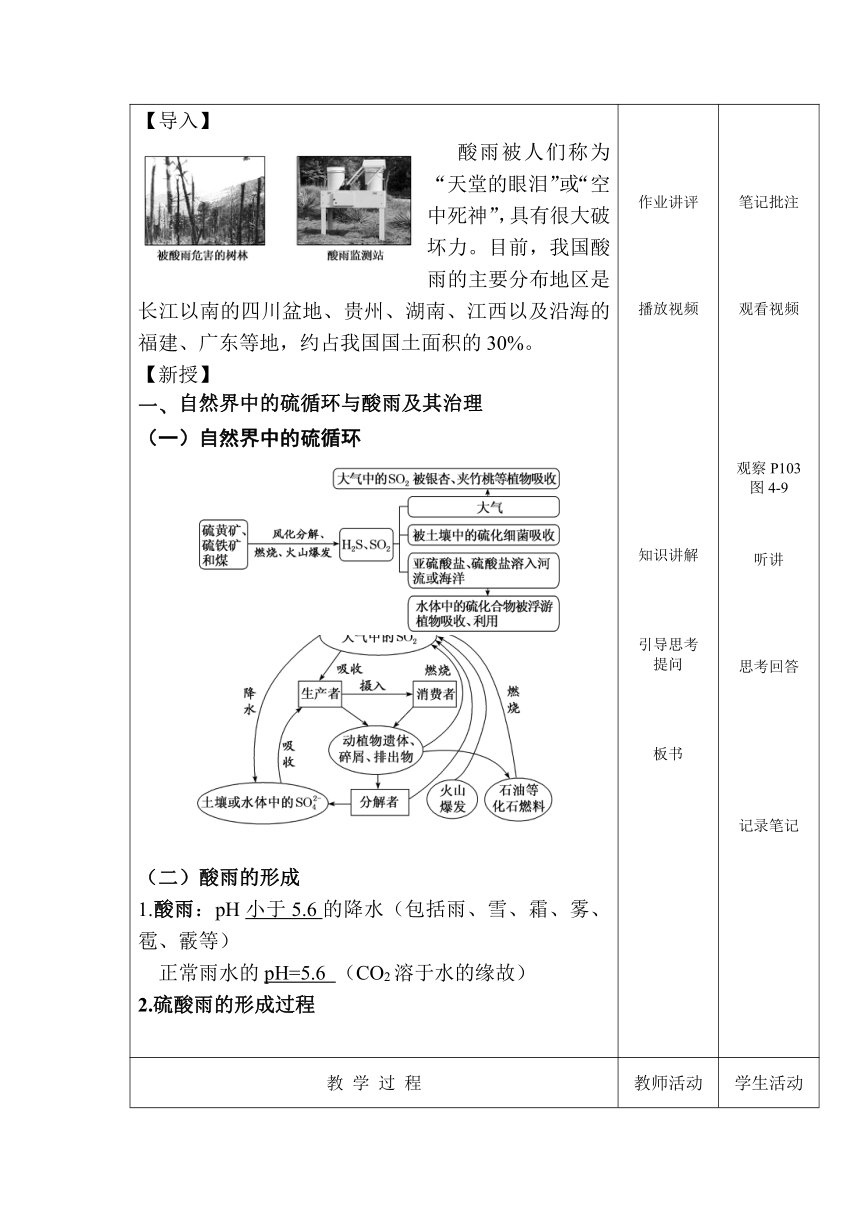
【导入】 酸雨被人们称为“天堂的眼泪”或“空中死神”,具有很大破坏力。目前,我国酸雨的主要分布地区是长江以南的四川盆地、贵州、湖南、江西以及沿海的福建、广东等地,约占我国国土面积的30%。 【新授】 (一)自然界中的硫循环 (二)酸雨的形成 1.酸雨:pH小于5.6的降水(包括雨、雪、霜、雾、雹、霰等) 正常雨水的pH=5.6 (CO2溶于水的缘故) 2.硫酸雨的形成过程 作业讲评 播放视频 知识讲解 引导思考 提问 板书 笔记批注 观看视频 观察P103 图4-9 听讲 思考回答 记录笔记
教 学 过 程 教师活动 学生活动
途径一: 途径二: 3.酸雨雨水样品的pH变化的原因 (1)酸雨放置时pH变小,是因为雨水中的H2SO3被空气中氧气氧化所致——途径一 (2)如果将酸雨雨水和自来水混合,混合后溶液pH将变小,是因为SO2与自来水中的Cl2(或H2SO3与HClO)反应:SO2+2H2O+Cl2===H2SO4+2HCl (或H2SO3+HClO===H2SO4+HCl)。 (三)酸雨的危害 1.酸化湖泊,导致鱼类难以生存,影响水生生物的繁殖。 2.酸化土壤,使钙、镁、磷等元素流失,降低土壤肥力,破坏植被,危害农作物生长。 3.加快桥梁、雕塑等建筑物的腐蚀,许多文物古迹被严重破坏。 4.导致地下水中重金属元素含量增加,污染水源,危害人体健康。 (四)硫酸型酸雨的治理 1.开发新能源(如太阳能、核能、氢能等)替代化石燃料,减少化石燃料的使用。 2.对含硫燃料预先进行脱硫处理,减少SO2的排放。 3.对生产中产生的SO2废气进行处理或回收利用。如用石灰乳吸收SO2:Ca(OH)2+SO2===CaSO3↓+H2O。 4.健全法律法规,严格规定污染物的排放标准,提高环境保护意识。 重点讲解 要点讲解 板书 知识讲解 要点讲解 记录笔记 笔记批注 听讲 记录笔记
教 学 过 程 教师活动 学生活动
[问题探讨] 1.实验室如何处理铜与浓硫酸反应生成的SO2尾气? 提示:实验室用NaOH溶液来吸收SO2尾气。 原理:2NaOH+SO2===Na2SO3+H2O。 2.工业上如何选择吸收SO2的物质? 提示:工业上选择脱硫物质的要求:廉价、成本低,工艺简单,节约资源,去除率高等。 3.消除SO2对环境污染的“三方法” (1)方法一:石灰石-石膏法 工艺原理:将石灰石粉末加水制成浆液作为吸收剂泵入吸收塔,与烟气充分接触混合并氧化,最终生成石膏(CaSO4·2H2O)。其化学方程式为: CaCO3+SO2===CaSO3+CO2,2CaSO3+O2===2CaSO4, 总反应方程式:2CaCO3+2SO2+O2===2CaSO4+2CO2。 (2)方法二:氨脱硫法 该脱硫法采用喷雾吸收法,雾化的氨水与烟气中的SO2直接接触从而吸收SO2,其反应的化学方程式为NH3+SO2(过量)+H2O===NH4HSO3,2NH3+SO2(少量)+H2O===(NH4)2SO3、2(NH4)2SO3+O2===2(NH4)2SO4。 (3)方法三:钠、碱脱硫法 钠、碱脱硫法是用NaOH或Na2CO3吸收烟气中的SO2,得到Na2SO3和NaHSO3,发生反应的化学方程式为2NaOH+SO2===Na2SO3+H2O或Na2CO3+SO2===Na2SO3+CO2,Na2SO3+SO2+H2O===2NaHSO3。 二、 1.空气质量指数(AQI) (1)概念:根据空气中的细颗粒物(PM2.5)、可吸入颗粒物(PM10)、二氧化硫、二氧化氮、臭氧和一氧化碳的浓度计算出来的数值。其中指数最大的污染物会被确 重点讲解 提问 拓展讲解 板书 知识小结 提问 思考回顾 阅读P104 [选择决策] 阅读P104 [拓展视野] 记录笔记 思考回答
教 学 过 程 教师活动 学生活动
定为首要污染物,首要污染物的质量指数即为该地区的空气质量指数。 (2)意义:空气质量指数越小,空气质量越好,对人体健康的危害就越小。 (3)空气污染物来源:煤、石油的燃烧,矿石冶炼,汽车尾气,工业废气等。 2.雾霾及其防治 (1)概念:大量极细微的颗粒物均匀地悬浮在空中,这些颗粒物容易吸附空气中的水蒸气形成雾滴,使空气水平能见度小于10 km,这种空气混浊现象叫作雾霾。 (2)分类:根据颗粒物直径的大小可以将其分为:细颗粒物(PM2.5,直径小于2.5μm)、可吸入颗粒物(PM10,直径小于10 μm)等。 (3)成因及防治 ①成因:悬浮在空气中的颗粒物的组成为有机颗粒物、硫酸盐、铵盐等,其中硫酸盐与空气中的SO2有关。 ②防治:从源头抓起,企业必须转变能源结构,坚持绿色发展,控制二氧化硫等有害气体的排放;政府要提高污染排放标准,社会各界要大力监督。 3.常见的污染现象及其危害 (1)酸雨:主要是由SO2和氮氧化物造成的;能使土壤酸化,腐蚀建筑物等。 (2)光化学烟雾:主要是由氮氧化物、碳氢化合物造成的;危害人体健康,影响植物生长。 (3)臭氧空洞::主要是由氮氧化物、氟氯代烃等的排放引起的;使地球上的生物受太阳紫外线的伤害加剧。 (4)温室效应:主要是由大气中CO2、CH4含量的不 要点强调 提问 知识讲解 拓展讲解 阅读P105 [学科链接] 记录笔记 思考回答 记录笔记 记录笔记
教 学 过 程 教师活动 学生活动
断增加造成的;会使全球气候变暖。 (5)白色污染:形成原因是废旧塑料如聚乙烯塑料等的大量使用以及随意丢弃;会破坏土壤结构和生态环境。 (6)赤潮和水华:形成原因是含磷洗衣粉的大量使用及工、农业生产、城市生活污水的任意排放;会使藻类过度繁殖,鱼类死亡,水质恶化,若发生在淡水中称为水华,发生在海水中称为赤潮。 (7)重金属污染:形成原因是含Pb、Hg、Cd、Cr等重金属的废旧电池的随意丢弃,破坏了土壤结构和生态环境。如水俣病、痛痛病是含汞、镉的工业废水引起的,人食用中毒后的鱼会造成人体汞、镉中毒。 【总结】 【作业】 知识梳理 课堂总结 作业布置 记录笔记 记录作业
板书设计 自然界中的硫循环及酸雨 空气质量指数(AQI) 自然界中的硫循环 一、概念及首要污染物指数 硫酸雨 二、雾霾及其防治 硫酸雨的形成 三、常见的污染现象及其危害 酸雨的危害 3.酸雨的防治
教学课后小结
教学目的要求: 1.了解自然界中硫元素的循环。2.了解酸雨的成因、危害及防治方法,形成环保意识。3.了解雾霾的形成及防治办法和空气质量评价。
教学重点: 酸雨的成因、硫酸雨的防治方法; 雾霾的防治和空气质量评价
教学难点:硫酸雨的防治方法; 雾霾的防治和空气质量评价
教 学 过 程 教师活动 学生活动
【课前回顾】 硫化合物间的相互转化图及其反应方程式性质 氧化还原反应的实质 3.氧化还原反应的规律 旧知巩固 提问学生 要点巩固 思考回答 记录笔记
教 学 过 程 教师活动 学生活动
【导入】 酸雨被人们称为“天堂的眼泪”或“空中死神”,具有很大破坏力。目前,我国酸雨的主要分布地区是长江以南的四川盆地、贵州、湖南、江西以及沿海的福建、广东等地,约占我国国土面积的30%。 【新授】 (一)自然界中的硫循环 (二)酸雨的形成 1.酸雨:pH小于5.6的降水(包括雨、雪、霜、雾、雹、霰等) 正常雨水的pH=5.6 (CO2溶于水的缘故) 2.硫酸雨的形成过程 作业讲评 播放视频 知识讲解 引导思考 提问 板书 笔记批注 观看视频 观察P103 图4-9 听讲 思考回答 记录笔记
教 学 过 程 教师活动 学生活动
途径一: 途径二: 3.酸雨雨水样品的pH变化的原因 (1)酸雨放置时pH变小,是因为雨水中的H2SO3被空气中氧气氧化所致——途径一 (2)如果将酸雨雨水和自来水混合,混合后溶液pH将变小,是因为SO2与自来水中的Cl2(或H2SO3与HClO)反应:SO2+2H2O+Cl2===H2SO4+2HCl (或H2SO3+HClO===H2SO4+HCl)。 (三)酸雨的危害 1.酸化湖泊,导致鱼类难以生存,影响水生生物的繁殖。 2.酸化土壤,使钙、镁、磷等元素流失,降低土壤肥力,破坏植被,危害农作物生长。 3.加快桥梁、雕塑等建筑物的腐蚀,许多文物古迹被严重破坏。 4.导致地下水中重金属元素含量增加,污染水源,危害人体健康。 (四)硫酸型酸雨的治理 1.开发新能源(如太阳能、核能、氢能等)替代化石燃料,减少化石燃料的使用。 2.对含硫燃料预先进行脱硫处理,减少SO2的排放。 3.对生产中产生的SO2废气进行处理或回收利用。如用石灰乳吸收SO2:Ca(OH)2+SO2===CaSO3↓+H2O。 4.健全法律法规,严格规定污染物的排放标准,提高环境保护意识。 重点讲解 要点讲解 板书 知识讲解 要点讲解 记录笔记 笔记批注 听讲 记录笔记
教 学 过 程 教师活动 学生活动
[问题探讨] 1.实验室如何处理铜与浓硫酸反应生成的SO2尾气? 提示:实验室用NaOH溶液来吸收SO2尾气。 原理:2NaOH+SO2===Na2SO3+H2O。 2.工业上如何选择吸收SO2的物质? 提示:工业上选择脱硫物质的要求:廉价、成本低,工艺简单,节约资源,去除率高等。 3.消除SO2对环境污染的“三方法” (1)方法一:石灰石-石膏法 工艺原理:将石灰石粉末加水制成浆液作为吸收剂泵入吸收塔,与烟气充分接触混合并氧化,最终生成石膏(CaSO4·2H2O)。其化学方程式为: CaCO3+SO2===CaSO3+CO2,2CaSO3+O2===2CaSO4, 总反应方程式:2CaCO3+2SO2+O2===2CaSO4+2CO2。 (2)方法二:氨脱硫法 该脱硫法采用喷雾吸收法,雾化的氨水与烟气中的SO2直接接触从而吸收SO2,其反应的化学方程式为NH3+SO2(过量)+H2O===NH4HSO3,2NH3+SO2(少量)+H2O===(NH4)2SO3、2(NH4)2SO3+O2===2(NH4)2SO4。 (3)方法三:钠、碱脱硫法 钠、碱脱硫法是用NaOH或Na2CO3吸收烟气中的SO2,得到Na2SO3和NaHSO3,发生反应的化学方程式为2NaOH+SO2===Na2SO3+H2O或Na2CO3+SO2===Na2SO3+CO2,Na2SO3+SO2+H2O===2NaHSO3。 二、 1.空气质量指数(AQI) (1)概念:根据空气中的细颗粒物(PM2.5)、可吸入颗粒物(PM10)、二氧化硫、二氧化氮、臭氧和一氧化碳的浓度计算出来的数值。其中指数最大的污染物会被确 重点讲解 提问 拓展讲解 板书 知识小结 提问 思考回顾 阅读P104 [选择决策] 阅读P104 [拓展视野] 记录笔记 思考回答
教 学 过 程 教师活动 学生活动
定为首要污染物,首要污染物的质量指数即为该地区的空气质量指数。 (2)意义:空气质量指数越小,空气质量越好,对人体健康的危害就越小。 (3)空气污染物来源:煤、石油的燃烧,矿石冶炼,汽车尾气,工业废气等。 2.雾霾及其防治 (1)概念:大量极细微的颗粒物均匀地悬浮在空中,这些颗粒物容易吸附空气中的水蒸气形成雾滴,使空气水平能见度小于10 km,这种空气混浊现象叫作雾霾。 (2)分类:根据颗粒物直径的大小可以将其分为:细颗粒物(PM2.5,直径小于2.5μm)、可吸入颗粒物(PM10,直径小于10 μm)等。 (3)成因及防治 ①成因:悬浮在空气中的颗粒物的组成为有机颗粒物、硫酸盐、铵盐等,其中硫酸盐与空气中的SO2有关。 ②防治:从源头抓起,企业必须转变能源结构,坚持绿色发展,控制二氧化硫等有害气体的排放;政府要提高污染排放标准,社会各界要大力监督。 3.常见的污染现象及其危害 (1)酸雨:主要是由SO2和氮氧化物造成的;能使土壤酸化,腐蚀建筑物等。 (2)光化学烟雾:主要是由氮氧化物、碳氢化合物造成的;危害人体健康,影响植物生长。 (3)臭氧空洞::主要是由氮氧化物、氟氯代烃等的排放引起的;使地球上的生物受太阳紫外线的伤害加剧。 (4)温室效应:主要是由大气中CO2、CH4含量的不 要点强调 提问 知识讲解 拓展讲解 阅读P105 [学科链接] 记录笔记 思考回答 记录笔记 记录笔记
教 学 过 程 教师活动 学生活动
断增加造成的;会使全球气候变暖。 (5)白色污染:形成原因是废旧塑料如聚乙烯塑料等的大量使用以及随意丢弃;会破坏土壤结构和生态环境。 (6)赤潮和水华:形成原因是含磷洗衣粉的大量使用及工、农业生产、城市生活污水的任意排放;会使藻类过度繁殖,鱼类死亡,水质恶化,若发生在淡水中称为水华,发生在海水中称为赤潮。 (7)重金属污染:形成原因是含Pb、Hg、Cd、Cr等重金属的废旧电池的随意丢弃,破坏了土壤结构和生态环境。如水俣病、痛痛病是含汞、镉的工业废水引起的,人食用中毒后的鱼会造成人体汞、镉中毒。 【总结】 【作业】 知识梳理 课堂总结 作业布置 记录笔记 记录作业
板书设计 自然界中的硫循环及酸雨 空气质量指数(AQI) 自然界中的硫循环 一、概念及首要污染物指数 硫酸雨 二、雾霾及其防治 硫酸雨的形成 三、常见的污染现象及其危害 酸雨的危害 3.酸雨的防治
教学课后小结
