第5章 金属的冶炼与利用 考点串讲课件(共38张PPT)-2023-2024学年九年级化学上学期期末考点大串讲(沪教版全国)
文档属性
| 名称 | 第5章 金属的冶炼与利用 考点串讲课件(共38张PPT)-2023-2024学年九年级化学上学期期末考点大串讲(沪教版全国) |

|
|
| 格式 | pptx | ||
| 文件大小 | 41.9MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-12-14 00:00:00 | ||
图片预览










文档简介
举一反三
典例精讲
考点梳理
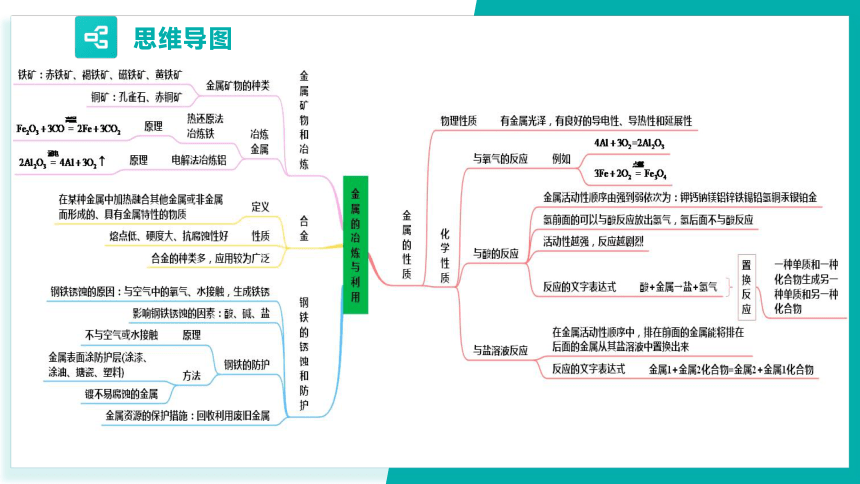
思维导图
金属的冶炼与利用
第5章
考点串讲PPT
目
录
CONTENTS
1
金属的性质和利用
2
金属矿物 铁的冶炼
3
金属防护和废金属回收
思维导图
金属的物理性质和用途
考点01
考点01 金属的物理性质和用途
{5940675A-B579-460E-94D1-54222C63F5DA}物理性质
用 途
共性
________性
制作导线
________性
制作炊具
________性
冲压成各种形状
有金属光泽
制作各种装饰品
特性
颜色:大多数金属呈 色,铜呈 色,金呈 色,
铁粉呈 色
状态:常温下,大多数金属为固体,而 为液体
导 电
导 热
延 展
银白
紫红
黄
汞
黑
考点梳理
典例精讲
【典例01】(2023年江西中考)大国工匠秦世俊展现数控技术所使用的铝箔,是由0.01mm铝块加工而成,这体现了铝具有
A.密度小 B.导电性 C.导热性 D.延展性
D
【典例02】(2023年四川巴中中考)牛奶盒内附有一层铝箔,利用了铝的 (选填“延展性”或“导热性”)。
考点01 金属的物理性质和用途
延展性
【典例03】(2023年辽宁丹东中考)铁铸成铁锅是利用了铁具有良好的 性;铁锅用于烹饪食物是利用铁具有良好的 性。
延展
导热
举一反三
【演练01】(2023年黑龙江中考)物质的性质决定用途。下列各物质的用途与性质对应关系正确的是
A.银有金属光泽,可用于制造电线
B.氮气是无色无味的气体,可用作保护气
C.石墨能导电,可用于制作铅笔芯
D.氢气具有可燃性,能作高能燃料
D
【演练02】(2023年甘肃金昌中考)下列生活用品利用金属良好导热性的是 (填序号)。
a.镀铬水龙头????????????????????b.铸铁暖气片????????????????c.包糖果的铝箔
b
考点01 金属的物理性质和用途
【演练03】(2023年江苏苏州中考)太阳能电池板需要使用铝合金箔片,铝合金能加工成箔片是利用了金属的 性。
延展
金属的化学性质
考点02
实验方案
实验课题
实验报告
实验总结
考点02 金属的化学性质——与氧气反应
考点梳理
与氧气反应
镁:在空气中点燃,剧烈燃烧,发出______________,生成白色固体,化学方程式为__________________
铝:具有很好的抗腐蚀性能,原因是__________________________ _____________________________________________________________。其与氧气反应的化学方程式为________________________
铁:在氧气中点燃,剧烈燃烧,_____________________________
铜:在空气中加热,表面生成_____色物质氧气反应
金:“真金不怕火炼”说明金在高温时________与氧气反应
耀眼的白光
2Mg+O2 ???点燃???? 2MgO
?
铝在空气中与氧气反应,表面生成一层致密的氧化铝(Al2O3)薄膜,阻止铝进一步氧化
4Al+3O2 ═══ 2Al2O3
火星四射,生成黑色固体
黑
不能
考点02 金属的化学性质——与酸反应
考点梳理
与酸反应
镁:与盐酸反应非常剧烈,化学方程式为________________________
锌:与盐酸反应较剧烈,化学方程式为_________________________
铁:与盐酸反应慢,化学方程式为_____________________________,
溶液由无色变为______色
铜:加入盐酸, 。
Mg+2HCl ═══ MgCl2+H2↑
Zn+2HCl ═══ ZnCl2+H2↑
Fe+2HCl ═══ FeCl2+H2↑
浅绿
无明显现象
考点02 金属的化学性质——与金属化合物溶液反应
考点梳理
与金属化合物溶液反应
铁与硫酸铜:
现象为___________________________________________________
化学方程式为_____________________________
铜与硝酸银:
现象为____________________________________________________
化学方程式为_______________________________
铜与硫酸铝:
无明显现象,证明活动性铝_____铜(填“>”或“<”)
铁的表面有红色固体析出,溶液由蓝色变为浅绿色
Fe+CuSO4 ══ FeSO4 +Cu
有银白色固体析出,溶液由无色变为蓝色
Cu + 2AgNO3 = 2Ag + Cu(NO3)2
>
典例精讲
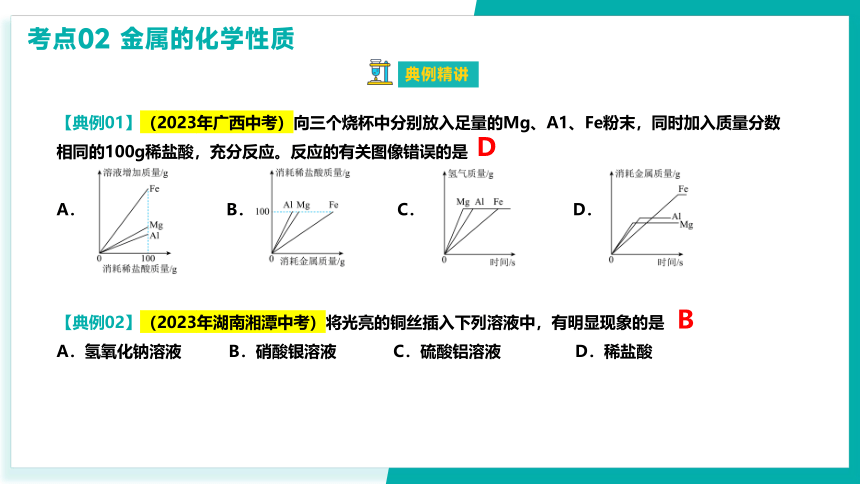
【典例01】(2023年广西中考)向三个烧杯中分别放入足量的Mg、A1、Fe粉末,同时加入质量分数相同的100g稀盐酸,充分反应。反应的有关图像错误的是
A. B. C. D.
D
【典例02】(2023年湖南湘潭中考)将光亮的铜丝插入下列溶液中,有明显现象的是
A.氢氧化钠溶液 B.硝酸银溶液 C.硫酸铝溶液 D.稀盐酸
B
考点02 金属的化学性质
举一反三
【演练01】(2023年山东潍坊中考)向两个盛有相同质量铝粉和铁粉的烧杯中,分别滴加相同浓度的稀硫酸,产生氢气的质量与加入稀硫酸的质量关系如图所示。下列说法正确的是
A.a点时,两个烧杯中的酸都恰好完全反应
B.b点时,两个烧杯中产生氢气的质量相同
C.c点时,两个烧杯中都有金属剩余
D.右侧曲线不能反映铁和铝的金属活动性强弱
CD
【演练02】(2023年山东聊城中考)为证明Fe、Cu、Ag三种金属的活动性强弱,下列实验方案能达到目的的是
A.将Fe、Cu、Ag分别放入稀盐酸中
B.将Cu分别放入FeCl2、AgNO3溶液中
C.将Cu、Ag分别放入FeSO4溶液中
D.将Fe放入稀盐酸、Cu放入AgNO3溶液中
B
考点02 金属的化学性质
合金的组成及性质
考点03
实验方案
实验课题
实验报告
实验总结
考点03 合金的组成及性质
考点梳理
合
金
概念:在金属中加热熔合某些金属或非金属,制得的具有 特性的 。
特性:合金与组成它的纯金属相比,一般硬度更 、熔点更 、抗腐蚀性更 。
举例:常见的铁合金有生铁(含碳__________)和钢(含碳__________)
金属
混合物
大
低
强
2%~4.3%
0.03%~2%
典例精讲
【典例01】(2023年湖南长沙中考)2023 年我国自主研制的大型灭火、水上救援水陆两栖飞机“鲲龙”已成功首飞,制造该飞机使用了铝锂合金等多种合金。下列有关铝锂合金的说法正确的是
A.铝锂合金的熔点比纯铝更高 B.铝锂合金的抗腐蚀性能非常差
C.铝锂合金是混合物 D.铝锂合金的硬度比纯铝小
C
A
考点03 合金的组成及性质
【典例02】(2023年甘肃兰州中考)中国文化博大精深。下列对相关内容解释不合理的是
A.“春蚕到死丝方尽,蜡炬成灰泪始干”——只涉及化学变化
B.“驱遣阳光充炭火,烧干海水变银山”——海水“晒盐”
C.“水晶帘动微风起,满架蔷薇一院香”——分子在不断地运动
D.“金柔锡柔,合两柔则刚”——合金的硬度比组成它的纯金属的大
举一反三
【演练01】(2023年宁夏中考)飞船使用了大量的铝合金材料,铝合金相比纯铝的优点是 (填序号)。
A.硬度高 B.熔点高 C.抗腐蚀性强
AC
【演练02】(2023年辽宁阜新中考)生铁和钢是常见的两种铁合金,其主要区别是 。
A
考点03 合金的组成及性质
含碳量不同
【演练03】(2023年内蒙古赤峰中考)金属及其合金的用途很大程度上取决于它们的特性。下列对钛及其合金性质与用途对应关系的描述,错误的是
A.钛的韧性强——做导线
B.钛合金强度高、耐腐蚀——做医疗器械
C.钛合金具有良好的生物相容性——制造人造骨骼
D.钛合金密度小、强度高、耐高温——用作航空航天材料
一氧化碳与氧化铁的反应
考点04
实验方案
实验课题
实验报告
实验总结
考点04 一氧化碳与氧化铁的反应
考点梳理
实验室炼铁
原理: 。
现象:玻璃管中粉末________________________,试管中澄清石灰水_________,导管口尾气燃烧并产生_____色火焰。
顺序: 开始要先通一段时间CO,再加热Fe2O3的目的:
;
结束要先停止加热,待物质冷却后再停止通CO的目的:
。
3CO+Fe2O3 ???高温???? 2Fe+3CO2
?
由红棕色逐渐变黑
变浑浊
蓝
排尽装置内的空气,防止加热时发生爆炸
防止石灰水倒吸
防止铁粉再次被氧化
典例精讲
【典例01】(2023年黑龙江中考)下列有关实验操作正确的是
A.氢氧化钠沾到皮肤上先用大量水冲洗,再涂上盐酸
B.一氧化碳还原氧化铁的实验开始时,要先点燃酒精喷灯,再通入一氧化碳
C.检验氢气纯度,试管口向上移近火焰
D.测定食醋的酸碱度时,用玻璃棒蘸取待测液滴到pH试纸上,把试纸显示的颜色与标准比色卡比较
D
考点04 一氧化碳与氧化铁的反应
【典例02】(2023年青海西宁中考)以实验为基础是化学学科的重要特征之一?下图所示实验是一氧化碳还原氧化铁的部分实验装置,实验中玻璃管内出现的现象是 ?
红棕色粉末逐渐变黑
【演练02】(2023年黑龙江绥化中考)将一氧化碳和铁的氧化物FexOy置于密闭容器中,一定条件下充分反应。反应过程中容器内部分物质的质量变化如图所示。下列说法正确的是
A.m的值为19.6
B.参加反应的铁的氧化物的质量为16g
C.当CO2质量为4.4g时,容器内CO的质量为14g
D.铁的氧化物中x:y=2:3
举一反三
【演练01】(2023年辽宁丹东中考)下列图示是CO还原Fe2O3的部分实验装置,写出装置A中CO还原Fe2O3的化学方程式 ;从环保角度考虑,写出一种尾气处理的方法 。
C
考点04 一氧化碳与氧化铁的反应
3CO+Fe2O3 ???高温???? 2Fe+3CO2
?
用一燃着的酒精灯放在尾气处理处,将尾气点燃
工业炼铁
考点05
实验方案
实验课题
实验报告
实验总结
考点05 工业炼铁
考点梳理
工业炼铁
原料:铁矿石、焦炭、石灰石和空气等
主要设备:炼铁高炉
主要反应:
(以赤铁矿为原料)
①____________________(提供热量)
②____________________(提供还原剂)
③___________________________
C+O2 ???高温???? CO2
?
CO2+C ???高温???? 2CO
?
3CO+Fe2O3 ???高温???? 2Fe+3CO2
?
典例精讲
【典例01】(2023内蒙古呼和浩特中考)人类社会的文明进步与金属材料的发展密切相关。
明代《天工开物》中记载“炒钢法”的生产工艺是现代钢铁冶炼的先者。现代高炉炼铁中一氧化碳与氧化铁反应的化学方程式为 ,原料中焦炭的作用是提供热量和 (用化学方程式回答)。
考点05 工业炼铁
【典例02】(2023江苏连云港中考)工业上冶炼钢铁的主要工艺流程如下:
??
①石灰石(主要成分为CaCO3)在高温下可将铁矿石中SiO2的转变为炉渣(CaSiO3),同时生成一种氧化物。该反应的化学方程式为 。
②从物质组成的角度分析,炼钢炉中通入O2的目的是 。
3CO+Fe2O3 ???高温???? 2Fe+3CO2
?
CO2+C ???高温???? 2CO
?
降低生铁中C元素的含量
CaCO3+SiO2 CaSiO3+CO2↑
高温
举一反三
【演练01】(2023年河北中考)某小组同学对炼铁高炉中发生的主要反应进行了知识网络建构,各物质之间的转化关系如图所示(反应条件已略去)。A~H是初中化学常见物质,其中B、D、G为高炉炼铁原料的主要成分,且G为红棕色氧化物。
??
请回答下列问题:
(1)G的化学式为 。
(2)反应②的基本反应类型为 。
(3)反应③的化学方程式为 。
(4)反应①在高炉炼铁中的作用是 (写一条即可)。
考点05 工业炼铁
Fe2O3
分解反应
CO2+C ???高温???? 2CO
?
提供热量/提供还原剂
钢铁锈蚀的条件及探究
考点06
实验方案
实验课题
实验报告
实验总结
考点06 钢铁锈蚀的条件及探究
考点梳理
钢铁的生锈
铁生锈的条件:铁与 同时接触。
酸和氯化钠溶液能 。
铁锈的主要成分:主要成分是 ,质地 ,不能阻止内层的铁与氧气和水接触,对铁起不到保护作用。
水和氧气
Fe2O3
疏松多孔
加快铁的锈蚀
典例精讲
【典例01】(2023年湖南常德中考)常德滨湖公园的“金刚塔”,俗称“铁树”,始建于北宋建隆年间。铁生锈的条件为 ,铁锈主要成分为 (填化学式)。
考点06 钢铁锈蚀的条件及探究
【典例02】(2023年安徽中考)某兴趣小组进行铁锈蚀的实验探究。该小组利用如下装置对铁钉锈蚀的条件进行探究、一段时间后,在A和B中没有观察到明显现象,C和D中铁钉有锈蚀。
??
(1)B中将蒸馏水煮沸的目的是 。
(2)ABD对比,说明铁钉锈蚀需要的物质是 ;C中的铁钉比D中的锈蚀更严重,原因是 。
与水和氧气同时接触
Fe2O3
除去水中溶解的氧气
氧气和水
C中的铁钉与氧气和水充分接触
举一反三
【演练01】(2023年湖南株洲中考)下列有关说法正确的是
A.纤维素不能被人体消化,所以食物中的纤维素对人体毫无意义
B.“墙内开花墙外香”是因为分子之间存在间隔
C.干冰升华时,吸收大量的热,因此可作制冷剂
D.铁表面能生成—层致密的氧化铁(Fe2O3)薄膜,阻止铁进一步氧化
考点06 钢铁锈蚀的条件及探究
c
【演练02】(2023年辽宁中考)早在春秋战国时期,我国就开始生产和使用铁器。
【铁的锈蚀和防护】下列环境中的铁制品最容易生锈的是_____(填字母)。
A.未擦干的铁锅 B.喷油漆的栏杆 C.盛水的不锈钢水杯
A
防止钢铁生锈的方法
考点07
实验方案
实验课题
实验报告
实验总结
考点07 防止钢铁生锈的方法
考点梳理
防止钢铁生锈的方法
原理:破坏铁生锈的条件,使铁制品 。
方法
①保持铁制品 ;
②在钢铁表面 (喷漆、涂油、电镀、搪瓷等);
③ 改变 (制成不锈钢)。
隔绝空气或隔绝水
表面洁净和干燥
覆盖保护膜
内部结构
典例精讲
【典例01】(2023山东青岛中考)防止金属锈蚀能有效保护金属资源。下列防锈方法中,与其它三种方法原理不同的是
A.表面涂油 B.表面刷漆 C.覆盖塑料 D.制成合金
D
【典例02】(2023山东淄博中考)在钢铁制品表面刷油漆可防止锈蚀,其原因是 。
考点07 防止钢铁生锈的方法
隔绝空气和水
【典例03】(2023辽宁阜新中考)防止自行车链条生锈常用的方法是 。
涂油
举一反三
【演练01】(2023年湖北中考)我国的钢铁年产量很高,但因锈蚀造成的损失也很惊人,铁制品锈蚀的过程实际上是铁与空气中的氧气和水等物质发生化学反应的过程。请写出一条防止铁制品生锈的具体方法: 。
【演练02】(2023年贵州中考)对钢铁制品进行“发蓝”处理,使其表面生成一层致密的氧化膜,能有效防止钢铁锈蚀。
①“发蓝”过程属于 (填“物理”或“化学”)变化。
②“发蓝”能防止钢铁锈蚀的原因是 。
考点07 防止钢铁生锈的方法
刷漆
化学
隔绝氧气和水
废金属的回收利用
考点08
实验方案
实验课题
实验报告
实验总结
考点08 废金属的回收利用
考点梳理
废金属的回收利用
危害
①造成 ;
②镉、汞等有毒金属会 。
保护金属资源的有效途径
①防止 ;
②有计划、合理地 ;
③ 废旧金属;
④寻找金属的 。
资源浪费
对环境造成污染
金属生锈
开采矿物
回收利用
替代品
典例精讲
【典例01】(2023四川眉山中考)金属矿物不能再生。下列能有效保护钛金属资源的措施是 。
A.回收利用废旧钛金属制品
B.任意开采钛金属矿石
C.钛金属抗腐蚀性能好,可随意堆放储存
D.寻找、开发钛金属的代替品
【典例02】(2023黑龙江哈尔滨中考)下列叙述错误的是
A.炒菜时油锅中的油不慎着火,可用锅盖盖灭
B.可以用肥皂水区分硬水和软水
C.废旧金属的回收和利用,可以节约金属资源
D.催化剂在化学反应后质量减少
考点08 废金属的回收利用
AD
D
举一反三
【演练01】(2023辽宁丹东中考)世界上每年因腐蚀而报废的铁,50%以上得到了回收利用。回收利用废旧金属的意义是 (答一点即可)。
【演练02】(2023广东中考)下列劳动实践与所述的化学知识没有关联的是
考点08 废金属的回收利用
节约资源
选项
劳动实践
化学知识
A
用铅笔芯制作电极
石墨有导电性
B
用食醋除水垢
水垢能与食醋反应
C
回收铝制易拉罐
铝易与氧气反应
D
用洗涤剂去油污
洗涤剂能乳化油污
C
实验方案
实验课题
实验报告
实验总结
谢谢您的观看
THANKS
汇报人 / 稻小壳 >
典例精讲
考点梳理
思维导图
金属的冶炼与利用
第5章
考点串讲PPT
目
录
CONTENTS
1
金属的性质和利用
2
金属矿物 铁的冶炼
3
金属防护和废金属回收
思维导图
金属的物理性质和用途
考点01
考点01 金属的物理性质和用途
{5940675A-B579-460E-94D1-54222C63F5DA}物理性质
用 途
共性
________性
制作导线
________性
制作炊具
________性
冲压成各种形状
有金属光泽
制作各种装饰品
特性
颜色:大多数金属呈 色,铜呈 色,金呈 色,
铁粉呈 色
状态:常温下,大多数金属为固体,而 为液体
导 电
导 热
延 展
银白
紫红
黄
汞
黑
考点梳理
典例精讲
【典例01】(2023年江西中考)大国工匠秦世俊展现数控技术所使用的铝箔,是由0.01mm铝块加工而成,这体现了铝具有
A.密度小 B.导电性 C.导热性 D.延展性
D
【典例02】(2023年四川巴中中考)牛奶盒内附有一层铝箔,利用了铝的 (选填“延展性”或“导热性”)。
考点01 金属的物理性质和用途
延展性
【典例03】(2023年辽宁丹东中考)铁铸成铁锅是利用了铁具有良好的 性;铁锅用于烹饪食物是利用铁具有良好的 性。
延展
导热
举一反三
【演练01】(2023年黑龙江中考)物质的性质决定用途。下列各物质的用途与性质对应关系正确的是
A.银有金属光泽,可用于制造电线
B.氮气是无色无味的气体,可用作保护气
C.石墨能导电,可用于制作铅笔芯
D.氢气具有可燃性,能作高能燃料
D
【演练02】(2023年甘肃金昌中考)下列生活用品利用金属良好导热性的是 (填序号)。
a.镀铬水龙头????????????????????b.铸铁暖气片????????????????c.包糖果的铝箔
b
考点01 金属的物理性质和用途
【演练03】(2023年江苏苏州中考)太阳能电池板需要使用铝合金箔片,铝合金能加工成箔片是利用了金属的 性。
延展
金属的化学性质
考点02
实验方案
实验课题
实验报告
实验总结
考点02 金属的化学性质——与氧气反应
考点梳理
与氧气反应
镁:在空气中点燃,剧烈燃烧,发出______________,生成白色固体,化学方程式为__________________
铝:具有很好的抗腐蚀性能,原因是__________________________ _____________________________________________________________。其与氧气反应的化学方程式为________________________
铁:在氧气中点燃,剧烈燃烧,_____________________________
铜:在空气中加热,表面生成_____色物质氧气反应
金:“真金不怕火炼”说明金在高温时________与氧气反应
耀眼的白光
2Mg+O2 ???点燃???? 2MgO
?
铝在空气中与氧气反应,表面生成一层致密的氧化铝(Al2O3)薄膜,阻止铝进一步氧化
4Al+3O2 ═══ 2Al2O3
火星四射,生成黑色固体
黑
不能
考点02 金属的化学性质——与酸反应
考点梳理
与酸反应
镁:与盐酸反应非常剧烈,化学方程式为________________________
锌:与盐酸反应较剧烈,化学方程式为_________________________
铁:与盐酸反应慢,化学方程式为_____________________________,
溶液由无色变为______色
铜:加入盐酸, 。
Mg+2HCl ═══ MgCl2+H2↑
Zn+2HCl ═══ ZnCl2+H2↑
Fe+2HCl ═══ FeCl2+H2↑
浅绿
无明显现象
考点02 金属的化学性质——与金属化合物溶液反应
考点梳理
与金属化合物溶液反应
铁与硫酸铜:
现象为___________________________________________________
化学方程式为_____________________________
铜与硝酸银:
现象为____________________________________________________
化学方程式为_______________________________
铜与硫酸铝:
无明显现象,证明活动性铝_____铜(填“>”或“<”)
铁的表面有红色固体析出,溶液由蓝色变为浅绿色
Fe+CuSO4 ══ FeSO4 +Cu
有银白色固体析出,溶液由无色变为蓝色
Cu + 2AgNO3 = 2Ag + Cu(NO3)2
>
典例精讲
【典例01】(2023年广西中考)向三个烧杯中分别放入足量的Mg、A1、Fe粉末,同时加入质量分数相同的100g稀盐酸,充分反应。反应的有关图像错误的是
A. B. C. D.
D
【典例02】(2023年湖南湘潭中考)将光亮的铜丝插入下列溶液中,有明显现象的是
A.氢氧化钠溶液 B.硝酸银溶液 C.硫酸铝溶液 D.稀盐酸
B
考点02 金属的化学性质
举一反三
【演练01】(2023年山东潍坊中考)向两个盛有相同质量铝粉和铁粉的烧杯中,分别滴加相同浓度的稀硫酸,产生氢气的质量与加入稀硫酸的质量关系如图所示。下列说法正确的是
A.a点时,两个烧杯中的酸都恰好完全反应
B.b点时,两个烧杯中产生氢气的质量相同
C.c点时,两个烧杯中都有金属剩余
D.右侧曲线不能反映铁和铝的金属活动性强弱
CD
【演练02】(2023年山东聊城中考)为证明Fe、Cu、Ag三种金属的活动性强弱,下列实验方案能达到目的的是
A.将Fe、Cu、Ag分别放入稀盐酸中
B.将Cu分别放入FeCl2、AgNO3溶液中
C.将Cu、Ag分别放入FeSO4溶液中
D.将Fe放入稀盐酸、Cu放入AgNO3溶液中
B
考点02 金属的化学性质
合金的组成及性质
考点03
实验方案
实验课题
实验报告
实验总结
考点03 合金的组成及性质
考点梳理
合
金
概念:在金属中加热熔合某些金属或非金属,制得的具有 特性的 。
特性:合金与组成它的纯金属相比,一般硬度更 、熔点更 、抗腐蚀性更 。
举例:常见的铁合金有生铁(含碳__________)和钢(含碳__________)
金属
混合物
大
低
强
2%~4.3%
0.03%~2%
典例精讲
【典例01】(2023年湖南长沙中考)2023 年我国自主研制的大型灭火、水上救援水陆两栖飞机“鲲龙”已成功首飞,制造该飞机使用了铝锂合金等多种合金。下列有关铝锂合金的说法正确的是
A.铝锂合金的熔点比纯铝更高 B.铝锂合金的抗腐蚀性能非常差
C.铝锂合金是混合物 D.铝锂合金的硬度比纯铝小
C
A
考点03 合金的组成及性质
【典例02】(2023年甘肃兰州中考)中国文化博大精深。下列对相关内容解释不合理的是
A.“春蚕到死丝方尽,蜡炬成灰泪始干”——只涉及化学变化
B.“驱遣阳光充炭火,烧干海水变银山”——海水“晒盐”
C.“水晶帘动微风起,满架蔷薇一院香”——分子在不断地运动
D.“金柔锡柔,合两柔则刚”——合金的硬度比组成它的纯金属的大
举一反三
【演练01】(2023年宁夏中考)飞船使用了大量的铝合金材料,铝合金相比纯铝的优点是 (填序号)。
A.硬度高 B.熔点高 C.抗腐蚀性强
AC
【演练02】(2023年辽宁阜新中考)生铁和钢是常见的两种铁合金,其主要区别是 。
A
考点03 合金的组成及性质
含碳量不同
【演练03】(2023年内蒙古赤峰中考)金属及其合金的用途很大程度上取决于它们的特性。下列对钛及其合金性质与用途对应关系的描述,错误的是
A.钛的韧性强——做导线
B.钛合金强度高、耐腐蚀——做医疗器械
C.钛合金具有良好的生物相容性——制造人造骨骼
D.钛合金密度小、强度高、耐高温——用作航空航天材料
一氧化碳与氧化铁的反应
考点04
实验方案
实验课题
实验报告
实验总结
考点04 一氧化碳与氧化铁的反应
考点梳理
实验室炼铁
原理: 。
现象:玻璃管中粉末________________________,试管中澄清石灰水_________,导管口尾气燃烧并产生_____色火焰。
顺序: 开始要先通一段时间CO,再加热Fe2O3的目的:
;
结束要先停止加热,待物质冷却后再停止通CO的目的:
。
3CO+Fe2O3 ???高温???? 2Fe+3CO2
?
由红棕色逐渐变黑
变浑浊
蓝
排尽装置内的空气,防止加热时发生爆炸
防止石灰水倒吸
防止铁粉再次被氧化
典例精讲
【典例01】(2023年黑龙江中考)下列有关实验操作正确的是
A.氢氧化钠沾到皮肤上先用大量水冲洗,再涂上盐酸
B.一氧化碳还原氧化铁的实验开始时,要先点燃酒精喷灯,再通入一氧化碳
C.检验氢气纯度,试管口向上移近火焰
D.测定食醋的酸碱度时,用玻璃棒蘸取待测液滴到pH试纸上,把试纸显示的颜色与标准比色卡比较
D
考点04 一氧化碳与氧化铁的反应
【典例02】(2023年青海西宁中考)以实验为基础是化学学科的重要特征之一?下图所示实验是一氧化碳还原氧化铁的部分实验装置,实验中玻璃管内出现的现象是 ?
红棕色粉末逐渐变黑
【演练02】(2023年黑龙江绥化中考)将一氧化碳和铁的氧化物FexOy置于密闭容器中,一定条件下充分反应。反应过程中容器内部分物质的质量变化如图所示。下列说法正确的是
A.m的值为19.6
B.参加反应的铁的氧化物的质量为16g
C.当CO2质量为4.4g时,容器内CO的质量为14g
D.铁的氧化物中x:y=2:3
举一反三
【演练01】(2023年辽宁丹东中考)下列图示是CO还原Fe2O3的部分实验装置,写出装置A中CO还原Fe2O3的化学方程式 ;从环保角度考虑,写出一种尾气处理的方法 。
C
考点04 一氧化碳与氧化铁的反应
3CO+Fe2O3 ???高温???? 2Fe+3CO2
?
用一燃着的酒精灯放在尾气处理处,将尾气点燃
工业炼铁
考点05
实验方案
实验课题
实验报告
实验总结
考点05 工业炼铁
考点梳理
工业炼铁
原料:铁矿石、焦炭、石灰石和空气等
主要设备:炼铁高炉
主要反应:
(以赤铁矿为原料)
①____________________(提供热量)
②____________________(提供还原剂)
③___________________________
C+O2 ???高温???? CO2
?
CO2+C ???高温???? 2CO
?
3CO+Fe2O3 ???高温???? 2Fe+3CO2
?
典例精讲
【典例01】(2023内蒙古呼和浩特中考)人类社会的文明进步与金属材料的发展密切相关。
明代《天工开物》中记载“炒钢法”的生产工艺是现代钢铁冶炼的先者。现代高炉炼铁中一氧化碳与氧化铁反应的化学方程式为 ,原料中焦炭的作用是提供热量和 (用化学方程式回答)。
考点05 工业炼铁
【典例02】(2023江苏连云港中考)工业上冶炼钢铁的主要工艺流程如下:
??
①石灰石(主要成分为CaCO3)在高温下可将铁矿石中SiO2的转变为炉渣(CaSiO3),同时生成一种氧化物。该反应的化学方程式为 。
②从物质组成的角度分析,炼钢炉中通入O2的目的是 。
3CO+Fe2O3 ???高温???? 2Fe+3CO2
?
CO2+C ???高温???? 2CO
?
降低生铁中C元素的含量
CaCO3+SiO2 CaSiO3+CO2↑
高温
举一反三
【演练01】(2023年河北中考)某小组同学对炼铁高炉中发生的主要反应进行了知识网络建构,各物质之间的转化关系如图所示(反应条件已略去)。A~H是初中化学常见物质,其中B、D、G为高炉炼铁原料的主要成分,且G为红棕色氧化物。
??
请回答下列问题:
(1)G的化学式为 。
(2)反应②的基本反应类型为 。
(3)反应③的化学方程式为 。
(4)反应①在高炉炼铁中的作用是 (写一条即可)。
考点05 工业炼铁
Fe2O3
分解反应
CO2+C ???高温???? 2CO
?
提供热量/提供还原剂
钢铁锈蚀的条件及探究
考点06
实验方案
实验课题
实验报告
实验总结
考点06 钢铁锈蚀的条件及探究
考点梳理
钢铁的生锈
铁生锈的条件:铁与 同时接触。
酸和氯化钠溶液能 。
铁锈的主要成分:主要成分是 ,质地 ,不能阻止内层的铁与氧气和水接触,对铁起不到保护作用。
水和氧气
Fe2O3
疏松多孔
加快铁的锈蚀
典例精讲
【典例01】(2023年湖南常德中考)常德滨湖公园的“金刚塔”,俗称“铁树”,始建于北宋建隆年间。铁生锈的条件为 ,铁锈主要成分为 (填化学式)。
考点06 钢铁锈蚀的条件及探究
【典例02】(2023年安徽中考)某兴趣小组进行铁锈蚀的实验探究。该小组利用如下装置对铁钉锈蚀的条件进行探究、一段时间后,在A和B中没有观察到明显现象,C和D中铁钉有锈蚀。
??
(1)B中将蒸馏水煮沸的目的是 。
(2)ABD对比,说明铁钉锈蚀需要的物质是 ;C中的铁钉比D中的锈蚀更严重,原因是 。
与水和氧气同时接触
Fe2O3
除去水中溶解的氧气
氧气和水
C中的铁钉与氧气和水充分接触
举一反三
【演练01】(2023年湖南株洲中考)下列有关说法正确的是
A.纤维素不能被人体消化,所以食物中的纤维素对人体毫无意义
B.“墙内开花墙外香”是因为分子之间存在间隔
C.干冰升华时,吸收大量的热,因此可作制冷剂
D.铁表面能生成—层致密的氧化铁(Fe2O3)薄膜,阻止铁进一步氧化
考点06 钢铁锈蚀的条件及探究
c
【演练02】(2023年辽宁中考)早在春秋战国时期,我国就开始生产和使用铁器。
【铁的锈蚀和防护】下列环境中的铁制品最容易生锈的是_____(填字母)。
A.未擦干的铁锅 B.喷油漆的栏杆 C.盛水的不锈钢水杯
A
防止钢铁生锈的方法
考点07
实验方案
实验课题
实验报告
实验总结
考点07 防止钢铁生锈的方法
考点梳理
防止钢铁生锈的方法
原理:破坏铁生锈的条件,使铁制品 。
方法
①保持铁制品 ;
②在钢铁表面 (喷漆、涂油、电镀、搪瓷等);
③ 改变 (制成不锈钢)。
隔绝空气或隔绝水
表面洁净和干燥
覆盖保护膜
内部结构
典例精讲
【典例01】(2023山东青岛中考)防止金属锈蚀能有效保护金属资源。下列防锈方法中,与其它三种方法原理不同的是
A.表面涂油 B.表面刷漆 C.覆盖塑料 D.制成合金
D
【典例02】(2023山东淄博中考)在钢铁制品表面刷油漆可防止锈蚀,其原因是 。
考点07 防止钢铁生锈的方法
隔绝空气和水
【典例03】(2023辽宁阜新中考)防止自行车链条生锈常用的方法是 。
涂油
举一反三
【演练01】(2023年湖北中考)我国的钢铁年产量很高,但因锈蚀造成的损失也很惊人,铁制品锈蚀的过程实际上是铁与空气中的氧气和水等物质发生化学反应的过程。请写出一条防止铁制品生锈的具体方法: 。
【演练02】(2023年贵州中考)对钢铁制品进行“发蓝”处理,使其表面生成一层致密的氧化膜,能有效防止钢铁锈蚀。
①“发蓝”过程属于 (填“物理”或“化学”)变化。
②“发蓝”能防止钢铁锈蚀的原因是 。
考点07 防止钢铁生锈的方法
刷漆
化学
隔绝氧气和水
废金属的回收利用
考点08
实验方案
实验课题
实验报告
实验总结
考点08 废金属的回收利用
考点梳理
废金属的回收利用
危害
①造成 ;
②镉、汞等有毒金属会 。
保护金属资源的有效途径
①防止 ;
②有计划、合理地 ;
③ 废旧金属;
④寻找金属的 。
资源浪费
对环境造成污染
金属生锈
开采矿物
回收利用
替代品
典例精讲
【典例01】(2023四川眉山中考)金属矿物不能再生。下列能有效保护钛金属资源的措施是 。
A.回收利用废旧钛金属制品
B.任意开采钛金属矿石
C.钛金属抗腐蚀性能好,可随意堆放储存
D.寻找、开发钛金属的代替品
【典例02】(2023黑龙江哈尔滨中考)下列叙述错误的是
A.炒菜时油锅中的油不慎着火,可用锅盖盖灭
B.可以用肥皂水区分硬水和软水
C.废旧金属的回收和利用,可以节约金属资源
D.催化剂在化学反应后质量减少
考点08 废金属的回收利用
AD
D
举一反三
【演练01】(2023辽宁丹东中考)世界上每年因腐蚀而报废的铁,50%以上得到了回收利用。回收利用废旧金属的意义是 (答一点即可)。
【演练02】(2023广东中考)下列劳动实践与所述的化学知识没有关联的是
考点08 废金属的回收利用
节约资源
选项
劳动实践
化学知识
A
用铅笔芯制作电极
石墨有导电性
B
用食醋除水垢
水垢能与食醋反应
C
回收铝制易拉罐
铝易与氧气反应
D
用洗涤剂去油污
洗涤剂能乳化油污
C
实验方案
实验课题
实验报告
实验总结
谢谢您的观看
THANKS
汇报人 / 稻小壳 >
同课章节目录
- 第1章 开启化学之门
- 第1节 化学给我们带来什么
- 第2节 化学研究些什么
- 第3节 怎样学习和研究化学
- 第2章 身边的化学物质
- 第1节 性质活泼的氧气
- 第2节 奇妙的二氧化碳
- 第3节 自然界中的水
- 基础实验1 氧气的制取与性质
- 基础实验2 二氧化碳的制取与性质
- 第3章 物质构成的奥秘
- 第1节 构成物质的基本微粒
- 第2节 组成物质的化学元素
- 第3节 物质的组成
- 第4章 认识化学变化
- 第1节 常见的化学反应——燃烧
- 第2节 化学反应中的质量关系
- 第3节 化学方程式的书写与运用
- 基础实验3 物质燃烧的条件
- 第5章 金属的冶炼与利用
- 第1节 金属的性质和利用
- 第2节 金属矿物 铁的冶炼
- 第3节 金属防护和废金属回收
- 基础实验4 常见金属的性质
