天津市南仓中学2023-2024学年高一上学期12月期中考试化学试题(无答案)
文档属性
| 名称 | 天津市南仓中学2023-2024学年高一上学期12月期中考试化学试题(无答案) |  | |
| 格式 | docx | ||
| 文件大小 | 247.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-12-12 10:50:05 | ||
图片预览

文档简介
天津市南仓中学2023-2024学年高一上学期12月期中考试
(化学学科)
本试卷分为第Ⅰ卷(选择题)和第Ⅱ卷两部分,共100分,考试用时60分钟.第Ⅰ卷1至2页,第Ⅱ卷第3页.
答卷前,考生务必将自己的姓名、考生号填写在答题纸上.答卷时,考生务必将答案涂写在答题纸上,答在试卷上的无效.
祝各位考生考试顺利!
第Ⅰ卷
注意事项:
1.每小题选出答案后,用铅笔将机读卡上对应题目的答案标号涂黑.如需改动,用橡皮擦干净后,再选涂其他答案标号.
2.本卷共14小题,共42分.
3.可能用到的相对原子质量:H 1 C 12 Na 23 O 16 S 32 Cl 35.5
一、选择题(每小题3分,共42分)
1.《本草纲目》记载到:“慈石治肾家诸病,而通耳明目.慈石,色轻紫,石上皲涩,可吸连针铁,俗谓之熁铁石.”“慈石”的主要成分是( )
A.铁 B.氧化铜 C.氧化铁 D.四氧化三铁
2.下列叙述不能体现“化学让生活更美好”这一主旨的是( )
A.风力发电,让能源更清洁 B.合成塑料,让材料更丰富
C.合成药物,让人类更健康 D.环保涂料,让环境更宜居
3.下列各组物质,按化合物、单质、混合物的顺序排列的是( )
A.烧碱、液态氧、碘酒 B.浓硫酸、苛性钠、磁性氧化铁
C.干冰、铁、氯化氢 D.空气、氮气、胆矾
4.下列离子方程式书写正确的是( )
A.将稀硫酸滴在铜片上:
B.将氧化镁与稀盐酸混合:
C.将铜片插入硝酸银溶液中:
D.将稀盐酸滴在石灰石上:
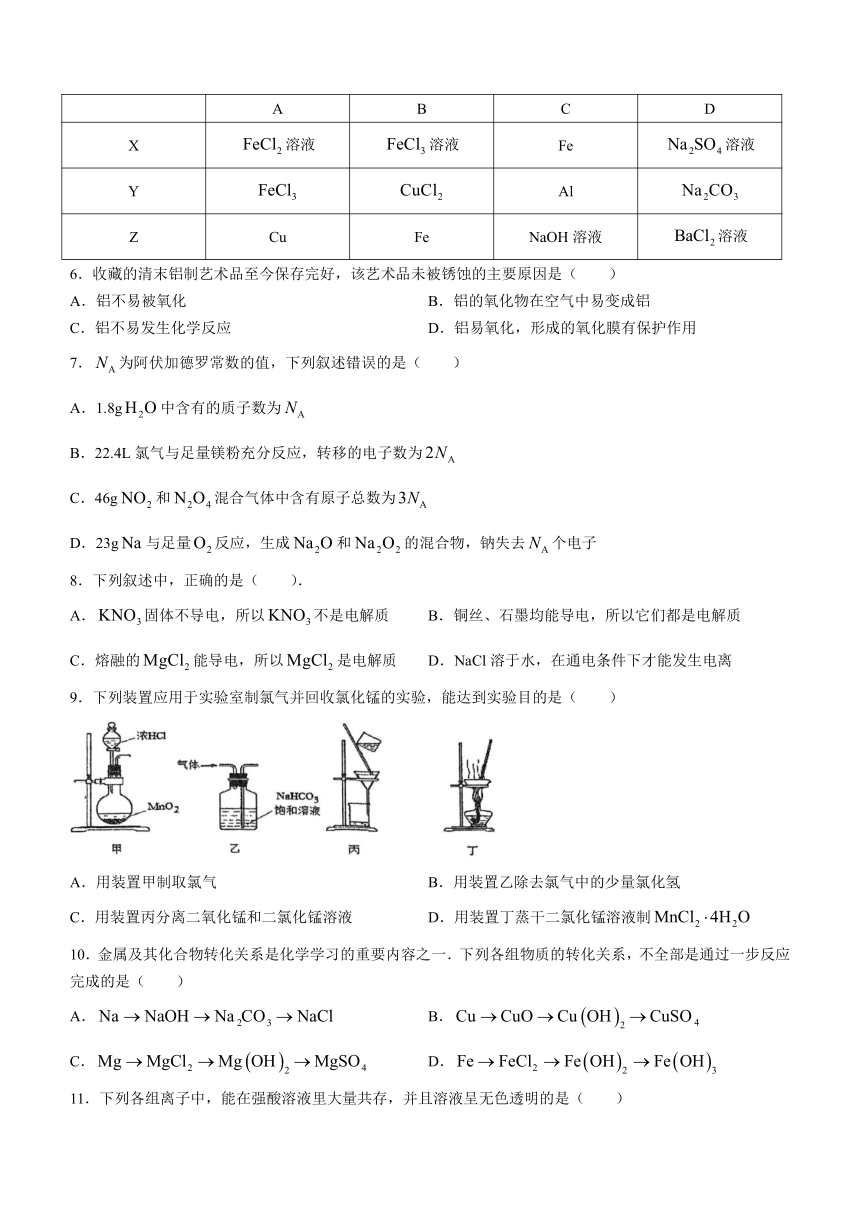
5.下列各组物质中,X是主要物质,Y是少量杂质,Z是为除去杂质所要加入的试剂,其中所加试剂正确的组合是( )
A B C D
X 溶液 溶液 Fe 溶液
Y Al
Z Cu Fe NaOH溶液 溶液
6.收藏的清末铝制艺术品至今保存完好,该艺术品未被锈蚀的主要原因是( )
A.铝不易被氧化 B.铝的氧化物在空气中易变成铝
C.铝不易发生化学反应 D.铝易氧化,形成的氧化膜有保护作用
7.为阿伏加德罗常数的值,下列叙述错误的是( )
A.1.8g中含有的质子数为
B.22.4L氯气与足量镁粉充分反应,转移的电子数为
C.46g和混合气体中含有原子总数为
D.23g与足量反应,生成和的混合物,钠失去个电子
8.下列叙述中,正确的是( ).
A.固体不导电,所以不是电解质 B.铜丝、石墨均能导电,所以它们都是电解质
C.熔融的能导电,所以是电解质 D.NaCl溶于水,在通电条件下才能发生电离
9.下列装置应用于实验室制氯气并回收氯化锰的实验,能达到实验目的是( )
A.用装置甲制取氯气 B.用装置乙除去氯气中的少量氯化氢
C.用装置丙分离二氧化锰和二氯化锰溶液 D.用装置丁蒸干二氯化锰溶液制
10.金属及其化合物转化关系是化学学习的重要内容之一.下列各组物质的转化关系,不全部是通过一步反应完成的是( )
A. B.
C. D.
11.下列各组离子中,能在强酸溶液里大量共存,并且溶液呈无色透明的是( )
A.、、、 B.、、、
C.、、、 D.、、、
12.下列实验现象,与新制氯水中的某些成分(括号内物质)没有关系的是( )
A.将固体加入新制氯水,有无色气泡()
B.使红色布条褪色(HClO)
C.向溶液中滴加氮水,再滴加KSCN溶液,发现呈红色()
D.滴加含有酚酞试液的NaOH溶液,红色褪去()
13.过氧化钠是一种制氧剂,它和二氧化碳反应方程式,下列说法正确的是( )
A.是氧化剂,是还原剂 B.是还原产物,是氧化产物
C.每转移4摩尔电子,有1摩尔氧气生成 D.1mol参加反应就会产生11.2L
14.下列叙述中,不正确的是( )
A.高温下,铁和水蒸气反应可以生成氢气
B.将饱和氯化铁溶液滴入沸水中,煮沸至红褐色,可以制得氢氧化铁胶体
C.在硫酸铁溶液中,加入铜粉至完全溶解后,又加入一定量的铁粉,充分反应后有残余固体,则残余固体可能为铁、铜混合物
D.加入氯化钡溶液有白色沉淀生成,再加稀盐酸,沉淀不消失,一定有
天津市南仓中学2023至2024学年度第一学期
高一年级教学质量过程性检测与诊断
(化学学科)
第Ⅱ卷
注意事项:
1.用黑色墨水的钢笔或签字笔将答案写在答题纸上.
2.本卷共4小题,共58分.
二、填空题(共4小题,共58分)
15.(共16分)和是两种常见的钠盐.
(1)用洁净的铂丝蘸取溶液置于酒精灯火焰上灼烧,火焰呈______色.
(2)等质量的和分别与足量的盐酸反应,在相同条件下产生的体积______(填“大于”“小于”或“等于”).
(3)若加热10.00g的碳酸钠和碳酸氢钠的混合物,使碳酸氢钠完全分解,混合物质量减少了2.48g,则原混合物中碳酸钠的质量分数为______.
(4)实验室中需2mol/L的溶液950mL,配制时应选用容量瓶的规格和称取的质量分别是______.
A.1000mL:212g B.950mL;543.4g C.任意规格;572g D.500mL;106g
需要的玻璃仪器有容量瓶、玻璃棒、烧杯、量筒,还缺少的玻璃仪器有______(填写仪器名称)若出现如下情况,其中将引起所配溶液浓度偏高的是______(填下列编号).
A.容量瓶实验前用蒸馏水洗干净,但未烘干 B.定容观察液面时俯视
C.未冷却至室温就开始定容 D.加蒸馏水时不慎超过了刻度
16.(共12分)
(1)电子工业常用的30%的溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板.刻蚀印刷电路板涉及的离子方程式为______,检验溶液中还有的试剂______.
(2)工业上制取漂白粉的化学反应方程式为______;
(3)铝分别与足量的NaOH溶液和稀硫酸反应,若两个反应在相同状况下放出等量的气体,则两个反应中消耗的铝的物质的量之比为______.
17.(共14分)现有金属单质A、B和气体甲、乙、丙及物质C、D、E、F、G,它们之间的转化关系如图所示(部分产物和反应条件省略).
请根据以上信息回答下列问题:
(1)写出下列物质的化学式:B______、丙______.
(2)写出下列反应的离子方程式:
反应①______;
反应④______.
(3)黄绿色气体乙的用途______(列举一例即可)
18.(共16分)根据要求填空:
(1)饮用水中的对人类健康会产生危害,为了降低饮用水中的浓度,可以在碱性条件下用铝粉将还原为,反应的化学方程式如下:
.
①请用“单线桥法”表示上述反应中电子转移的方向和数目.(请在答题纸的方程式上作答)
②该反应中,______是氧化剂,______是氧化产物.
③转移3mol电子,则所产生的氮气在标准状况下的体积为______.
(2)铁是人类较早使用的金属之一.
①鉴别胶体和溶液的常用方法是______.
②某研究性学习小组为测定溶液腐蚀铜后所得溶液的组成,进行了如下实验:取少量待测溶液,要验证上述溶液中含有,下列叙述正确的是______(填序号).
A.观察溶液是否呈浅绿色
B.取适量溶液,滴入酸性高锰酸钾溶液,若紫红色退去,证明溶液中含有
C.取适量溶液,滴入氯水,再滴入KSCN溶液,若显红色,证明溶液中含有
(化学学科)
本试卷分为第Ⅰ卷(选择题)和第Ⅱ卷两部分,共100分,考试用时60分钟.第Ⅰ卷1至2页,第Ⅱ卷第3页.
答卷前,考生务必将自己的姓名、考生号填写在答题纸上.答卷时,考生务必将答案涂写在答题纸上,答在试卷上的无效.
祝各位考生考试顺利!
第Ⅰ卷
注意事项:
1.每小题选出答案后,用铅笔将机读卡上对应题目的答案标号涂黑.如需改动,用橡皮擦干净后,再选涂其他答案标号.
2.本卷共14小题,共42分.
3.可能用到的相对原子质量:H 1 C 12 Na 23 O 16 S 32 Cl 35.5
一、选择题(每小题3分,共42分)
1.《本草纲目》记载到:“慈石治肾家诸病,而通耳明目.慈石,色轻紫,石上皲涩,可吸连针铁,俗谓之熁铁石.”“慈石”的主要成分是( )
A.铁 B.氧化铜 C.氧化铁 D.四氧化三铁
2.下列叙述不能体现“化学让生活更美好”这一主旨的是( )
A.风力发电,让能源更清洁 B.合成塑料,让材料更丰富
C.合成药物,让人类更健康 D.环保涂料,让环境更宜居
3.下列各组物质,按化合物、单质、混合物的顺序排列的是( )
A.烧碱、液态氧、碘酒 B.浓硫酸、苛性钠、磁性氧化铁
C.干冰、铁、氯化氢 D.空气、氮气、胆矾
4.下列离子方程式书写正确的是( )
A.将稀硫酸滴在铜片上:
B.将氧化镁与稀盐酸混合:
C.将铜片插入硝酸银溶液中:
D.将稀盐酸滴在石灰石上:
5.下列各组物质中,X是主要物质,Y是少量杂质,Z是为除去杂质所要加入的试剂,其中所加试剂正确的组合是( )
A B C D
X 溶液 溶液 Fe 溶液
Y Al
Z Cu Fe NaOH溶液 溶液
6.收藏的清末铝制艺术品至今保存完好,该艺术品未被锈蚀的主要原因是( )
A.铝不易被氧化 B.铝的氧化物在空气中易变成铝
C.铝不易发生化学反应 D.铝易氧化,形成的氧化膜有保护作用
7.为阿伏加德罗常数的值,下列叙述错误的是( )
A.1.8g中含有的质子数为
B.22.4L氯气与足量镁粉充分反应,转移的电子数为
C.46g和混合气体中含有原子总数为
D.23g与足量反应,生成和的混合物,钠失去个电子
8.下列叙述中,正确的是( ).
A.固体不导电,所以不是电解质 B.铜丝、石墨均能导电,所以它们都是电解质
C.熔融的能导电,所以是电解质 D.NaCl溶于水,在通电条件下才能发生电离
9.下列装置应用于实验室制氯气并回收氯化锰的实验,能达到实验目的是( )
A.用装置甲制取氯气 B.用装置乙除去氯气中的少量氯化氢
C.用装置丙分离二氧化锰和二氯化锰溶液 D.用装置丁蒸干二氯化锰溶液制
10.金属及其化合物转化关系是化学学习的重要内容之一.下列各组物质的转化关系,不全部是通过一步反应完成的是( )
A. B.
C. D.
11.下列各组离子中,能在强酸溶液里大量共存,并且溶液呈无色透明的是( )
A.、、、 B.、、、
C.、、、 D.、、、
12.下列实验现象,与新制氯水中的某些成分(括号内物质)没有关系的是( )
A.将固体加入新制氯水,有无色气泡()
B.使红色布条褪色(HClO)
C.向溶液中滴加氮水,再滴加KSCN溶液,发现呈红色()
D.滴加含有酚酞试液的NaOH溶液,红色褪去()
13.过氧化钠是一种制氧剂,它和二氧化碳反应方程式,下列说法正确的是( )
A.是氧化剂,是还原剂 B.是还原产物,是氧化产物
C.每转移4摩尔电子,有1摩尔氧气生成 D.1mol参加反应就会产生11.2L
14.下列叙述中,不正确的是( )
A.高温下,铁和水蒸气反应可以生成氢气
B.将饱和氯化铁溶液滴入沸水中,煮沸至红褐色,可以制得氢氧化铁胶体
C.在硫酸铁溶液中,加入铜粉至完全溶解后,又加入一定量的铁粉,充分反应后有残余固体,则残余固体可能为铁、铜混合物
D.加入氯化钡溶液有白色沉淀生成,再加稀盐酸,沉淀不消失,一定有
天津市南仓中学2023至2024学年度第一学期
高一年级教学质量过程性检测与诊断
(化学学科)
第Ⅱ卷
注意事项:
1.用黑色墨水的钢笔或签字笔将答案写在答题纸上.
2.本卷共4小题,共58分.
二、填空题(共4小题,共58分)
15.(共16分)和是两种常见的钠盐.
(1)用洁净的铂丝蘸取溶液置于酒精灯火焰上灼烧,火焰呈______色.
(2)等质量的和分别与足量的盐酸反应,在相同条件下产生的体积______(填“大于”“小于”或“等于”).
(3)若加热10.00g的碳酸钠和碳酸氢钠的混合物,使碳酸氢钠完全分解,混合物质量减少了2.48g,则原混合物中碳酸钠的质量分数为______.
(4)实验室中需2mol/L的溶液950mL,配制时应选用容量瓶的规格和称取的质量分别是______.
A.1000mL:212g B.950mL;543.4g C.任意规格;572g D.500mL;106g
需要的玻璃仪器有容量瓶、玻璃棒、烧杯、量筒,还缺少的玻璃仪器有______(填写仪器名称)若出现如下情况,其中将引起所配溶液浓度偏高的是______(填下列编号).
A.容量瓶实验前用蒸馏水洗干净,但未烘干 B.定容观察液面时俯视
C.未冷却至室温就开始定容 D.加蒸馏水时不慎超过了刻度
16.(共12分)
(1)电子工业常用的30%的溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板.刻蚀印刷电路板涉及的离子方程式为______,检验溶液中还有的试剂______.
(2)工业上制取漂白粉的化学反应方程式为______;
(3)铝分别与足量的NaOH溶液和稀硫酸反应,若两个反应在相同状况下放出等量的气体,则两个反应中消耗的铝的物质的量之比为______.
17.(共14分)现有金属单质A、B和气体甲、乙、丙及物质C、D、E、F、G,它们之间的转化关系如图所示(部分产物和反应条件省略).
请根据以上信息回答下列问题:
(1)写出下列物质的化学式:B______、丙______.
(2)写出下列反应的离子方程式:
反应①______;
反应④______.
(3)黄绿色气体乙的用途______(列举一例即可)
18.(共16分)根据要求填空:
(1)饮用水中的对人类健康会产生危害,为了降低饮用水中的浓度,可以在碱性条件下用铝粉将还原为,反应的化学方程式如下:
.
①请用“单线桥法”表示上述反应中电子转移的方向和数目.(请在答题纸的方程式上作答)
②该反应中,______是氧化剂,______是氧化产物.
③转移3mol电子,则所产生的氮气在标准状况下的体积为______.
(2)铁是人类较早使用的金属之一.
①鉴别胶体和溶液的常用方法是______.
②某研究性学习小组为测定溶液腐蚀铜后所得溶液的组成,进行了如下实验:取少量待测溶液,要验证上述溶液中含有,下列叙述正确的是______(填序号).
A.观察溶液是否呈浅绿色
B.取适量溶液,滴入酸性高锰酸钾溶液,若紫红色退去,证明溶液中含有
C.取适量溶液,滴入氯水,再滴入KSCN溶液,若显红色,证明溶液中含有
同课章节目录
