2023-2024学年高二下学期化学人教版(2019)选择性必修2课件 2-3-2分子的极性(共21张PPT)
文档属性
| 名称 | 2023-2024学年高二下学期化学人教版(2019)选择性必修2课件 2-3-2分子的极性(共21张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-12-12 00:00:00 | ||
图片预览






文档简介
(共21张PPT)
第二章 分子结构与性质
第三节 分子结构与物质性质
第2课时 分子的极性
共价键的极性:
键合原子的______不同,共用电子对发生_____,电负性小的原子显_________,电负性大的原子显_________。
知识回顾
电负性
正电性(δ+)
负电性(δ-)
偏移
共价键有极性和非极性,那么由共价键构成的分子是否也有极性和非极性呢?
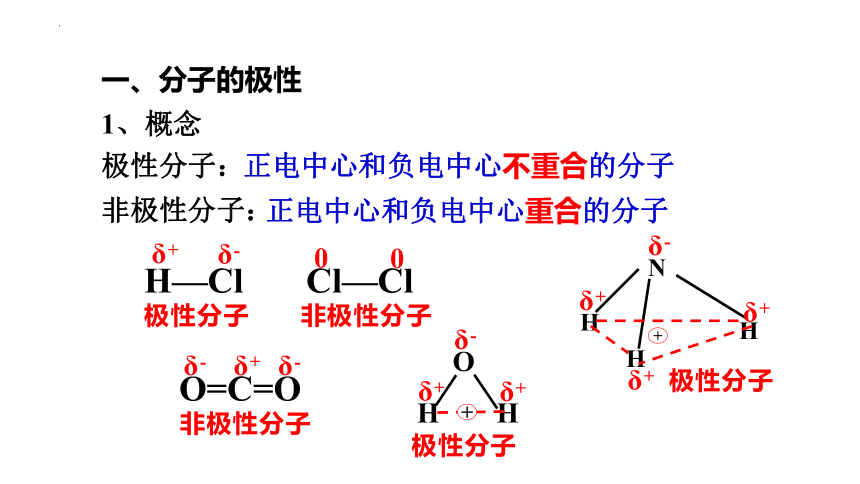
一、分子的极性
1、概念
极性分子:
非极性分子:
正电中心和负电中心不重合的分子
正电中心和负电中心重合的分子
H—Cl
O=C=O
Cl—Cl
δ-
δ+
δ-
0
0
δ+
δ-
极性分子
非极性分子
非极性分子
O
H H
N
H
H
H
δ-
δ+
δ+
+
极性分子
δ-
δ+
δ+
δ+
+
极性分子
2、分子极性的判断
(1)单原子分子
——非极性分子
(稀有气体)
(2)双原子分子
: 成键原子之间的共价键是否有极性
如:H2、O2、Cl2
如:HF、HCl
含非极性键的双原子分子——非极性分子
含极性键的双原子分子——极性分子
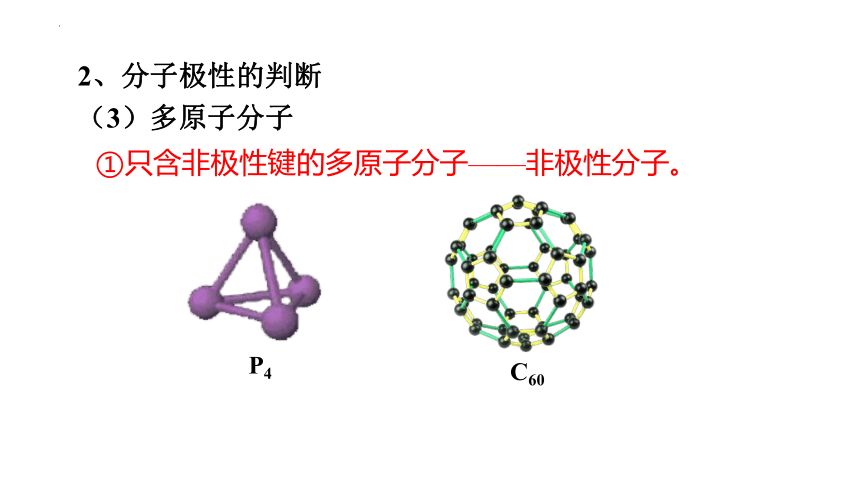
(3)多原子分子
2、分子极性的判断
①只含非极性键的多原子分子——非极性分子。
C60
P4
只含非极性键的分子一定是非极性分子。
资料卡片
臭氧是一种重要物质。大气高空的臭氧层保护了地球生物的生存;空气质量预报中臭氧含量是空气质量的重要指标;它还是有机合成的氧化剂、替代氯气的净水剂······
臭氧分子的空间结构与水分子的相似,其分子
有极性,但很微弱,仅是水分子的极性的28%。臭
氧分子中的共价键是极性键,其中心氧原子是呈正
电性的,而端位的两个氧原子是呈负电性的。由于臭氧的极性微弱,它在四氯化碳里的溶解度高于在水中的溶解度。
δ+
δ-
δ-
a.极性的向量和是否等于零
(3)多原子分子
2、分子极性的判断
②含极性键的多原子分子
向量和=0
: 非极性分子
向量和≠0
: 极性分子
极性向量可形象地描述极性键的电荷分布情况,极性向量指向的一端,说明该处负电荷更为集中。
H—Cl
δ+
δ-
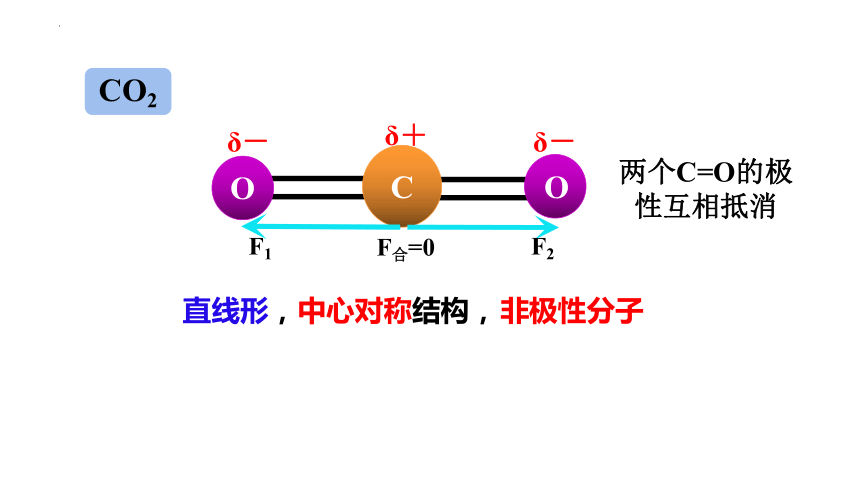
CO2
O
O
C
δ+
δ-
δ-
直线形,中心对称结构,
非极性分子
两个C=O的极性互相抵消
F1
F2
F合=0
H2O
δ+
δ+
δ-
H
H
O
V形,
中心不对称结构,
两个O-H键的极性向量和不为零
F1
F2
F合≠0
极性分子
δ-
δ+
δ+
δ+
NH3
H
H
N
H
三角锥形,
不对称结构,
极性分子
F合≠0
BF3
B
F
F
F
δ-
δ-
δ-
δ+
F合=0
平面三角形,
对称结构,
非极性分子
H
H
C
H
H
CH4
δ+
δ+
δ+
δ-
δ+
正四面体形,
对称结构,
非极性分子
V形、三角锥,四面体
a.极性的向量和是否等于零
(3)多原子分子
2、分子极性的判断
②含极性键的多原子分子
向量和=0
: 非极性分子
向量和≠0
: 极性分子
分子空间结构是否对称
对称
不对称
直线形、平面正三角形
正四面体、正八面体
→ 非极性分子
→ 极性分子
b.|中心原子化合价|
(3)多原子分子
2、分子极性的判断
②含极性键的多原子分子
=该元素的价电子数
: 非极性分子
≠0该元素的价电子数
: 极性分子
分子 BF3 CO2 PCl5 SO3 H2O NH3 SO2
化合价绝对值
价电子数
分子极性
3
3
4
4
5
5
6
6
2
6
3
5
4
6
非极性
非极性
非极性
非极性
极性
极性
极性
1.正误判断
(1)以非极性键结合的双原子分子一定是非极性分子( )
(2)以极性键结合的双原子分子一定是极性分子( )
(3)以极性键结合的分子一定是极性分子( )
(4)非极性分子只能是双原子单质分子( )
(5)非极性分子中一定含有非极性共价键( )
(6)由同种元素组成的非金属单质分子一定是非极性分子( )
(7)空间结构对称的ABn型分子为非极性分子( )
√
√
×
×
×
×
√
①只含非极性键的分子一定是非极性分子。
②含有极性键的分子,如果分子中各个键的极性的向量和等于零,则为非极性分子,否则为极性分子。
③极性分子中一定有极性键,非极性分子中不一定含有非极性键。例如CH4是非极性分子,只含有极性键。
含有非极性键的分子不一定为非极性分子,如H2O2是含有非极性键的极性分子。
2.回答下列问题。
①H2 ②O2 ③HCl ④P4 ⑤C60 ⑥CO2
⑦CH2==CH2 ⑧HCN ⑨H2O ⑩NH3 BF3
CH4 SO3 CH3Cl Ar H2O2
(1)只含非极性键的是_________(填序号,下同);,既含极性键又含非极性键的是______。
(2)属于非极性分子的是______________________,属于极性分子的是_____________。
①②④⑤
⑦
①②④⑤⑥⑦
③⑧⑨⑩
二、分子的极性的应用
1、微波炉加热原理
水是极性分子,正电中心和负电中心不重合,众多的水分子随电磁场定向转动,微波炉内的微波场以几亿的高频改变电场的方向,水分子间因频繁相互摩擦产生热能。
+
通电
-
二、分子的极性的应用
2、相似相溶
极性分子易溶于极性溶剂中,非极性分子易溶于非极性溶剂中。
水是极性溶剂,CCl4和苯是非极性溶剂,所以极性分子NH3易溶于水,难溶于CCl4和苯;
CCl4和苯能互溶。
表面活性剂的去污原理
表面活性剂在水中会形成亲水基团向外,疏水基团向内的胶束,由于油渍等污垢是疏水的,会被包裹在胶束内腔,在摩擦力的作用下油渍脱离,达到去污目的。
科学 技术 社会
表面活性剂:
有机分子,一端有极性(亲水基团),另一端非极性(疏水基团)
细胞膜是双分子膜,为什么双分子膜以头向外而尾向内的方式排列?
科学 技术 社会
细胞膜的两侧都是水溶液,水是极性分子,而构成膜的两性分子的头基是极性基团,尾基是非极性基 。
第二章 分子结构与性质
第三节 分子结构与物质性质
第2课时 分子的极性
共价键的极性:
键合原子的______不同,共用电子对发生_____,电负性小的原子显_________,电负性大的原子显_________。
知识回顾
电负性
正电性(δ+)
负电性(δ-)
偏移
共价键有极性和非极性,那么由共价键构成的分子是否也有极性和非极性呢?
一、分子的极性
1、概念
极性分子:
非极性分子:
正电中心和负电中心不重合的分子
正电中心和负电中心重合的分子
H—Cl
O=C=O
Cl—Cl
δ-
δ+
δ-
0
0
δ+
δ-
极性分子
非极性分子
非极性分子
O
H H
N
H
H
H
δ-
δ+
δ+
+
极性分子
δ-
δ+
δ+
δ+
+
极性分子
2、分子极性的判断
(1)单原子分子
——非极性分子
(稀有气体)
(2)双原子分子
: 成键原子之间的共价键是否有极性
如:H2、O2、Cl2
如:HF、HCl
含非极性键的双原子分子——非极性分子
含极性键的双原子分子——极性分子
(3)多原子分子
2、分子极性的判断
①只含非极性键的多原子分子——非极性分子。
C60
P4
只含非极性键的分子一定是非极性分子。
资料卡片
臭氧是一种重要物质。大气高空的臭氧层保护了地球生物的生存;空气质量预报中臭氧含量是空气质量的重要指标;它还是有机合成的氧化剂、替代氯气的净水剂······
臭氧分子的空间结构与水分子的相似,其分子
有极性,但很微弱,仅是水分子的极性的28%。臭
氧分子中的共价键是极性键,其中心氧原子是呈正
电性的,而端位的两个氧原子是呈负电性的。由于臭氧的极性微弱,它在四氯化碳里的溶解度高于在水中的溶解度。
δ+
δ-
δ-
a.极性的向量和是否等于零
(3)多原子分子
2、分子极性的判断
②含极性键的多原子分子
向量和=0
: 非极性分子
向量和≠0
: 极性分子
极性向量可形象地描述极性键的电荷分布情况,极性向量指向的一端,说明该处负电荷更为集中。
H—Cl
δ+
δ-
CO2
O
O
C
δ+
δ-
δ-
直线形,中心对称结构,
非极性分子
两个C=O的极性互相抵消
F1
F2
F合=0
H2O
δ+
δ+
δ-
H
H
O
V形,
中心不对称结构,
两个O-H键的极性向量和不为零
F1
F2
F合≠0
极性分子
δ-
δ+
δ+
δ+
NH3
H
H
N
H
三角锥形,
不对称结构,
极性分子
F合≠0
BF3
B
F
F
F
δ-
δ-
δ-
δ+
F合=0
平面三角形,
对称结构,
非极性分子
H
H
C
H
H
CH4
δ+
δ+
δ+
δ-
δ+
正四面体形,
对称结构,
非极性分子
V形、三角锥,四面体
a.极性的向量和是否等于零
(3)多原子分子
2、分子极性的判断
②含极性键的多原子分子
向量和=0
: 非极性分子
向量和≠0
: 极性分子
分子空间结构是否对称
对称
不对称
直线形、平面正三角形
正四面体、正八面体
→ 非极性分子
→ 极性分子
b.|中心原子化合价|
(3)多原子分子
2、分子极性的判断
②含极性键的多原子分子
=该元素的价电子数
: 非极性分子
≠0该元素的价电子数
: 极性分子
分子 BF3 CO2 PCl5 SO3 H2O NH3 SO2
化合价绝对值
价电子数
分子极性
3
3
4
4
5
5
6
6
2
6
3
5
4
6
非极性
非极性
非极性
非极性
极性
极性
极性
1.正误判断
(1)以非极性键结合的双原子分子一定是非极性分子( )
(2)以极性键结合的双原子分子一定是极性分子( )
(3)以极性键结合的分子一定是极性分子( )
(4)非极性分子只能是双原子单质分子( )
(5)非极性分子中一定含有非极性共价键( )
(6)由同种元素组成的非金属单质分子一定是非极性分子( )
(7)空间结构对称的ABn型分子为非极性分子( )
√
√
×
×
×
×
√
①只含非极性键的分子一定是非极性分子。
②含有极性键的分子,如果分子中各个键的极性的向量和等于零,则为非极性分子,否则为极性分子。
③极性分子中一定有极性键,非极性分子中不一定含有非极性键。例如CH4是非极性分子,只含有极性键。
含有非极性键的分子不一定为非极性分子,如H2O2是含有非极性键的极性分子。
2.回答下列问题。
①H2 ②O2 ③HCl ④P4 ⑤C60 ⑥CO2
⑦CH2==CH2 ⑧HCN ⑨H2O ⑩NH3 BF3
CH4 SO3 CH3Cl Ar H2O2
(1)只含非极性键的是_________(填序号,下同);,既含极性键又含非极性键的是______。
(2)属于非极性分子的是______________________,属于极性分子的是_____________。
①②④⑤
⑦
①②④⑤⑥⑦
③⑧⑨⑩
二、分子的极性的应用
1、微波炉加热原理
水是极性分子,正电中心和负电中心不重合,众多的水分子随电磁场定向转动,微波炉内的微波场以几亿的高频改变电场的方向,水分子间因频繁相互摩擦产生热能。
+
通电
-
二、分子的极性的应用
2、相似相溶
极性分子易溶于极性溶剂中,非极性分子易溶于非极性溶剂中。
水是极性溶剂,CCl4和苯是非极性溶剂,所以极性分子NH3易溶于水,难溶于CCl4和苯;
CCl4和苯能互溶。
表面活性剂的去污原理
表面活性剂在水中会形成亲水基团向外,疏水基团向内的胶束,由于油渍等污垢是疏水的,会被包裹在胶束内腔,在摩擦力的作用下油渍脱离,达到去污目的。
科学 技术 社会
表面活性剂:
有机分子,一端有极性(亲水基团),另一端非极性(疏水基团)
细胞膜是双分子膜,为什么双分子膜以头向外而尾向内的方式排列?
科学 技术 社会
细胞膜的两侧都是水溶液,水是极性分子,而构成膜的两性分子的头基是极性基团,尾基是非极性基 。
