化学人教版(2019)选择性必修2 2.2.2价层电子对互斥模型(共17张PPT)
文档属性
| 名称 | 化学人教版(2019)选择性必修2 2.2.2价层电子对互斥模型(共17张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 3.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-12-13 00:00:00 | ||
图片预览



文档简介
(共17张PPT)
第二节
分子的空间结构
第2课时
价层电子对互斥模型
人教版(2019)化学选择性必修二
第二章 分子结构与性质
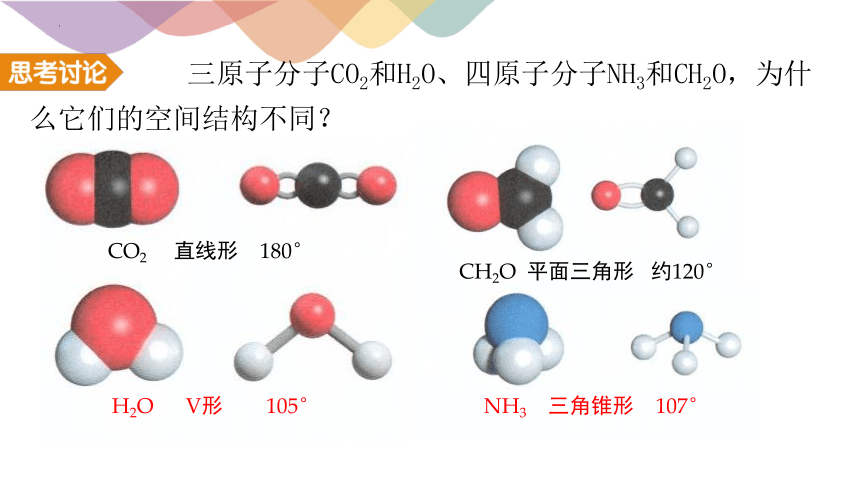
CO2 直线形 180°
H2O V形 105°
CH2O 平面三角形 约120°
NH3 三角锥形 107°
三原子分子CO2和H2O、四原子分子NH3和CH2O,为什么它们的空间结构不同?
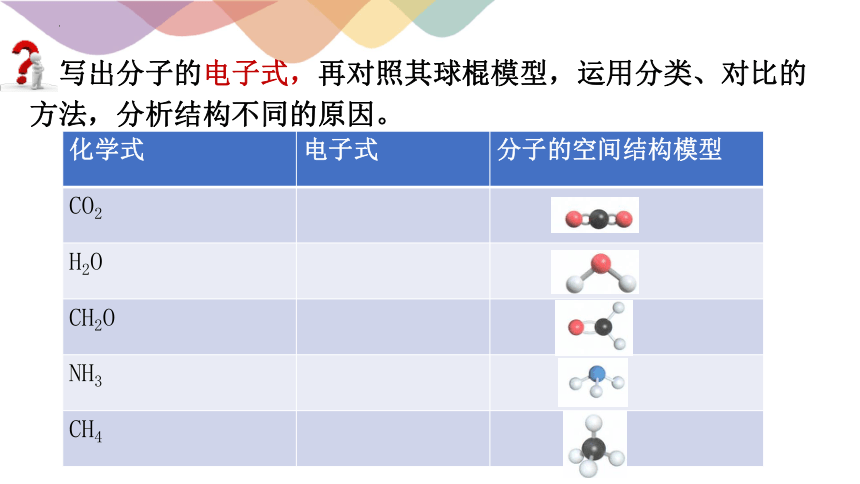
化学式 电子式 分子的空间结构模型
CO2
H2O
CH2O
NH3
CH4
写出分子的电子式,再对照其球棍模型,运用分类、对比的方法,分析结构不同的原因。
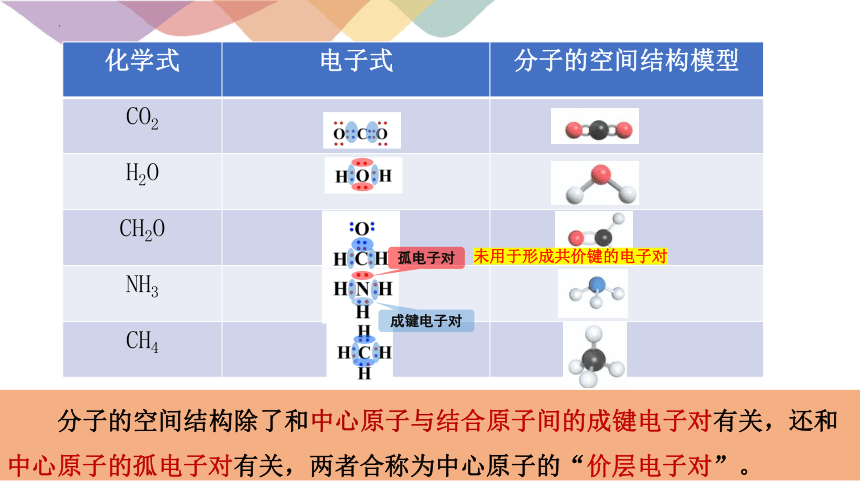
化学式 电子式 分子的空间结构模型
CO2
H2O
CH2O
NH3
CH4
成键电子对
孤电子对
结论:由于中心原子的孤电子对占有一定空间,对其他成键电子对存在排斥力,影响其分子的空间结构。
未用于形成共价键的电子对
分子的空间结构除了和中心原子与结合原子间的成键电子对有关,还和中心原子的孤电子对有关,两者合称为中心原子的“价层电子对”。
价层电子对互斥(VSEPR)模型
1.内容
对ABn型的分子或离子,中心原子A“价层电子对”(包括成键σ键电子对和未成键的孤电子对)之间由于存在排斥力,将使分子的几何构型总是采取电子对相互排斥最小的那种构型,以使彼此之间斥力最小,分子体系能量最低,最稳定
A B n
中心原子
配位体(可以是原子、分子或原于团)
配位体个数
多重键只计σ键的电子对,不计π键的电子对
价层电子对数=σ键电子对数+孤电子对数
2.判断空间构型的具体步骤
(1)确定中心原子的σ键数目
σ键电子对数 = 与中心原子结合的原子数
化学式
中心原子
H2O
NH3
SO3
SO42-
σ键电子对数
化学式
2
3
σ键电子对数
O
N
中心原子
S
S
3
4
(2)中心原子上的孤电子对数的确定
中心原子上孤电子对数= (a-xb)
2
1
中心原子价电子数(主族元素为原子最外层电子数)
与中心原子结合的原子数
与中心原子结合的原子最多容纳电子数(H为1,其它原子为:8-价电子数)
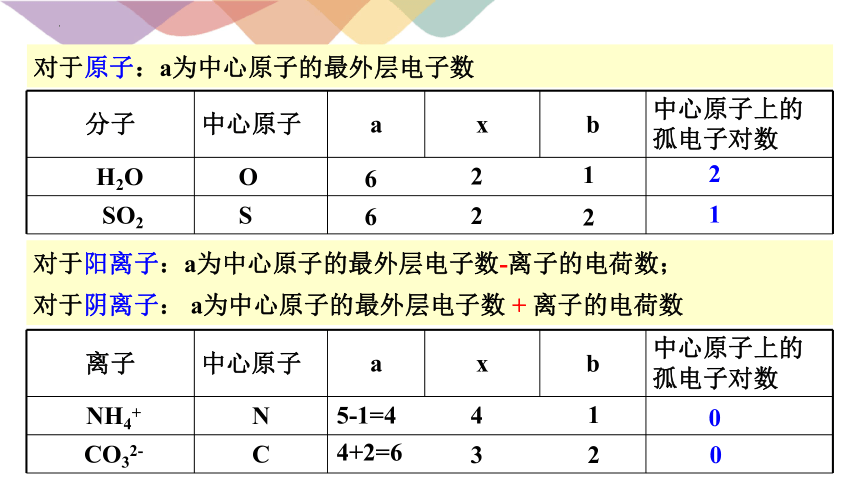
对于原子:a为中心原子的最外层电子数
对于阳离子:a为中心原子的最外层电子数-离子的电荷数;
对于阴离子: a为中心原子的最外层电子数 + 离子的电荷数
分子 中心原子 a x b 中心原子上的孤电子对数
H2O O
SO2 S
6
1
2
2
6
2
1
2
离子 中心原子 a x b 中心原子上的孤电子对数
NH4+ N
CO32- C
5-1=4
0
4
1
4+2=6
0
3
2
(3)确定中心原子价层电子对数
= σ键电子对 + 中心原子上的孤电子对
价层电子对数
代表物 电子式 中心原子结合原子数 σ键电子对 孤电子对数 价层电子对数
H2O
NH3
CO2
CH4
:
:
:
H O H
:
:
:
:
H N H
:
H
:
:
:
H C H
:
H
H
O C O
::
::
:
:
:
:
2
3
4
2
2
2
4
3
1
4
4
0
4
2
0
2
3.VSEPR模型应用——预测分子立体构型
价层电子对数目: 2 3 4
VSEPR模型:
直线
平面三角形
正四面体
价层电子对数目: 5 6
VSEPR模型: 三角双锥形 正八面体形
略去中心原子 的孤对电子
中心原子σ键电子对数+中心上孤电子对数=中心原子价层电子对数
互相排斥
尽可能远离
能量最低最稳定
VSEPR
模型
分子空间模型
H2O
孤电子对
中心原子
价层电子对
NH3
化学式
结构式
含孤电子对的VSEPR模型
分子空结构模型
电子式
成键电子对
价层电子对数 成键电子对数 孤对电子对数 分子类型 VSEPR模型 分子构型 实 例
2
3
2 0 AB2
直线形
3 0 AB3
2 1 AB2
平面三角形
V形
SO2
CO2
BF3
中心原子的孤对电子也要占据中心原子的空间,并与成键电子对互相排斥
推测分子的立体模型必须略去VSEPR模型中的孤电子对
价层电子对数 成键电子对数 孤对电子对数 分子类型 VSEPR模型 分子构型 实 例
4
4 0 AB4
3 1 AB3
2 2 AB2
正四面体
三角锥形
V形
H2O
CH4
NH3
分子或 离子 中心原子的 孤电子对数 价层电 子对数 VSEPR 模型名称 空间结
构名称
BeCl2
SCl2
PF3
N
S
0
2
直线形
直线形
2
0
1
1
4
4
4
4
四面体形
四面体形
四面体形
正四面体形
正四面体形
三角锥形
三角锥形
V形
实验测得NH3的键角为107°,H2O的键角为105°, 为什么NH3和H2O的键角均小于109°28′?
相较成键电子对,孤电子对有较大的排斥力,含孤对电子的分子实测键角都小于VSEPR模型的预测值。
一对孤电子对对成键电子对排斥
两对孤电子对对成键电子对排斥
成键电子对相互排斥
109°28′
107°
105°
CH4
H2O
NH3
1.若ABn分子的中心原子A上没有未用于形成共价键的孤电子对,根据价层电子对互斥理论,下列说法正确的是( )
A.若n=2,则分子的空间结构为V形
B.若n=3,则分子的空间结构为三角锥形
C.若n=4,则分子的空间结构为正四面体形
D.以上说法都不正确
C
2.下列微粒的VSEPR模型与空间结构一致的是( )
A.BF3 B.SO2 C.H2O D.S
3.下列物质中,分子的空间结构与氨分子相似的是( )
A.CO2 B.H2S C.PCl3 D.SiCl4
A
C
第二节
分子的空间结构
第2课时
价层电子对互斥模型
人教版(2019)化学选择性必修二
第二章 分子结构与性质
CO2 直线形 180°
H2O V形 105°
CH2O 平面三角形 约120°
NH3 三角锥形 107°
三原子分子CO2和H2O、四原子分子NH3和CH2O,为什么它们的空间结构不同?
化学式 电子式 分子的空间结构模型
CO2
H2O
CH2O
NH3
CH4
写出分子的电子式,再对照其球棍模型,运用分类、对比的方法,分析结构不同的原因。
化学式 电子式 分子的空间结构模型
CO2
H2O
CH2O
NH3
CH4
成键电子对
孤电子对
结论:由于中心原子的孤电子对占有一定空间,对其他成键电子对存在排斥力,影响其分子的空间结构。
未用于形成共价键的电子对
分子的空间结构除了和中心原子与结合原子间的成键电子对有关,还和中心原子的孤电子对有关,两者合称为中心原子的“价层电子对”。
价层电子对互斥(VSEPR)模型
1.内容
对ABn型的分子或离子,中心原子A“价层电子对”(包括成键σ键电子对和未成键的孤电子对)之间由于存在排斥力,将使分子的几何构型总是采取电子对相互排斥最小的那种构型,以使彼此之间斥力最小,分子体系能量最低,最稳定
A B n
中心原子
配位体(可以是原子、分子或原于团)
配位体个数
多重键只计σ键的电子对,不计π键的电子对
价层电子对数=σ键电子对数+孤电子对数
2.判断空间构型的具体步骤
(1)确定中心原子的σ键数目
σ键电子对数 = 与中心原子结合的原子数
化学式
中心原子
H2O
NH3
SO3
SO42-
σ键电子对数
化学式
2
3
σ键电子对数
O
N
中心原子
S
S
3
4
(2)中心原子上的孤电子对数的确定
中心原子上孤电子对数= (a-xb)
2
1
中心原子价电子数(主族元素为原子最外层电子数)
与中心原子结合的原子数
与中心原子结合的原子最多容纳电子数(H为1,其它原子为:8-价电子数)
对于原子:a为中心原子的最外层电子数
对于阳离子:a为中心原子的最外层电子数-离子的电荷数;
对于阴离子: a为中心原子的最外层电子数 + 离子的电荷数
分子 中心原子 a x b 中心原子上的孤电子对数
H2O O
SO2 S
6
1
2
2
6
2
1
2
离子 中心原子 a x b 中心原子上的孤电子对数
NH4+ N
CO32- C
5-1=4
0
4
1
4+2=6
0
3
2
(3)确定中心原子价层电子对数
= σ键电子对 + 中心原子上的孤电子对
价层电子对数
代表物 电子式 中心原子结合原子数 σ键电子对 孤电子对数 价层电子对数
H2O
NH3
CO2
CH4
:
:
:
H O H
:
:
:
:
H N H
:
H
:
:
:
H C H
:
H
H
O C O
::
::
:
:
:
:
2
3
4
2
2
2
4
3
1
4
4
0
4
2
0
2
3.VSEPR模型应用——预测分子立体构型
价层电子对数目: 2 3 4
VSEPR模型:
直线
平面三角形
正四面体
价层电子对数目: 5 6
VSEPR模型: 三角双锥形 正八面体形
略去中心原子 的孤对电子
中心原子σ键电子对数+中心上孤电子对数=中心原子价层电子对数
互相排斥
尽可能远离
能量最低最稳定
VSEPR
模型
分子空间模型
H2O
孤电子对
中心原子
价层电子对
NH3
化学式
结构式
含孤电子对的VSEPR模型
分子空结构模型
电子式
成键电子对
价层电子对数 成键电子对数 孤对电子对数 分子类型 VSEPR模型 分子构型 实 例
2
3
2 0 AB2
直线形
3 0 AB3
2 1 AB2
平面三角形
V形
SO2
CO2
BF3
中心原子的孤对电子也要占据中心原子的空间,并与成键电子对互相排斥
推测分子的立体模型必须略去VSEPR模型中的孤电子对
价层电子对数 成键电子对数 孤对电子对数 分子类型 VSEPR模型 分子构型 实 例
4
4 0 AB4
3 1 AB3
2 2 AB2
正四面体
三角锥形
V形
H2O
CH4
NH3
分子或 离子 中心原子的 孤电子对数 价层电 子对数 VSEPR 模型名称 空间结
构名称
BeCl2
SCl2
PF3
N
S
0
2
直线形
直线形
2
0
1
1
4
4
4
4
四面体形
四面体形
四面体形
正四面体形
正四面体形
三角锥形
三角锥形
V形
实验测得NH3的键角为107°,H2O的键角为105°, 为什么NH3和H2O的键角均小于109°28′?
相较成键电子对,孤电子对有较大的排斥力,含孤对电子的分子实测键角都小于VSEPR模型的预测值。
一对孤电子对对成键电子对排斥
两对孤电子对对成键电子对排斥
成键电子对相互排斥
109°28′
107°
105°
CH4
H2O
NH3
1.若ABn分子的中心原子A上没有未用于形成共价键的孤电子对,根据价层电子对互斥理论,下列说法正确的是( )
A.若n=2,则分子的空间结构为V形
B.若n=3,则分子的空间结构为三角锥形
C.若n=4,则分子的空间结构为正四面体形
D.以上说法都不正确
C
2.下列微粒的VSEPR模型与空间结构一致的是( )
A.BF3 B.SO2 C.H2O D.S
3.下列物质中,分子的空间结构与氨分子相似的是( )
A.CO2 B.H2S C.PCl3 D.SiCl4
A
C
