3.2 醇酚 同步训练(含解析)2023-2024学年高二下学期化学人教版(2019)选择性必修3
文档属性
| 名称 | 3.2 醇酚 同步训练(含解析)2023-2024学年高二下学期化学人教版(2019)选择性必修3 |

|
|
| 格式 | docx | ||
| 文件大小 | 233.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-12-13 00:00:00 | ||
图片预览




文档简介
3.2 醇酚 同步训练
一、单选题
1.下列实验操作、现象和结论均正确的是选项( )
选项 操作 现象 结论
A 在苯酚溶液中滴加FeCl3溶液 溶液变紫色 羟基使苯环上的H变活泼
B 在酸性KMnO4溶液中加入苯样品 溶液褪色 苯样品中一定含有甲苯
C 在2-溴丁烷中加入AgNO3溶液 产生浅黄色沉淀 2-溴丁烷含溴元素
D 在某种油中加入NaOH溶液,加热 油层消失 该油可能是植物油
A.A B.B C.C D.D
2.2001年5月,中国宣布将推广“车用乙醇汽油”,乙醇汽油就是在汽油里加入适量乙醇混合而成的一种燃料。下列叙述错误的是( )
A.乙醇汽油是一种新型的化合物
B.汽车使用乙醇汽油能减小有害气体的排放
C.工业常用裂化的方法提高汽油的产量
D.用玉米、高梁发酵可以制得乙醇
3.下列说法不正确的是( )
A.钠和钾的合金在常温下是液体,可用于快中子反应堆的热交换剂
B.氯化铁、硫酸亚铁是优良的净水剂
C.碳酸钡可作为检查肠胃的内服药剂,俗称“钡餐”
D.乙醇可以直接作为燃料,也可以和汽油混合后作发动机燃料
4.下列事实不能说明有机物分子中原子或原子团直接相连时而产生相互影响的是( )
A.苯酚能与NaOH溶液反应而乙醇不能
B.等物质的量的乙醇和甘油与足量的金属钠反应,后者产生的氢气比前者多
C.苯与液溴在铁作催化剂下发生反应,而苯酚与浓溴水混合就能发生反应
D.甲苯能使酸性高锰酸钾溶液褪色而甲烷不能
5.下列说法错误的是( )
A.七氟丙烷可用作灭火剂
B.乙醇钠可由乙醇与NaOH溶液反应制得
C.“氢化油”可用于生产人造奶油
D.甘油醛是最简单的醛糖
6.以下说法不正确的是( )
A.1mol乙醇可以与足量金属钠反应,生成0.5molH2,能证明乙醇分子有一个H原子与其余的H原子不同
B.下列反应可证明苯环受甲基的影响,甲苯易被酸性高锰酸钾氧化
C.下列反应可证明由于羟基对苯环的影响,导致苯酚的取代比苯容易
D.苯不能使溴的四氯化碳溶液褪色可以说明苯分子中没有与乙烯分子中类似的碳碳双键
7.稀土是我国的丰产元素,17种稀土元素性质非常接近,用有机萃取剂来分离稀土元素是一种重要的技术。有机萃取剂A的结构式如图所示,据你所学知识判断A属于( )
A.酸类 B.酯类 C.醛类 D.醚类
8.下列关于乙烯和苯的叙述中,错误的是( )
A.乙烯能发生加聚反应
B.乙烯可以燃烧
C.苯能使酸性高锰酸钾溶液褪色
D.苯分子中6个碳碳化学键完全相同
9.中药黄芪中具有抗癌作用的毛蕊异黄酮结构如图。下列说法错误的是( )
A.分子式为 C16H12O5
B.所有碳原子可能共平面
C.遇FeCl3溶液显紫色
D.1mol 该物质与溴水反应,最多消耗 4mol Br2
10.在有机合成中官能团的引入或改变是极为重要的,下列说法正确的是( )
A.甲苯在光照下与Cl2反应,主反应为苯环上引入氯原子
B.将CH2=CH-CH2OH与酸性KMnO4溶液反应即可得到CH2=CH-COOH
C.引入羟基的方法通常有卤代烃和酯的水解、烯烃的加成、醛类的还原
D.HC≡CH、(CN)2、CH3COOH三种单体在一定条件下发生加成、酯化反应即可得到
11.向盛有乙醇的烧杯中投入一小块钠,可以观察到的现象是( )
A.钠在乙醇的液面上游动 B.钠沉在液面以下
C.钠反应剧烈 D.钠块熔成小球
12.有机化合物分子中基团之间会相互影响,下列叙述没有表现出基团间相互影响的是( )
A.苯酚易与NaOH溶液反应,环已醇不与NaOH溶液反应
B.苯酚可以发生加成反应,乙醇不能发生加成反应
C.苯与浓硝酸发生硝化反应生成硝基苯,甲苯与浓硝酸发生硝化反应生成2,4,6-三硝基甲苯
D.甲苯可以使酸性高锰酸钾溶液褪色,乙烷不能使酸性高锰酸钾溶液褪色
13.乙醇催化氧化为乙醛过程中化学键的断裂与形成情况可表示如图:
下列醇能被氧化为醛类化合物的是( )
A. B.
C. D.
14.化学与生产、生活联系密切。下列有关说法错误的是( )
A.光导纤维的主要成分是二氧化硅
B.乙醇用作消毒剂,主要是利用其强氧化性
C.“臭氧空洞”的形成与氮氧化合物和氟氯烃的排放有关
D.电动汽车的推广使用,有效地减少了温室气体的排放
15.化学与生产、生活密切相关。下列说法错误的是( )
A.疫苗一般应冷藏存放,以避免蛋白质变性
B.医用口罩无纺布的原材料成分之一是聚丙烯,其结构简式为
C.“84”消毒液是以NaClO为主要成分的消毒液,为了提升消毒效果,可以和洁厕灵(主要成分是盐酸)混合使用
D.不可向密闭空间的空气中喷洒酒精进行消毒,易引发火灾
16.乙醇可以发生下列反应,在反应里乙醇分子断裂C﹣O键而失去羟基的是( )
A.乙醇与乙酸发生酯化反应
B.乙醇的催化氧化
C.乙醇与钠反应生成氢气
D.乙醇在浓硫酸存在下加热至170℃
二、综合题
17.
(1)I.乳酸在多种生物化学过程中起着重要作用,酸牛奶中含有乳酸,其结构简式如图所示:
下列物质与乳酸互为同系物的是 ,与乳酸互为同分异构体的是 。
①②③④
(2)研究人员在珠峰山顶发现了“微塑料”,这是目前地球上发现塑料污染海拔最高的地方。聚乳酸(PLA)可微生物降解,是理想的绿色高分子材料,可以代替塑料制品减少“微塑料”带来的环境污染。写出用乳酸制取聚乳酸的化学方程式 。
(3)II.当有机化合物分子中碳原子连有四个不同基团时称为手性碳原子,如A中星号“*”碳原子就是手性碳原子,则B中手性碳原子的个数为 ;若使A失去手性,则采取的方法为 (用化学方程式表示)。
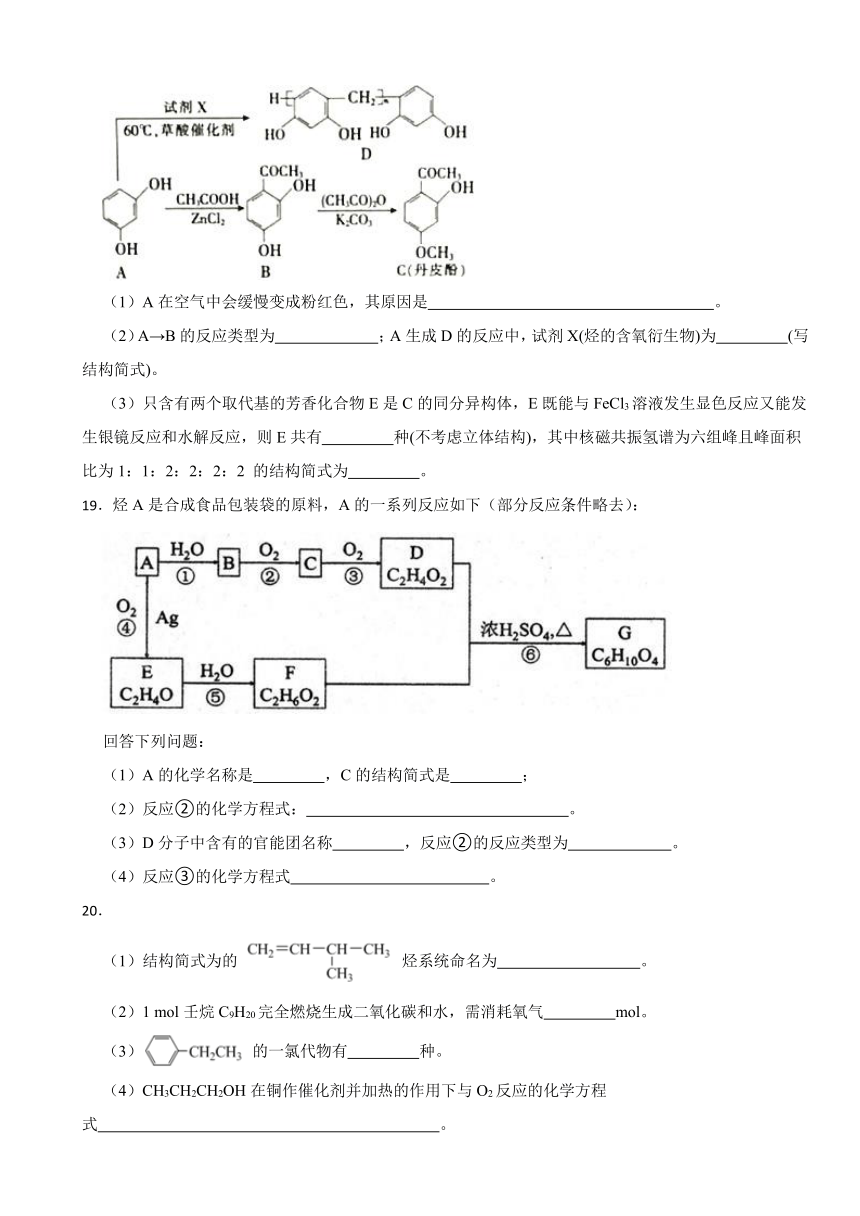
18.以A为原料可制备C(丹皮酚)和D(树脂),其合成路线如下:
(1)A在空气中会缓慢变成粉红色,其原因是 。
(2)A→B的反应类型为 ;A生成D的反应中,试剂X(烃的含氧衍生物)为 (写结构简式)。
(3)只含有两个取代基的芳香化合物E是C的同分异构体,E既能与FeCl3溶液发生显色反应又能发生银镜反应和水解反应,则E共有 种(不考虑立体结构),其中核磁共振氢谱为六组峰且峰面积比为1:1:2:2:2:2 的结构简式为 。
19.烃A是合成食品包装袋的原料,A的一系列反应如下(部分反应条件略去):
回答下列问题:
(1)A的化学名称是 ,C的结构简式是 ;
(2)反应②的化学方程式: 。
(3)D分子中含有的官能团名称 ,反应②的反应类型为 。
(4)反应③的化学方程式 。
20.
(1)结构简式为的 烃系统命名为 。
(2)1 mol壬烷C9H20完全燃烧生成二氧化碳和水,需消耗氧气 mol。
(3) 的一氯代物有 种。
(4)CH3CH2CH2OH在铜作催化剂并加热的作用下与O2反应的化学方程式 。
21.工业上乙醚可用于制造无烟火药。实验室合成乙醚的原理如下。
主反应 2CH3CH2OH CH3CH2OCH2CH3+H2O
副反应CH3CH2OH H2C=CH2 ↑+H2O
【乙醚制备】装置设计如下图(部分装置略)
(1)仪器a是 (写名称);仪器b应更换为下列的 (填序号)。
A.干燥器
B.直形冷凝管
C.玻璃管
D.安全瓶
(2)实验操作的正确排序为 (填序号),取出乙醚立即密闭保存。
a.安装实验仪器 b.加入12 mL浓硫酸和少量乙醇的混合物 c.检查装置气密性 d.熄灭酒精灯 e.通冷却水并加热烧瓶 f.拆除装置 g.控制滴加乙醇速率与馏出液速率相等
(3)加热后发现a 中没有添加碎瓷片,处理方法是 ;反应温度不超过145℃,其目的是 。若滴入乙醇的速率显著超过馏出液速率,反应速率会降低,可能原因是 。
(4)【乙醚提纯】
粗乙醚中含有的主要杂质为 ;无水氯化镁的作用是 。
(5)操作a 的名称是 ;进行该操作时,必须用水浴代替酒精灯加热,其目的与制备实验中将尾接管支管通入室外相同,均为 。
答案解析部分
1.【答案】D
【解析】【解答】A.苯酚遇 FeCl3溶液 显紫色,说明苯酚使羟基氢变活泼,操作和现象均正确,结论错误,故A不符合题意;
B.使酸性高锰酸钾溶液褪色的物质有苯的同系物、乙烯、乙醇等很多物质,不一定是甲苯,说法错误,故B不符合题意;
C. 碳溴键不能电离, 在2-溴丁烷中加入AgNO3溶液不会产生沉淀,说法错误,故C不符合题意;
D.植物油在 NaOH 条件下水解生成可溶性物质,说法正确,故D符合题意。
故答案为:
【分析】本题考查了有机物的性质,考察点简单。
2.【答案】A
【解析】【解答】A、乙醇汽油是用90%的普通汽油与10%的燃料乙醇调和而成,由此可知乙醇汽油是混合物,A符合题意;
B、乙醇可以有效改善油品的性能和质量,降低一氧化碳、碳氢化合物等主要污染物排放,它不影响汽车的行驶性能,还减少有害气体的排放量,是一种改善环境的清洁能源,叙述符合题意,B不符合题意;
C、石油通过裂化可以提高汽油的产量,叙述符合题意,C不符合题意;
D、发酵法制乙醇是在酿酒的基础上发展起来的,发酵法的原料可以是含淀粉的农产品,如高粱、玉米和薯类等,D不符合题意。
故答案为:A。
【分析】A.乙醇汽油是一种混合物;
B.乙醇燃烧后生成二氧化碳和水;
C.裂化是提高汽油产量的主要方法;
D.玉米、高粱的主要成分是淀粉,淀粉可知的乙醇。
3.【答案】C
【解析】【解答】A.钠钾合金熔点低,常温下为液体,导热性强,可用于快中子反应堆的热交换剂,故A不符合题意;
B.硫酸亚铁在溶液中被氧化为硫酸铁,硫酸铁、氯化铁在溶液中水解生成氢氧化铁胶体,氢氧化铁胶体能够吸附水中悬浮杂质,达到净水作用,故B不符合题意;
C.碳酸钡可与胃中盐酸反应生成氯化钡、二氧化碳和水,钡离子有毒,应用硫酸钡作为检查肠胃的内服药剂,故C符合题意;
D.乙醇易燃烧,可作为能源,可以直接作为燃料,也可以和汽油混合后作发动机燃料,故D不符合题意。
故答案为:C。
【分析】钡餐指的是硫酸钡,碳酸钡进入胃部后会生成钡离子,对人体有害。
4.【答案】B
【解析】【解答】A.苯酚能够与氢氧化钠反应而乙醇不能是因为在苯酚中羟基受到苯环的影响具有了酸性,选项A不符合题意;
B.等物质的量的乙醇和甘油与足量的金属钠反应,后者产生的氢气比前者多是因为甘油属于三元醇,一个甘油分子中含有三个羟基,所以等物质的量的乙醇和甘油所含的羟基的数目不同,选项B符合题意;
C.苯酚与浓溴水反应是因为羟基对苯环的影响是羟基的邻对位活化,选项C不符合题意,
D.甲苯能够使溴水褪色是因为苯环对甲基的影响使甲基活性增强,选项D不符合题意。
故答案为:B。
【分析】B、是由数量决定的,而不是由原子或原子团引起的
5.【答案】B
【解析】【解答】A.七氟丙烷不能燃烧,也不支持燃烧,可用作灭火剂,实际上七氟丙烷具有清洁、低毒、良好电绝缘性、灭火效率高、不破坏大气臭氧层的特点,是替代卤代烷灭火剂的洁净气体中的较优者,A不符合题意;
B.乙醇与NaOH不反应,乙醇钠可由乙醇与Na反应制得,B符合题意;
C.“氢化油”是含较多不饱和高级脂肪酸甘油酯与氢气加成的产物,可用于生产人造奶油,C不符合题意;
D.甘油醛即2,3-二羟基丙醛,是最简单的醛糖,D不符合题意;
故答案为:B。
【分析】A、七氟丙烷不能燃烧,也不支持燃烧,可用作灭火剂;
B、乙醇钠是乙醇和钠反应得到;
C、植物油经过和氢气加成反应后得到人造奶油;
D、甘油醛是最简单的醛糖。
6.【答案】B
【解析】【解答】解:A.1mol乙醇可以与足量金属钠反应,生成0.5molH2,说明乙醇中只有一个羟基,故A正确;
B.甲苯能被高锰酸钾溶液氧化,说明是苯环对甲基产生了影响,不是甲基影响了苯环,故B错误;
C.苯酚与溴水反应生成三溴苯酚,说明羟基影响了苯环,故C正确;
D.苯中不含有碳碳双键,不能与溴发生加成反应,故D正确,
故选B.
【分析】A.醇中含有的氢原子,只有羟基上的H能被钠取代生成氢气,据此解答;
B.甲苯能被高锰酸钾溶液氧化,说明是苯环对甲基产生了影响;
C.由于羟基对苯环的影响,导致苯环羟基邻位和对位上的H变得活泼,据此解答;
D.含有碳碳双键或三键的物质能与溴发生加成反应使其褪色,据此解答.
7.【答案】B
【解析】【解答】根据有机萃取剂A的结构简式可知分子中含有羟基和磷酸形成的酯基,所以可以看作是酯类,分子中没有羧基、醛基和醚键,不能看作是羧酸类、醛类和醚类,
故答案为:B。
【分析】根据有机物的结构简式中含有的官能团判断物质的分类,注意磷酸形成的酯类的结构。
8.【答案】C
【解析】【解答】A.乙烯中含碳碳双键,能发生加聚反应,故A不符合题意;
B.均为烃类物质,均能燃烧生成二氧化碳和水,故B不符合题意;
C.苯中不含双键,不能使酸性高锰酸钾溶液褪色,故C符合题意;
D.苯分子结构中碳碳键为特殊键,不是单键也不是双键,6个碳碳化学键完全相同,故D不符合题意;
故答案为:C。
【分析】苯分子中的六个化学键完全相同,不存在单双建的交替结构,故不能使酸性高锰酸钾溶液褪色。
9.【答案】D
【解析】【解答】A.根据有机物的结构,有机物的分子式为C16H12O5,A不符合题意;
B.该有机物有多个苯环复合在一起,故所有碳原子可能共平面,B不符合题意;
C.该有机物中含有酚羟基,故可以遇FeCl3溶液显紫色,C不符合题意;
D.一个酚羟基的两个邻位发生取代,一个酚羟基的一个邻位和一个对位发生取代,再一个碳碳双键发生加成,最多消耗 5mol 溴单质,D符合题意;
故答案为:D。
【分析】根据结构简式即可写出分子式,一个分子中含有4个酚羟基、一个醚基、一个羰基和一个碳碳双键。苯环和双键的碳原子均共面,连接苯环和双键的是单键可以通过旋转可共面。含有酚羟基,遇氯化铁显色反应,根据双键以及酚羟基的对位和邻位可与溴水反应即可计算出溴的物质的量
10.【答案】C
【解析】【解答】A.甲苯在光照下与氯气反应,主反应为甲基上的氢原子被取代,故A不符合题意;
B. 碳碳双键能被酸性高锰酸钾溶液氧化,故B不符合题意;
C. 卤代烃水解、烯烃加成、酯的水解和醛的还原等能够引入羟基,故C符合题意;
D. 三种单体在一定条件下发生加成和加聚反应能生成该物质,故D不符合题意。
故故答案为:C。
【分析】A.光照条件的取代主要是发生在烷基上
B.羟基和碳碳双键均可被酸性高锰酸钾氧化
C.羟基的产生可以是取代、加成反应、以及醛基或酮基的还原,主要是卤代烃、酯的取代反应、烯烃或者炔烃的加成反应、醛或酮的加成还原
D.此生成物是高聚物,因此发生的不是简单的加成反应,而是加聚反应
11.【答案】B
【解析】【解答】A.乙醇的密度比钠小,钠不会在乙醇的液面上游动,A不符合题意;
B.乙醇的密度比钠小,钠块沉在乙醇液面以下,B符合题意;
C.钠和乙醇的反应比在水中反应缓慢,并不剧烈,C不符合题意;
D.钠和乙醇的反应不如钠和水的反应剧烈,产生热量不度多,钠粒逐渐变小,不会将金属钠熔成小球,D不符合题意;
故答案为:B。
【分析】A.乙醇的密度比钠小,应在液面下;
B.由A分析可知;
C.钠和乙醇的反应比在水中反应缓慢;
D.反应产生热量少,不会熔化;
12.【答案】B
【解析】【解答】A.苯环使羟基中的O-H键极性增强,使苯酚具有弱酸性,能与NaOH溶液反应,A不符合题意;
B.苯酚分子中含有苯环,可以发生加成反应,而乙醇分子中的乙基是饱和的,不能发生加成反应,与基团间相互影响无关,B符合题意;
C.甲基使苯环上的氢原子活性增强,所以甲苯与浓硝酸发生硝化反应生成2,4,6-三硝基甲苯,C不符合题意;
D.苯环使甲基活化,能与酸性高锰酸钾溶液发生反应,D不符合题意;
故答案为:B。
【分析】A.苯酚具有酸性;环乙醇不具有酸性;
C.甲基使苯环上的氢原子活性增强;
D.苯环使甲基活化,能与酸性高锰酸钾溶液发生反应。
13.【答案】C
【解析】【解答】解:A. 中与羟基相连的碳原子上没有氢原子,不能被氧化生成醛类,故A不选;
B. 中与羟基相连的碳原子上有1个氢原子,能被氧化生成酮,不能被氧化生成醛类,故B不选;
C. 中与羟基相连的碳原子上有2个氢原子,能被氧化生成醛类,故C选;
D. 中与羟基相连的碳原子上有1个氢原子,能被氧化生成酮,不能被氧化生成醛类,故D不选;
故选:C.
【分析】如果醇能被氧化为醛类化合物时,与羟基相连的碳原子上至少有2个氢原子,据此分析.
14.【答案】B
【解析】【解答】A.二氧化硅能对光进行全反射,可用作光导纤维,故光导纤维的主要成分是二氧化硅,A不符合题意;
B.乙醇用作消毒剂,是由于75%的乙醇能使病毒中的蛋白质发生变性,而不是利用其强氧化性,B符合题意;
C.“臭氧空洞”的形成与氮氧化合物和氟氯烃的排放有关,C不符合题意;
D.电动汽车的推广使用,可以减少化石能源石油的燃烧,从而减少CO2的排放,故能有效地减少了温室气体的排放,D不符合题意;
故答案为:B。
【分析】A、光导纤维的主要成分是二氧化硅,芯片的主要成分是硅
B、医院里常用乙醇进行消毒,病毒的主要成分是蛋白质
C、臭氧空洞主要来自于氮氧化物的排放和氟氯烃的排放,如氟利昂
D、温室气体的主要来源是化石燃料的使用。
15.【答案】C
【解析】【解答】A.疫苗是将病原微生物(如细菌、立克次氏体、病毒等)及其代谢产物,经过人工减毒、灭活或利用转基因等方法制成的用于预防传染病的自动免疫制剂,疫苗受热作用可使蛋白质变性,不仅失去应有的免疫原性,甚至会形成有害物质而产生不良反应,因此疫苗必须冷藏运输和保存,故A不符合题意;
B.医用口罩无纺布的主要原料为聚丙烯,聚丙烯是丙烯发生加聚反应生成的高分子化合物,其结构简式为 ,故B不符合题意;
C.若将“84”消毒液与洁厕灵(主要成分是盐酸)混合使用,则会产生黄绿色的有毒气体,是次氯酸钠和盐酸反应生成氯气,不能提升消毒效果,产生有毒气体,故C符合题意;
D.向密闭空间的空气中喷洒酒精进行消毒,会增大可燃物与氧气的接触面积,使酒精更易燃烧,故不可向密闭空间的空气中喷洒酒精进行消毒,易引发火灾,故D不符合题意;
故答案为:C。
【分析】A.温度过高疫苗失活,一般需要低温保存
B.聚丙烯是丙烯发生聚合反应制取的物质,属于有机高分子材料
C.84消毒液和洁厕灵发生氧化还原反应产生氯气降低了效果
D.乙醇很容易挥发,遇到明火在有限的空间内发生爆炸
16.【答案】D
【解析】【解答】解:A、酯化反应是酸脱羟基醇脱氢,乙醇断裂羟基上的氢氧键,故A错误;
B、乙醇被氧化为乙醛,断开的是第二个碳上的碳氢键和氢氧键,故B错误;
C、乙醇与与金属钠反应生成乙醇钠和氢气,断开的羟基上的氢氧键,故C错误;
D、乙醇在浓硫酸存在下发生消去反应生成乙烯和水,断开的是第一个甲基上的碳氢键和碳氧键,故D正确;
故选D.
【分析】根据乙醇的性质,运用反应机理、结合反应物与产物的结构来判断断键与成键位置.
17.【答案】(1)④;②
(2)n +(n-1) H2O
(3)3;2CH3CH(OH)COOH+O2 2 +2H2O或
【解析】【解答】(1)题中物质与乳酸互为同系物的是④,与乳酸互为同分异构体的是②;
(2)用乳酸制取聚乳酸的化学方程式n +(n-1) H2O;
II.碳原子连接四个不同的原子或者原子团时,该碳原子是手性碳原子,则有机物B中手性碳原子有3个,若使A失去手性,则采取的方法为2CH3CH(OH)COOH+O2 2 +2H2O或
【分析】(1)组成和结构相似,在分子组成上相差一个或若干个CH2原子团的物质称为同系物,同分异构体是分子式相同结构不同,找出即可
(2)乳酸含有羟基和羧基,羟基和羧基发生的是缩聚反应,根据缩聚反应的发生方式即可写出
(3)找出有机化合物分子中碳原子连有四个不同基团的碳原子即可,含有羟基的碳原子是手性碳原子,因此可以消去或催化氧化进行失去手性碳原子
18.【答案】(1)A中的酚羟基易被空气中的氧气氧化
(2)取代反应;HCHO
(3)6;
【解析】【解答】(1)类比苯酚在空气中变为粉红色,可知A在空气中会缓慢变成粉红色的原因是A中的酚羟基易被空气中的氧气氧化。
(2)A→B的反应类型为取代反应;A生成D的反应中,试剂X(烃的含氧衍生物)为HCHO。
(3)只含有两个取代基的芳香化合物E是C( )的同分异构体,E既能与FeCl3溶液发生显色反应又能发生银镜反应和水解反应,则E分子中有酚羟基、醛基、酯基,E的苯环上只有两个取代基,则其中一个一定是羟基,另一个可能是—CH(CH3)OCHO或—CH2CH2OCHO,这两个取代基在苯环上有邻、间、对三种位置关系,故E共有6种,其中核磁共振氢谱为六组峰且峰面积比为1:1:2:2:2:2 的结构简式为 。
【分析】由合成路线可知,A为间二酚,间二酚与醋酸发生取代反应生成B,B与乙酸酐发生取代反应生成C;类比酚醛树脂的制备,可以推断A与试剂X发生缩聚反应生成D,则X为甲醛。
(1)酚羟基易被氧化;
(2)由反应物和生成物的结构特点确定反应类型;结合酚醛树脂的反应确定试剂X的结构简式;
(3)能与FeCl3溶液发生显色反应,说明结构中含有苯酚结构、既能发生银镜反应又能发生水解反应,说明结构中含有HCOO-结构,据此确定符合条件的同分异构数;核磁共振氢谱中峰面积比为氢原子个数比,据此确定有机物的结构简式。
19.【答案】(1)乙烯;
(2)
(3)羧基;氧化反应
(4)2CH3CHO+O2→2CH3COOH
【解析】【解答】(1)由分析可知,A的结构简式为CH2=CH2,因此A的化学名称为乙烯;C的结构简式为CH3CHO。
(2)反应②是CH3CH2OH的催化氧化反应,该反应的化学方程式为2CH3CH2OH+O22CH3CHO+H2O。
(3)由分析可知,D的结构简式为CH3COOH,其所含的官能团为羧基;反应②是乙醇的催化氧化反应,因此其反应类型为氧化反应。
(4)反应③是乙醛的氧化反应,该反应的化学方程式为2CH3CHO+O2→2CH3COOH。
【分析】烃A是合成食品包装袋的原料,因此A为CH2=CH2;A与H2O反应生成B,因此B为CH3CH2OH;B与O2发生氧化反应生成乙醛,因此C为CH3CHO;C与O2进一步发生氧化反应,生成乙酸,因此D为CH3COOH。A与O2在银的催化作用下反应E,因此E为环氧乙烷;E与H2O进一步反应生成F(C2H6O2),因此F的结构简式为HOCH2CH2OH。D与F在浓硫酸加热条件下发生酯化反应,生成G(C6H10O4),因此G的结构简式为CH3COOCH2CH2OOCCH3。
20.【答案】(1)3-甲基-1-丁烯
(2)14
(3)5
(4)2CH3CH2CH2OH+O2 2CH3CH2CHO+2H2O
【解析】【解答】(1)该烃含有碳碳双键,故为烯烃,选取含有碳碳双键的最长碳链为主链,主链含有4个C,从离双键最近一端给主链碳原子编号,在3号碳原子上有一个甲基,则该烃系统命名为:3-甲基-1-丁烯,故答案为:3-甲基-1-丁烯;(2)1 mol壬烷C9H20完全燃烧生成二氧化碳和水,需消耗氧气的物质的量为:(9+ mol=14mol,故答案为:14;(3) 分子中有5种氢原子,所以一氯代物有5种,故答案为:5;(4)CH3CH2CH2OH与O2在Cu作催化剂下加热生成CH3CH2CHO和水,其反应的方程式为:2CH3CH2CH2OH+O2 2CH3CH2CHO+2H2O,
故答案为:2CH3CH2CH2OH+O2 2CH3CH2CHO+2H2O。
【分析】(1)从官能团一侧开始编号
(2)根据产物是二氧化碳和水计算
(3)注意等效氢
(4)有机化学方程式(非可逆)的书写一般用键号
21.【答案】(1)三颈烧瓶;B
(2)a c b e g d f
(3)停止加热,将烧瓶中的溶液冷却至室温,再重新加入碎瓷片;避免副反应发生;温度骤降导致反应速率降低
(4)乙醇;干燥乙醚
(5)蒸馏;避免引发乙醚蒸汽燃烧或爆炸
【解析】【解答】(1)仪器a是三颈烧瓶;仪器b是球形冷凝管,为避免冷凝时积液,应更换为直形冷凝管,
故答案为:B; (2)实验操作的符合题意排序为a.安装实验仪器→c.检查装置气密性→b.加入12 mL浓硫酸和少量乙醇的混合物→e.通冷却水并加热烧瓶→g.控制滴加乙醇速率与馏出液速率相等→d.熄灭酒精灯→f.拆除装置,取出乙醚立即密闭保存。即答案为a c b e g d f;(3)加热后发现a 中没有添加碎瓷片,处理方法是停止加热,将烧瓶中的溶液冷却至室温,再重新加入碎瓷片;反应温度不超过145℃,其目的是避免副反应发生;若滴入乙醇的速率显著超过馏出液速率,反应速率会降低,可能是温度骤降导致反应速率降低;(4)粗乙醚中含有的主要杂质为未反应的乙醇;无水氯化镁的作用是干燥乙醚;(5)操作a 的名称是蒸馏;进行该操作时,必须用水浴代替酒精灯加热,其目的与制备实验中将尾接管支管通入室外相同,均为避免引发乙醚蒸汽燃烧或爆炸。
【分析】本题探究乙醚的实验室制备。根据制备原理:主反应 2CH3CH2OH CH3CH2OCH2CH3+H2O,副反应CH3CH2OH H2C=CH2 ↑+H2O分析,要注意题所给乙醚的信息;
一、单选题
1.下列实验操作、现象和结论均正确的是选项( )
选项 操作 现象 结论
A 在苯酚溶液中滴加FeCl3溶液 溶液变紫色 羟基使苯环上的H变活泼
B 在酸性KMnO4溶液中加入苯样品 溶液褪色 苯样品中一定含有甲苯
C 在2-溴丁烷中加入AgNO3溶液 产生浅黄色沉淀 2-溴丁烷含溴元素
D 在某种油中加入NaOH溶液,加热 油层消失 该油可能是植物油
A.A B.B C.C D.D
2.2001年5月,中国宣布将推广“车用乙醇汽油”,乙醇汽油就是在汽油里加入适量乙醇混合而成的一种燃料。下列叙述错误的是( )
A.乙醇汽油是一种新型的化合物
B.汽车使用乙醇汽油能减小有害气体的排放
C.工业常用裂化的方法提高汽油的产量
D.用玉米、高梁发酵可以制得乙醇
3.下列说法不正确的是( )
A.钠和钾的合金在常温下是液体,可用于快中子反应堆的热交换剂
B.氯化铁、硫酸亚铁是优良的净水剂
C.碳酸钡可作为检查肠胃的内服药剂,俗称“钡餐”
D.乙醇可以直接作为燃料,也可以和汽油混合后作发动机燃料
4.下列事实不能说明有机物分子中原子或原子团直接相连时而产生相互影响的是( )
A.苯酚能与NaOH溶液反应而乙醇不能
B.等物质的量的乙醇和甘油与足量的金属钠反应,后者产生的氢气比前者多
C.苯与液溴在铁作催化剂下发生反应,而苯酚与浓溴水混合就能发生反应
D.甲苯能使酸性高锰酸钾溶液褪色而甲烷不能
5.下列说法错误的是( )
A.七氟丙烷可用作灭火剂
B.乙醇钠可由乙醇与NaOH溶液反应制得
C.“氢化油”可用于生产人造奶油
D.甘油醛是最简单的醛糖
6.以下说法不正确的是( )
A.1mol乙醇可以与足量金属钠反应,生成0.5molH2,能证明乙醇分子有一个H原子与其余的H原子不同
B.下列反应可证明苯环受甲基的影响,甲苯易被酸性高锰酸钾氧化
C.下列反应可证明由于羟基对苯环的影响,导致苯酚的取代比苯容易
D.苯不能使溴的四氯化碳溶液褪色可以说明苯分子中没有与乙烯分子中类似的碳碳双键
7.稀土是我国的丰产元素,17种稀土元素性质非常接近,用有机萃取剂来分离稀土元素是一种重要的技术。有机萃取剂A的结构式如图所示,据你所学知识判断A属于( )
A.酸类 B.酯类 C.醛类 D.醚类
8.下列关于乙烯和苯的叙述中,错误的是( )
A.乙烯能发生加聚反应
B.乙烯可以燃烧
C.苯能使酸性高锰酸钾溶液褪色
D.苯分子中6个碳碳化学键完全相同
9.中药黄芪中具有抗癌作用的毛蕊异黄酮结构如图。下列说法错误的是( )
A.分子式为 C16H12O5
B.所有碳原子可能共平面
C.遇FeCl3溶液显紫色
D.1mol 该物质与溴水反应,最多消耗 4mol Br2
10.在有机合成中官能团的引入或改变是极为重要的,下列说法正确的是( )
A.甲苯在光照下与Cl2反应,主反应为苯环上引入氯原子
B.将CH2=CH-CH2OH与酸性KMnO4溶液反应即可得到CH2=CH-COOH
C.引入羟基的方法通常有卤代烃和酯的水解、烯烃的加成、醛类的还原
D.HC≡CH、(CN)2、CH3COOH三种单体在一定条件下发生加成、酯化反应即可得到
11.向盛有乙醇的烧杯中投入一小块钠,可以观察到的现象是( )
A.钠在乙醇的液面上游动 B.钠沉在液面以下
C.钠反应剧烈 D.钠块熔成小球
12.有机化合物分子中基团之间会相互影响,下列叙述没有表现出基团间相互影响的是( )
A.苯酚易与NaOH溶液反应,环已醇不与NaOH溶液反应
B.苯酚可以发生加成反应,乙醇不能发生加成反应
C.苯与浓硝酸发生硝化反应生成硝基苯,甲苯与浓硝酸发生硝化反应生成2,4,6-三硝基甲苯
D.甲苯可以使酸性高锰酸钾溶液褪色,乙烷不能使酸性高锰酸钾溶液褪色
13.乙醇催化氧化为乙醛过程中化学键的断裂与形成情况可表示如图:
下列醇能被氧化为醛类化合物的是( )
A. B.
C. D.
14.化学与生产、生活联系密切。下列有关说法错误的是( )
A.光导纤维的主要成分是二氧化硅
B.乙醇用作消毒剂,主要是利用其强氧化性
C.“臭氧空洞”的形成与氮氧化合物和氟氯烃的排放有关
D.电动汽车的推广使用,有效地减少了温室气体的排放
15.化学与生产、生活密切相关。下列说法错误的是( )
A.疫苗一般应冷藏存放,以避免蛋白质变性
B.医用口罩无纺布的原材料成分之一是聚丙烯,其结构简式为
C.“84”消毒液是以NaClO为主要成分的消毒液,为了提升消毒效果,可以和洁厕灵(主要成分是盐酸)混合使用
D.不可向密闭空间的空气中喷洒酒精进行消毒,易引发火灾
16.乙醇可以发生下列反应,在反应里乙醇分子断裂C﹣O键而失去羟基的是( )
A.乙醇与乙酸发生酯化反应
B.乙醇的催化氧化
C.乙醇与钠反应生成氢气
D.乙醇在浓硫酸存在下加热至170℃
二、综合题
17.
(1)I.乳酸在多种生物化学过程中起着重要作用,酸牛奶中含有乳酸,其结构简式如图所示:
下列物质与乳酸互为同系物的是 ,与乳酸互为同分异构体的是 。
①②③④
(2)研究人员在珠峰山顶发现了“微塑料”,这是目前地球上发现塑料污染海拔最高的地方。聚乳酸(PLA)可微生物降解,是理想的绿色高分子材料,可以代替塑料制品减少“微塑料”带来的环境污染。写出用乳酸制取聚乳酸的化学方程式 。
(3)II.当有机化合物分子中碳原子连有四个不同基团时称为手性碳原子,如A中星号“*”碳原子就是手性碳原子,则B中手性碳原子的个数为 ;若使A失去手性,则采取的方法为 (用化学方程式表示)。
18.以A为原料可制备C(丹皮酚)和D(树脂),其合成路线如下:
(1)A在空气中会缓慢变成粉红色,其原因是 。
(2)A→B的反应类型为 ;A生成D的反应中,试剂X(烃的含氧衍生物)为 (写结构简式)。
(3)只含有两个取代基的芳香化合物E是C的同分异构体,E既能与FeCl3溶液发生显色反应又能发生银镜反应和水解反应,则E共有 种(不考虑立体结构),其中核磁共振氢谱为六组峰且峰面积比为1:1:2:2:2:2 的结构简式为 。
19.烃A是合成食品包装袋的原料,A的一系列反应如下(部分反应条件略去):
回答下列问题:
(1)A的化学名称是 ,C的结构简式是 ;
(2)反应②的化学方程式: 。
(3)D分子中含有的官能团名称 ,反应②的反应类型为 。
(4)反应③的化学方程式 。
20.
(1)结构简式为的 烃系统命名为 。
(2)1 mol壬烷C9H20完全燃烧生成二氧化碳和水,需消耗氧气 mol。
(3) 的一氯代物有 种。
(4)CH3CH2CH2OH在铜作催化剂并加热的作用下与O2反应的化学方程式 。
21.工业上乙醚可用于制造无烟火药。实验室合成乙醚的原理如下。
主反应 2CH3CH2OH CH3CH2OCH2CH3+H2O
副反应CH3CH2OH H2C=CH2 ↑+H2O
【乙醚制备】装置设计如下图(部分装置略)
(1)仪器a是 (写名称);仪器b应更换为下列的 (填序号)。
A.干燥器
B.直形冷凝管
C.玻璃管
D.安全瓶
(2)实验操作的正确排序为 (填序号),取出乙醚立即密闭保存。
a.安装实验仪器 b.加入12 mL浓硫酸和少量乙醇的混合物 c.检查装置气密性 d.熄灭酒精灯 e.通冷却水并加热烧瓶 f.拆除装置 g.控制滴加乙醇速率与馏出液速率相等
(3)加热后发现a 中没有添加碎瓷片,处理方法是 ;反应温度不超过145℃,其目的是 。若滴入乙醇的速率显著超过馏出液速率,反应速率会降低,可能原因是 。
(4)【乙醚提纯】
粗乙醚中含有的主要杂质为 ;无水氯化镁的作用是 。
(5)操作a 的名称是 ;进行该操作时,必须用水浴代替酒精灯加热,其目的与制备实验中将尾接管支管通入室外相同,均为 。
答案解析部分
1.【答案】D
【解析】【解答】A.苯酚遇 FeCl3溶液 显紫色,说明苯酚使羟基氢变活泼,操作和现象均正确,结论错误,故A不符合题意;
B.使酸性高锰酸钾溶液褪色的物质有苯的同系物、乙烯、乙醇等很多物质,不一定是甲苯,说法错误,故B不符合题意;
C. 碳溴键不能电离, 在2-溴丁烷中加入AgNO3溶液不会产生沉淀,说法错误,故C不符合题意;
D.植物油在 NaOH 条件下水解生成可溶性物质,说法正确,故D符合题意。
故答案为:
【分析】本题考查了有机物的性质,考察点简单。
2.【答案】A
【解析】【解答】A、乙醇汽油是用90%的普通汽油与10%的燃料乙醇调和而成,由此可知乙醇汽油是混合物,A符合题意;
B、乙醇可以有效改善油品的性能和质量,降低一氧化碳、碳氢化合物等主要污染物排放,它不影响汽车的行驶性能,还减少有害气体的排放量,是一种改善环境的清洁能源,叙述符合题意,B不符合题意;
C、石油通过裂化可以提高汽油的产量,叙述符合题意,C不符合题意;
D、发酵法制乙醇是在酿酒的基础上发展起来的,发酵法的原料可以是含淀粉的农产品,如高粱、玉米和薯类等,D不符合题意。
故答案为:A。
【分析】A.乙醇汽油是一种混合物;
B.乙醇燃烧后生成二氧化碳和水;
C.裂化是提高汽油产量的主要方法;
D.玉米、高粱的主要成分是淀粉,淀粉可知的乙醇。
3.【答案】C
【解析】【解答】A.钠钾合金熔点低,常温下为液体,导热性强,可用于快中子反应堆的热交换剂,故A不符合题意;
B.硫酸亚铁在溶液中被氧化为硫酸铁,硫酸铁、氯化铁在溶液中水解生成氢氧化铁胶体,氢氧化铁胶体能够吸附水中悬浮杂质,达到净水作用,故B不符合题意;
C.碳酸钡可与胃中盐酸反应生成氯化钡、二氧化碳和水,钡离子有毒,应用硫酸钡作为检查肠胃的内服药剂,故C符合题意;
D.乙醇易燃烧,可作为能源,可以直接作为燃料,也可以和汽油混合后作发动机燃料,故D不符合题意。
故答案为:C。
【分析】钡餐指的是硫酸钡,碳酸钡进入胃部后会生成钡离子,对人体有害。
4.【答案】B
【解析】【解答】A.苯酚能够与氢氧化钠反应而乙醇不能是因为在苯酚中羟基受到苯环的影响具有了酸性,选项A不符合题意;
B.等物质的量的乙醇和甘油与足量的金属钠反应,后者产生的氢气比前者多是因为甘油属于三元醇,一个甘油分子中含有三个羟基,所以等物质的量的乙醇和甘油所含的羟基的数目不同,选项B符合题意;
C.苯酚与浓溴水反应是因为羟基对苯环的影响是羟基的邻对位活化,选项C不符合题意,
D.甲苯能够使溴水褪色是因为苯环对甲基的影响使甲基活性增强,选项D不符合题意。
故答案为:B。
【分析】B、是由数量决定的,而不是由原子或原子团引起的
5.【答案】B
【解析】【解答】A.七氟丙烷不能燃烧,也不支持燃烧,可用作灭火剂,实际上七氟丙烷具有清洁、低毒、良好电绝缘性、灭火效率高、不破坏大气臭氧层的特点,是替代卤代烷灭火剂的洁净气体中的较优者,A不符合题意;
B.乙醇与NaOH不反应,乙醇钠可由乙醇与Na反应制得,B符合题意;
C.“氢化油”是含较多不饱和高级脂肪酸甘油酯与氢气加成的产物,可用于生产人造奶油,C不符合题意;
D.甘油醛即2,3-二羟基丙醛,是最简单的醛糖,D不符合题意;
故答案为:B。
【分析】A、七氟丙烷不能燃烧,也不支持燃烧,可用作灭火剂;
B、乙醇钠是乙醇和钠反应得到;
C、植物油经过和氢气加成反应后得到人造奶油;
D、甘油醛是最简单的醛糖。
6.【答案】B
【解析】【解答】解:A.1mol乙醇可以与足量金属钠反应,生成0.5molH2,说明乙醇中只有一个羟基,故A正确;
B.甲苯能被高锰酸钾溶液氧化,说明是苯环对甲基产生了影响,不是甲基影响了苯环,故B错误;
C.苯酚与溴水反应生成三溴苯酚,说明羟基影响了苯环,故C正确;
D.苯中不含有碳碳双键,不能与溴发生加成反应,故D正确,
故选B.
【分析】A.醇中含有的氢原子,只有羟基上的H能被钠取代生成氢气,据此解答;
B.甲苯能被高锰酸钾溶液氧化,说明是苯环对甲基产生了影响;
C.由于羟基对苯环的影响,导致苯环羟基邻位和对位上的H变得活泼,据此解答;
D.含有碳碳双键或三键的物质能与溴发生加成反应使其褪色,据此解答.
7.【答案】B
【解析】【解答】根据有机萃取剂A的结构简式可知分子中含有羟基和磷酸形成的酯基,所以可以看作是酯类,分子中没有羧基、醛基和醚键,不能看作是羧酸类、醛类和醚类,
故答案为:B。
【分析】根据有机物的结构简式中含有的官能团判断物质的分类,注意磷酸形成的酯类的结构。
8.【答案】C
【解析】【解答】A.乙烯中含碳碳双键,能发生加聚反应,故A不符合题意;
B.均为烃类物质,均能燃烧生成二氧化碳和水,故B不符合题意;
C.苯中不含双键,不能使酸性高锰酸钾溶液褪色,故C符合题意;
D.苯分子结构中碳碳键为特殊键,不是单键也不是双键,6个碳碳化学键完全相同,故D不符合题意;
故答案为:C。
【分析】苯分子中的六个化学键完全相同,不存在单双建的交替结构,故不能使酸性高锰酸钾溶液褪色。
9.【答案】D
【解析】【解答】A.根据有机物的结构,有机物的分子式为C16H12O5,A不符合题意;
B.该有机物有多个苯环复合在一起,故所有碳原子可能共平面,B不符合题意;
C.该有机物中含有酚羟基,故可以遇FeCl3溶液显紫色,C不符合题意;
D.一个酚羟基的两个邻位发生取代,一个酚羟基的一个邻位和一个对位发生取代,再一个碳碳双键发生加成,最多消耗 5mol 溴单质,D符合题意;
故答案为:D。
【分析】根据结构简式即可写出分子式,一个分子中含有4个酚羟基、一个醚基、一个羰基和一个碳碳双键。苯环和双键的碳原子均共面,连接苯环和双键的是单键可以通过旋转可共面。含有酚羟基,遇氯化铁显色反应,根据双键以及酚羟基的对位和邻位可与溴水反应即可计算出溴的物质的量
10.【答案】C
【解析】【解答】A.甲苯在光照下与氯气反应,主反应为甲基上的氢原子被取代,故A不符合题意;
B. 碳碳双键能被酸性高锰酸钾溶液氧化,故B不符合题意;
C. 卤代烃水解、烯烃加成、酯的水解和醛的还原等能够引入羟基,故C符合题意;
D. 三种单体在一定条件下发生加成和加聚反应能生成该物质,故D不符合题意。
故故答案为:C。
【分析】A.光照条件的取代主要是发生在烷基上
B.羟基和碳碳双键均可被酸性高锰酸钾氧化
C.羟基的产生可以是取代、加成反应、以及醛基或酮基的还原,主要是卤代烃、酯的取代反应、烯烃或者炔烃的加成反应、醛或酮的加成还原
D.此生成物是高聚物,因此发生的不是简单的加成反应,而是加聚反应
11.【答案】B
【解析】【解答】A.乙醇的密度比钠小,钠不会在乙醇的液面上游动,A不符合题意;
B.乙醇的密度比钠小,钠块沉在乙醇液面以下,B符合题意;
C.钠和乙醇的反应比在水中反应缓慢,并不剧烈,C不符合题意;
D.钠和乙醇的反应不如钠和水的反应剧烈,产生热量不度多,钠粒逐渐变小,不会将金属钠熔成小球,D不符合题意;
故答案为:B。
【分析】A.乙醇的密度比钠小,应在液面下;
B.由A分析可知;
C.钠和乙醇的反应比在水中反应缓慢;
D.反应产生热量少,不会熔化;
12.【答案】B
【解析】【解答】A.苯环使羟基中的O-H键极性增强,使苯酚具有弱酸性,能与NaOH溶液反应,A不符合题意;
B.苯酚分子中含有苯环,可以发生加成反应,而乙醇分子中的乙基是饱和的,不能发生加成反应,与基团间相互影响无关,B符合题意;
C.甲基使苯环上的氢原子活性增强,所以甲苯与浓硝酸发生硝化反应生成2,4,6-三硝基甲苯,C不符合题意;
D.苯环使甲基活化,能与酸性高锰酸钾溶液发生反应,D不符合题意;
故答案为:B。
【分析】A.苯酚具有酸性;环乙醇不具有酸性;
C.甲基使苯环上的氢原子活性增强;
D.苯环使甲基活化,能与酸性高锰酸钾溶液发生反应。
13.【答案】C
【解析】【解答】解:A. 中与羟基相连的碳原子上没有氢原子,不能被氧化生成醛类,故A不选;
B. 中与羟基相连的碳原子上有1个氢原子,能被氧化生成酮,不能被氧化生成醛类,故B不选;
C. 中与羟基相连的碳原子上有2个氢原子,能被氧化生成醛类,故C选;
D. 中与羟基相连的碳原子上有1个氢原子,能被氧化生成酮,不能被氧化生成醛类,故D不选;
故选:C.
【分析】如果醇能被氧化为醛类化合物时,与羟基相连的碳原子上至少有2个氢原子,据此分析.
14.【答案】B
【解析】【解答】A.二氧化硅能对光进行全反射,可用作光导纤维,故光导纤维的主要成分是二氧化硅,A不符合题意;
B.乙醇用作消毒剂,是由于75%的乙醇能使病毒中的蛋白质发生变性,而不是利用其强氧化性,B符合题意;
C.“臭氧空洞”的形成与氮氧化合物和氟氯烃的排放有关,C不符合题意;
D.电动汽车的推广使用,可以减少化石能源石油的燃烧,从而减少CO2的排放,故能有效地减少了温室气体的排放,D不符合题意;
故答案为:B。
【分析】A、光导纤维的主要成分是二氧化硅,芯片的主要成分是硅
B、医院里常用乙醇进行消毒,病毒的主要成分是蛋白质
C、臭氧空洞主要来自于氮氧化物的排放和氟氯烃的排放,如氟利昂
D、温室气体的主要来源是化石燃料的使用。
15.【答案】C
【解析】【解答】A.疫苗是将病原微生物(如细菌、立克次氏体、病毒等)及其代谢产物,经过人工减毒、灭活或利用转基因等方法制成的用于预防传染病的自动免疫制剂,疫苗受热作用可使蛋白质变性,不仅失去应有的免疫原性,甚至会形成有害物质而产生不良反应,因此疫苗必须冷藏运输和保存,故A不符合题意;
B.医用口罩无纺布的主要原料为聚丙烯,聚丙烯是丙烯发生加聚反应生成的高分子化合物,其结构简式为 ,故B不符合题意;
C.若将“84”消毒液与洁厕灵(主要成分是盐酸)混合使用,则会产生黄绿色的有毒气体,是次氯酸钠和盐酸反应生成氯气,不能提升消毒效果,产生有毒气体,故C符合题意;
D.向密闭空间的空气中喷洒酒精进行消毒,会增大可燃物与氧气的接触面积,使酒精更易燃烧,故不可向密闭空间的空气中喷洒酒精进行消毒,易引发火灾,故D不符合题意;
故答案为:C。
【分析】A.温度过高疫苗失活,一般需要低温保存
B.聚丙烯是丙烯发生聚合反应制取的物质,属于有机高分子材料
C.84消毒液和洁厕灵发生氧化还原反应产生氯气降低了效果
D.乙醇很容易挥发,遇到明火在有限的空间内发生爆炸
16.【答案】D
【解析】【解答】解:A、酯化反应是酸脱羟基醇脱氢,乙醇断裂羟基上的氢氧键,故A错误;
B、乙醇被氧化为乙醛,断开的是第二个碳上的碳氢键和氢氧键,故B错误;
C、乙醇与与金属钠反应生成乙醇钠和氢气,断开的羟基上的氢氧键,故C错误;
D、乙醇在浓硫酸存在下发生消去反应生成乙烯和水,断开的是第一个甲基上的碳氢键和碳氧键,故D正确;
故选D.
【分析】根据乙醇的性质,运用反应机理、结合反应物与产物的结构来判断断键与成键位置.
17.【答案】(1)④;②
(2)n +(n-1) H2O
(3)3;2CH3CH(OH)COOH+O2 2 +2H2O或
【解析】【解答】(1)题中物质与乳酸互为同系物的是④,与乳酸互为同分异构体的是②;
(2)用乳酸制取聚乳酸的化学方程式n +(n-1) H2O;
II.碳原子连接四个不同的原子或者原子团时,该碳原子是手性碳原子,则有机物B中手性碳原子有3个,若使A失去手性,则采取的方法为2CH3CH(OH)COOH+O2 2 +2H2O或
【分析】(1)组成和结构相似,在分子组成上相差一个或若干个CH2原子团的物质称为同系物,同分异构体是分子式相同结构不同,找出即可
(2)乳酸含有羟基和羧基,羟基和羧基发生的是缩聚反应,根据缩聚反应的发生方式即可写出
(3)找出有机化合物分子中碳原子连有四个不同基团的碳原子即可,含有羟基的碳原子是手性碳原子,因此可以消去或催化氧化进行失去手性碳原子
18.【答案】(1)A中的酚羟基易被空气中的氧气氧化
(2)取代反应;HCHO
(3)6;
【解析】【解答】(1)类比苯酚在空气中变为粉红色,可知A在空气中会缓慢变成粉红色的原因是A中的酚羟基易被空气中的氧气氧化。
(2)A→B的反应类型为取代反应;A生成D的反应中,试剂X(烃的含氧衍生物)为HCHO。
(3)只含有两个取代基的芳香化合物E是C( )的同分异构体,E既能与FeCl3溶液发生显色反应又能发生银镜反应和水解反应,则E分子中有酚羟基、醛基、酯基,E的苯环上只有两个取代基,则其中一个一定是羟基,另一个可能是—CH(CH3)OCHO或—CH2CH2OCHO,这两个取代基在苯环上有邻、间、对三种位置关系,故E共有6种,其中核磁共振氢谱为六组峰且峰面积比为1:1:2:2:2:2 的结构简式为 。
【分析】由合成路线可知,A为间二酚,间二酚与醋酸发生取代反应生成B,B与乙酸酐发生取代反应生成C;类比酚醛树脂的制备,可以推断A与试剂X发生缩聚反应生成D,则X为甲醛。
(1)酚羟基易被氧化;
(2)由反应物和生成物的结构特点确定反应类型;结合酚醛树脂的反应确定试剂X的结构简式;
(3)能与FeCl3溶液发生显色反应,说明结构中含有苯酚结构、既能发生银镜反应又能发生水解反应,说明结构中含有HCOO-结构,据此确定符合条件的同分异构数;核磁共振氢谱中峰面积比为氢原子个数比,据此确定有机物的结构简式。
19.【答案】(1)乙烯;
(2)
(3)羧基;氧化反应
(4)2CH3CHO+O2→2CH3COOH
【解析】【解答】(1)由分析可知,A的结构简式为CH2=CH2,因此A的化学名称为乙烯;C的结构简式为CH3CHO。
(2)反应②是CH3CH2OH的催化氧化反应,该反应的化学方程式为2CH3CH2OH+O22CH3CHO+H2O。
(3)由分析可知,D的结构简式为CH3COOH,其所含的官能团为羧基;反应②是乙醇的催化氧化反应,因此其反应类型为氧化反应。
(4)反应③是乙醛的氧化反应,该反应的化学方程式为2CH3CHO+O2→2CH3COOH。
【分析】烃A是合成食品包装袋的原料,因此A为CH2=CH2;A与H2O反应生成B,因此B为CH3CH2OH;B与O2发生氧化反应生成乙醛,因此C为CH3CHO;C与O2进一步发生氧化反应,生成乙酸,因此D为CH3COOH。A与O2在银的催化作用下反应E,因此E为环氧乙烷;E与H2O进一步反应生成F(C2H6O2),因此F的结构简式为HOCH2CH2OH。D与F在浓硫酸加热条件下发生酯化反应,生成G(C6H10O4),因此G的结构简式为CH3COOCH2CH2OOCCH3。
20.【答案】(1)3-甲基-1-丁烯
(2)14
(3)5
(4)2CH3CH2CH2OH+O2 2CH3CH2CHO+2H2O
【解析】【解答】(1)该烃含有碳碳双键,故为烯烃,选取含有碳碳双键的最长碳链为主链,主链含有4个C,从离双键最近一端给主链碳原子编号,在3号碳原子上有一个甲基,则该烃系统命名为:3-甲基-1-丁烯,故答案为:3-甲基-1-丁烯;(2)1 mol壬烷C9H20完全燃烧生成二氧化碳和水,需消耗氧气的物质的量为:(9+ mol=14mol,故答案为:14;(3) 分子中有5种氢原子,所以一氯代物有5种,故答案为:5;(4)CH3CH2CH2OH与O2在Cu作催化剂下加热生成CH3CH2CHO和水,其反应的方程式为:2CH3CH2CH2OH+O2 2CH3CH2CHO+2H2O,
故答案为:2CH3CH2CH2OH+O2 2CH3CH2CHO+2H2O。
【分析】(1)从官能团一侧开始编号
(2)根据产物是二氧化碳和水计算
(3)注意等效氢
(4)有机化学方程式(非可逆)的书写一般用键号
21.【答案】(1)三颈烧瓶;B
(2)a c b e g d f
(3)停止加热,将烧瓶中的溶液冷却至室温,再重新加入碎瓷片;避免副反应发生;温度骤降导致反应速率降低
(4)乙醇;干燥乙醚
(5)蒸馏;避免引发乙醚蒸汽燃烧或爆炸
【解析】【解答】(1)仪器a是三颈烧瓶;仪器b是球形冷凝管,为避免冷凝时积液,应更换为直形冷凝管,
故答案为:B; (2)实验操作的符合题意排序为a.安装实验仪器→c.检查装置气密性→b.加入12 mL浓硫酸和少量乙醇的混合物→e.通冷却水并加热烧瓶→g.控制滴加乙醇速率与馏出液速率相等→d.熄灭酒精灯→f.拆除装置,取出乙醚立即密闭保存。即答案为a c b e g d f;(3)加热后发现a 中没有添加碎瓷片,处理方法是停止加热,将烧瓶中的溶液冷却至室温,再重新加入碎瓷片;反应温度不超过145℃,其目的是避免副反应发生;若滴入乙醇的速率显著超过馏出液速率,反应速率会降低,可能是温度骤降导致反应速率降低;(4)粗乙醚中含有的主要杂质为未反应的乙醇;无水氯化镁的作用是干燥乙醚;(5)操作a 的名称是蒸馏;进行该操作时,必须用水浴代替酒精灯加热,其目的与制备实验中将尾接管支管通入室外相同,均为避免引发乙醚蒸汽燃烧或爆炸。
【分析】本题探究乙醚的实验室制备。根据制备原理:主反应 2CH3CH2OH CH3CH2OCH2CH3+H2O,副反应CH3CH2OH H2C=CH2 ↑+H2O分析,要注意题所给乙醚的信息;
