专题7初识酸、碱和盐检测题(含解析)2023-2024学年九年级化学仁爱版下册
文档属性
| 名称 | 专题7初识酸、碱和盐检测题(含解析)2023-2024学年九年级化学仁爱版下册 |

|
|
| 格式 | docx | ||
| 文件大小 | 151.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 仁爱科普版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-12-14 00:00:00 | ||
图片预览




文档简介
专题7 初识酸、碱和盐 检测题
一、单选题
1.下列实验需要使用烧杯的是( )
①过滤 ②稀释浓硫酸 ③用过氧化氢溶液制取氧气 ④用固体溶质配制一定质量分数的溶液.
A.只有①② B.只有①④ C.只有①②④ D.①②③④
2.下列物质的主要成分不属于盐的是
A.建筑用的熟石灰 B.作建筑材料的大理石
C.洗涤用的纯碱 D.用于治疗胃酸过多的小苏打
3.下列实验目的能通过对应实验方法达到的是
选项 实验目的 实验方法
A 探究蜡烛的组成 点燃,在火焰上方罩个烧杯
B 验证质量守恒定律 称量镁条燃烧前后固体质量
C 证明稀硫酸与氢氧化钠溶液反应 取样,滴加稀硫酸至基本不变
D 鉴别化肥硫酸钾和氯化钾 取样,看颜色、闻气味、溶于水
A.A B.B C.C D.D
4.2023年3月29日,四川泸州市森林火灾实战演练在纳溪区举行,模拟树木被雷击引发火灾。下列说法不正确的是
A.树木为可燃物 B.雷击使温度达到树木的着火点
C.可以喷洒干粉(NaHCO3)进行灭火 D.开辟隔离带隔绝空气
5.“证据推理与模型认知”是化学学科核心素养的重要组成部分。下列推断合理的是
A.碱的溶液都显碱性,但显碱性的溶液不一定是碱的溶液
B.有机物含有碳元素,因此所有含碳的化合物都是有机物
C.燃烧都发光、放热,则有发光、放热现象的变化一定是燃烧
D.化合物中含有不同种元素,所以由不同种元素组成的物质一定是化合物
6.下列设计方案合理且化学方程式书写正确的是( )
A.证明金属活动性Mg>Ag:
B.用硝酸钡区别氢氧化钠和硫酸钾:
C.用氢氧化钾除去氯化钾中的少量杂质氯化镁:
D.用氢氧化钙治疗胃酸过多症:
7.下列化学肥料中属于复合肥料的是
A.K2SO4 B.CO(NH2)2 C.KNO3 D.(NH4)2CO3
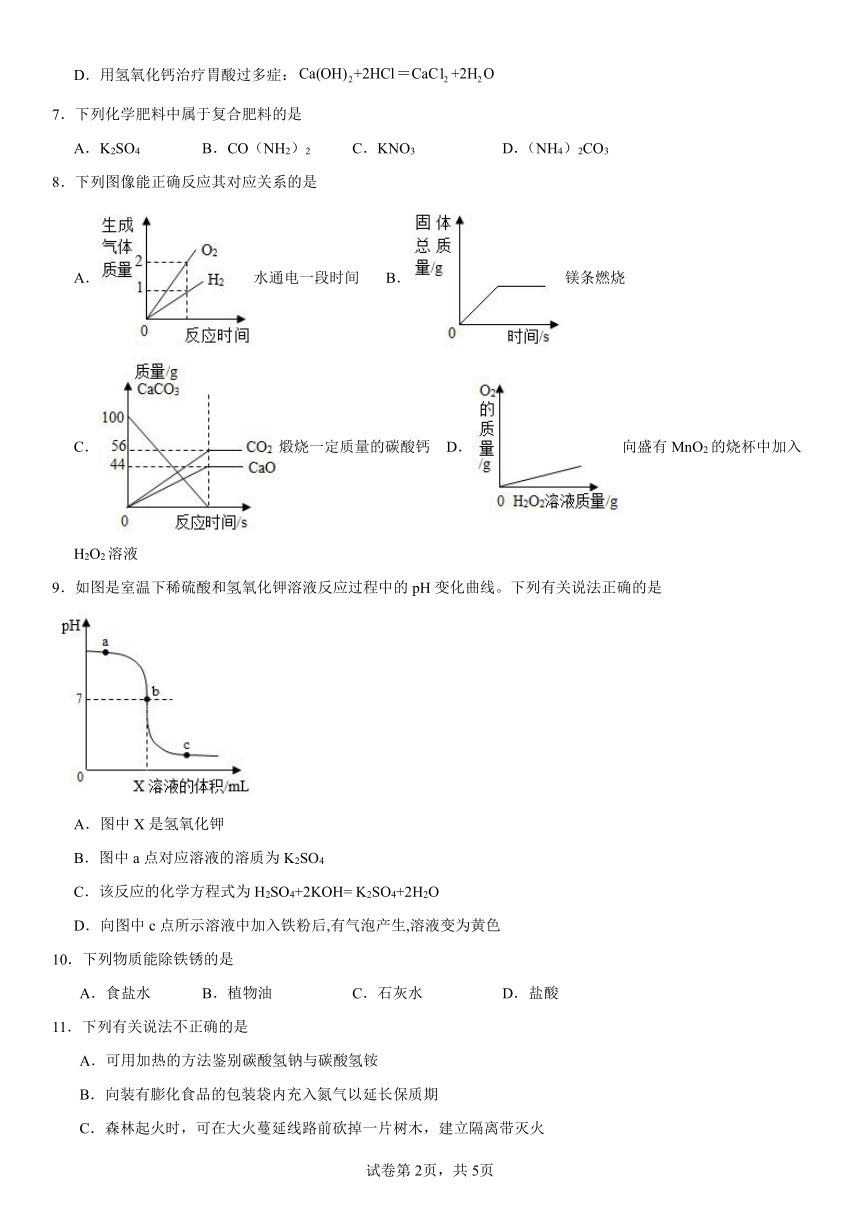
8.下列图像能正确反应其对应关系的是
A.水通电一段时间 B.镁条燃烧
C.煅烧一定质量的碳酸钙 D.向盛有MnO2的烧杯中加入H2O2溶液
9.如图是室温下稀硫酸和氢氧化钾溶液反应过程中的pH变化曲线。下列有关说法正确的是
A.图中X是氢氧化钾
B.图中a点对应溶液的溶质为K2SO4
C.该反应的化学方程式为H2SO4+2KOH= K2SO4+2H2O
D.向图中c点所示溶液中加入铁粉后,有气泡产生,溶液变为黄色
10.下列物质能除铁锈的是
A.食盐水 B.植物油 C.石灰水 D.盐酸
11.下列有关说法不正确的是
A.可用加热的方法鉴别碳酸氢钠与碳酸氢铵
B.向装有膨化食品的包装袋内充入氮气以延长保质期
C.森林起火时,可在大火蔓延线路前砍掉一片树木,建立隔离带灭火
D.将100g10%的稀盐酸加热蒸发掉50g水,使其溶质质量分数变成20%
二、填空题
12.某化工厂购买的固体氢氧化钠没有密封保存,结果有部分变质,我的分析是: 因为它在空气中不仅易 ,而且还能跟 发生反应,该反应的化学方程式为 ;检验该固体是否变质可选用的试剂化学式为 。
13.根据碱的四条化学性质回答下列问题:
(1)广泛应用于肥皂、石油、造纸、纺织、印染等工业中的一种碱是 (填化学式)。
(2)根据反应①将某种试剂加入碱溶液中,观察到溶液变蓝,则该指示剂是 。
(3)若碱为氢氧化钠溶液,请写出符合性质③的一个化学反应方程 。
(4)反应④中加入氯化铁溶液,出现的明显现象为 。
14.用化学用语填空。
(1)2个氮分子 ;
(2)氦气 ;
(3)2个钡离子 ;
(4)含硝酸根的复合肥 。
15.物质的组成与构成
(1)请按要求填写下列表格
物质名称 化学式 物质组成(元素符号) 物质构成(微粒符号)
蔗糖
二氧化硫
碳
氢氧化钠
硫酸铜溶液
(2)通过对比和比较获得结论是化学学习中重要的方法和手段。请按要求填空:
H2O、H2O2和NH3 相似之处: ① ②
不同之处: ① ②
16.“果导片”是一种常用缓泻剂,主要成分是酚酞.某同学欲将其作为酚酞指示剂的替代品,他将“果导片”研成粉末放入酒精中,搅拌、静置,取上清液滴入白醋和食盐水,看到 ,滴入澄清石灰水发现 ;确定“果导片”可作酸碱指示剂使用.当他用饮料吸管向滴有“果导片”清液的澄清石灰水吹气时,可观察到 现象.
17.火药是我国古代四大发明之一.火药由硫磺、硝石、木炭三种物质按一定质量比混合而成.请回答下列问题:
(1)火药属于 (填“纯净物”或“混合物”).
(2)已知某种配比的火药,在空气中燃烧的化学方程式如下:S+2KNO3+3CK2S+N2↑+3X↑,则X的化学式为 .
(3)硝石的主要成分为硝酸钾,硝酸钾在现代农业上有重要用途,它能给农作物提供 和 两种营养元素.
(4)硫磺的主要成分为硫,硫在空气中燃烧产生 火焰;其生成的二氧化硫是形成 的主要物质(填“酸雨”或“臭氧空洞”).
(5)木炭是我国古代炼铁的重要原料(作燃料和还原性物质),试写出其与氧化铁高温反应制铁的化学方程式 .
三、实验题
18.氨气是一种重要的化工原料,有广泛的应用。某兴趣小组的同学为了探究氨气的某些性质,进行以下实验。从左到右依次是实验步骤及相应的现象如下图所示。
请根据图中所示的信息,归纳出有关氨气的性质:
(1)物理性质:① ;② 。
(2)化学性质:氨气与水反应后所得氨水显 性
19.某小组利用如图装置制备常见的气体。请你回答下列问题。
(1)仪器a的名称是 。
(2)实验室用氯酸钾和二氧化锰制取氧气的发生装置为 (填字母序号)。实验室制取二氧化碳的化学方程式为 。
(3)以上装置(A~E)中有一处明显的错误,请加以改正 。
(4)F装置不能干燥、收集氨气,原因是 。
四、计算题
20.中和反应在工农业生产中应用广泛。现将溶质质量分数为10%的氢氧化钠溶液滴加到60g稀硫酸中,测得溶液PH与加入的氢氧化钠溶液的质量关系如图所示:
(1)当氢氧化钠溶液质量加到 g时,溶液中的硫酸恰好完全反应。
(2)求该稀硫酸溶质的质量分数。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.C
【详解】①在过滤实验中要用烧杯盛放滤液;②稀释浓硫酸的操作是:把浓硫酸沿着烧杯壁慢慢注入水中,并不断搅拌,故稀释浓硫酸也能用到;③用过氧化氢制氧气的实验中用到的仪器有锥形瓶、带导管的双孔橡皮塞、水槽、集气瓶等,用不到烧杯;④用固体配制一定质量分数的溶液实验能用到烧杯溶解固体物质,就是说①②④要用到烧杯。故选C。
2.A
【详解】A、熟石灰是氢氧化钙,氢氧化钙由钙离子和氢氧根离子组成,属于碱,不属于盐,故选项正确;
B、大理石的主要成分是碳酸钙,碳酸钙是由金属钙离子和碳酸根离子组成,属于盐,故选项错误;
C、纯碱是碳酸钠,碳酸钠由金属钠离子与碳酸根离子组成,属于盐,故选项错误;
D、小苏打是碳酸氢钠,是由金属钠离子和碳酸氢根离子组成,属于盐,故选项错误。
故选:A。
3.C
【详解】A、点燃蜡烛,在火焰上方罩个烧杯,能观察到烧杯壁有水珠出现,说明蜡烛燃烧生成水,证明蜡烛中含有氢元素,但只能证明蜡烛中含有氢元素,故A错误;
B、镁和氧气点燃条件下反应生成氧化镁,有气体氧气参与反应,只称量镁条燃烧前后固体质量,不能验证质量守恒定律,故B错误;
C、氢氧化钠溶液显碱性,pH>7,滴加稀硫酸,反应生成硫酸钠和水,pH逐渐减小到7,为恰好完全反应,继续加入稀硫酸,溶液显酸性,pH<7,可以证明稀硫酸与氢氧化钠溶液反应,故C正确;
D、硫酸钾和氯化钾都是白色固体,无味,溶于水,无法鉴别,故D错误。
故选C。
4.D
【详解】A、树木可以燃烧,属于可燃物,故选项A说法正确;
B、雷击使温度达到树木的着火点,故选项B说法正确;
C、碳酸氢钠受热会分解生成碳酸钠、水和二氧化碳,可以喷洒干粉(NaHCO3)进行灭火,故选项C说法正确;
D、开辟隔离带是清除了可燃物,故选项D说法错误;
故选:D。
5.A
【详解】A. 碱的溶液都显碱性,但显碱性的溶液不一定是碱的溶液,如:碳酸钠溶液显碱性,但碳酸钠溶液是盐的溶液,此选项正确;
B. 有机物含有碳元素,但含碳的化合物不一定都是有机物,如:一氧化碳、二氧化碳、碳酸钠等,虽然含有碳元素,但属于无机物,此选项错误;
C. 燃烧都发光、放热,但有发光、放热现象的变化不一定是燃烧,如:电灯亮时,发光、发热,只是能量的转化,无新物质生成,发生的是物理变化,此选项错误;
D. 化合物是由不同种元素组成的纯净物,化合物中含有不同种元素,由不同种元素组成的物质不一定是化合物,如空气中含有N、O等元素,但空气属于混合物,不是化合物,此选项错误。
故选A。
6.C
【分析】根据反应物、生成物、反应条件及其质量守恒定律可以书写反应的化学方程式。
【详解】A、镁不能和氯化银反应,该选项不正确;
B、硫酸钾和硝酸钡反应生成硫酸钡沉淀和硝酸钾,反应的化学方程式:,该选项书写不正确;
C、氯化镁和氢氧化钾反应生成白色沉淀氢氧化镁和氯化钾,反应的化学方程式:,该选项书写正确;
D、氢氧化钙腐蚀性较强,因此不能用氢氧化钙治疗胃酸过多症,该选项不正确。
故选C。
【点睛】书写化学方程式要注意四步:一是反应物和生成物的化学式要正确;二是要遵循质量守恒定律,即配平;三是要有必要的条件;四是看是否需要“↑”或“↓”。
7.C
【详解】A、K2SO4中含有钾元素,属于钾肥,故错误;
B、CO(NH2)2中含有氮元素,属于氮肥,故错误;
C、KNO3中含有氮和钾两种元素,属于复合肥,故正确;
D、(NH4)2CO3中含有氮元素,属于氮肥,故错误。
故选C。
8.D
【详解】A、水通电电解生成氢气和氧气,化学方程式为:,生成的氢气和氧气的体积比为2:1,质量比为4:32=1:8,故A错误;
B、镁燃烧,是镁与氧气反应生成氧化镁固体,所以固体的质量逐渐增加,直到反应结束,固体的质量不再发生改变,但固体的质量不是从0开始增加,故B错误;
C、碳酸钙高温下分解生成氧化钙和二氧化碳,化学方程式为:,碳酸钙、氧化钙、二氧化碳的质量比为100:56:44,故C错误;
D、过氧化氢在二氧化锰的催化作用下分解生成水和氧气,氧气的量逐渐增加,故D正确。
故选D。
9.C
【详解】A、图中的起点位置的pH>7,所以是向氢氧化钾溶液中加入稀硫酸,X是稀硫酸,此选项错误;
B、图中a点的pH>7,对应溶液的溶质为K2SO4、KOH,此选项错误;
C、该反应的化学方程式为H2SO4+2KOH= K2SO4+2H2O,此选项正确;
D、向图中c点所示溶液中加入铁粉后,铁与硫酸反应生成硫酸亚铁和氢气,可观察到有气泡产生,溶液变为浅绿色,此选项错误。
故选C。
10.D
【详解】A、铁锈的主要成分是氧化铁,食盐水不能与氧化铁反应,食盐水能加快铁制品锈蚀的速率,不能用来除铁锈,故A选项不符合题意;
B、铁锈的主要成分是氧化铁,植物油不能与氧化铁反应,不能用来除铁锈,故B选项不符合题意;
C、铁锈的主要成分是氧化铁,石灰水的主要成分是氢氧化钙,氢氧化钙不能与氧化铁反应,不能用来除铁锈,故C选项不符合题意;
D、铁锈的主要成分是氧化铁,能与稀盐酸反应生成氯化铁和水,盐酸能用来除铁锈,故D选项符合题意。
故选D。
11.D
【详解】A、可用加热的方法鉴别碳酸氢钠与碳酸氢铵,有气体生成的是碳酸氢钠,没有气体生成的碳酸钠,说法正确;
B、氮气的化学性质稳定,可以用作食品的保护气,向装有膨化食品的包装袋内充入氮气以延长保质期,说法正确;
C、灭火的原理:移除可燃物、温度降到着火点一下,隔绝空气或氧气,森林起火时,可在大火蔓延线路前砍掉一片树木,建立隔离带灭火,说法正确;
D、盐酸具有挥发性,将100g10%的稀盐酸加热蒸发掉50g水,溶质氯化氢也挥发减少,使其溶质质量分数不一定是20%,说法错误;
答案:D。
12. 吸收水分发生潮解 二氧化碳 CO2+2NaOH═Na2CO3+H2O HCl
【详解】氢氧化钠在空气中不仅易吸收水分发生潮解,而且还能跟空气中的二氧化碳反应生成碳酸钠和水,反应的化学方程式为:CO2+2NaOH═Na2CO3+H2O;碳酸钠能与稀盐酸反应生成氯化钠、水和二氧化碳气体,检验该固体是否变质可选用的试剂是稀盐酸,其化学式为:HCl。
13. NaOH 石蕊 HCl+NaOH=NaCl+H2O 红褐色沉淀.
【详解】(1)广泛应用于肥皂、石油、造纸、纺织、印染等工业中的一种碱是NaOH。
故填:NaOH。
(2)根据反应①将某种试剂加入碱溶液中,观察到溶液变蓝,则该指示剂是石蕊试液。
故填:石蕊。
(3)若碱为氢氧化钠溶液,氢氧化钠能和盐酸反应生成氯化钠和水,反应的化学方程式:HCl+NaOH=NaCl+H2O。
故填:HCl+NaOH=NaCl+H2O。
(4)氯化铁能和溶于水的碱反应生成红褐色沉淀氢氧化铁,因此反应④中加入氯化铁溶液,能够观察到产生红褐色沉淀。
故填:产生红褐色沉淀。
14.(1)2N2
(2)He
(3)2Ba2+
(4)KNO3
【解析】(1)
分子用化学式表示,多个分子就是在化学式前面加上相应的数字,故2个氮分子表示为:2N2;
(2)
氦气由氦原子构成,化学式为:He;
(3)
离子的表示方法:在该离子元素符号的右上角标上该离子所带的正负电荷数,数字在前,正负号在后,带一个电荷时,1通常省略,多个离子,就是在元素符号前面加上相应的数字;故2个钡离子表示为:2Ba2+;
(4)
硝酸钾含K、N元素,属于复合肥,且含硝酸根离子,故填:KNO3。
15. C6H12O6 C、H、O C6H12O6 SO2 S、O SO2 C C C NaOH Na、O、H Na+、OH Cu、S、O 、H Cu2+、SO42 、H2O 都是含有氢元素的化合物 都是由分子构成的物质 元素不同 一种是离子,一种是原子
【详解】(1)蔗糖化学式为C6H12O6,由C、H、O三种元素组成,由C6H12O6分子构成;二氧化硫化学式为SO2,由S、O两种元素组成,由SO2分子构成;碳化学式为C,由C元素组成,由C原子构成;氢氧化钠化学式为NaOH,由Na、O、H三种元素组成,由钠离子、氢氧根离子构成;硫酸铜溶液中含有硫酸铜和水,含有Cu、S、O 、H四种元素,溶液中含有Cu2+、SO42 、H2O三种微粒;
(2)从H2O,H2O2和NH3三种物质的组成来看都含有氢元素,都是由两种元素组成的纯净物,所以都是化合物;都是由分子构成的物质;从钠离子和氟原子结构示意图可看出二者的质子数分别是11、9,最外层上的电子数分别是8、7,一种是离子,一种是原子;元素种类不同。
16. 无明显变化; 变红色; 溶液浑浊颜色变浅(或消失).
【分析】根据酚酞遇酸性溶液不会变色,酚酞遇中性溶液不变色,酚酞遇碱性溶液红色进行分析解答。
【详解】由指示剂的知识可知酚酞遇酸性溶液不会变色,酚酞遇中性溶液不变色,酚酞遇碱性溶液红色。白醋属于酸,其溶液显酸性,食盐水呈中性,所以取上述清液滴入白醋和食盐水,看到无明显变化,澄清石灰水是氢氧化钙是的水溶液,氢氧化钙溶液呈碱性,取上述清液滴入澄清石灰水,发现溶液变红色,向澄清石灰中吹气时,石灰水与二氧化碳反应会生成碳酸钙的沉淀和水,氢氧化钙不断被消耗,溶液的碱性逐渐减弱直至消失,所以可观察到溶液浑浊颜色变浅(或消失)。
17. 混合物 CO2 K N 淡蓝色 酸雨
【详解】(1)“黑火药”是由木炭粉(C)、硫磺(S)和硝石(KNO3)等多种物质混合而成的,属于混合物;
(2)根据反应的化学方程式S+2KNO3+3CK2S+N2+3X,反应物中钾、氮、氧、碳、硫原子个数分别为2、2、6、3、1,反应后的生成物中钾、氮、氧、碳、硫原子个数分别为2、2、0、0、1,根据反应前后原子种类、数目不变,则3X中含有3个碳原子和6个氧原子,则每个X分子由1个碳原子和2个氧原子构成,则物质X的化学式为CO2;
(3)KNO3中含有钾元素和氮元素;
(4)硫粉在空气中燃烧,产生微弱的淡蓝色火焰,其生成的二氧化硫是形成酸雨的主要物质;
(5)高温条件下,木炭还原氧化铁生成铁和二氧化碳,反应的化学方程式为:。
18. 密度比空气小 易溶于水 碱
【详解】 (1)①由图示信息可以看出,用的是向下排空气法收集氨气,可知氨气具有密度比空气小的性质;②由图示信息可以看出,把水挤入试管后会形成喷泉,说明试管内压强减小,而压强变小的原因就是氨气溶解在水中,可知氨气具有易溶于水的性质;
(2)能形成红色喷泉,说明氨气溶于水后呈碱性,能无色的酚酞变红色。
19.(1)锥形瓶
(2) A
(3)E中的导气管应伸到集气瓶的底部
(4)浓硫酸能和氨气反应
【详解】(1)仪器a的名称是锥形瓶
(2)实验室用氯酸钾和二氧化锰制取氧气,属于固体加热型,故选择A作为发生装置;
实验室制取二氧化碳原理是碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:;
(3)E中的导气管应伸到集气瓶的底部,否则不利于空气的排出,是收集的气体不纯;
(4)氨气溶于水会形成氨水,氨水属于碱能和浓硫酸反应,因此无法使用浓硫酸干燥氨气
20.(1)40
(2)解:40g10%的氢氧化钠溶液中氢氧化钠的质量为,设60g稀硫酸中硫酸的质量为x。
所以该稀硫酸中溶质的质量分数为。
答:该稀硫酸中溶质的质量分数约为8.2%。
【详解】(1)由图知,当溶液的pH=7时溶液中的硫酸恰好完全反应,此时加入氢氧化钠溶液的质量为40g,故填:40。
(2)见答案。
答案第1页,共2页
答案第1页,共2页
一、单选题
1.下列实验需要使用烧杯的是( )
①过滤 ②稀释浓硫酸 ③用过氧化氢溶液制取氧气 ④用固体溶质配制一定质量分数的溶液.
A.只有①② B.只有①④ C.只有①②④ D.①②③④
2.下列物质的主要成分不属于盐的是
A.建筑用的熟石灰 B.作建筑材料的大理石
C.洗涤用的纯碱 D.用于治疗胃酸过多的小苏打
3.下列实验目的能通过对应实验方法达到的是
选项 实验目的 实验方法
A 探究蜡烛的组成 点燃,在火焰上方罩个烧杯
B 验证质量守恒定律 称量镁条燃烧前后固体质量
C 证明稀硫酸与氢氧化钠溶液反应 取样,滴加稀硫酸至基本不变
D 鉴别化肥硫酸钾和氯化钾 取样,看颜色、闻气味、溶于水
A.A B.B C.C D.D
4.2023年3月29日,四川泸州市森林火灾实战演练在纳溪区举行,模拟树木被雷击引发火灾。下列说法不正确的是
A.树木为可燃物 B.雷击使温度达到树木的着火点
C.可以喷洒干粉(NaHCO3)进行灭火 D.开辟隔离带隔绝空气
5.“证据推理与模型认知”是化学学科核心素养的重要组成部分。下列推断合理的是
A.碱的溶液都显碱性,但显碱性的溶液不一定是碱的溶液
B.有机物含有碳元素,因此所有含碳的化合物都是有机物
C.燃烧都发光、放热,则有发光、放热现象的变化一定是燃烧
D.化合物中含有不同种元素,所以由不同种元素组成的物质一定是化合物
6.下列设计方案合理且化学方程式书写正确的是( )
A.证明金属活动性Mg>Ag:
B.用硝酸钡区别氢氧化钠和硫酸钾:
C.用氢氧化钾除去氯化钾中的少量杂质氯化镁:
D.用氢氧化钙治疗胃酸过多症:
7.下列化学肥料中属于复合肥料的是
A.K2SO4 B.CO(NH2)2 C.KNO3 D.(NH4)2CO3
8.下列图像能正确反应其对应关系的是
A.水通电一段时间 B.镁条燃烧
C.煅烧一定质量的碳酸钙 D.向盛有MnO2的烧杯中加入H2O2溶液
9.如图是室温下稀硫酸和氢氧化钾溶液反应过程中的pH变化曲线。下列有关说法正确的是
A.图中X是氢氧化钾
B.图中a点对应溶液的溶质为K2SO4
C.该反应的化学方程式为H2SO4+2KOH= K2SO4+2H2O
D.向图中c点所示溶液中加入铁粉后,有气泡产生,溶液变为黄色
10.下列物质能除铁锈的是
A.食盐水 B.植物油 C.石灰水 D.盐酸
11.下列有关说法不正确的是
A.可用加热的方法鉴别碳酸氢钠与碳酸氢铵
B.向装有膨化食品的包装袋内充入氮气以延长保质期
C.森林起火时,可在大火蔓延线路前砍掉一片树木,建立隔离带灭火
D.将100g10%的稀盐酸加热蒸发掉50g水,使其溶质质量分数变成20%
二、填空题
12.某化工厂购买的固体氢氧化钠没有密封保存,结果有部分变质,我的分析是: 因为它在空气中不仅易 ,而且还能跟 发生反应,该反应的化学方程式为 ;检验该固体是否变质可选用的试剂化学式为 。
13.根据碱的四条化学性质回答下列问题:
(1)广泛应用于肥皂、石油、造纸、纺织、印染等工业中的一种碱是 (填化学式)。
(2)根据反应①将某种试剂加入碱溶液中,观察到溶液变蓝,则该指示剂是 。
(3)若碱为氢氧化钠溶液,请写出符合性质③的一个化学反应方程 。
(4)反应④中加入氯化铁溶液,出现的明显现象为 。
14.用化学用语填空。
(1)2个氮分子 ;
(2)氦气 ;
(3)2个钡离子 ;
(4)含硝酸根的复合肥 。
15.物质的组成与构成
(1)请按要求填写下列表格
物质名称 化学式 物质组成(元素符号) 物质构成(微粒符号)
蔗糖
二氧化硫
碳
氢氧化钠
硫酸铜溶液
(2)通过对比和比较获得结论是化学学习中重要的方法和手段。请按要求填空:
H2O、H2O2和NH3 相似之处: ① ②
不同之处: ① ②
16.“果导片”是一种常用缓泻剂,主要成分是酚酞.某同学欲将其作为酚酞指示剂的替代品,他将“果导片”研成粉末放入酒精中,搅拌、静置,取上清液滴入白醋和食盐水,看到 ,滴入澄清石灰水发现 ;确定“果导片”可作酸碱指示剂使用.当他用饮料吸管向滴有“果导片”清液的澄清石灰水吹气时,可观察到 现象.
17.火药是我国古代四大发明之一.火药由硫磺、硝石、木炭三种物质按一定质量比混合而成.请回答下列问题:
(1)火药属于 (填“纯净物”或“混合物”).
(2)已知某种配比的火药,在空气中燃烧的化学方程式如下:S+2KNO3+3CK2S+N2↑+3X↑,则X的化学式为 .
(3)硝石的主要成分为硝酸钾,硝酸钾在现代农业上有重要用途,它能给农作物提供 和 两种营养元素.
(4)硫磺的主要成分为硫,硫在空气中燃烧产生 火焰;其生成的二氧化硫是形成 的主要物质(填“酸雨”或“臭氧空洞”).
(5)木炭是我国古代炼铁的重要原料(作燃料和还原性物质),试写出其与氧化铁高温反应制铁的化学方程式 .
三、实验题
18.氨气是一种重要的化工原料,有广泛的应用。某兴趣小组的同学为了探究氨气的某些性质,进行以下实验。从左到右依次是实验步骤及相应的现象如下图所示。
请根据图中所示的信息,归纳出有关氨气的性质:
(1)物理性质:① ;② 。
(2)化学性质:氨气与水反应后所得氨水显 性
19.某小组利用如图装置制备常见的气体。请你回答下列问题。
(1)仪器a的名称是 。
(2)实验室用氯酸钾和二氧化锰制取氧气的发生装置为 (填字母序号)。实验室制取二氧化碳的化学方程式为 。
(3)以上装置(A~E)中有一处明显的错误,请加以改正 。
(4)F装置不能干燥、收集氨气,原因是 。
四、计算题
20.中和反应在工农业生产中应用广泛。现将溶质质量分数为10%的氢氧化钠溶液滴加到60g稀硫酸中,测得溶液PH与加入的氢氧化钠溶液的质量关系如图所示:
(1)当氢氧化钠溶液质量加到 g时,溶液中的硫酸恰好完全反应。
(2)求该稀硫酸溶质的质量分数。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.C
【详解】①在过滤实验中要用烧杯盛放滤液;②稀释浓硫酸的操作是:把浓硫酸沿着烧杯壁慢慢注入水中,并不断搅拌,故稀释浓硫酸也能用到;③用过氧化氢制氧气的实验中用到的仪器有锥形瓶、带导管的双孔橡皮塞、水槽、集气瓶等,用不到烧杯;④用固体配制一定质量分数的溶液实验能用到烧杯溶解固体物质,就是说①②④要用到烧杯。故选C。
2.A
【详解】A、熟石灰是氢氧化钙,氢氧化钙由钙离子和氢氧根离子组成,属于碱,不属于盐,故选项正确;
B、大理石的主要成分是碳酸钙,碳酸钙是由金属钙离子和碳酸根离子组成,属于盐,故选项错误;
C、纯碱是碳酸钠,碳酸钠由金属钠离子与碳酸根离子组成,属于盐,故选项错误;
D、小苏打是碳酸氢钠,是由金属钠离子和碳酸氢根离子组成,属于盐,故选项错误。
故选:A。
3.C
【详解】A、点燃蜡烛,在火焰上方罩个烧杯,能观察到烧杯壁有水珠出现,说明蜡烛燃烧生成水,证明蜡烛中含有氢元素,但只能证明蜡烛中含有氢元素,故A错误;
B、镁和氧气点燃条件下反应生成氧化镁,有气体氧气参与反应,只称量镁条燃烧前后固体质量,不能验证质量守恒定律,故B错误;
C、氢氧化钠溶液显碱性,pH>7,滴加稀硫酸,反应生成硫酸钠和水,pH逐渐减小到7,为恰好完全反应,继续加入稀硫酸,溶液显酸性,pH<7,可以证明稀硫酸与氢氧化钠溶液反应,故C正确;
D、硫酸钾和氯化钾都是白色固体,无味,溶于水,无法鉴别,故D错误。
故选C。
4.D
【详解】A、树木可以燃烧,属于可燃物,故选项A说法正确;
B、雷击使温度达到树木的着火点,故选项B说法正确;
C、碳酸氢钠受热会分解生成碳酸钠、水和二氧化碳,可以喷洒干粉(NaHCO3)进行灭火,故选项C说法正确;
D、开辟隔离带是清除了可燃物,故选项D说法错误;
故选:D。
5.A
【详解】A. 碱的溶液都显碱性,但显碱性的溶液不一定是碱的溶液,如:碳酸钠溶液显碱性,但碳酸钠溶液是盐的溶液,此选项正确;
B. 有机物含有碳元素,但含碳的化合物不一定都是有机物,如:一氧化碳、二氧化碳、碳酸钠等,虽然含有碳元素,但属于无机物,此选项错误;
C. 燃烧都发光、放热,但有发光、放热现象的变化不一定是燃烧,如:电灯亮时,发光、发热,只是能量的转化,无新物质生成,发生的是物理变化,此选项错误;
D. 化合物是由不同种元素组成的纯净物,化合物中含有不同种元素,由不同种元素组成的物质不一定是化合物,如空气中含有N、O等元素,但空气属于混合物,不是化合物,此选项错误。
故选A。
6.C
【分析】根据反应物、生成物、反应条件及其质量守恒定律可以书写反应的化学方程式。
【详解】A、镁不能和氯化银反应,该选项不正确;
B、硫酸钾和硝酸钡反应生成硫酸钡沉淀和硝酸钾,反应的化学方程式:,该选项书写不正确;
C、氯化镁和氢氧化钾反应生成白色沉淀氢氧化镁和氯化钾,反应的化学方程式:,该选项书写正确;
D、氢氧化钙腐蚀性较强,因此不能用氢氧化钙治疗胃酸过多症,该选项不正确。
故选C。
【点睛】书写化学方程式要注意四步:一是反应物和生成物的化学式要正确;二是要遵循质量守恒定律,即配平;三是要有必要的条件;四是看是否需要“↑”或“↓”。
7.C
【详解】A、K2SO4中含有钾元素,属于钾肥,故错误;
B、CO(NH2)2中含有氮元素,属于氮肥,故错误;
C、KNO3中含有氮和钾两种元素,属于复合肥,故正确;
D、(NH4)2CO3中含有氮元素,属于氮肥,故错误。
故选C。
8.D
【详解】A、水通电电解生成氢气和氧气,化学方程式为:,生成的氢气和氧气的体积比为2:1,质量比为4:32=1:8,故A错误;
B、镁燃烧,是镁与氧气反应生成氧化镁固体,所以固体的质量逐渐增加,直到反应结束,固体的质量不再发生改变,但固体的质量不是从0开始增加,故B错误;
C、碳酸钙高温下分解生成氧化钙和二氧化碳,化学方程式为:,碳酸钙、氧化钙、二氧化碳的质量比为100:56:44,故C错误;
D、过氧化氢在二氧化锰的催化作用下分解生成水和氧气,氧气的量逐渐增加,故D正确。
故选D。
9.C
【详解】A、图中的起点位置的pH>7,所以是向氢氧化钾溶液中加入稀硫酸,X是稀硫酸,此选项错误;
B、图中a点的pH>7,对应溶液的溶质为K2SO4、KOH,此选项错误;
C、该反应的化学方程式为H2SO4+2KOH= K2SO4+2H2O,此选项正确;
D、向图中c点所示溶液中加入铁粉后,铁与硫酸反应生成硫酸亚铁和氢气,可观察到有气泡产生,溶液变为浅绿色,此选项错误。
故选C。
10.D
【详解】A、铁锈的主要成分是氧化铁,食盐水不能与氧化铁反应,食盐水能加快铁制品锈蚀的速率,不能用来除铁锈,故A选项不符合题意;
B、铁锈的主要成分是氧化铁,植物油不能与氧化铁反应,不能用来除铁锈,故B选项不符合题意;
C、铁锈的主要成分是氧化铁,石灰水的主要成分是氢氧化钙,氢氧化钙不能与氧化铁反应,不能用来除铁锈,故C选项不符合题意;
D、铁锈的主要成分是氧化铁,能与稀盐酸反应生成氯化铁和水,盐酸能用来除铁锈,故D选项符合题意。
故选D。
11.D
【详解】A、可用加热的方法鉴别碳酸氢钠与碳酸氢铵,有气体生成的是碳酸氢钠,没有气体生成的碳酸钠,说法正确;
B、氮气的化学性质稳定,可以用作食品的保护气,向装有膨化食品的包装袋内充入氮气以延长保质期,说法正确;
C、灭火的原理:移除可燃物、温度降到着火点一下,隔绝空气或氧气,森林起火时,可在大火蔓延线路前砍掉一片树木,建立隔离带灭火,说法正确;
D、盐酸具有挥发性,将100g10%的稀盐酸加热蒸发掉50g水,溶质氯化氢也挥发减少,使其溶质质量分数不一定是20%,说法错误;
答案:D。
12. 吸收水分发生潮解 二氧化碳 CO2+2NaOH═Na2CO3+H2O HCl
【详解】氢氧化钠在空气中不仅易吸收水分发生潮解,而且还能跟空气中的二氧化碳反应生成碳酸钠和水,反应的化学方程式为:CO2+2NaOH═Na2CO3+H2O;碳酸钠能与稀盐酸反应生成氯化钠、水和二氧化碳气体,检验该固体是否变质可选用的试剂是稀盐酸,其化学式为:HCl。
13. NaOH 石蕊 HCl+NaOH=NaCl+H2O 红褐色沉淀.
【详解】(1)广泛应用于肥皂、石油、造纸、纺织、印染等工业中的一种碱是NaOH。
故填:NaOH。
(2)根据反应①将某种试剂加入碱溶液中,观察到溶液变蓝,则该指示剂是石蕊试液。
故填:石蕊。
(3)若碱为氢氧化钠溶液,氢氧化钠能和盐酸反应生成氯化钠和水,反应的化学方程式:HCl+NaOH=NaCl+H2O。
故填:HCl+NaOH=NaCl+H2O。
(4)氯化铁能和溶于水的碱反应生成红褐色沉淀氢氧化铁,因此反应④中加入氯化铁溶液,能够观察到产生红褐色沉淀。
故填:产生红褐色沉淀。
14.(1)2N2
(2)He
(3)2Ba2+
(4)KNO3
【解析】(1)
分子用化学式表示,多个分子就是在化学式前面加上相应的数字,故2个氮分子表示为:2N2;
(2)
氦气由氦原子构成,化学式为:He;
(3)
离子的表示方法:在该离子元素符号的右上角标上该离子所带的正负电荷数,数字在前,正负号在后,带一个电荷时,1通常省略,多个离子,就是在元素符号前面加上相应的数字;故2个钡离子表示为:2Ba2+;
(4)
硝酸钾含K、N元素,属于复合肥,且含硝酸根离子,故填:KNO3。
15. C6H12O6 C、H、O C6H12O6 SO2 S、O SO2 C C C NaOH Na、O、H Na+、OH Cu、S、O 、H Cu2+、SO42 、H2O 都是含有氢元素的化合物 都是由分子构成的物质 元素不同 一种是离子,一种是原子
【详解】(1)蔗糖化学式为C6H12O6,由C、H、O三种元素组成,由C6H12O6分子构成;二氧化硫化学式为SO2,由S、O两种元素组成,由SO2分子构成;碳化学式为C,由C元素组成,由C原子构成;氢氧化钠化学式为NaOH,由Na、O、H三种元素组成,由钠离子、氢氧根离子构成;硫酸铜溶液中含有硫酸铜和水,含有Cu、S、O 、H四种元素,溶液中含有Cu2+、SO42 、H2O三种微粒;
(2)从H2O,H2O2和NH3三种物质的组成来看都含有氢元素,都是由两种元素组成的纯净物,所以都是化合物;都是由分子构成的物质;从钠离子和氟原子结构示意图可看出二者的质子数分别是11、9,最外层上的电子数分别是8、7,一种是离子,一种是原子;元素种类不同。
16. 无明显变化; 变红色; 溶液浑浊颜色变浅(或消失).
【分析】根据酚酞遇酸性溶液不会变色,酚酞遇中性溶液不变色,酚酞遇碱性溶液红色进行分析解答。
【详解】由指示剂的知识可知酚酞遇酸性溶液不会变色,酚酞遇中性溶液不变色,酚酞遇碱性溶液红色。白醋属于酸,其溶液显酸性,食盐水呈中性,所以取上述清液滴入白醋和食盐水,看到无明显变化,澄清石灰水是氢氧化钙是的水溶液,氢氧化钙溶液呈碱性,取上述清液滴入澄清石灰水,发现溶液变红色,向澄清石灰中吹气时,石灰水与二氧化碳反应会生成碳酸钙的沉淀和水,氢氧化钙不断被消耗,溶液的碱性逐渐减弱直至消失,所以可观察到溶液浑浊颜色变浅(或消失)。
17. 混合物 CO2 K N 淡蓝色 酸雨
【详解】(1)“黑火药”是由木炭粉(C)、硫磺(S)和硝石(KNO3)等多种物质混合而成的,属于混合物;
(2)根据反应的化学方程式S+2KNO3+3CK2S+N2+3X,反应物中钾、氮、氧、碳、硫原子个数分别为2、2、6、3、1,反应后的生成物中钾、氮、氧、碳、硫原子个数分别为2、2、0、0、1,根据反应前后原子种类、数目不变,则3X中含有3个碳原子和6个氧原子,则每个X分子由1个碳原子和2个氧原子构成,则物质X的化学式为CO2;
(3)KNO3中含有钾元素和氮元素;
(4)硫粉在空气中燃烧,产生微弱的淡蓝色火焰,其生成的二氧化硫是形成酸雨的主要物质;
(5)高温条件下,木炭还原氧化铁生成铁和二氧化碳,反应的化学方程式为:。
18. 密度比空气小 易溶于水 碱
【详解】 (1)①由图示信息可以看出,用的是向下排空气法收集氨气,可知氨气具有密度比空气小的性质;②由图示信息可以看出,把水挤入试管后会形成喷泉,说明试管内压强减小,而压强变小的原因就是氨气溶解在水中,可知氨气具有易溶于水的性质;
(2)能形成红色喷泉,说明氨气溶于水后呈碱性,能无色的酚酞变红色。
19.(1)锥形瓶
(2) A
(3)E中的导气管应伸到集气瓶的底部
(4)浓硫酸能和氨气反应
【详解】(1)仪器a的名称是锥形瓶
(2)实验室用氯酸钾和二氧化锰制取氧气,属于固体加热型,故选择A作为发生装置;
实验室制取二氧化碳原理是碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:;
(3)E中的导气管应伸到集气瓶的底部,否则不利于空气的排出,是收集的气体不纯;
(4)氨气溶于水会形成氨水,氨水属于碱能和浓硫酸反应,因此无法使用浓硫酸干燥氨气
20.(1)40
(2)解:40g10%的氢氧化钠溶液中氢氧化钠的质量为,设60g稀硫酸中硫酸的质量为x。
所以该稀硫酸中溶质的质量分数为。
答:该稀硫酸中溶质的质量分数约为8.2%。
【详解】(1)由图知,当溶液的pH=7时溶液中的硫酸恰好完全反应,此时加入氢氧化钠溶液的质量为40g,故填:40。
(2)见答案。
答案第1页,共2页
答案第1页,共2页
