1.2 化学能转化为电能——电池(含解析) 同步练习2023-2024学年高二上学期化学鲁科版(2019)选择性必修1
文档属性
| 名称 | 1.2 化学能转化为电能——电池(含解析) 同步练习2023-2024学年高二上学期化学鲁科版(2019)选择性必修1 |
|
|
| 格式 | docx | ||
| 文件大小 | 678.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-12-14 00:00:00 | ||
图片预览


文档简介
1.2 化学能转化为电能——电池 同步练习
一、单选题
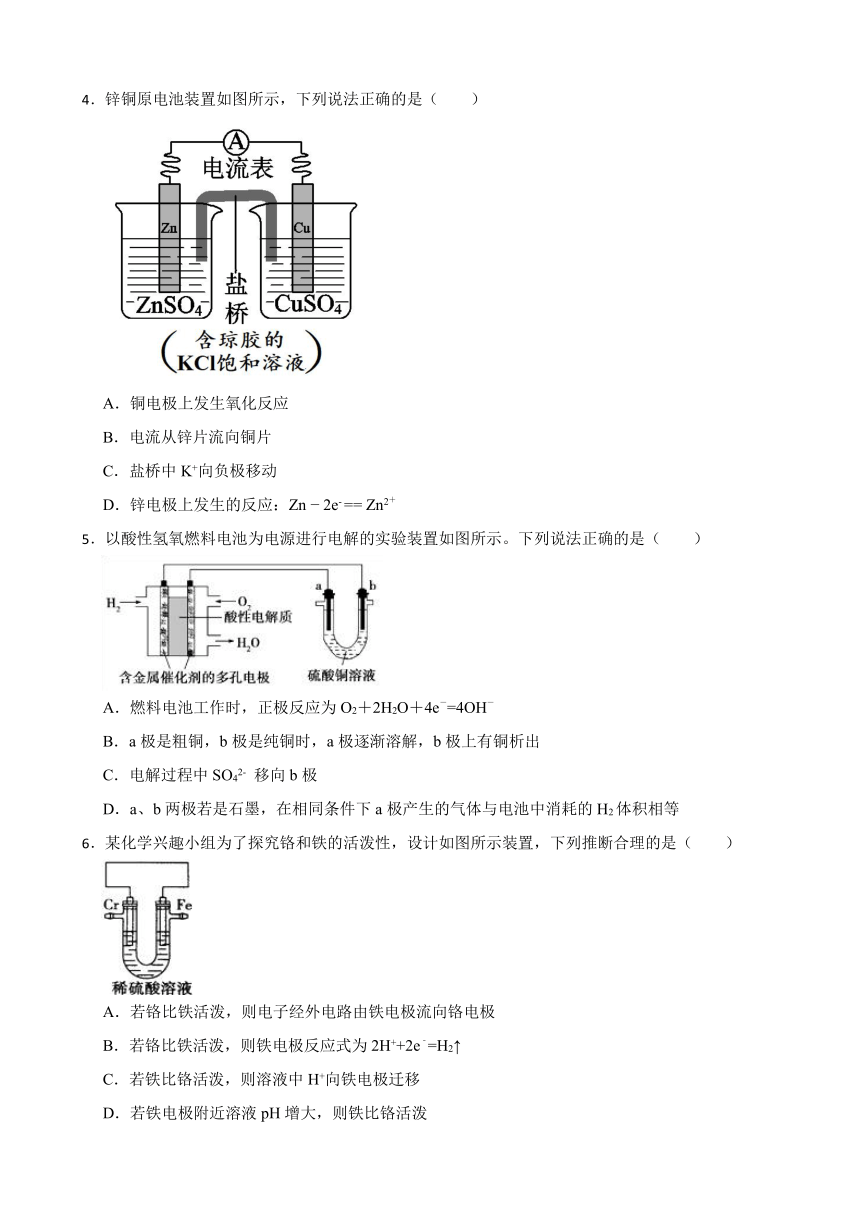
1.锌铜原电池装置如图所示,下列说法正确的是( )
A.电流从锌片流向铜片
B.锌电极的反应式:Zn 2e-=Zn2+
C.铜片作负极
D.盐桥的作用是传递电子
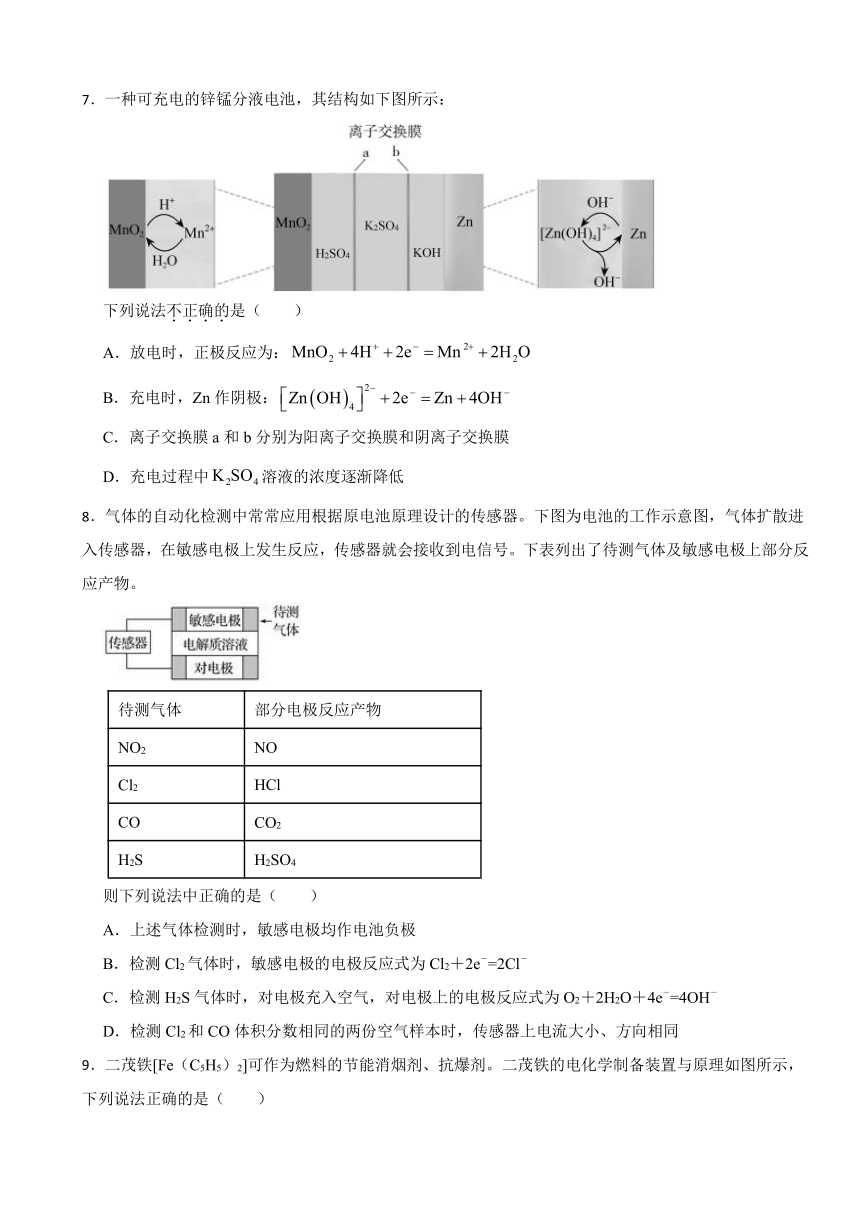
2.一些常见反应的热化学反应方程式如下:
①
②
③
④
欲利用以上反应设计原电池装置,下列说法正确的是( )
A.①不可以设计成原电池装置
B.②不可以设计成原电池装置
C.③可以设计成原电池装置
D.④中反应物只有接触才能形成原电池装置
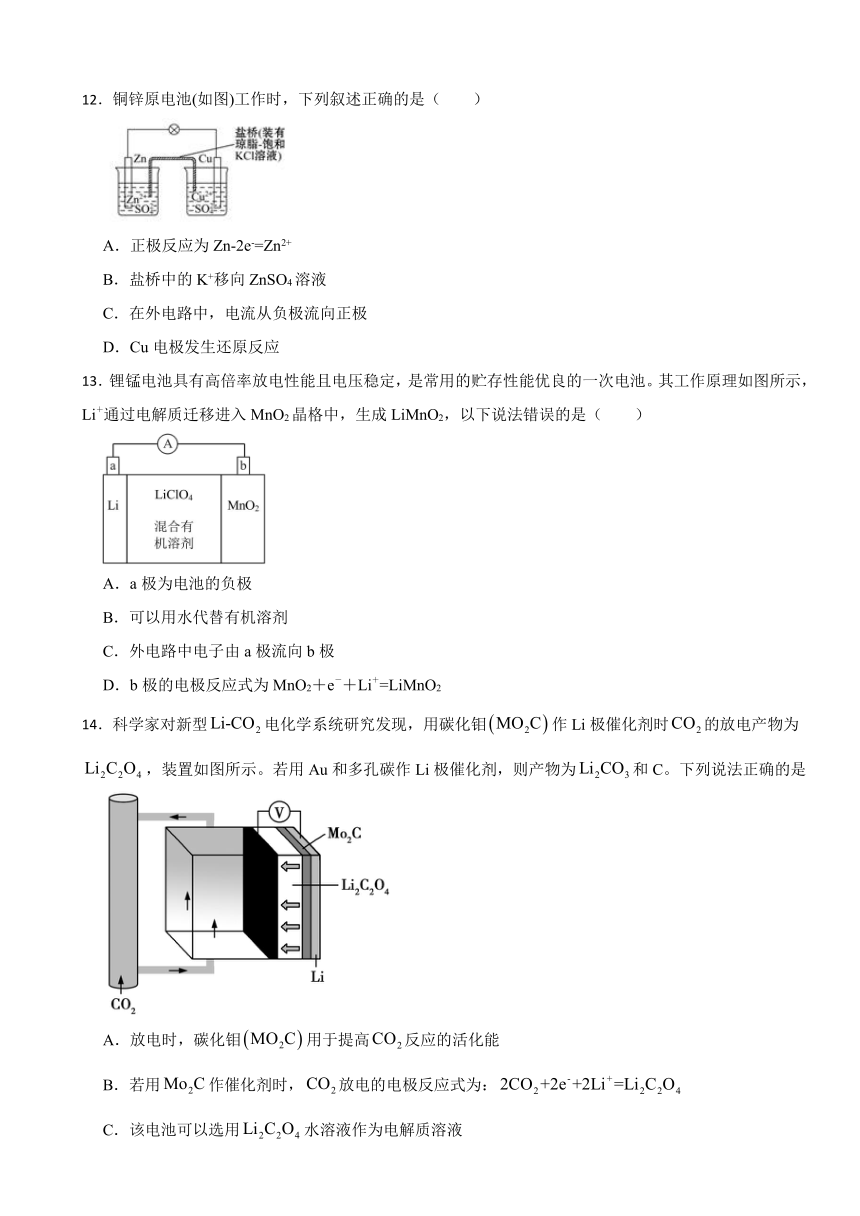
3.下列装置中,属于原电池的是( )
A. B.
C. D.
4.锌铜原电池装置如图所示,下列说法正确的是( )
A.铜电极上发生氧化反应
B.电流从锌片流向铜片
C.盐桥中K+向负极移动
D.锌电极上发生的反应:Zn 2e- == Zn2+
5.以酸性氢氧燃料电池为电源进行电解的实验装置如图所示。下列说法正确的是( )
A.燃料电池工作时,正极反应为O2+2H2O+4e-=4OH-
B.a极是粗铜,b极是纯铜时,a极逐渐溶解,b极上有铜析出
C.电解过程中SO42- 移向b极
D.a、b两极若是石墨,在相同条件下a极产生的气体与电池中消耗的H2体积相等
6.某化学兴趣小组为了探究铬和铁的活泼性,设计如图所示装置,下列推断合理的是( )
A.若铬比铁活泼,则电子经外电路由铁电极流向铬电极
B.若铬比铁活泼,则铁电极反应式为2H++2e﹣=H2↑
C.若铁比铬活泼,则溶液中H+向铁电极迁移
D.若铁电极附近溶液pH增大,则铁比铬活泼
7.一种可充电的锌锰分液电池,其结构如下图所示:
下列说法不正确的是( )
A.放电时,正极反应为:
B.充电时,Zn作阴极:
C.离子交换膜a和b分别为阳离子交换膜和阴离子交换膜
D.充电过程中溶液的浓度逐渐降低
8.气体的自动化检测中常常应用根据原电池原理设计的传感器。下图为电池的工作示意图,气体扩散进入传感器,在敏感电极上发生反应,传感器就会接收到电信号。下表列出了待测气体及敏感电极上部分反应产物。
待测气体 部分电极反应产物
NO2 NO
Cl2 HCl
CO CO2
H2S H2SO4
则下列说法中正确的是( )
A.上述气体检测时,敏感电极均作电池负极
B.检测Cl2气体时,敏感电极的电极反应式为Cl2+2e-=2Cl-
C.检测H2S气体时,对电极充入空气,对电极上的电极反应式为O2+2H2O+4e-=4OH-
D.检测Cl2和CO体积分数相同的两份空气样本时,传感器上电流大小、方向相同
9.二茂铁[Fe(C5H5)2]可作为燃料的节能消烟剂、抗爆剂。二茂铁的电化学制备装置与原理如图所示,下列说法正确的是( )
A.a为电源的正极
B.电解质溶液是NaBr水溶液和DMF溶液的混合液
C.电解池的总反应化学方程式为Fe+2C5H6 [Fe(C5H5)2]+H2↑
D.混合液中Na+移向阳极
10.锂(Li)—空气电池的工作原理如图所示下列说法错误的是( )
A.金属锂作负极,发生氧化反应
B.Li+通过有机电解质向水溶液处移动
C.正极的电极反应:O2+4e-=2O2-
D.电池总反应:4Li+O2+2H2O=4LiOH
11.用VB2-空气电池电解硝酸银溶液(a、b、c均为惰性电极)装置如图所示。VB2电极的反应式为:2VB2+22OH--22e-=V2O5+2B2O3+11H2O,当外电路中通过0.04mol电子时,B装置内共收集到0.448 L气体(标准状况),则下列说法错误的是( )
A.原电池工作时总反应为:4VB2+11O2=4B2O3+2V2O5
B.b电极为阳极,发生氧化反应
C.电解过程中,c电极表面先有固体物质析出,后有气泡产生
D.若B装置内的液体体积为100 mL(忽略体积变化),则硝酸银溶液的物质的量浓度为0.4mol L-1
12.铜锌原电池(如图)工作时,下列叙述正确的是( )
A.正极反应为Zn-2e-=Zn2+
B.盐桥中的K+移向ZnSO4溶液
C.在外电路中,电流从负极流向正极
D.Cu电极发生还原反应
13.锂锰电池具有高倍率放电性能且电压稳定,是常用的贮存性能优良的一次电池。其工作原理如图所示,Li+通过电解质迁移进入MnO2晶格中,生成LiMnO2,以下说法错误的是( )
A.a极为电池的负极
B.可以用水代替有机溶剂
C.外电路中电子由a极流向b极
D.b极的电极反应式为MnO2+e-+Li+=LiMnO2
14.科学家对新型电化学系统研究发现,用碳化钼作Li极催化剂时的放电产物为,装置如图所示。若用Au和多孔碳作Li极催化剂,则产物为和C。下列说法正确的是
A.放电时,碳化钼用于提高反应的活化能
B.若用作催化剂时,放电的电极反应式为:
C.该电池可以选用水溶液作为电解质溶液
D.生成等物质的量的和时,转移电子数不相同
15.如图是课外活动小组设计的用化学电源使LED灯发光装置.下列说法不正确的是( )
A.锌是负极,电子从锌片经导线流向铜片
B.氢离子在铜片表面被还原
C.装置中存在“化学能→电能→光能”的转换
D.如果将硫酸换成橙汁,导线中不会有电子流动
16.某科研小组公司开发了Li-SO2Cl2军用电池,其示意图如下图所示,已知电池总反应为:2Li+ SO2Cl2= 2LiCl+SO2↑。下列叙述中错误的是( )
A.电池工作时负极材料是Li,发生氧化反应
B.电池工作时电子流向:锂电极→导线→负载→碳棒
C.电池工作时,外电路流过0.2 mol电子,标准状况下生成4.48 L气体
D.电池工作过程中,石墨电极反应式为SO2Cl2+2e-=2Cl-+SO2↑
二、综合题
17.利用化学反应将储存在物质内部的化学能转化为电能,科学家设计出了原电池,从而为人类生产、生活提供能量。 一同学依据氧化还原反应:2Ag++Cu=Cu2++2Ag设计的原电池如图所示:
①负极的材料是 ,发生的电极反应为 ;正极发生的电极反应为 。
②外电路中的电子是从 电极流向 电极。(写出电极材料的名称)
③当反应进行到一段时间后取出电极材料,测得某一电极增重了5.4 g,则该原电池反应共转移的电子数目是 。
18.甲醛有毒,被世界卫生组织列为一类致癌物。但甲醛是重要的工业原料,在化工、纺织、医疗等领域有广泛应用。
(1)Ⅰ.回收利用是一种减弱温室效应的有效途径。科学家研究发现可利用回收的与反应制备甲醛。
已知:①甲醛的燃烧热为
②的燃烧热为
③
与制备甲醛的反应: 。
(2)在2L恒容密闭容器中通入0.2mol和0.4mol,在三种不同条件下发生(1)中反应,测得的转化率与时间的关系如图所示。曲线X对应温度下反应的平衡常数K= ,由曲线Y到曲线X采取的措施可能是 ;由曲线Z到曲线X采取的措施可能是 。
(3)反应速率,,、分别为正、逆向反应速率常数,计算m点 。
(4)Ⅱ.甲醇直接脱氢是工业上合成甲醛的一种新方法,该法得到无水甲醛的同时得到副产品氢气。
在一个2L恒容密闭容器中投入2mol,在催化剂作用下发生反应: ,同时存在副反应:。。20min后,测得甲醇的转化率与甲醛的选择性分别与温度的关系如图所示。温度高于650℃,甲醇的转化率升高,甲醛的产率 ,原因可能是 。
(5)甲醛被称为室内污染“第一杀手”。室内甲醛的含量可以通过传感器来监测。一种燃料电池型甲醛气体传感器的工作原理如图所示,则a电极反应式为 。国家标准是室内甲醛不能超过,传感器在室内空间测定,电路中有电子通过,该室内甲醛含量为 。
19.
(1)铅蓄电池是典型的可充型电池,电池总反应式为:Pb+PbO2+4H++2SO42- 2PbSO4+2H2O。请回答下列问题(不考虑氢、氧的氧化还原):放电时,正极的电极反应式是 ;电解液中H2SO4的浓度将变 ;当外电路通过1 mol电子时,理论上负极板的质量增加 g。
(2)微型纽扣电池在现代生活中有广泛应用。有一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH溶液,电极反应为Zn+2OH--2e-=ZnO+H2O,Ag2O+H2O+2e-=2Ag+2OH-。
根据上述反应式,完成下列题目。
①下列叙述正确的是 。
A.在使用过程中,电解质KOH被不断消耗
B.使用过程中,电子由Ag2O极经外电路流向Zn极
C.Zn是负极,Ag2O是正极
D.Zn电极发生还原反应,Ag2O电极发生氧化反应
②写出电池的总反应式: 。
③使用时,负极区的pH (填“增大”“减小”或“不变”,下同),正极区的pH ,电解质溶液的pH 。
20.熔融盐燃料电池具有较高的发电效率,因而受到重视.某燃料电池以熔融的K2CO3(其中不含O2﹣和HCO﹣3)为电解质,以丁烷为燃料,以空气为氧化剂,以具有催化作用和导电性能的稀土金属材料为电极.该燃料电池负极电极反应式为:2C4H10+26CO32﹣﹣52e﹣═34CO2+10H2O.
试回答下列问题:
(1)该燃料电池中发生氧化反应的物质是 .
(2)该燃料电池的化学反应方程式为 ;
(3)某学生想用该燃料电池电解饱和食盐水,写出反应的离子方程式 .
(4)当电路中通过0.26NA的电子时,消耗的氧气的体积(标况)为 ;此时电解饱和食盐水生成的氯气的物质的量是 ;若此时溶液体积为200mL,则生成的NaOH的物质的量浓度为 .
21.利用电极反应可探究物质氧化性、还原性的变化规律。
已知:酸性介质中,1mol/L不同电对的电极电势见下表。电极电势越高,其氧化型物质的氧化性越强;电极电势越低,其还原型物质的还原性越强。
电对(氧化型/还原型)
电极电势/V 0.771 1.776 0.695 1.224 0.536
回答下列问题:
(1)I.探究的分解反应
催化分解反应过程包括i、ii两步:
反应i: (未配平)
反应ii:
反应i的离子方程式为 。
(2)验证生成:反应过程中,加入 溶液,产生蓝色沉淀,证明有生成。
(3)酸性条件下也可催化分解。结合表中数据判断,上述条件下、、的氧化性由强到弱的顺序为 。
(4)Ⅱ.探究物质氧化性变化对电化学反应方向的影响
用可逆反应设计电池,按图a装置进行实验,测得电压E()随时间t的变化如图b所示:
电池初始工作时,正极的电极反应式为 。
(5)某小组从还原型物质浓度、氧化性变化的角度分析图b,提出以下猜想:
猜想1:增大,的氧化性减弱,正极的电极电势降低。
猜想2:减小,的氧化性增强,负极的电极电势升高。
①时间后,按图a装置探究,验证上述猜想的合理性,完成表中填空。
实验 实验操作 电压E/V 结论
i 往烧杯A中加入适量Fe E 0 猜想1成立
ii 往烧杯B中加入适量 E<0 猜想2成立
②有同学认为,上述实验不足以证明猜想1成立。利用上述反应,从化学平衡移动的角度解释猜想1不足以成立的理由 。
③为进一步验证猜想1,进行实验Ⅱi,完成表中填空。
实验 实验操作 电压E/V 结论
iii 往烧杯A中加入适量 E<0 猜想1成立
结论:可逆氧化还原反应中,浓度的变化引起电对氧化性变化,从而改变电池反应方向。
答案解析部分
1.【答案】B
【解析】【解答】A. 原电池中,电流从正极流向负极,从铜片流向锌片,A不符合题意;
B. Zn作负极,失电子,发生氧化反应,锌电极的反应式:Zn-2e-=Zn2+,B符合题意;
C. 较为活泼的金属作负极,锌作负极,铜作正极,C不符合题意;
D. 盐桥的作用是传递离子,电子不能通过溶液,D不符合题意;
故答案为:B。
【分析】锌铜原电池中Zn作负极,失电子,发生氧化反应,盐桥的作用是传递离子。
2.【答案】B
【解析】【解答】A.①是自发的氧化还原反应可以设计成燃料电池,故A不符合题意;
B.②不是氧化还原反应,不能设计成原电池,故B符合题意;
C.③是吸热反应,不能设计成原电池,故C不符合题意;
D.将铁放入FeCl2溶液中,将FeCl3放入另一个装置中,两个装置之间用盐桥连接,反应物不直接接触,④也可形成原电池,故D不符合题意;
故答案为:B。
【分析】能设计成原电池的反应,则其反应过程中存在电子转移,据此结合所给反应中是否存在元素化合价变化进行分析。
3.【答案】D
【解析】【解答】解:A、两电极材料相同,所以不能形成原电池,故A错误.
B、酒精不是电解质,锌和酒精不能自发的进行氧化还原反应,所以不能形成原电池,故B错误.
C、该装置两电极间不能构成闭合回路,所以不能形成原电池,故C错误.
D、该装置符合原电池的构成条件,所以能形成原电池,故D正确.
故选D.
【分析】根据原电池的构成条件分析,原电池的构成条件是:①有两个活泼性不同的电极,②将电极插入电解质溶液中,③两电极间构成闭合回路,④能自发的进行氧化还原反应.
4.【答案】D
【解析】【解答】A、Cu电极作正极,发生还原反应,A不符合题意;
B、Cu电极作正极,Zn电极作负极,则电流由铜片流向锌片,B不符合题意;
C、电流在外电路中由正极流向负极,则盐桥中K+向正极移动,C不符合题意;
D、Zn电极作负极,电极反应为Zn-2e-=Zn2+,D符合题意;
故答案为:D。
【分析】A、正极失电子,发生还原反应;
B、电流由正极沿导线流向负极;
C、盐桥中阳离子流向正极;
D、负极失电子发生氧化反应。
5.【答案】B
【解析】【解答】A.因该燃料电池是在酸性电解质中工作,所以正极反应为:O2+4e-+4H+=2H2O, 选项A不符合题意;
B.a极是粗铜,b极是纯铜时,为粗铜的精炼,电解时,a极逐渐溶解,b极上有铜析出,符合精炼铜原理,选项B符合题意;
C. b与电池的负极相连,b为电解池的阴极,a极是阳极,阴离子SO42- 移向阳极a极移动,选项C不符合题意;
D.电解CuSO4溶液时,a极产生的气体为O2,产生1molO2需4mol电子,所以需要燃料电池的2molH2,二者的体积并不相等,选项D不符合题意;
故答案为:B。
【分析】通过氧化还原反应而产生电流的装置称为原电池,也可以说是把化学能转变成电能的装置。有的原电池可以构成可逆电池,有的原电池则不属于可逆电池。原电池放电时,负极发生氧化反应,正极发生还原反应。
6.【答案】B
【解析】【解答】解:A.若铬比铁活泼,则负极为铬失电子发生氧化反应,正极为铁,电子经外电路由铬电极流向铁电极,故A错误;
B.若铬比铁活泼,则负极为铬失电子发生氧化反应,正极为铁,氢离子在铁上得电子发生还原反应,反应式为2H++2e﹣=H2↑,故B正确;
C.若铁比铬活泼,则负极为铁失电子发生氧化反应,正极为铬,氢离子向正极铬移动,故C错误;
D.若铁电极附近溶液pH增大,则发生2H++2e﹣=H2↑,所以铁为正极,则铬比铁活泼,故D错误.
故选:B.
【分析】若铬比铁活泼,则负极为铬失电子发生氧化反应,正极为铁,氢离子在铁上得电子发生还原反应,电子经外电路由铬电极流向铁电极;若铁比铬活泼,则负极为铁失电子发生氧化反应,正极为铬,氢离子在铬上得电子发生还原反应,电子经外电路由铁电极流向铬电极.
7.【答案】C
【解析】【解答】A.放电时,Zn是负极、MnO2是正极,根据图示正极反应为:,故A不符合题意;;
B.放电时,Zn是负极,充电时,Zn作阴极,根据图示,阴极反应式为,故B不符合题意;
C.放电过程中,负极区通过离子交换膜a进入硫酸钾溶液, 正极区K+通过离子交换膜b进入硫酸钾溶液,所以a和b分别为阴离子交换膜和阳离子交换膜,故C符合题意;
D.充电过程中,K+通过离子交换膜b进入负极区,通过离子交换膜a 进入正极区,所以溶液的浓度逐渐降低,故D不符合题意;
故答案为:C。
【分析】A.Zn作负极,MnO2作正极,正极发生还原反应,根据图示可写出电极反应式;
B.阴极发生还原反应,根据图示分析可知阴极电极反应式;
C.分析电池工作原理可知a为阴离子交换膜,b为阳离子交换膜;
D.充电时,钾离子和硫酸根离子的移动方向和放电时相反,分析工作原理,判断移动方向。
8.【答案】B
【解析】【解答】A. NO2、Cl2在正极得电子发生还原反应,H2S、CO在负极失电子发生氧化反应,A项不符合题意;
B. Cl2得电子生成HCl,电极反应式为Cl2+2e-=2Cl-,B项符合题意;
C. H2S失去电子生成硫酸,在酸性条件下,氧气得电子应该生成水,其电极反应式为:O2+4H++4e-=2H2O,C项不符合题意;
D. 等体积的Cl2和CO发生原电池反应时,1 mol Cl2得2 mol电子,1 mol CO失去2 mol电子,传感器上电流方向相反,D项不符合题意;
故答案为:B。
【分析】A、二氧化氮、氯气化合价降低为正极
C、酸性条件,电荷守恒配氢离子
D、氯气化合价降低,CO化合价升高,电流方向相反
9.【答案】C
【解析】【解答】A.由分析可知,a为电源的负极,b为电源的正极,故A不符合题意;
B.与电源负极a相连的镍为电解池的阴极,钠离子在阴极上得电子发生还原反应生成钠,钠能与水反应,则电解质溶液不可能为NaBr水溶液,故B不符合题意;
C.由分析可知,制备二茂铁的总反应方程式为Fe+2 +H2↑,故C符合题意;
D.二茂铁制备过程中阴极上钠离子得电子发生还原反应生成钠,电极反应式为 ,Na+移向阴极,故D不符合题意;
故答案为:C。
【分析】根据图示,铁失去电子因此Fe做阳极,Ni做阴极,故a为负极,b为正极,根据反应流程得出有钠单质产生,在阴极生成,因此钠离子向阴极移动,因此电解质溶液不能存在水,根据反应物和生成物即可写出电解池反应式
10.【答案】C
【解析】【解答】A.在锂空气电池中,金属锂失去电子,发生氧化反应,为负极,故A项不符合题意;
B.Li在负极失去电子变成了Li+,会通过有机电解质向水溶液处(正极)移动,故B项不符合题意;
C.正极氧气得到了电子后与氢结合形成氢氧根,电极方程式为O2+4e-+2H2O=4OH-,故C项符合题意;
D.负极的反应式为Li-e-=Li+,正极反应式为O2+4e-+2H2O=4OH-,电池的总反应则为4Li+O2+2H2O=4LiOH,故D项不符合题意。
故答案为:C。
【分析】锂(Li)-空气电池中,锂为负极,发生氧化反应,电极反应为4Li-4e-=4Li+,生成的Li+
向正极移动,通入空气的一极为正极,正极的电极反应为O2+4e-+2H2O=4OH-,把正、负极的电极反应相加可得电池总反应:4Li+O2+2H2O=4LiOH
11.【答案】D
【解析】【解答】A. VB2电极为负极,负极反应式为:2VB2+22OH--22e-=V2O5+2B2O3+11H2O,正极氧气得到电子转化为氢氧根离子,则原电池工作时总反应为:4VB2+11O2=4B2O3+2V2O5,A不符合题意;
B. b电极与电源的正极相连为阳极,发生失去电子的氧化反应,B不符合题意;
C. 电解过程中,c电极为阴极,开始银离子得到电子,然后氢离子得到电子,则表面先有固体物质析出,后有气泡产生,C不符合题意;
D. 当外电路中通过0.04mol电子时,B装置内共收集到0.448 L气体(标准状况),其中阳极产生氧气,物质的量是0.01mol,体积是0.224L,则阴极产生0.01 mol氢气,所以析出单质银的物质的量是0.02mol,所以硝酸银的物质的量是0.02mol,若B装置内的液体体积为100 mL(忽略体积变化),则硝酸银溶液的物质的量浓度为0.2mol L-1,D符合题意;
故答案为:D。
【分析】A中是做的原电池,VB2电极做的是负极,发生的氧化反应,a电极是做正极,氧气发生还原反应,与b连接的是阳极,吸引大量的氢氧根离子和硝酸根离子,氢氧根离子先放电,生成氧气,与c连接的是阴极,吸引大量的氢离子和银离子,银离子先放电,变成银单质。
12.【答案】D
【解析】【解答】A.铜做正极,发生还原反应,电极反应为:Cu2++2e-=Cu,故A不符合题意;
B.锌作负极,发生氧化反应,电极反应为:Zn-2e-=Zn2+;硫酸锌溶液中锌离子浓度增大,盐桥中的氯离子移向硫酸锌溶液;盐桥中的K+移向CuSO4溶液,故B不符合题意;
C.原电池工作时,在外电路中,电子从电池负极经外电路流向正极,电流方向与之相反,故C不符合题意;
D.Cu电极做正极,发生还原反应,故D符合题意;
故答案为:D。
【分析】锌铜构成的原电池,锌作负极,发生氧化反应,电极反应为:Zn-2e-=Zn2+;铜做正极,发生还原反应,电极反应为:Cu2++2e-=Cu,原电池工作时,电子从电池负极经外电路流向正极,由此分析。
13.【答案】B
【解析】【解答】A.由分析可知,a极为Li电极,是电池的负极,故A不符合题意;
B.水能与金属Li直接发生化学反应,不能用水代替有机溶剂,故B符合题意;
C.电子由负极经导线流向正极,a极为电池的负极,b极为电池的正极,则电子从负极a经导线流向正极b,故C不符合题意;
D.MnO2在正极得到电子发生还原反应生成LiMnO2,电极反应式为MnO2+e-+Li+=LiMnO2,故D不符合题意;
故答案为:B。
【分析】新型电池的判断:
1、化合价升高的为负极,失去电子,化合价降低的为正极,得到电子;
2、电极反应式的书写要注意,负极反应为负极材料失去电子化合价升高,正极反应为正极材料得到电子化合价降低,且要根据电解质溶液的酸碱性判断,酸性溶液不能出现氢氧根,碱性溶液不能出现氢离子,且电极反应式要满足原子守恒。
14.【答案】B
【解析】【解答】A.放电时,碳化钼作催化剂、用于降低反应的活化能,A不符合题意;
B.已知碳化钼作Li极催化剂时的放电产物为,反应过程中二氧化碳被还原,则若用作催化剂时,放电的电极反应式为: ,B符合题意;
C. Li能与水反应,则该电池不能选用水溶液作为电解质溶液,C不符合题意;
D.用金作催化剂时电极反应为,若用作催化剂时,放电的电极反应式为: ,则生成等物质的量的和时,转移电子数相同,D不符合题意;
故答案为:B。
【分析】新型电池的判断:
1、化合价升高的为负极,失去电子,化合价降低的为正极,得到电子;
2、电极反应式的书写要注意,负极反应为负极材料失去电子化合价升高,正极反应为正极材料得到电子化合价降低,且要根据电解质溶液的酸碱性判断,酸性溶液不能出现氢氧根,碱性溶液不能出现氢离子,且电极反应式要满足原子守恒。
15.【答案】D
【解析】【解答】解:A.Zn、Cu和稀硫酸构成原电池,锌为负极,铜为正极,电子从负极锌沿导线流向正极铜,故A正确;
B.该原电池中,Cu是正极,Cu电极上氢离子得电子生成氢气被还原,电极反应式为2H++2e﹣=H2↑,故B正确;
C.该装置中化学能转化为电能而产生电流,电流通过LED时,LED发光,则装置中存在“化学能→电能→光能”的转换,故C正确;
D.橙汁溶液呈酸性,Zn、Cu和橙汁能构成原电池,所以将硫酸换成橙汁,导线中仍有电子流动,故D错误;
故选D.
【分析】A.Zn、Cu和稀硫酸构成原电池,锌为负极,铜为正极,电子从负极沿导线流向正极;
B.该原电池中,Cu是正极,Cu电极上氢离子得电子生成氢气;
C.该装置中化学能转化为电能而产生电流,电流通过LED时,LED发光;
D.橙汁溶液呈酸性,Zn、Cu和橙汁能构成原电池.
16.【答案】C
【解析】【解答】A.根据电池的总反应:2Li+ SO2Cl2= 2LiCl+SO2↑。得到单质锂在反应中失电子化合价升高,所以单质锂是该电池的负极,发生失电子的氧化反应,选项A符合题意。
B.锂电极为负极,所以电子从锂电极流出,经导线、负载,到达石墨电极,选项B符合题意。
C.总反应的电子转移数为2e-,所以转移电子是生成的SO2气体的2倍,外电路流过0.2 mol电子,标准状况下生成2.24 L(0.1mol)气体,选项C不符合题意。
D.石墨电极是反应的正极,正极上是SO2Cl2得电子,转化为SO2和Cl-,方程式为:SO2Cl2+2e-=2Cl-+SO2↑,选项D符合题意。
【分析】根据原电池原理分析电极和电极反应,然后书写电极方程式、计算产生的气体体积即可。
17.【答案】铜;Cu-2e-=Cu2+;2Ag++2e-=2Ag;铜;银;0.05NA(或3.01×1022)
【解析】【解答】③正极:
Ag++e-= Ag
0.05 mol 0.05 mol
转移电子数为0.05NA。
【分析】关于原电池的题目,核心在于判断正负极,掌握正向正、负向负的电荷移动原理,结合核心产物与溶液环境,书写电极反应式,根据电极反应式进行计算。
18.【答案】(1)
(2)5;加催化剂;降低温度
(3)25.6
(4)降低;温度升高,平衡正向移动,甲醇转化率升高,但由于温度高于650℃后,催化生成甲醛的催化剂活性降低或副反应生成的氢气浓度增大,导致主反应平衡逆向移动,生成甲醛量减少
(5);0.003
【解析】【解答】(1)氢气燃烧热反应方程式的2倍减去甲醛燃烧热反应方程式,再减去③得到与制备甲醛的反应: ;故答案为:。
(2)根据题意曲线X对应温度下平衡时,消耗二氧化碳物质的量为0.1mol,消耗氢气物质的量为0.2mol,生成甲醛、水蒸气物质的量为0.1mol,剩余二氧化碳物质的量为0.1mol,剩余氢气物质的量为0.2mol,则该温度下平衡常数,分析曲线Y和曲线X,平衡时各物质的量相等,但达到平衡时时间不相同,说明由曲线Y到曲线X采取的措施可能是加入催化剂;曲线Z与曲线X分析,曲线Z所需时间比曲线X时间短,但二氧化碳转化率比X低,由曲线Z到曲线X是平衡正向移动,反应速率减慢了,因此采取的措施可能是降低温度;故答案为:5;加催化剂;降低温度。
(3)根据平衡常数得到,在m点时消耗二氧化碳物质的量为0.04mol,消耗氢气物质的量为0.08mol,生成甲醛、水蒸气物质的量为0.04mol,剩余二氧化碳物质的量为0.16mol,剩余氢气物质的量为0.32mol,则m点;故答案为:25.6。
(4)根据图中信息得到,温度高于650℃,甲醇的转化率升高,甲醛的产率降低,根据两个方程式分析,两个方程式都为吸热反应,升高温度,平衡正向移动,甲醇转化率升高,由于副反应生成氢气,氢气量增大,对主反应来说,氢气浓度增大,导致主反应逆向移动,生成甲醛的量减少,也可能是甲醛催化剂的催化活性降低即温度升高,平衡正向移动,甲醇转化率升高,但由于温度高于650℃后,催化生成甲醛的催化剂活性降低或副反应生成的氢气浓度增大,导致主反应平衡逆向移动,生成甲醛量减少;故答案为:降低;温度升高,平衡正向移动,甲醇转化率升高,但由于温度高于650℃后,催化生成甲醛的催化剂活性降低或副反应生成的氢气浓度增大,导致主反应平衡逆向移动,生成甲醛量减少。
(5)根据题意甲醛变为二氧化碳,甲醛中碳化合价升高,失去电子,作负极,因此a电极反应式为。国家标准是室内甲醛不能超过,传感器在室内空间测定,电路中有电子通过,则含有甲醛物质的量为,该室内甲醛含量为;故答案为:;0.003。
【分析】(1)首先写出甲醛、氢气的燃烧热,利用盖斯定律,即可得到二氧化碳与氢气反应的热化学反应方程式。
(2)根据二氧化碳转化率,列出三段式,求出各物质平衡浓度,带入平衡常数表达式即可。
(3)根据达到平衡时V正=V逆,结合平衡常数表达式可以得到,K正/K逆=K=5,根据m点转化率,求出各物质浓度,带入表达式即可得到其比值。
(4)平衡图像解题技巧:对应化学反应速率图像和化学平衡图像,应该注意下列几点:1、横轴坐标和纵坐标含有;2、曲线斜率或者趋势;3、曲线上特殊点,如起点、终点、交点和拐点等;4、根据需要运用辅助线,如等温线、等压线等
19.【答案】(1)PbO2+2e-+4H++2SO42-=PbSO4+2H2O;小;48
(2)C;Zn+Ag2O=2Ag+ZnO;减小;增大;不变
【解析】【解答】(1)关键电池总反应式为Pb+PbO2+4H++2SO42- 2PbSO4+2H2O可判断负极是铅失去电子发生氧化反应,负极电极反应为Pb-2e-+SO42-=PbSO4;正极是二氧化铅得到电子,发生还原反应,正极电极反应式为PbO2+2e-+4H++2SO42-=PbSO4+2H2O,因此放电时电解液中硫酸的浓度将减少;当外电路通过1mol电子时,依据电子守恒计算理论上负极板的质量增加0.5mol×303g/mol-0.5mol×207g/mol=48g;
(2)①A、负极电极反应式为Zn+2OH--2e-=ZnO+H2O、正极电极反应式为 Ag2O+H2O+2e-=2Ag+2OH-,所以电池反应式为Zn+Ag2O=2Ag+ZnO,因此氢氧化钾的量不变,A错误;
B、由电极反应式可知,Zn的化合价由0价升高到+2价,被氧化,为原电池的负极,则正极为Ag2O,原电池中电子从负极流向正极,即从锌经导线流向Ag2O,B错误;
C、正极电极反应为:Ag2O+H2O+2e-=2Ag+2OH-,负极电极反应:Zn+2OH--2e-=ZnO+H2O,所以Zn是负极,Ag2O是正极,C正确;
D、由电极反应式可知,Zn的化合价由0价升高到+2价,为原电池的负极,发生氧化反应,Ag2O是正极发生还原反应,D错误;
故答案为:C。
②负极电极反应式为Zn+2OH--2e-=ZnO+H2O、正极电极反应式为 Ag2O+H2O+2e-=2Ag+2OH-,所以电池反应式为Zn+Ag2O=2Ag+ZnO;
③该原电池中,Zn元素化合价由0价变为+2价、Ag元素化合价由+1价变为0价,所以Zn是负极失电子发生氧化反应,Ag2O是正极得电子发生还原反应;负极的电极反应式为:Zn+2OH--2e-=ZnO+H2O,则负极附近pH减小;正极电极反应式为 Ag2O+H2O+2e-=2Ag+2OH-,所以正极溶液的pH增大,电子转移相等的情况下负极消耗的氢氧根与正极产生的氢氧根离子的物质的量相等,所以溶液的pH值不变。
【分析】(1)铅蓄电池放电时相当于原电池,正极发生氧化反应,放电时消耗硫酸,所以硫酸浓度减小,根据电荷守恒计算负极板得质量增加两;
(2)①纽扣电池的负极发生氧化反应,正极发生还原反应;
②两电极之和即为原电池的总反应方程式;
③根据电极方程式和总反应方程式进行分析溶液的pH变化。
20.【答案】(1)丁烷
(2)2C4H10+13O2=8CO2+10H2O
(3)2Cl﹣+2H2O Cl2↑+H2↑+2OH﹣
(4)1.456L;0.13mol;1.3mol/L
【解析】【解答】解:(1)燃料电池中发生氧化反应的物质为负极燃料,所以该燃料电池中发生氧化反应的物质是丁烷,故答案为:丁烷;(2)该电池中,丁烷和氧气反应生成二氧化碳和水,反应方程式为:2C4H10+13O2=8CO2+10H2O,
故答案为:2C4H10+13O2=8CO2+10H2O;(3)电解饱和食盐水时,阳极上氯离子放电生成氯气,阴极上氢离子放电生成氢气,同时还生成氢氧化钠,离子方程式为:2Cl﹣+2H2O Cl2↑+H2↑+2OH﹣,故答案为:2Cl﹣+2H2O Cl2↑+H2↑+2OH﹣;(4)电路中通过0.26NA的电子时,因为串联电池中转移电子数相等,所以消耗的氧气的体积(标况)为 ×22.4=1.456L,电解饱和食盐水生成的氯气的物质的量是 =0.13mol,生成氢氧化钠的物质的量为0.26mol,所以NaOH的物质的量浓度为
=1.3mol/L,故答案为:1.456;0.13mol;1.3mol/L.
【分析】(1)燃料电池中发生氧化反应的物质为负极燃料;(2)丁烷和氧气反应生成二氧化碳和水;(3)电解饱和食盐水时,阳极上氯离子放电,阴极上氢离子放电;(4)电路中通过0.26NA的电子时,根据串联电池中转移电子数相等计算.
21.【答案】(1)
(2)
(3)>>
(4)
(5)<;AgNO3固体;加入铁粉后,同时造成增大,减小,都能使平衡逆移,使E<0;FeCl2固体
【解析】【解答】(1)结合分析可知,反应i中铁离子把双氧水氧化了,生成亚铁离子、氧气和水,离子方程式为;
(2)遇二价铁发生反应:,生成深蓝色沉淀,则反应过程中,加入溶液,产生蓝色沉淀,证明有二价铁生成;
(3)据分析,上述条件下过氧化氢、二氧化锰、氧的氧化性由强到弱的顺序:过氧化氢>二氧化锰>氧气。
(4)电池初始工作时,由可知,铁离子得电子发生还原反应转变为亚铁离子,为正极,则正极的电极反应式为。
【分析】要通过反应探究对电化学反应方向的影响,从某还原型物质浓度、氧化性变化的角度分析图b,对于2个猜想,只能通过改变一个变量观察是否使E<0来探究——猜想1:二价铁浓度增大,三价铁的氧化性减弱,正极的电极电势降低,故只能通过A烧杯加适量氯化亚铁固体,增加亚铁离子浓度,猜想2:碘离子浓度减小,碘的氧化性增强,负极的电极电势升高,只能通过B烧杯加适量硝酸银固体减少碘离子浓度来实现。
一、单选题
1.锌铜原电池装置如图所示,下列说法正确的是( )
A.电流从锌片流向铜片
B.锌电极的反应式:Zn 2e-=Zn2+
C.铜片作负极
D.盐桥的作用是传递电子
2.一些常见反应的热化学反应方程式如下:
①
②
③
④
欲利用以上反应设计原电池装置,下列说法正确的是( )
A.①不可以设计成原电池装置
B.②不可以设计成原电池装置
C.③可以设计成原电池装置
D.④中反应物只有接触才能形成原电池装置
3.下列装置中,属于原电池的是( )
A. B.
C. D.
4.锌铜原电池装置如图所示,下列说法正确的是( )
A.铜电极上发生氧化反应
B.电流从锌片流向铜片
C.盐桥中K+向负极移动
D.锌电极上发生的反应:Zn 2e- == Zn2+
5.以酸性氢氧燃料电池为电源进行电解的实验装置如图所示。下列说法正确的是( )
A.燃料电池工作时,正极反应为O2+2H2O+4e-=4OH-
B.a极是粗铜,b极是纯铜时,a极逐渐溶解,b极上有铜析出
C.电解过程中SO42- 移向b极
D.a、b两极若是石墨,在相同条件下a极产生的气体与电池中消耗的H2体积相等
6.某化学兴趣小组为了探究铬和铁的活泼性,设计如图所示装置,下列推断合理的是( )
A.若铬比铁活泼,则电子经外电路由铁电极流向铬电极
B.若铬比铁活泼,则铁电极反应式为2H++2e﹣=H2↑
C.若铁比铬活泼,则溶液中H+向铁电极迁移
D.若铁电极附近溶液pH增大,则铁比铬活泼
7.一种可充电的锌锰分液电池,其结构如下图所示:
下列说法不正确的是( )
A.放电时,正极反应为:
B.充电时,Zn作阴极:
C.离子交换膜a和b分别为阳离子交换膜和阴离子交换膜
D.充电过程中溶液的浓度逐渐降低
8.气体的自动化检测中常常应用根据原电池原理设计的传感器。下图为电池的工作示意图,气体扩散进入传感器,在敏感电极上发生反应,传感器就会接收到电信号。下表列出了待测气体及敏感电极上部分反应产物。
待测气体 部分电极反应产物
NO2 NO
Cl2 HCl
CO CO2
H2S H2SO4
则下列说法中正确的是( )
A.上述气体检测时,敏感电极均作电池负极
B.检测Cl2气体时,敏感电极的电极反应式为Cl2+2e-=2Cl-
C.检测H2S气体时,对电极充入空气,对电极上的电极反应式为O2+2H2O+4e-=4OH-
D.检测Cl2和CO体积分数相同的两份空气样本时,传感器上电流大小、方向相同
9.二茂铁[Fe(C5H5)2]可作为燃料的节能消烟剂、抗爆剂。二茂铁的电化学制备装置与原理如图所示,下列说法正确的是( )
A.a为电源的正极
B.电解质溶液是NaBr水溶液和DMF溶液的混合液
C.电解池的总反应化学方程式为Fe+2C5H6 [Fe(C5H5)2]+H2↑
D.混合液中Na+移向阳极
10.锂(Li)—空气电池的工作原理如图所示下列说法错误的是( )
A.金属锂作负极,发生氧化反应
B.Li+通过有机电解质向水溶液处移动
C.正极的电极反应:O2+4e-=2O2-
D.电池总反应:4Li+O2+2H2O=4LiOH
11.用VB2-空气电池电解硝酸银溶液(a、b、c均为惰性电极)装置如图所示。VB2电极的反应式为:2VB2+22OH--22e-=V2O5+2B2O3+11H2O,当外电路中通过0.04mol电子时,B装置内共收集到0.448 L气体(标准状况),则下列说法错误的是( )
A.原电池工作时总反应为:4VB2+11O2=4B2O3+2V2O5
B.b电极为阳极,发生氧化反应
C.电解过程中,c电极表面先有固体物质析出,后有气泡产生
D.若B装置内的液体体积为100 mL(忽略体积变化),则硝酸银溶液的物质的量浓度为0.4mol L-1
12.铜锌原电池(如图)工作时,下列叙述正确的是( )
A.正极反应为Zn-2e-=Zn2+
B.盐桥中的K+移向ZnSO4溶液
C.在外电路中,电流从负极流向正极
D.Cu电极发生还原反应
13.锂锰电池具有高倍率放电性能且电压稳定,是常用的贮存性能优良的一次电池。其工作原理如图所示,Li+通过电解质迁移进入MnO2晶格中,生成LiMnO2,以下说法错误的是( )
A.a极为电池的负极
B.可以用水代替有机溶剂
C.外电路中电子由a极流向b极
D.b极的电极反应式为MnO2+e-+Li+=LiMnO2
14.科学家对新型电化学系统研究发现,用碳化钼作Li极催化剂时的放电产物为,装置如图所示。若用Au和多孔碳作Li极催化剂,则产物为和C。下列说法正确的是
A.放电时,碳化钼用于提高反应的活化能
B.若用作催化剂时,放电的电极反应式为:
C.该电池可以选用水溶液作为电解质溶液
D.生成等物质的量的和时,转移电子数不相同
15.如图是课外活动小组设计的用化学电源使LED灯发光装置.下列说法不正确的是( )
A.锌是负极,电子从锌片经导线流向铜片
B.氢离子在铜片表面被还原
C.装置中存在“化学能→电能→光能”的转换
D.如果将硫酸换成橙汁,导线中不会有电子流动
16.某科研小组公司开发了Li-SO2Cl2军用电池,其示意图如下图所示,已知电池总反应为:2Li+ SO2Cl2= 2LiCl+SO2↑。下列叙述中错误的是( )
A.电池工作时负极材料是Li,发生氧化反应
B.电池工作时电子流向:锂电极→导线→负载→碳棒
C.电池工作时,外电路流过0.2 mol电子,标准状况下生成4.48 L气体
D.电池工作过程中,石墨电极反应式为SO2Cl2+2e-=2Cl-+SO2↑
二、综合题
17.利用化学反应将储存在物质内部的化学能转化为电能,科学家设计出了原电池,从而为人类生产、生活提供能量。 一同学依据氧化还原反应:2Ag++Cu=Cu2++2Ag设计的原电池如图所示:
①负极的材料是 ,发生的电极反应为 ;正极发生的电极反应为 。
②外电路中的电子是从 电极流向 电极。(写出电极材料的名称)
③当反应进行到一段时间后取出电极材料,测得某一电极增重了5.4 g,则该原电池反应共转移的电子数目是 。
18.甲醛有毒,被世界卫生组织列为一类致癌物。但甲醛是重要的工业原料,在化工、纺织、医疗等领域有广泛应用。
(1)Ⅰ.回收利用是一种减弱温室效应的有效途径。科学家研究发现可利用回收的与反应制备甲醛。
已知:①甲醛的燃烧热为
②的燃烧热为
③
与制备甲醛的反应: 。
(2)在2L恒容密闭容器中通入0.2mol和0.4mol,在三种不同条件下发生(1)中反应,测得的转化率与时间的关系如图所示。曲线X对应温度下反应的平衡常数K= ,由曲线Y到曲线X采取的措施可能是 ;由曲线Z到曲线X采取的措施可能是 。
(3)反应速率,,、分别为正、逆向反应速率常数,计算m点 。
(4)Ⅱ.甲醇直接脱氢是工业上合成甲醛的一种新方法,该法得到无水甲醛的同时得到副产品氢气。
在一个2L恒容密闭容器中投入2mol,在催化剂作用下发生反应: ,同时存在副反应:。。20min后,测得甲醇的转化率与甲醛的选择性分别与温度的关系如图所示。温度高于650℃,甲醇的转化率升高,甲醛的产率 ,原因可能是 。
(5)甲醛被称为室内污染“第一杀手”。室内甲醛的含量可以通过传感器来监测。一种燃料电池型甲醛气体传感器的工作原理如图所示,则a电极反应式为 。国家标准是室内甲醛不能超过,传感器在室内空间测定,电路中有电子通过,该室内甲醛含量为 。
19.
(1)铅蓄电池是典型的可充型电池,电池总反应式为:Pb+PbO2+4H++2SO42- 2PbSO4+2H2O。请回答下列问题(不考虑氢、氧的氧化还原):放电时,正极的电极反应式是 ;电解液中H2SO4的浓度将变 ;当外电路通过1 mol电子时,理论上负极板的质量增加 g。
(2)微型纽扣电池在现代生活中有广泛应用。有一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH溶液,电极反应为Zn+2OH--2e-=ZnO+H2O,Ag2O+H2O+2e-=2Ag+2OH-。
根据上述反应式,完成下列题目。
①下列叙述正确的是 。
A.在使用过程中,电解质KOH被不断消耗
B.使用过程中,电子由Ag2O极经外电路流向Zn极
C.Zn是负极,Ag2O是正极
D.Zn电极发生还原反应,Ag2O电极发生氧化反应
②写出电池的总反应式: 。
③使用时,负极区的pH (填“增大”“减小”或“不变”,下同),正极区的pH ,电解质溶液的pH 。
20.熔融盐燃料电池具有较高的发电效率,因而受到重视.某燃料电池以熔融的K2CO3(其中不含O2﹣和HCO﹣3)为电解质,以丁烷为燃料,以空气为氧化剂,以具有催化作用和导电性能的稀土金属材料为电极.该燃料电池负极电极反应式为:2C4H10+26CO32﹣﹣52e﹣═34CO2+10H2O.
试回答下列问题:
(1)该燃料电池中发生氧化反应的物质是 .
(2)该燃料电池的化学反应方程式为 ;
(3)某学生想用该燃料电池电解饱和食盐水,写出反应的离子方程式 .
(4)当电路中通过0.26NA的电子时,消耗的氧气的体积(标况)为 ;此时电解饱和食盐水生成的氯气的物质的量是 ;若此时溶液体积为200mL,则生成的NaOH的物质的量浓度为 .
21.利用电极反应可探究物质氧化性、还原性的变化规律。
已知:酸性介质中,1mol/L不同电对的电极电势见下表。电极电势越高,其氧化型物质的氧化性越强;电极电势越低,其还原型物质的还原性越强。
电对(氧化型/还原型)
电极电势/V 0.771 1.776 0.695 1.224 0.536
回答下列问题:
(1)I.探究的分解反应
催化分解反应过程包括i、ii两步:
反应i: (未配平)
反应ii:
反应i的离子方程式为 。
(2)验证生成:反应过程中,加入 溶液,产生蓝色沉淀,证明有生成。
(3)酸性条件下也可催化分解。结合表中数据判断,上述条件下、、的氧化性由强到弱的顺序为 。
(4)Ⅱ.探究物质氧化性变化对电化学反应方向的影响
用可逆反应设计电池,按图a装置进行实验,测得电压E()随时间t的变化如图b所示:
电池初始工作时,正极的电极反应式为 。
(5)某小组从还原型物质浓度、氧化性变化的角度分析图b,提出以下猜想:
猜想1:增大,的氧化性减弱,正极的电极电势降低。
猜想2:减小,的氧化性增强,负极的电极电势升高。
①时间后,按图a装置探究,验证上述猜想的合理性,完成表中填空。
实验 实验操作 电压E/V 结论
i 往烧杯A中加入适量Fe E 0 猜想1成立
ii 往烧杯B中加入适量 E<0 猜想2成立
②有同学认为,上述实验不足以证明猜想1成立。利用上述反应,从化学平衡移动的角度解释猜想1不足以成立的理由 。
③为进一步验证猜想1,进行实验Ⅱi,完成表中填空。
实验 实验操作 电压E/V 结论
iii 往烧杯A中加入适量 E<0 猜想1成立
结论:可逆氧化还原反应中,浓度的变化引起电对氧化性变化,从而改变电池反应方向。
答案解析部分
1.【答案】B
【解析】【解答】A. 原电池中,电流从正极流向负极,从铜片流向锌片,A不符合题意;
B. Zn作负极,失电子,发生氧化反应,锌电极的反应式:Zn-2e-=Zn2+,B符合题意;
C. 较为活泼的金属作负极,锌作负极,铜作正极,C不符合题意;
D. 盐桥的作用是传递离子,电子不能通过溶液,D不符合题意;
故答案为:B。
【分析】锌铜原电池中Zn作负极,失电子,发生氧化反应,盐桥的作用是传递离子。
2.【答案】B
【解析】【解答】A.①是自发的氧化还原反应可以设计成燃料电池,故A不符合题意;
B.②不是氧化还原反应,不能设计成原电池,故B符合题意;
C.③是吸热反应,不能设计成原电池,故C不符合题意;
D.将铁放入FeCl2溶液中,将FeCl3放入另一个装置中,两个装置之间用盐桥连接,反应物不直接接触,④也可形成原电池,故D不符合题意;
故答案为:B。
【分析】能设计成原电池的反应,则其反应过程中存在电子转移,据此结合所给反应中是否存在元素化合价变化进行分析。
3.【答案】D
【解析】【解答】解:A、两电极材料相同,所以不能形成原电池,故A错误.
B、酒精不是电解质,锌和酒精不能自发的进行氧化还原反应,所以不能形成原电池,故B错误.
C、该装置两电极间不能构成闭合回路,所以不能形成原电池,故C错误.
D、该装置符合原电池的构成条件,所以能形成原电池,故D正确.
故选D.
【分析】根据原电池的构成条件分析,原电池的构成条件是:①有两个活泼性不同的电极,②将电极插入电解质溶液中,③两电极间构成闭合回路,④能自发的进行氧化还原反应.
4.【答案】D
【解析】【解答】A、Cu电极作正极,发生还原反应,A不符合题意;
B、Cu电极作正极,Zn电极作负极,则电流由铜片流向锌片,B不符合题意;
C、电流在外电路中由正极流向负极,则盐桥中K+向正极移动,C不符合题意;
D、Zn电极作负极,电极反应为Zn-2e-=Zn2+,D符合题意;
故答案为:D。
【分析】A、正极失电子,发生还原反应;
B、电流由正极沿导线流向负极;
C、盐桥中阳离子流向正极;
D、负极失电子发生氧化反应。
5.【答案】B
【解析】【解答】A.因该燃料电池是在酸性电解质中工作,所以正极反应为:O2+4e-+4H+=2H2O, 选项A不符合题意;
B.a极是粗铜,b极是纯铜时,为粗铜的精炼,电解时,a极逐渐溶解,b极上有铜析出,符合精炼铜原理,选项B符合题意;
C. b与电池的负极相连,b为电解池的阴极,a极是阳极,阴离子SO42- 移向阳极a极移动,选项C不符合题意;
D.电解CuSO4溶液时,a极产生的气体为O2,产生1molO2需4mol电子,所以需要燃料电池的2molH2,二者的体积并不相等,选项D不符合题意;
故答案为:B。
【分析】通过氧化还原反应而产生电流的装置称为原电池,也可以说是把化学能转变成电能的装置。有的原电池可以构成可逆电池,有的原电池则不属于可逆电池。原电池放电时,负极发生氧化反应,正极发生还原反应。
6.【答案】B
【解析】【解答】解:A.若铬比铁活泼,则负极为铬失电子发生氧化反应,正极为铁,电子经外电路由铬电极流向铁电极,故A错误;
B.若铬比铁活泼,则负极为铬失电子发生氧化反应,正极为铁,氢离子在铁上得电子发生还原反应,反应式为2H++2e﹣=H2↑,故B正确;
C.若铁比铬活泼,则负极为铁失电子发生氧化反应,正极为铬,氢离子向正极铬移动,故C错误;
D.若铁电极附近溶液pH增大,则发生2H++2e﹣=H2↑,所以铁为正极,则铬比铁活泼,故D错误.
故选:B.
【分析】若铬比铁活泼,则负极为铬失电子发生氧化反应,正极为铁,氢离子在铁上得电子发生还原反应,电子经外电路由铬电极流向铁电极;若铁比铬活泼,则负极为铁失电子发生氧化反应,正极为铬,氢离子在铬上得电子发生还原反应,电子经外电路由铁电极流向铬电极.
7.【答案】C
【解析】【解答】A.放电时,Zn是负极、MnO2是正极,根据图示正极反应为:,故A不符合题意;;
B.放电时,Zn是负极,充电时,Zn作阴极,根据图示,阴极反应式为,故B不符合题意;
C.放电过程中,负极区通过离子交换膜a进入硫酸钾溶液, 正极区K+通过离子交换膜b进入硫酸钾溶液,所以a和b分别为阴离子交换膜和阳离子交换膜,故C符合题意;
D.充电过程中,K+通过离子交换膜b进入负极区,通过离子交换膜a 进入正极区,所以溶液的浓度逐渐降低,故D不符合题意;
故答案为:C。
【分析】A.Zn作负极,MnO2作正极,正极发生还原反应,根据图示可写出电极反应式;
B.阴极发生还原反应,根据图示分析可知阴极电极反应式;
C.分析电池工作原理可知a为阴离子交换膜,b为阳离子交换膜;
D.充电时,钾离子和硫酸根离子的移动方向和放电时相反,分析工作原理,判断移动方向。
8.【答案】B
【解析】【解答】A. NO2、Cl2在正极得电子发生还原反应,H2S、CO在负极失电子发生氧化反应,A项不符合题意;
B. Cl2得电子生成HCl,电极反应式为Cl2+2e-=2Cl-,B项符合题意;
C. H2S失去电子生成硫酸,在酸性条件下,氧气得电子应该生成水,其电极反应式为:O2+4H++4e-=2H2O,C项不符合题意;
D. 等体积的Cl2和CO发生原电池反应时,1 mol Cl2得2 mol电子,1 mol CO失去2 mol电子,传感器上电流方向相反,D项不符合题意;
故答案为:B。
【分析】A、二氧化氮、氯气化合价降低为正极
C、酸性条件,电荷守恒配氢离子
D、氯气化合价降低,CO化合价升高,电流方向相反
9.【答案】C
【解析】【解答】A.由分析可知,a为电源的负极,b为电源的正极,故A不符合题意;
B.与电源负极a相连的镍为电解池的阴极,钠离子在阴极上得电子发生还原反应生成钠,钠能与水反应,则电解质溶液不可能为NaBr水溶液,故B不符合题意;
C.由分析可知,制备二茂铁的总反应方程式为Fe+2 +H2↑,故C符合题意;
D.二茂铁制备过程中阴极上钠离子得电子发生还原反应生成钠,电极反应式为 ,Na+移向阴极,故D不符合题意;
故答案为:C。
【分析】根据图示,铁失去电子因此Fe做阳极,Ni做阴极,故a为负极,b为正极,根据反应流程得出有钠单质产生,在阴极生成,因此钠离子向阴极移动,因此电解质溶液不能存在水,根据反应物和生成物即可写出电解池反应式
10.【答案】C
【解析】【解答】A.在锂空气电池中,金属锂失去电子,发生氧化反应,为负极,故A项不符合题意;
B.Li在负极失去电子变成了Li+,会通过有机电解质向水溶液处(正极)移动,故B项不符合题意;
C.正极氧气得到了电子后与氢结合形成氢氧根,电极方程式为O2+4e-+2H2O=4OH-,故C项符合题意;
D.负极的反应式为Li-e-=Li+,正极反应式为O2+4e-+2H2O=4OH-,电池的总反应则为4Li+O2+2H2O=4LiOH,故D项不符合题意。
故答案为:C。
【分析】锂(Li)-空气电池中,锂为负极,发生氧化反应,电极反应为4Li-4e-=4Li+,生成的Li+
向正极移动,通入空气的一极为正极,正极的电极反应为O2+4e-+2H2O=4OH-,把正、负极的电极反应相加可得电池总反应:4Li+O2+2H2O=4LiOH
11.【答案】D
【解析】【解答】A. VB2电极为负极,负极反应式为:2VB2+22OH--22e-=V2O5+2B2O3+11H2O,正极氧气得到电子转化为氢氧根离子,则原电池工作时总反应为:4VB2+11O2=4B2O3+2V2O5,A不符合题意;
B. b电极与电源的正极相连为阳极,发生失去电子的氧化反应,B不符合题意;
C. 电解过程中,c电极为阴极,开始银离子得到电子,然后氢离子得到电子,则表面先有固体物质析出,后有气泡产生,C不符合题意;
D. 当外电路中通过0.04mol电子时,B装置内共收集到0.448 L气体(标准状况),其中阳极产生氧气,物质的量是0.01mol,体积是0.224L,则阴极产生0.01 mol氢气,所以析出单质银的物质的量是0.02mol,所以硝酸银的物质的量是0.02mol,若B装置内的液体体积为100 mL(忽略体积变化),则硝酸银溶液的物质的量浓度为0.2mol L-1,D符合题意;
故答案为:D。
【分析】A中是做的原电池,VB2电极做的是负极,发生的氧化反应,a电极是做正极,氧气发生还原反应,与b连接的是阳极,吸引大量的氢氧根离子和硝酸根离子,氢氧根离子先放电,生成氧气,与c连接的是阴极,吸引大量的氢离子和银离子,银离子先放电,变成银单质。
12.【答案】D
【解析】【解答】A.铜做正极,发生还原反应,电极反应为:Cu2++2e-=Cu,故A不符合题意;
B.锌作负极,发生氧化反应,电极反应为:Zn-2e-=Zn2+;硫酸锌溶液中锌离子浓度增大,盐桥中的氯离子移向硫酸锌溶液;盐桥中的K+移向CuSO4溶液,故B不符合题意;
C.原电池工作时,在外电路中,电子从电池负极经外电路流向正极,电流方向与之相反,故C不符合题意;
D.Cu电极做正极,发生还原反应,故D符合题意;
故答案为:D。
【分析】锌铜构成的原电池,锌作负极,发生氧化反应,电极反应为:Zn-2e-=Zn2+;铜做正极,发生还原反应,电极反应为:Cu2++2e-=Cu,原电池工作时,电子从电池负极经外电路流向正极,由此分析。
13.【答案】B
【解析】【解答】A.由分析可知,a极为Li电极,是电池的负极,故A不符合题意;
B.水能与金属Li直接发生化学反应,不能用水代替有机溶剂,故B符合题意;
C.电子由负极经导线流向正极,a极为电池的负极,b极为电池的正极,则电子从负极a经导线流向正极b,故C不符合题意;
D.MnO2在正极得到电子发生还原反应生成LiMnO2,电极反应式为MnO2+e-+Li+=LiMnO2,故D不符合题意;
故答案为:B。
【分析】新型电池的判断:
1、化合价升高的为负极,失去电子,化合价降低的为正极,得到电子;
2、电极反应式的书写要注意,负极反应为负极材料失去电子化合价升高,正极反应为正极材料得到电子化合价降低,且要根据电解质溶液的酸碱性判断,酸性溶液不能出现氢氧根,碱性溶液不能出现氢离子,且电极反应式要满足原子守恒。
14.【答案】B
【解析】【解答】A.放电时,碳化钼作催化剂、用于降低反应的活化能,A不符合题意;
B.已知碳化钼作Li极催化剂时的放电产物为,反应过程中二氧化碳被还原,则若用作催化剂时,放电的电极反应式为: ,B符合题意;
C. Li能与水反应,则该电池不能选用水溶液作为电解质溶液,C不符合题意;
D.用金作催化剂时电极反应为,若用作催化剂时,放电的电极反应式为: ,则生成等物质的量的和时,转移电子数相同,D不符合题意;
故答案为:B。
【分析】新型电池的判断:
1、化合价升高的为负极,失去电子,化合价降低的为正极,得到电子;
2、电极反应式的书写要注意,负极反应为负极材料失去电子化合价升高,正极反应为正极材料得到电子化合价降低,且要根据电解质溶液的酸碱性判断,酸性溶液不能出现氢氧根,碱性溶液不能出现氢离子,且电极反应式要满足原子守恒。
15.【答案】D
【解析】【解答】解:A.Zn、Cu和稀硫酸构成原电池,锌为负极,铜为正极,电子从负极锌沿导线流向正极铜,故A正确;
B.该原电池中,Cu是正极,Cu电极上氢离子得电子生成氢气被还原,电极反应式为2H++2e﹣=H2↑,故B正确;
C.该装置中化学能转化为电能而产生电流,电流通过LED时,LED发光,则装置中存在“化学能→电能→光能”的转换,故C正确;
D.橙汁溶液呈酸性,Zn、Cu和橙汁能构成原电池,所以将硫酸换成橙汁,导线中仍有电子流动,故D错误;
故选D.
【分析】A.Zn、Cu和稀硫酸构成原电池,锌为负极,铜为正极,电子从负极沿导线流向正极;
B.该原电池中,Cu是正极,Cu电极上氢离子得电子生成氢气;
C.该装置中化学能转化为电能而产生电流,电流通过LED时,LED发光;
D.橙汁溶液呈酸性,Zn、Cu和橙汁能构成原电池.
16.【答案】C
【解析】【解答】A.根据电池的总反应:2Li+ SO2Cl2= 2LiCl+SO2↑。得到单质锂在反应中失电子化合价升高,所以单质锂是该电池的负极,发生失电子的氧化反应,选项A符合题意。
B.锂电极为负极,所以电子从锂电极流出,经导线、负载,到达石墨电极,选项B符合题意。
C.总反应的电子转移数为2e-,所以转移电子是生成的SO2气体的2倍,外电路流过0.2 mol电子,标准状况下生成2.24 L(0.1mol)气体,选项C不符合题意。
D.石墨电极是反应的正极,正极上是SO2Cl2得电子,转化为SO2和Cl-,方程式为:SO2Cl2+2e-=2Cl-+SO2↑,选项D符合题意。
【分析】根据原电池原理分析电极和电极反应,然后书写电极方程式、计算产生的气体体积即可。
17.【答案】铜;Cu-2e-=Cu2+;2Ag++2e-=2Ag;铜;银;0.05NA(或3.01×1022)
【解析】【解答】③正极:
Ag++e-= Ag
0.05 mol 0.05 mol
转移电子数为0.05NA。
【分析】关于原电池的题目,核心在于判断正负极,掌握正向正、负向负的电荷移动原理,结合核心产物与溶液环境,书写电极反应式,根据电极反应式进行计算。
18.【答案】(1)
(2)5;加催化剂;降低温度
(3)25.6
(4)降低;温度升高,平衡正向移动,甲醇转化率升高,但由于温度高于650℃后,催化生成甲醛的催化剂活性降低或副反应生成的氢气浓度增大,导致主反应平衡逆向移动,生成甲醛量减少
(5);0.003
【解析】【解答】(1)氢气燃烧热反应方程式的2倍减去甲醛燃烧热反应方程式,再减去③得到与制备甲醛的反应: ;故答案为:。
(2)根据题意曲线X对应温度下平衡时,消耗二氧化碳物质的量为0.1mol,消耗氢气物质的量为0.2mol,生成甲醛、水蒸气物质的量为0.1mol,剩余二氧化碳物质的量为0.1mol,剩余氢气物质的量为0.2mol,则该温度下平衡常数,分析曲线Y和曲线X,平衡时各物质的量相等,但达到平衡时时间不相同,说明由曲线Y到曲线X采取的措施可能是加入催化剂;曲线Z与曲线X分析,曲线Z所需时间比曲线X时间短,但二氧化碳转化率比X低,由曲线Z到曲线X是平衡正向移动,反应速率减慢了,因此采取的措施可能是降低温度;故答案为:5;加催化剂;降低温度。
(3)根据平衡常数得到,在m点时消耗二氧化碳物质的量为0.04mol,消耗氢气物质的量为0.08mol,生成甲醛、水蒸气物质的量为0.04mol,剩余二氧化碳物质的量为0.16mol,剩余氢气物质的量为0.32mol,则m点;故答案为:25.6。
(4)根据图中信息得到,温度高于650℃,甲醇的转化率升高,甲醛的产率降低,根据两个方程式分析,两个方程式都为吸热反应,升高温度,平衡正向移动,甲醇转化率升高,由于副反应生成氢气,氢气量增大,对主反应来说,氢气浓度增大,导致主反应逆向移动,生成甲醛的量减少,也可能是甲醛催化剂的催化活性降低即温度升高,平衡正向移动,甲醇转化率升高,但由于温度高于650℃后,催化生成甲醛的催化剂活性降低或副反应生成的氢气浓度增大,导致主反应平衡逆向移动,生成甲醛量减少;故答案为:降低;温度升高,平衡正向移动,甲醇转化率升高,但由于温度高于650℃后,催化生成甲醛的催化剂活性降低或副反应生成的氢气浓度增大,导致主反应平衡逆向移动,生成甲醛量减少。
(5)根据题意甲醛变为二氧化碳,甲醛中碳化合价升高,失去电子,作负极,因此a电极反应式为。国家标准是室内甲醛不能超过,传感器在室内空间测定,电路中有电子通过,则含有甲醛物质的量为,该室内甲醛含量为;故答案为:;0.003。
【分析】(1)首先写出甲醛、氢气的燃烧热,利用盖斯定律,即可得到二氧化碳与氢气反应的热化学反应方程式。
(2)根据二氧化碳转化率,列出三段式,求出各物质平衡浓度,带入平衡常数表达式即可。
(3)根据达到平衡时V正=V逆,结合平衡常数表达式可以得到,K正/K逆=K=5,根据m点转化率,求出各物质浓度,带入表达式即可得到其比值。
(4)平衡图像解题技巧:对应化学反应速率图像和化学平衡图像,应该注意下列几点:1、横轴坐标和纵坐标含有;2、曲线斜率或者趋势;3、曲线上特殊点,如起点、终点、交点和拐点等;4、根据需要运用辅助线,如等温线、等压线等
19.【答案】(1)PbO2+2e-+4H++2SO42-=PbSO4+2H2O;小;48
(2)C;Zn+Ag2O=2Ag+ZnO;减小;增大;不变
【解析】【解答】(1)关键电池总反应式为Pb+PbO2+4H++2SO42- 2PbSO4+2H2O可判断负极是铅失去电子发生氧化反应,负极电极反应为Pb-2e-+SO42-=PbSO4;正极是二氧化铅得到电子,发生还原反应,正极电极反应式为PbO2+2e-+4H++2SO42-=PbSO4+2H2O,因此放电时电解液中硫酸的浓度将减少;当外电路通过1mol电子时,依据电子守恒计算理论上负极板的质量增加0.5mol×303g/mol-0.5mol×207g/mol=48g;
(2)①A、负极电极反应式为Zn+2OH--2e-=ZnO+H2O、正极电极反应式为 Ag2O+H2O+2e-=2Ag+2OH-,所以电池反应式为Zn+Ag2O=2Ag+ZnO,因此氢氧化钾的量不变,A错误;
B、由电极反应式可知,Zn的化合价由0价升高到+2价,被氧化,为原电池的负极,则正极为Ag2O,原电池中电子从负极流向正极,即从锌经导线流向Ag2O,B错误;
C、正极电极反应为:Ag2O+H2O+2e-=2Ag+2OH-,负极电极反应:Zn+2OH--2e-=ZnO+H2O,所以Zn是负极,Ag2O是正极,C正确;
D、由电极反应式可知,Zn的化合价由0价升高到+2价,为原电池的负极,发生氧化反应,Ag2O是正极发生还原反应,D错误;
故答案为:C。
②负极电极反应式为Zn+2OH--2e-=ZnO+H2O、正极电极反应式为 Ag2O+H2O+2e-=2Ag+2OH-,所以电池反应式为Zn+Ag2O=2Ag+ZnO;
③该原电池中,Zn元素化合价由0价变为+2价、Ag元素化合价由+1价变为0价,所以Zn是负极失电子发生氧化反应,Ag2O是正极得电子发生还原反应;负极的电极反应式为:Zn+2OH--2e-=ZnO+H2O,则负极附近pH减小;正极电极反应式为 Ag2O+H2O+2e-=2Ag+2OH-,所以正极溶液的pH增大,电子转移相等的情况下负极消耗的氢氧根与正极产生的氢氧根离子的物质的量相等,所以溶液的pH值不变。
【分析】(1)铅蓄电池放电时相当于原电池,正极发生氧化反应,放电时消耗硫酸,所以硫酸浓度减小,根据电荷守恒计算负极板得质量增加两;
(2)①纽扣电池的负极发生氧化反应,正极发生还原反应;
②两电极之和即为原电池的总反应方程式;
③根据电极方程式和总反应方程式进行分析溶液的pH变化。
20.【答案】(1)丁烷
(2)2C4H10+13O2=8CO2+10H2O
(3)2Cl﹣+2H2O Cl2↑+H2↑+2OH﹣
(4)1.456L;0.13mol;1.3mol/L
【解析】【解答】解:(1)燃料电池中发生氧化反应的物质为负极燃料,所以该燃料电池中发生氧化反应的物质是丁烷,故答案为:丁烷;(2)该电池中,丁烷和氧气反应生成二氧化碳和水,反应方程式为:2C4H10+13O2=8CO2+10H2O,
故答案为:2C4H10+13O2=8CO2+10H2O;(3)电解饱和食盐水时,阳极上氯离子放电生成氯气,阴极上氢离子放电生成氢气,同时还生成氢氧化钠,离子方程式为:2Cl﹣+2H2O Cl2↑+H2↑+2OH﹣,故答案为:2Cl﹣+2H2O Cl2↑+H2↑+2OH﹣;(4)电路中通过0.26NA的电子时,因为串联电池中转移电子数相等,所以消耗的氧气的体积(标况)为 ×22.4=1.456L,电解饱和食盐水生成的氯气的物质的量是 =0.13mol,生成氢氧化钠的物质的量为0.26mol,所以NaOH的物质的量浓度为
=1.3mol/L,故答案为:1.456;0.13mol;1.3mol/L.
【分析】(1)燃料电池中发生氧化反应的物质为负极燃料;(2)丁烷和氧气反应生成二氧化碳和水;(3)电解饱和食盐水时,阳极上氯离子放电,阴极上氢离子放电;(4)电路中通过0.26NA的电子时,根据串联电池中转移电子数相等计算.
21.【答案】(1)
(2)
(3)>>
(4)
(5)<;AgNO3固体;加入铁粉后,同时造成增大,减小,都能使平衡逆移,使E<0;FeCl2固体
【解析】【解答】(1)结合分析可知,反应i中铁离子把双氧水氧化了,生成亚铁离子、氧气和水,离子方程式为;
(2)遇二价铁发生反应:,生成深蓝色沉淀,则反应过程中,加入溶液,产生蓝色沉淀,证明有二价铁生成;
(3)据分析,上述条件下过氧化氢、二氧化锰、氧的氧化性由强到弱的顺序:过氧化氢>二氧化锰>氧气。
(4)电池初始工作时,由可知,铁离子得电子发生还原反应转变为亚铁离子,为正极,则正极的电极反应式为。
【分析】要通过反应探究对电化学反应方向的影响,从某还原型物质浓度、氧化性变化的角度分析图b,对于2个猜想,只能通过改变一个变量观察是否使E<0来探究——猜想1:二价铁浓度增大,三价铁的氧化性减弱,正极的电极电势降低,故只能通过A烧杯加适量氯化亚铁固体,增加亚铁离子浓度,猜想2:碘离子浓度减小,碘的氧化性增强,负极的电极电势升高,只能通过B烧杯加适量硝酸银固体减少碘离子浓度来实现。
同课章节目录
- 第1章 化学反应与能量转化
- 第1节 化学反应的热效应
- 第2节 化学能转化为电能——电池
- 第3节 电能转化为化学能——电解
- 第4节 金属的腐蚀与防护
- 微项目 设计载人航天器用化学电池与氧气再生方案——化学反应中能量及物质的转化利用
- 第2章 化学反应的方向、 限度与速率
- 第1节 化学反应的方向
- 第2节 化学反应的限度
- 第3节 化学反应的速率
- 第4节 化学反应条件的优化——工业合成氨
- 微项目 探讨如何利用工业废气中的二氧化碳合成甲醇——化学反应选择与反应条件优化
- 第3章 物质在水溶液中的行为
- 第1节 水与水溶液
- 第2节 弱电解质的电离 盐类的水解
- 第3节 沉淀溶解平衡
- 第4节 离子反应
- 微项目 揭秘索尔维制碱法和侯氏制碱法——化学平衡思想的创造性应用
