2.8《化学与可持续发展》章节基础测(含答案)2023~2024学年高中化学人教版(2019)必修2
文档属性
| 名称 | 2.8《化学与可持续发展》章节基础测(含答案)2023~2024学年高中化学人教版(2019)必修2 |  | |
| 格式 | doc | ||
| 文件大小 | 352.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-12-15 08:31:35 | ||
图片预览




文档简介
2.8《化学与可持续发展》章节基础测
(满分:100分;时间:90分钟)
一、选择题(本题共10小题,每小题2分,共20分,每题只有一个选项符合题意)
1.下列关于物质制备原理错误的是( )
A.工业制备金属钠:2NaCl(熔融) 2Na+Cl2↑
B.工业生产铁:Fe2O3+3CO 2Fe+3CO2
C.湿法炼铜:Fe+CuSO4 Cu+FeSO4
D.以S为原料,工业生产硫酸在沸腾炉中的反应:2S+3O2 2SO3
2.正确使用化肥和农药可以促进农业生产,下列说法正确的是( )
A.长期使用DDT不会导致残留污染
B.使用可溶性磷肥有利于植物对磷的吸收
C.(NH4)2SO4和草木灰混合使用肥效更佳
D.有机磷杀虫剂可降解,可以大量使用
3.水资源是发展国民经济不可缺少的重要自然资源。下列关于水的说法错误的是( )
A.蒸馏法是海水淡化的方法之一
B.淡水的密度小于海水的密度
C.融化的雪水中矿物质含量比深井水中的少
D.0 ℃以上,温度越高,水的密度越小
4.食品中可以按规定加入一定量的食品添加剂、干燥剂或除氧剂,下列说法正确的是( )
A.补血营养品红桃K中添加微量铁粉,作为补铁剂
B.中秋月饼包装袋内有小袋铁粉,作为干燥剂
C.苏打饼干包装盒中有小袋生石灰,作为补钙剂
D.卤制品中加入大量亚硝酸钠,作为保鲜剂
5.如图所示是石油分馏塔的示意图,a、b、c三种馏分中( )
A.a的沸点最高
B.b的沸点最低
C.c的平均相对分子质量最大
D.每一种馏分都是纯净物
6.合理开发和利用海水资源是世界各国研究的课题。下列对于海水利用的认识错误的是( )
A.海水中蕴藏有丰富的资源,人类可以无限制地开发,以弥补资源的短缺
B.淡化海水的方法主要有蒸馏法、电渗析法、离子交换法
C.可以用太阳能电池电解海水以获取氢能源
D.以海水中获取的NaCl为原料可以生产烧碱、纯碱、金属钠、氯气、盐酸等化工产品
7.海水提溴过程中将Br-氧化成Br2,可向其中加入氧化剂,合适的是( )
A.酸性KMnO4溶液 B.氯气
C.FeCl3溶液 D.碘水
8.人体胃酸的主要成分是盐酸。胃酸可助消化食物,但胃酸过多会损伤胃黏膜,使人感觉不适。抗酸药(又称抑酸剂)可以减少胃里过多的胃酸。下列物质不属于抗酸药的是( )
A.阿司匹林(主要成分:乙酰水杨酸)
B.胃舒平[主要成分:Al(OH)3]
C.碳酸氢钠片(主要成分:NaHCO3)
D.胃得乐(主要成分:MgCO3)
9.下列关于食品添加剂的说法不正确的是( )
A.食品添加剂必须按卫生部门的规定使用
B.食品添加剂必须用天然植物制造
C.柠檬黄常用来作着色剂,改善食品色泽
D.醋可用作调味品
10.“绿水青山就是金山银山”。下列做法不利于保护环境的是( )
A.推广使用电动汽车等低碳交通工具
B.推广垃圾分类,电子设备以旧换新
C.用生物方法脱除生活污水中的氮和磷
D.加大铅酸蓄电池、含汞锌锰电池的生产
二、选择题(本题包括5小题,每小题4分,共20分。每小题有一个或两个选项符合题意,全部选对得4分,选对但不全的得1分,有选错的得0分)
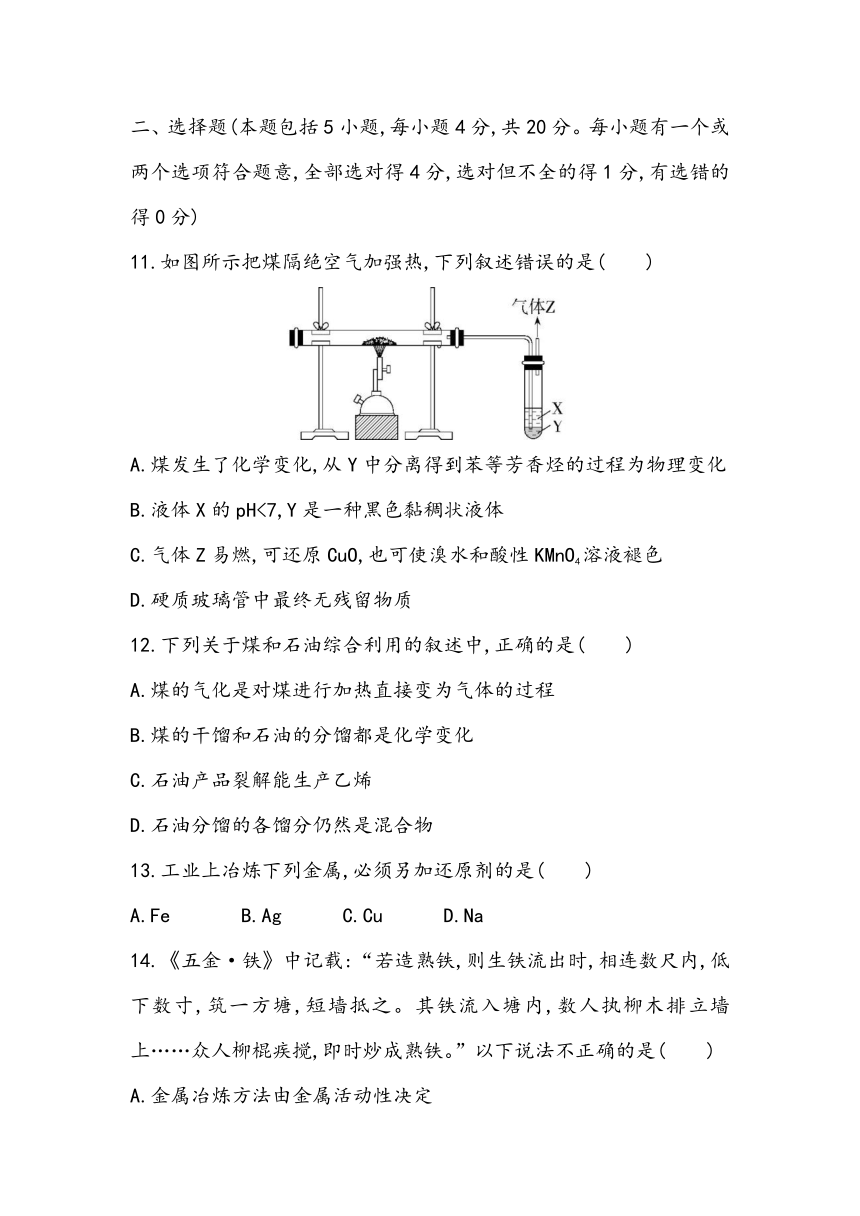
11.如图所示把煤隔绝空气加强热,下列叙述错误的是( )
A.煤发生了化学变化,从Y中分离得到苯等芳香烃的过程为物理变化
B.液体X的pH<7,Y是一种黑色黏稠状液体
C.气体Z易燃,可还原CuO,也可使溴水和酸性KMnO4溶液褪色
D.硬质玻璃管中最终无残留物质
12.下列关于煤和石油综合利用的叙述中,正确的是( )
A.煤的气化是对煤进行加热直接变为气体的过程
B.煤的干馏和石油的分馏都是化学变化
C.石油产品裂解能生产乙烯
D.石油分馏的各馏分仍然是混合物
13.工业上冶炼下列金属,必须另加还原剂的是( )
A.Fe B.Ag C.Cu D.Na
14.《五金·铁》中记载:“若造熟铁,则生铁流出时,相连数尺内,低下数寸,筑一方塘,短墙抵之。其铁流入塘内,数人执柳木排立墙上……众人柳棍疾搅,即时炒成熟铁。”以下说法不正确的是( )
A.金属冶炼方法由金属活动性决定
B.生铁比熟铁质地更硬,延展性也更好
C.炒铁是为了提高铁水中的碳含量
D.该法与近代往生铁水中吹空气炼钢异曲同工
15.BHT是一种常用的食品抗氧化剂,从出发合成BHT的方法有如下两种。下列说法错误的是( )
A.方法一的反应类型是加成反应
B.方法二中除生成BHT外,还生成水
C.BHT与互为同系物
D.从原子经济角度分析方法二优于方法一
三、非选择题(本题共5小题,共60分)
16.(14分)为研究海水提溴工艺,甲、乙两同学分别设计了如下实验流程:
甲:苦卤含溴海水含溴空气溴水混合物溴蒸气液溴
乙:苦卤含溴海水溴蒸气液溴
(1)甲、乙两同学在第一阶段得到的含溴海水中,氯气的利用率较高的是 (填“甲”或“乙”),原因是 。
(2)甲同学步骤④所发生反应的离子方程式为 。
(3)某同学在进行蒸馏操作时,采用如图所示装置:
①写出图中两处明显的错误: 。
②实验时A中除加入混合溶液外,还需加入少量 ,其作用是 。
(4)对比甲、乙两流程,最大的区别在于对含溴海水的处理方法不同,其中符合工业生产要求的是 (填“甲”或“乙”),理由是 。
17.(14分)来自石油的有机化工原料A,可以发生如下转化:
已知:E是具有果香味的有机物,F是一种高分子化合物。请回答下列问题:
(1)A的分子式是 ,C的名称是 。
(2)D分子中的官能团名称是 。
(3)反应③的化学方程式是 ,该反应属于 反应。反应④的化学方程式是 ,该反应属于 反应。
18.(14分)二氧化硫是一种危害严重的大气污染物,烟气脱硫是控制二氧化硫污染的主要技术手段。
利用海水脱硫是一种有效的方法,其工艺流程如图所示:
某研究小组为探究提高含硫烟气中SO2的吸收效率的措施,进行了天然海水吸收含硫烟气的模拟实验,实验结果如图所示。
(1)根据图示实验结果,为了提高一定浓度含硫烟气中SO2的吸收效率,下列措施正确的是 (填字母)。
A.降低通入含硫烟气的温度
B.减小通入含硫烟气的流速
C.减少天然海水的进入量
D.在天然海水中加入生石灰
(2)天然海水吸收了含硫烟气后会溶有H2SO3,利用空气中的氧气将其氧化,写出该反应的离子方程式: 。
(3)该小组采用如图装置在实验室测定烟气中SO2的体积分数(假设烟气中其余组分不能与水反应且不溶于水,实验在标准状况下进行):
上述装置连接的正确顺序是:原料气→ → → →
→ 。(填接口字母)
19.(12分)汽车的发明与使用,是人类智慧的杰出体现,它为人们的生活和生产带来了极大的方便,同时由此引发的环境污染问题也越来越引起人们的关注。
(1)汽车排放的尾气中因含有氮的氧化物而污染大气,产生氮的氧化物的主要原因是 (填字母,下同)。
A.燃烧含氮燃料 B.燃烧含铅汽油
C.汽油燃烧不充分 D.汽缸中的N2被氧化
(2)下列有关城市各项污染源与其造成的恶果对应关系正确的是 。
A.汽车尾气——光化学烟雾;工业废气——酸雨;工业废水——“公害病”
B.汽车尾气——酸雨;工业废气——“公害病”;工业废水——光化学烟雾
C.汽车尾气——“公害病”;工业废气——酸雨;工业废水——光化学烟雾
D.汽车尾气——光化学烟雾;工业废气——“公害病”;工业废水——酸雨
(3)一氧化氮和一氧化碳都是汽车尾气里的有害物质,它们能缓慢地发生如下反应:2NO(g)+2CO(g) N2(g)+2CO2(g)(放热反应)。现利用此反应,拟设计一种环保装置以消除汽车尾气对大气的污染。下列设计方案可以提高尾气处理效果的是 。
①选用适当的催化剂 ②提高装置的温度
③降低装置的压强 ④在装置中装入碱石灰
A.①③ B.②④ C.①④ D.②③
(4)新型环保出租车采用LPG+汽油的双燃料系统,其尾气中的有毒成分较普通车型下降80%左右,缓解了汽车尾气排放给城市环境造成的污染问题。下列不属于上述有毒成分的是 。
A.CO2和H2 B.NO2和NO
C.CO和SO2 D.C粒和含铅化合物
(5)所谓“绿色汽车”是指使用液化石油气等无污染或污染较小的能源作燃料的汽车。绿色汽车可避免有毒的铅、苯和苯的同系物以及稠环芳烃的排放。燃烧等质量的液化石油气(主要成分是含3~4个碳原子的烃)与汽油相比较 。
A.前者生成的水少
B.前者消耗氧气量少
C.前者燃烧产生的污染物多
D.前者产生的含碳化合物种类少
(6)为了减少大气污染,许多城市推广汽车使用清洁燃料。目前使用的清洁燃料主要有两类:一类是压缩天然气,另一类是液化石油气。这两类燃料的主要成分都是 。
A.碳水化合物 B.碳氢化合物
C.氢气 D.醇类
20.(6分)营养平衡、科学使用食品添加剂有助于保持人体健康和提高免疫力。
(1)向食品中加入调味剂,能改善或改变食品的口味,下列不属于调味剂的是 (填字母)。
a.食盐 b.辣椒粉 c.小苏打
(2)人体如果缺乏某种微量元素将导致血液输送氧气的能力下降,人体内就无法获得充足的氧气,生理机能就会下降,该微量元素是 (填字母)。
a.碘 b.锌 c.铁
(3)抗生素是能抑制某些微生物生长或能杀灭某些微生物的一类物质,下列属于抗生素的是 (填字母)。
a.阿莫西林 b.胃舒平 c.阿司匹林
参考答案:
1-5DBDAC
6-10ABABD
11.BD
12.CD
13.AC
14.BC
15.D
16.
(1)甲 酸化后可抑制Cl2、Br2与H2O反应,减少Cl2的消耗,提高Cl2的利用率
(2)SO2+Br2+2H2O 4H++S+2Br-
(3)①温度计水银球插入了液体中,冷却水上进下出 ②碎瓷片 防止暴沸
(4)甲 含溴海水中溴的浓度低,直接蒸馏成本高,甲流程中③④⑤步实际上是溴的富集过程,可提高溴的浓度,减少能源消耗,降低成本
17.
(1)C2H4 乙醛
(2)羧基
(3)CH3CH2OH+CH3COOH CH3COOCH2CH3+H2O 取代(或酯化) nCH2CH2 CH2—CH2 加聚
18.
(1)ABD
(2)2H2SO3+O2 4H++2S
(3)c d b a e
19.
(1)D (2)A (3)C (4)A (5)D (6)B
20.
(1)c (2)c (3)a
(满分:100分;时间:90分钟)
一、选择题(本题共10小题,每小题2分,共20分,每题只有一个选项符合题意)
1.下列关于物质制备原理错误的是( )
A.工业制备金属钠:2NaCl(熔融) 2Na+Cl2↑
B.工业生产铁:Fe2O3+3CO 2Fe+3CO2
C.湿法炼铜:Fe+CuSO4 Cu+FeSO4
D.以S为原料,工业生产硫酸在沸腾炉中的反应:2S+3O2 2SO3
2.正确使用化肥和农药可以促进农业生产,下列说法正确的是( )
A.长期使用DDT不会导致残留污染
B.使用可溶性磷肥有利于植物对磷的吸收
C.(NH4)2SO4和草木灰混合使用肥效更佳
D.有机磷杀虫剂可降解,可以大量使用
3.水资源是发展国民经济不可缺少的重要自然资源。下列关于水的说法错误的是( )
A.蒸馏法是海水淡化的方法之一
B.淡水的密度小于海水的密度
C.融化的雪水中矿物质含量比深井水中的少
D.0 ℃以上,温度越高,水的密度越小
4.食品中可以按规定加入一定量的食品添加剂、干燥剂或除氧剂,下列说法正确的是( )
A.补血营养品红桃K中添加微量铁粉,作为补铁剂
B.中秋月饼包装袋内有小袋铁粉,作为干燥剂
C.苏打饼干包装盒中有小袋生石灰,作为补钙剂
D.卤制品中加入大量亚硝酸钠,作为保鲜剂
5.如图所示是石油分馏塔的示意图,a、b、c三种馏分中( )
A.a的沸点最高
B.b的沸点最低
C.c的平均相对分子质量最大
D.每一种馏分都是纯净物
6.合理开发和利用海水资源是世界各国研究的课题。下列对于海水利用的认识错误的是( )
A.海水中蕴藏有丰富的资源,人类可以无限制地开发,以弥补资源的短缺
B.淡化海水的方法主要有蒸馏法、电渗析法、离子交换法
C.可以用太阳能电池电解海水以获取氢能源
D.以海水中获取的NaCl为原料可以生产烧碱、纯碱、金属钠、氯气、盐酸等化工产品
7.海水提溴过程中将Br-氧化成Br2,可向其中加入氧化剂,合适的是( )
A.酸性KMnO4溶液 B.氯气
C.FeCl3溶液 D.碘水
8.人体胃酸的主要成分是盐酸。胃酸可助消化食物,但胃酸过多会损伤胃黏膜,使人感觉不适。抗酸药(又称抑酸剂)可以减少胃里过多的胃酸。下列物质不属于抗酸药的是( )
A.阿司匹林(主要成分:乙酰水杨酸)
B.胃舒平[主要成分:Al(OH)3]
C.碳酸氢钠片(主要成分:NaHCO3)
D.胃得乐(主要成分:MgCO3)
9.下列关于食品添加剂的说法不正确的是( )
A.食品添加剂必须按卫生部门的规定使用
B.食品添加剂必须用天然植物制造
C.柠檬黄常用来作着色剂,改善食品色泽
D.醋可用作调味品
10.“绿水青山就是金山银山”。下列做法不利于保护环境的是( )
A.推广使用电动汽车等低碳交通工具
B.推广垃圾分类,电子设备以旧换新
C.用生物方法脱除生活污水中的氮和磷
D.加大铅酸蓄电池、含汞锌锰电池的生产
二、选择题(本题包括5小题,每小题4分,共20分。每小题有一个或两个选项符合题意,全部选对得4分,选对但不全的得1分,有选错的得0分)
11.如图所示把煤隔绝空气加强热,下列叙述错误的是( )
A.煤发生了化学变化,从Y中分离得到苯等芳香烃的过程为物理变化
B.液体X的pH<7,Y是一种黑色黏稠状液体
C.气体Z易燃,可还原CuO,也可使溴水和酸性KMnO4溶液褪色
D.硬质玻璃管中最终无残留物质
12.下列关于煤和石油综合利用的叙述中,正确的是( )
A.煤的气化是对煤进行加热直接变为气体的过程
B.煤的干馏和石油的分馏都是化学变化
C.石油产品裂解能生产乙烯
D.石油分馏的各馏分仍然是混合物
13.工业上冶炼下列金属,必须另加还原剂的是( )
A.Fe B.Ag C.Cu D.Na
14.《五金·铁》中记载:“若造熟铁,则生铁流出时,相连数尺内,低下数寸,筑一方塘,短墙抵之。其铁流入塘内,数人执柳木排立墙上……众人柳棍疾搅,即时炒成熟铁。”以下说法不正确的是( )
A.金属冶炼方法由金属活动性决定
B.生铁比熟铁质地更硬,延展性也更好
C.炒铁是为了提高铁水中的碳含量
D.该法与近代往生铁水中吹空气炼钢异曲同工
15.BHT是一种常用的食品抗氧化剂,从出发合成BHT的方法有如下两种。下列说法错误的是( )
A.方法一的反应类型是加成反应
B.方法二中除生成BHT外,还生成水
C.BHT与互为同系物
D.从原子经济角度分析方法二优于方法一
三、非选择题(本题共5小题,共60分)
16.(14分)为研究海水提溴工艺,甲、乙两同学分别设计了如下实验流程:
甲:苦卤含溴海水含溴空气溴水混合物溴蒸气液溴
乙:苦卤含溴海水溴蒸气液溴
(1)甲、乙两同学在第一阶段得到的含溴海水中,氯气的利用率较高的是 (填“甲”或“乙”),原因是 。
(2)甲同学步骤④所发生反应的离子方程式为 。
(3)某同学在进行蒸馏操作时,采用如图所示装置:
①写出图中两处明显的错误: 。
②实验时A中除加入混合溶液外,还需加入少量 ,其作用是 。
(4)对比甲、乙两流程,最大的区别在于对含溴海水的处理方法不同,其中符合工业生产要求的是 (填“甲”或“乙”),理由是 。
17.(14分)来自石油的有机化工原料A,可以发生如下转化:
已知:E是具有果香味的有机物,F是一种高分子化合物。请回答下列问题:
(1)A的分子式是 ,C的名称是 。
(2)D分子中的官能团名称是 。
(3)反应③的化学方程式是 ,该反应属于 反应。反应④的化学方程式是 ,该反应属于 反应。
18.(14分)二氧化硫是一种危害严重的大气污染物,烟气脱硫是控制二氧化硫污染的主要技术手段。
利用海水脱硫是一种有效的方法,其工艺流程如图所示:
某研究小组为探究提高含硫烟气中SO2的吸收效率的措施,进行了天然海水吸收含硫烟气的模拟实验,实验结果如图所示。
(1)根据图示实验结果,为了提高一定浓度含硫烟气中SO2的吸收效率,下列措施正确的是 (填字母)。
A.降低通入含硫烟气的温度
B.减小通入含硫烟气的流速
C.减少天然海水的进入量
D.在天然海水中加入生石灰
(2)天然海水吸收了含硫烟气后会溶有H2SO3,利用空气中的氧气将其氧化,写出该反应的离子方程式: 。
(3)该小组采用如图装置在实验室测定烟气中SO2的体积分数(假设烟气中其余组分不能与水反应且不溶于水,实验在标准状况下进行):
上述装置连接的正确顺序是:原料气→ → → →
→ 。(填接口字母)
19.(12分)汽车的发明与使用,是人类智慧的杰出体现,它为人们的生活和生产带来了极大的方便,同时由此引发的环境污染问题也越来越引起人们的关注。
(1)汽车排放的尾气中因含有氮的氧化物而污染大气,产生氮的氧化物的主要原因是 (填字母,下同)。
A.燃烧含氮燃料 B.燃烧含铅汽油
C.汽油燃烧不充分 D.汽缸中的N2被氧化
(2)下列有关城市各项污染源与其造成的恶果对应关系正确的是 。
A.汽车尾气——光化学烟雾;工业废气——酸雨;工业废水——“公害病”
B.汽车尾气——酸雨;工业废气——“公害病”;工业废水——光化学烟雾
C.汽车尾气——“公害病”;工业废气——酸雨;工业废水——光化学烟雾
D.汽车尾气——光化学烟雾;工业废气——“公害病”;工业废水——酸雨
(3)一氧化氮和一氧化碳都是汽车尾气里的有害物质,它们能缓慢地发生如下反应:2NO(g)+2CO(g) N2(g)+2CO2(g)(放热反应)。现利用此反应,拟设计一种环保装置以消除汽车尾气对大气的污染。下列设计方案可以提高尾气处理效果的是 。
①选用适当的催化剂 ②提高装置的温度
③降低装置的压强 ④在装置中装入碱石灰
A.①③ B.②④ C.①④ D.②③
(4)新型环保出租车采用LPG+汽油的双燃料系统,其尾气中的有毒成分较普通车型下降80%左右,缓解了汽车尾气排放给城市环境造成的污染问题。下列不属于上述有毒成分的是 。
A.CO2和H2 B.NO2和NO
C.CO和SO2 D.C粒和含铅化合物
(5)所谓“绿色汽车”是指使用液化石油气等无污染或污染较小的能源作燃料的汽车。绿色汽车可避免有毒的铅、苯和苯的同系物以及稠环芳烃的排放。燃烧等质量的液化石油气(主要成分是含3~4个碳原子的烃)与汽油相比较 。
A.前者生成的水少
B.前者消耗氧气量少
C.前者燃烧产生的污染物多
D.前者产生的含碳化合物种类少
(6)为了减少大气污染,许多城市推广汽车使用清洁燃料。目前使用的清洁燃料主要有两类:一类是压缩天然气,另一类是液化石油气。这两类燃料的主要成分都是 。
A.碳水化合物 B.碳氢化合物
C.氢气 D.醇类
20.(6分)营养平衡、科学使用食品添加剂有助于保持人体健康和提高免疫力。
(1)向食品中加入调味剂,能改善或改变食品的口味,下列不属于调味剂的是 (填字母)。
a.食盐 b.辣椒粉 c.小苏打
(2)人体如果缺乏某种微量元素将导致血液输送氧气的能力下降,人体内就无法获得充足的氧气,生理机能就会下降,该微量元素是 (填字母)。
a.碘 b.锌 c.铁
(3)抗生素是能抑制某些微生物生长或能杀灭某些微生物的一类物质,下列属于抗生素的是 (填字母)。
a.阿莫西林 b.胃舒平 c.阿司匹林
参考答案:
1-5DBDAC
6-10ABABD
11.BD
12.CD
13.AC
14.BC
15.D
16.
(1)甲 酸化后可抑制Cl2、Br2与H2O反应,减少Cl2的消耗,提高Cl2的利用率
(2)SO2+Br2+2H2O 4H++S+2Br-
(3)①温度计水银球插入了液体中,冷却水上进下出 ②碎瓷片 防止暴沸
(4)甲 含溴海水中溴的浓度低,直接蒸馏成本高,甲流程中③④⑤步实际上是溴的富集过程,可提高溴的浓度,减少能源消耗,降低成本
17.
(1)C2H4 乙醛
(2)羧基
(3)CH3CH2OH+CH3COOH CH3COOCH2CH3+H2O 取代(或酯化) nCH2CH2 CH2—CH2 加聚
18.
(1)ABD
(2)2H2SO3+O2 4H++2S
(3)c d b a e
19.
(1)D (2)A (3)C (4)A (5)D (6)B
20.
(1)c (2)c (3)a
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
