福建省厦门第一名校2023-2024学年高三上学期期中考试化学试题(PDF版无答案)
文档属性
| 名称 | 福建省厦门第一名校2023-2024学年高三上学期期中考试化学试题(PDF版无答案) |

|
|
| 格式 | |||
| 文件大小 | 2.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-12-15 00:00:00 | ||
图片预览


文档简介
厦 中 2024届 三年化学科期中考试卷
说明:1.本试卷满分 100分,考试时间 75分钟。
2.可能 到的相对原 质量:H-1 C-12 O-16 V-51
、选择题(本题共 10 题,每 题 4分,共 40分,每 题只有 个选项符合题意)
1.材料的应 是社会进步的阶梯。下列有关材料的解读不正确的是( )
选项 材料 解读
A 玻璃浸泡 材或纺织品防 溶液阻燃、耐 温
B 成功合成 熵合 FeCoNiMnPtIr,作为锂氧电池的催化剂 该合 易被酸腐蚀
C 外接电流的阴极保护法 于钢铁管道防腐 阳极材料组成元素的 属性强于铁
制备纳 纤维脱硫材料 ,将捕获的 催化转化为 该材料中元素均位于周期表前四周
D
期
硫酸
2.下列有关物质的性质与 途具有对应关系的是( )
A. 极易溶于 ,可 于 业制冷剂
B. 炭具有还原性,可 于冰箱和居室除臭剂
C. 是两性氧化物,可 于制造 温材料
D. 、 合 熔点低且导热,可 于快中 反应堆的导热剂
3. 炔 化法、 烯氧化法是 业上制备 醛的两个重要 法,反应原理分别为:
, 。以下叙述不正确的是
A. 的电 式为
B. 的中 原 含有 孤电 对
C. 烯氧化法中, 成 醛时,转移的电 数约为
D.标准状况下, 中含有 键的数 约为
4.能正确表示下列反应的离 程式或电极反应式的是( )
A.少量 通 溶液中:
B.电解液为 溶液的 燃料电池的负极反应式:
C.向四羟基合铝酸钠溶液中加 苏打溶液:
D. 醋和 84消毒液混合:
学 科 ( 北 京 ) 股 份 有 限 公 司
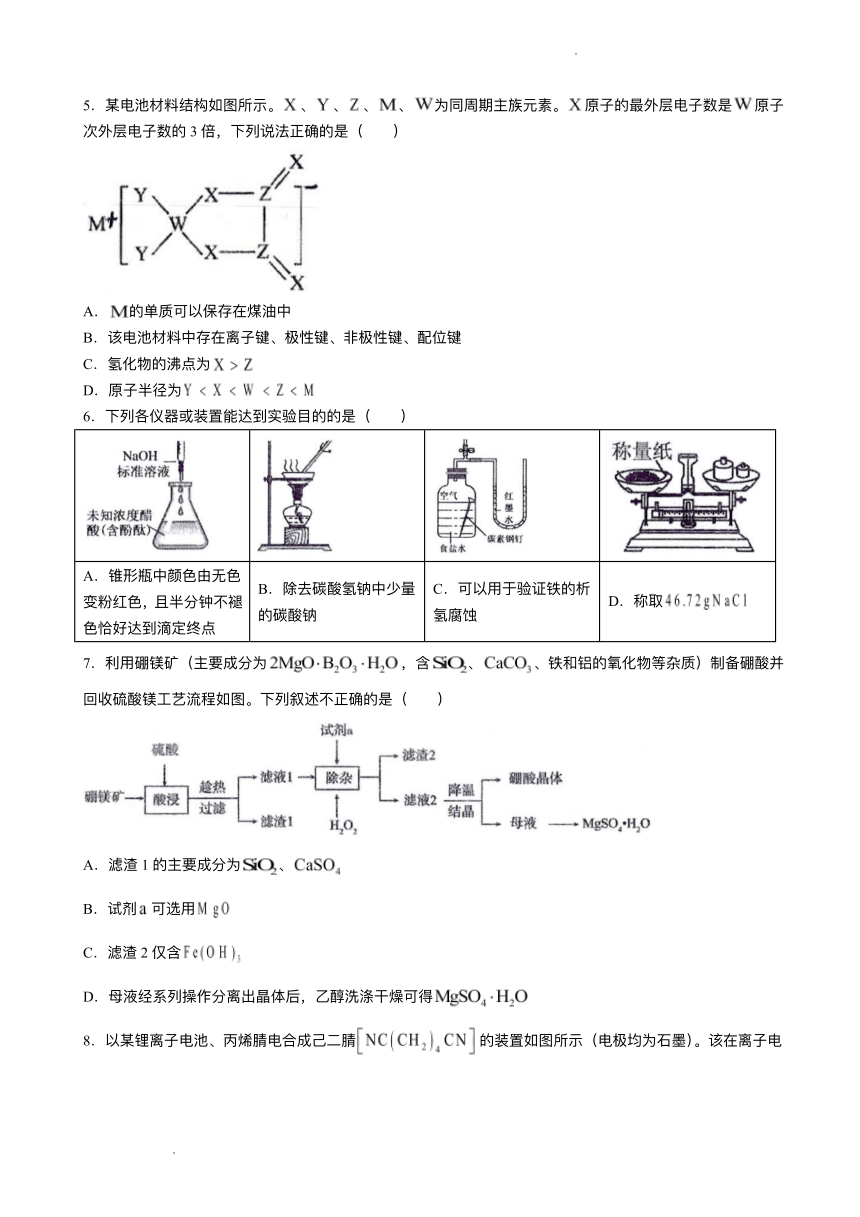
5.某电池材料结构如图所示。 、 、 、 、 为同周期主族元素。 原 的最外层电 数是 原
次外层电 数的 3倍,下列说法正确的是( )
A. 的单质可以保存在煤油中
B.该电池材料中存在离 键、极性键、 极性键、配位键
C.氢化物的沸点为
D.原 半径为
6.下列各仪器或装置能达到实验 的的是( )
A.锥形瓶中颜 由
B.除去碳酸氢钠中少量 C.可以 于验证铁的析
变粉红 ,且半分钟不褪 D.称取
的碳酸钠 氢腐蚀
恰好达到滴定终点
7.利 硼镁矿(主要成分为 ,含 、 、铁和铝的氧化物等杂质)制备硼酸并
回收硫酸镁 艺流程如图。下列叙述不正确的是( )
A.滤渣 1的主要成分为 、
B.试剂 可选
C.滤渣 2仅含
D. 液经系列操作分离出晶体后, 醇洗涤 燥可得
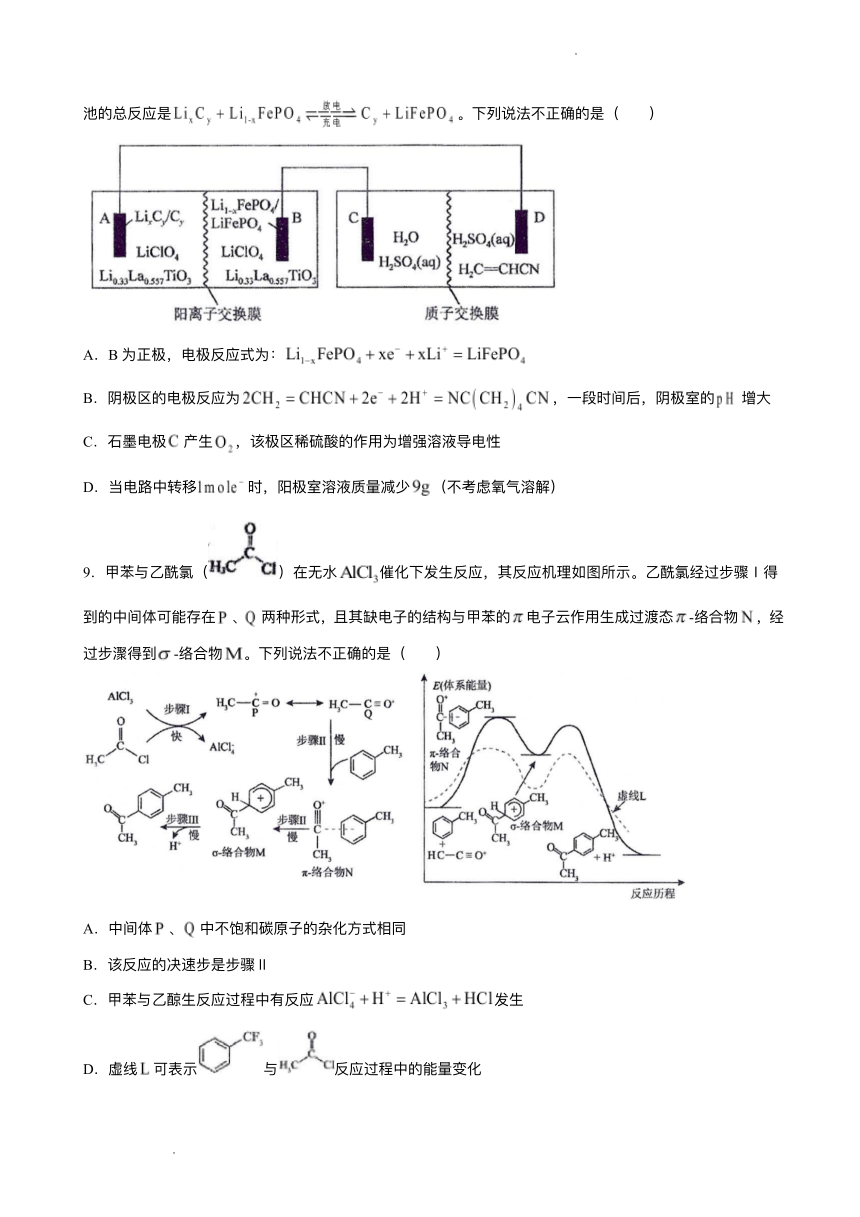
8.以某锂离 电池、丙烯腈电合成 腈 的装置如图所示(电极均为 墨)。该在离 电
学 科 ( 北 京 ) 股 份 有 限 公 司
池的总反应是 。下列说法不正确的是( )
A.B为正极,电极反应式为:
B.阴极区的电极反应为 , 段时间后,阴极室的 增
C. 墨电极 产 ,该极区稀硫酸的作 为增强溶液导电性
D.当电路中转移 时,阳极室溶液质量减少 (不考虑氧 溶解)
9.甲苯与 酰氯( )在 催化下发 反应,其反应机理如图所示。 酰氯经过步骤Ⅰ得
到的中间体可能存在 、 两种形式,且其缺电 的结构与甲苯的 电 云作 成过渡态 -络合物 ,经
过步 得到 -络合物 。下列说法不正确的是( )
A.中间体 、 中不饱和碳原 的杂化 式相同
B.该反应的决速步是步骤Ⅱ
C.甲苯与 反应过程中有反应 发
D.虚线 可表示 与 反应过程中的能量变化
学 科 ( 北 京 ) 股 份 有 限 公 司
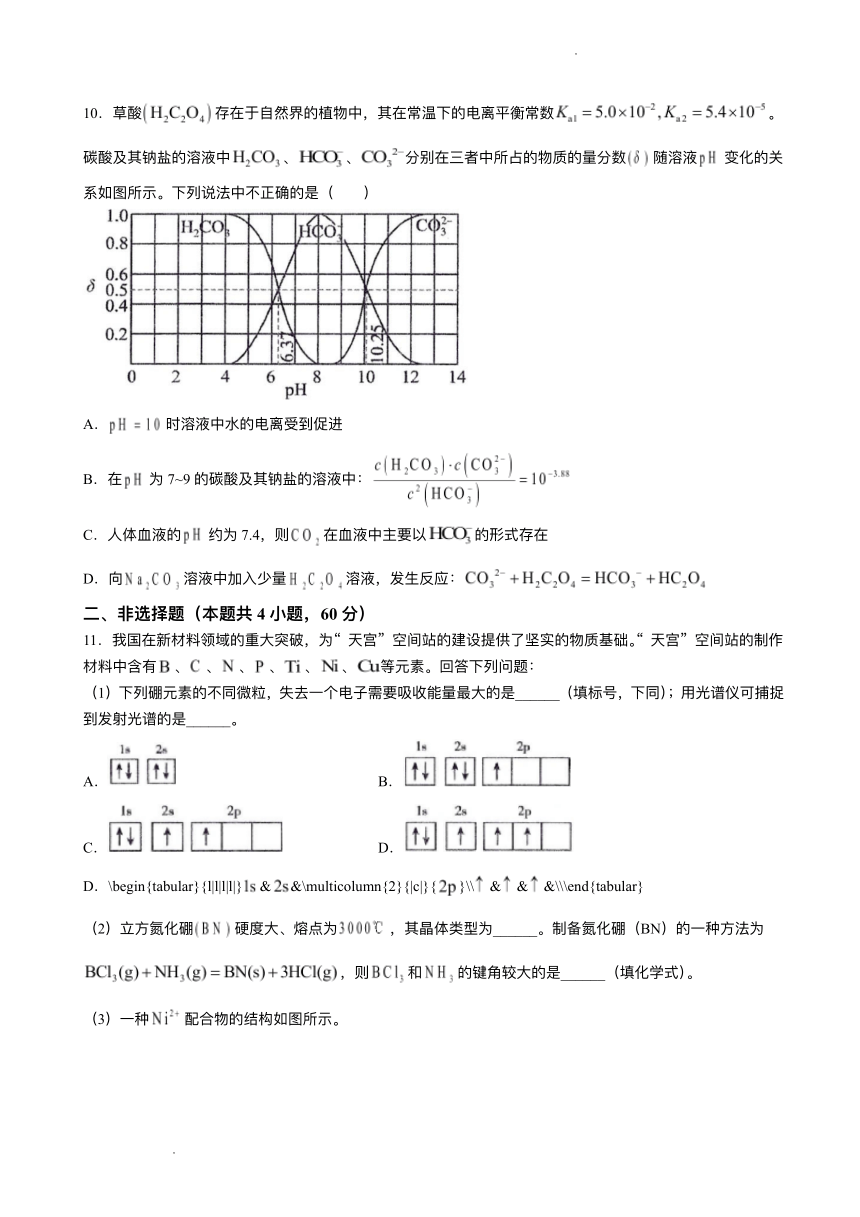
10.草酸 存在于 然界的植物中,其在常温下的电离平衡常数 。
碳酸及其钠盐的溶液中 、 、 分别在三者中所占的物质的量分数 随溶液 变化的关
系如图所示。下列说法中不正确的是( )
A. 时溶液中 的电离受到促进
B.在 为 7~9的碳酸及其钠盐的溶液中:
C. 体 液的 约为 7.4,则 在 液中主要以 的形式存在
D.向 溶液中加 少量 溶液,发 反应:
、 选择题(本题共 4 题,60分)
11.我国在新材料领域的重 突破,为“ 天宫” 空间站的建设提供了坚实的物质基础。“ 天宫” 空间站的制作
材料中含有 、 、 、 、 、 、 等元素。回答下列问题:
(1)下列硼元素的不同微粒,失去 个电 需要吸收能量最 的是______(填标号,下同); 光谱仪可捕捉
到发射光谱的是______。
A. B.
C. D.
D.\begin{tabular}{l|l|l|l|} & &\multicolumn{2}{|c|}{ }\\ & & &\\\end{tabular}
(2) 氮化硼 硬度 、熔点为 ,其晶体类型为______。制备氮化硼(BN)的 种 法为
,则 和 的键 较 的是______(填化学式)。
(3) 种 配合物的结构如图所示。
学 科 ( 北 京 ) 股 份 有 限 公 司
①组成该配合物的第 周期元素的电负性由 到 的顺序是______(填元素符号)。
②该配合物中 的配位数为______。
③该配合物中存在的化学键类型有______(填标号)。
A.离 键 B. 键 C. 键 D.氢键 E.配位键
(4)铁基合 中掺 B、N、P等元素可提 韧性、强度、耐磨性等。
① 的沸点 于 的主要原因为______。
②液态磷酸的导电机理如下图所示。液态磷酸中存在的两种离 符号为______,其中阳离 中 原 的杂化
式为______。
(5)GaAs的晶胞结构如图甲。将 掺杂到 GaAs的晶体中得到稀磁性半导体材料(图 )。
(1)GaAs晶体密度为 ,相对分 质量为 表示阿伏伽德罗常数的数值,则晶胞中距离最近的
两个 原 问距离为______ 。
(2)掺杂 之后,晶体中 、 、 的原 个数 为______(化为最简整数 )。
12.酸性矿 废 中锌、铁、锰元素的分离及回收流程如图:
已知:①酸性矿 废 成分如表:
pH
学 科 ( 北 京 ) 股 份 有 限 公 司
1. 0
②
③
(1)“ 研磨” 的 的是______。
(2)“ 沉锌” 过程中, 先转化为 和 ,所得 ______。
(3)“ 沉锌”过程中,完全沉淀时 ,测得溶液 为 4,则 ______
。
(4)“ 氧化” 过程发 反应的离 程式为______。
(5)“ 沉铁” 过程中,加 调节 ,废 对铁、锰元素去除率的影响如图所示,为提 铁、锰
元素的分离效果,废 控制______。
(6)“ 沉锰” 后,溶液中 ,锰元素去除率为______。 (保留 1位 数,忽略
体积变化)。
13. 氧化钒 是 种新型热敏材料,实验室以 为原料合成 于制备 的氧钒(IV)碱式碳酸
铵晶体{化学式为 },过程如下:
已知: 价钒在弱酸性条件下具有还原性。
(1)步骤 中 成 同时 成 的化学 程式为______。常温下,只 浓盐酸与 反应也能制备
溶液,但该 法未被推 ,从环保 度分析该 法未被推 的主要原因是______( 化学 程式说明)。
学 科 ( 北 京 ) 股 份 有 限 公 司
(2)步骤 ii可 下图仪器组装完成。
(1)装置D中盛放 溶液的仪器名称是______;上述装置从左到右的连接顺序为______( 各接
字 表示)。
(2)澄清 灰 的作 是______。
(3)反应结束后,将 D置于 保护下的 燥器中,静置过滤可得到紫红 晶体,然后抽滤,先 饱和
溶液洗涤 3次,再 醇洗涤 2次,最后 醚洗涤 2次。检验晶体已经洗涤 净的操作是
______。
(3)测定粗产品中钒的含量。实验步骤如下:
称量 ag产品于锥形瓶中, 蒸馏 与 稀硫酸溶解后,加 溶液 稍过量,
充分反应后继续滴加 的 溶液 稍过量,再 尿素除去过量 ,最后
标准溶液滴定 终点,消耗标准溶液的体积为 。
(已知: )
①滴定时,向锥形瓶中加 滴______溶液作指示剂。
②粗产品中钒的质量分数表达式为______(以 计)。
③若 标准溶液部分变质,会使测定结果______(填“ 偏 ”、“ 偏低” 或“ 影响”)。
14.氮的氧化物是 污染物之 ,研究它们的反应机理,对于消除环境污染,促进社会可持续发展有重要意
义。回答下列问题:
(1)碘蒸 的存在能 幅度提 的分解速率,反应历程为:
第 步: (快反应)
第 步: (慢反应)
第三步: (快反应)
实验表明,含碘时 分解速率 程 ( 为速率常数)。下列表述正确的是______
学 科 ( 北 京 ) 股 份 有 限 公 司
A.升 温度,第 步向右进 的程度变
B.第 步的活化能 第三步
C. 为反应的催化剂
D. 分解反应的速率与是否含碘蒸 有关
(2)对反应 ,分别在不同温度、不同催化剂
下,保持其它初始条件不变,重复实验,在相同时间内测得 NO转化率与温度的关系如图所示。
图中 点对应的速率(对应温度 ) ______ (填“ >”、“ <” 或“ =”),温度 于 ,NO
转化率降低的原因可能是______。
(3)在密闭容器中充 和 ,发 反应: 。
平衡时 NO的体积分数随温度、压强的变化关系如图。
①下列物理量中,图中 点 于 点的是______(填字 )。
A.正反应速率 B.逆反应速率
C. 的浓度 D.对应温度的平衡常数
(2) 点 的平衡转化率为______。
(3)若在 点对反应容器升温的同时扩 容器体积使体系压强减 ,重新达到的平衡状态可能是图中 a、b、
c、d中的______点。
(4) 时,向容积为 的恒容容器中充 、 ,发 反应:
学 科 ( 北 京 ) 股 份 有 限 公 司
说明:1.本试卷满分 100分,考试时间 75分钟。
2.可能 到的相对原 质量:H-1 C-12 O-16 V-51
、选择题(本题共 10 题,每 题 4分,共 40分,每 题只有 个选项符合题意)
1.材料的应 是社会进步的阶梯。下列有关材料的解读不正确的是( )
选项 材料 解读
A 玻璃浸泡 材或纺织品防 溶液阻燃、耐 温
B 成功合成 熵合 FeCoNiMnPtIr,作为锂氧电池的催化剂 该合 易被酸腐蚀
C 外接电流的阴极保护法 于钢铁管道防腐 阳极材料组成元素的 属性强于铁
制备纳 纤维脱硫材料 ,将捕获的 催化转化为 该材料中元素均位于周期表前四周
D
期
硫酸
2.下列有关物质的性质与 途具有对应关系的是( )
A. 极易溶于 ,可 于 业制冷剂
B. 炭具有还原性,可 于冰箱和居室除臭剂
C. 是两性氧化物,可 于制造 温材料
D. 、 合 熔点低且导热,可 于快中 反应堆的导热剂
3. 炔 化法、 烯氧化法是 业上制备 醛的两个重要 法,反应原理分别为:
, 。以下叙述不正确的是
A. 的电 式为
B. 的中 原 含有 孤电 对
C. 烯氧化法中, 成 醛时,转移的电 数约为
D.标准状况下, 中含有 键的数 约为
4.能正确表示下列反应的离 程式或电极反应式的是( )
A.少量 通 溶液中:
B.电解液为 溶液的 燃料电池的负极反应式:
C.向四羟基合铝酸钠溶液中加 苏打溶液:
D. 醋和 84消毒液混合:
学 科 ( 北 京 ) 股 份 有 限 公 司
5.某电池材料结构如图所示。 、 、 、 、 为同周期主族元素。 原 的最外层电 数是 原
次外层电 数的 3倍,下列说法正确的是( )
A. 的单质可以保存在煤油中
B.该电池材料中存在离 键、极性键、 极性键、配位键
C.氢化物的沸点为
D.原 半径为
6.下列各仪器或装置能达到实验 的的是( )
A.锥形瓶中颜 由
B.除去碳酸氢钠中少量 C.可以 于验证铁的析
变粉红 ,且半分钟不褪 D.称取
的碳酸钠 氢腐蚀
恰好达到滴定终点
7.利 硼镁矿(主要成分为 ,含 、 、铁和铝的氧化物等杂质)制备硼酸并
回收硫酸镁 艺流程如图。下列叙述不正确的是( )
A.滤渣 1的主要成分为 、
B.试剂 可选
C.滤渣 2仅含
D. 液经系列操作分离出晶体后, 醇洗涤 燥可得
8.以某锂离 电池、丙烯腈电合成 腈 的装置如图所示(电极均为 墨)。该在离 电
学 科 ( 北 京 ) 股 份 有 限 公 司
池的总反应是 。下列说法不正确的是( )
A.B为正极,电极反应式为:
B.阴极区的电极反应为 , 段时间后,阴极室的 增
C. 墨电极 产 ,该极区稀硫酸的作 为增强溶液导电性
D.当电路中转移 时,阳极室溶液质量减少 (不考虑氧 溶解)
9.甲苯与 酰氯( )在 催化下发 反应,其反应机理如图所示。 酰氯经过步骤Ⅰ得
到的中间体可能存在 、 两种形式,且其缺电 的结构与甲苯的 电 云作 成过渡态 -络合物 ,经
过步 得到 -络合物 。下列说法不正确的是( )
A.中间体 、 中不饱和碳原 的杂化 式相同
B.该反应的决速步是步骤Ⅱ
C.甲苯与 反应过程中有反应 发
D.虚线 可表示 与 反应过程中的能量变化
学 科 ( 北 京 ) 股 份 有 限 公 司
10.草酸 存在于 然界的植物中,其在常温下的电离平衡常数 。
碳酸及其钠盐的溶液中 、 、 分别在三者中所占的物质的量分数 随溶液 变化的关
系如图所示。下列说法中不正确的是( )
A. 时溶液中 的电离受到促进
B.在 为 7~9的碳酸及其钠盐的溶液中:
C. 体 液的 约为 7.4,则 在 液中主要以 的形式存在
D.向 溶液中加 少量 溶液,发 反应:
、 选择题(本题共 4 题,60分)
11.我国在新材料领域的重 突破,为“ 天宫” 空间站的建设提供了坚实的物质基础。“ 天宫” 空间站的制作
材料中含有 、 、 、 、 、 、 等元素。回答下列问题:
(1)下列硼元素的不同微粒,失去 个电 需要吸收能量最 的是______(填标号,下同); 光谱仪可捕捉
到发射光谱的是______。
A. B.
C. D.
D.\begin{tabular}{l|l|l|l|} & &\multicolumn{2}{|c|}{ }\\ & & &\\\end{tabular}
(2) 氮化硼 硬度 、熔点为 ,其晶体类型为______。制备氮化硼(BN)的 种 法为
,则 和 的键 较 的是______(填化学式)。
(3) 种 配合物的结构如图所示。
学 科 ( 北 京 ) 股 份 有 限 公 司
①组成该配合物的第 周期元素的电负性由 到 的顺序是______(填元素符号)。
②该配合物中 的配位数为______。
③该配合物中存在的化学键类型有______(填标号)。
A.离 键 B. 键 C. 键 D.氢键 E.配位键
(4)铁基合 中掺 B、N、P等元素可提 韧性、强度、耐磨性等。
① 的沸点 于 的主要原因为______。
②液态磷酸的导电机理如下图所示。液态磷酸中存在的两种离 符号为______,其中阳离 中 原 的杂化
式为______。
(5)GaAs的晶胞结构如图甲。将 掺杂到 GaAs的晶体中得到稀磁性半导体材料(图 )。
(1)GaAs晶体密度为 ,相对分 质量为 表示阿伏伽德罗常数的数值,则晶胞中距离最近的
两个 原 问距离为______ 。
(2)掺杂 之后,晶体中 、 、 的原 个数 为______(化为最简整数 )。
12.酸性矿 废 中锌、铁、锰元素的分离及回收流程如图:
已知:①酸性矿 废 成分如表:
pH
学 科 ( 北 京 ) 股 份 有 限 公 司
1. 0
②
③
(1)“ 研磨” 的 的是______。
(2)“ 沉锌” 过程中, 先转化为 和 ,所得 ______。
(3)“ 沉锌”过程中,完全沉淀时 ,测得溶液 为 4,则 ______
。
(4)“ 氧化” 过程发 反应的离 程式为______。
(5)“ 沉铁” 过程中,加 调节 ,废 对铁、锰元素去除率的影响如图所示,为提 铁、锰
元素的分离效果,废 控制______。
(6)“ 沉锰” 后,溶液中 ,锰元素去除率为______。 (保留 1位 数,忽略
体积变化)。
13. 氧化钒 是 种新型热敏材料,实验室以 为原料合成 于制备 的氧钒(IV)碱式碳酸
铵晶体{化学式为 },过程如下:
已知: 价钒在弱酸性条件下具有还原性。
(1)步骤 中 成 同时 成 的化学 程式为______。常温下,只 浓盐酸与 反应也能制备
溶液,但该 法未被推 ,从环保 度分析该 法未被推 的主要原因是______( 化学 程式说明)。
学 科 ( 北 京 ) 股 份 有 限 公 司
(2)步骤 ii可 下图仪器组装完成。
(1)装置D中盛放 溶液的仪器名称是______;上述装置从左到右的连接顺序为______( 各接
字 表示)。
(2)澄清 灰 的作 是______。
(3)反应结束后,将 D置于 保护下的 燥器中,静置过滤可得到紫红 晶体,然后抽滤,先 饱和
溶液洗涤 3次,再 醇洗涤 2次,最后 醚洗涤 2次。检验晶体已经洗涤 净的操作是
______。
(3)测定粗产品中钒的含量。实验步骤如下:
称量 ag产品于锥形瓶中, 蒸馏 与 稀硫酸溶解后,加 溶液 稍过量,
充分反应后继续滴加 的 溶液 稍过量,再 尿素除去过量 ,最后
标准溶液滴定 终点,消耗标准溶液的体积为 。
(已知: )
①滴定时,向锥形瓶中加 滴______溶液作指示剂。
②粗产品中钒的质量分数表达式为______(以 计)。
③若 标准溶液部分变质,会使测定结果______(填“ 偏 ”、“ 偏低” 或“ 影响”)。
14.氮的氧化物是 污染物之 ,研究它们的反应机理,对于消除环境污染,促进社会可持续发展有重要意
义。回答下列问题:
(1)碘蒸 的存在能 幅度提 的分解速率,反应历程为:
第 步: (快反应)
第 步: (慢反应)
第三步: (快反应)
实验表明,含碘时 分解速率 程 ( 为速率常数)。下列表述正确的是______
学 科 ( 北 京 ) 股 份 有 限 公 司
A.升 温度,第 步向右进 的程度变
B.第 步的活化能 第三步
C. 为反应的催化剂
D. 分解反应的速率与是否含碘蒸 有关
(2)对反应 ,分别在不同温度、不同催化剂
下,保持其它初始条件不变,重复实验,在相同时间内测得 NO转化率与温度的关系如图所示。
图中 点对应的速率(对应温度 ) ______ (填“ >”、“ <” 或“ =”),温度 于 ,NO
转化率降低的原因可能是______。
(3)在密闭容器中充 和 ,发 反应: 。
平衡时 NO的体积分数随温度、压强的变化关系如图。
①下列物理量中,图中 点 于 点的是______(填字 )。
A.正反应速率 B.逆反应速率
C. 的浓度 D.对应温度的平衡常数
(2) 点 的平衡转化率为______。
(3)若在 点对反应容器升温的同时扩 容器体积使体系压强减 ,重新达到的平衡状态可能是图中 a、b、
c、d中的______点。
(4) 时,向容积为 的恒容容器中充 、 ,发 反应:
学 科 ( 北 京 ) 股 份 有 限 公 司
同课章节目录
