高中化学必修第一册2.2《氯及其化合物》练习题含答案-人教版(2019)(解析版)
文档属性
| 名称 | 高中化学必修第一册2.2《氯及其化合物》练习题含答案-人教版(2019)(解析版) |

|
|
| 格式 | docx | ||
| 文件大小 | 413.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-12-15 00:00:00 | ||
图片预览




文档简介
2.2《氯及其化合物》练习题含答案
一、选择题(单选,每小题3分,共42分)
1、下列说法中正确的是( )
A、Cl2在与金属反应时表现强氧化性。
B、任何物质的燃烧必须有O2参与
C、Cl2与H2O反应的离子方程式为Cl2+H2O===2H++Cl-+ClO-
D、漂白粉的有效成分是Ca(ClO)2和CaCl2
答案:A
2、下列关于氯气的叙述正确的是( )
A.钠在氯气中燃烧产生白色烟雾
B.红热的铜丝在氯气中燃烧生成CuCl
C.纯净的氢气可以在氯气中安静地燃烧,发出黄色火焰
D.向田鼠洞里通入氯气杀灭田鼠,利用了氯气有毒和密度比空气大的性质
解析 A中钠在氯气中燃烧,生成NaCl固体小颗粒,形成白烟,没有雾出现(雾为小液滴),A错误;B中红热的铜丝在氯气中燃烧生成CuCl2,B错误;C中氢气在氯气中燃烧发出苍白色火焰,C错误;D中氯气有毒,密度比空气的大,可杀灭田鼠,D正确。
答案 D
3、下列关于氯水的叙述中正确的是( )
A.新制氯水中只含有Cl2和H2O分子
B.新制氯水可使蓝色石蕊试纸先变红后褪色
C.光照氯水有气泡逸出,该气体是Cl2 HClO有漂白性
D.氯水放置数天后,酸性减弱2HClO2HCl+O2↑
解析:A新制备的氯水成分是7种,3分子,4离子,B正确,氯水既有酸性又有氧化性(漂白性),C光照氯水有气泡逸出,该气体主要是O2,D,酸性增强,因为HClO光照变成盐酸了,酸性增强。
答案 B
4、下列各化合物不能由单质直接化合制取的是( )
A.FeCl3 B.CuCl2
C.AlCl3 D.FeCl2
解析 因Cl2氧化性很强,与变价金属反应时生成高价态金属氯化物,Fe元素有+2价、+3价,Cu元素有+1价、+2价,Al元素只有+3价,所以选D。
答案 D
5、新制氯水中存在多种分子和离子,可通过实验的方法加以确定。下列有关新制氯水中存在的粒子的说法错误的是( )
A.加入含有硫酸氢钠的红色石蕊溶液红色褪去,说明有Cl2存在
B.加入有色布条,有色布条褪色,说明有HClO存在
C.新制氯水呈浅黄绿色,且有刺激性气味,说明有Cl2存在
D.加入硝酸酸化的硝酸银溶液产生白色沉淀,说明有Cl-存在
解析 氯气与水反应生成盐酸(强酸)和次氯酸(弱酸),反应后的溶液中含有氯气分子(新制氯水为浅黄绿色)、次氯酸分子(使石蕊溶液褪色,具有漂白性)、氢离子、氯离子(与硝酸银溶液产生白色沉淀)、次氯酸根离子等粒子。
答案 A
6、欲除去Cl2中的少量HCl气体,可选用( )
A.NaOH溶液 B.饱和食盐水
C.浓硫酸 D.石灰水
解析 利用了HCl极易溶于水而Cl2在饱和食盐水中溶解度很小的原理。
答案 B
7、用下列两种方法制取氯气:
①用含氯化氢146 g的浓盐酸与足量的二氧化锰反应;②用87 g二氧化锰与足量的浓盐酸反应。则所得氯气( )
A.②比①多 B.①比②多
C.一样多 D.无法比较
解析 浓盐酸与MnO2反应的化学方程式为4HCl(浓)+MnO2MnCl2+Cl2↑+2H2O,随着反应进行,盐酸浓度逐渐减小,变为稀盐酸后不再与MnO2反应。①中HCl不能完全反应,产生的Cl2少,②中能完全反应,制得Cl2多。故产生Cl2②>①。
答案 A
8、下列实验过程中,不会产生气体的是( )
解析 A项,新制氯水中的HClO见光分解生成氧气,不符合题意;B项,新制氯水中的H+与发酵粉中的NaHCO3反应生成CO2,不符合题意;C项,新制氯水中的Cl2与NaBr反应生成Br2和NaCl,没有气体产生,符合题意;D项,H2O与Na2O2反应生成O2,不符合题意。
答案 C
9、已知KMnO4与浓盐酸在常温下反应能产生Cl2。若用下图所示的实验装置来制备纯净、干燥的氯气,并试验其与金属的反应,每个虚线框表示一个单元装置,其中有错误的是( )
A.①和②处 B.只有②处
C.②和③处 D.②、③、④处
解析 ①是制备氯气的装置,②是除去氯气中氯化氢杂质的装置,③是干燥装置,④是用于氯气与金属反应的装置。除杂时不能消耗欲保留的气体,因为氯气可与NaOH溶液反应,化学方程式为Cl2+2NaOH===NaCl+NaClO+H2O,所以②处错误;③中进气管短,出气管却插入液面下,所以无法干燥气体,也不能使气体进入④中与金属反应,所以③处错误;④是一个封闭体系,未反应的气体不断蓄积会使容器内压强过大而发生爆炸,所以④处错误。
答案 D
10、下列检验Cl-的方法正确的是( )
A.在某溶液中滴加AgNO3溶液,若产生白色沉淀说明该溶液中有Cl-
B.在某溶液中先滴加盐酸,再滴加AgNO3溶液,若产生白色沉淀,说明溶液中有Cl-
C.在某溶液中先滴加AgNO3溶液,产生白色沉淀,再滴加盐酸,沉淀不消失,说明溶液中有Cl-
D.在某溶液中滴加用HNO3酸化的AgNO3溶液,若产生白色沉淀,说明溶液中有Cl-
解析 可能有CO、PO等的干扰,A错误;加入盐酸,引入Cl-,B、C错误;硝酸酸化排除干扰,加硝酸银溶液得到不溶于稀硝酸的白色沉淀即为AgCl,由此说明原溶液中有Cl-,D正确。
答案 D
11、下列实验现象,与新制氯水中的某些成分(括号内物质)没有关系的是( )
A.使红色布条褪色(HCl)
B.将NaHCO3固体加入新制氯水,有无色气泡(H+)
C.向FeCl2溶液中滴加氯水,再滴加KSCN溶液,发现呈红色(Cl2)
D.滴加AgNO3溶液生成白色沉淀(Cl-)
解析 A项,次氯酸具有强氧化性,能氧化有色布条而使其褪色,与氯化氢无关,错误;B项,氯水显酸性,能与碳酸氢钠反应生成CO2气体,正确;C项,氯气氧化了亚铁离子生成三价铁离子,再滴加KSCN溶液,发现呈红色,正确;D项,氯离子和硝酸银反应生成氯化银白色沉淀,正确。
答案 A
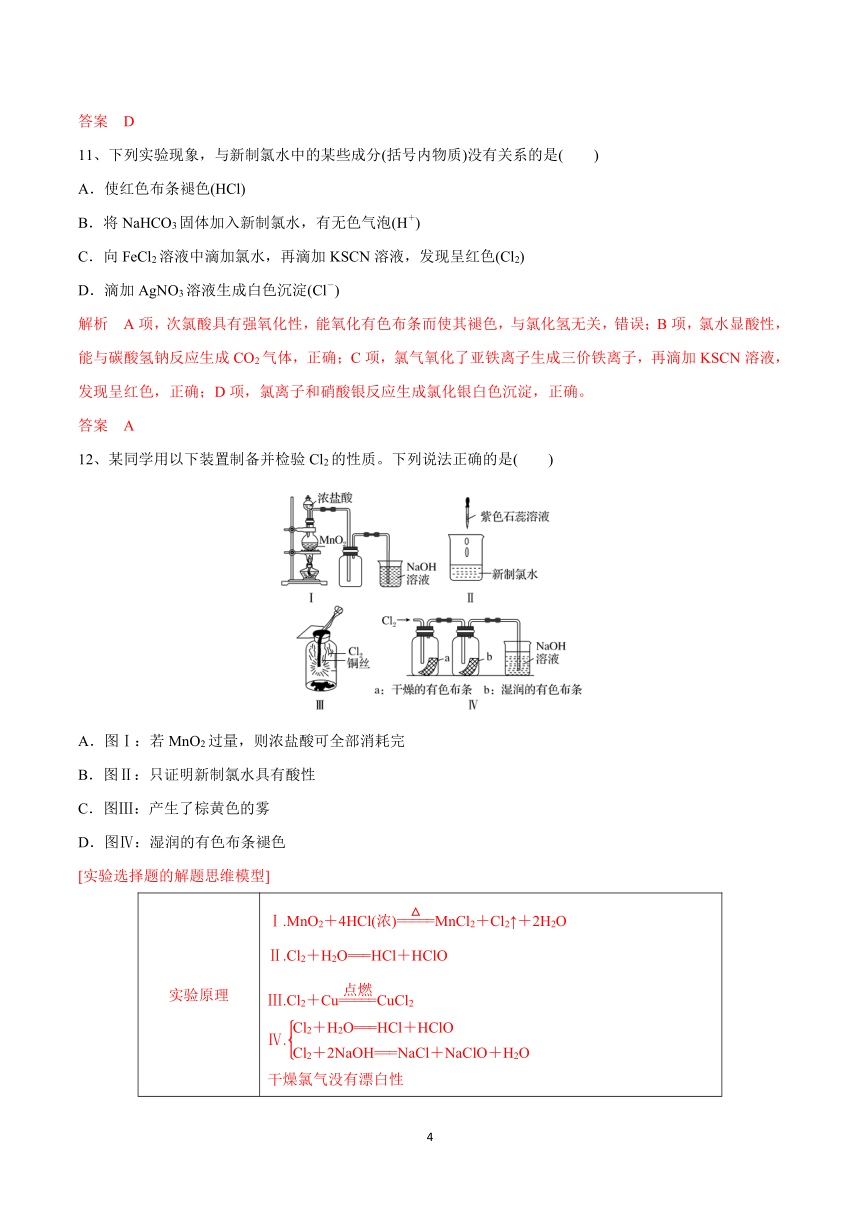
12、某同学用以下装置制备并检验Cl2的性质。下列说法正确的是( )
A.图Ⅰ:若MnO2过量,则浓盐酸可全部消耗完
B.图Ⅱ:只证明新制氯水具有酸性
C.图Ⅲ:产生了棕黄色的雾
D.图Ⅳ:湿润的有色布条褪色
[实验选择题的解题思维模型]
实验原理 Ⅰ.MnO2+4HCl(浓)MnCl2+Cl2↑+2H2O Ⅱ.Cl2+H2O===HCl+HClO Ⅲ.Cl2+CuCuCl2 Ⅳ. 干燥氯气没有漂白性
提取关键点 Ⅰ.只有浓盐酸才能反应 Ⅱ.HCl显酸性、HClO有漂白性 Ⅲ.CuCl2固体 Ⅳ.湿润有色布条含水
得出结论 A错;B不全面;C雾错,应是烟;D正确。
答案 D
13、已知:KClO3+6HCl(浓)===KCl+3Cl2↑+3H2O,如图所示,将少量试剂分别放入培养皿中的相应位置,实验时将浓盐酸滴在KClO3晶体上,并用表面皿盖好。如表中由实验现象得出的结论完全正确的是( )
选项 实验现象 结论
A FeCl2溶液由浅绿色变为棕黄色 Cl2具有还原性
B 滴有酚酞的NaOH溶液褪色 Cl2具有酸性
C 紫色石蕊溶液先变红后褪色 Cl2具有漂白性
D 淀粉-KI溶液变为蓝色 Cl2具有氧化性
解析 A项说明Cl2具有氧化性。B项是Cl2与H2O反应生成了HCl、HClO,都可以使滴有酚酞的NaOH溶液褪色。C项是Cl2与H2O反应生成的HCl具有酸性,HClO具有漂白性。D项的反应为Cl2+2KI===2KCl+I2,说明Cl2具有氧化性。
答案 D
14、已知氯气和NaOH溶液在一定温度下能发生反应:Cl2+2NaOH===NaCl+NaClO+H2O,3Cl2+6NaOH===5NaCl+NaClO3+3H2O。某温度下,将氯气通入NaOH溶液中,反应得到NaCl、NaClO和NaClO3的混合溶液,经测定ClO-与ClO的个数比为1∶3,则氯气与氢氧化钠反应时,被还原的氯原子和被氧化的氯原子的个数比为( )
A.21∶5 B.11∶3
C.3∶1 D.4∶1
解析 假设反应后溶液中的ClO-为1个,根据ClO-与ClO的个数之比为1∶3,且由Cl到ClO-失去1个电子,由Cl到ClO失去5个电子可知,一共失去的电子为(1+3×5)=16个;由Cl到Cl-得到1个电子,则16个Cl被还原得到16个电子,所以被还原的氯原子与被氧化的氯原子的个数比为16∶(1+3)=4∶1。
答案 D
二、非选择(共58分)
15、(9分)为探究氯水中含有的部分粒子及某些粒子的性质,某化学兴趣小组做了如下实验:
(1)观察氯水颜色,发现氯水呈黄绿色,证明氯水中含有的粒子是________。
(2)向氯水中滴入碳酸钠溶液,有气体生成,说明氯水中含有的粒子是________。
(3)在盛有氯水的试管中的有色布条褪色,说明氯水中含有的粒子是________。
(4)将紫色石蕊溶液滴入新制氯水中,溶液显红色,起作用的微粒是________,过一会儿,溶液的颜色褪去,起作用的微粒是________。
(5)向氯水中滴加AgNO3溶液有白色沉淀生成,证明氯水中含有的粒子是________。
(6)氯水经光照后,颜色逐渐消失,并放出的气体是________,溶液的酸性________(填“增强”、“不变”或“减弱”)。
(7)将Cl2通入水中,所得溶液中具有氧化性的含氯微粒是__________。
解析 (1)氯水中含有的微粒有Cl2、HClO、H2O、H+、Cl-、ClO-和OH-,含有Cl2,使溶液呈现黄绿色;(2)滴入Na2CO3溶液有气体生成,证明溶液呈酸性,含H+;(3)氯水能使有色布条褪色,说明具有漂白性,证明氯水中含有HClO;(4)紫色石蕊溶液滴入新制氯水中,溶液呈红色,说明有H+存在,很快褪色,则是因为HClO起漂白作用;(5)向氯水中滴加AgNO3溶液有白色沉淀生成,证明氯水中有Cl-;(6)HClO不稳定,见光易分解放出O2,并生成盐酸,由于HClO为弱酸,而盐酸是强酸,故溶液酸性增强;(7)氯水中的Cl2、ClO-、HClO具有强氧化性。
答案 (1)Cl2 (2)H+ (3)HClO (4)H+ HClO
(5)Cl- (6)O2 增强 (7)Cl2、ClO-、HClO
16、(11分)Cl2是一种重要的化工原料。下图是一些含氯产品。
(1)①中钢瓶上应贴的标签为________。
A.腐蚀品 B.爆炸品
C.有毒品 D.易燃品
(2)下列有关漂白粉和漂白液的说法正确的是________。
A.漂白粉是纯净物,漂白液是混合物
B.漂白粉的有效成分是Ca(ClO)2
C.工业上将氯气通入澄清石灰水制取漂白粉
D.漂白液的有效成分是Na2O2
(3)工业上利用Cl2制盐酸,其化学方程式为_____________________________
________________________________________________________。
Cl2溶于水可制得氯水,检验一瓶氯水是否已经完全变质,可选用的试剂是________。
A.硝酸银溶液 B.酚酞溶液
C.碳酸钠溶液 D.紫色石蕊溶液
解析 (1)Cl2有毒,贮存Cl2的钢瓶应贴的标签为有毒品。
(2)漂白粉的有效成分是Ca(ClO)2,漂白液的有效成分是NaClO,二者均是混合物,A、D项错误;制取漂白粉时,不用澄清石灰水,因氢氧化钙的溶解度较小,一般用石灰乳,也可用氯气与稍湿的消石灰作用制得,C项错误。
(3)久置氯水的成分为稀盐酸,新制氯水的主要成分为Cl2、HCl、HClO,新制氯水和稀盐酸均与AgNO3溶液反应生成白色沉淀,均与Na2CO3溶液反应放出CO2气体,遇酚酞溶液均无明显现象。新制氯水中加入紫色石蕊溶液先变红后褪色,而稀盐酸中加入紫色石蕊溶液只变红色。
答案 (1)C (2)B (3)H2+Cl22HCl D
17、(14分)常温下,A是可用来对自来水进行消毒的黄绿色单质气体,A、B、C、D、E都含X元素,其转化关系如图所示:
(1)请分别写出A、B、D的化学式(如为溶液请填溶质的化学式):
A________、B________、D________。
(2)写出下列反应的化学方程式或离子方程式(请注明条件):
A+H2O(离子方程式):____________________________;
A+NaOH(离子方程式): _____________________;
D→A(化学方程式):________________________。
解析 由题意可知A为氯气,B为次氯酸,D为盐酸,C为氯化钠,E为次氯酸钠。
答案 (1)Cl2 HClO HCl
(2)Cl2+H2O===H++Cl-+HClO
Cl2+2OH-===Cl-+ClO-+H2O
4HCl(浓)+MnO2MnCl2+Cl2↑+2H2O
18、(14分)如图所示是某学生设计的实验室制备并干燥Cl2及吸收多余氯气的实验装置图,请回答:
(1)指出上述图中的各处错误:
①__________________________________________;
②__________________________________________;
③__________________________________________;
④__________________________________________。
(2)在改进后的装置中,下列物质的作用分别是:
①饱和食盐水___________________________________;
②浓硫酸_______________________________________;
③NaOH溶液____________________________________。
(3)制备实验开始时,先检查装置的气密性,接下来的操作依次是________。
A.向烧瓶中加入MnO2粉末
B.加热
C.向烧瓶中加入浓盐酸
(4)如果将过量二氧化锰与含HCl 8.76 g的浓盐酸混合加热,充分反应后生成的氯气明显少于4.26 g。其主要原因有:①_______________________________,
②____________________________________________________。
(5)为了提高浓盐酸的利用率,你对实验的建议是_______________________
_______________________________________________________。
(6)圆底烧瓶中发生反应的离子方程式是____________________________。
实验结束清洗仪器时,为了减少烧瓶中残留氯气对环境的污染,可以向烧瓶中加入的溶液是________,有关的离子方程式是________________________。
解析 (2)先除HCl,后干燥,再收集,最后尾气吸收。(3)检查装置气密性后的操作顺序为先加固体药品,然后加入液体药品,最后加热。(4)题中所给盐酸中HCl的质量是8.76 g,但由于盐酸受热易挥发,且随反应的不断进行,盐酸浓度越来越小,变为稀盐酸后不再与MnO2反应,所以产生的Cl2的质量小于4.26 g。(5)为减少盐酸的挥发,慢慢滴加浓盐酸,用小火加热。(6)利用Cl2和NaOH溶液反应除多余的Cl2。
答案 (1)①不能用稀盐酸,而应用浓盐酸 ②应有加热装置,应用酒精灯加热 ③盛浓硫酸和盛饱和食盐水的洗气瓶位置颠倒 ④两洗气瓶里进气导管和出气导管的长短颠倒
(2)①除去Cl2中的氯化氢 ②除去氯气中的水蒸气
③吸收多余的氯气
(3)ACB
(4)①加热使HCl大量挥发 ②浓盐酸变稀后不再发生反应
(5)将浓盐酸慢慢滴下;加热用小火
(6)MnO2+4H++2Cl-Mn2++Cl2↑+2H2O
NaOH溶液 Cl2+2OH-===Cl-+ClO-+H2O、
H++OH-===H2O
19、(10分)某研究小组为了制备84消毒液(主要成分为NaClO)设计了如图装置。并查阅到下列资料:“卤素与水的反应是放热反应,在加热情况下卤素与碱液发生如下反应:
3X2+6OH-5X-+XO+3H2O”。
回答下列问题:
(1)装置中的试管内发生反应的离子方程式为_________________________
(2)装置中能否省去盛饱和NaCl溶液的洗气瓶?________(填“能”或“不能”,下同),理由是_______________________________。
(3)装置中能否省去盛浓硫酸的洗气瓶?________,理由是__________________。
(4)装置中能否省去盛冰水的烧杯?________,理由是___________________
解析 本题具有较强的综合性,装置产生的Cl2在冰水冷却下与NaOH发生反应制得消毒液。运用该装置必须通过饱和NaCl溶液除去HCl,否则HCl与NaOH反应将生成NaCl,降低NaClO的纯度;但干燥装置可以省略,因为少量水蒸气不会影响反应;冷却装置不可省略,因为题给信息:氯气与水的反应是放热反应,温度升高,引起副反应:3Cl2+6OH-5Cl-+ClO+3H2O。
答案 (1)Cl2+2OH-===Cl-+ClO-+H2O
(2)不能 氯气中混有的HCl气体进入试管中也会和氢氧化钠溶液反应,降低了NaClO的产量和纯度
(3)能 少量水蒸气进入试管中不影响反应
(4)不能 氯气与水的反应是放热反应,反应时温度升高,可能引起副反应,生成NaClO3
10
一、选择题(单选,每小题3分,共42分)
1、下列说法中正确的是( )
A、Cl2在与金属反应时表现强氧化性。
B、任何物质的燃烧必须有O2参与
C、Cl2与H2O反应的离子方程式为Cl2+H2O===2H++Cl-+ClO-
D、漂白粉的有效成分是Ca(ClO)2和CaCl2
答案:A
2、下列关于氯气的叙述正确的是( )
A.钠在氯气中燃烧产生白色烟雾
B.红热的铜丝在氯气中燃烧生成CuCl
C.纯净的氢气可以在氯气中安静地燃烧,发出黄色火焰
D.向田鼠洞里通入氯气杀灭田鼠,利用了氯气有毒和密度比空气大的性质
解析 A中钠在氯气中燃烧,生成NaCl固体小颗粒,形成白烟,没有雾出现(雾为小液滴),A错误;B中红热的铜丝在氯气中燃烧生成CuCl2,B错误;C中氢气在氯气中燃烧发出苍白色火焰,C错误;D中氯气有毒,密度比空气的大,可杀灭田鼠,D正确。
答案 D
3、下列关于氯水的叙述中正确的是( )
A.新制氯水中只含有Cl2和H2O分子
B.新制氯水可使蓝色石蕊试纸先变红后褪色
C.光照氯水有气泡逸出,该气体是Cl2 HClO有漂白性
D.氯水放置数天后,酸性减弱2HClO2HCl+O2↑
解析:A新制备的氯水成分是7种,3分子,4离子,B正确,氯水既有酸性又有氧化性(漂白性),C光照氯水有气泡逸出,该气体主要是O2,D,酸性增强,因为HClO光照变成盐酸了,酸性增强。
答案 B
4、下列各化合物不能由单质直接化合制取的是( )
A.FeCl3 B.CuCl2
C.AlCl3 D.FeCl2
解析 因Cl2氧化性很强,与变价金属反应时生成高价态金属氯化物,Fe元素有+2价、+3价,Cu元素有+1价、+2价,Al元素只有+3价,所以选D。
答案 D
5、新制氯水中存在多种分子和离子,可通过实验的方法加以确定。下列有关新制氯水中存在的粒子的说法错误的是( )
A.加入含有硫酸氢钠的红色石蕊溶液红色褪去,说明有Cl2存在
B.加入有色布条,有色布条褪色,说明有HClO存在
C.新制氯水呈浅黄绿色,且有刺激性气味,说明有Cl2存在
D.加入硝酸酸化的硝酸银溶液产生白色沉淀,说明有Cl-存在
解析 氯气与水反应生成盐酸(强酸)和次氯酸(弱酸),反应后的溶液中含有氯气分子(新制氯水为浅黄绿色)、次氯酸分子(使石蕊溶液褪色,具有漂白性)、氢离子、氯离子(与硝酸银溶液产生白色沉淀)、次氯酸根离子等粒子。
答案 A
6、欲除去Cl2中的少量HCl气体,可选用( )
A.NaOH溶液 B.饱和食盐水
C.浓硫酸 D.石灰水
解析 利用了HCl极易溶于水而Cl2在饱和食盐水中溶解度很小的原理。
答案 B
7、用下列两种方法制取氯气:
①用含氯化氢146 g的浓盐酸与足量的二氧化锰反应;②用87 g二氧化锰与足量的浓盐酸反应。则所得氯气( )
A.②比①多 B.①比②多
C.一样多 D.无法比较
解析 浓盐酸与MnO2反应的化学方程式为4HCl(浓)+MnO2MnCl2+Cl2↑+2H2O,随着反应进行,盐酸浓度逐渐减小,变为稀盐酸后不再与MnO2反应。①中HCl不能完全反应,产生的Cl2少,②中能完全反应,制得Cl2多。故产生Cl2②>①。
答案 A
8、下列实验过程中,不会产生气体的是( )
解析 A项,新制氯水中的HClO见光分解生成氧气,不符合题意;B项,新制氯水中的H+与发酵粉中的NaHCO3反应生成CO2,不符合题意;C项,新制氯水中的Cl2与NaBr反应生成Br2和NaCl,没有气体产生,符合题意;D项,H2O与Na2O2反应生成O2,不符合题意。
答案 C
9、已知KMnO4与浓盐酸在常温下反应能产生Cl2。若用下图所示的实验装置来制备纯净、干燥的氯气,并试验其与金属的反应,每个虚线框表示一个单元装置,其中有错误的是( )
A.①和②处 B.只有②处
C.②和③处 D.②、③、④处
解析 ①是制备氯气的装置,②是除去氯气中氯化氢杂质的装置,③是干燥装置,④是用于氯气与金属反应的装置。除杂时不能消耗欲保留的气体,因为氯气可与NaOH溶液反应,化学方程式为Cl2+2NaOH===NaCl+NaClO+H2O,所以②处错误;③中进气管短,出气管却插入液面下,所以无法干燥气体,也不能使气体进入④中与金属反应,所以③处错误;④是一个封闭体系,未反应的气体不断蓄积会使容器内压强过大而发生爆炸,所以④处错误。
答案 D
10、下列检验Cl-的方法正确的是( )
A.在某溶液中滴加AgNO3溶液,若产生白色沉淀说明该溶液中有Cl-
B.在某溶液中先滴加盐酸,再滴加AgNO3溶液,若产生白色沉淀,说明溶液中有Cl-
C.在某溶液中先滴加AgNO3溶液,产生白色沉淀,再滴加盐酸,沉淀不消失,说明溶液中有Cl-
D.在某溶液中滴加用HNO3酸化的AgNO3溶液,若产生白色沉淀,说明溶液中有Cl-
解析 可能有CO、PO等的干扰,A错误;加入盐酸,引入Cl-,B、C错误;硝酸酸化排除干扰,加硝酸银溶液得到不溶于稀硝酸的白色沉淀即为AgCl,由此说明原溶液中有Cl-,D正确。
答案 D
11、下列实验现象,与新制氯水中的某些成分(括号内物质)没有关系的是( )
A.使红色布条褪色(HCl)
B.将NaHCO3固体加入新制氯水,有无色气泡(H+)
C.向FeCl2溶液中滴加氯水,再滴加KSCN溶液,发现呈红色(Cl2)
D.滴加AgNO3溶液生成白色沉淀(Cl-)
解析 A项,次氯酸具有强氧化性,能氧化有色布条而使其褪色,与氯化氢无关,错误;B项,氯水显酸性,能与碳酸氢钠反应生成CO2气体,正确;C项,氯气氧化了亚铁离子生成三价铁离子,再滴加KSCN溶液,发现呈红色,正确;D项,氯离子和硝酸银反应生成氯化银白色沉淀,正确。
答案 A
12、某同学用以下装置制备并检验Cl2的性质。下列说法正确的是( )
A.图Ⅰ:若MnO2过量,则浓盐酸可全部消耗完
B.图Ⅱ:只证明新制氯水具有酸性
C.图Ⅲ:产生了棕黄色的雾
D.图Ⅳ:湿润的有色布条褪色
[实验选择题的解题思维模型]
实验原理 Ⅰ.MnO2+4HCl(浓)MnCl2+Cl2↑+2H2O Ⅱ.Cl2+H2O===HCl+HClO Ⅲ.Cl2+CuCuCl2 Ⅳ. 干燥氯气没有漂白性
提取关键点 Ⅰ.只有浓盐酸才能反应 Ⅱ.HCl显酸性、HClO有漂白性 Ⅲ.CuCl2固体 Ⅳ.湿润有色布条含水
得出结论 A错;B不全面;C雾错,应是烟;D正确。
答案 D
13、已知:KClO3+6HCl(浓)===KCl+3Cl2↑+3H2O,如图所示,将少量试剂分别放入培养皿中的相应位置,实验时将浓盐酸滴在KClO3晶体上,并用表面皿盖好。如表中由实验现象得出的结论完全正确的是( )
选项 实验现象 结论
A FeCl2溶液由浅绿色变为棕黄色 Cl2具有还原性
B 滴有酚酞的NaOH溶液褪色 Cl2具有酸性
C 紫色石蕊溶液先变红后褪色 Cl2具有漂白性
D 淀粉-KI溶液变为蓝色 Cl2具有氧化性
解析 A项说明Cl2具有氧化性。B项是Cl2与H2O反应生成了HCl、HClO,都可以使滴有酚酞的NaOH溶液褪色。C项是Cl2与H2O反应生成的HCl具有酸性,HClO具有漂白性。D项的反应为Cl2+2KI===2KCl+I2,说明Cl2具有氧化性。
答案 D
14、已知氯气和NaOH溶液在一定温度下能发生反应:Cl2+2NaOH===NaCl+NaClO+H2O,3Cl2+6NaOH===5NaCl+NaClO3+3H2O。某温度下,将氯气通入NaOH溶液中,反应得到NaCl、NaClO和NaClO3的混合溶液,经测定ClO-与ClO的个数比为1∶3,则氯气与氢氧化钠反应时,被还原的氯原子和被氧化的氯原子的个数比为( )
A.21∶5 B.11∶3
C.3∶1 D.4∶1
解析 假设反应后溶液中的ClO-为1个,根据ClO-与ClO的个数之比为1∶3,且由Cl到ClO-失去1个电子,由Cl到ClO失去5个电子可知,一共失去的电子为(1+3×5)=16个;由Cl到Cl-得到1个电子,则16个Cl被还原得到16个电子,所以被还原的氯原子与被氧化的氯原子的个数比为16∶(1+3)=4∶1。
答案 D
二、非选择(共58分)
15、(9分)为探究氯水中含有的部分粒子及某些粒子的性质,某化学兴趣小组做了如下实验:
(1)观察氯水颜色,发现氯水呈黄绿色,证明氯水中含有的粒子是________。
(2)向氯水中滴入碳酸钠溶液,有气体生成,说明氯水中含有的粒子是________。
(3)在盛有氯水的试管中的有色布条褪色,说明氯水中含有的粒子是________。
(4)将紫色石蕊溶液滴入新制氯水中,溶液显红色,起作用的微粒是________,过一会儿,溶液的颜色褪去,起作用的微粒是________。
(5)向氯水中滴加AgNO3溶液有白色沉淀生成,证明氯水中含有的粒子是________。
(6)氯水经光照后,颜色逐渐消失,并放出的气体是________,溶液的酸性________(填“增强”、“不变”或“减弱”)。
(7)将Cl2通入水中,所得溶液中具有氧化性的含氯微粒是__________。
解析 (1)氯水中含有的微粒有Cl2、HClO、H2O、H+、Cl-、ClO-和OH-,含有Cl2,使溶液呈现黄绿色;(2)滴入Na2CO3溶液有气体生成,证明溶液呈酸性,含H+;(3)氯水能使有色布条褪色,说明具有漂白性,证明氯水中含有HClO;(4)紫色石蕊溶液滴入新制氯水中,溶液呈红色,说明有H+存在,很快褪色,则是因为HClO起漂白作用;(5)向氯水中滴加AgNO3溶液有白色沉淀生成,证明氯水中有Cl-;(6)HClO不稳定,见光易分解放出O2,并生成盐酸,由于HClO为弱酸,而盐酸是强酸,故溶液酸性增强;(7)氯水中的Cl2、ClO-、HClO具有强氧化性。
答案 (1)Cl2 (2)H+ (3)HClO (4)H+ HClO
(5)Cl- (6)O2 增强 (7)Cl2、ClO-、HClO
16、(11分)Cl2是一种重要的化工原料。下图是一些含氯产品。
(1)①中钢瓶上应贴的标签为________。
A.腐蚀品 B.爆炸品
C.有毒品 D.易燃品
(2)下列有关漂白粉和漂白液的说法正确的是________。
A.漂白粉是纯净物,漂白液是混合物
B.漂白粉的有效成分是Ca(ClO)2
C.工业上将氯气通入澄清石灰水制取漂白粉
D.漂白液的有效成分是Na2O2
(3)工业上利用Cl2制盐酸,其化学方程式为_____________________________
________________________________________________________。
Cl2溶于水可制得氯水,检验一瓶氯水是否已经完全变质,可选用的试剂是________。
A.硝酸银溶液 B.酚酞溶液
C.碳酸钠溶液 D.紫色石蕊溶液
解析 (1)Cl2有毒,贮存Cl2的钢瓶应贴的标签为有毒品。
(2)漂白粉的有效成分是Ca(ClO)2,漂白液的有效成分是NaClO,二者均是混合物,A、D项错误;制取漂白粉时,不用澄清石灰水,因氢氧化钙的溶解度较小,一般用石灰乳,也可用氯气与稍湿的消石灰作用制得,C项错误。
(3)久置氯水的成分为稀盐酸,新制氯水的主要成分为Cl2、HCl、HClO,新制氯水和稀盐酸均与AgNO3溶液反应生成白色沉淀,均与Na2CO3溶液反应放出CO2气体,遇酚酞溶液均无明显现象。新制氯水中加入紫色石蕊溶液先变红后褪色,而稀盐酸中加入紫色石蕊溶液只变红色。
答案 (1)C (2)B (3)H2+Cl22HCl D
17、(14分)常温下,A是可用来对自来水进行消毒的黄绿色单质气体,A、B、C、D、E都含X元素,其转化关系如图所示:
(1)请分别写出A、B、D的化学式(如为溶液请填溶质的化学式):
A________、B________、D________。
(2)写出下列反应的化学方程式或离子方程式(请注明条件):
A+H2O(离子方程式):____________________________;
A+NaOH(离子方程式): _____________________;
D→A(化学方程式):________________________。
解析 由题意可知A为氯气,B为次氯酸,D为盐酸,C为氯化钠,E为次氯酸钠。
答案 (1)Cl2 HClO HCl
(2)Cl2+H2O===H++Cl-+HClO
Cl2+2OH-===Cl-+ClO-+H2O
4HCl(浓)+MnO2MnCl2+Cl2↑+2H2O
18、(14分)如图所示是某学生设计的实验室制备并干燥Cl2及吸收多余氯气的实验装置图,请回答:
(1)指出上述图中的各处错误:
①__________________________________________;
②__________________________________________;
③__________________________________________;
④__________________________________________。
(2)在改进后的装置中,下列物质的作用分别是:
①饱和食盐水___________________________________;
②浓硫酸_______________________________________;
③NaOH溶液____________________________________。
(3)制备实验开始时,先检查装置的气密性,接下来的操作依次是________。
A.向烧瓶中加入MnO2粉末
B.加热
C.向烧瓶中加入浓盐酸
(4)如果将过量二氧化锰与含HCl 8.76 g的浓盐酸混合加热,充分反应后生成的氯气明显少于4.26 g。其主要原因有:①_______________________________,
②____________________________________________________。
(5)为了提高浓盐酸的利用率,你对实验的建议是_______________________
_______________________________________________________。
(6)圆底烧瓶中发生反应的离子方程式是____________________________。
实验结束清洗仪器时,为了减少烧瓶中残留氯气对环境的污染,可以向烧瓶中加入的溶液是________,有关的离子方程式是________________________。
解析 (2)先除HCl,后干燥,再收集,最后尾气吸收。(3)检查装置气密性后的操作顺序为先加固体药品,然后加入液体药品,最后加热。(4)题中所给盐酸中HCl的质量是8.76 g,但由于盐酸受热易挥发,且随反应的不断进行,盐酸浓度越来越小,变为稀盐酸后不再与MnO2反应,所以产生的Cl2的质量小于4.26 g。(5)为减少盐酸的挥发,慢慢滴加浓盐酸,用小火加热。(6)利用Cl2和NaOH溶液反应除多余的Cl2。
答案 (1)①不能用稀盐酸,而应用浓盐酸 ②应有加热装置,应用酒精灯加热 ③盛浓硫酸和盛饱和食盐水的洗气瓶位置颠倒 ④两洗气瓶里进气导管和出气导管的长短颠倒
(2)①除去Cl2中的氯化氢 ②除去氯气中的水蒸气
③吸收多余的氯气
(3)ACB
(4)①加热使HCl大量挥发 ②浓盐酸变稀后不再发生反应
(5)将浓盐酸慢慢滴下;加热用小火
(6)MnO2+4H++2Cl-Mn2++Cl2↑+2H2O
NaOH溶液 Cl2+2OH-===Cl-+ClO-+H2O、
H++OH-===H2O
19、(10分)某研究小组为了制备84消毒液(主要成分为NaClO)设计了如图装置。并查阅到下列资料:“卤素与水的反应是放热反应,在加热情况下卤素与碱液发生如下反应:
3X2+6OH-5X-+XO+3H2O”。
回答下列问题:
(1)装置中的试管内发生反应的离子方程式为_________________________
(2)装置中能否省去盛饱和NaCl溶液的洗气瓶?________(填“能”或“不能”,下同),理由是_______________________________。
(3)装置中能否省去盛浓硫酸的洗气瓶?________,理由是__________________。
(4)装置中能否省去盛冰水的烧杯?________,理由是___________________
解析 本题具有较强的综合性,装置产生的Cl2在冰水冷却下与NaOH发生反应制得消毒液。运用该装置必须通过饱和NaCl溶液除去HCl,否则HCl与NaOH反应将生成NaCl,降低NaClO的纯度;但干燥装置可以省略,因为少量水蒸气不会影响反应;冷却装置不可省略,因为题给信息:氯气与水的反应是放热反应,温度升高,引起副反应:3Cl2+6OH-5Cl-+ClO+3H2O。
答案 (1)Cl2+2OH-===Cl-+ClO-+H2O
(2)不能 氯气中混有的HCl气体进入试管中也会和氢氧化钠溶液反应,降低了NaClO的产量和纯度
(3)能 少量水蒸气进入试管中不影响反应
(4)不能 氯气与水的反应是放热反应,反应时温度升高,可能引起副反应,生成NaClO3
10
