2024年中考二轮复习专题《水壶清洁小妙招——酸的化学性质专题复习》 课件(共17张PPT内嵌视频)
文档属性
| 名称 | 2024年中考二轮复习专题《水壶清洁小妙招——酸的化学性质专题复习》 课件(共17张PPT内嵌视频) |

|
|
| 格式 | pptx | ||
| 文件大小 | 24.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-12-16 00:00:00 | ||
图片预览



文档简介
(共17张PPT)
水壶清洁小妙招
—— 酸的化学性质复习专题
生活妙招
问题: 如何除去水垢?
生活中除水垢小妙招
设置情境、提出问题
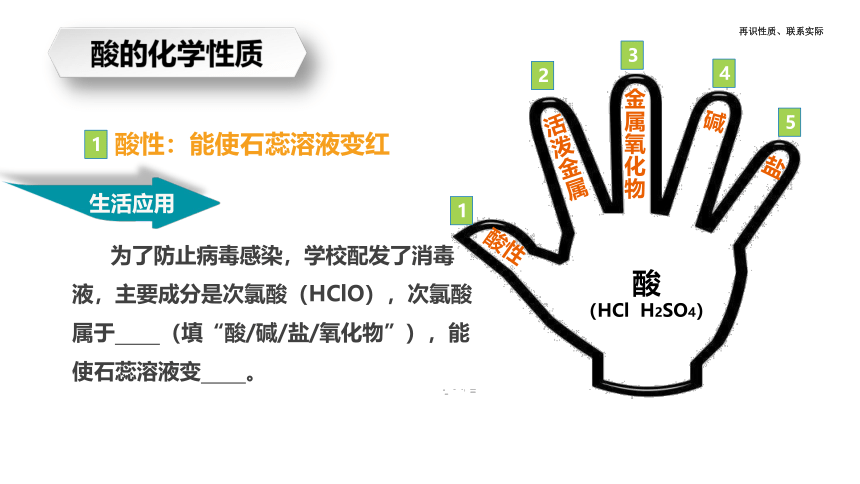
酸的化学性质
活泼金属
金属氧化物
碱
盐
酸
(HCl H2SO4)
酸性
1
5
4
3
2
生活应用
为了防止病毒感染,学校配发了消毒液,主要成分是次氯酸(HClO),次氯酸属于 (填“酸/碱/盐/氧化物”),能使石蕊溶液变 。
酸性:能使石蕊溶液变红
1
再识性质、联系实际
生活应用
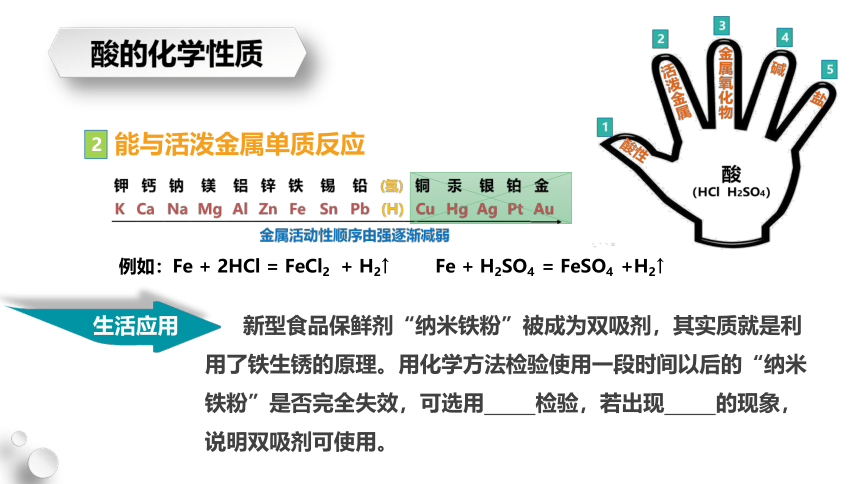
新型食品保鲜剂“纳米铁粉”被成为双吸剂,其实质就是利用了铁生锈的原理。用化学方法检验使用一段时间以后的“纳米铁粉”是否完全失效,可选用 检验,若出现 的现象,说明双吸剂可使用。
能与活泼金属单质反应
2
例如:Fe + 2HCl = FeCl2 + H2↑
Fe + H2SO4 = FeSO4 +H2↑
酸的化学性质
生活应用
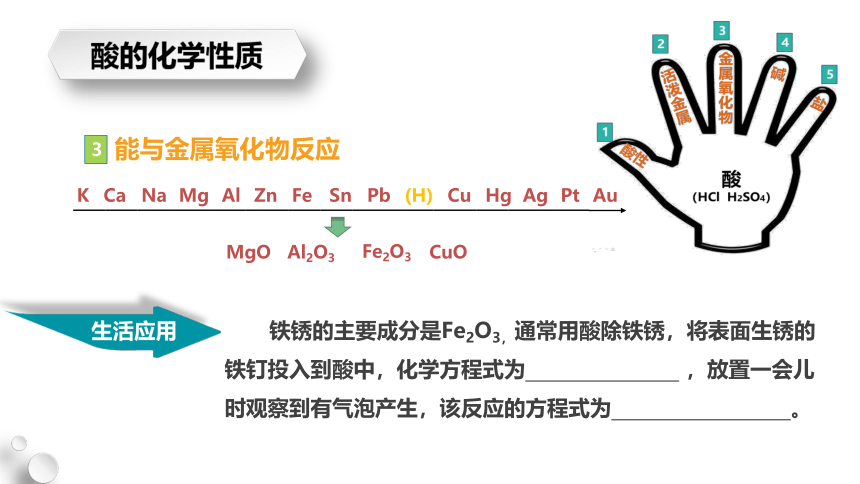
铁锈的主要成分是Fe2O3,通常用酸除铁锈,将表面生锈的铁钉投入到酸中,化学方程式为 ,放置一会儿时观察到有气泡产生,该反应的方程式为 。
能与金属氧化物反应
3
K
Ca
Na
Mg
Al
Zn
Fe
Sn
Pb
(H)
Cu
Hg
Ag
Pt
Au
MgO
Al2O3
Fe2O3
CuO
酸的化学性质
反思交流
能否用NaOH来改良酸性土壤或治疗胃酸过多?
能与碱反应
4
Ca(OH)2
H2SO4
+
=
+
例1—改良酸性土壤
例2—处理盐酸工厂的废水
例3—治疗胃酸过多
例4—蚊虫叮咬后产生的蚁酸用碱性的牙膏或肥皂水涂抹
CaSO4
2H2O
Ca(OH)2
2HCl
+
=
+
CaCl2
2H2O
Al(OH)3
3HCl
+
=
+
AlCl3
3H2O
中和反应实质H++OH- =H2O
酸的化学性质
反思交流
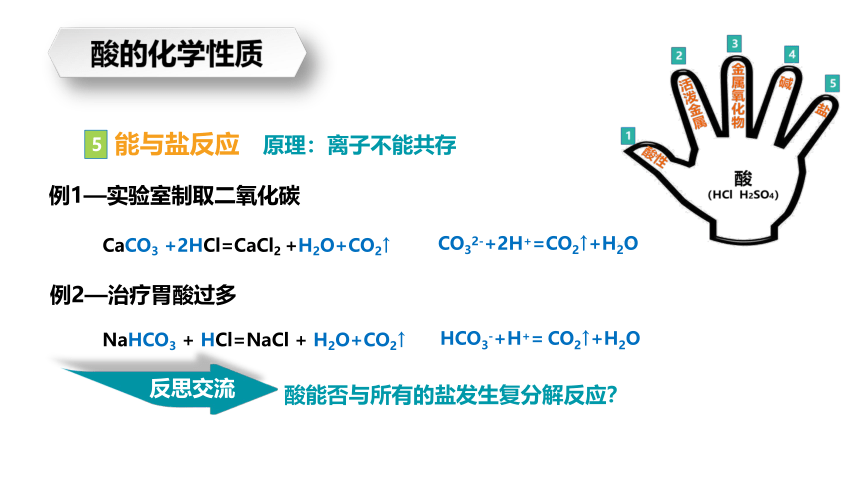
酸能否与所有的盐发生复分解反应?
能与盐反应
5
例1—实验室制取二氧化碳
例2—治疗胃酸过多
原理:离子不能共存
NaHCO3 + HCl=NaCl + H2O+CO2↑
CO32-+2H+=CO2↑+H2O
CaCO3 +2HCl=CaCl2 +H2O+CO2↑
HCO3-+H+= CO2↑+H2O
酸的化学性质
例如:CaCO3 +2HCl=CaCl2 +H2O+CO2↑
酸性:能使石蕊溶液变红
1
反思交流
检验酸常用的方法
能与活泼金属单质反应
2
例如:2HCl +Fe = FeCl2 + H2↑
能与金属氧化物反应
3
能与碱反应
4
能与碳酸盐反应
5
例如:6HCl+2Fe2O3 =2FeCl3 +3H2O
例如:HCl+NaOH=NaCl + H2O
酸的检验
活泼金属
金属氧化物
碱
盐
酸
能使石蕊变红
1
5
4
3
2
Fe
Zn
Fe2O3
CuO
NaOH
Ca(OH)2
CaCO3
Na2CO3
HCl
H2SO4
归纳总结
再识性质、联系实际
探究问题——食醋为什么能去除水垢?
答:醋酸CH3COOH
问题1:水垢的主要成分是什么?
答:CaCO3和Mg(OH)2
问题2:食醋的有效成分是什么?
运用性质、解决问题
探究问题——食醋为什么能去除水垢?
问题3:食醋去除水垢发生的反应是什么?(仿写方程式)
CaCO3 +2 HCl =CaCl2 +H2O+CO2↑
Mg(OH)2 +2 HCl =MgCl2 +2H2O
CaCO3 + CH3COOH =
Mg(OH)2 + CH3COOH=
运用性质、解决问题
解决问题——如何去除水壶表面的铁锈?
问题1:铁锈的主要成分是什么?
答:Fe2O3
问题2:厨房中能与铁锈反应的物质都有什么?
运用性质、解决问题
解决问题——如何去除水壶表面的铁锈?
问题4:酸性物质能否长时间浸泡生锈的铁质水壶?
问题3:寻找除锈最好的物质?
运用性质、解决问题
总结提升——解决生活问题的思路
生活问题
化学知识
目 的
核心物质
物质性质
物质间反应
总结知识、提炼方法
课堂检测
某同学在做氢氧化钠溶液中和稀硫酸的实验时,滴加氢氧化钠溶液前忘记了加入指示剂,导致无法判断中和反应进行的程度,请你参与艾尔肯对加入氢氧化钠溶液后所得溶液酸碱性的探究。
[探究目的] 探究所得溶液的酸碱性和溶质成分
[提出猜想] 猜想一:所得溶液可能显酸性,溶质是 ;
猜想二:所得溶液可能显 性,溶质是Na2SO4;
猜想三:所得溶液可能显碱性,溶质是 。
课堂检测
[实验步骤]
实验操作 实验现象 实验结论
取少量所得溶液于试管中,滴加2滴无色酚酞溶液并振荡 无色溶液变 色 溶液显碱性
无色溶液不变色 溶液显 性
课堂检测
[实验反思] 若加入无色酚酞溶液后不变色,为进一步确定所得溶液中硫酸是否有剩余。请你在除酸碱指示剂外的物质(单质,氧化物,碱,盐)中选择适当的物质完成下表实验。
实验步骤 实验现象 实验结论及化学反应方程式
取所得溶液于试管中, 加入 :____________ 。 硫酸有剩余,溶液显 性,
烧杯中溶液溶质是 。
课内检测、内化提高
课后实践
实践计划: 家庭污垢清除
实践对象: 水壶水垢、铁锅铁锈等
实践策略: 酸的化学性质相关知识
实践人员: 每一位学生
实践评价: 照片、并写出化学原理
课后实践、提升素养
水壶清洁小妙招
—— 酸的化学性质复习专题
生活妙招
问题: 如何除去水垢?
生活中除水垢小妙招
设置情境、提出问题
酸的化学性质
活泼金属
金属氧化物
碱
盐
酸
(HCl H2SO4)
酸性
1
5
4
3
2
生活应用
为了防止病毒感染,学校配发了消毒液,主要成分是次氯酸(HClO),次氯酸属于 (填“酸/碱/盐/氧化物”),能使石蕊溶液变 。
酸性:能使石蕊溶液变红
1
再识性质、联系实际
生活应用
新型食品保鲜剂“纳米铁粉”被成为双吸剂,其实质就是利用了铁生锈的原理。用化学方法检验使用一段时间以后的“纳米铁粉”是否完全失效,可选用 检验,若出现 的现象,说明双吸剂可使用。
能与活泼金属单质反应
2
例如:Fe + 2HCl = FeCl2 + H2↑
Fe + H2SO4 = FeSO4 +H2↑
酸的化学性质
生活应用
铁锈的主要成分是Fe2O3,通常用酸除铁锈,将表面生锈的铁钉投入到酸中,化学方程式为 ,放置一会儿时观察到有气泡产生,该反应的方程式为 。
能与金属氧化物反应
3
K
Ca
Na
Mg
Al
Zn
Fe
Sn
Pb
(H)
Cu
Hg
Ag
Pt
Au
MgO
Al2O3
Fe2O3
CuO
酸的化学性质
反思交流
能否用NaOH来改良酸性土壤或治疗胃酸过多?
能与碱反应
4
Ca(OH)2
H2SO4
+
=
+
例1—改良酸性土壤
例2—处理盐酸工厂的废水
例3—治疗胃酸过多
例4—蚊虫叮咬后产生的蚁酸用碱性的牙膏或肥皂水涂抹
CaSO4
2H2O
Ca(OH)2
2HCl
+
=
+
CaCl2
2H2O
Al(OH)3
3HCl
+
=
+
AlCl3
3H2O
中和反应实质H++OH- =H2O
酸的化学性质
反思交流
酸能否与所有的盐发生复分解反应?
能与盐反应
5
例1—实验室制取二氧化碳
例2—治疗胃酸过多
原理:离子不能共存
NaHCO3 + HCl=NaCl + H2O+CO2↑
CO32-+2H+=CO2↑+H2O
CaCO3 +2HCl=CaCl2 +H2O+CO2↑
HCO3-+H+= CO2↑+H2O
酸的化学性质
例如:CaCO3 +2HCl=CaCl2 +H2O+CO2↑
酸性:能使石蕊溶液变红
1
反思交流
检验酸常用的方法
能与活泼金属单质反应
2
例如:2HCl +Fe = FeCl2 + H2↑
能与金属氧化物反应
3
能与碱反应
4
能与碳酸盐反应
5
例如:6HCl+2Fe2O3 =2FeCl3 +3H2O
例如:HCl+NaOH=NaCl + H2O
酸的检验
活泼金属
金属氧化物
碱
盐
酸
能使石蕊变红
1
5
4
3
2
Fe
Zn
Fe2O3
CuO
NaOH
Ca(OH)2
CaCO3
Na2CO3
HCl
H2SO4
归纳总结
再识性质、联系实际
探究问题——食醋为什么能去除水垢?
答:醋酸CH3COOH
问题1:水垢的主要成分是什么?
答:CaCO3和Mg(OH)2
问题2:食醋的有效成分是什么?
运用性质、解决问题
探究问题——食醋为什么能去除水垢?
问题3:食醋去除水垢发生的反应是什么?(仿写方程式)
CaCO3 +2 HCl =CaCl2 +H2O+CO2↑
Mg(OH)2 +2 HCl =MgCl2 +2H2O
CaCO3 + CH3COOH =
Mg(OH)2 + CH3COOH=
运用性质、解决问题
解决问题——如何去除水壶表面的铁锈?
问题1:铁锈的主要成分是什么?
答:Fe2O3
问题2:厨房中能与铁锈反应的物质都有什么?
运用性质、解决问题
解决问题——如何去除水壶表面的铁锈?
问题4:酸性物质能否长时间浸泡生锈的铁质水壶?
问题3:寻找除锈最好的物质?
运用性质、解决问题
总结提升——解决生活问题的思路
生活问题
化学知识
目 的
核心物质
物质性质
物质间反应
总结知识、提炼方法
课堂检测
某同学在做氢氧化钠溶液中和稀硫酸的实验时,滴加氢氧化钠溶液前忘记了加入指示剂,导致无法判断中和反应进行的程度,请你参与艾尔肯对加入氢氧化钠溶液后所得溶液酸碱性的探究。
[探究目的] 探究所得溶液的酸碱性和溶质成分
[提出猜想] 猜想一:所得溶液可能显酸性,溶质是 ;
猜想二:所得溶液可能显 性,溶质是Na2SO4;
猜想三:所得溶液可能显碱性,溶质是 。
课堂检测
[实验步骤]
实验操作 实验现象 实验结论
取少量所得溶液于试管中,滴加2滴无色酚酞溶液并振荡 无色溶液变 色 溶液显碱性
无色溶液不变色 溶液显 性
课堂检测
[实验反思] 若加入无色酚酞溶液后不变色,为进一步确定所得溶液中硫酸是否有剩余。请你在除酸碱指示剂外的物质(单质,氧化物,碱,盐)中选择适当的物质完成下表实验。
实验步骤 实验现象 实验结论及化学反应方程式
取所得溶液于试管中, 加入 :____________ 。 硫酸有剩余,溶液显 性,
烧杯中溶液溶质是 。
课内检测、内化提高
课后实践
实践计划: 家庭污垢清除
实践对象: 水壶水垢、铁锅铁锈等
实践策略: 酸的化学性质相关知识
实践人员: 每一位学生
实践评价: 照片、并写出化学原理
课后实践、提升素养
同课章节目录
