9.1 溶液的形成 课件(共45张PPT)2022-2023学年九年级化学人教版下册
文档属性
| 名称 | 9.1 溶液的形成 课件(共45张PPT)2022-2023学年九年级化学人教版下册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 78.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-12-17 00:00:00 | ||
图片预览










文档简介
(共45张PPT)
课题1 溶液的形成
九下 化学
人教版
学习目标
新课引入
新知学习
课堂小结
1
2
3
4
学习目标
难点
重点
1.认识溶解现象,知道溶液、溶剂和溶质的概念
2.了解溶液在生活、生产和科学研究中的广泛用途
3.知道物质在溶解过程中通常伴随着热量的变化
4.知道一些常见的乳化现象
5.练习观察、记录和分析实验现象,以及简单实验的设计
重点
地球上的大部分表面被蓝色的海洋覆盖着。海水是又苦又咸的,这是为什么呢?海水是纯净物还是混合物呢?
新课引入
海水中溶解了许多物质,它是一种混合物。
你们知道这些好喝的饮料又是如何制成的吗?
新知学习
Ⅰ 溶液
9-1
实验
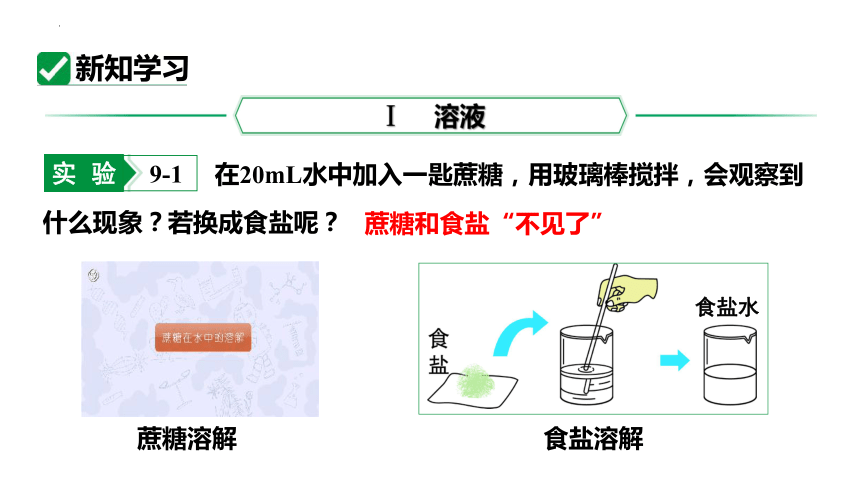
在20mL水中加入一匙蔗糖,用玻璃棒搅拌,会观察到什么现象?若换成食盐呢?
蔗糖溶解
食盐溶解
食盐水
蔗糖和食盐“不见了”
蔗糖去哪儿了——从微观角度分析
蔗糖分子在水分子的作用下,逐步向水中扩散,最终均一地分散到水分子中间。
食盐去哪儿了——从微观角度分析
食盐固体表面的Na+和Cl-在水分子的作用下,逐步向水中扩散,最终均一地分散到水分子中间。
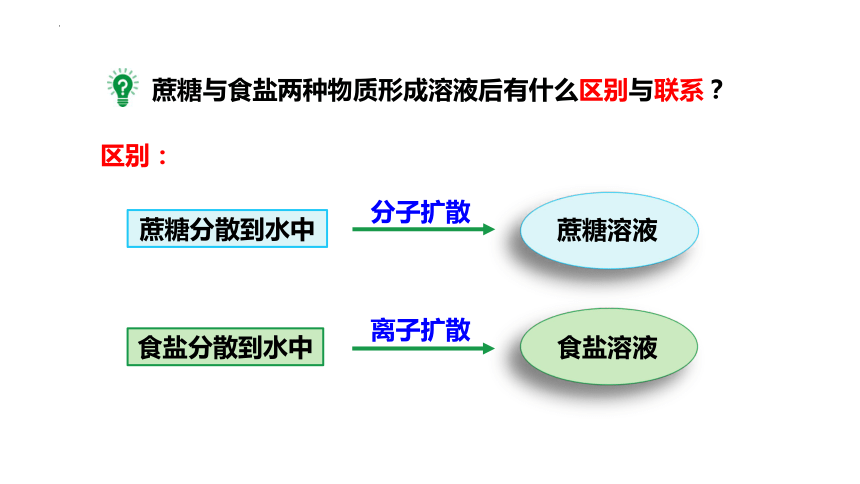
蔗糖与食盐两种物质形成溶液后有什么区别与联系?
区别:
蔗糖分散到水中
食盐分散到水中
蔗糖溶液
食盐溶液
分子扩散
离子扩散
蔗糖与食盐两种物质形成溶液后有什么区别与联系?
联系:
微小的粒子分散到水分子中。
取出溶液中的任意一部分进行比较,发现它们的组成完全相同,即溶液是均一的。
形成溶液后在外界条件不改变时蔗糖与水或氯化钠与水不会分离,即溶液是稳定的。
溶液
一种或几种物质分散到另一种物质里,形成均一、稳定的混合物,叫做溶液。
能溶解其他物质的物质叫做溶剂;
被溶解的物质叫做溶质。
想一想
2.溶液一定是无色透明的吗?
1.溶液的特征是什么?
均一性、稳定性。
不一定。
紫红色
蓝色
浅绿色
黄色
硫酸亚铁溶液
氯化铁溶液
硫酸铜溶液
高锰酸钾溶液
想一想
4.均一、稳定的液体一定是溶液吗?
3.如果加入的是细沙,我们能称它为“细沙溶液”吗?
不能,因为它的成分不是均一的,停止搅拌后细沙会沉淀在杯底,不具有稳定性。
不一定。如水、酒精均不是溶液,它们是纯净物,没有溶解其他物质。
1.溶液的质量
= 溶质的质量+溶剂的质量
2.溶液的体积
≠ 溶质的体积 + 溶剂的体积
溶液、溶质和溶剂之间量的关系
(因为分子之间有间隙)
下列溶液中,溶质和溶剂是什么?
溶液 溶质 溶剂
硫酸铜溶液
蔗糖溶液
食盐溶液
硫酸铜
水
水能溶解很多物质,是一种最常用的溶剂。
蔗糖
水
食盐
水
水能溶解所有的物质吗?除了水还有其他的溶剂吗?
碘和高锰酸钾在汽油或水中的溶解实验
9-2
实验
溶质 溶剂 现象
碘 水
碘 汽油
高锰酸钾 水
高锰酸钾 汽油
几乎不溶于水
溶解,溶液呈棕色
溶解,溶液呈紫红色
不溶于汽油
实验结论
1. 水是一种最常见的溶剂,汽油等也是常用的溶剂;
3. 不同的物质在同一溶剂中的溶解性也是不同的。
2. 同一种物质在不同的溶剂中的溶解性是不同的;
水和乙醇能够互溶吗?
9-3
实验
振荡前现象
振荡后现象
静置后现象
结论
分层
混合均匀
不分层
乙醇与水互溶
在这个实验中,水和乙醇哪个是溶质,哪个是溶剂呢?
体系 溶质 溶剂
气 + 液
固 + 液
液 + 液 无水
有水
气体 液体
固体 液体
量少 量多
非水物质 水
溶液中溶质和溶剂的判断
小试牛刀
溶 液 溶 质 溶 剂
石灰水
碘 酒
稀硫酸
汽 水
硫酸铜溶液
硝酸钾溶液
医用酒精
氢氧化钙 Ca(OH)2
H2O
硫酸铜 CuSO4
硝酸钾 KNO3
酒精 C2H5OH
CO2 等
碘 I2
硫酸 H2SO4
酒精C2H5OH
H2O
H2O
H2O
H2O
H2O
指出下列常见溶液中的溶质和溶剂。
溶液的广泛应用
农业生产上,无土栽培的植物生活在营养液中
化学实验室中的溶液
医疗上用的溶液
食用品中的溶液
1. 溶液在我们的生活中有着广泛的用途,下列物质属于溶液的是
( )
A.泥水 B.食醋
C.冰水混合物 D.牛奶
B
针对训练
2. 下列各组物质里,前者是后者的溶质的是( )
A.生石灰、石灰水
B.酒精、酒精的水溶液
C.盐酸、稀盐酸
D.二氧化碳、碳酸溶液
B
氢氧化钙
氯化氢
碳酸
用潮湿的手触摸食盐时,感觉温度没有明显变化,但触摸洗衣粉时,会有温热的感觉,这是为什么呢?
Ⅱ 溶解时的吸热或放热现象
溶解时的吸热或放热现象
水中加入的溶质 NaCl NH4NO3 NaOH
加入溶质前水的温度/℃
溶解现象
溶质溶解后溶液的温度/℃
固体溶解
固体溶解
固体溶解
24
24
24
21.3
25
32
氯化钠溶解时温度变化不明显;
硝酸铵溶解时温度降低,说明吸收了热量;
氢氧化钠溶解时温度升高,说明放出了热量。
实验结论
溶解过程中的两种变化
溶质分子(或离子)向水中扩散
溶质分子(或离子)和水分子作用生成水合分子(或水合离子)
放出热量
扩散过程
水合过程
吸收热量
若Q吸<Q放,则溶液温度升高;
若Q吸>Q放,则溶液温度降低;
如 NH4NO3
若Q吸=Q放,则溶液温度不变。
如NaOH固体、浓硫酸、生石灰
如NaCl
1. 小琪往如图所示的烧杯中加入一种物质,轻轻搅拌后,粘在烧杯上的塑料片脱落,加入的物质可能是( )
A.食盐 B.硝酸铵
C.氢氧化钠 D.碳酸钙
C
针对训练
日常生活中,衣物上的油污是如何除去的呢?
为什么用洗洁精能去除盘子上的油污呢?
洗发水是怎么使头发变得干净呢?
Ⅲ 乳化现象
乳化现象
9-4
实验
未加洗涤剂:
液体变浑浊,试管内壁沾有油滴
分层
振荡
静置
分层
油与水不能互溶,不能形成溶液,振荡后形成乳状浑浊的液体,静置后分层,用水不能冲洗干净。
实验结论
在油水混合物中加入洗涤剂,振荡后可得到较稳定的乳状浑浊液体,这种液体能被水冲洗干净。
实验结论
加入洗涤剂:
液体变浑浊,有大量泡沫
分层
振荡
静置
不分层
乳浊液
小液滴分散到液体里形成的混合物叫做乳浊液。如水中加入油形成的是乳浊液。
特征:不均一、不稳定、静置后分层。
密度小的在上层,密度大的在下层
洗涤剂能使植物油在水中分散成无数细小的液滴,而不聚集成大的油珠,从而使油和水不再分层,所形成的乳浊液稳定性增强,这种现象称为乳化。
乳化现象
乳化和溶解都是分散,但乳化作用=溶解吗?
乳化作用
溶解
是将大颗粒的油珠变为小颗粒的液滴,最终形成乳浊液
溶解是溶质以分子或离子的形式均匀分散到溶剂中,最终形成溶液
乳化作用和溶解的比较
洗头发(洗发露);洗澡(沐浴露);
清洗餐具上的油污(洗洁精);制农药。
乳化剂的应用
用汽油等溶解油污;
利用洗洁精等乳化剂的乳化作用去除油污;
把厨房中的碱面(即苏打)用热水溶解后与油污发生化学反应。
生活中去除油污的方法主要有三种,原理各不相同。
溶液、悬浊液、乳浊液的比较
常见混合物有溶液和浊液两大体系。溶液是均一、稳定的;
浊液是不均一、不稳定的。
阅读课本P31,总结归纳它们之间的区别和联系。
自主阅读
溶液 悬浊液 乳浊液
定义 一种或几种物质分散到另一种物质里形成的均一稳定的混合物 固体小颗粒悬浮在液体里形成的混合物 小液滴分散在液体里形成的混合物
特征
实例
相同点 均一、稳定
浑浊、不均一、不稳定,静置分层
浑浊、不均一、不稳定,静置分层
食盐水、碘酒
泥水
牛奶
都是混合物
1. 下列洗涤污物的方法属于乳化的是( )
A.用汽油除去衣服上的油污
B.用酒精清洗内壁有碘的试管
C.用水洗去盘子中的水果渣
D.用洗洁精清洗餐具上的油污
D
针对训练
课堂小结
一种或几
种物质
分散
水是
常用
溶剂
溶剂
固
液
气
溶质
另一种
物质
均一稳定的
混合物
溶液
吸热:硝酸铵
放热:浓硫酸、氢氧化钠、生石灰
溶解与乳化
物质溶解时的吸热或放热现象
无明显热现象:氯化钠
乳浊液
乳化剂
应用
乳化作用
1.下列物质分别加入水中,能形成溶液的是( )
A. 泥土 B. 面粉
C. 植物油 D. 蔗糖
D
随堂检测
2. (2022重庆A)王亚平在太空做了油和水“难分难舍”的神奇实验:她用力摇晃装有油和水的瓶子,让油水充分混合、静置,发现油水不分层。下列说法不正确的是( )
A. 太空中水不能作溶剂
B. 在地面油水混合物会产生分层现象
C. 在不同环境中同一实验可能现象不同
D. 在地面向油水混合物中加入洗涤剂会产生乳化现象
A
3. 如图所示,下列胶头滴管内的液体滴入到锥形瓶中,不会引起气球膨胀的是( )
D
选项 A B C D
胶头滴管内液体 H2O2溶液 H2O 稀H2SO4 H2O
锥形瓶内固体 MnO2 CaO Zn NH4NO3
课题1 溶液的形成
九下 化学
人教版
学习目标
新课引入
新知学习
课堂小结
1
2
3
4
学习目标
难点
重点
1.认识溶解现象,知道溶液、溶剂和溶质的概念
2.了解溶液在生活、生产和科学研究中的广泛用途
3.知道物质在溶解过程中通常伴随着热量的变化
4.知道一些常见的乳化现象
5.练习观察、记录和分析实验现象,以及简单实验的设计
重点
地球上的大部分表面被蓝色的海洋覆盖着。海水是又苦又咸的,这是为什么呢?海水是纯净物还是混合物呢?
新课引入
海水中溶解了许多物质,它是一种混合物。
你们知道这些好喝的饮料又是如何制成的吗?
新知学习
Ⅰ 溶液
9-1
实验
在20mL水中加入一匙蔗糖,用玻璃棒搅拌,会观察到什么现象?若换成食盐呢?
蔗糖溶解
食盐溶解
食盐水
蔗糖和食盐“不见了”
蔗糖去哪儿了——从微观角度分析
蔗糖分子在水分子的作用下,逐步向水中扩散,最终均一地分散到水分子中间。
食盐去哪儿了——从微观角度分析
食盐固体表面的Na+和Cl-在水分子的作用下,逐步向水中扩散,最终均一地分散到水分子中间。
蔗糖与食盐两种物质形成溶液后有什么区别与联系?
区别:
蔗糖分散到水中
食盐分散到水中
蔗糖溶液
食盐溶液
分子扩散
离子扩散
蔗糖与食盐两种物质形成溶液后有什么区别与联系?
联系:
微小的粒子分散到水分子中。
取出溶液中的任意一部分进行比较,发现它们的组成完全相同,即溶液是均一的。
形成溶液后在外界条件不改变时蔗糖与水或氯化钠与水不会分离,即溶液是稳定的。
溶液
一种或几种物质分散到另一种物质里,形成均一、稳定的混合物,叫做溶液。
能溶解其他物质的物质叫做溶剂;
被溶解的物质叫做溶质。
想一想
2.溶液一定是无色透明的吗?
1.溶液的特征是什么?
均一性、稳定性。
不一定。
紫红色
蓝色
浅绿色
黄色
硫酸亚铁溶液
氯化铁溶液
硫酸铜溶液
高锰酸钾溶液
想一想
4.均一、稳定的液体一定是溶液吗?
3.如果加入的是细沙,我们能称它为“细沙溶液”吗?
不能,因为它的成分不是均一的,停止搅拌后细沙会沉淀在杯底,不具有稳定性。
不一定。如水、酒精均不是溶液,它们是纯净物,没有溶解其他物质。
1.溶液的质量
= 溶质的质量+溶剂的质量
2.溶液的体积
≠ 溶质的体积 + 溶剂的体积
溶液、溶质和溶剂之间量的关系
(因为分子之间有间隙)
下列溶液中,溶质和溶剂是什么?
溶液 溶质 溶剂
硫酸铜溶液
蔗糖溶液
食盐溶液
硫酸铜
水
水能溶解很多物质,是一种最常用的溶剂。
蔗糖
水
食盐
水
水能溶解所有的物质吗?除了水还有其他的溶剂吗?
碘和高锰酸钾在汽油或水中的溶解实验
9-2
实验
溶质 溶剂 现象
碘 水
碘 汽油
高锰酸钾 水
高锰酸钾 汽油
几乎不溶于水
溶解,溶液呈棕色
溶解,溶液呈紫红色
不溶于汽油
实验结论
1. 水是一种最常见的溶剂,汽油等也是常用的溶剂;
3. 不同的物质在同一溶剂中的溶解性也是不同的。
2. 同一种物质在不同的溶剂中的溶解性是不同的;
水和乙醇能够互溶吗?
9-3
实验
振荡前现象
振荡后现象
静置后现象
结论
分层
混合均匀
不分层
乙醇与水互溶
在这个实验中,水和乙醇哪个是溶质,哪个是溶剂呢?
体系 溶质 溶剂
气 + 液
固 + 液
液 + 液 无水
有水
气体 液体
固体 液体
量少 量多
非水物质 水
溶液中溶质和溶剂的判断
小试牛刀
溶 液 溶 质 溶 剂
石灰水
碘 酒
稀硫酸
汽 水
硫酸铜溶液
硝酸钾溶液
医用酒精
氢氧化钙 Ca(OH)2
H2O
硫酸铜 CuSO4
硝酸钾 KNO3
酒精 C2H5OH
CO2 等
碘 I2
硫酸 H2SO4
酒精C2H5OH
H2O
H2O
H2O
H2O
H2O
指出下列常见溶液中的溶质和溶剂。
溶液的广泛应用
农业生产上,无土栽培的植物生活在营养液中
化学实验室中的溶液
医疗上用的溶液
食用品中的溶液
1. 溶液在我们的生活中有着广泛的用途,下列物质属于溶液的是
( )
A.泥水 B.食醋
C.冰水混合物 D.牛奶
B
针对训练
2. 下列各组物质里,前者是后者的溶质的是( )
A.生石灰、石灰水
B.酒精、酒精的水溶液
C.盐酸、稀盐酸
D.二氧化碳、碳酸溶液
B
氢氧化钙
氯化氢
碳酸
用潮湿的手触摸食盐时,感觉温度没有明显变化,但触摸洗衣粉时,会有温热的感觉,这是为什么呢?
Ⅱ 溶解时的吸热或放热现象
溶解时的吸热或放热现象
水中加入的溶质 NaCl NH4NO3 NaOH
加入溶质前水的温度/℃
溶解现象
溶质溶解后溶液的温度/℃
固体溶解
固体溶解
固体溶解
24
24
24
21.3
25
32
氯化钠溶解时温度变化不明显;
硝酸铵溶解时温度降低,说明吸收了热量;
氢氧化钠溶解时温度升高,说明放出了热量。
实验结论
溶解过程中的两种变化
溶质分子(或离子)向水中扩散
溶质分子(或离子)和水分子作用生成水合分子(或水合离子)
放出热量
扩散过程
水合过程
吸收热量
若Q吸<Q放,则溶液温度升高;
若Q吸>Q放,则溶液温度降低;
如 NH4NO3
若Q吸=Q放,则溶液温度不变。
如NaOH固体、浓硫酸、生石灰
如NaCl
1. 小琪往如图所示的烧杯中加入一种物质,轻轻搅拌后,粘在烧杯上的塑料片脱落,加入的物质可能是( )
A.食盐 B.硝酸铵
C.氢氧化钠 D.碳酸钙
C
针对训练
日常生活中,衣物上的油污是如何除去的呢?
为什么用洗洁精能去除盘子上的油污呢?
洗发水是怎么使头发变得干净呢?
Ⅲ 乳化现象
乳化现象
9-4
实验
未加洗涤剂:
液体变浑浊,试管内壁沾有油滴
分层
振荡
静置
分层
油与水不能互溶,不能形成溶液,振荡后形成乳状浑浊的液体,静置后分层,用水不能冲洗干净。
实验结论
在油水混合物中加入洗涤剂,振荡后可得到较稳定的乳状浑浊液体,这种液体能被水冲洗干净。
实验结论
加入洗涤剂:
液体变浑浊,有大量泡沫
分层
振荡
静置
不分层
乳浊液
小液滴分散到液体里形成的混合物叫做乳浊液。如水中加入油形成的是乳浊液。
特征:不均一、不稳定、静置后分层。
密度小的在上层,密度大的在下层
洗涤剂能使植物油在水中分散成无数细小的液滴,而不聚集成大的油珠,从而使油和水不再分层,所形成的乳浊液稳定性增强,这种现象称为乳化。
乳化现象
乳化和溶解都是分散,但乳化作用=溶解吗?
乳化作用
溶解
是将大颗粒的油珠变为小颗粒的液滴,最终形成乳浊液
溶解是溶质以分子或离子的形式均匀分散到溶剂中,最终形成溶液
乳化作用和溶解的比较
洗头发(洗发露);洗澡(沐浴露);
清洗餐具上的油污(洗洁精);制农药。
乳化剂的应用
用汽油等溶解油污;
利用洗洁精等乳化剂的乳化作用去除油污;
把厨房中的碱面(即苏打)用热水溶解后与油污发生化学反应。
生活中去除油污的方法主要有三种,原理各不相同。
溶液、悬浊液、乳浊液的比较
常见混合物有溶液和浊液两大体系。溶液是均一、稳定的;
浊液是不均一、不稳定的。
阅读课本P31,总结归纳它们之间的区别和联系。
自主阅读
溶液 悬浊液 乳浊液
定义 一种或几种物质分散到另一种物质里形成的均一稳定的混合物 固体小颗粒悬浮在液体里形成的混合物 小液滴分散在液体里形成的混合物
特征
实例
相同点 均一、稳定
浑浊、不均一、不稳定,静置分层
浑浊、不均一、不稳定,静置分层
食盐水、碘酒
泥水
牛奶
都是混合物
1. 下列洗涤污物的方法属于乳化的是( )
A.用汽油除去衣服上的油污
B.用酒精清洗内壁有碘的试管
C.用水洗去盘子中的水果渣
D.用洗洁精清洗餐具上的油污
D
针对训练
课堂小结
一种或几
种物质
分散
水是
常用
溶剂
溶剂
固
液
气
溶质
另一种
物质
均一稳定的
混合物
溶液
吸热:硝酸铵
放热:浓硫酸、氢氧化钠、生石灰
溶解与乳化
物质溶解时的吸热或放热现象
无明显热现象:氯化钠
乳浊液
乳化剂
应用
乳化作用
1.下列物质分别加入水中,能形成溶液的是( )
A. 泥土 B. 面粉
C. 植物油 D. 蔗糖
D
随堂检测
2. (2022重庆A)王亚平在太空做了油和水“难分难舍”的神奇实验:她用力摇晃装有油和水的瓶子,让油水充分混合、静置,发现油水不分层。下列说法不正确的是( )
A. 太空中水不能作溶剂
B. 在地面油水混合物会产生分层现象
C. 在不同环境中同一实验可能现象不同
D. 在地面向油水混合物中加入洗涤剂会产生乳化现象
A
3. 如图所示,下列胶头滴管内的液体滴入到锥形瓶中,不会引起气球膨胀的是( )
D
选项 A B C D
胶头滴管内液体 H2O2溶液 H2O 稀H2SO4 H2O
锥形瓶内固体 MnO2 CaO Zn NH4NO3
同课章节目录
