高中化学必修第二册《第一节 认识有机化合物》ppt课件(共18张PPT)
文档属性
| 名称 | 高中化学必修第二册《第一节 认识有机化合物》ppt课件(共18张PPT) |

|
|
| 格式 | ppt | ||
| 文件大小 | 5.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-12-18 00:00:00 | ||
图片预览






文档简介
(共18张PPT)
第七章 第一节 认识有机化合物
1.了解烷烃的主要物理性质和化学性质,培养“变化观念与平衡思想”的
素养。
2.熟练掌握甲烷的主要性质,提高“证据推理与模型认知”能力。
3.认识取代反应的概念及特点,培养“微观探析及变化观念”。
核心素养发展目标
1.烷烃的物理性质
知识梳理
相似性 递变性(随分子中碳原子数增加)
熔、沸点 较低 逐渐_____
密度 比水___ 逐渐_____
状态 气态→液态→固态,常温常压下分子中碳原子数n≤4的烷烃为气态(常温常压下,新戊烷为气态)
溶解性 难溶于 ,易溶于汽油等_________
升高
增大
小
水
有机溶剂
2.化学性质
(1)稳定性:通常条件下与 、 或 等强氧化剂不反应。
(2)可燃性:烷烃都能燃烧。
CH4燃烧方程式:________________________
C3H8燃烧方程式:__________________________
链状烷烃燃烧通式:_____________________________________
强酸
强碱
高锰酸钾
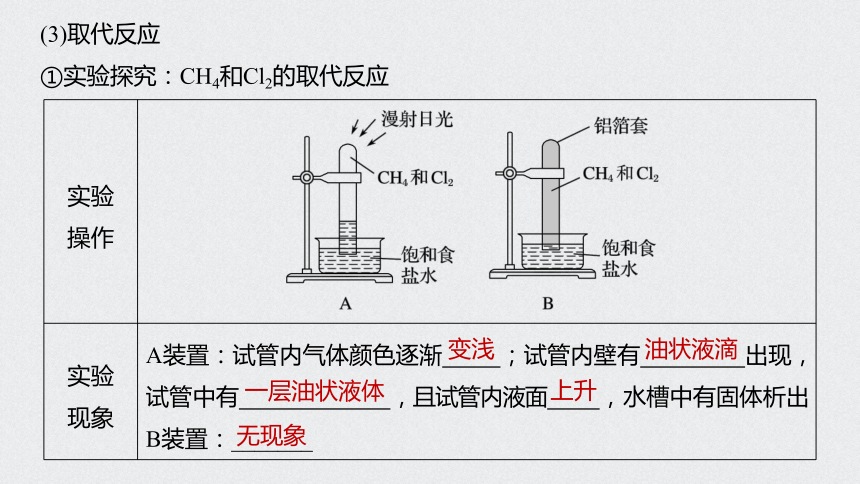
(3)取代反应
①实验探究:CH4和Cl2的取代反应
实验
操作
实验
现象 A装置:试管内气体颜色逐渐 ;试管内壁有 出现,试管中有 ,且试管内液面 ,水槽中有固体析出
B装置:_______
变浅
油状液滴
一层油状液体
上升
无现象
实验
结论 CH4与Cl2在 条件下发生化学反应,有关化学方程式为:
________________________;
__________________________;
__________________________;
________________________
光照
②甲烷的四种氯代产物的性质。
a.水溶性:CH3Cl、CH2Cl2、CHCl3、CCl4均 。
b.状态:常温下除CH3Cl是 ,其余三种均为 。
③取代反应:有机物分子里的 被其他 所替代的反应。
(4)分解反应:烷烃在较高的温度下会发生分解。
不溶于水
气体
油状液体
某些原子或原子团
原子或原子团
(1)C4H10的熔、沸点比CH4的熔、沸点高( )
(2)常温常压下,C3H8、C4H10和C6H14都呈液态( )
√
×
判断正误
提示 常温常压下,分子中碳原子数n≤4的烷烃为气态,故C6H14为液态。
提示 CH4和Cl2发生取代反应生成物除CH3Cl和HCl外,还有CH2Cl2、CHCl3、CCl4。
(3)烷烃的密度都小于水的密度( )
(4)乙烷也可以和氯气在光照条件下,发生取代反应( )
(5)CH4和Cl2按体积比1∶1混合,发生取代反应生成的产物只有两种( )
√
√
×
1.CH4和Cl2发生取代反应中,产物的物质的量最多的是什么?如1 mol CH4和Cl2发生取代反应,生成的氯代物的物质的量相等,则消耗的氯气为多少摩尔?
提示 产物中最多的为HCl,根据取代反应的特点,每取代一个氢原子,则消耗一个氯气分子,故生成1 mol CH3Cl、CH2Cl2、CHCl3、CCl4所消耗的氯气为1 mol、2 mol、3 mol、4 mol,则1 mol CH4和Cl2反应生成等物质的量的氯代物消耗的氯气为0.25×(1+2+3+4) mol=2.5 mol。
深度思考
2.乙烷和甲烷性质相似,乙烷和氯气按体积比1∶1混合,光照条件下能生成纯净的一氯乙烷吗?
提示 不能,因为烷烃和氯气的反应是连锁反应,故乙烷分子中的氢原子是被氯原子逐步取代,故产物是一氯乙烷到六氯乙烷和HCl的混合物,不能得到纯净的一氯乙烷。
归纳总结
烷烃(以甲烷为例)发生取代反应的有关规律
(1)反应条件:反应条件为光照,其光照为漫射光,强光直射易发生爆炸。
(2)反应物:反应物为卤素单质,如甲烷与氯水、溴水不反应,但可以与氯气、溴蒸气发生取代反应。
(3)反应产物:虽然反应物的比例、反应的时间长短等因素会造成各种产物的比例不同,但甲烷与氯气反应生成的产物都是CH3Cl、CH2Cl2、CHCl3和CCl4四种有机物与HCl形成的混合物。反应产物中HCl的物质的量最多。
(4)反应特点
①连锁反应
甲烷分子中的氢原子被氯原子逐步取代,第一步反应一旦开始,后续反应立即进行,且各步反应可同时进行。即当n(CH4)∶n(Cl2)=1∶1时,并
不只发生反应CH4+Cl2 CH3Cl+HCl,其他反应也在进行。
②数量关系
CH4与Cl2发生取代反应时,每有1 mol H被取代,则消耗1 mol Cl2,同时生成1 mol HCl,即n(Cl2)=n(H)=n(HCl)。1 mol CH4与Cl2发生取代反应,最多消耗4 mol Cl2。
1.(2019·济南月考)下列关于烷烃性质的叙述正确的是
A.烷烃的沸点随碳原子数增加而逐渐降低
B.烷烃易被酸性高锰酸钾溶液氧化
C.在光照条件下,烷烃易与溴水发生取代反应
D.烷烃的卤代反应很难得到纯净的产物
跟踪强化
1
2
3
4
√
解析 烷烃的沸点一般随碳原子数增加而逐渐升高,A项错误;
烷烃通常情况下性质稳定,不与酸性高锰酸钾溶液反应,B项错误;
在光照条件下,烷烃只能与纯净的卤素单质发生取代反应,不与溴水反应,C项错误;
由于卤素原子取代烷烃分子中氢原子的位置和个数难以控制,故很难得到纯净的产物,D项正确。
1
3
4
2
2.几种烷烃的沸点如下:
解析 随着碳原子数的增加,烷烃的沸点逐渐升高,丙烷的沸点应介于乙烷和丁烷的沸点之间。
1
2
3
4
烷烃 甲烷 乙烷 丁烷 戊烷
沸点/℃ -162 -89 -1 36
根据以上数据推断丙烷的沸点可能是
A.约-40 ℃ B.低于-162 ℃
C.低于-89 ℃ D.高于36 ℃
√
3.若甲烷与氯气以物质的量之比1∶3混合,在光照下得到的有机产物:①CH3Cl,②CH2Cl2,③CHCl3,④CCl4,其中正确的是
A.只有① B.只有③
C.①②③的混合物 D.①②③④的混合物
解析 CH4和Cl2的取代反应为连锁反应,无论两者的物质的量之比为多少,其产物都是HCl和CH3Cl、CH2Cl2、CHCl3、CCl4的混合物,故选D。
1
3
4
√
2
4.(2018·上海静安区高一检测)将体积比为1∶4的甲烷与氯气混合于一集气瓶中,加盖后置于光亮处,下列有关此实验的现象和结论叙述不正确的是
A.产物中只有四氯化碳分子是正四面体结构
B.瓶中气体的黄绿色逐渐变浅,瓶内壁有油状液滴形成
C.若日光直射,可能发生爆炸
D.生成物只有CCl4、HCl
1
3
4
√
2
解析 A项,CCl4与CH4结构一样,为正四面体,正确。
B项,CH4与Cl2反应消耗Cl2,所以黄绿色逐渐变浅,反应生成的CH2Cl2、CHCl3、CCl4都是油状液体,正确。
C项,若日光直射,反应剧烈,放出大量的热,气体体积膨胀,可能发生爆炸,正确。
D项,CH4与Cl2反应,生成CH3Cl、CH2Cl2、CHCl3、CCl4和HCl,错误。
1
3
4
2
第七章 第一节 认识有机化合物
1.了解烷烃的主要物理性质和化学性质,培养“变化观念与平衡思想”的
素养。
2.熟练掌握甲烷的主要性质,提高“证据推理与模型认知”能力。
3.认识取代反应的概念及特点,培养“微观探析及变化观念”。
核心素养发展目标
1.烷烃的物理性质
知识梳理
相似性 递变性(随分子中碳原子数增加)
熔、沸点 较低 逐渐_____
密度 比水___ 逐渐_____
状态 气态→液态→固态,常温常压下分子中碳原子数n≤4的烷烃为气态(常温常压下,新戊烷为气态)
溶解性 难溶于 ,易溶于汽油等_________
升高
增大
小
水
有机溶剂
2.化学性质
(1)稳定性:通常条件下与 、 或 等强氧化剂不反应。
(2)可燃性:烷烃都能燃烧。
CH4燃烧方程式:________________________
C3H8燃烧方程式:__________________________
链状烷烃燃烧通式:_____________________________________
强酸
强碱
高锰酸钾
(3)取代反应
①实验探究:CH4和Cl2的取代反应
实验
操作
实验
现象 A装置:试管内气体颜色逐渐 ;试管内壁有 出现,试管中有 ,且试管内液面 ,水槽中有固体析出
B装置:_______
变浅
油状液滴
一层油状液体
上升
无现象
实验
结论 CH4与Cl2在 条件下发生化学反应,有关化学方程式为:
________________________;
__________________________;
__________________________;
________________________
光照
②甲烷的四种氯代产物的性质。
a.水溶性:CH3Cl、CH2Cl2、CHCl3、CCl4均 。
b.状态:常温下除CH3Cl是 ,其余三种均为 。
③取代反应:有机物分子里的 被其他 所替代的反应。
(4)分解反应:烷烃在较高的温度下会发生分解。
不溶于水
气体
油状液体
某些原子或原子团
原子或原子团
(1)C4H10的熔、沸点比CH4的熔、沸点高( )
(2)常温常压下,C3H8、C4H10和C6H14都呈液态( )
√
×
判断正误
提示 常温常压下,分子中碳原子数n≤4的烷烃为气态,故C6H14为液态。
提示 CH4和Cl2发生取代反应生成物除CH3Cl和HCl外,还有CH2Cl2、CHCl3、CCl4。
(3)烷烃的密度都小于水的密度( )
(4)乙烷也可以和氯气在光照条件下,发生取代反应( )
(5)CH4和Cl2按体积比1∶1混合,发生取代反应生成的产物只有两种( )
√
√
×
1.CH4和Cl2发生取代反应中,产物的物质的量最多的是什么?如1 mol CH4和Cl2发生取代反应,生成的氯代物的物质的量相等,则消耗的氯气为多少摩尔?
提示 产物中最多的为HCl,根据取代反应的特点,每取代一个氢原子,则消耗一个氯气分子,故生成1 mol CH3Cl、CH2Cl2、CHCl3、CCl4所消耗的氯气为1 mol、2 mol、3 mol、4 mol,则1 mol CH4和Cl2反应生成等物质的量的氯代物消耗的氯气为0.25×(1+2+3+4) mol=2.5 mol。
深度思考
2.乙烷和甲烷性质相似,乙烷和氯气按体积比1∶1混合,光照条件下能生成纯净的一氯乙烷吗?
提示 不能,因为烷烃和氯气的反应是连锁反应,故乙烷分子中的氢原子是被氯原子逐步取代,故产物是一氯乙烷到六氯乙烷和HCl的混合物,不能得到纯净的一氯乙烷。
归纳总结
烷烃(以甲烷为例)发生取代反应的有关规律
(1)反应条件:反应条件为光照,其光照为漫射光,强光直射易发生爆炸。
(2)反应物:反应物为卤素单质,如甲烷与氯水、溴水不反应,但可以与氯气、溴蒸气发生取代反应。
(3)反应产物:虽然反应物的比例、反应的时间长短等因素会造成各种产物的比例不同,但甲烷与氯气反应生成的产物都是CH3Cl、CH2Cl2、CHCl3和CCl4四种有机物与HCl形成的混合物。反应产物中HCl的物质的量最多。
(4)反应特点
①连锁反应
甲烷分子中的氢原子被氯原子逐步取代,第一步反应一旦开始,后续反应立即进行,且各步反应可同时进行。即当n(CH4)∶n(Cl2)=1∶1时,并
不只发生反应CH4+Cl2 CH3Cl+HCl,其他反应也在进行。
②数量关系
CH4与Cl2发生取代反应时,每有1 mol H被取代,则消耗1 mol Cl2,同时生成1 mol HCl,即n(Cl2)=n(H)=n(HCl)。1 mol CH4与Cl2发生取代反应,最多消耗4 mol Cl2。
1.(2019·济南月考)下列关于烷烃性质的叙述正确的是
A.烷烃的沸点随碳原子数增加而逐渐降低
B.烷烃易被酸性高锰酸钾溶液氧化
C.在光照条件下,烷烃易与溴水发生取代反应
D.烷烃的卤代反应很难得到纯净的产物
跟踪强化
1
2
3
4
√
解析 烷烃的沸点一般随碳原子数增加而逐渐升高,A项错误;
烷烃通常情况下性质稳定,不与酸性高锰酸钾溶液反应,B项错误;
在光照条件下,烷烃只能与纯净的卤素单质发生取代反应,不与溴水反应,C项错误;
由于卤素原子取代烷烃分子中氢原子的位置和个数难以控制,故很难得到纯净的产物,D项正确。
1
3
4
2
2.几种烷烃的沸点如下:
解析 随着碳原子数的增加,烷烃的沸点逐渐升高,丙烷的沸点应介于乙烷和丁烷的沸点之间。
1
2
3
4
烷烃 甲烷 乙烷 丁烷 戊烷
沸点/℃ -162 -89 -1 36
根据以上数据推断丙烷的沸点可能是
A.约-40 ℃ B.低于-162 ℃
C.低于-89 ℃ D.高于36 ℃
√
3.若甲烷与氯气以物质的量之比1∶3混合,在光照下得到的有机产物:①CH3Cl,②CH2Cl2,③CHCl3,④CCl4,其中正确的是
A.只有① B.只有③
C.①②③的混合物 D.①②③④的混合物
解析 CH4和Cl2的取代反应为连锁反应,无论两者的物质的量之比为多少,其产物都是HCl和CH3Cl、CH2Cl2、CHCl3、CCl4的混合物,故选D。
1
3
4
√
2
4.(2018·上海静安区高一检测)将体积比为1∶4的甲烷与氯气混合于一集气瓶中,加盖后置于光亮处,下列有关此实验的现象和结论叙述不正确的是
A.产物中只有四氯化碳分子是正四面体结构
B.瓶中气体的黄绿色逐渐变浅,瓶内壁有油状液滴形成
C.若日光直射,可能发生爆炸
D.生成物只有CCl4、HCl
1
3
4
√
2
解析 A项,CCl4与CH4结构一样,为正四面体,正确。
B项,CH4与Cl2反应消耗Cl2,所以黄绿色逐渐变浅,反应生成的CH2Cl2、CHCl3、CCl4都是油状液体,正确。
C项,若日光直射,反应剧烈,放出大量的热,气体体积膨胀,可能发生爆炸,正确。
D项,CH4与Cl2反应,生成CH3Cl、CH2Cl2、CHCl3、CCl4和HCl,错误。
1
3
4
2
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
