2024中考化学 第一部分 成都中考考点研究 第三单元 物质构成的奥秘 课件 (共33张PPT)
文档属性
| 名称 | 2024中考化学 第一部分 成都中考考点研究 第三单元 物质构成的奥秘 课件 (共33张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 764.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-12-20 00:00:00 | ||
图片预览







文档简介
(共33张PPT)
第三单元 物质构成的
奥秘
考点特训营
2
纵横过实验 · 纵向实验逐个过
3
1
成都10年真题子母题+2年诊断检测
成都10年真题子母题+2年诊断检测
命题点
1
构成物质的微粒(10年3考)
1. (成都真题组合)(1)C60这种物质是由_____(填“分子”或“原子”)构成。[2016成都15(1)②题1分]
(2)C60分子是由_______构成的。[2014成都15(1)③题1分]
分子
碳原子
命题点
2
微粒的性质(10年9考)
2. (2019成都5题3分)下列事例不能用分子的相关知识解释的是( )
A. 品红溶解
B. 篮球充气
C. 酒精挥发
D. 柳絮飞扬
D
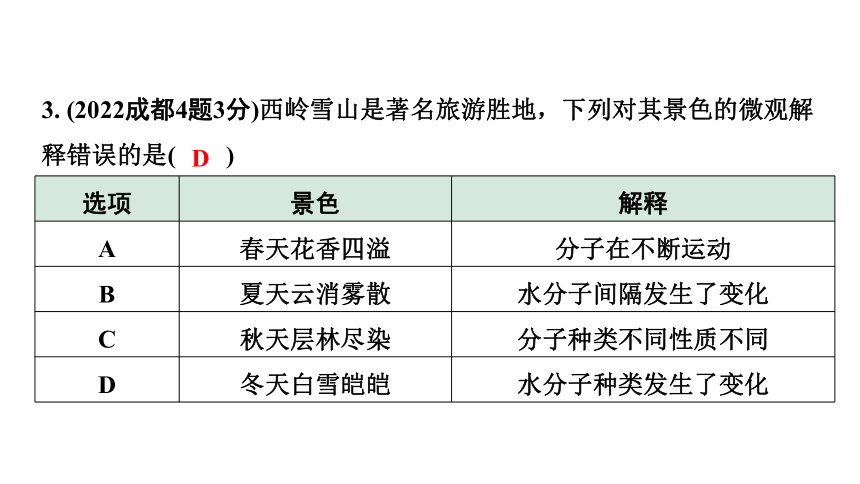
3. (2022成都4题3分)西岭雪山是著名旅游胜地,下列对其景色的微观解释错误的是( )
选项 景色 解释
A 春天花香四溢 分子在不断运动
B 夏天云消雾散 水分子间隔发生了变化
C 秋天层林尽染 分子种类不同性质不同
D 冬天白雪皑皑 水分子种类发生了变化
D
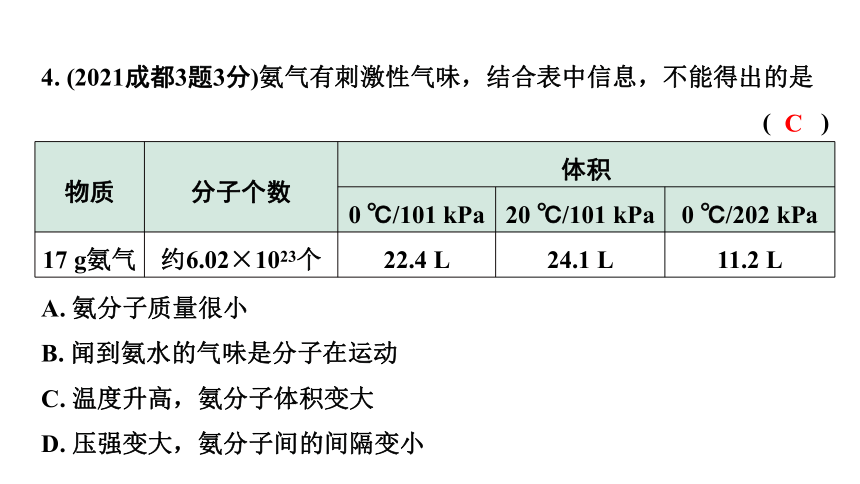
4. (2021成都3题3分)氨气有刺激性气味,结合表中信息,不能得出的是
( )
物质 分子个数 体积 0 ℃/101 kPa 20 ℃/101 kPa 0 ℃/202 kPa
17 g氨气 约6.02×1023个 22.4 L 24.1 L 11.2 L
A. 氨分子质量很小
B. 闻到氨水的气味是分子在运动
C. 温度升高,氨分子体积变大
D. 压强变大,氨分子间的间隔变小
C
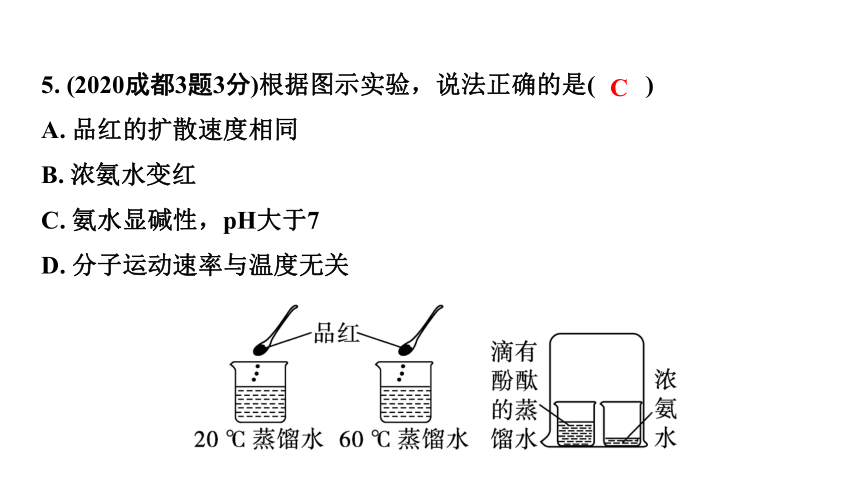
5. (2020成都3题3分)根据图示实验,说法正确的是( )
A. 品红的扩散速度相同
B. 浓氨水变红
C. 氨水显碱性,pH大于7
D. 分子运动速率与温度无关
C
6. (2015成都10题3分)两种微粒的结构示意图是Na 和Na+ ,其中相同的是( )
A. 电子数
B. 质子数
C. 电子层数
D. 所带电荷数
命题点
3
微粒结构示意图(10年5考)
B
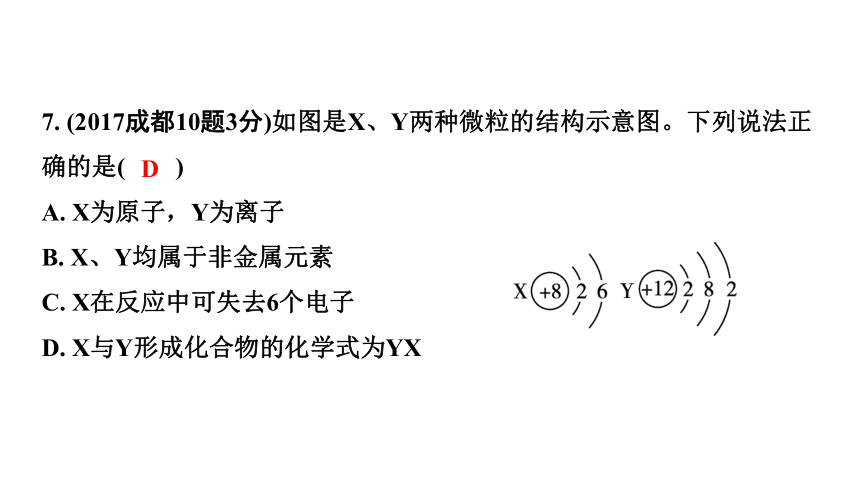
7. (2017成都10题3分)如图是X、Y两种微粒的结构示意图。下列说法正确的是( )
A. X为原子,Y为离子
B. X、Y均属于非金属元素
C. X在反应中可失去6个电子
D. X与Y形成化合物的化学式为YX
D
命题点
4
相对原子质量(2023.11)
8. (2023成都11题3分)化学家张青莲主持测定了铟、铱、锌等元素相对原子质量的新值。碳-12原子的质量为1.993×10-26 kg,一种锌原子的质量为1.096×10-25 kg,该锌原子的相对原子质量是( )
A. 12 B. 64
C. 66 D. 1.096×10-25 kg
C
命题点
5
元素与元素周期表(10年9考)
9. (2018成都7题3分)钕玻璃是激光聚变装置的核心元件。根据元素周期表中钕的信息判断错误的是( )
A. 属于金属元素
B. 质子数为60
C. 中子数为60
D. 相对原子质量是144.2
C
10. (2017成都8题改编3分)2017年5月9日,我国发布了四种人造新元素的中文名称,其中115号镆元素的“镆”取自古代剑名“镆铘”,下列说法不正确的是( )
A. 镆原子的核外电子数为115
B. 镆铘剑含有镆元素
C. 镆原子的质子数为115
D. 镆铘剑由合金铸造
B
11. (2019成都7题3分)2019年是元素周期表诞生第150周年。如图是元素周期表的一部分,从表中不能获取的信息是( )
A. 元素在周期表中的位置 B. 原子的质子数
C. 元素的相对原子质量 D. 原子的中子数
D
12. [2017成都15(2)①题1分]营养成分表中的“钠”是指_____(填“元素”或“单质”)。
13. [2019成都15(4)题2分]将太阳能转化为电能的常用材料是硅。硅属于_______(填“金属”或“非金属”)元素,它在地壳里的含量居第_______位。
元素
非金属
二(或2)
14. (2021成都7题改编3分)科学家利用“基因剪刀”技术降低了水稻中砷的含量。结合图示,有关砷的说法正确的是( )
A. 属于金属元素
B. 最外层电子数为33
C. 原子质量为74.92 g
D. 表示原子核及核电荷数
元素周期表与原子结构示意图(10年3考)
命题点
6
D
物质构成的奥秘
思维导图
元素及元素周期表
元素
符号
元素周期表
含量
分类
构成物质的微观粒子
性质
分子运动现象的探究
原子的构成
相对原子质量
分类
意义
阳离子
阴离子
原子
分子
离子
组合
分裂
得失电子
表示
原子和离子之间的区别与联系
考点特训营
一、构成物质的微观粒子
分子
性质
定义:由分子构成的物质,分子是保持物质_________的最小粒子
a.小:分子的_____和_____都很小,如一个水分子的质量约是
3×10-26 kg
b.动:分子总是在___________。温度越高,分子运动速率越___。
如:湿衣服在阳光下比阴凉处干得快
化学性质
体积
质量
不断运动着
快
一、构成物质的微观粒子
分子
性质
c.间:分子之间有_____。温度升高,间隔变大;压强增大,间隔变
小。例如:热胀冷缩、气体可压缩储存于钢瓶中
d.同:同种物质分子的化学性质_____,不同种物质分子的化学性质
_____。如液氧与氧气化学性质相同
间隔
相同
不同
分子运动现象的探究(详见纵横过实验)
一、构成物质的微观粒子
原子
原子的构成
构成
定义:_________中的最小粒子
原子核
质子:每个质子带1个单位___电荷
_____:不带电
数量关系:核电荷数=质子数=核外电子数=原子序数
_________:每个电子带1个单位___电荷
化学变化
正
中子
核外电子
负
原子
原子的构成
一、构成物质的微观粒子
原子核外电子排布
原子结构示意图:
(以钠原子为例)
弧线表示电子层,电子层数等于元素所在周期数
数字表示各电子层上容纳的_______
表示最外层电子数,与元素的________密切相关
圆圈表示_______,圈内的数字表示_________,
决定元素的_____
电子数
化学性质
原子核
核电荷数
种类
原子
原子的构成
一、构成物质的微观粒子
原子核外电子排布
最外层电子数(n)的应用
最外层电子数 原子得失电子(一般情况下)
n<4(氦、硼除外) 易_____电子
4≤n<8 易_____电子
n=8(氦为2) 不易得失电子(相对稳定结构)
失去
得到
原子的最外层电子数相等,对应元素的化学性质相似(H、
He除外)
___________________
_______________________
表达式:相对原子质量=
单位为“1”,一般省略不写
原子
一、构成物质的微观粒子
相对原子质量
一个原子的实际质量
一个碳-12原子质量的
离子
定义:带电的原子或原子团
表示:在元素符号的右上角用“+”或“-”号表示离子的电性,数字表示一个离
子所带的电荷数,先写_____,后写_______,数字为“1”时可省略不写
数字
正负号
__________
一、构成物质的微观粒子
离子
分类
阳离子:带_______的原子(或原子团),如Ca2+、 等
阴离子:带_______的原子(或原子团),如Cl-、 等
正电荷
负电荷
意义:
____________________________
每个镁离子带两个单位的正电荷
两个镁离子
一、构成物质的微观粒子
原子和离子之间的区别与联系
区别和联系 原子 离子 _______ _______
结构示意图
粒子符号 Na ____ ____
质子数与核外 电子数的关系 质子数=核外电子数 质子数>核外电子数 质子数<核外电子数
阳离子
阴离子
Na+
Cl-
二、元素及元素周期表
元素
定义:_______(即核电荷数)相同的一类原子的总称
含量:地壳中含量居于前四位的元素:______>______>______>______
分类
金属元素:“钅”字旁(金、汞除外),如钠、镁
非金属元素:“ ”字旁、“氵”字旁、“ ”字头,如硅、溴、氧
稀有气体元素:氦、氖、氩、氪、氙和氡
质子数
氧(O)
硅(Si)
铝(Al)
铁(Fe)
意义
宏观
微观
二、元素及元素周期表
元素
符号
书写(“一大二小”):元素符号由两个字母组成时,第一个字母要_____,
第二个字母要_____,如Na、Cu
表示一种元素,如Fe表示_______
表示由原子构成的一种物质,如Fe表示___________
表示这种元素的一个原子,如Fe表示___________
表示一种原子,如Fe表示_______
铁元素
铁这种物质
一个铁原子
铁原子
大写
小写
________
原子序数
________
________
二、元素及元素周期表
元素周期表
化学史:俄国科学家_________发现了元素周期律并编制出元素周期表
横行:每一个横行叫做一个周期,共有7个周期
纵列:每一个纵列叫做一个族,共有18个纵列、16个族(8、9、10三个
纵列共同组成一个族)
门捷列夫
一格(以锡
元素为例):
____________
相对原子质量
元素符号
元素名称
微点诊断
下列说法正确的是___。
①水结冰后水分子停止运动
②热胀冷缩是因为分子的大小发生了变化
③水和过氧化氢元素组成相同,化学性质也相同
④原子都是由电子、中子和质子构成的
⑤带电的微粒不一定是离子
⑥质子数相同的两种粒子其核外电子数一定相等
⑦最外层电子数相同的粒子,元素的化学性质一定相似
⑤
纵横过实验 · 纵向实验逐个过
小实验满分练
分子运动现象的探究(2020.3)
实验
(1)品红在水中扩散
①如图,实验中可观察到两个烧杯中液体都变为红色且装_____(填“热水”或“冷水”)的烧杯中液体变红得更快。
②由该实验可知,分子具有的性质是_______________,且温度越高,_________________。
人教上P48 图3-1改编
热水
分子在不断运动
分子运动速率越快
(2)探究分子运动实验
①过程Ⅱ中观察到溶液不变色,过程Ⅲ中观察到_____________。
人教上P49 图3-4改编
图1
溶液变为红色
②过程Ⅳ开始时,两烧杯中溶液均为无色,一段时间后可观察到______
_______________,产生这一现象的原因是_________________,说明微粒具有的性质是_______________。
③若将过程Ⅳ中B烧杯内的浓氨水换成浓盐酸,能否达到实验目的,并分析原因_________________________________________________。
人教上P49 图3-4改编
图1
A烧杯中溶液变为红色
浓氨水具有挥发性
分子在不断运动
不能,浓盐酸挥发出的氯化氢气体不能使酚酞溶液变色
④[微型实验]如图2实验,若 A 处的X为_______,可观察到 B 处的滤纸条变红,若给 A 处稍加热,在更短时间内可观察到现象,请从微观角度解释______________________________。
图2
浓氨水
温度越高,分子的运动速率越快
请完成精练本习题
第三单元 物质构成的
奥秘
考点特训营
2
纵横过实验 · 纵向实验逐个过
3
1
成都10年真题子母题+2年诊断检测
成都10年真题子母题+2年诊断检测
命题点
1
构成物质的微粒(10年3考)
1. (成都真题组合)(1)C60这种物质是由_____(填“分子”或“原子”)构成。[2016成都15(1)②题1分]
(2)C60分子是由_______构成的。[2014成都15(1)③题1分]
分子
碳原子
命题点
2
微粒的性质(10年9考)
2. (2019成都5题3分)下列事例不能用分子的相关知识解释的是( )
A. 品红溶解
B. 篮球充气
C. 酒精挥发
D. 柳絮飞扬
D
3. (2022成都4题3分)西岭雪山是著名旅游胜地,下列对其景色的微观解释错误的是( )
选项 景色 解释
A 春天花香四溢 分子在不断运动
B 夏天云消雾散 水分子间隔发生了变化
C 秋天层林尽染 分子种类不同性质不同
D 冬天白雪皑皑 水分子种类发生了变化
D
4. (2021成都3题3分)氨气有刺激性气味,结合表中信息,不能得出的是
( )
物质 分子个数 体积 0 ℃/101 kPa 20 ℃/101 kPa 0 ℃/202 kPa
17 g氨气 约6.02×1023个 22.4 L 24.1 L 11.2 L
A. 氨分子质量很小
B. 闻到氨水的气味是分子在运动
C. 温度升高,氨分子体积变大
D. 压强变大,氨分子间的间隔变小
C
5. (2020成都3题3分)根据图示实验,说法正确的是( )
A. 品红的扩散速度相同
B. 浓氨水变红
C. 氨水显碱性,pH大于7
D. 分子运动速率与温度无关
C
6. (2015成都10题3分)两种微粒的结构示意图是Na 和Na+ ,其中相同的是( )
A. 电子数
B. 质子数
C. 电子层数
D. 所带电荷数
命题点
3
微粒结构示意图(10年5考)
B
7. (2017成都10题3分)如图是X、Y两种微粒的结构示意图。下列说法正确的是( )
A. X为原子,Y为离子
B. X、Y均属于非金属元素
C. X在反应中可失去6个电子
D. X与Y形成化合物的化学式为YX
D
命题点
4
相对原子质量(2023.11)
8. (2023成都11题3分)化学家张青莲主持测定了铟、铱、锌等元素相对原子质量的新值。碳-12原子的质量为1.993×10-26 kg,一种锌原子的质量为1.096×10-25 kg,该锌原子的相对原子质量是( )
A. 12 B. 64
C. 66 D. 1.096×10-25 kg
C
命题点
5
元素与元素周期表(10年9考)
9. (2018成都7题3分)钕玻璃是激光聚变装置的核心元件。根据元素周期表中钕的信息判断错误的是( )
A. 属于金属元素
B. 质子数为60
C. 中子数为60
D. 相对原子质量是144.2
C
10. (2017成都8题改编3分)2017年5月9日,我国发布了四种人造新元素的中文名称,其中115号镆元素的“镆”取自古代剑名“镆铘”,下列说法不正确的是( )
A. 镆原子的核外电子数为115
B. 镆铘剑含有镆元素
C. 镆原子的质子数为115
D. 镆铘剑由合金铸造
B
11. (2019成都7题3分)2019年是元素周期表诞生第150周年。如图是元素周期表的一部分,从表中不能获取的信息是( )
A. 元素在周期表中的位置 B. 原子的质子数
C. 元素的相对原子质量 D. 原子的中子数
D
12. [2017成都15(2)①题1分]营养成分表中的“钠”是指_____(填“元素”或“单质”)。
13. [2019成都15(4)题2分]将太阳能转化为电能的常用材料是硅。硅属于_______(填“金属”或“非金属”)元素,它在地壳里的含量居第_______位。
元素
非金属
二(或2)
14. (2021成都7题改编3分)科学家利用“基因剪刀”技术降低了水稻中砷的含量。结合图示,有关砷的说法正确的是( )
A. 属于金属元素
B. 最外层电子数为33
C. 原子质量为74.92 g
D. 表示原子核及核电荷数
元素周期表与原子结构示意图(10年3考)
命题点
6
D
物质构成的奥秘
思维导图
元素及元素周期表
元素
符号
元素周期表
含量
分类
构成物质的微观粒子
性质
分子运动现象的探究
原子的构成
相对原子质量
分类
意义
阳离子
阴离子
原子
分子
离子
组合
分裂
得失电子
表示
原子和离子之间的区别与联系
考点特训营
一、构成物质的微观粒子
分子
性质
定义:由分子构成的物质,分子是保持物质_________的最小粒子
a.小:分子的_____和_____都很小,如一个水分子的质量约是
3×10-26 kg
b.动:分子总是在___________。温度越高,分子运动速率越___。
如:湿衣服在阳光下比阴凉处干得快
化学性质
体积
质量
不断运动着
快
一、构成物质的微观粒子
分子
性质
c.间:分子之间有_____。温度升高,间隔变大;压强增大,间隔变
小。例如:热胀冷缩、气体可压缩储存于钢瓶中
d.同:同种物质分子的化学性质_____,不同种物质分子的化学性质
_____。如液氧与氧气化学性质相同
间隔
相同
不同
分子运动现象的探究(详见纵横过实验)
一、构成物质的微观粒子
原子
原子的构成
构成
定义:_________中的最小粒子
原子核
质子:每个质子带1个单位___电荷
_____:不带电
数量关系:核电荷数=质子数=核外电子数=原子序数
_________:每个电子带1个单位___电荷
化学变化
正
中子
核外电子
负
原子
原子的构成
一、构成物质的微观粒子
原子核外电子排布
原子结构示意图:
(以钠原子为例)
弧线表示电子层,电子层数等于元素所在周期数
数字表示各电子层上容纳的_______
表示最外层电子数,与元素的________密切相关
圆圈表示_______,圈内的数字表示_________,
决定元素的_____
电子数
化学性质
原子核
核电荷数
种类
原子
原子的构成
一、构成物质的微观粒子
原子核外电子排布
最外层电子数(n)的应用
最外层电子数 原子得失电子(一般情况下)
n<4(氦、硼除外) 易_____电子
4≤n<8 易_____电子
n=8(氦为2) 不易得失电子(相对稳定结构)
失去
得到
原子的最外层电子数相等,对应元素的化学性质相似(H、
He除外)
___________________
_______________________
表达式:相对原子质量=
单位为“1”,一般省略不写
原子
一、构成物质的微观粒子
相对原子质量
一个原子的实际质量
一个碳-12原子质量的
离子
定义:带电的原子或原子团
表示:在元素符号的右上角用“+”或“-”号表示离子的电性,数字表示一个离
子所带的电荷数,先写_____,后写_______,数字为“1”时可省略不写
数字
正负号
__________
一、构成物质的微观粒子
离子
分类
阳离子:带_______的原子(或原子团),如Ca2+、 等
阴离子:带_______的原子(或原子团),如Cl-、 等
正电荷
负电荷
意义:
____________________________
每个镁离子带两个单位的正电荷
两个镁离子
一、构成物质的微观粒子
原子和离子之间的区别与联系
区别和联系 原子 离子 _______ _______
结构示意图
粒子符号 Na ____ ____
质子数与核外 电子数的关系 质子数=核外电子数 质子数>核外电子数 质子数<核外电子数
阳离子
阴离子
Na+
Cl-
二、元素及元素周期表
元素
定义:_______(即核电荷数)相同的一类原子的总称
含量:地壳中含量居于前四位的元素:______>______>______>______
分类
金属元素:“钅”字旁(金、汞除外),如钠、镁
非金属元素:“ ”字旁、“氵”字旁、“ ”字头,如硅、溴、氧
稀有气体元素:氦、氖、氩、氪、氙和氡
质子数
氧(O)
硅(Si)
铝(Al)
铁(Fe)
意义
宏观
微观
二、元素及元素周期表
元素
符号
书写(“一大二小”):元素符号由两个字母组成时,第一个字母要_____,
第二个字母要_____,如Na、Cu
表示一种元素,如Fe表示_______
表示由原子构成的一种物质,如Fe表示___________
表示这种元素的一个原子,如Fe表示___________
表示一种原子,如Fe表示_______
铁元素
铁这种物质
一个铁原子
铁原子
大写
小写
________
原子序数
________
________
二、元素及元素周期表
元素周期表
化学史:俄国科学家_________发现了元素周期律并编制出元素周期表
横行:每一个横行叫做一个周期,共有7个周期
纵列:每一个纵列叫做一个族,共有18个纵列、16个族(8、9、10三个
纵列共同组成一个族)
门捷列夫
一格(以锡
元素为例):
____________
相对原子质量
元素符号
元素名称
微点诊断
下列说法正确的是___。
①水结冰后水分子停止运动
②热胀冷缩是因为分子的大小发生了变化
③水和过氧化氢元素组成相同,化学性质也相同
④原子都是由电子、中子和质子构成的
⑤带电的微粒不一定是离子
⑥质子数相同的两种粒子其核外电子数一定相等
⑦最外层电子数相同的粒子,元素的化学性质一定相似
⑤
纵横过实验 · 纵向实验逐个过
小实验满分练
分子运动现象的探究(2020.3)
实验
(1)品红在水中扩散
①如图,实验中可观察到两个烧杯中液体都变为红色且装_____(填“热水”或“冷水”)的烧杯中液体变红得更快。
②由该实验可知,分子具有的性质是_______________,且温度越高,_________________。
人教上P48 图3-1改编
热水
分子在不断运动
分子运动速率越快
(2)探究分子运动实验
①过程Ⅱ中观察到溶液不变色,过程Ⅲ中观察到_____________。
人教上P49 图3-4改编
图1
溶液变为红色
②过程Ⅳ开始时,两烧杯中溶液均为无色,一段时间后可观察到______
_______________,产生这一现象的原因是_________________,说明微粒具有的性质是_______________。
③若将过程Ⅳ中B烧杯内的浓氨水换成浓盐酸,能否达到实验目的,并分析原因_________________________________________________。
人教上P49 图3-4改编
图1
A烧杯中溶液变为红色
浓氨水具有挥发性
分子在不断运动
不能,浓盐酸挥发出的氯化氢气体不能使酚酞溶液变色
④[微型实验]如图2实验,若 A 处的X为_______,可观察到 B 处的滤纸条变红,若给 A 处稍加热,在更短时间内可观察到现象,请从微观角度解释______________________________。
图2
浓氨水
温度越高,分子的运动速率越快
请完成精练本习题
同课章节目录
