第八章 复习课 课件(共20张PPT) 2023-2024学年高一下学期化学人教版(2019)必修第二册
文档属性
| 名称 | 第八章 复习课 课件(共20张PPT) 2023-2024学年高一下学期化学人教版(2019)必修第二册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 3.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-12-21 00:00:00 | ||
图片预览







文档简介
(共20张PPT)
第八章总复习
在恒容密闭容器中进行如下反应:
反应1:2NO(g)+O2(g) 2NO2(g) 反应2:H2(g)+I2(g) 2HI(g)
反应3:C(s)+ CO2(g) 2CO(g) 反应4:NH4Cl(s) NH3(g)+HCl(g)
①各组分的物质的量(或质量) ②反应混合物中各气体的体积分数
③混合气体的颜色不再改变 ④混合气体的密度不再改变
⑤恒温容器中混合气体的压强不再改变
⑥混合气体的平均相对分子质量不再改变
⑦绝热容器中反应体系的温度不再改变
以上可作为反应达到平衡的标志的是:
反应1:___________反应2: 反应3: 反应4:________
①②③⑤⑥⑦
①②③⑦
①②④⑤⑥⑦
①④⑤⑦
各坐标轴所代表量的意义;
分清正反应和逆反应;理解曲线斜率代表意义;
先拐先平的规律;
即:先出现拐点的曲线所表示的反应先达到平衡,
对应的温度高、压强大。
①看面:
②看线:
③看点:
坐标轴的交点、曲线的交叉点、转折点
④看量变化
物质的量的变化、浓度的变化、转化率的变化
一看 ——看图像
二想——想规律
转化量、反应速率之比与化学计量数之比
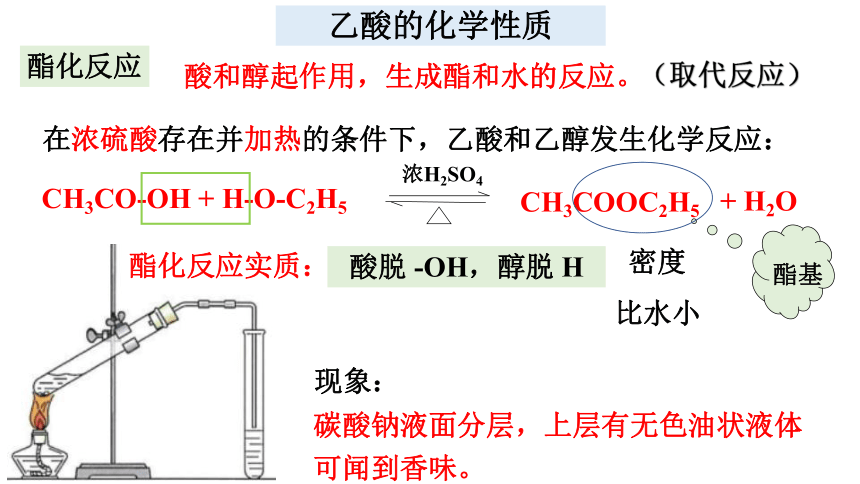
乙酸的化学性质
酯化反应
现象:
碳酸钠液面分层,上层有无色油状液体
可闻到香味。
酸和醇起作用,生成酯和水的反应。
(取代反应)
酯基
在浓硫酸存在并加热的条件下,乙酸和乙醇发生化学反应:
CH3CO-OH + H-O-C2H5
浓H2SO4
密度
比水小
酸脱 -OH,醇脱 H
CH3COOC2H5
+ H2O
酯化反应实质:
【实验注意事项】
4、为什么用酒精灯小心加热?
减少乙酸、乙醇的挥发
1、装药品的顺序如何?
乙醇 浓硫酸 乙酸
3、碎瓷片的作用是什么?
防止暴沸
5、导管不能伸入液面以下:
防止溶液倒吸
2、浓硫酸的作用:
催化剂、吸水剂
6、得到的实验产物是否纯净?主要杂质是什么?
主要杂质是乙酸和乙醇
制备乙酸乙酯饱和碳酸钠作用:____;中和___;
溶解___;
提高乙酸转化率和乙酸乙酯产率的措施是什么?
能否将饱和碳酸钠换成氢氧化钠?
7、饱和Na2CO3作用?
反应乙酸、吸收乙醇、
降低乙酸乙酯的溶解度
8、酯的分离方法是什么?
分液,密度小于水
情况 现象A 现象B 结论
①
②
③
溶液呈蓝色
溶液呈蓝色
溶液不呈蓝色
未产生银镜
出现银镜
出现银镜
未水解
部分水解
完全水解
现象A
中和液
现象B
NaOH 溶液
淀粉
水解液
稀H2SO4
△
碘水
银氨溶液
△
课本85页
淀粉的水解
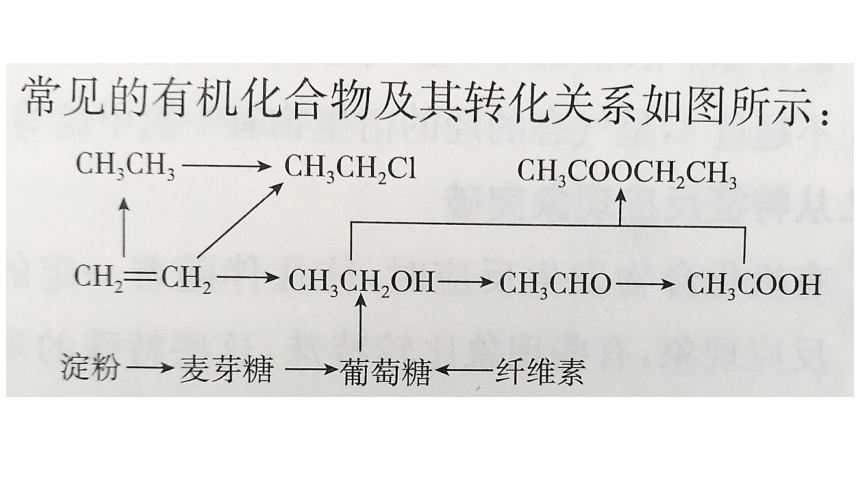
有机推断:【特征反应】
能使溴的四氯化碳褪色:
能使酸性高锰酸钾褪色:
能与NaHCO3/Na2CO3反应产生气泡:
能与H2发生加成反应的:
能与银氨溶液/新制氢氧化铜特征反应:
能遇碘变蓝:
加浓硝酸变黄:
能够水解的有机物:
可能是蛋白质
可能含有碳碳双键、碳碳三键
可能含有碳碳双键、碳碳三键、醇羟基
含有—COOH
可能是葡萄糖
淀粉
可能含有碳碳双键、碳碳三键、
醛基、酮羰基、苯环
二糖、淀粉、纤维素、酯、蛋白质
电 解 法
热还原法
热分解法
物理方法
金属冶炼的方法
金属的其他冶炼方法
火法炼铜:__________________;湿法炼铜:__________________
工业上采用电解法冶炼镁的材料是MgCl2,而不是MgO;
MgO虽是离子化合物,但熔点太高,熔融时会消耗大量热能,成本较高。
工业上采用电解法冶炼铝的材料是Al2O3,而不是AlCl3;
AlCl3是共价化合物,熔融时无法电离出自由移动的离子,不能导电;
铝热反应
原理:利用铝的强还原性,在高温条件下将某些较不活泼的金属
从其氧化物中(Fe2O3、MnO2、Cr2O3等)中还原出来。
镁条的作用?
KClO3的作用?
镁条做引燃剂,
提供能量使KClO3分解
KClO3做助燃剂,分解产生O2
应用:冶炼(高熔点的金属)、焊接钢轨
①缺石棉网 ②缺沸石 ③温度计水银球位置 ④冷凝管进出水方向
海水资源综合利用
——海水提镁
苦卤 (含Mg2+)
Mg(OH)2沉淀
MgCl2 溶液
Mg
无水MgCl2
干燥
脱水
过滤
盐酸
MgCl2·6H2O
蒸发浓缩冷却结晶过滤
Ca(OH)2
Cl2
循环利用
蒸发
熔融
电解
Mg
晒盐
海水
酸化
硫酸
氧化
氯气
吹出
热空气
吸收
Na2CO3
酸化
分液
硫酸
有机溶剂
液溴
海水资源综合利用
——海水提溴
浸取
过滤
氧化
萃取
海带中提碘—工艺流程
蒸馏/反萃取
(1) 萃取
知识必备
物质分离的一种方法:萃取、分液
选择萃取剂的条件是什么?
(1)与原溶液互不相溶、互不反应
(2)与溶质互不反应
(3)溶质在萃取剂中的溶解度 > 原溶液中的溶解度
(2) 分液
萃取后,用分液漏斗把互不相溶的两种液体分开,达到分离目的。
利用某种溶质在两种互不相溶的溶剂里溶解能力的不同,
用一种溶剂(萃取剂)将其从原溶剂中提取出来的方法叫萃取。
×
×
√
×
(3)因为金属越活泼,其离子的氧化性越弱,就越难被还原,故制取和利用的时间越晚。
(1)通过电解法冶炼Na、Mg、Al,是因为Na、Mg、Al还原性很强 ( )
(2) 利用CO冶炼铁的反应是置换反应 ( )
(3) 对一些不活泼的金属如Hg、Ag、Pt、Au可直接用加热分解的方法从其化合物中还原出来 ( )
(4) 采用热还原法冶炼金属时,常用的还原剂有C、CO、H2、Al等 ( )
(5) 由于地球上金属矿物资源有限,因此要加强金属资源的回收和再利用 ( )
√
×
×
√
√
SO2(过) + NaHCO3 == NaHSO3 + CO2
SO2(少) + 2NaHCO3== Na2SO3 + 2CO2 + H2O
SO2与盐反应:
(除去CO2中的SO2)
Ca(OH)2 + SO2(少) == CaSO3↓+ H2O
Ca(OH)2 + 2SO2(过) == Ca( HSO3)2
2NaOH + SO2(少) == Na2SO3+ H2O
NaOH + SO2(过) == NaHSO3
SO2与碱反应:
SO2(少) + 3ClO-+H2O === SO42- + Cl-+2HClO
SO2(过) + ClO- + H2O === SO42-+ Cl- +2H+
无机非金属材料分为:_________________和_______________
陶瓷以_______为主要原料;普通玻璃以_______________为原料
水泥以_____________为主要原料;
有哪些物质主要成分是SiO2:_______________________
陶瓷、普通玻璃、水泥制备过程中发生复杂的_____和_____变化
硅在自然界的存在形式:______________
纯硅的用途:______________________________
二氧化硅是_____氧化物;能与酸反应吗?__________
SiO2的用途___________;硅与二氧化硅属于_____________材料
常见的新型无机非金属材料有_____________________________
传统无机非金属材料
新型无机非金属材料
黏土
纯碱、石灰石、SiO2
黏土、石灰石
沙子、玛瑙、水晶、石英、光导纤维
物理
化学
都以硅酸盐和氧化物的形式存在
半导体材料、硅太阳能电池、计算机芯片
酸性
只与HF反应
制备光导纤维
新型无机非金属
新型陶瓷、富勒烯、
碳纳米管、石墨烯
第八章总复习
在恒容密闭容器中进行如下反应:
反应1:2NO(g)+O2(g) 2NO2(g) 反应2:H2(g)+I2(g) 2HI(g)
反应3:C(s)+ CO2(g) 2CO(g) 反应4:NH4Cl(s) NH3(g)+HCl(g)
①各组分的物质的量(或质量) ②反应混合物中各气体的体积分数
③混合气体的颜色不再改变 ④混合气体的密度不再改变
⑤恒温容器中混合气体的压强不再改变
⑥混合气体的平均相对分子质量不再改变
⑦绝热容器中反应体系的温度不再改变
以上可作为反应达到平衡的标志的是:
反应1:___________反应2: 反应3: 反应4:________
①②③⑤⑥⑦
①②③⑦
①②④⑤⑥⑦
①④⑤⑦
各坐标轴所代表量的意义;
分清正反应和逆反应;理解曲线斜率代表意义;
先拐先平的规律;
即:先出现拐点的曲线所表示的反应先达到平衡,
对应的温度高、压强大。
①看面:
②看线:
③看点:
坐标轴的交点、曲线的交叉点、转折点
④看量变化
物质的量的变化、浓度的变化、转化率的变化
一看 ——看图像
二想——想规律
转化量、反应速率之比与化学计量数之比
乙酸的化学性质
酯化反应
现象:
碳酸钠液面分层,上层有无色油状液体
可闻到香味。
酸和醇起作用,生成酯和水的反应。
(取代反应)
酯基
在浓硫酸存在并加热的条件下,乙酸和乙醇发生化学反应:
CH3CO-OH + H-O-C2H5
浓H2SO4
密度
比水小
酸脱 -OH,醇脱 H
CH3COOC2H5
+ H2O
酯化反应实质:
【实验注意事项】
4、为什么用酒精灯小心加热?
减少乙酸、乙醇的挥发
1、装药品的顺序如何?
乙醇 浓硫酸 乙酸
3、碎瓷片的作用是什么?
防止暴沸
5、导管不能伸入液面以下:
防止溶液倒吸
2、浓硫酸的作用:
催化剂、吸水剂
6、得到的实验产物是否纯净?主要杂质是什么?
主要杂质是乙酸和乙醇
制备乙酸乙酯饱和碳酸钠作用:____;中和___;
溶解___;
提高乙酸转化率和乙酸乙酯产率的措施是什么?
能否将饱和碳酸钠换成氢氧化钠?
7、饱和Na2CO3作用?
反应乙酸、吸收乙醇、
降低乙酸乙酯的溶解度
8、酯的分离方法是什么?
分液,密度小于水
情况 现象A 现象B 结论
①
②
③
溶液呈蓝色
溶液呈蓝色
溶液不呈蓝色
未产生银镜
出现银镜
出现银镜
未水解
部分水解
完全水解
现象A
中和液
现象B
NaOH 溶液
淀粉
水解液
稀H2SO4
△
碘水
银氨溶液
△
课本85页
淀粉的水解
有机推断:【特征反应】
能使溴的四氯化碳褪色:
能使酸性高锰酸钾褪色:
能与NaHCO3/Na2CO3反应产生气泡:
能与H2发生加成反应的:
能与银氨溶液/新制氢氧化铜特征反应:
能遇碘变蓝:
加浓硝酸变黄:
能够水解的有机物:
可能是蛋白质
可能含有碳碳双键、碳碳三键
可能含有碳碳双键、碳碳三键、醇羟基
含有—COOH
可能是葡萄糖
淀粉
可能含有碳碳双键、碳碳三键、
醛基、酮羰基、苯环
二糖、淀粉、纤维素、酯、蛋白质
电 解 法
热还原法
热分解法
物理方法
金属冶炼的方法
金属的其他冶炼方法
火法炼铜:__________________;湿法炼铜:__________________
工业上采用电解法冶炼镁的材料是MgCl2,而不是MgO;
MgO虽是离子化合物,但熔点太高,熔融时会消耗大量热能,成本较高。
工业上采用电解法冶炼铝的材料是Al2O3,而不是AlCl3;
AlCl3是共价化合物,熔融时无法电离出自由移动的离子,不能导电;
铝热反应
原理:利用铝的强还原性,在高温条件下将某些较不活泼的金属
从其氧化物中(Fe2O3、MnO2、Cr2O3等)中还原出来。
镁条的作用?
KClO3的作用?
镁条做引燃剂,
提供能量使KClO3分解
KClO3做助燃剂,分解产生O2
应用:冶炼(高熔点的金属)、焊接钢轨
①缺石棉网 ②缺沸石 ③温度计水银球位置 ④冷凝管进出水方向
海水资源综合利用
——海水提镁
苦卤 (含Mg2+)
Mg(OH)2沉淀
MgCl2 溶液
Mg
无水MgCl2
干燥
脱水
过滤
盐酸
MgCl2·6H2O
蒸发浓缩冷却结晶过滤
Ca(OH)2
Cl2
循环利用
蒸发
熔融
电解
Mg
晒盐
海水
酸化
硫酸
氧化
氯气
吹出
热空气
吸收
Na2CO3
酸化
分液
硫酸
有机溶剂
液溴
海水资源综合利用
——海水提溴
浸取
过滤
氧化
萃取
海带中提碘—工艺流程
蒸馏/反萃取
(1) 萃取
知识必备
物质分离的一种方法:萃取、分液
选择萃取剂的条件是什么?
(1)与原溶液互不相溶、互不反应
(2)与溶质互不反应
(3)溶质在萃取剂中的溶解度 > 原溶液中的溶解度
(2) 分液
萃取后,用分液漏斗把互不相溶的两种液体分开,达到分离目的。
利用某种溶质在两种互不相溶的溶剂里溶解能力的不同,
用一种溶剂(萃取剂)将其从原溶剂中提取出来的方法叫萃取。
×
×
√
×
(3)因为金属越活泼,其离子的氧化性越弱,就越难被还原,故制取和利用的时间越晚。
(1)通过电解法冶炼Na、Mg、Al,是因为Na、Mg、Al还原性很强 ( )
(2) 利用CO冶炼铁的反应是置换反应 ( )
(3) 对一些不活泼的金属如Hg、Ag、Pt、Au可直接用加热分解的方法从其化合物中还原出来 ( )
(4) 采用热还原法冶炼金属时,常用的还原剂有C、CO、H2、Al等 ( )
(5) 由于地球上金属矿物资源有限,因此要加强金属资源的回收和再利用 ( )
√
×
×
√
√
SO2(过) + NaHCO3 == NaHSO3 + CO2
SO2(少) + 2NaHCO3== Na2SO3 + 2CO2 + H2O
SO2与盐反应:
(除去CO2中的SO2)
Ca(OH)2 + SO2(少) == CaSO3↓+ H2O
Ca(OH)2 + 2SO2(过) == Ca( HSO3)2
2NaOH + SO2(少) == Na2SO3+ H2O
NaOH + SO2(过) == NaHSO3
SO2与碱反应:
SO2(少) + 3ClO-+H2O === SO42- + Cl-+2HClO
SO2(过) + ClO- + H2O === SO42-+ Cl- +2H+
无机非金属材料分为:_________________和_______________
陶瓷以_______为主要原料;普通玻璃以_______________为原料
水泥以_____________为主要原料;
有哪些物质主要成分是SiO2:_______________________
陶瓷、普通玻璃、水泥制备过程中发生复杂的_____和_____变化
硅在自然界的存在形式:______________
纯硅的用途:______________________________
二氧化硅是_____氧化物;能与酸反应吗?__________
SiO2的用途___________;硅与二氧化硅属于_____________材料
常见的新型无机非金属材料有_____________________________
传统无机非金属材料
新型无机非金属材料
黏土
纯碱、石灰石、SiO2
黏土、石灰石
沙子、玛瑙、水晶、石英、光导纤维
物理
化学
都以硅酸盐和氧化物的形式存在
半导体材料、硅太阳能电池、计算机芯片
酸性
只与HF反应
制备光导纤维
新型无机非金属
新型陶瓷、富勒烯、
碳纳米管、石墨烯
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
