2023—2024学年鲁教版(五四学制)化学九年级全一册 第二单元 常见的酸和碱 期末复习基础题(含答案)
文档属性
| 名称 | 2023—2024学年鲁教版(五四学制)化学九年级全一册 第二单元 常见的酸和碱 期末复习基础题(含答案) |

|
|
| 格式 | doc | ||
| 文件大小 | 604.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-12-22 00:00:00 | ||
图片预览




文档简介
2023—2024学年鲁教版(五四学制)化学九年级全一册第2单元 常见的酸和碱 期末复习基础题附答案
鲁教版(五四学制)第2单元 常见的酸和碱
一、选择题。(16题)
1、工人师傅除去锅炉内的水垢[主要成分是CaCO3和Mg(OH)2]时,选用的试剂是( )
A. 稀盐酸 B. 烧碱溶液 C. 石灰水 D. 食盐水
2、下列物质的性质与用途对应关系错误的是( )
A. 金刚石硬度大,可制造钻头
B. 镁燃烧发出耀眼白光,可用制作烟花
C. 铜有良好的导电性,可制作导线
D. 氢氧化钠具有碱性,常用于改良酸性土壤
3、向pH=3的溶液中滴加石蕊试剂,溶液呈( )
A. 无色 B. 紫色 C. 红色 D. 蓝色
4、下列各组离子在pH=1的溶液中能大量共存的是( )
A. NH4+ NO3﹣ Na+ Cl﹣ B. CO32﹣ K+ Na+ SO42﹣
C. Cu2+ OH﹣ Cl﹣ Ba2+ D. Ag+ NO3﹣ Cl﹣ Na+
5、下列说法正确的是( )
A. 酒精是最常用是消毒药,体积分数为95%的酒精杀菌能力最强
B. 亚硝酸钠(NaNO2)外观极像食盐,且具有与食盐一样的咸味,但被误作食盐食用,会导致中毒事故发生
C. 为了防止大脖子病,食用的是加入碘化钾的食盐
D. 市售食醋中含乙酸约为30%﹣50%
6、化学实验中常会出现一些“出乎意料”的现象或结果,下列各项对相关异常情况的解释不合理的是( )
实验 验证氧气的化学性质 除去粗盐中的泥沙 测定空气中氧气的含量 检验实验室制出的二氧化碳
异常情况 未看到火星四射 滤液浑浊 测定结果偏大 澄清石灰水未变浑浊
选项 A.可能是温度未达到铁丝的着火点 B.可能是滤纸破损 C.可能是红磷的量不足 D.可能是二氧化碳中混有氯化氢气体
A.A B.B C.C D.D
7、下列实验基本操作错误的是( )
A. B. C. D.
8、下列做法符合科学常识的是( )
A. 天然气泄漏,用燃着的木条检验
B. 胃酸过多的人,可以喝一点氢氧化钠溶液来中和
C. 保险丝烧断了,可以用铜丝代替
D. 有人触电,不可以用手直接拿开电线
9、下列物质属于酸类的是( )
A.CO2 B. HNO3 C.NaOH D. NaCl
10、某同学的化学笔记上有以下知识总结,你认为正确的是( )
A. 生成盐和水的反应不一定是中和反应
B. 含有氧元素的化合物称为氧化物
C. 由同种元素组成的物质称为单质
D. 固体物质的溶解度都随温度的升高而增大
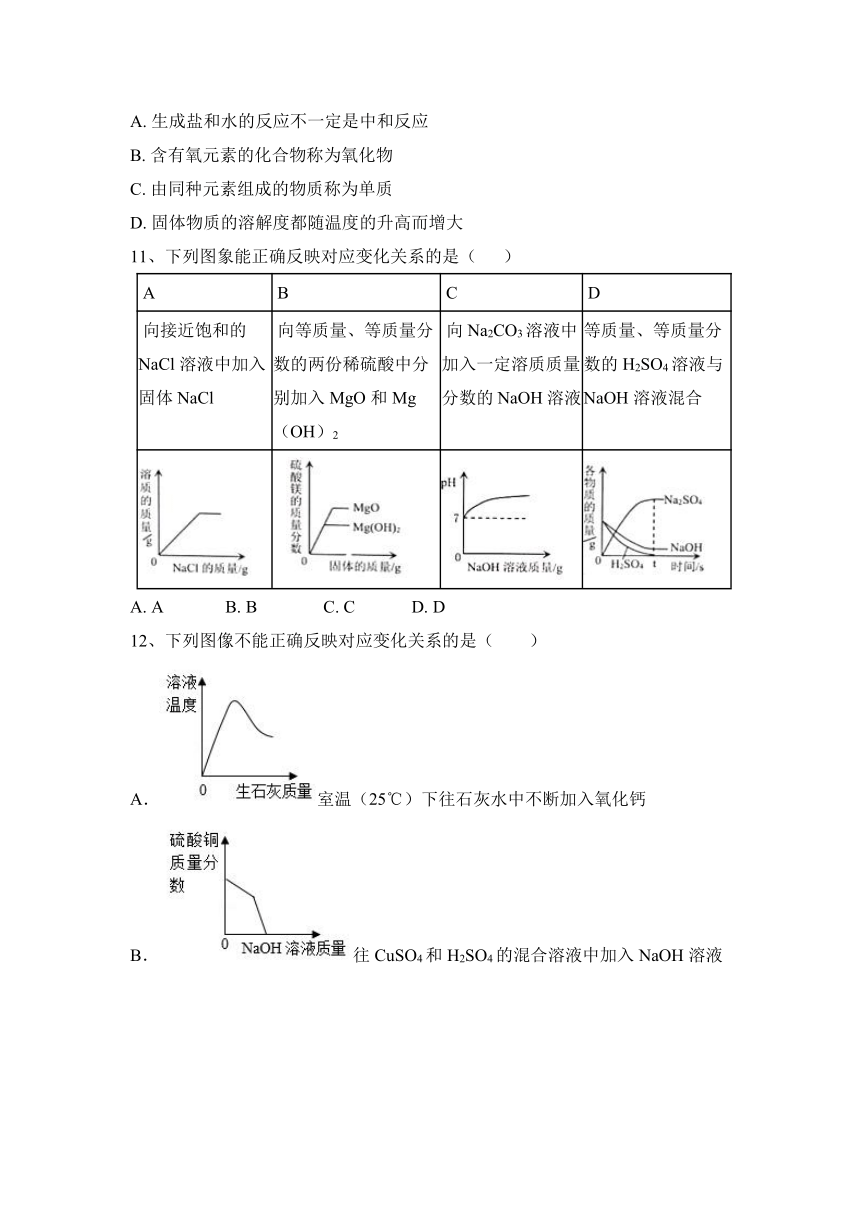
11、下列图象能正确反映对应变化关系的是( )
A B C D
向接近饱和的NaCl溶液中加入固体NaCl 向等质量、等质量分数的两份稀硫酸中分别加入MgO和Mg(OH)2 向Na2CO3溶液中加入一定溶质质量分数的NaOH溶液 等质量、等质量分数的H2SO4溶液与NaOH溶液混合
A. A B. B C. C D. D
12、下列图像不能正确反映对应变化关系的是( )
A.室温(25℃)下往石灰水中不断加入氧化钙
B.往CuSO4和H2SO4的混合溶液中加入NaOH溶液
C.碳酸钙高温分解
D.往硫酸和盐酸的混合液中不断加入氢氧化钡溶液
13、推理是化学学习中常见的思维方法,下列推理正确的是( )
A. 锌和铜均是金属,锌与稀硫酸反应生成氢气,则铜也能与稀硫酸反应生成氢气
B. 气体的溶解度随温度的升高而减小,所以温度越高,氧气的溶解度越小
C. 稀盐酸与稀硫酸的化学性质相似,所以实验室可以用大理石与稀硫酸制取二氧化碳
D. 催化剂在反应前后质量不变,因此反应前后质量不变的物质一定是催化剂
14、某同学在用pH试纸测定氢氧化钠溶液的pH时,错误地将pH试纸先进行了湿润,则其测定的数值应该是( )
A. 变大 B. 变小 C. 不变 D. 无法确定
15、某环境监测兴趣小组的同学监测到南京市某年近60%的降雨PH<5.6,这种雨水( )
A.能是酚酞试液变红 B.中性 C.酸性 D.碱性
16、 “关爱生命,注意安全,拥抱健康”是永恒的主题。下列有关叙述错误的是( )
A. 健康人体胃液的pH范围在0.9~1.5
B. 幼儿及青少年缺钙会产生骨质疏松
C. 人体缺乏维生素A会引起夜盲症
D. 霉变食物绝对不能食用
二、填空题。
17、化学与生活密切相关。
醋和食盐是日常生活中必备调味品
(1)食盐通过晾晒海水或煮盐井水、盐湖水再经过净化得到;醋通过大米、高粱等粮食发酵酿制而成.晾晒和发酵两种变化的本质区别是______ 。
(2)醋的有效成分是乙酸(CH3COOH),也叫醋酸.正在服碳酸氢钠片、复方氢氧化铝等药品的人,不宜食用醋,原因是______ 。
18、经过“碱的化学性质”的学习,小明同学用如图所示的示意图归纳总结了NaOH四条化学性质。
(1)为了验证反应②,小明同学向NaOH溶液中滴入无色酚酞试液,观察到无色酚酞试液变为红色,使无色酚酞试液变为红色的微粒是_ __(填微粒符号)。
(2)为了验证反应③能够发生,可以选用的试剂是__ __。
A.CuCl2 B.NaCl C.CuSO4 D.Na2CO3
(3)NaOH溶液露置于空气中易变质,所以必须密封保存。请你写出NaOH溶液变质的化学方程式:__ __。
(4)第(3)问中的化学反应是体现了图中NaOH的性质__ __(填“①”“②”“③”或“④”)。
(5)根据第(2)问提供的试剂写出反应③时可观察到的现象是__ __,反应方程式为: 、
。
19、化学实验小组的同学尝试寻找生活中的物质制作酸碱指示剂。以下表格是分别向不同试剂中滴加2滴自制紫薯汁的现象,请回答:
试剂 稀盐酸 氢氧化钠溶液 蒸馏水 白醋 草木灰溶液
现象 红色 绿色 紫色 红色 绿色
(1)紫薯汁______(填“能”或“不能”)作酸碱指示剂。
(2)草木灰溶液呈______(填“酸性”“中性”或“碱性”)。
20、有A、B、C、D四种元素,其原子结构示意图如图:
(1)D元素的名称为________ ,D元素与图中________ (填写字母序号)元素的化学性质相似,D元素的离子符号为________ 。
(2)A、B、C三种元素能形成一种化合物,其水溶液的pH________ 7。
(填>、<、=)
(3)A、B两种元素的原子以1:1的比例形成的化合物为(写化学式)________ ,其中B元素化合价为________。
21、金属是一种非常重要的资源,在生产、生活中有着广泛的用途。
(1)人类每年从自然界提取大量的金属,其中提取量最大的是铁.用赤铁矿和一氧化碳炼铁的化学方程式为________。
(2)央视3 15晚会曝光某品牌汽车厂为了节约成本,采用价格相对便宜的普通钢板代替防腐性能较好的镀锌板,造成钢板生锈,给车主带来极大安全隐患.普通钢板在空气中锈蚀,实际上是铁跟空气中的________共同作用的结果。
(3)请写出工业上用稀硫酸除铁锈的化学反应方程式________。
(4)亮亮同学用稀盐酸和另一种溶液,验证了Mg、Fe、Cu、Ag四种金属的活动性顺序是依次减弱的.请问亮亮所用的另一种溶液是________。
22、将稀盐酸分别滴入如图所示盛有不同物质的试管中、请回答下列问题:
(1)有气泡产生的试管为______(填序号)。
(2)不与稀盐酸发生反应的物质是______。
(3)实验后试管②中溶液变为______色,该试管中发生反应的化学方程式为:
______ 。
三、推断题。
23、如图所示:已知A、B、C、D、E均为常见的物质,且A是一种最常用的溶剂,C可改良酸性土壤,B、C、D、E属于不同种类物质且含有相同的一种元素,图中“—”表示相连的物质在一定条件下可以反应,“→”表示物质间存在转化关系。请回答下列问题。
(1)D的化学式为__________,A→C反应的基本反应类型为__________。
(2)B与C反应的化学方程式为__________ 。
(3)C、E反应可用于制取烧碱,请写出该反应的化学方程式:__________。
四、实验题。
24、在保存药品时,可能会在容器中放置铁粉与碱石灰。现有久置的铁粉和碱石灰固体,同学们设计实验进行探究。
【提出问题】该固体样品的成分是什么?
【查阅资料】(1)碱石灰是一种常用干燥剂,是CaO和NaOH的混合物。
(2)BaCl2溶液显中性。
【猜想与假设】固体样品中可能含有Fe、Fe2O3、CaO、NaOH、Ca(OH)2、Na2CO3和_________等物质。
【进行实验】
甲组同学对滤渣B的成分进行探究,记录如下:
实验操作 实验现象 实验结论及化学方程式
取少量滤渣B于试管中,加入足量稀盐酸,将生成的气体通入澄清的石灰水中 ①__________。②__________。 结论:滤渣B中有Fe2O3,CaCO3。盐酸和Fe2O3反应的化学方程式为:____________。
乙组同学对滤液C的成分进行探究,记录如下:
实验操作 实验现象 实验结论
取少量滤液C于试管中,加入过量BaC12溶液,静置,向上层清液中滴加无色酚酞试液,振荡 ①有白色沉淀生成②酚酞试液由无色变成红色 溶液C中有__________。
(1)乙组同学实验中加入过量BaCl2溶液的目的是____________ 。
(2)通过以上实验探究,该固体样品的组成一定有___________ _,可能有____________。
25、某市初中化学实验操作考查内容为“溶液酸碱性的检验”。请根据实验回答下列问题。
(1)测得碳酸饮料的pH _____ 7(填“<”或“=”或“>”)。
(2)下列使用pH试纸的方法中,正确的是_____(填序号)。
A.将pH试纸剪成几段使用
B.将pH试纸直接插入待测液中
C.将pH试纸放在表面皿上,用干净的玻璃棒蘸取待测液滴在pH试纸上
D.将pH试纸湿润后放在表面皿上,用干净的玻璃棒蘸取待测液滴在pH试纸上
E.读数时,在30秒内将pH试纸呈现的颜色与标准比色卡对照
(3)本次实验中滴管使用出现了如图1~图2所示的四种常见错误操作。请你从这四幅图中任意选择一幅(请写明所选图的序号),具体说明改正错误的方法:
_____ 。
图1 图2 图3 图4
(4)使用白色点滴板完成实验有显色明显、便于对比、_____(填一项)等优点。
五、计算类综合题。
26、长久使用的热水壶内都会有一层水垢,已知其主要成分是碳酸钙和氢氧化镁,用稀盐酸可以清除这些水垢。某校化学课外活动小组同学在测定水垢中碳酸钙的含量时,在200g水垢中加入足量的稀盐酸,并同时测量了3分钟内产生气体的质量,有关数据如下:
时间/s 0 30 50 90 120 150 180
气体质量/g 0 30 50 60 80 66 66
请回答下列问题:
(1)表中有一项测量结果有较大的误差,其对应的时间是________。
(2)水垢中碳酸钙的质量分数是多少?________ 。
2023—2024学年鲁教版(五四学制)化学九年级全一册第2单元 常见的酸和碱 期末复习基础题附答案
鲁教版(五四学制)第2单元 常见的酸和碱
一、选择题。(16题)
1、工人师傅除去锅炉内的水垢[主要成分是CaCO3和Mg(OH)2]时,选用的试剂是( )
A. 稀盐酸 B. 烧碱溶液 C. 石灰水 D. 食盐水
【答案】A
2、下列物质的性质与用途对应关系错误的是( )
A. 金刚石硬度大,可制造钻头
B. 镁燃烧发出耀眼白光,可用制作烟花
C. 铜有良好的导电性,可制作导线
D. 氢氧化钠具有碱性,常用于改良酸性土壤
【答案】D
3、向pH=3的溶液中滴加石蕊试剂,溶液呈( )
A. 无色 B. 紫色 C. 红色 D. 蓝色
【答案】C
4、下列各组离子在pH=1的溶液中能大量共存的是( )
A. NH4+ NO3﹣ Na+ Cl﹣ B. CO32﹣ K+ Na+ SO42﹣
C. Cu2+ OH﹣ Cl﹣ Ba2+ D. Ag+ NO3﹣ Cl﹣ Na+
【答案】A
5、下列说法正确的是( )
A. 酒精是最常用是消毒药,体积分数为95%的酒精杀菌能力最强
B. 亚硝酸钠(NaNO2)外观极像食盐,且具有与食盐一样的咸味,但被误作食盐食用,会导致中毒事故发生
C. 为了防止大脖子病,食用的是加入碘化钾的食盐
D. 市售食醋中含乙酸约为30%﹣50%
【答案】B
6、化学实验中常会出现一些“出乎意料”的现象或结果,下列各项对相关异常情况的解释不合理的是( )
实验 验证氧气的化学性质 除去粗盐中的泥沙 测定空气中氧气的含量 检验实验室制出的二氧化碳
异常情况 未看到火星四射 滤液浑浊 测定结果偏大 澄清石灰水未变浑浊
选项 A.可能是温度未达到铁丝的着火点 B.可能是滤纸破损 C.可能是红磷的量不足 D.可能是二氧化碳中混有氯化氢气体
A.A B.B C.C D.D
【答案】C
7、下列实验基本操作错误的是( )
A. B. C. D.
【答案】A
8、下列做法符合科学常识的是( )
A. 天然气泄漏,用燃着的木条检验
B. 胃酸过多的人,可以喝一点氢氧化钠溶液来中和
C. 保险丝烧断了,可以用铜丝代替
D. 有人触电,不可以用手直接拿开电线
【答案】D
9、下列物质属于酸类的是( )
A.CO2 B. HNO3 C.NaOH D. NaCl
【答案】B
10、某同学的化学笔记上有以下知识总结,你认为正确的是( )
A. 生成盐和水的反应不一定是中和反应
B. 含有氧元素的化合物称为氧化物
C. 由同种元素组成的物质称为单质
D. 固体物质的溶解度都随温度的升高而增大
【答案】A
11、下列图象能正确反映对应变化关系的是( )
A B C D
向接近饱和的NaCl溶液中加入固体NaCl 向等质量、等质量分数的两份稀硫酸中分别加入MgO和Mg(OH)2 向Na2CO3溶液中加入一定溶质质量分数的NaOH溶液 等质量、等质量分数的H2SO4溶液与NaOH溶液混合
A. A B. B C. C D. D
【答案】D
12、下列图像不能正确反映对应变化关系的是( )
A.室温(25℃)下往石灰水中不断加入氧化钙
B.往CuSO4和H2SO4的混合溶液中加入NaOH溶液
C.碳酸钙高温分解
D.往硫酸和盐酸的混合液中不断加入氢氧化钡溶液
【答案】A
13、推理是化学学习中常见的思维方法,下列推理正确的是( )
A. 锌和铜均是金属,锌与稀硫酸反应生成氢气,则铜也能与稀硫酸反应生成氢气
B. 气体的溶解度随温度的升高而减小,所以温度越高,氧气的溶解度越小
C. 稀盐酸与稀硫酸的化学性质相似,所以实验室可以用大理石与稀硫酸制取二氧化碳
D. 催化剂在反应前后质量不变,因此反应前后质量不变的物质一定是催化剂
【答案】B
14、某同学在用pH试纸测定氢氧化钠溶液的pH时,错误地将pH试纸先进行了湿润,则其测定的数值应该是( )
A. 变大 B. 变小 C. 不变 D. 无法确定
【答案】B
15、某环境监测兴趣小组的同学监测到南京市某年近60%的降雨PH<5.6,这种雨水( )
A.能是酚酞试液变红 B.中性 C.酸性 D.碱性
【答案】C
16、 “关爱生命,注意安全,拥抱健康”是永恒的主题。下列有关叙述错误的是( )
A. 健康人体胃液的pH范围在0.9~1.5
B. 幼儿及青少年缺钙会产生骨质疏松
C. 人体缺乏维生素A会引起夜盲症
D. 霉变食物绝对不能食用
【答案】B
二、填空题。
17、化学与生活密切相关。
醋和食盐是日常生活中必备调味品
(1)食盐通过晾晒海水或煮盐井水、盐湖水再经过净化得到;醋通过大米、高粱等粮食发酵酿制而成.晾晒和发酵两种变化的本质区别是______ 。
(2)醋的有效成分是乙酸(CH3COOH),也叫醋酸.正在服碳酸氢钠片、复方氢氧化铝等药品的人,不宜食用醋,原因是______ 。
【答案】是否有新物质生成 乙酸能和服用的药品反应,降低药效
18、经过“碱的化学性质”的学习,小明同学用如图所示的示意图归纳总结了NaOH四条化学性质。
(1)为了验证反应②,小明同学向NaOH溶液中滴入无色酚酞试液,观察到无色酚酞试液变为红色,使无色酚酞试液变为红色的微粒是_ __(填微粒符号)。
(2)为了验证反应③能够发生,可以选用的试剂是__ __。
A.CuCl2 B.NaCl C.CuSO4 D.Na2CO3
(3)NaOH溶液露置于空气中易变质,所以必须密封保存。请你写出NaOH溶液变质的化学方程式:__ __。
(4)第(3)问中的化学反应是体现了图中NaOH的性质__ __(填“①”“②”“③”或“④”)。
(5)根据第(2)问提供的试剂写出反应③时可观察到的现象是__ __,反应方程式为: 、
。
【答案】(1)OH- (2)AC (3)2NaOH+CO2===Na2CO3+H2O (4)④
(5)产生蓝色沉淀 CuCl2+2NaOH===Cu(OH)2↓+2NaCl
CuSO4+2NaOH===Cu(OH)2↓+Na2SO4
19、化学实验小组的同学尝试寻找生活中的物质制作酸碱指示剂。以下表格是分别向不同试剂中滴加2滴自制紫薯汁的现象,请回答:
试剂 稀盐酸 氢氧化钠溶液 蒸馏水 白醋 草木灰溶液
现象 红色 绿色 紫色 红色 绿色
(1)紫薯汁______(填“能”或“不能”)作酸碱指示剂。
(2)草木灰溶液呈______(填“酸性”“中性”或“碱性”)。
【答案】(1)能 (2)碱性
20、有A、B、C、D四种元素,其原子结构示意图如图:
(1)D元素的名称为________ ,D元素与图中________ (填写字母序号)元素的化学性质相似,D元素的离子符号为________ 。
(2)A、B、C三种元素能形成一种化合物,其水溶液的pH________ 7。
(填>、<、=)
(3)A、B两种元素的原子以1:1的比例形成的化合物为(写化学式)________ ,其中B元素化合价为________。
【答案】硫;B;S2﹣;>;H2O2;﹣1
21、金属是一种非常重要的资源,在生产、生活中有着广泛的用途。
(1)人类每年从自然界提取大量的金属,其中提取量最大的是铁.用赤铁矿和一氧化碳炼铁的化学方程式为________。
(2)央视3 15晚会曝光某品牌汽车厂为了节约成本,采用价格相对便宜的普通钢板代替防腐性能较好的镀锌板,造成钢板生锈,给车主带来极大安全隐患.普通钢板在空气中锈蚀,实际上是铁跟空气中的________共同作用的结果。
(3)请写出工业上用稀硫酸除铁锈的化学反应方程式________。
(4)亮亮同学用稀盐酸和另一种溶液,验证了Mg、Fe、Cu、Ag四种金属的活动性顺序是依次减弱的.请问亮亮所用的另一种溶液是________。
【答案】(1)Fe2O3+3CO 2Fe+3CO2 (2)氧气和水
(3)Fe2O3+3H2SO4═Fe2(SO4)3+3H2O (4)硝酸银溶液
22、将稀盐酸分别滴入如图所示盛有不同物质的试管中、请回答下列问题:
(1)有气泡产生的试管为______(填序号)。
(2)不与稀盐酸发生反应的物质是______。
(3)实验后试管②中溶液变为______色,该试管中发生反应的化学方程式为:
______ 。
【答案】(1)③⑤ (2)铜片 (3) 黄色
三、推断题。
23、如图所示:已知A、B、C、D、E均为常见的物质,且A是一种最常用的溶剂,C可改良酸性土壤,B、C、D、E属于不同种类物质且含有相同的一种元素,图中“—”表示相连的物质在一定条件下可以反应,“→”表示物质间存在转化关系。请回答下列问题。
(1)D的化学式为__________,A→C反应的基本反应类型为__________。
(2)B与C反应的化学方程式为__________ 。
(3)C、E反应可用于制取烧碱,请写出该反应的化学方程式:__________。
【答案】(1)H2SO4 化合反应
(2) (3)
四、实验题。
24、在保存药品时,可能会在容器中放置铁粉与碱石灰。现有久置的铁粉和碱石灰固体,同学们设计实验进行探究。
【提出问题】该固体样品的成分是什么?
【查阅资料】(1)碱石灰是一种常用干燥剂,是CaO和NaOH的混合物。
(2)BaCl2溶液显中性。
【猜想与假设】固体样品中可能含有Fe、Fe2O3、CaO、NaOH、Ca(OH)2、Na2CO3和_________等物质。
【进行实验】
甲组同学对滤渣B的成分进行探究,记录如下:
实验操作 实验现象 实验结论及化学方程式
取少量滤渣B于试管中,加入足量稀盐酸,将生成的气体通入澄清的石灰水中 ①__________。②__________。 结论:滤渣B中有Fe2O3,CaCO3。盐酸和Fe2O3反应的化学方程式为:____________。
乙组同学对滤液C的成分进行探究,记录如下:
实验操作 实验现象 实验结论
取少量滤液C于试管中,加入过量BaC12溶液,静置,向上层清液中滴加无色酚酞试液,振荡 ①有白色沉淀生成②酚酞试液由无色变成红色 溶液C中有__________。
(1)乙组同学实验中加入过量BaCl2溶液的目的是____________ 。
(2)通过以上实验探究,该固体样品的组成一定有___________ _,可能有____________。
【答案】【猜想与假设】CaCO3##碳酸钙
【进行实验】
滤渣完全溶解,溶液变为黄色 澄清石灰水变浑浊
Fe2O3+6HCl=2FeCl3+3H2O
Na2CO3和NaOH
(1)检验并除去碳酸钠,以防止对检验氢氧化钠产生影响
(2)Fe、Fe2O3、Ca(OH)2、Na2CO3 CaCO3##碳酸钙
25、某市初中化学实验操作考查内容为“溶液酸碱性的检验”。请根据实验回答下列问题。
(1)测得碳酸饮料的pH _____ 7(填“<”或“=”或“>”)。
(2)下列使用pH试纸的方法中,正确的是_____(填序号)。
A.将pH试纸剪成几段使用
B.将pH试纸直接插入待测液中
C.将pH试纸放在表面皿上,用干净的玻璃棒蘸取待测液滴在pH试纸上
D.将pH试纸湿润后放在表面皿上,用干净的玻璃棒蘸取待测液滴在pH试纸上
E.读数时,在30秒内将pH试纸呈现的颜色与标准比色卡对照
(3)本次实验中滴管使用出现了如图1~图2所示的四种常见错误操作。请你从这四幅图中任意选择一幅(请写明所选图的序号),具体说明改正错误的方法:
_____ 。
图1 图2 图3 图4
(4)使用白色点滴板完成实验有显色明显、便于对比、_____(填一项)等优点。
【答案】(1)<7 (2)ACE
(3)(任答其中一点)
图1,用滴管吸取液体时,应先捏扁胶头赶尽气体,再伸入试剂瓶中吸液
图2,滴管应放在洁净的烧杯内
图3,滴瓶上的滴管用后应不经洗涤直接放回原滴瓶
图4,应将滴管尖口向下
(4)节约药品
五、计算类综合题。
26、长久使用的热水壶内都会有一层水垢,已知其主要成分是碳酸钙和氢氧化镁,用稀盐酸可以清除这些水垢。某校化学课外活动小组同学在测定水垢中碳酸钙的含量时,在200g水垢中加入足量的稀盐酸,并同时测量了3分钟内产生气体的质量,有关数据如下:
时间/s 0 30 50 90 120 150 180
气体质量/g 0 30 50 60 80 66 66
请回答下列问题:
(1)表中有一项测量结果有较大的误差,其对应的时间是________。
(2)水垢中碳酸钙的质量分数是多少?________ 。
【答案】 120 ;75%
【详解】(1)根据表格中的前四次的数据分析,二氧化碳的生成量应该逐渐增多的,但在120s时突然增大,而后又减下来了,说明此时间时的测量有较大的误差。
(2)由于稀盐酸是足量的,由表格中的最后两次数据没变可知,在150s时碳酸钙已完全反应了,由此可得到生成气体(CO2)的质量为66g,再根据碳酸钙与盐酸反应的化学方程式可以计算出碳酸钙的质量。
解:设200g水垢中碳酸钙的质量为x
CaCO3 + 2HCl = CaCl2 + H2O +CO2↑
100 44
x 66g
解得,x=150g
则水垢中碳酸钙的质量分数是×100%=75%。
答:水垢中碳酸钙的质量分数是75%。
鲁教版(五四学制)第2单元 常见的酸和碱
一、选择题。(16题)
1、工人师傅除去锅炉内的水垢[主要成分是CaCO3和Mg(OH)2]时,选用的试剂是( )
A. 稀盐酸 B. 烧碱溶液 C. 石灰水 D. 食盐水
2、下列物质的性质与用途对应关系错误的是( )
A. 金刚石硬度大,可制造钻头
B. 镁燃烧发出耀眼白光,可用制作烟花
C. 铜有良好的导电性,可制作导线
D. 氢氧化钠具有碱性,常用于改良酸性土壤
3、向pH=3的溶液中滴加石蕊试剂,溶液呈( )
A. 无色 B. 紫色 C. 红色 D. 蓝色
4、下列各组离子在pH=1的溶液中能大量共存的是( )
A. NH4+ NO3﹣ Na+ Cl﹣ B. CO32﹣ K+ Na+ SO42﹣
C. Cu2+ OH﹣ Cl﹣ Ba2+ D. Ag+ NO3﹣ Cl﹣ Na+
5、下列说法正确的是( )
A. 酒精是最常用是消毒药,体积分数为95%的酒精杀菌能力最强
B. 亚硝酸钠(NaNO2)外观极像食盐,且具有与食盐一样的咸味,但被误作食盐食用,会导致中毒事故发生
C. 为了防止大脖子病,食用的是加入碘化钾的食盐
D. 市售食醋中含乙酸约为30%﹣50%
6、化学实验中常会出现一些“出乎意料”的现象或结果,下列各项对相关异常情况的解释不合理的是( )
实验 验证氧气的化学性质 除去粗盐中的泥沙 测定空气中氧气的含量 检验实验室制出的二氧化碳
异常情况 未看到火星四射 滤液浑浊 测定结果偏大 澄清石灰水未变浑浊
选项 A.可能是温度未达到铁丝的着火点 B.可能是滤纸破损 C.可能是红磷的量不足 D.可能是二氧化碳中混有氯化氢气体
A.A B.B C.C D.D
7、下列实验基本操作错误的是( )
A. B. C. D.
8、下列做法符合科学常识的是( )
A. 天然气泄漏,用燃着的木条检验
B. 胃酸过多的人,可以喝一点氢氧化钠溶液来中和
C. 保险丝烧断了,可以用铜丝代替
D. 有人触电,不可以用手直接拿开电线
9、下列物质属于酸类的是( )
A.CO2 B. HNO3 C.NaOH D. NaCl
10、某同学的化学笔记上有以下知识总结,你认为正确的是( )
A. 生成盐和水的反应不一定是中和反应
B. 含有氧元素的化合物称为氧化物
C. 由同种元素组成的物质称为单质
D. 固体物质的溶解度都随温度的升高而增大
11、下列图象能正确反映对应变化关系的是( )
A B C D
向接近饱和的NaCl溶液中加入固体NaCl 向等质量、等质量分数的两份稀硫酸中分别加入MgO和Mg(OH)2 向Na2CO3溶液中加入一定溶质质量分数的NaOH溶液 等质量、等质量分数的H2SO4溶液与NaOH溶液混合
A. A B. B C. C D. D
12、下列图像不能正确反映对应变化关系的是( )
A.室温(25℃)下往石灰水中不断加入氧化钙
B.往CuSO4和H2SO4的混合溶液中加入NaOH溶液
C.碳酸钙高温分解
D.往硫酸和盐酸的混合液中不断加入氢氧化钡溶液
13、推理是化学学习中常见的思维方法,下列推理正确的是( )
A. 锌和铜均是金属,锌与稀硫酸反应生成氢气,则铜也能与稀硫酸反应生成氢气
B. 气体的溶解度随温度的升高而减小,所以温度越高,氧气的溶解度越小
C. 稀盐酸与稀硫酸的化学性质相似,所以实验室可以用大理石与稀硫酸制取二氧化碳
D. 催化剂在反应前后质量不变,因此反应前后质量不变的物质一定是催化剂
14、某同学在用pH试纸测定氢氧化钠溶液的pH时,错误地将pH试纸先进行了湿润,则其测定的数值应该是( )
A. 变大 B. 变小 C. 不变 D. 无法确定
15、某环境监测兴趣小组的同学监测到南京市某年近60%的降雨PH<5.6,这种雨水( )
A.能是酚酞试液变红 B.中性 C.酸性 D.碱性
16、 “关爱生命,注意安全,拥抱健康”是永恒的主题。下列有关叙述错误的是( )
A. 健康人体胃液的pH范围在0.9~1.5
B. 幼儿及青少年缺钙会产生骨质疏松
C. 人体缺乏维生素A会引起夜盲症
D. 霉变食物绝对不能食用
二、填空题。
17、化学与生活密切相关。
醋和食盐是日常生活中必备调味品
(1)食盐通过晾晒海水或煮盐井水、盐湖水再经过净化得到;醋通过大米、高粱等粮食发酵酿制而成.晾晒和发酵两种变化的本质区别是______ 。
(2)醋的有效成分是乙酸(CH3COOH),也叫醋酸.正在服碳酸氢钠片、复方氢氧化铝等药品的人,不宜食用醋,原因是______ 。
18、经过“碱的化学性质”的学习,小明同学用如图所示的示意图归纳总结了NaOH四条化学性质。
(1)为了验证反应②,小明同学向NaOH溶液中滴入无色酚酞试液,观察到无色酚酞试液变为红色,使无色酚酞试液变为红色的微粒是_ __(填微粒符号)。
(2)为了验证反应③能够发生,可以选用的试剂是__ __。
A.CuCl2 B.NaCl C.CuSO4 D.Na2CO3
(3)NaOH溶液露置于空气中易变质,所以必须密封保存。请你写出NaOH溶液变质的化学方程式:__ __。
(4)第(3)问中的化学反应是体现了图中NaOH的性质__ __(填“①”“②”“③”或“④”)。
(5)根据第(2)问提供的试剂写出反应③时可观察到的现象是__ __,反应方程式为: 、
。
19、化学实验小组的同学尝试寻找生活中的物质制作酸碱指示剂。以下表格是分别向不同试剂中滴加2滴自制紫薯汁的现象,请回答:
试剂 稀盐酸 氢氧化钠溶液 蒸馏水 白醋 草木灰溶液
现象 红色 绿色 紫色 红色 绿色
(1)紫薯汁______(填“能”或“不能”)作酸碱指示剂。
(2)草木灰溶液呈______(填“酸性”“中性”或“碱性”)。
20、有A、B、C、D四种元素,其原子结构示意图如图:
(1)D元素的名称为________ ,D元素与图中________ (填写字母序号)元素的化学性质相似,D元素的离子符号为________ 。
(2)A、B、C三种元素能形成一种化合物,其水溶液的pH________ 7。
(填>、<、=)
(3)A、B两种元素的原子以1:1的比例形成的化合物为(写化学式)________ ,其中B元素化合价为________。
21、金属是一种非常重要的资源,在生产、生活中有着广泛的用途。
(1)人类每年从自然界提取大量的金属,其中提取量最大的是铁.用赤铁矿和一氧化碳炼铁的化学方程式为________。
(2)央视3 15晚会曝光某品牌汽车厂为了节约成本,采用价格相对便宜的普通钢板代替防腐性能较好的镀锌板,造成钢板生锈,给车主带来极大安全隐患.普通钢板在空气中锈蚀,实际上是铁跟空气中的________共同作用的结果。
(3)请写出工业上用稀硫酸除铁锈的化学反应方程式________。
(4)亮亮同学用稀盐酸和另一种溶液,验证了Mg、Fe、Cu、Ag四种金属的活动性顺序是依次减弱的.请问亮亮所用的另一种溶液是________。
22、将稀盐酸分别滴入如图所示盛有不同物质的试管中、请回答下列问题:
(1)有气泡产生的试管为______(填序号)。
(2)不与稀盐酸发生反应的物质是______。
(3)实验后试管②中溶液变为______色,该试管中发生反应的化学方程式为:
______ 。
三、推断题。
23、如图所示:已知A、B、C、D、E均为常见的物质,且A是一种最常用的溶剂,C可改良酸性土壤,B、C、D、E属于不同种类物质且含有相同的一种元素,图中“—”表示相连的物质在一定条件下可以反应,“→”表示物质间存在转化关系。请回答下列问题。
(1)D的化学式为__________,A→C反应的基本反应类型为__________。
(2)B与C反应的化学方程式为__________ 。
(3)C、E反应可用于制取烧碱,请写出该反应的化学方程式:__________。
四、实验题。
24、在保存药品时,可能会在容器中放置铁粉与碱石灰。现有久置的铁粉和碱石灰固体,同学们设计实验进行探究。
【提出问题】该固体样品的成分是什么?
【查阅资料】(1)碱石灰是一种常用干燥剂,是CaO和NaOH的混合物。
(2)BaCl2溶液显中性。
【猜想与假设】固体样品中可能含有Fe、Fe2O3、CaO、NaOH、Ca(OH)2、Na2CO3和_________等物质。
【进行实验】
甲组同学对滤渣B的成分进行探究,记录如下:
实验操作 实验现象 实验结论及化学方程式
取少量滤渣B于试管中,加入足量稀盐酸,将生成的气体通入澄清的石灰水中 ①__________。②__________。 结论:滤渣B中有Fe2O3,CaCO3。盐酸和Fe2O3反应的化学方程式为:____________。
乙组同学对滤液C的成分进行探究,记录如下:
实验操作 实验现象 实验结论
取少量滤液C于试管中,加入过量BaC12溶液,静置,向上层清液中滴加无色酚酞试液,振荡 ①有白色沉淀生成②酚酞试液由无色变成红色 溶液C中有__________。
(1)乙组同学实验中加入过量BaCl2溶液的目的是____________ 。
(2)通过以上实验探究,该固体样品的组成一定有___________ _,可能有____________。
25、某市初中化学实验操作考查内容为“溶液酸碱性的检验”。请根据实验回答下列问题。
(1)测得碳酸饮料的pH _____ 7(填“<”或“=”或“>”)。
(2)下列使用pH试纸的方法中,正确的是_____(填序号)。
A.将pH试纸剪成几段使用
B.将pH试纸直接插入待测液中
C.将pH试纸放在表面皿上,用干净的玻璃棒蘸取待测液滴在pH试纸上
D.将pH试纸湿润后放在表面皿上,用干净的玻璃棒蘸取待测液滴在pH试纸上
E.读数时,在30秒内将pH试纸呈现的颜色与标准比色卡对照
(3)本次实验中滴管使用出现了如图1~图2所示的四种常见错误操作。请你从这四幅图中任意选择一幅(请写明所选图的序号),具体说明改正错误的方法:
_____ 。
图1 图2 图3 图4
(4)使用白色点滴板完成实验有显色明显、便于对比、_____(填一项)等优点。
五、计算类综合题。
26、长久使用的热水壶内都会有一层水垢,已知其主要成分是碳酸钙和氢氧化镁,用稀盐酸可以清除这些水垢。某校化学课外活动小组同学在测定水垢中碳酸钙的含量时,在200g水垢中加入足量的稀盐酸,并同时测量了3分钟内产生气体的质量,有关数据如下:
时间/s 0 30 50 90 120 150 180
气体质量/g 0 30 50 60 80 66 66
请回答下列问题:
(1)表中有一项测量结果有较大的误差,其对应的时间是________。
(2)水垢中碳酸钙的质量分数是多少?________ 。
2023—2024学年鲁教版(五四学制)化学九年级全一册第2单元 常见的酸和碱 期末复习基础题附答案
鲁教版(五四学制)第2单元 常见的酸和碱
一、选择题。(16题)
1、工人师傅除去锅炉内的水垢[主要成分是CaCO3和Mg(OH)2]时,选用的试剂是( )
A. 稀盐酸 B. 烧碱溶液 C. 石灰水 D. 食盐水
【答案】A
2、下列物质的性质与用途对应关系错误的是( )
A. 金刚石硬度大,可制造钻头
B. 镁燃烧发出耀眼白光,可用制作烟花
C. 铜有良好的导电性,可制作导线
D. 氢氧化钠具有碱性,常用于改良酸性土壤
【答案】D
3、向pH=3的溶液中滴加石蕊试剂,溶液呈( )
A. 无色 B. 紫色 C. 红色 D. 蓝色
【答案】C
4、下列各组离子在pH=1的溶液中能大量共存的是( )
A. NH4+ NO3﹣ Na+ Cl﹣ B. CO32﹣ K+ Na+ SO42﹣
C. Cu2+ OH﹣ Cl﹣ Ba2+ D. Ag+ NO3﹣ Cl﹣ Na+
【答案】A
5、下列说法正确的是( )
A. 酒精是最常用是消毒药,体积分数为95%的酒精杀菌能力最强
B. 亚硝酸钠(NaNO2)外观极像食盐,且具有与食盐一样的咸味,但被误作食盐食用,会导致中毒事故发生
C. 为了防止大脖子病,食用的是加入碘化钾的食盐
D. 市售食醋中含乙酸约为30%﹣50%
【答案】B
6、化学实验中常会出现一些“出乎意料”的现象或结果,下列各项对相关异常情况的解释不合理的是( )
实验 验证氧气的化学性质 除去粗盐中的泥沙 测定空气中氧气的含量 检验实验室制出的二氧化碳
异常情况 未看到火星四射 滤液浑浊 测定结果偏大 澄清石灰水未变浑浊
选项 A.可能是温度未达到铁丝的着火点 B.可能是滤纸破损 C.可能是红磷的量不足 D.可能是二氧化碳中混有氯化氢气体
A.A B.B C.C D.D
【答案】C
7、下列实验基本操作错误的是( )
A. B. C. D.
【答案】A
8、下列做法符合科学常识的是( )
A. 天然气泄漏,用燃着的木条检验
B. 胃酸过多的人,可以喝一点氢氧化钠溶液来中和
C. 保险丝烧断了,可以用铜丝代替
D. 有人触电,不可以用手直接拿开电线
【答案】D
9、下列物质属于酸类的是( )
A.CO2 B. HNO3 C.NaOH D. NaCl
【答案】B
10、某同学的化学笔记上有以下知识总结,你认为正确的是( )
A. 生成盐和水的反应不一定是中和反应
B. 含有氧元素的化合物称为氧化物
C. 由同种元素组成的物质称为单质
D. 固体物质的溶解度都随温度的升高而增大
【答案】A
11、下列图象能正确反映对应变化关系的是( )
A B C D
向接近饱和的NaCl溶液中加入固体NaCl 向等质量、等质量分数的两份稀硫酸中分别加入MgO和Mg(OH)2 向Na2CO3溶液中加入一定溶质质量分数的NaOH溶液 等质量、等质量分数的H2SO4溶液与NaOH溶液混合
A. A B. B C. C D. D
【答案】D
12、下列图像不能正确反映对应变化关系的是( )
A.室温(25℃)下往石灰水中不断加入氧化钙
B.往CuSO4和H2SO4的混合溶液中加入NaOH溶液
C.碳酸钙高温分解
D.往硫酸和盐酸的混合液中不断加入氢氧化钡溶液
【答案】A
13、推理是化学学习中常见的思维方法,下列推理正确的是( )
A. 锌和铜均是金属,锌与稀硫酸反应生成氢气,则铜也能与稀硫酸反应生成氢气
B. 气体的溶解度随温度的升高而减小,所以温度越高,氧气的溶解度越小
C. 稀盐酸与稀硫酸的化学性质相似,所以实验室可以用大理石与稀硫酸制取二氧化碳
D. 催化剂在反应前后质量不变,因此反应前后质量不变的物质一定是催化剂
【答案】B
14、某同学在用pH试纸测定氢氧化钠溶液的pH时,错误地将pH试纸先进行了湿润,则其测定的数值应该是( )
A. 变大 B. 变小 C. 不变 D. 无法确定
【答案】B
15、某环境监测兴趣小组的同学监测到南京市某年近60%的降雨PH<5.6,这种雨水( )
A.能是酚酞试液变红 B.中性 C.酸性 D.碱性
【答案】C
16、 “关爱生命,注意安全,拥抱健康”是永恒的主题。下列有关叙述错误的是( )
A. 健康人体胃液的pH范围在0.9~1.5
B. 幼儿及青少年缺钙会产生骨质疏松
C. 人体缺乏维生素A会引起夜盲症
D. 霉变食物绝对不能食用
【答案】B
二、填空题。
17、化学与生活密切相关。
醋和食盐是日常生活中必备调味品
(1)食盐通过晾晒海水或煮盐井水、盐湖水再经过净化得到;醋通过大米、高粱等粮食发酵酿制而成.晾晒和发酵两种变化的本质区别是______ 。
(2)醋的有效成分是乙酸(CH3COOH),也叫醋酸.正在服碳酸氢钠片、复方氢氧化铝等药品的人,不宜食用醋,原因是______ 。
【答案】是否有新物质生成 乙酸能和服用的药品反应,降低药效
18、经过“碱的化学性质”的学习,小明同学用如图所示的示意图归纳总结了NaOH四条化学性质。
(1)为了验证反应②,小明同学向NaOH溶液中滴入无色酚酞试液,观察到无色酚酞试液变为红色,使无色酚酞试液变为红色的微粒是_ __(填微粒符号)。
(2)为了验证反应③能够发生,可以选用的试剂是__ __。
A.CuCl2 B.NaCl C.CuSO4 D.Na2CO3
(3)NaOH溶液露置于空气中易变质,所以必须密封保存。请你写出NaOH溶液变质的化学方程式:__ __。
(4)第(3)问中的化学反应是体现了图中NaOH的性质__ __(填“①”“②”“③”或“④”)。
(5)根据第(2)问提供的试剂写出反应③时可观察到的现象是__ __,反应方程式为: 、
。
【答案】(1)OH- (2)AC (3)2NaOH+CO2===Na2CO3+H2O (4)④
(5)产生蓝色沉淀 CuCl2+2NaOH===Cu(OH)2↓+2NaCl
CuSO4+2NaOH===Cu(OH)2↓+Na2SO4
19、化学实验小组的同学尝试寻找生活中的物质制作酸碱指示剂。以下表格是分别向不同试剂中滴加2滴自制紫薯汁的现象,请回答:
试剂 稀盐酸 氢氧化钠溶液 蒸馏水 白醋 草木灰溶液
现象 红色 绿色 紫色 红色 绿色
(1)紫薯汁______(填“能”或“不能”)作酸碱指示剂。
(2)草木灰溶液呈______(填“酸性”“中性”或“碱性”)。
【答案】(1)能 (2)碱性
20、有A、B、C、D四种元素,其原子结构示意图如图:
(1)D元素的名称为________ ,D元素与图中________ (填写字母序号)元素的化学性质相似,D元素的离子符号为________ 。
(2)A、B、C三种元素能形成一种化合物,其水溶液的pH________ 7。
(填>、<、=)
(3)A、B两种元素的原子以1:1的比例形成的化合物为(写化学式)________ ,其中B元素化合价为________。
【答案】硫;B;S2﹣;>;H2O2;﹣1
21、金属是一种非常重要的资源,在生产、生活中有着广泛的用途。
(1)人类每年从自然界提取大量的金属,其中提取量最大的是铁.用赤铁矿和一氧化碳炼铁的化学方程式为________。
(2)央视3 15晚会曝光某品牌汽车厂为了节约成本,采用价格相对便宜的普通钢板代替防腐性能较好的镀锌板,造成钢板生锈,给车主带来极大安全隐患.普通钢板在空气中锈蚀,实际上是铁跟空气中的________共同作用的结果。
(3)请写出工业上用稀硫酸除铁锈的化学反应方程式________。
(4)亮亮同学用稀盐酸和另一种溶液,验证了Mg、Fe、Cu、Ag四种金属的活动性顺序是依次减弱的.请问亮亮所用的另一种溶液是________。
【答案】(1)Fe2O3+3CO 2Fe+3CO2 (2)氧气和水
(3)Fe2O3+3H2SO4═Fe2(SO4)3+3H2O (4)硝酸银溶液
22、将稀盐酸分别滴入如图所示盛有不同物质的试管中、请回答下列问题:
(1)有气泡产生的试管为______(填序号)。
(2)不与稀盐酸发生反应的物质是______。
(3)实验后试管②中溶液变为______色,该试管中发生反应的化学方程式为:
______ 。
【答案】(1)③⑤ (2)铜片 (3) 黄色
三、推断题。
23、如图所示:已知A、B、C、D、E均为常见的物质,且A是一种最常用的溶剂,C可改良酸性土壤,B、C、D、E属于不同种类物质且含有相同的一种元素,图中“—”表示相连的物质在一定条件下可以反应,“→”表示物质间存在转化关系。请回答下列问题。
(1)D的化学式为__________,A→C反应的基本反应类型为__________。
(2)B与C反应的化学方程式为__________ 。
(3)C、E反应可用于制取烧碱,请写出该反应的化学方程式:__________。
【答案】(1)H2SO4 化合反应
(2) (3)
四、实验题。
24、在保存药品时,可能会在容器中放置铁粉与碱石灰。现有久置的铁粉和碱石灰固体,同学们设计实验进行探究。
【提出问题】该固体样品的成分是什么?
【查阅资料】(1)碱石灰是一种常用干燥剂,是CaO和NaOH的混合物。
(2)BaCl2溶液显中性。
【猜想与假设】固体样品中可能含有Fe、Fe2O3、CaO、NaOH、Ca(OH)2、Na2CO3和_________等物质。
【进行实验】
甲组同学对滤渣B的成分进行探究,记录如下:
实验操作 实验现象 实验结论及化学方程式
取少量滤渣B于试管中,加入足量稀盐酸,将生成的气体通入澄清的石灰水中 ①__________。②__________。 结论:滤渣B中有Fe2O3,CaCO3。盐酸和Fe2O3反应的化学方程式为:____________。
乙组同学对滤液C的成分进行探究,记录如下:
实验操作 实验现象 实验结论
取少量滤液C于试管中,加入过量BaC12溶液,静置,向上层清液中滴加无色酚酞试液,振荡 ①有白色沉淀生成②酚酞试液由无色变成红色 溶液C中有__________。
(1)乙组同学实验中加入过量BaCl2溶液的目的是____________ 。
(2)通过以上实验探究,该固体样品的组成一定有___________ _,可能有____________。
【答案】【猜想与假设】CaCO3##碳酸钙
【进行实验】
滤渣完全溶解,溶液变为黄色 澄清石灰水变浑浊
Fe2O3+6HCl=2FeCl3+3H2O
Na2CO3和NaOH
(1)检验并除去碳酸钠,以防止对检验氢氧化钠产生影响
(2)Fe、Fe2O3、Ca(OH)2、Na2CO3 CaCO3##碳酸钙
25、某市初中化学实验操作考查内容为“溶液酸碱性的检验”。请根据实验回答下列问题。
(1)测得碳酸饮料的pH _____ 7(填“<”或“=”或“>”)。
(2)下列使用pH试纸的方法中,正确的是_____(填序号)。
A.将pH试纸剪成几段使用
B.将pH试纸直接插入待测液中
C.将pH试纸放在表面皿上,用干净的玻璃棒蘸取待测液滴在pH试纸上
D.将pH试纸湿润后放在表面皿上,用干净的玻璃棒蘸取待测液滴在pH试纸上
E.读数时,在30秒内将pH试纸呈现的颜色与标准比色卡对照
(3)本次实验中滴管使用出现了如图1~图2所示的四种常见错误操作。请你从这四幅图中任意选择一幅(请写明所选图的序号),具体说明改正错误的方法:
_____ 。
图1 图2 图3 图4
(4)使用白色点滴板完成实验有显色明显、便于对比、_____(填一项)等优点。
【答案】(1)<7 (2)ACE
(3)(任答其中一点)
图1,用滴管吸取液体时,应先捏扁胶头赶尽气体,再伸入试剂瓶中吸液
图2,滴管应放在洁净的烧杯内
图3,滴瓶上的滴管用后应不经洗涤直接放回原滴瓶
图4,应将滴管尖口向下
(4)节约药品
五、计算类综合题。
26、长久使用的热水壶内都会有一层水垢,已知其主要成分是碳酸钙和氢氧化镁,用稀盐酸可以清除这些水垢。某校化学课外活动小组同学在测定水垢中碳酸钙的含量时,在200g水垢中加入足量的稀盐酸,并同时测量了3分钟内产生气体的质量,有关数据如下:
时间/s 0 30 50 90 120 150 180
气体质量/g 0 30 50 60 80 66 66
请回答下列问题:
(1)表中有一项测量结果有较大的误差,其对应的时间是________。
(2)水垢中碳酸钙的质量分数是多少?________ 。
【答案】 120 ;75%
【详解】(1)根据表格中的前四次的数据分析,二氧化碳的生成量应该逐渐增多的,但在120s时突然增大,而后又减下来了,说明此时间时的测量有较大的误差。
(2)由于稀盐酸是足量的,由表格中的最后两次数据没变可知,在150s时碳酸钙已完全反应了,由此可得到生成气体(CO2)的质量为66g,再根据碳酸钙与盐酸反应的化学方程式可以计算出碳酸钙的质量。
解:设200g水垢中碳酸钙的质量为x
CaCO3 + 2HCl = CaCl2 + H2O +CO2↑
100 44
x 66g
解得,x=150g
则水垢中碳酸钙的质量分数是×100%=75%。
答:水垢中碳酸钙的质量分数是75%。
同课章节目录
- 第一单元 溶液
- 1 溶液的形成
- 2 溶液组成的定量表示
- 3物质的溶解性
- 到实验室去:配制一定溶质质量分数的溶液
- 第二单元 常见的酸和碱
- 1 酸及其性质
- 2 碱及其性质
- 3 溶液的酸碱性
- 4 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 到图书馆去:分子变成离子
- 第三单元 海水中的化学
- 1 海洋化学资源
- 2 海水“晒盐”
- 3 海水“制碱”
- 到实验室去:粗盐中难溶性杂质的去除
- 第四单元 金属
- 1 常见的金属材料
- 2 金属的化学性质
- 3 钢铁的锈蚀与防护
- 到实验室去:探究金属的性质
- 第五单元 化学与健康
- 1 食物中的有机物
- 2 化学元素与人体健康
- 3 远离有毒物质
- 第六单元 化学与社会发展
- 1 化学与能源开发
- 2 化学与材料研制
- 3 化学与农业生产
- 4 化学与环境保护
