2023—2024学年鲁教版化学九年级上册第五单元 定量研究化学反应 单元训练题(含答案)
文档属性
| 名称 | 2023—2024学年鲁教版化学九年级上册第五单元 定量研究化学反应 单元训练题(含答案) |

|
|
| 格式 | doc | ||
| 文件大小 | 520.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-12-22 00:00:00 | ||
图片预览



文档简介
2023—2024学年鲁教版化学九年级上册第五单元 定量研究化学反应 单元训练题含答案
鲁教版第五单元 定量研究化学反应
一、选择题。(16题)
1、在化学方程式:C2H8N2 + 2N2O4 = 3X + 2CO2 + 4H2O中,X 的化学式为( )
A. N2 B. H2 C. O2 D. CO
2、已知 分别表示X、Y、Z三种不同的气体分子,在一定条件下的变化如图所示,由图示获得的下列信息中错误的是( )
A.在化学变化中,分子、原子一定发生改变
B.该反应的基本反应类型属于化合反应
C.保持三种物质化学性质最小的微粒是分子
D.若是氧分子,则该反应会放热
3、高纯度的单晶硅是制做电子集成电路的基础材料。工业上制备高纯硅的化学反应原理为:
①SiO2+2CSi +2CO↑、②Si+3HClHSiCl3+H2、③HSiCl3+H2Si+3X,反应①制得粗硅,通过反应②③进一步得到高纯硅;三氯硅烷(HSiCl3)的沸点是31.8℃。下列有关说法不正确的是( )
A.反应③中X的化学式为HCl
B.三氯硅烷由氢、硅、氯三种元素组成
C.三氯硅烷中硅、氯元素的质量比为1∶3
D.反应②③实现了硅元素的富集,将粗硅转化为高纯硅
4、在密闭容器中有甲、乙、丙、丁四种物质,在一定条件下充分反应,测得反应前后各物质的质量分数如图所示:下列说法中正确的是( )
A.丙可能是单质
B.在该反应中丁一定没有参加化学反应
C.甲和乙的质量之和一定等于生成丙的质量
D.该反应是化合反应
5、吐火,是川剧中独一无二的神秘绝技。吐火有一个绝窍,那就是眼前的火尚未熄灭之时,绝对不能吸气,否则最直接的后果就是“引火焚身”。屏住呼吸时,嘴巴里的煤油没有燃烧的原因是( )
A.缺乏氧气 B.没有达到煤油的着火点
C.缺乏可燃物 D.嘴巴里的唾液使煤油不易着火
6、利用催化剂可消除室内装修材料释放的甲醛,如图所示为该反应的微观示意图。下列说法不正确的是( )
A.甲醛的化学式为CH2O
B.生成物丙和丁中氧元素的化合价相同
C.生成物丙由1个碳原子和2个氧原子构成
D.参加反应的甲和生成的丁分子个数比为1:1
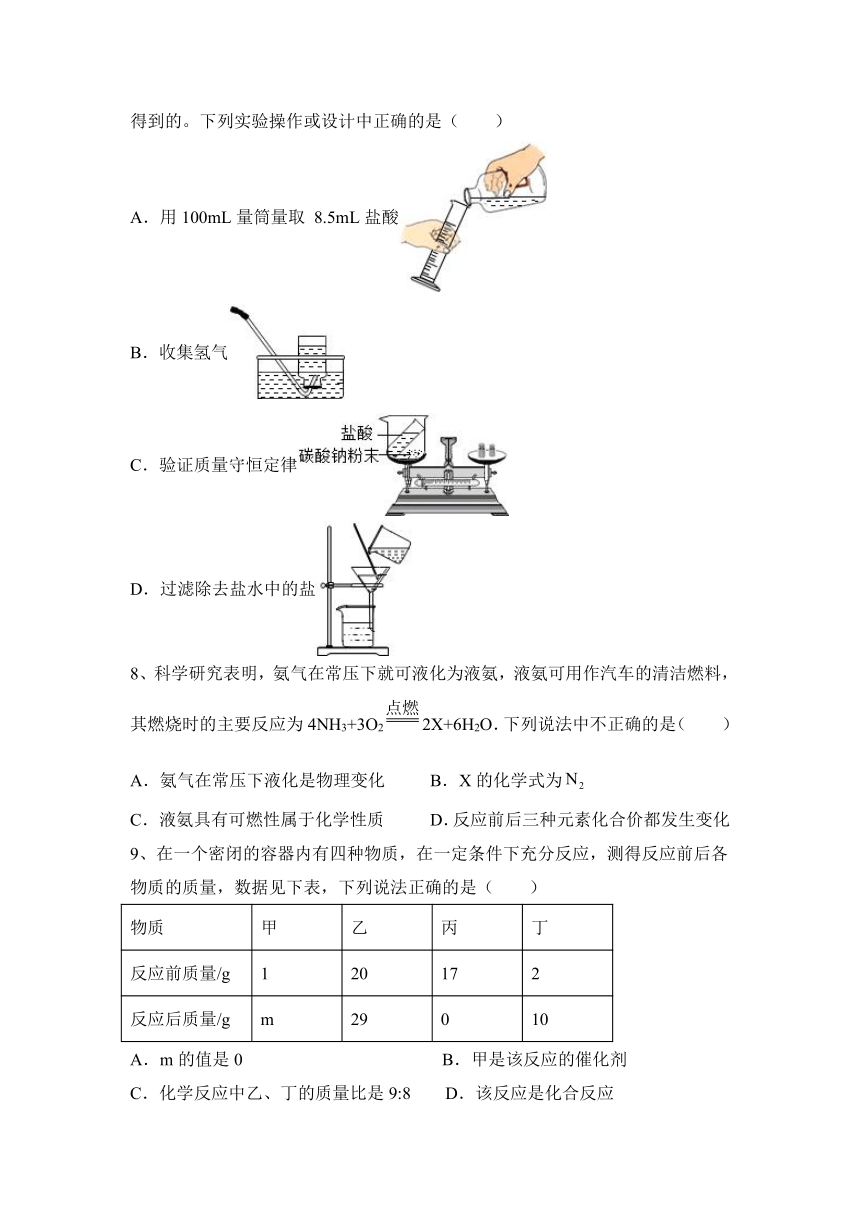
7、化学是一门以实验为基础的科学,许多化学重大发现和研究成果都是通过实验得到的。下列实验操作或设计中正确的是( )
A.用100mL量筒量取 8.5mL盐酸
B.收集氢气
C.验证质量守恒定律
D.过滤除去盐水中的盐
8、科学研究表明,氨气在常压下就可液化为液氨,液氨可用作汽车的清洁燃料,其燃烧时的主要反应为4NH3+3O22X+6H2O.下列说法中不正确的是( )
A.氨气在常压下液化是物理变化 B.X的化学式为
C.液氨具有可燃性属于化学性质 D.反应前后三种元素化合价都发生变化
9、在一个密闭的容器内有四种物质,在一定条件下充分反应,测得反应前后各物质的质量,数据见下表,下列说法正确的是( )
物质 甲 乙 丙 丁
反应前质量/g 1 20 17 2
反应后质量/g m 29 0 10
A.m的值是0 B.甲是该反应的催化剂
C.化学反应中乙、丁的质量比是9:8 D.该反应是化合反应
10、古语道:“人要实,火要虚”。从燃烧的条件看,“火要虚”的实质是( )
A.增大可燃物的热值 B.提高空气中氧气的含量
C.提高可燃物的着火点 D.增大可燃物与空气的接触面积
11、在一个密闭容器中放入P、Q、R、W四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表。则关于此反应的认识正确的是( )
物质 P Q R W
反应前的质量(g) 5 2 14 18
反应后的质量(g) 20 x 4 13
A.参加化学反应的P和W的质量比为3:2
B.该反应用现象表示为:
C.反应后容器中R与Q的质量比为1:2
D.Q在反应中可能作催化剂
12、推理是学习化学的一种重要方法,但不合理的推理会得出错误的结论。以下推理正确的是( )
A.分子可以构成物质,物质一定是由分子构成的
B.离子是带电荷的微粒,带电荷的微粒一定是离子
C.最外层电子数相同的原子化学性质相似,氦原子和镁原子的化学性质也相似
D.含碳元素的物质充分燃烧会生成CO2,燃烧能生成CO2的物质一定含碳元素
13、下列关于S+O2SO2的理解正确的是( )
A.表示硫与氧气在点燃条件下反应生成二氧化硫
B.参加反应的硫与氧气的质量比是2:1
C.反应前后硫原子、氧分子的个数均不变
D.参加反应的氧气与生成的二氧化硫的分子个数比为2:1
14、在一个密闭容器中,充入2m个CO分子和n个O2分子,在一定条件下充分反应后容器内碳原子与氧原子的个数比为
A.m/(m+2m) B.m/2(m+n) C.m/n D.m/(m+n)
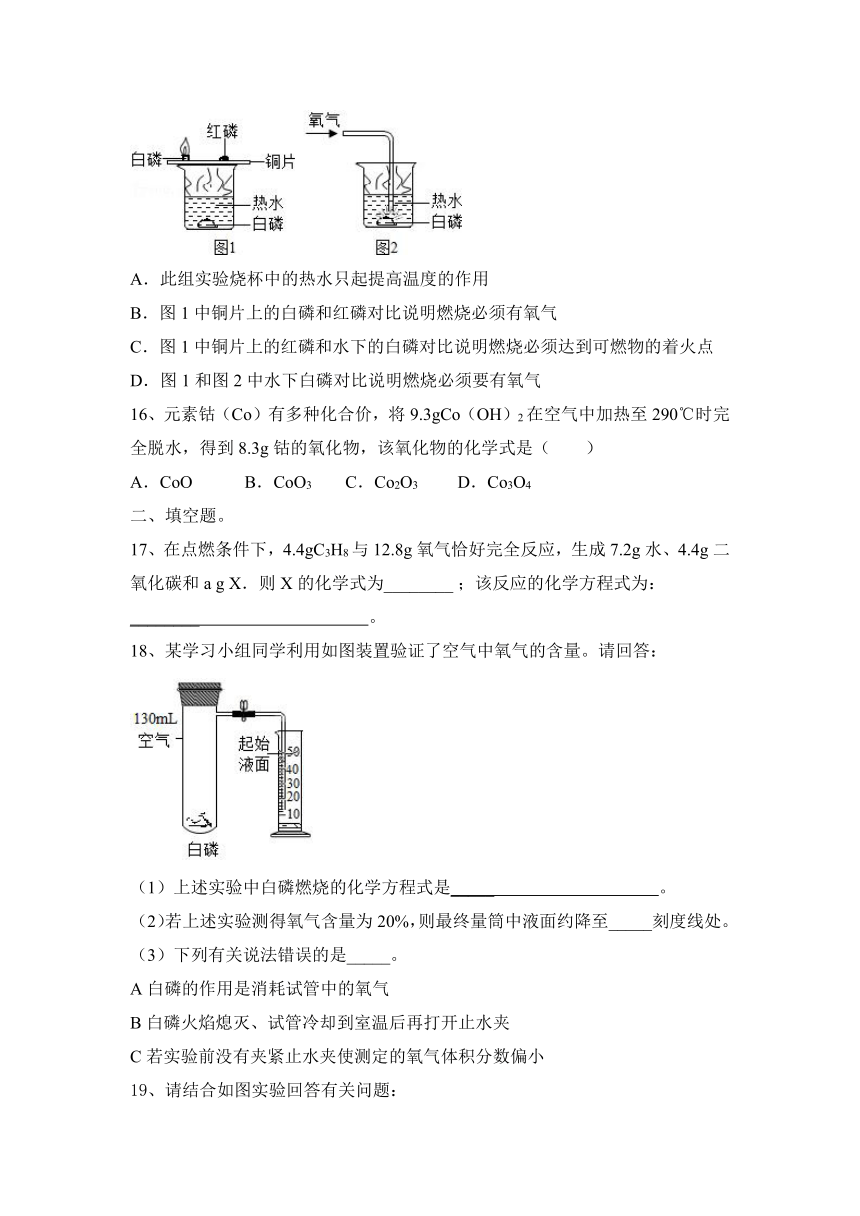
15、如图所示的一组实验可用于研究燃烧条件。下列说法中,正确的是( )
A.此组实验烧杯中的热水只起提高温度的作用
B.图1中铜片上的白磷和红磷对比说明燃烧必须有氧气
C.图1中铜片上的红磷和水下的白磷对比说明燃烧必须达到可燃物的着火点
D.图1和图2中水下白磷对比说明燃烧必须要有氧气
16、元素钴(Co)有多种化合价,将9.3gCo(OH)2在空气中加热至290℃时完全脱水,得到8.3g钴的氧化物,该氧化物的化学式是( )
A.CoO B.CoO3 C.Co2O3 D.Co3O4
二、填空题。
17、在点燃条件下,4.4gC3H8与12.8g氧气恰好完全反应,生成7.2g水、4.4g二氧化碳和a g X.则X的化学式为________ ;该反应的化学方程式为: ________ 。
18、某学习小组同学利用如图装置验证了空气中氧气的含量。请回答:
(1)上述实验中白磷燃烧的化学方程式是_____ 。
(2)若上述实验测得氧气含量为20%,则最终量筒中液面约降至_____刻度线处。
(3)下列有关说法错误的是_____。
A白磷的作用是消耗试管中的氧气
B白磷火焰熄灭、试管冷却到室温后再打开止水夹
C若实验前没有夹紧止水夹使测定的氧气体积分数偏小
19、请结合如图实验回答有关问题:
(1)图中操作a的名称是 ,该操作中所需的玻璃仪器有烧杯、玻璃棒和 。
(2)图中x的值为 。
(3)检验上述实验中产生的气体用 ,反应中共产生该气体的质量为 g。
(4)计算参加反应的过氧化氢的质量是多少
20、某学校化学学习小组设计出如图所示装置,并进行白磷燃烧实验。
(1)当烧杯内的水受热,温度计显示30℃时,打开活塞,在盛有水的试管中有气泡均匀逸出,白磷未燃烧,关闭活塞.锥形瓶内反应的化学方程式是:
。白磷未燃烧的原因是 。
(2)随着水温升高,温度计显示45℃时,再次打开活塞,白磷在水里燃烧.常言道,水火不相容.而本实验中白磷在水里还能够燃烧的原因是:
。水能灭火的原因是:
。
21、绥中化学兴趣小组为了探究质量守恒定律,进行了如图所示的小实验。
在一根用细铜丝吊着的长玻璃管两端,分别绕上40cm长的粗铜丝,并使玻璃棒保持水平。然后用酒精灯给左边一端铜丝加热1~2分钟。停止加热后冷却,仔细观察发生的现象。冷却后,他观察到的现象是:
(1)______ ;
(2)______ 。
(3)写出下沉一端的原因______ 。
三、实验题。
22、回答下列有关实验的问题:
(1)实验中,打开弹簧夹进入瓶中的水不足五分之一,其原因可能是______ 。(答一种即可)
(2)实验中观察到的现象是______ ,该实验说明______ 。
(3)实验中反应结束后小华发现天平指针向右偏转,其原因可能是:
______ 。要通过该实验来验证质量守恒定律,在不更换药品的情况下,你的改进方法是______ 。
23、根据下图完成下列问题。
(1)仪器a的名称是:____________。
(2)加热KMnO4制取O2的化学方程式为____________。
(3)收集O2的装置是____________(选填B或C);
(4)将带火星的木条放在____________,若观察到木条复燃,说明瓶中已充满O2;
(5)若用如图D装置收集氢气,气体应从____________(填“m”或“n”)端进入。
四、计算类综合题。
24、某实验小组的同学为了测定实验室中氯酸钾样品的纯度,取一定质量的该样品与1g二氧化锰混合,其总质量为6g。依次加热该混合物t1、t2、t3、t4时间后,分别冷却称量剩余固体质量,记录的有关数据如下表(样品中的杂质不参与化学反应):
加热时间 t1 t2 t3 t4
剩余固体质量(g) 4.24 4.16 4.08 4.08
试计算:(1)完全反应后产生的氧气的总质量为 。
(2)样品中氯酸钾的纯度是多少?。
2023—2024学年鲁教版化学九年级上册第五单元 定量研究化学反应 单元训练题含答案
鲁教版第五单元 定量研究化学反应
一、选择题。(16题)
1、在化学方程式:C2H8N2 + 2N2O4 = 3X + 2CO2 + 4H2O中,X 的化学式为( )
A. N2 B. H2 C. O2 D. CO
【答案】A
2、已知 分别表示X、Y、Z三种不同的气体分子,在一定条件下的变化如图所示,由图示获得的下列信息中错误的是( )
A.在化学变化中,分子、原子一定发生改变
B.该反应的基本反应类型属于化合反应
C.保持三种物质化学性质最小的微粒是分子
D.若是氧分子,则该反应会放热
【答案】A
3、高纯度的单晶硅是制做电子集成电路的基础材料。工业上制备高纯硅的化学反应原理为:
①SiO2+2CSi +2CO↑、②Si+3HClHSiCl3+H2、③HSiCl3+H2Si+3X,反应①制得粗硅,通过反应②③进一步得到高纯硅;三氯硅烷(HSiCl3)的沸点是31.8℃。下列有关说法不正确的是( )
A.反应③中X的化学式为HCl
B.三氯硅烷由氢、硅、氯三种元素组成
C.三氯硅烷中硅、氯元素的质量比为1∶3
D.反应②③实现了硅元素的富集,将粗硅转化为高纯硅
【答案】 C
4、在密闭容器中有甲、乙、丙、丁四种物质,在一定条件下充分反应,测得反应前后各物质的质量分数如图所示:下列说法中正确的是( )
A.丙可能是单质
B.在该反应中丁一定没有参加化学反应
C.甲和乙的质量之和一定等于生成丙的质量
D.该反应是化合反应
【答案】D
5、吐火,是川剧中独一无二的神秘绝技。吐火有一个绝窍,那就是眼前的火尚未熄灭之时,绝对不能吸气,否则最直接的后果就是“引火焚身”。屏住呼吸时,嘴巴里的煤油没有燃烧的原因是( )
A.缺乏氧气 B.没有达到煤油的着火点
C.缺乏可燃物 D.嘴巴里的唾液使煤油不易着火
【答案】A
6、利用催化剂可消除室内装修材料释放的甲醛,如图所示为该反应的微观示意图。下列说法不正确的是( )
A.甲醛的化学式为CH2O
B.生成物丙和丁中氧元素的化合价相同
C.生成物丙由1个碳原子和2个氧原子构成
D.参加反应的甲和生成的丁分子个数比为1:1
【答案】C
7、化学是一门以实验为基础的科学,许多化学重大发现和研究成果都是通过实验得到的。下列实验操作或设计中正确的是( )
A.用100mL量筒量取 8.5mL盐酸
B.收集氢气
C.验证质量守恒定律
D.过滤除去盐水中的盐
【答案】B
8、科学研究表明,氨气在常压下就可液化为液氨,液氨可用作汽车的清洁燃料,其燃烧时的主要反应为4NH3+3O22X+6H2O.下列说法中不正确的是( )
A.氨气在常压下液化是物理变化 B.X的化学式为
C.液氨具有可燃性属于化学性质 D.反应前后三种元素化合价都发生变化
【答案】 D
9、在一个密闭的容器内有四种物质,在一定条件下充分反应,测得反应前后各物质的质量,数据见下表,下列说法正确的是( )
物质 甲 乙 丙 丁
反应前质量/g 1 20 17 2
反应后质量/g m 29 0 10
A.m的值是0 B.甲是该反应的催化剂
C.化学反应中乙、丁的质量比是9:8 D.该反应是化合反应
【答案】C
10、古语道:“人要实,火要虚”。从燃烧的条件看,“火要虚”的实质是( )
A.增大可燃物的热值 B.提高空气中氧气的含量
C.提高可燃物的着火点 D.增大可燃物与空气的接触面积
【答案】D
11、在一个密闭容器中放入P、Q、R、W四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表。则关于此反应的认识正确的是( )
物质 P Q R W
反应前的质量(g) 5 2 14 18
反应后的质量(g) 20 x 4 13
A.参加化学反应的P和W的质量比为3:2
B.该反应用现象表示为:
C.反应后容器中R与Q的质量比为1:2
D.Q在反应中可能作催化剂
【答案】D
12、推理是学习化学的一种重要方法,但不合理的推理会得出错误的结论。以下推理正确的是( )
A.分子可以构成物质,物质一定是由分子构成的
B.离子是带电荷的微粒,带电荷的微粒一定是离子
C.最外层电子数相同的原子化学性质相似,氦原子和镁原子的化学性质也相似
D.含碳元素的物质充分燃烧会生成CO2,燃烧能生成CO2的物质一定含碳元素
【答案】D
13、下列关于S+O2SO2的理解正确的是( )
A.表示硫与氧气在点燃条件下反应生成二氧化硫
B.参加反应的硫与氧气的质量比是2:1
C.反应前后硫原子、氧分子的个数均不变
D.参加反应的氧气与生成的二氧化硫的分子个数比为2:1
【答案】 A
14、在一个密闭容器中,充入2m个CO分子和n个O2分子,在一定条件下充分反应后容器内碳原子与氧原子的个数比为
A.m/(m+2m) B.m/2(m+n) C.m/n D.m/(m+n)
【答案】D
15、如图所示的一组实验可用于研究燃烧条件。下列说法中,正确的是( )
A.此组实验烧杯中的热水只起提高温度的作用
B.图1中铜片上的白磷和红磷对比说明燃烧必须有氧气
C.图1中铜片上的红磷和水下的白磷对比说明燃烧必须达到可燃物的着火点
D.图1和图2中水下白磷对比说明燃烧必须要有氧气
【答案】D
16、元素钴(Co)有多种化合价,将9.3gCo(OH)2在空气中加热至290℃时完全脱水,得到8.3g钴的氧化物,该氧化物的化学式是( )
A.CoO B.CoO3 C.Co2O3 D.Co3O4
【答案】C
二、填空题。
17、在点燃条件下,4.4gC3H8与12.8g氧气恰好完全反应,生成7.2g水、4.4g二氧化碳和a g X.则X的化学式为________ ;该反应的化学方程式为: ________ 。
【答案】 CO ;C3H8+4O2CO2+4H2O+2CO
18、某学习小组同学利用如图装置验证了空气中氧气的含量。请回答:
(1)上述实验中白磷燃烧的化学方程式是_____ 。
(2)若上述实验测得氧气含量为20%,则最终量筒中液面约降至_____刻度线处。
(3)下列有关说法错误的是_____。
A白磷的作用是消耗试管中的氧气
B白磷火焰熄灭、试管冷却到室温后再打开止水夹
C若实验前没有夹紧止水夹使测定的氧气体积分数偏小
【答案】4P+5O22P2O5 24 C
19、请结合如图实验回答有关问题:
(1)图中操作a的名称是 ,该操作中所需的玻璃仪器有烧杯、玻璃棒和 。
(2)图中x的值为 。
(3)检验上述实验中产生的气体用 ,反应中共产生该气体的质量为 g。
(4)计算参加反应的过氧化氢的质量是多少
【答案】(1)过滤 漏斗 (2)5 (3)带火星的木条 2.4 (4)5.1 g
20、某学校化学学习小组设计出如图所示装置,并进行白磷燃烧实验。
(1)当烧杯内的水受热,温度计显示30℃时,打开活塞,在盛有水的试管中有气泡均匀逸出,白磷未燃烧,关闭活塞.锥形瓶内反应的化学方程式是:
。白磷未燃烧的原因是 。
(2)随着水温升高,温度计显示45℃时,再次打开活塞,白磷在水里燃烧.常言道,水火不相容.而本实验中白磷在水里还能够燃烧的原因是:
。水能灭火的原因是:
。
【答案】(1)2H2O2 2H2O+O2↑;温度未达到白磷的着火点。
(2)温度达到着火点,同时又与氧气充分接触。
可以使可燃物温度降至着火点以下和隔绝氧气。
21、绥中化学兴趣小组为了探究质量守恒定律,进行了如图所示的小实验。
在一根用细铜丝吊着的长玻璃管两端,分别绕上40cm长的粗铜丝,并使玻璃棒保持水平。然后用酒精灯给左边一端铜丝加热1~2分钟。停止加热后冷却,仔细观察发生的现象。冷却后,他观察到的现象是:
(1)______ ;
(2)______ 。
(3)写出下沉一端的原因______ 。
【答案】(1)红色固体变为黑色
(2)玻璃棒向左侧倾斜
(3)铜与氧气反应后固体质量增加
三、实验题。
22、回答下列有关实验的问题:
(1)实验中,打开弹簧夹进入瓶中的水不足五分之一,其原因可能是______ 。(答一种即可)
(2)实验中观察到的现象是______ ,该实验说明______ 。
(3)实验中反应结束后小华发现天平指针向右偏转,其原因可能是:
______ 。要通过该实验来验证质量守恒定律,在不更换药品的情况下,你的改进方法是______ 。
【答案】(1)装置漏气(红磷量不足;未完全冷却就打开弹簧夹读数)
(2)烧杯甲中溶液变为红色 分子在不停地运动 生
(3)成的CO2气体逸散到空气中,未称量到
将烧杯换成密闭容器(将装置改成密闭装置)
23、根据下图完成下列问题。
(1)仪器a的名称是:____________。
(2)加热KMnO4制取O2的化学方程式为____________。
(3)收集O2的装置是____________(选填B或C);
(4)将带火星的木条放在____________,若观察到木条复燃,说明瓶中已充满O2;
(5)若用如图D装置收集氢气,气体应从____________(填“m”或“n”)端进入。
【答案】(1)酒精灯 (2)
(3)B (4)集气瓶口 (5)n
四、计算类综合题。
24、某实验小组的同学为了测定实验室中氯酸钾样品的纯度,取一定质量的该样品与1g二氧化锰混合,其总质量为6g。依次加热该混合物t1、t2、t3、t4时间后,分别冷却称量剩余固体质量,记录的有关数据如下表(样品中的杂质不参与化学反应):
加热时间 t1 t2 t3 t4
剩余固体质量(g) 4.24 4.16 4.08 4.08
试计算:(1)完全反应后产生的氧气的总质量为 。
(2)样品中氯酸钾的纯度是多少?。
【答案及解析】(1)生成氧气的质量为
6g﹣4.08g=1.92g
(2)设样品中氯酸钾的纯度为x。
2KClO32KCl+3O2↑
245 96
(6g﹣1g)×x 1.92g
=,x=98%
答:(1)完全反应后产生的氧气的总质量为1.92g。
(2)样品中氯酸钾的纯度为98%。
鲁教版第五单元 定量研究化学反应
一、选择题。(16题)
1、在化学方程式:C2H8N2 + 2N2O4 = 3X + 2CO2 + 4H2O中,X 的化学式为( )
A. N2 B. H2 C. O2 D. CO
2、已知 分别表示X、Y、Z三种不同的气体分子,在一定条件下的变化如图所示,由图示获得的下列信息中错误的是( )
A.在化学变化中,分子、原子一定发生改变
B.该反应的基本反应类型属于化合反应
C.保持三种物质化学性质最小的微粒是分子
D.若是氧分子,则该反应会放热
3、高纯度的单晶硅是制做电子集成电路的基础材料。工业上制备高纯硅的化学反应原理为:
①SiO2+2CSi +2CO↑、②Si+3HClHSiCl3+H2、③HSiCl3+H2Si+3X,反应①制得粗硅,通过反应②③进一步得到高纯硅;三氯硅烷(HSiCl3)的沸点是31.8℃。下列有关说法不正确的是( )
A.反应③中X的化学式为HCl
B.三氯硅烷由氢、硅、氯三种元素组成
C.三氯硅烷中硅、氯元素的质量比为1∶3
D.反应②③实现了硅元素的富集,将粗硅转化为高纯硅
4、在密闭容器中有甲、乙、丙、丁四种物质,在一定条件下充分反应,测得反应前后各物质的质量分数如图所示:下列说法中正确的是( )
A.丙可能是单质
B.在该反应中丁一定没有参加化学反应
C.甲和乙的质量之和一定等于生成丙的质量
D.该反应是化合反应
5、吐火,是川剧中独一无二的神秘绝技。吐火有一个绝窍,那就是眼前的火尚未熄灭之时,绝对不能吸气,否则最直接的后果就是“引火焚身”。屏住呼吸时,嘴巴里的煤油没有燃烧的原因是( )
A.缺乏氧气 B.没有达到煤油的着火点
C.缺乏可燃物 D.嘴巴里的唾液使煤油不易着火
6、利用催化剂可消除室内装修材料释放的甲醛,如图所示为该反应的微观示意图。下列说法不正确的是( )
A.甲醛的化学式为CH2O
B.生成物丙和丁中氧元素的化合价相同
C.生成物丙由1个碳原子和2个氧原子构成
D.参加反应的甲和生成的丁分子个数比为1:1
7、化学是一门以实验为基础的科学,许多化学重大发现和研究成果都是通过实验得到的。下列实验操作或设计中正确的是( )
A.用100mL量筒量取 8.5mL盐酸
B.收集氢气
C.验证质量守恒定律
D.过滤除去盐水中的盐
8、科学研究表明,氨气在常压下就可液化为液氨,液氨可用作汽车的清洁燃料,其燃烧时的主要反应为4NH3+3O22X+6H2O.下列说法中不正确的是( )
A.氨气在常压下液化是物理变化 B.X的化学式为
C.液氨具有可燃性属于化学性质 D.反应前后三种元素化合价都发生变化
9、在一个密闭的容器内有四种物质,在一定条件下充分反应,测得反应前后各物质的质量,数据见下表,下列说法正确的是( )
物质 甲 乙 丙 丁
反应前质量/g 1 20 17 2
反应后质量/g m 29 0 10
A.m的值是0 B.甲是该反应的催化剂
C.化学反应中乙、丁的质量比是9:8 D.该反应是化合反应
10、古语道:“人要实,火要虚”。从燃烧的条件看,“火要虚”的实质是( )
A.增大可燃物的热值 B.提高空气中氧气的含量
C.提高可燃物的着火点 D.增大可燃物与空气的接触面积
11、在一个密闭容器中放入P、Q、R、W四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表。则关于此反应的认识正确的是( )
物质 P Q R W
反应前的质量(g) 5 2 14 18
反应后的质量(g) 20 x 4 13
A.参加化学反应的P和W的质量比为3:2
B.该反应用现象表示为:
C.反应后容器中R与Q的质量比为1:2
D.Q在反应中可能作催化剂
12、推理是学习化学的一种重要方法,但不合理的推理会得出错误的结论。以下推理正确的是( )
A.分子可以构成物质,物质一定是由分子构成的
B.离子是带电荷的微粒,带电荷的微粒一定是离子
C.最外层电子数相同的原子化学性质相似,氦原子和镁原子的化学性质也相似
D.含碳元素的物质充分燃烧会生成CO2,燃烧能生成CO2的物质一定含碳元素
13、下列关于S+O2SO2的理解正确的是( )
A.表示硫与氧气在点燃条件下反应生成二氧化硫
B.参加反应的硫与氧气的质量比是2:1
C.反应前后硫原子、氧分子的个数均不变
D.参加反应的氧气与生成的二氧化硫的分子个数比为2:1
14、在一个密闭容器中,充入2m个CO分子和n个O2分子,在一定条件下充分反应后容器内碳原子与氧原子的个数比为
A.m/(m+2m) B.m/2(m+n) C.m/n D.m/(m+n)
15、如图所示的一组实验可用于研究燃烧条件。下列说法中,正确的是( )
A.此组实验烧杯中的热水只起提高温度的作用
B.图1中铜片上的白磷和红磷对比说明燃烧必须有氧气
C.图1中铜片上的红磷和水下的白磷对比说明燃烧必须达到可燃物的着火点
D.图1和图2中水下白磷对比说明燃烧必须要有氧气
16、元素钴(Co)有多种化合价,将9.3gCo(OH)2在空气中加热至290℃时完全脱水,得到8.3g钴的氧化物,该氧化物的化学式是( )
A.CoO B.CoO3 C.Co2O3 D.Co3O4
二、填空题。
17、在点燃条件下,4.4gC3H8与12.8g氧气恰好完全反应,生成7.2g水、4.4g二氧化碳和a g X.则X的化学式为________ ;该反应的化学方程式为: ________ 。
18、某学习小组同学利用如图装置验证了空气中氧气的含量。请回答:
(1)上述实验中白磷燃烧的化学方程式是_____ 。
(2)若上述实验测得氧气含量为20%,则最终量筒中液面约降至_____刻度线处。
(3)下列有关说法错误的是_____。
A白磷的作用是消耗试管中的氧气
B白磷火焰熄灭、试管冷却到室温后再打开止水夹
C若实验前没有夹紧止水夹使测定的氧气体积分数偏小
19、请结合如图实验回答有关问题:
(1)图中操作a的名称是 ,该操作中所需的玻璃仪器有烧杯、玻璃棒和 。
(2)图中x的值为 。
(3)检验上述实验中产生的气体用 ,反应中共产生该气体的质量为 g。
(4)计算参加反应的过氧化氢的质量是多少
20、某学校化学学习小组设计出如图所示装置,并进行白磷燃烧实验。
(1)当烧杯内的水受热,温度计显示30℃时,打开活塞,在盛有水的试管中有气泡均匀逸出,白磷未燃烧,关闭活塞.锥形瓶内反应的化学方程式是:
。白磷未燃烧的原因是 。
(2)随着水温升高,温度计显示45℃时,再次打开活塞,白磷在水里燃烧.常言道,水火不相容.而本实验中白磷在水里还能够燃烧的原因是:
。水能灭火的原因是:
。
21、绥中化学兴趣小组为了探究质量守恒定律,进行了如图所示的小实验。
在一根用细铜丝吊着的长玻璃管两端,分别绕上40cm长的粗铜丝,并使玻璃棒保持水平。然后用酒精灯给左边一端铜丝加热1~2分钟。停止加热后冷却,仔细观察发生的现象。冷却后,他观察到的现象是:
(1)______ ;
(2)______ 。
(3)写出下沉一端的原因______ 。
三、实验题。
22、回答下列有关实验的问题:
(1)实验中,打开弹簧夹进入瓶中的水不足五分之一,其原因可能是______ 。(答一种即可)
(2)实验中观察到的现象是______ ,该实验说明______ 。
(3)实验中反应结束后小华发现天平指针向右偏转,其原因可能是:
______ 。要通过该实验来验证质量守恒定律,在不更换药品的情况下,你的改进方法是______ 。
23、根据下图完成下列问题。
(1)仪器a的名称是:____________。
(2)加热KMnO4制取O2的化学方程式为____________。
(3)收集O2的装置是____________(选填B或C);
(4)将带火星的木条放在____________,若观察到木条复燃,说明瓶中已充满O2;
(5)若用如图D装置收集氢气,气体应从____________(填“m”或“n”)端进入。
四、计算类综合题。
24、某实验小组的同学为了测定实验室中氯酸钾样品的纯度,取一定质量的该样品与1g二氧化锰混合,其总质量为6g。依次加热该混合物t1、t2、t3、t4时间后,分别冷却称量剩余固体质量,记录的有关数据如下表(样品中的杂质不参与化学反应):
加热时间 t1 t2 t3 t4
剩余固体质量(g) 4.24 4.16 4.08 4.08
试计算:(1)完全反应后产生的氧气的总质量为 。
(2)样品中氯酸钾的纯度是多少?。
2023—2024学年鲁教版化学九年级上册第五单元 定量研究化学反应 单元训练题含答案
鲁教版第五单元 定量研究化学反应
一、选择题。(16题)
1、在化学方程式:C2H8N2 + 2N2O4 = 3X + 2CO2 + 4H2O中,X 的化学式为( )
A. N2 B. H2 C. O2 D. CO
【答案】A
2、已知 分别表示X、Y、Z三种不同的气体分子,在一定条件下的变化如图所示,由图示获得的下列信息中错误的是( )
A.在化学变化中,分子、原子一定发生改变
B.该反应的基本反应类型属于化合反应
C.保持三种物质化学性质最小的微粒是分子
D.若是氧分子,则该反应会放热
【答案】A
3、高纯度的单晶硅是制做电子集成电路的基础材料。工业上制备高纯硅的化学反应原理为:
①SiO2+2CSi +2CO↑、②Si+3HClHSiCl3+H2、③HSiCl3+H2Si+3X,反应①制得粗硅,通过反应②③进一步得到高纯硅;三氯硅烷(HSiCl3)的沸点是31.8℃。下列有关说法不正确的是( )
A.反应③中X的化学式为HCl
B.三氯硅烷由氢、硅、氯三种元素组成
C.三氯硅烷中硅、氯元素的质量比为1∶3
D.反应②③实现了硅元素的富集,将粗硅转化为高纯硅
【答案】 C
4、在密闭容器中有甲、乙、丙、丁四种物质,在一定条件下充分反应,测得反应前后各物质的质量分数如图所示:下列说法中正确的是( )
A.丙可能是单质
B.在该反应中丁一定没有参加化学反应
C.甲和乙的质量之和一定等于生成丙的质量
D.该反应是化合反应
【答案】D
5、吐火,是川剧中独一无二的神秘绝技。吐火有一个绝窍,那就是眼前的火尚未熄灭之时,绝对不能吸气,否则最直接的后果就是“引火焚身”。屏住呼吸时,嘴巴里的煤油没有燃烧的原因是( )
A.缺乏氧气 B.没有达到煤油的着火点
C.缺乏可燃物 D.嘴巴里的唾液使煤油不易着火
【答案】A
6、利用催化剂可消除室内装修材料释放的甲醛,如图所示为该反应的微观示意图。下列说法不正确的是( )
A.甲醛的化学式为CH2O
B.生成物丙和丁中氧元素的化合价相同
C.生成物丙由1个碳原子和2个氧原子构成
D.参加反应的甲和生成的丁分子个数比为1:1
【答案】C
7、化学是一门以实验为基础的科学,许多化学重大发现和研究成果都是通过实验得到的。下列实验操作或设计中正确的是( )
A.用100mL量筒量取 8.5mL盐酸
B.收集氢气
C.验证质量守恒定律
D.过滤除去盐水中的盐
【答案】B
8、科学研究表明,氨气在常压下就可液化为液氨,液氨可用作汽车的清洁燃料,其燃烧时的主要反应为4NH3+3O22X+6H2O.下列说法中不正确的是( )
A.氨气在常压下液化是物理变化 B.X的化学式为
C.液氨具有可燃性属于化学性质 D.反应前后三种元素化合价都发生变化
【答案】 D
9、在一个密闭的容器内有四种物质,在一定条件下充分反应,测得反应前后各物质的质量,数据见下表,下列说法正确的是( )
物质 甲 乙 丙 丁
反应前质量/g 1 20 17 2
反应后质量/g m 29 0 10
A.m的值是0 B.甲是该反应的催化剂
C.化学反应中乙、丁的质量比是9:8 D.该反应是化合反应
【答案】C
10、古语道:“人要实,火要虚”。从燃烧的条件看,“火要虚”的实质是( )
A.增大可燃物的热值 B.提高空气中氧气的含量
C.提高可燃物的着火点 D.增大可燃物与空气的接触面积
【答案】D
11、在一个密闭容器中放入P、Q、R、W四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表。则关于此反应的认识正确的是( )
物质 P Q R W
反应前的质量(g) 5 2 14 18
反应后的质量(g) 20 x 4 13
A.参加化学反应的P和W的质量比为3:2
B.该反应用现象表示为:
C.反应后容器中R与Q的质量比为1:2
D.Q在反应中可能作催化剂
【答案】D
12、推理是学习化学的一种重要方法,但不合理的推理会得出错误的结论。以下推理正确的是( )
A.分子可以构成物质,物质一定是由分子构成的
B.离子是带电荷的微粒,带电荷的微粒一定是离子
C.最外层电子数相同的原子化学性质相似,氦原子和镁原子的化学性质也相似
D.含碳元素的物质充分燃烧会生成CO2,燃烧能生成CO2的物质一定含碳元素
【答案】D
13、下列关于S+O2SO2的理解正确的是( )
A.表示硫与氧气在点燃条件下反应生成二氧化硫
B.参加反应的硫与氧气的质量比是2:1
C.反应前后硫原子、氧分子的个数均不变
D.参加反应的氧气与生成的二氧化硫的分子个数比为2:1
【答案】 A
14、在一个密闭容器中,充入2m个CO分子和n个O2分子,在一定条件下充分反应后容器内碳原子与氧原子的个数比为
A.m/(m+2m) B.m/2(m+n) C.m/n D.m/(m+n)
【答案】D
15、如图所示的一组实验可用于研究燃烧条件。下列说法中,正确的是( )
A.此组实验烧杯中的热水只起提高温度的作用
B.图1中铜片上的白磷和红磷对比说明燃烧必须有氧气
C.图1中铜片上的红磷和水下的白磷对比说明燃烧必须达到可燃物的着火点
D.图1和图2中水下白磷对比说明燃烧必须要有氧气
【答案】D
16、元素钴(Co)有多种化合价,将9.3gCo(OH)2在空气中加热至290℃时完全脱水,得到8.3g钴的氧化物,该氧化物的化学式是( )
A.CoO B.CoO3 C.Co2O3 D.Co3O4
【答案】C
二、填空题。
17、在点燃条件下,4.4gC3H8与12.8g氧气恰好完全反应,生成7.2g水、4.4g二氧化碳和a g X.则X的化学式为________ ;该反应的化学方程式为: ________ 。
【答案】 CO ;C3H8+4O2CO2+4H2O+2CO
18、某学习小组同学利用如图装置验证了空气中氧气的含量。请回答:
(1)上述实验中白磷燃烧的化学方程式是_____ 。
(2)若上述实验测得氧气含量为20%,则最终量筒中液面约降至_____刻度线处。
(3)下列有关说法错误的是_____。
A白磷的作用是消耗试管中的氧气
B白磷火焰熄灭、试管冷却到室温后再打开止水夹
C若实验前没有夹紧止水夹使测定的氧气体积分数偏小
【答案】4P+5O22P2O5 24 C
19、请结合如图实验回答有关问题:
(1)图中操作a的名称是 ,该操作中所需的玻璃仪器有烧杯、玻璃棒和 。
(2)图中x的值为 。
(3)检验上述实验中产生的气体用 ,反应中共产生该气体的质量为 g。
(4)计算参加反应的过氧化氢的质量是多少
【答案】(1)过滤 漏斗 (2)5 (3)带火星的木条 2.4 (4)5.1 g
20、某学校化学学习小组设计出如图所示装置,并进行白磷燃烧实验。
(1)当烧杯内的水受热,温度计显示30℃时,打开活塞,在盛有水的试管中有气泡均匀逸出,白磷未燃烧,关闭活塞.锥形瓶内反应的化学方程式是:
。白磷未燃烧的原因是 。
(2)随着水温升高,温度计显示45℃时,再次打开活塞,白磷在水里燃烧.常言道,水火不相容.而本实验中白磷在水里还能够燃烧的原因是:
。水能灭火的原因是:
。
【答案】(1)2H2O2 2H2O+O2↑;温度未达到白磷的着火点。
(2)温度达到着火点,同时又与氧气充分接触。
可以使可燃物温度降至着火点以下和隔绝氧气。
21、绥中化学兴趣小组为了探究质量守恒定律,进行了如图所示的小实验。
在一根用细铜丝吊着的长玻璃管两端,分别绕上40cm长的粗铜丝,并使玻璃棒保持水平。然后用酒精灯给左边一端铜丝加热1~2分钟。停止加热后冷却,仔细观察发生的现象。冷却后,他观察到的现象是:
(1)______ ;
(2)______ 。
(3)写出下沉一端的原因______ 。
【答案】(1)红色固体变为黑色
(2)玻璃棒向左侧倾斜
(3)铜与氧气反应后固体质量增加
三、实验题。
22、回答下列有关实验的问题:
(1)实验中,打开弹簧夹进入瓶中的水不足五分之一,其原因可能是______ 。(答一种即可)
(2)实验中观察到的现象是______ ,该实验说明______ 。
(3)实验中反应结束后小华发现天平指针向右偏转,其原因可能是:
______ 。要通过该实验来验证质量守恒定律,在不更换药品的情况下,你的改进方法是______ 。
【答案】(1)装置漏气(红磷量不足;未完全冷却就打开弹簧夹读数)
(2)烧杯甲中溶液变为红色 分子在不停地运动 生
(3)成的CO2气体逸散到空气中,未称量到
将烧杯换成密闭容器(将装置改成密闭装置)
23、根据下图完成下列问题。
(1)仪器a的名称是:____________。
(2)加热KMnO4制取O2的化学方程式为____________。
(3)收集O2的装置是____________(选填B或C);
(4)将带火星的木条放在____________,若观察到木条复燃,说明瓶中已充满O2;
(5)若用如图D装置收集氢气,气体应从____________(填“m”或“n”)端进入。
【答案】(1)酒精灯 (2)
(3)B (4)集气瓶口 (5)n
四、计算类综合题。
24、某实验小组的同学为了测定实验室中氯酸钾样品的纯度,取一定质量的该样品与1g二氧化锰混合,其总质量为6g。依次加热该混合物t1、t2、t3、t4时间后,分别冷却称量剩余固体质量,记录的有关数据如下表(样品中的杂质不参与化学反应):
加热时间 t1 t2 t3 t4
剩余固体质量(g) 4.24 4.16 4.08 4.08
试计算:(1)完全反应后产生的氧气的总质量为 。
(2)样品中氯酸钾的纯度是多少?。
【答案及解析】(1)生成氧气的质量为
6g﹣4.08g=1.92g
(2)设样品中氯酸钾的纯度为x。
2KClO32KCl+3O2↑
245 96
(6g﹣1g)×x 1.92g
=,x=98%
答:(1)完全反应后产生的氧气的总质量为1.92g。
(2)样品中氯酸钾的纯度为98%。
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 水分子的变化
- 第三节 原子的构成
- 第四节 元素
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 溶液
- 第一节 溶液的形成
- 第二节 溶液组成的定量表示
- 到实验室去:配制一定溶质质量分数的溶液
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 物质组成的表示
- 第三节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去:二氧化碳的实验室制取与性质
