化学人教版(2019)选择性必修3 3.3醛(共18张ppt)
文档属性
| 名称 | 化学人教版(2019)选择性必修3 3.3醛(共18张ppt) |  | |
| 格式 | pptx | ||
| 文件大小 | 1.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-12-22 19:17:40 | ||
图片预览




文档简介
(共18张PPT)
醛
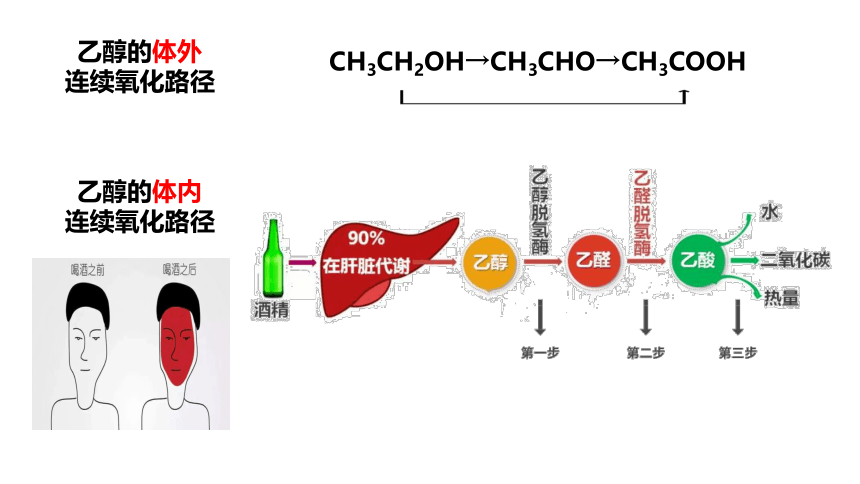
乙醇的体外
连续氧化路径
乙醇的体内
连续氧化路径
CH3CH2OH→CH3CHO→CH3COOH
任务 1
认识最熟悉的醛(乙醛)的结构与物理性质
颜色及状态?
易挥发吗?
溶解性情况?
最多几原子共面情况?
熔点:-123℃
沸点:20.8℃
任务 2
基于乙醛的结构,预测其化学性质
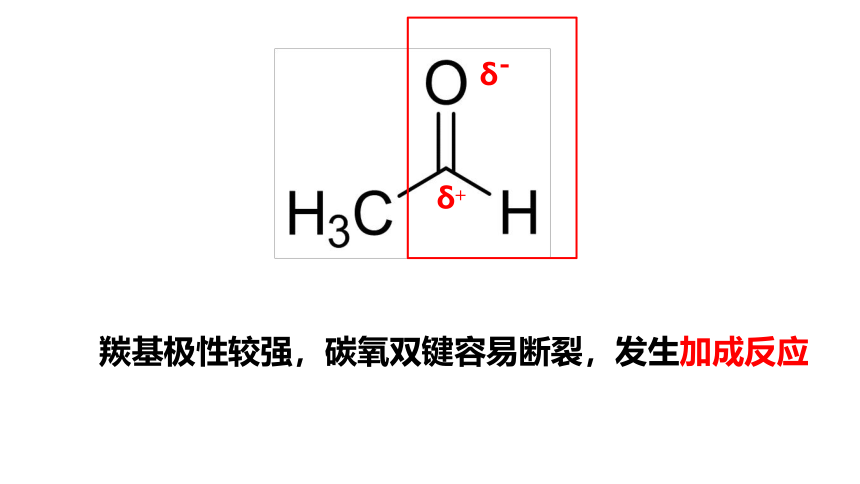
δ+
δ-
羰基极性较强,碳氧双键容易断裂,发生加成反应
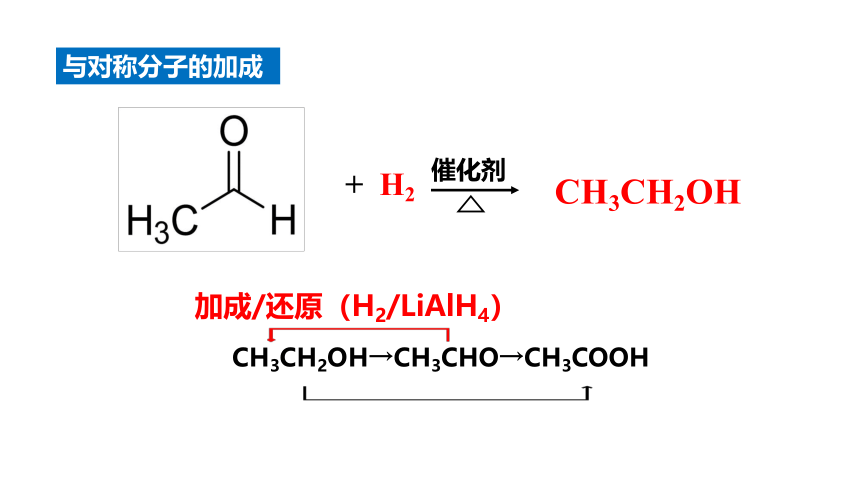
与对称分子的加成
+ H2
催化剂
CH3CH2OH
CH3CH2OH→CH3CHO→CH3COOH
加成/还原(H2/LiAlH4)
与不对称分子的加成
+ H-CN
催化剂
CH3-CH-CN
OH
当极性分子与醛基发生加成反应时,带正电荷的原子或原子团连接在氧原子上,带负电荷的原子或原子团连接在碳原子上。
δ+
δ-
δ+
δ-
2-羟基丙腈
有剧毒,主要用作溶剂和制备丙烯腈、丙烯酸酯和乳酸乙酯等。
δ+
δ-
醛基中的氢原子受羰基的影响,变得比较活泼,
醛基容易被氧化成羧基。
与强氧化剂反应(KMnO4溶液、O2)
CH3CH2OH→CH3CHO→CH3COOH
氧化(O2/KMnO4)
醛基与酸性高锰酸钾溶液的反应:用葡萄糖溶液代替
2CH3CHO+O2
2CH3COOH
催化剂
△
与弱氧化剂反应
(新制氢氧化铜、银氨溶液、溴水)
醛基与新制氢氧化铜的反应:
用葡萄糖溶液代替
与新制氢氧化铜反应注意事项:
1.氢氧化钠要过量
2.氢氧化铜现配现用
在试管里加入 2 mL10% 的NaOH 溶液,加入5 滴5%CuSO4 溶液,得到新制的Cu(OH)2。振荡后加入0.5 mL 乙醛溶液,加热,观察实验现象。
CH3CHO+2Cu(OH)2+NaOH →CH3COONa+Cu2O↓ +3H2O
△
砖红色沉淀
检验
醛基
醛基与新制Cu(OH)2反应的比例关系?
写出乙二醛与新制Cu(OH)2反应的化学方程式?
OHCCHO+4Cu(OH)2+2NaOH →NaOOCCOONa+2Cu2O↓ +6H2O
△
醛基与银氨溶液的反应:
用葡萄糖溶液代替
与弱氧化剂反应
(新制氢氧化铜、银氨溶液、溴水)
在试管里加入 1 mL2% 的AgNO3 溶液,边振荡边逐滴滴入2%氨水,形成[Ag(NH3)2]OH。再滴入3滴乙醛溶液,热水浴加热,观察现象。
与银氨溶液反应注意事项:
1.加热要水浴加热
2.银氨溶液现配现用
CH3CHO+2[Ag(NH3)2]OH →CH3COONH4+2Ag↓ +3NH3+ H2O
△
检验醛基
制镜面或保温瓶内胆
醛基与银氨溶液反应的比例关系?
写出乙二醛与银氨溶液反应的化学方程式?
OHCCHO+4[Ag(NH3)2]OH →NH4OOCCOONH4+4Ag↓ +6NH3+ 2H2O
△
醛基与浓溴水的反应:
用甲酸溶液代替
与弱氧化剂反应
(新制氢氧化铜、银氨溶液、溴水)
CH3CH2OH→CH3CHO→CH3COOH
氧化(O2/Br2/KMnO4)
CH3CHO+Br2+H2O →CH3COOH+2HBr
CH3CH2OH→CH3CHO→CH3COOH
氧化
(O2/Br2/KMnO4/
新制Cu(OH)2/银氨溶液)
加成/还原
(H2/LiAlH4)
氧化
(K2Cr2O7/KMnO4)
催化氧化
任务3
类比乙醛的性质,认识其他醛类有机物的
结构与性质
甲醛(蚁醛)
结构?
颜色及状态?
易挥发吗?
溶解性情况?
最多几原子共面情况?
35% ~ 40% 的甲醛水溶液称为“福尔马林”,它可以用于浸制生物标本,稀的甲醛水溶液还可以为种子消毒
甲醛与新制Cu(OH)2、银氨溶液反应的化学方程式为?
HCHO+4Cu(OH)2+2NaOH →Na2CO3+2Cu2O↓ +6H2O
△
HCHO+4[Ag(NH3)2]OH →(NH4)2CO3+4Ag↓ +6NH3+ 2H2O
△
苯甲醛
结构?
颜色及状态?
最多几原子共面情况?
苯甲醛在空气中久置,在容器内壁会出现结晶,结晶是什么?
产生结晶的原因?
苯甲醛熔点:-26℃
苯甲酸熔点:122℃
饱和一元醛
其他醛
2-甲基丁醛
CnH2nO(Ω=1)
对氯苯甲醛
对苯二甲醛
丙烯醛
醛
乙醇的体外
连续氧化路径
乙醇的体内
连续氧化路径
CH3CH2OH→CH3CHO→CH3COOH
任务 1
认识最熟悉的醛(乙醛)的结构与物理性质
颜色及状态?
易挥发吗?
溶解性情况?
最多几原子共面情况?
熔点:-123℃
沸点:20.8℃
任务 2
基于乙醛的结构,预测其化学性质
δ+
δ-
羰基极性较强,碳氧双键容易断裂,发生加成反应
与对称分子的加成
+ H2
催化剂
CH3CH2OH
CH3CH2OH→CH3CHO→CH3COOH
加成/还原(H2/LiAlH4)
与不对称分子的加成
+ H-CN
催化剂
CH3-CH-CN
OH
当极性分子与醛基发生加成反应时,带正电荷的原子或原子团连接在氧原子上,带负电荷的原子或原子团连接在碳原子上。
δ+
δ-
δ+
δ-
2-羟基丙腈
有剧毒,主要用作溶剂和制备丙烯腈、丙烯酸酯和乳酸乙酯等。
δ+
δ-
醛基中的氢原子受羰基的影响,变得比较活泼,
醛基容易被氧化成羧基。
与强氧化剂反应(KMnO4溶液、O2)
CH3CH2OH→CH3CHO→CH3COOH
氧化(O2/KMnO4)
醛基与酸性高锰酸钾溶液的反应:用葡萄糖溶液代替
2CH3CHO+O2
2CH3COOH
催化剂
△
与弱氧化剂反应
(新制氢氧化铜、银氨溶液、溴水)
醛基与新制氢氧化铜的反应:
用葡萄糖溶液代替
与新制氢氧化铜反应注意事项:
1.氢氧化钠要过量
2.氢氧化铜现配现用
在试管里加入 2 mL10% 的NaOH 溶液,加入5 滴5%CuSO4 溶液,得到新制的Cu(OH)2。振荡后加入0.5 mL 乙醛溶液,加热,观察实验现象。
CH3CHO+2Cu(OH)2+NaOH →CH3COONa+Cu2O↓ +3H2O
△
砖红色沉淀
检验
醛基
醛基与新制Cu(OH)2反应的比例关系?
写出乙二醛与新制Cu(OH)2反应的化学方程式?
OHCCHO+4Cu(OH)2+2NaOH →NaOOCCOONa+2Cu2O↓ +6H2O
△
醛基与银氨溶液的反应:
用葡萄糖溶液代替
与弱氧化剂反应
(新制氢氧化铜、银氨溶液、溴水)
在试管里加入 1 mL2% 的AgNO3 溶液,边振荡边逐滴滴入2%氨水,形成[Ag(NH3)2]OH。再滴入3滴乙醛溶液,热水浴加热,观察现象。
与银氨溶液反应注意事项:
1.加热要水浴加热
2.银氨溶液现配现用
CH3CHO+2[Ag(NH3)2]OH →CH3COONH4+2Ag↓ +3NH3+ H2O
△
检验醛基
制镜面或保温瓶内胆
醛基与银氨溶液反应的比例关系?
写出乙二醛与银氨溶液反应的化学方程式?
OHCCHO+4[Ag(NH3)2]OH →NH4OOCCOONH4+4Ag↓ +6NH3+ 2H2O
△
醛基与浓溴水的反应:
用甲酸溶液代替
与弱氧化剂反应
(新制氢氧化铜、银氨溶液、溴水)
CH3CH2OH→CH3CHO→CH3COOH
氧化(O2/Br2/KMnO4)
CH3CHO+Br2+H2O →CH3COOH+2HBr
CH3CH2OH→CH3CHO→CH3COOH
氧化
(O2/Br2/KMnO4/
新制Cu(OH)2/银氨溶液)
加成/还原
(H2/LiAlH4)
氧化
(K2Cr2O7/KMnO4)
催化氧化
任务3
类比乙醛的性质,认识其他醛类有机物的
结构与性质
甲醛(蚁醛)
结构?
颜色及状态?
易挥发吗?
溶解性情况?
最多几原子共面情况?
35% ~ 40% 的甲醛水溶液称为“福尔马林”,它可以用于浸制生物标本,稀的甲醛水溶液还可以为种子消毒
甲醛与新制Cu(OH)2、银氨溶液反应的化学方程式为?
HCHO+4Cu(OH)2+2NaOH →Na2CO3+2Cu2O↓ +6H2O
△
HCHO+4[Ag(NH3)2]OH →(NH4)2CO3+4Ag↓ +6NH3+ 2H2O
△
苯甲醛
结构?
颜色及状态?
最多几原子共面情况?
苯甲醛在空气中久置,在容器内壁会出现结晶,结晶是什么?
产生结晶的原因?
苯甲醛熔点:-26℃
苯甲酸熔点:122℃
饱和一元醛
其他醛
2-甲基丁醛
CnH2nO(Ω=1)
对氯苯甲醛
对苯二甲醛
丙烯醛
