化学人教版(2019)必修第一册4.1原子结构(共17张ppt)
文档属性
| 名称 | 化学人教版(2019)必修第一册4.1原子结构(共17张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 4.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-12-23 00:00:00 | ||
图片预览




文档简介
(共17张PPT)
4.1 原子结构
任务1:原子结构
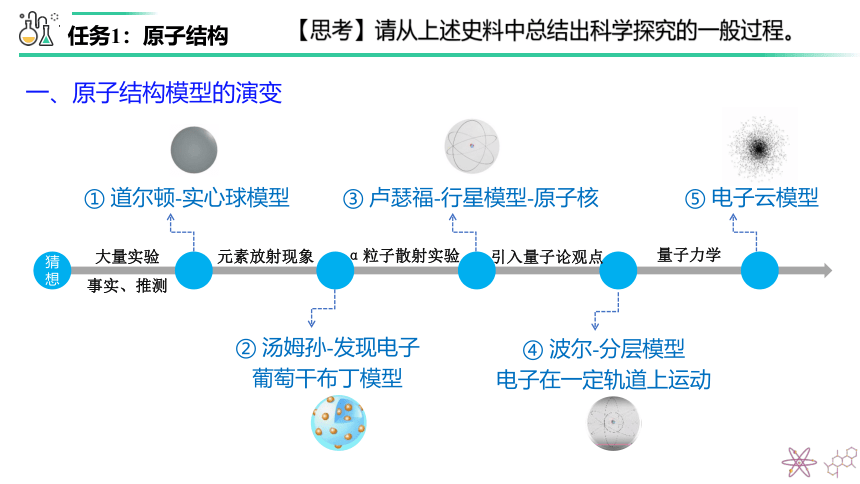
一、原子结构模型的演变
⑤ 电子云模型
① 道尔顿-实心球模型
③ 卢瑟福-行星模型-原子核
α粒子散射实验
④ 波尔-分层模型
电子在一定轨道上运动
量子力学
大量实验
事实、推测
猜想
元素放射现象
【思考】请从上述史料中总结出科学探究的一般过程。
引入量子论观点
② 汤姆孙-发现电子
葡萄干布丁模型
任务1:原子结构
原子
原子核
核外电子
质子
中子
带1个负电荷,忽略质量
(带正电)
(带负电)
(不带电)
二、原子结构
带1个正电荷,相对质量近似为1
不带电,相对质量近似为1
原子序数 = 质子数 = 核电荷数 = 核外电子数
原子质量 = 原子核质量 + 电子质量
≈ 原子核质量 ≈ 质子质量 + 中子质量
任务1:原子结构
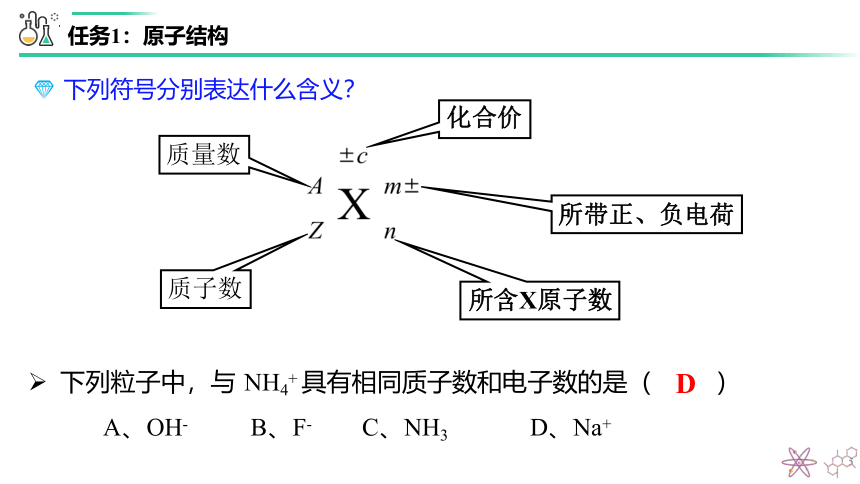
表示原子组成的一种方法:
X
A
Z
—元素符号
质量数 —
质子数 —
质量数:将原子核内所有质子和中子的相对质量取近似整数相加所得的数值
质量数(A) = 质子数(Z) + 中子数(N)
元素 表示方法 微粒种类 质子数(Z) 中子数(N) 核外电子数
Na
Na
Na
X2-
12
11
11
原子
11
12
10
阳离子
O
阴离子
10
8
10
核外电子数=质子数 - 电荷数
核外电子数=质子数=核电荷数
核外电子数=质子数 + 电荷数
任务1:原子结构下列符号分别表达什么含义?下列粒子中,与NH4+具有相同质子数和电子数的是( )A、OH-B、F-C、NH3D、Na+D质量数v质子数v所含X原子数v所带正、负电荷v化合价原子符号 元素 质子数(Z) 中子数(N) 氢原子名称
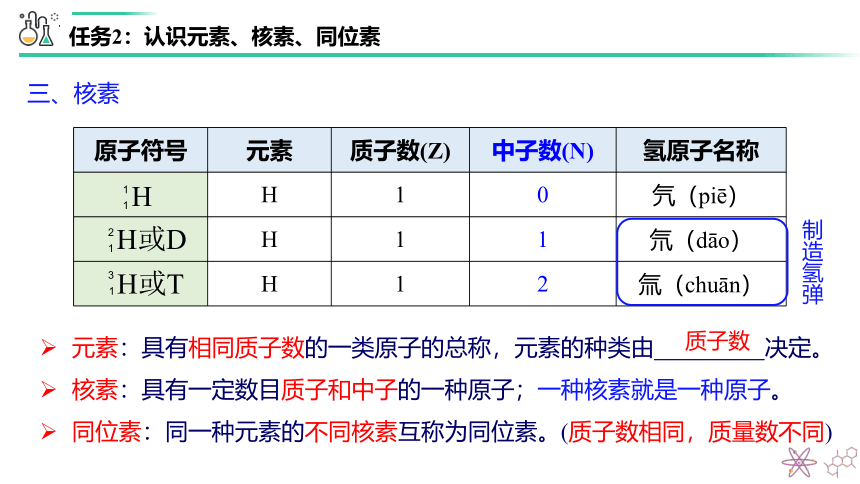
H 1 0 氕(piē)
H 1 1 氘(dāo)
H 1 2 氚(chuān)
1
1
H
1
2
H或D
1
3
H或T
元素:具有相同质子数的一类原子的总称,元素的种类由 决定。
核素:具有一定数目质子和中子的一种原子;一种核素就是一种原子。
同位素:同一种元素的不同核素互称为同位素。(质子数相同,质量数不同)
任务2:认识元素、核素、同位素
三、核素
质子数
制造氢弹
任务2:认识元素、核素、同位素
碳元素
C
12
6
C
13
6
C
14
6
铀元素
U
234
92
U
235
92
U
238
92
同位素的特点及应用?
氧元素
O
16
8
O
17
8
O
18
6
治疗恶性肿瘤
同位素中,有些含有放射性,有些不含放射性。
同位素的特点:质子数相同、中子数不同、质量数不同
物理性质不同,化学性质相似
相对质量的标准
考古断代
放射性同位素用途:射线育种、金属探伤、诊断和治疗疾病
任务3:原子核外电子排布
假想的,能量不同的区域
1.电子层
表示方法
数字表示法
字母表示法
电子层数 1 2 3 4 5 6 7
字母代号
能量 离核远近 低 —————> 高
近 —————> 远
K L M N O P Q
任务3:原子核外电子排布元素各电子层的电子数KLMNOP2He(氦)2 10Ne(氖)28 18Ar(氩)288 36Kr(氪)28188 54Xe(氙)2818188 86Rn(氡)281832188最外层时,最多能容纳的电子数是多少?次外层时,最多能容纳的电子数是多少?你能归纳出第n层最多能容纳的电子数吗?1234n281832任务3:原子核外电子排布2.原子核外电子的排布规律最外层电子数不超过8个(当K层为最外层时不超过2个)次外层电子数不超过18个倒数第3层电子数不超过32个各层电子数不超过2n2个(n为电子层数)能量最低原理(电子优先排在能量较低的轨道)思考与讨论
请你根据所归纳的规律,写出钾原子的原子结构示意图。
①S2-: ,Cl-: ; ②Ar: ,Ca2+: 。
3.电子层的表示方法——原子结构示意图
任务三:原子核外电子排布
【评价训练】画出下列原子或离子的结构示意图
某微粒共有18个e-,该微粒可能是哪些分子呢?
② 最外层电子数是次外层电子数的2倍的元素:___ __
是次外层3倍的是:_ __
③ 电子层数与最外层电子数相等的元素:__________
① 最外层电子数等于次外层电子数的一半的元素: 。
④ M层电子数是L层电子数的一半的元素:__________
⑤ 核电荷数是电子层数的5倍的元素:__________
Li、Si
C
O
H、Be、Al
Si
P
根据电子排布情况,推断前20号元素中符合要求的所有元素
【当堂练习】
小结【交流研讨】如何找出常见的10e-和18e-的微粒?
(1)常见的10e-微粒
F-、O2-、N3-、OH-
HF、H2O、NH3、CH4
Na+、Mg2+、Al3+、、H3O+
H2S
F2
K+、Ca2+
【课堂延伸】
(2)常见的18e-微粒
任务1:原子结构1.据报道,上海某医院正在研究用放射性的一种碘 治疗肿瘤。该碘原子的核内的中子数与核外电子数之差是( )I12553A. 72 B.19 C.53 D.1252.某二价阴离子,核外有18个电子,质量数为32,则其中子数为:A.12 B.14 C.16 D.18牛刀小试任务2:认识元素、核素、同位素
随堂练习
1.在① Li、② N 、③ Na、④ Mg、⑤ Li、⑥ C中:
(1) 和 互为同位素。
(2) 和 质量数相等,但不能互称同位素。
(3) 和 的中子数相等,但质子数不相等,所以不是同一种元素。
①
⑤
2.下列粒子中,与 NH4+ 具有相同质子数和电子数的是( )
A、OH- B、F- C、NH3 D、Na+
⑥
②
④
③
D
4.1 原子结构
任务1:原子结构
一、原子结构模型的演变
⑤ 电子云模型
① 道尔顿-实心球模型
③ 卢瑟福-行星模型-原子核
α粒子散射实验
④ 波尔-分层模型
电子在一定轨道上运动
量子力学
大量实验
事实、推测
猜想
元素放射现象
【思考】请从上述史料中总结出科学探究的一般过程。
引入量子论观点
② 汤姆孙-发现电子
葡萄干布丁模型
任务1:原子结构
原子
原子核
核外电子
质子
中子
带1个负电荷,忽略质量
(带正电)
(带负电)
(不带电)
二、原子结构
带1个正电荷,相对质量近似为1
不带电,相对质量近似为1
原子序数 = 质子数 = 核电荷数 = 核外电子数
原子质量 = 原子核质量 + 电子质量
≈ 原子核质量 ≈ 质子质量 + 中子质量
任务1:原子结构
表示原子组成的一种方法:
X
A
Z
—元素符号
质量数 —
质子数 —
质量数:将原子核内所有质子和中子的相对质量取近似整数相加所得的数值
质量数(A) = 质子数(Z) + 中子数(N)
元素 表示方法 微粒种类 质子数(Z) 中子数(N) 核外电子数
Na
Na
Na
X2-
12
11
11
原子
11
12
10
阳离子
O
阴离子
10
8
10
核外电子数=质子数 - 电荷数
核外电子数=质子数=核电荷数
核外电子数=质子数 + 电荷数
任务1:原子结构下列符号分别表达什么含义?下列粒子中,与NH4+具有相同质子数和电子数的是( )A、OH-B、F-C、NH3D、Na+D质量数v质子数v所含X原子数v所带正、负电荷v化合价原子符号 元素 质子数(Z) 中子数(N) 氢原子名称
H 1 0 氕(piē)
H 1 1 氘(dāo)
H 1 2 氚(chuān)
1
1
H
1
2
H或D
1
3
H或T
元素:具有相同质子数的一类原子的总称,元素的种类由 决定。
核素:具有一定数目质子和中子的一种原子;一种核素就是一种原子。
同位素:同一种元素的不同核素互称为同位素。(质子数相同,质量数不同)
任务2:认识元素、核素、同位素
三、核素
质子数
制造氢弹
任务2:认识元素、核素、同位素
碳元素
C
12
6
C
13
6
C
14
6
铀元素
U
234
92
U
235
92
U
238
92
同位素的特点及应用?
氧元素
O
16
8
O
17
8
O
18
6
治疗恶性肿瘤
同位素中,有些含有放射性,有些不含放射性。
同位素的特点:质子数相同、中子数不同、质量数不同
物理性质不同,化学性质相似
相对质量的标准
考古断代
放射性同位素用途:射线育种、金属探伤、诊断和治疗疾病
任务3:原子核外电子排布
假想的,能量不同的区域
1.电子层
表示方法
数字表示法
字母表示法
电子层数 1 2 3 4 5 6 7
字母代号
能量 离核远近 低 —————> 高
近 —————> 远
K L M N O P Q
任务3:原子核外电子排布元素各电子层的电子数KLMNOP2He(氦)2 10Ne(氖)28 18Ar(氩)288 36Kr(氪)28188 54Xe(氙)2818188 86Rn(氡)281832188最外层时,最多能容纳的电子数是多少?次外层时,最多能容纳的电子数是多少?你能归纳出第n层最多能容纳的电子数吗?1234n281832任务3:原子核外电子排布2.原子核外电子的排布规律最外层电子数不超过8个(当K层为最外层时不超过2个)次外层电子数不超过18个倒数第3层电子数不超过32个各层电子数不超过2n2个(n为电子层数)能量最低原理(电子优先排在能量较低的轨道)思考与讨论
请你根据所归纳的规律,写出钾原子的原子结构示意图。
①S2-: ,Cl-: ; ②Ar: ,Ca2+: 。
3.电子层的表示方法——原子结构示意图
任务三:原子核外电子排布
【评价训练】画出下列原子或离子的结构示意图
某微粒共有18个e-,该微粒可能是哪些分子呢?
② 最外层电子数是次外层电子数的2倍的元素:___ __
是次外层3倍的是:_ __
③ 电子层数与最外层电子数相等的元素:__________
① 最外层电子数等于次外层电子数的一半的元素: 。
④ M层电子数是L层电子数的一半的元素:__________
⑤ 核电荷数是电子层数的5倍的元素:__________
Li、Si
C
O
H、Be、Al
Si
P
根据电子排布情况,推断前20号元素中符合要求的所有元素
【当堂练习】
小结【交流研讨】如何找出常见的10e-和18e-的微粒?
(1)常见的10e-微粒
F-、O2-、N3-、OH-
HF、H2O、NH3、CH4
Na+、Mg2+、Al3+、、H3O+
H2S
F2
K+、Ca2+
【课堂延伸】
(2)常见的18e-微粒
任务1:原子结构1.据报道,上海某医院正在研究用放射性的一种碘 治疗肿瘤。该碘原子的核内的中子数与核外电子数之差是( )I12553A. 72 B.19 C.53 D.1252.某二价阴离子,核外有18个电子,质量数为32,则其中子数为:A.12 B.14 C.16 D.18牛刀小试任务2:认识元素、核素、同位素
随堂练习
1.在① Li、② N 、③ Na、④ Mg、⑤ Li、⑥ C中:
(1) 和 互为同位素。
(2) 和 质量数相等,但不能互称同位素。
(3) 和 的中子数相等,但质子数不相等,所以不是同一种元素。
①
⑤
2.下列粒子中,与 NH4+ 具有相同质子数和电子数的是( )
A、OH- B、F- C、NH3 D、Na+
⑥
②
④
③
D
