化学人教版(2019)必修第一册4.1.2核素 元素周期表(共24张ppt)
文档属性
| 名称 | 化学人教版(2019)必修第一册4.1.2核素 元素周期表(共24张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-12-23 00:00:00 | ||
图片预览





文档简介
(共24张PPT)
第四章 物质结构 元素周期律
第一节 原子结构与元素周期表
第二课时 核素 元素周期表
1.知道元素、核素、同位素的含义,认识符号 的含义。
2.通过了解元素周期表的结构,认识原子结构与元素周期表中位置间的关系。从微观角度认识元素周期表的编排原则、结构及其价值,明确周期表的基本关系、规律、元素种类及元素分布等,发展学生”宏观辨识与微观探析“、”证据推理与模型认知”化学学科核心素养。
核心素养
A
Z
X
情境导学
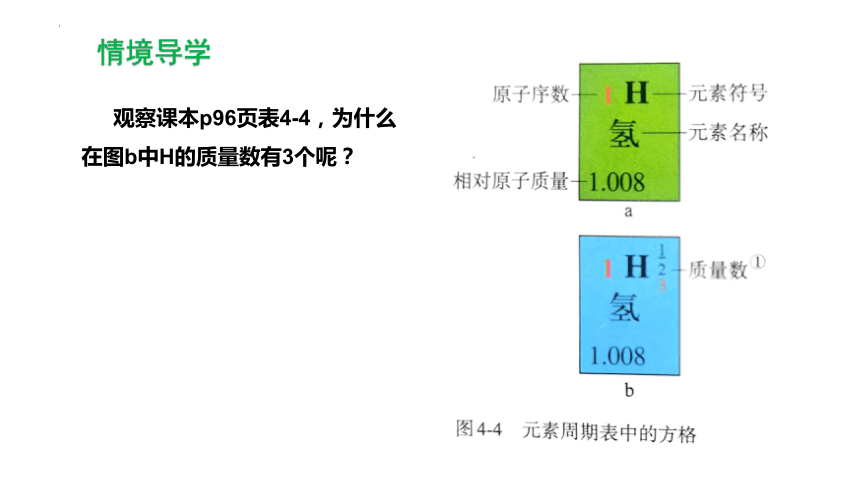
观察课本p96页表4-4,为什么在图b中H的质量数有3个呢?
原子符号 质子数(Z) 中子数(N) 氢原子名称
1 氕(piē)
1 氘(dāo)
1 氚(chuān)
1
1
H
1
2
H或D
1
3
H或T
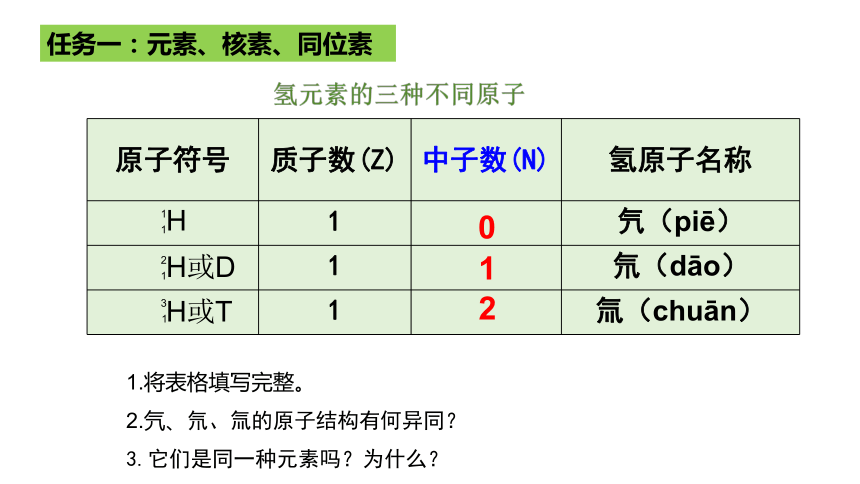
1.将表格填写完整。
2.氕、氘、氚的原子结构有何异同?
3.它们是同一种元素吗?为什么?
任务一:元素、核素、同位素
氢元素的三种不同原子
0
1
2
任务一:元素、核素、同位素
1、元素:具有相同质子数(核电荷数)的一类原子的总称。
同种元素原子的质子数 相同,中子数 相同。
元素属于宏观概念,只讲种类不讲个数。
一定
不一定
2、核素:具有一定数目质子和一定数目中子的一种原子。
同一种核素的质子数 相同,中子数 相同。
核素属于微观概念。
一定
一定
思考:氕、氘、氚三者的关系?
同一元素的三种不同核素。互为同位素。
任务一:元素、核素、同位素
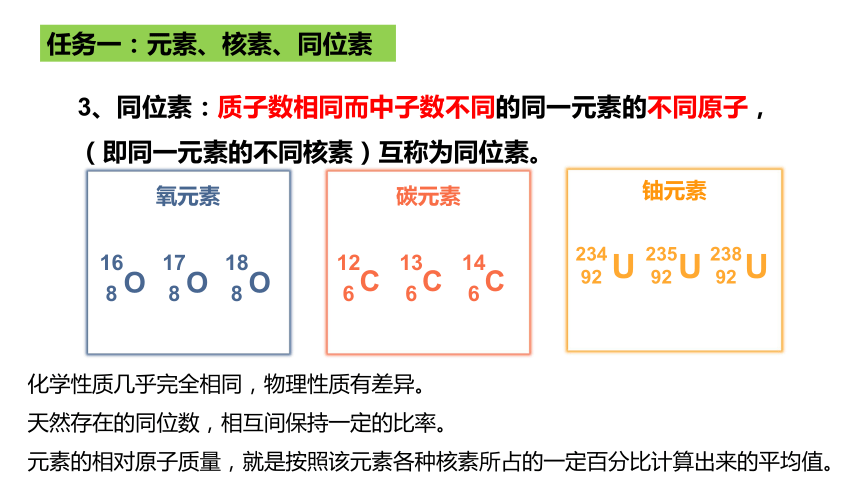
3、同位素:质子数相同而中子数不同的同一元素的不同原子,(即同一元素的不同核素)互称为同位素。
氧元素
O
16
8
O
17
8
O
18
8
碳元素
C
12
6
C
13
6
C
14
6
铀元素
U
234
92
U
235
92
U
238
92
化学性质几乎完全相同,物理性质有差异。
天然存在的同位数,相互间保持一定的比率。
元素的相对原子质量,就是按照该元素各种核素所占的一定百分比计算出来的平均值。
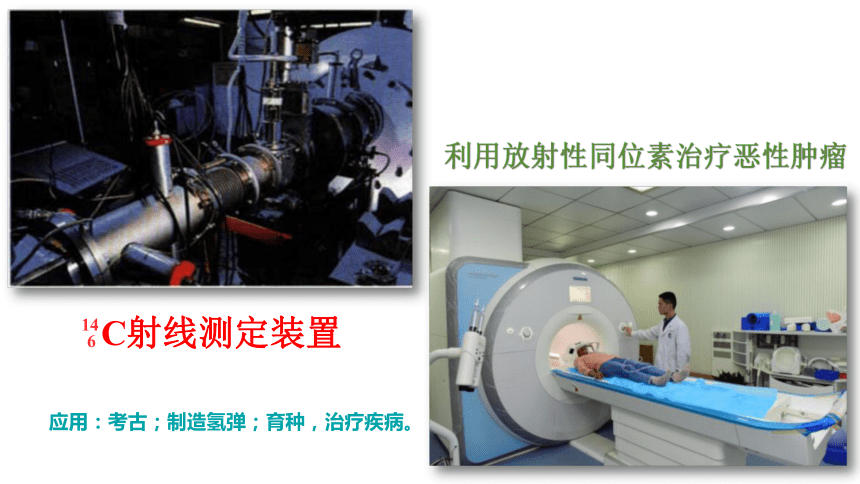
应用:考古;制造氢弹;育种,治疗疾病。
利用放射性同位素治疗恶性肿瘤
1.在① Li、② N 、③ Na、④ Mg、⑤ Li、⑥ C中:
(1) 和 互为同位素。
(2) 和 质量数相等,但不能互称同位素。
(3) 和 的中子数相等,但质子数不相等,所以不是同一种元素。
①
⑤
2.下列各组中属于同位素的是( )
A、40K与40Ca B、T2O和H2O
C、40K与39K D、金刚石与石墨
⑥
②
④
③
C
3.金属钛对人体无毒且能与肌肉和骨骼生长在一起,有“生物金属”之称。下列有关和的说法正确的是
A.和的质量数不同,属于两种元素
B. 和的质子数相同,互称同位素
C. 和的质子数相同,是同一种核素
D. 和核外电子数相同,中子数不同,互称为同素异形体
B
同素异形体:由同种元素形成的不同单质,互称为同素异形体。
项目 元素 核素 同位素 同素异形体
本质
范畴
特性
决定 因素
举例
项目 元素 核素 同位素 同素异形体
本质 质子数相同 的一类原子 质子数、中子数都一定的原子 同种元素不同的核素之间的互称 同种元素形成的不同单质之间的互称
范畴 同类原子,可存在游离态、化合态两种形式 原子 原子 单质
特性 只讲种类 不讲个数 化学反应中 的最小微粒 化学性质几乎完全相同 由一种元素组成,
可独立存在
决定 因素 质子数 质子数 中子数 质子数 中子数 组成元素
结构
举例 H、C、N三种元素 三种核素 互为同位素 O2与O3互为
同素异形体
任务二:认识元素周期表
一、元素周期表的编排原则
(1)原子序数:按照元素__________________给元素编的序号。
(2)原子序数=__________=_______=____________。
在周期表中的顺序
核电荷数
质子数
核外电子数
(3)横行原则:
把___________相同的元素,按_______________的顺序从左到右排列。
电子层数目
原子序数递增
画出前18号元素原子结构示意图,并分析元素周期表中横行和纵行的排列特点。
(4)纵行原则:
把不同横行中_____________相同的元素,按______________的顺序
由上而下排列。
最外层电子数
电子层数递增
二、元素周期表的结构
1.每周期开头的是什么类型元素?靠近尾部的是什么类型元素?结尾又是什么类型的元素?
2.元素周期表上共有几个横行和几个纵行?周期的数目是多少?族的数目是多少?
3.每个周期包括的元素种类有几种?周期序数与原子核外电子层数有什么关系?
4. 主族序数与原子最外层电子数有什么关系?
5. 根据元素周期表的方格,你能确定元素的哪些信息?
仔细观察教材附加的元素周期表,完成课本p95页表格,并回答下列问题:
周期序数 起止元素 包括元素种类 核外电子层数
1 H~He
2
3
4
5
6
Fr~Og(118号) 7 Li~Ne
Na~Ar
K~Kr
Rb~Xe
Cs~Rn
2
8
8
18
18
32
32
1
2
3
4
5
6
7
第六周期中的镧系有15种元素;第七周期中的锕系有15种元素。
周 期
短周期
长周期
第一周期:2种元素
第二周期:8种元素
第三周期:8种元素
第四周期:18种元素
第五周期:18种元素
第六周期:32种元素 (含镧系15种元素)
第七周期:32种元素 (含锕系15种元素)
1、七个周期
元素周期表有7个横行,18个纵列。每一个横行叫做一个周期,每一个纵列叫做一个族(8、9、10三个纵列共同组成第 Ⅷ 族)。
族
主族
副族
0 族
(由稀有气体元素构成) (1)
ⅠA 、ⅡA、ⅢA、ⅣA、ⅤA、ⅥA、 ⅦA (7)
表中各族从左到右的的顺序: ⅠA、 ⅡA、 ⅢB—— ⅦB、 Ⅷ、 ⅠB、ⅡB、
ⅢA—— ⅦA、0
ⅠB 、 ⅡB、ⅢB、ⅣB、ⅤB、ⅥB、ⅦB、Ⅷ (8)
数字相连 , 遇Ⅲ则变
2、16个族
第Ⅷ族:第8、9、10三个纵行一个族
口诀:7主8副和0族
族 别名
第ⅠA族(除氢外) _______元素
第ⅦA族 _____元素
0族 稀有气体元素
碱金属
卤族
常见族的特别名称
周期序数=电子层数 主族序数=最外层电子数
二、元素周期表的结构
原子序数
相对原子质量
元素符号
元素名称
知识拓展
U
铀
5f36d17s2
238.0
元素符号,红色指放射性元素
原子序数
元素名称注*的是人造元素
3、方格
不一定,可能是第ⅡA族,也可能是0族或副族元素。
2、8、18、32。
第六周期ⅢB为镧系,共15种元素;第七周期ⅢB为锕系,共15种元素,比四、五周期多出14种元素。
1、最外层电子数是2的元素一定为第ⅡA族的元素吗?
2、在现行周期表中第四、五、六、七周期均有18列,为什么第四、五周期各有18种元素,而第六、七周期各有32种元素?
3、同主族相邻元素间原子序数差值可能是多少?说明原因。
第二、三周期差1,第四、五周期差11,原因是中间隔10格过渡元素,第六、七周期差25,原因是中间隔10格过渡元素,且ⅢB一格为15种元素。
4、同周期的第ⅡA、ⅢA元素间原子序数差值可能为多少?并说明原因。
【思考交流】
5、含有元素种类最多的族是哪一族?
ⅢB族
三、判断元素在元素周期表中的位置
1. 利用元素的位置与原子结构的关系推断(适用于主族元素)
第三周期ⅥA族。
周期序数=电子层数;
主族序数=最外层电子数
+19
2
8
8
1
+56
2
8
18
18
8
2
练习:判断下列元素原子在元素周期表的位置:
第四周期第ⅠA族
第六周期第ⅡA族
第二周期第ⅥA族
2. 0族元素定位法
(1)明确0族元素信息
0族元素 He Ne Ar Kr Xe Rn Og
所在周期 一 二 三 四 五 六 七
原子序数
2
10
18
36
54
86
118
(2)比大小定周期
(3)求差值定族序数
比较该元素原子序数与0族元素的原子序数大小,找出相邻的0族元素,确定所在周期。
若某元素原子序数比相应的0族元素大1或2,则处于下一周期的第ⅠA族或第ⅡA族;
若某元素原子序数比相应的0族元素小1~5,则处于同周期的第ⅦA族~ⅢA族。
推算原子序数为34、56、88、82的元素在周期表中的位置。
34号:第四周期第ⅥA族
53号:第五周期第ⅦA 族
53-54= -1
34-36= -2
88-86 = 2
88号:第七周期第ⅡA 族
82号:第六周期第ⅣA 族
82-86 = -4
稀有气体元素信息:2、10、18、36、54、86、118
第四章 物质结构 元素周期律
第一节 原子结构与元素周期表
第二课时 核素 元素周期表
1.知道元素、核素、同位素的含义,认识符号 的含义。
2.通过了解元素周期表的结构,认识原子结构与元素周期表中位置间的关系。从微观角度认识元素周期表的编排原则、结构及其价值,明确周期表的基本关系、规律、元素种类及元素分布等,发展学生”宏观辨识与微观探析“、”证据推理与模型认知”化学学科核心素养。
核心素养
A
Z
X
情境导学
观察课本p96页表4-4,为什么在图b中H的质量数有3个呢?
原子符号 质子数(Z) 中子数(N) 氢原子名称
1 氕(piē)
1 氘(dāo)
1 氚(chuān)
1
1
H
1
2
H或D
1
3
H或T
1.将表格填写完整。
2.氕、氘、氚的原子结构有何异同?
3.它们是同一种元素吗?为什么?
任务一:元素、核素、同位素
氢元素的三种不同原子
0
1
2
任务一:元素、核素、同位素
1、元素:具有相同质子数(核电荷数)的一类原子的总称。
同种元素原子的质子数 相同,中子数 相同。
元素属于宏观概念,只讲种类不讲个数。
一定
不一定
2、核素:具有一定数目质子和一定数目中子的一种原子。
同一种核素的质子数 相同,中子数 相同。
核素属于微观概念。
一定
一定
思考:氕、氘、氚三者的关系?
同一元素的三种不同核素。互为同位素。
任务一:元素、核素、同位素
3、同位素:质子数相同而中子数不同的同一元素的不同原子,(即同一元素的不同核素)互称为同位素。
氧元素
O
16
8
O
17
8
O
18
8
碳元素
C
12
6
C
13
6
C
14
6
铀元素
U
234
92
U
235
92
U
238
92
化学性质几乎完全相同,物理性质有差异。
天然存在的同位数,相互间保持一定的比率。
元素的相对原子质量,就是按照该元素各种核素所占的一定百分比计算出来的平均值。
应用:考古;制造氢弹;育种,治疗疾病。
利用放射性同位素治疗恶性肿瘤
1.在① Li、② N 、③ Na、④ Mg、⑤ Li、⑥ C中:
(1) 和 互为同位素。
(2) 和 质量数相等,但不能互称同位素。
(3) 和 的中子数相等,但质子数不相等,所以不是同一种元素。
①
⑤
2.下列各组中属于同位素的是( )
A、40K与40Ca B、T2O和H2O
C、40K与39K D、金刚石与石墨
⑥
②
④
③
C
3.金属钛对人体无毒且能与肌肉和骨骼生长在一起,有“生物金属”之称。下列有关和的说法正确的是
A.和的质量数不同,属于两种元素
B. 和的质子数相同,互称同位素
C. 和的质子数相同,是同一种核素
D. 和核外电子数相同,中子数不同,互称为同素异形体
B
同素异形体:由同种元素形成的不同单质,互称为同素异形体。
项目 元素 核素 同位素 同素异形体
本质
范畴
特性
决定 因素
举例
项目 元素 核素 同位素 同素异形体
本质 质子数相同 的一类原子 质子数、中子数都一定的原子 同种元素不同的核素之间的互称 同种元素形成的不同单质之间的互称
范畴 同类原子,可存在游离态、化合态两种形式 原子 原子 单质
特性 只讲种类 不讲个数 化学反应中 的最小微粒 化学性质几乎完全相同 由一种元素组成,
可独立存在
决定 因素 质子数 质子数 中子数 质子数 中子数 组成元素
结构
举例 H、C、N三种元素 三种核素 互为同位素 O2与O3互为
同素异形体
任务二:认识元素周期表
一、元素周期表的编排原则
(1)原子序数:按照元素__________________给元素编的序号。
(2)原子序数=__________=_______=____________。
在周期表中的顺序
核电荷数
质子数
核外电子数
(3)横行原则:
把___________相同的元素,按_______________的顺序从左到右排列。
电子层数目
原子序数递增
画出前18号元素原子结构示意图,并分析元素周期表中横行和纵行的排列特点。
(4)纵行原则:
把不同横行中_____________相同的元素,按______________的顺序
由上而下排列。
最外层电子数
电子层数递增
二、元素周期表的结构
1.每周期开头的是什么类型元素?靠近尾部的是什么类型元素?结尾又是什么类型的元素?
2.元素周期表上共有几个横行和几个纵行?周期的数目是多少?族的数目是多少?
3.每个周期包括的元素种类有几种?周期序数与原子核外电子层数有什么关系?
4. 主族序数与原子最外层电子数有什么关系?
5. 根据元素周期表的方格,你能确定元素的哪些信息?
仔细观察教材附加的元素周期表,完成课本p95页表格,并回答下列问题:
周期序数 起止元素 包括元素种类 核外电子层数
1 H~He
2
3
4
5
6
Fr~Og(118号) 7 Li~Ne
Na~Ar
K~Kr
Rb~Xe
Cs~Rn
2
8
8
18
18
32
32
1
2
3
4
5
6
7
第六周期中的镧系有15种元素;第七周期中的锕系有15种元素。
周 期
短周期
长周期
第一周期:2种元素
第二周期:8种元素
第三周期:8种元素
第四周期:18种元素
第五周期:18种元素
第六周期:32种元素 (含镧系15种元素)
第七周期:32种元素 (含锕系15种元素)
1、七个周期
元素周期表有7个横行,18个纵列。每一个横行叫做一个周期,每一个纵列叫做一个族(8、9、10三个纵列共同组成第 Ⅷ 族)。
族
主族
副族
0 族
(由稀有气体元素构成) (1)
ⅠA 、ⅡA、ⅢA、ⅣA、ⅤA、ⅥA、 ⅦA (7)
表中各族从左到右的的顺序: ⅠA、 ⅡA、 ⅢB—— ⅦB、 Ⅷ、 ⅠB、ⅡB、
ⅢA—— ⅦA、0
ⅠB 、 ⅡB、ⅢB、ⅣB、ⅤB、ⅥB、ⅦB、Ⅷ (8)
数字相连 , 遇Ⅲ则变
2、16个族
第Ⅷ族:第8、9、10三个纵行一个族
口诀:7主8副和0族
族 别名
第ⅠA族(除氢外) _______元素
第ⅦA族 _____元素
0族 稀有气体元素
碱金属
卤族
常见族的特别名称
周期序数=电子层数 主族序数=最外层电子数
二、元素周期表的结构
原子序数
相对原子质量
元素符号
元素名称
知识拓展
U
铀
5f36d17s2
238.0
元素符号,红色指放射性元素
原子序数
元素名称注*的是人造元素
3、方格
不一定,可能是第ⅡA族,也可能是0族或副族元素。
2、8、18、32。
第六周期ⅢB为镧系,共15种元素;第七周期ⅢB为锕系,共15种元素,比四、五周期多出14种元素。
1、最外层电子数是2的元素一定为第ⅡA族的元素吗?
2、在现行周期表中第四、五、六、七周期均有18列,为什么第四、五周期各有18种元素,而第六、七周期各有32种元素?
3、同主族相邻元素间原子序数差值可能是多少?说明原因。
第二、三周期差1,第四、五周期差11,原因是中间隔10格过渡元素,第六、七周期差25,原因是中间隔10格过渡元素,且ⅢB一格为15种元素。
4、同周期的第ⅡA、ⅢA元素间原子序数差值可能为多少?并说明原因。
【思考交流】
5、含有元素种类最多的族是哪一族?
ⅢB族
三、判断元素在元素周期表中的位置
1. 利用元素的位置与原子结构的关系推断(适用于主族元素)
第三周期ⅥA族。
周期序数=电子层数;
主族序数=最外层电子数
+19
2
8
8
1
+56
2
8
18
18
8
2
练习:判断下列元素原子在元素周期表的位置:
第四周期第ⅠA族
第六周期第ⅡA族
第二周期第ⅥA族
2. 0族元素定位法
(1)明确0族元素信息
0族元素 He Ne Ar Kr Xe Rn Og
所在周期 一 二 三 四 五 六 七
原子序数
2
10
18
36
54
86
118
(2)比大小定周期
(3)求差值定族序数
比较该元素原子序数与0族元素的原子序数大小,找出相邻的0族元素,确定所在周期。
若某元素原子序数比相应的0族元素大1或2,则处于下一周期的第ⅠA族或第ⅡA族;
若某元素原子序数比相应的0族元素小1~5,则处于同周期的第ⅦA族~ⅢA族。
推算原子序数为34、56、88、82的元素在周期表中的位置。
34号:第四周期第ⅥA族
53号:第五周期第ⅦA 族
53-54= -1
34-36= -2
88-86 = 2
88号:第七周期第ⅡA 族
82号:第六周期第ⅣA 族
82-86 = -4
稀有气体元素信息:2、10、18、36、54、86、118
