第十单元酸和碱单元同步训练题(含答案)2023-2024学年九年级化学人教版下册
文档属性
| 名称 | 第十单元酸和碱单元同步训练题(含答案)2023-2024学年九年级化学人教版下册 |
|
|
| 格式 | docx | ||
| 文件大小 | 406.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-12-24 00:00:00 | ||
图片预览




文档简介
第十单元 酸和碱 单元同步训练题
一、单选题
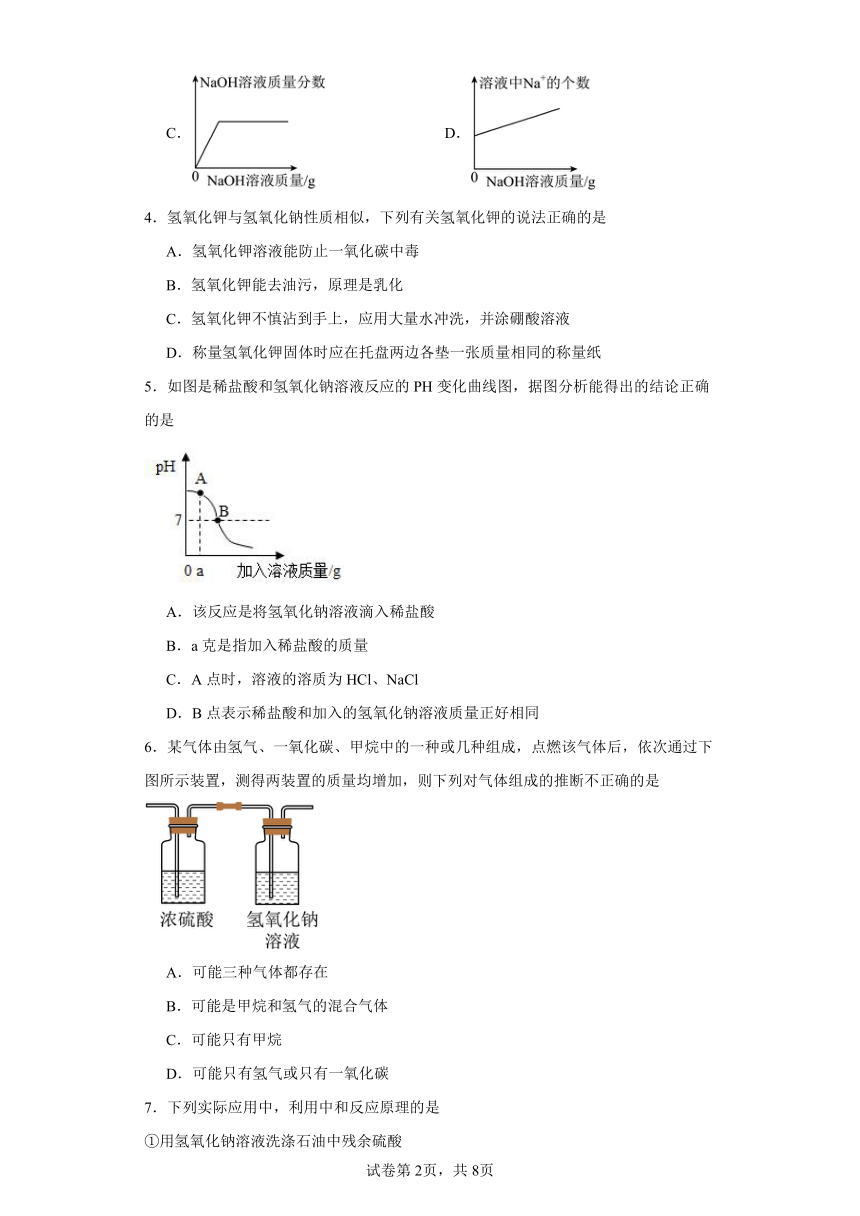
1.如图表示化学反应中溶液的颜色变化。下列叙述不正确的是
A.若X是稀盐酸,a可能是紫色石蕊试液
B.若X是稀盐酸,b可能是氧化物
C.若X是稀硫酸,c不可能是单质
D.若X是稀硫酸,d不一定是碱类物质
2.小明往氢氧化钠溶液中滴加稀盐酸研究中和反应时,忘记了滴加酸碱指示剂。为了确认滴加的盐酸是否已经过量,他取少量反应后的溶液于试管中,用某种试剂进行检验。下表是小明同学设计的实验方案,其中不正确的是
实验方案 使用的试剂 判断的方法
A 铁粉 如果有气泡产生,表明盐酸已经过量
B 氢氧化铜 如果蓝色固体消失,表明盐酸已经过量
C 硝酸银溶液 如果有白色沉淀产生,表明盐酸已经过量
D 紫色石蕊试剂 如果溶液变成红色,表明盐酸已经过量
A.A B.B C.C D.D
3.在NaCl和HCl的混合溶液中,逐滴加入NaOH溶液至过量。下列图象正确的是
A. B.
C. D.
4.氢氧化钾与氢氧化钠性质相似,下列有关氢氧化钾的说法正确的是
A.氢氧化钾溶液能防止一氧化碳中毒
B.氢氧化钾能去油污,原理是乳化
C.氢氧化钾不慎沾到手上,应用大量水冲洗,并涂硼酸溶液
D.称量氢氧化钾固体时应在托盘两边各垫一张质量相同的称量纸
5.如图是稀盐酸和氢氧化钠溶液反应的PH变化曲线图,据图分析能得出的结论正确的是
A.该反应是将氢氧化钠溶液滴入稀盐酸
B.a克是指加入稀盐酸的质量
C.A点时,溶液的溶质为HCl、NaCl
D.B点表示稀盐酸和加入的氢氧化钠溶液质量正好相同
6.某气体由氢气、一氧化碳、甲烷中的一种或几种组成,点燃该气体后,依次通过下图所示装置,测得两装置的质量均增加,则下列对气体组成的推断不正确的是
A.可能三种气体都存在
B.可能是甲烷和氢气的混合气体
C.可能只有甲烷
D.可能只有氢气或只有一氧化碳
7.下列实际应用中,利用中和反应原理的是
①用氢氧化钠溶液洗涤石油中残余硫酸
②用氢氧化铝治疗胃酸
③用熟石灰改良酸性土壤
④将稀氨水(含有、OH-)涂抹在蚊虫叮咬处(分泌出蚁酸)止痒
A.①②③④ B.仅①②③ C.仅②③④ D.仅①③④
8.下列有关实验方案设计正确的是
选项 实验目的 实验方案
A 区别稀盐酸和氯化钠溶液 滴加酚酞观察现象
B 检验生石灰是否变质 滴加酚酞观察现象
C 除去KCl固体中的MnO2 溶解后过滤
D 除去FeSO4溶液中少量的CuSO4 加入足量的铁粉充分反应后过滤
A.A B.B C.C D.D
9.为测定NaOH溶液中溶质的质量分数,向盛有一定量NaOH溶液的锥形瓶中滴加几滴酚酞溶液,再逐滴滴加已知溶质质量分数的稀盐酸,边滴边振荡、室温下用pH计测得锥形瓶中溶液pH变化如图。下列相关叙述正确的是
A.锥形瓶中溶液为无色时其pH=7
B.a点溶液能使紫色石蕊溶液变红
C.b点时盐酸与NaOH恰好完全反应
D.c点溶液的溶质有NaCl和NaOH
10.某兴趣小组利用图1装置研究稀盐酸与氢氧化钠溶液反应的过程,并用pH和温度传感器测量反应过程中的变化情况,记录得到图2和图3。则下列说法中不正确的是
A.图1的仪器A中盛装的是稀盐酸
B.将图2中d点所示溶液加热蒸干所得固体为纯净物
C.图2中c→d所示溶液中NaCl的质量不断增加
D.由图3中e→f的变化趋势可说明该反应是放热反应
11.稀HCl和NaOH溶液混合后无明显现象,要证明两者已发生化学反应,如图操作及实验现象(或结果),不能证明反应发生的是
A.在混合液中加金属Zn,无气泡产生
B.在混合液中加无色酚酞,溶液呈无色的
C.在混合液中加AgNO3溶液,有白色沉淀
D.用pH试纸测混合液的pH,测得pH等于7
12.物质的检验、鉴别与除杂是重要的实验技能。下列依据实验目的所设计的实验方案中,不正确的是
选项 实验目的 实验方法
A 检验某气体是否为O2 用带火星的木条检验
B 除去NaCl溶液中的Na2CO3 向溶液中加入适量稀盐酸
C 鉴别NH4NO3和NaCl 取样,加水,观察温度的变化
D 除去CaO中的CaCO3 加水溶解,过滤
A.A B.B C.C D.D
13.向一包久置于空气中的生石灰干燥剂样品中加入100g溶质质量分数为3.65%的稀盐酸,恰好完全反应,有气泡产生,下列说法正确的是
A.样品加水溶解,静置,上层清液中可能含有2种溶质
B.样品中钙元素的质量分数可能为75%
C.样品中钙元素的质量一定为2g
D.产生二氧化碳的质量一定为2.2g
14.现有一包金属粉末,可能是由A1、Mg、Zn、Fe、Ag中的一种或几种组成。取该样品2.4g,向其加入100g一定溶质质量分数的稀硫酸,恰好完全反应,产生0.2g H2,溶液呈无色,无固体剩余。则下列结论正确的是
A.该样品的组成仅有两种可能 B.所用稀硫酸的溶质质量分数为19.6%
C.该样品中一定含有Mg D.所得溶液中溶质的总质量为12g
二、填空题
15.化学兴趣小组的同学做中和反应实验时,将稀盐酸滴入氢氧化钠溶液中,看到有气泡产生。是不是拿错了药品?经检验确认没有拿错药品,而是氢氧化钠溶液变质了。小组同学另取未变质的氢氧化钠溶液继续实验,记录信息如下:
(1)氢氧化钠溶液变质的原因是 ;(用化学方程式表示)。
(2)图一中表示盐酸和氢氧化钠恰好反应的稀盐酸用量是 g。
(3)图二说明中和反应 (填“吸热”或“放热”)。
(4)由图三知中和反应的实质是 。
(5)氢氧化钠与盐酸反应的化学方程式 。
16.化学的学科特征让在原子、分子的水平上研究物成和创造物质。请从微观的角度回答下列问题。
(1)物质的结构决定性质。
①根据Na、Al的原子结构示意图可推知,金属Na、Al的化学性质不同的原因是
②CO和CO2化学性质不同的原因是 .
③稀盐酸和稀硫酸都可使紫色石蕊试剂变红,原因是 。
(2)下图是氢气在氧气中燃烧的微观示意图(图中“O”代表氢原子,“●“代表氧原子)。
①参加该化学反应的最小粒子是 ( 填微粒符号)。
②写出该反应的化学方程式 。
17.某化学实验小组同学经查阅资料,得知一些植物的花汁可作酸碱指示剂。他们取三种花汁分别用酒精(中性试剂)、稀酸溶液和稀碱溶液做实验,实验结果如下表所示。
花的种类 花汁在酒精中的颜色 花汁在稀酸中的颜色 花汁在稀碱中的颜色
玫瑰花 粉红 粉红 绿
万寿菊花 黄 黄 黄
大红花 粉红 橙 绿
请回答下列问题:
(1)为测定生活中常见的食盐水、肥皂水、汽水三种物质的酸碱性,你选择 花汁,原因是 。
(2)取所选花汁少许分别滴入上述三种物质中,请将花汁在待测物质中所显颜色填入下表:
待测物质 汽水 肥皂水 食盐水
所显颜色
18.亚硝酸钠(化学式为)是一种常用的防腐剂。亚硝酸钠是一种淡黄色或白色晶体,有咸味,易潮解,易溶于水,其水溶液呈碱性;在320℃时能分解产生氧化钠固体、一氧化氮气体和一种常见的助燃性气体。亚硝酸钠有毒性,能将人体血红蛋白中的﹢2价亚铁离子转化为﹢3价铁离子,使血红蛋白失去携氧能力,结合上述信息,完成下列实验探究:
(1)要测定亚硝酸钠溶液的酸碱度,可使用 。
(2)写出亚硝酸钠在320℃时分解的化学反应方程式: 。
(3)利用亚硝酸钠溶液进行如有图所示的实验,试管中可能产生的实验现象是 。
三、计算题
19.化学小组参与“铅蓄废电池中硫酸回收”的研学项目,回收时需要测定电池废液中硫酸的质量分数。向装有50g废液的锥形瓶中加入质量分数为20%的氢氧化钠溶液,并充分搅拌,利用温度传感器等电子设备采集信息并绘制成下图,请据图回答相关问题。(杂可溶但不参加反应)
(1)该反应是 (选填“吸热”或“放热”)反应。
(2)恰好完全反应时,溶液的温度为 ℃。
(3)计算废液中硫酸的质量分数 。(写出计算过程)
(4)配制上述实验所用的氢氧化钠溶液。
①氢氧化钠固体应放在玻璃器皿中称量的原因是 ;
②用量筒量水时仰视读数,会导致测定废液中硫酸的质量分数结果 (选填“偏大”、“偏小”或“不变”)。
20.盐酸是一种重要的化工原料,但在使用前一般需测定其中HCl的质量分数。现取200g未知溶质质量分数的盐酸溶液于锥形瓶中,然后向锥形瓶中滴加溶质质量分数为20%的氢氧化钠溶液至pH=7(常温)时消耗氢氧化钠溶液200g,求盐酸中HCl的质量分数?
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.C
2.C
3.D
4.C
5.B
6.D
7.A
8.D
9.C
10.C
11.C
12.D
13.C
14.D
15. 20 放热 或酸中的氢离子和碱中的氢氧根离子反应生成水分子
16. 钠元素与铝原子的最外层电子数不同 一氧化碳分子与二氧化碳分子结构不同 它们电离时产生的阳离子都是氢离子 H、O
17. 大红 它的花汁能够在中性、酸性溶液和碱性溶液中呈现不同的颜色 橙 绿 粉红
18. 试纸 溶液由浅绿色变为黄色
19.(1)放热
(2)t3
(3)解:设废液中硫酸的质量分数为x
x=19.6%
答:废液中硫酸的质量分数为19.6%
(4) 氢氧化钠固体易潮解,且腐蚀性较强 偏大
20.解:设盐酸溶液中HCl的质量分数为
答:盐酸中HCl的质量分数为18.25%。
答案第1页,共2页
答案第1页,共2页
一、单选题
1.如图表示化学反应中溶液的颜色变化。下列叙述不正确的是
A.若X是稀盐酸,a可能是紫色石蕊试液
B.若X是稀盐酸,b可能是氧化物
C.若X是稀硫酸,c不可能是单质
D.若X是稀硫酸,d不一定是碱类物质
2.小明往氢氧化钠溶液中滴加稀盐酸研究中和反应时,忘记了滴加酸碱指示剂。为了确认滴加的盐酸是否已经过量,他取少量反应后的溶液于试管中,用某种试剂进行检验。下表是小明同学设计的实验方案,其中不正确的是
实验方案 使用的试剂 判断的方法
A 铁粉 如果有气泡产生,表明盐酸已经过量
B 氢氧化铜 如果蓝色固体消失,表明盐酸已经过量
C 硝酸银溶液 如果有白色沉淀产生,表明盐酸已经过量
D 紫色石蕊试剂 如果溶液变成红色,表明盐酸已经过量
A.A B.B C.C D.D
3.在NaCl和HCl的混合溶液中,逐滴加入NaOH溶液至过量。下列图象正确的是
A. B.
C. D.
4.氢氧化钾与氢氧化钠性质相似,下列有关氢氧化钾的说法正确的是
A.氢氧化钾溶液能防止一氧化碳中毒
B.氢氧化钾能去油污,原理是乳化
C.氢氧化钾不慎沾到手上,应用大量水冲洗,并涂硼酸溶液
D.称量氢氧化钾固体时应在托盘两边各垫一张质量相同的称量纸
5.如图是稀盐酸和氢氧化钠溶液反应的PH变化曲线图,据图分析能得出的结论正确的是
A.该反应是将氢氧化钠溶液滴入稀盐酸
B.a克是指加入稀盐酸的质量
C.A点时,溶液的溶质为HCl、NaCl
D.B点表示稀盐酸和加入的氢氧化钠溶液质量正好相同
6.某气体由氢气、一氧化碳、甲烷中的一种或几种组成,点燃该气体后,依次通过下图所示装置,测得两装置的质量均增加,则下列对气体组成的推断不正确的是
A.可能三种气体都存在
B.可能是甲烷和氢气的混合气体
C.可能只有甲烷
D.可能只有氢气或只有一氧化碳
7.下列实际应用中,利用中和反应原理的是
①用氢氧化钠溶液洗涤石油中残余硫酸
②用氢氧化铝治疗胃酸
③用熟石灰改良酸性土壤
④将稀氨水(含有、OH-)涂抹在蚊虫叮咬处(分泌出蚁酸)止痒
A.①②③④ B.仅①②③ C.仅②③④ D.仅①③④
8.下列有关实验方案设计正确的是
选项 实验目的 实验方案
A 区别稀盐酸和氯化钠溶液 滴加酚酞观察现象
B 检验生石灰是否变质 滴加酚酞观察现象
C 除去KCl固体中的MnO2 溶解后过滤
D 除去FeSO4溶液中少量的CuSO4 加入足量的铁粉充分反应后过滤
A.A B.B C.C D.D
9.为测定NaOH溶液中溶质的质量分数,向盛有一定量NaOH溶液的锥形瓶中滴加几滴酚酞溶液,再逐滴滴加已知溶质质量分数的稀盐酸,边滴边振荡、室温下用pH计测得锥形瓶中溶液pH变化如图。下列相关叙述正确的是
A.锥形瓶中溶液为无色时其pH=7
B.a点溶液能使紫色石蕊溶液变红
C.b点时盐酸与NaOH恰好完全反应
D.c点溶液的溶质有NaCl和NaOH
10.某兴趣小组利用图1装置研究稀盐酸与氢氧化钠溶液反应的过程,并用pH和温度传感器测量反应过程中的变化情况,记录得到图2和图3。则下列说法中不正确的是
A.图1的仪器A中盛装的是稀盐酸
B.将图2中d点所示溶液加热蒸干所得固体为纯净物
C.图2中c→d所示溶液中NaCl的质量不断增加
D.由图3中e→f的变化趋势可说明该反应是放热反应
11.稀HCl和NaOH溶液混合后无明显现象,要证明两者已发生化学反应,如图操作及实验现象(或结果),不能证明反应发生的是
A.在混合液中加金属Zn,无气泡产生
B.在混合液中加无色酚酞,溶液呈无色的
C.在混合液中加AgNO3溶液,有白色沉淀
D.用pH试纸测混合液的pH,测得pH等于7
12.物质的检验、鉴别与除杂是重要的实验技能。下列依据实验目的所设计的实验方案中,不正确的是
选项 实验目的 实验方法
A 检验某气体是否为O2 用带火星的木条检验
B 除去NaCl溶液中的Na2CO3 向溶液中加入适量稀盐酸
C 鉴别NH4NO3和NaCl 取样,加水,观察温度的变化
D 除去CaO中的CaCO3 加水溶解,过滤
A.A B.B C.C D.D
13.向一包久置于空气中的生石灰干燥剂样品中加入100g溶质质量分数为3.65%的稀盐酸,恰好完全反应,有气泡产生,下列说法正确的是
A.样品加水溶解,静置,上层清液中可能含有2种溶质
B.样品中钙元素的质量分数可能为75%
C.样品中钙元素的质量一定为2g
D.产生二氧化碳的质量一定为2.2g
14.现有一包金属粉末,可能是由A1、Mg、Zn、Fe、Ag中的一种或几种组成。取该样品2.4g,向其加入100g一定溶质质量分数的稀硫酸,恰好完全反应,产生0.2g H2,溶液呈无色,无固体剩余。则下列结论正确的是
A.该样品的组成仅有两种可能 B.所用稀硫酸的溶质质量分数为19.6%
C.该样品中一定含有Mg D.所得溶液中溶质的总质量为12g
二、填空题
15.化学兴趣小组的同学做中和反应实验时,将稀盐酸滴入氢氧化钠溶液中,看到有气泡产生。是不是拿错了药品?经检验确认没有拿错药品,而是氢氧化钠溶液变质了。小组同学另取未变质的氢氧化钠溶液继续实验,记录信息如下:
(1)氢氧化钠溶液变质的原因是 ;(用化学方程式表示)。
(2)图一中表示盐酸和氢氧化钠恰好反应的稀盐酸用量是 g。
(3)图二说明中和反应 (填“吸热”或“放热”)。
(4)由图三知中和反应的实质是 。
(5)氢氧化钠与盐酸反应的化学方程式 。
16.化学的学科特征让在原子、分子的水平上研究物成和创造物质。请从微观的角度回答下列问题。
(1)物质的结构决定性质。
①根据Na、Al的原子结构示意图可推知,金属Na、Al的化学性质不同的原因是
②CO和CO2化学性质不同的原因是 .
③稀盐酸和稀硫酸都可使紫色石蕊试剂变红,原因是 。
(2)下图是氢气在氧气中燃烧的微观示意图(图中“O”代表氢原子,“●“代表氧原子)。
①参加该化学反应的最小粒子是 ( 填微粒符号)。
②写出该反应的化学方程式 。
17.某化学实验小组同学经查阅资料,得知一些植物的花汁可作酸碱指示剂。他们取三种花汁分别用酒精(中性试剂)、稀酸溶液和稀碱溶液做实验,实验结果如下表所示。
花的种类 花汁在酒精中的颜色 花汁在稀酸中的颜色 花汁在稀碱中的颜色
玫瑰花 粉红 粉红 绿
万寿菊花 黄 黄 黄
大红花 粉红 橙 绿
请回答下列问题:
(1)为测定生活中常见的食盐水、肥皂水、汽水三种物质的酸碱性,你选择 花汁,原因是 。
(2)取所选花汁少许分别滴入上述三种物质中,请将花汁在待测物质中所显颜色填入下表:
待测物质 汽水 肥皂水 食盐水
所显颜色
18.亚硝酸钠(化学式为)是一种常用的防腐剂。亚硝酸钠是一种淡黄色或白色晶体,有咸味,易潮解,易溶于水,其水溶液呈碱性;在320℃时能分解产生氧化钠固体、一氧化氮气体和一种常见的助燃性气体。亚硝酸钠有毒性,能将人体血红蛋白中的﹢2价亚铁离子转化为﹢3价铁离子,使血红蛋白失去携氧能力,结合上述信息,完成下列实验探究:
(1)要测定亚硝酸钠溶液的酸碱度,可使用 。
(2)写出亚硝酸钠在320℃时分解的化学反应方程式: 。
(3)利用亚硝酸钠溶液进行如有图所示的实验,试管中可能产生的实验现象是 。
三、计算题
19.化学小组参与“铅蓄废电池中硫酸回收”的研学项目,回收时需要测定电池废液中硫酸的质量分数。向装有50g废液的锥形瓶中加入质量分数为20%的氢氧化钠溶液,并充分搅拌,利用温度传感器等电子设备采集信息并绘制成下图,请据图回答相关问题。(杂可溶但不参加反应)
(1)该反应是 (选填“吸热”或“放热”)反应。
(2)恰好完全反应时,溶液的温度为 ℃。
(3)计算废液中硫酸的质量分数 。(写出计算过程)
(4)配制上述实验所用的氢氧化钠溶液。
①氢氧化钠固体应放在玻璃器皿中称量的原因是 ;
②用量筒量水时仰视读数,会导致测定废液中硫酸的质量分数结果 (选填“偏大”、“偏小”或“不变”)。
20.盐酸是一种重要的化工原料,但在使用前一般需测定其中HCl的质量分数。现取200g未知溶质质量分数的盐酸溶液于锥形瓶中,然后向锥形瓶中滴加溶质质量分数为20%的氢氧化钠溶液至pH=7(常温)时消耗氢氧化钠溶液200g,求盐酸中HCl的质量分数?
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.C
2.C
3.D
4.C
5.B
6.D
7.A
8.D
9.C
10.C
11.C
12.D
13.C
14.D
15. 20 放热 或酸中的氢离子和碱中的氢氧根离子反应生成水分子
16. 钠元素与铝原子的最外层电子数不同 一氧化碳分子与二氧化碳分子结构不同 它们电离时产生的阳离子都是氢离子 H、O
17. 大红 它的花汁能够在中性、酸性溶液和碱性溶液中呈现不同的颜色 橙 绿 粉红
18. 试纸 溶液由浅绿色变为黄色
19.(1)放热
(2)t3
(3)解:设废液中硫酸的质量分数为x
x=19.6%
答:废液中硫酸的质量分数为19.6%
(4) 氢氧化钠固体易潮解,且腐蚀性较强 偏大
20.解:设盐酸溶液中HCl的质量分数为
答:盐酸中HCl的质量分数为18.25%。
答案第1页,共2页
答案第1页,共2页
同课章节目录
