第十单元酸和碱单元同步训练卷(含答案)--2023-2024学年九年级化学人教版下册
文档属性
| 名称 | 第十单元酸和碱单元同步训练卷(含答案)--2023-2024学年九年级化学人教版下册 |

|
|
| 格式 | docx | ||
| 文件大小 | 542.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-12-24 00:00:00 | ||
图片预览




文档简介
第十单元 酸和碱 单元同步训练卷
一、单选题
1.小丽同学梳理了以下知识:①燃烧需要同时满足三个条件,故破坏其中一个条件就可以灭火;②单质只含有一种元素,所以含一种元素的物质一定属于单质;③在置换反应时,元素化合价一定会改变;④生成盐和水的反应一定是中和反应;其中正确的个数是
A.1个 B.2个 C.3个 D.4个
2.向一定量硫酸和硫酸铜的混合溶液中,滴加氢氧化钠溶液,边滴边搅拌,反应过程中生成沉淀的质量与加入氢氧化钠溶液的质量变化如图所示。下列说法不正确的是
A.OP段发生了中和反应
B.Q点时,溶液中一定有三种离子
C.M点时,溶液中可能含有两种溶质
D.N点时,溶液中加入酚酞溶液,溶液呈红色
3.物质的性质很大程度上决定了物质的用途,下列对应关系不正确的是
选项 物质 性质 用途
A 一氧化碳 有毒 冶炼金属
B 活性炭 吸附性 作冰箱除味剂
C 生石灰 与水反应放热 自热饭盒
D 稀有气体 在通电时能发出不同颜色的光 制作霓虹灯
A.A B.B C.C D.D
4.类推是学习化学的重要方法之一,但盲目类推又可能得出错误结论。下列类推正确的是
A.H2SO4与HCl均是酸,H2SO4在水溶液中能电离出H+,则HCl在水溶液中也能电离出H+
B.锌和银均是金属,锌能与稀硫酸反应放出氢气,则银也能与稀硫酸反应放出氢气
C.溶液是均一、稳定的,则均一稳定的液体一定是溶液
D.能使石蕊变蓝的一定是碱溶液
5.推理是化学学习中常用的思维方法,下列推理正确的是
A.溶液具有均一、稳定的特征,则均一、稳定的物质一定是溶液
B.浓盐酸和浓硫酸在空气中敞口放置一段时间,溶质质量分数变小的原理相同
C.活泼金属与酸反应产生气体,与酸反应产生气体的物质不一定是活泼金属
D.向某溶液中滴加无色酚酞试液,酚酞试液不变色,说明该溶液一定显酸性
6.天宫课堂中,宇航员通过实验呈现了“奥运五环”,实验中使用了指示剂——溴百里酚蓝,溴百里酚蓝溶液在不同环境中的显色情况如表:
溶液 中性溶液 碱性溶液 酸性溶液
颜色 绿色 蓝色 黄色
下列溶液能使绿色溴百里酚蓝溶液变为黄色的是
A.氯化钠溶液 B.醋酸溶液 C.氢氧化钾溶液 D.蔗糖溶液
7.对下列事实的微观解释错误的是
选项 事实 解释
A 溶液具有均一性和稳定性 溶液中各种粒子都静止不动
B 固体溶于水时液体温度升高 溶质离子向水中扩散吸收的热量小于水合 过程放出的热量
C 溶液、溶液化学 性质存在差异 溶液中含有金属阳离子不同
D 盐酸的酸性比碳酸强 一定量的水溶液中,盐酸中含有的多
A.A B.B C.C D.D
8.做氧化铜与稀盐酸反应的实验,容器中溶液总质量随时间的变化曲线如图所示。下列说法错误的是
①该实验是将稀盐酸逐渐加到盛有氧化铜的容器中
②a点表示氧化铜与稀盐酸恰好完全反应
③a点和b点对应溶液中铜元素的质量不相等
④a点和b点对应溶液蒸发结晶后得到的固体成分不相同
A.②③ B.①②③ C.③④ D.②③④
9.下列应用中和反应的原理(用化学方程式表示)正确的是
A.高炉炼铁:Fe2O3+3CO=2Fe+3CO2
B.稀盐酸除铁锈:Fe2O3+6HCl=3FeCl2+3H2O
C.用硫酸处理印染厂的废水:H2SO4+Ca(OH)2=CaSO4+2H2O
D.用氢氧化钠溶液吸收SO2:2NaOH+SO2=Na2SO3+H2O
10.取四种植物的花瓣,分别放在研钵中,加入酒精研磨。各取少许,用稀酸或稀碱进行检验,结果如下表所示。不能做酸碱指示剂的花汁有
花的种类 花汁在酒精中的颜色 花汁在酸溶液中的颜色 花汁在碱溶液中的颜色
大红花 粉红色 橙色 绿色
玫瑰 粉红色 粉红色 绿色
万寿菊 黄色 黄色 黄色
雏菊 无色 无色 黄色
A.万寿菊 B.大红花 C.玫瑰 D.雏菊
11.一些食物近似pH如下表
食物 葡萄 牛奶 面汤 苹果汁
pH 4.0~4.4 6.3~6.6 7.6~8.0 2.9~3.3
则下列说法不正确的是
A.胃酸过多的人应少食葡萄 B.面汤属于酸性食品
C.葡萄和牛奶均为酸性食品 D.苹果汁酸性比牛奶强
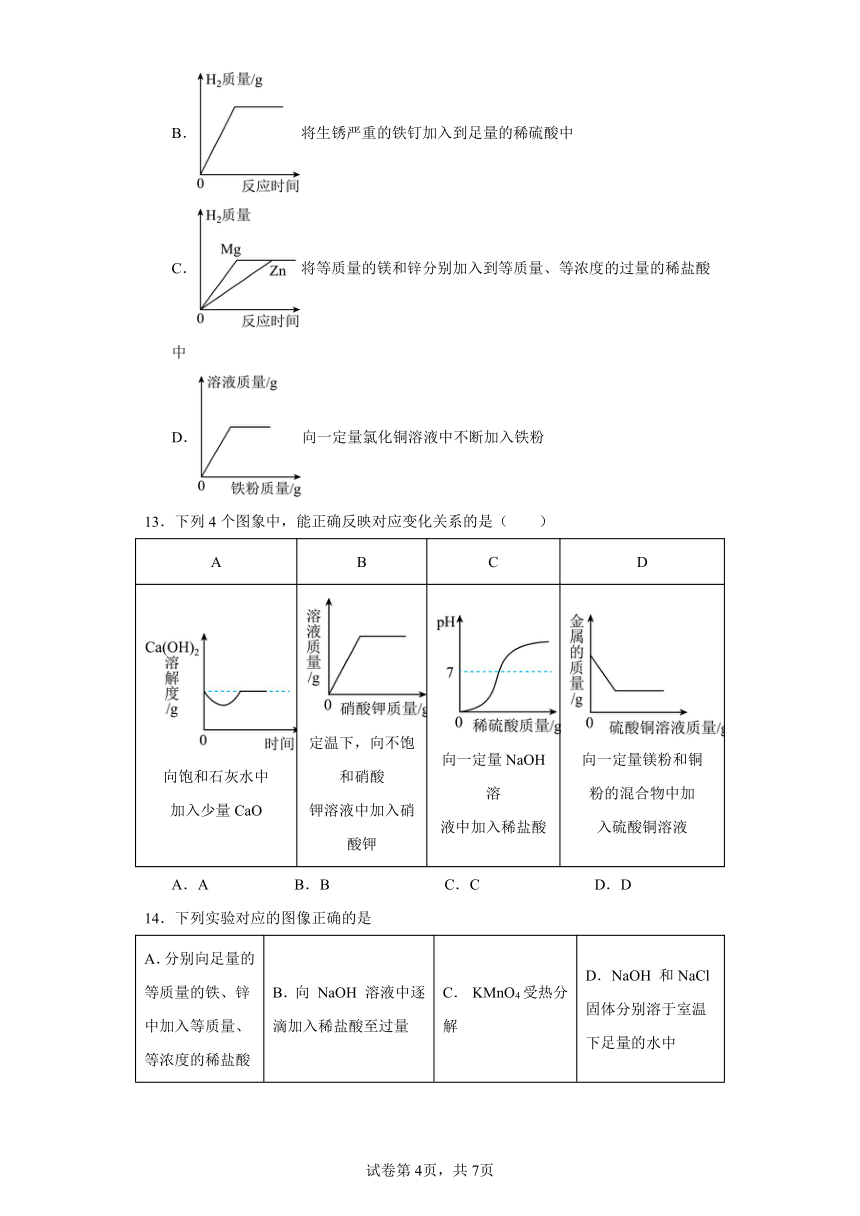
12.下列能正确反映对应变化关系的图象是
A.向稀盐酸中加入少量氧化铜粉末
B.将生锈严重的铁钉加入到足量的稀硫酸中
C.将等质量的镁和锌分别加入到等质量、等浓度的过量的稀盐酸中
D.向一定量氯化铜溶液中不断加入铁粉
13.下列4个图象中,能正确反映对应变化关系的是( )
A B C D
向饱和石灰水中 加入少量CaO 定温下,向不饱和硝酸 钾溶液中加入硝酸钾 向一定量NaOH 溶 液中加入稀盐酸 向一定量镁粉和铜 粉的混合物中加 入硫酸铜溶液
A.A B.B C.C D.D
14.下列实验对应的图像正确的是
A.分别向足量的等质量的铁、锌中加入等质量、等浓度的稀盐酸 B.向 NaOH 溶液中逐滴加入稀盐酸至过量 C. KMnO4受热分解 D.NaOH 和NaCl固体分别溶于室温下足量的水中
A.A B.B C.C D.D
15.某校化学兴趣小组利用数字化传感器探究稀盐酸和氢氧化钠溶液的反应过程,测得烧杯中溶液的随滴加液体体积变化的曲线如图所示。下列说法正确的是
A.图中a点所示溶液中,含有的溶质是NaCl和NaOH
B.由a点到c点的 变化过程证明酸和碱发生了中和反应
C.向图中c点所示溶液中滴加无色酚酞,溶液不变色
D.该实验是将盐酸逐滴滴入到盛有氢氧化钠溶液的烧杯中
二、非选择题
16.化学与人类生活、生产活动息息相关,根据所学化学知识回答下列问题:
(1)2023 年 1 月 6 日,全省首批高品质夜间经济街区名单公布,南昌 699 夜市街区入选。街区内川味凉粉深受市民喜爱,川味凉粉的主料是绿豆淀粉,制作绿豆淀粉的步骤之一是用 80 目以上的筛子使淀粉乳与豆皮、豆渣分离,筛子的作用与实验室组装的过滤器中的 相同。
(2)街区内各式烧烤也深受市民喜爱,烧烤炉的材料主要是铁,烧烤炉的某些部位常涂有油漆,可以防止生锈,其原理是 ;
(3)装饰房屋的玻璃雕刻着美丽的花纹,带给我们美的享受。使用氢氟酸(HF)刻画玻璃,发生的主要反应是4HF+SiO2=X+2H2O,则 X 的化学式为 。
(4)使用时间较久的水壶中会出现水垢,要除去水垢可选用厨房调味品中的 。
(5)用如图所示装置进行电解水的实验, N 导管口产生的气体是 。M导管口和N导管口产生气体的质量比为 。电解水过程中常加入氢氧化钠,则电解后溶液的pH (填“增大”“减小”或“不变”)。
17.下表是几种家用清洁剂的功能和有效成分。
清洁剂 洁厕灵 彩漂液
功能 清除污垢,除异味 漂洗衣物,使色彩鲜艳
有效成分 盐酸(HCl) 过氧化氢
根据表中信息,回答下列问题。
(1)若大理石的污垢用洁厕灵清洗,主要现象是 。
(2)在盛有少量“彩漂液”的试管中,加少量二氧化锰,发生反应的化学方程式为 。
18.科学食用营养物质,可以保障人体健康。
(1)某同学的部分体液的pH如图所示。
①图中碱性最强的体液是 。
②该同学胃酸(主要成分为盐酸)过多,可服用胃舒平【主要成分为Al(OH)3】治疗,其原理是 (用化学方程式表示)。
(2)某84消毒液产品的部分说明如下表。
84消毒液 【产品特点】主要成分为次氯酸钠(NaClO),有效氯的质量分数为5.19%-6.9%。 【餐具消毒】用有效氯的质量分数为0.04%的消毒液浸泡,20min后用生活饮用水冲净。 【注意事项】①外用消毒剂,须稀释后使用。 ②不得将本产品与酸性产品(如洁厕类清洁产品)同时使用。
①次氯酸钠中氯元素的化合价为 ,次氯酸的化学式为 。
②据表信息,将有效氧的质量分数为6.0%的84消毒液与水按质量比为1: 进行稀释,即可用于餐具消毒。
③洁厕灵(主要成分为盐酸)与84消毒液混合会产生有毒的氯气(Cl2)。请将该反应的化学方程式补充完整:2HCl+NaClO= +Cl2↑+H2O。
19.有限的元素可以组成种类繁多的物质,请根据H、C、O、Cl、Fe、Cu元素回答问题:
(1)我国著名科学家、化学家侯德榜先生发明了侯式制碱法,其中一步是向反应液体中通入大量气体(约占空气体积0.03%)而生成NaHCO。该气体的化学式为: 。
(2)请写出一种常用作食品干燥剂的化学式 。
(3)请写出一种能够鉴别出铜和黄铜(铜锌合金)两种物质的化学式 。
(4)《天工开物》记载:以炉甘石(ZnCO3)…掺和赤铜矿(CuO)与木炭粉,高温炼制转色为黄铜(铜、锌合金)。请用化学方程式表示该反应的原理: 。
(5)甲、乙、丙是由上述部分元素组成的初中化学常见物质,它们之间有如图所示转化关系(部分反应物、生成物及反应条件已略去,“-”表示相邻一的两种物质能发生反应,“→”表示某一物质经一步反应可转化为另一种物质)。则下列判断错误的是______。(填字母序号)
A.甲、乙、丙可能都是单质 B.甲可能是碱
C.反应① 不可能是化合反应 D.丙不可能为氯化铜
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.B
2.C
3.A
4.A
5.C
6.B
7.A
8.C
9.D
10.A
11.B
12.A
13.A
14.B
15.B
16.(1)滤纸
(2)隔绝氧气和水
(3)SiF4
(4)食醋(合理即可)
(5) 氢气/H2 8:1 增大
17.(1)大理石表面有气泡冒出
(2)2H2O22H2O+O2↑
18.(1) 胰液
(2) +1 HClO 149 NaCl
19.(1)CO2
(2)Fe
(3)HCl
(4)
(5)B
答案第1页,共2页
答案第1页,共2页
一、单选题
1.小丽同学梳理了以下知识:①燃烧需要同时满足三个条件,故破坏其中一个条件就可以灭火;②单质只含有一种元素,所以含一种元素的物质一定属于单质;③在置换反应时,元素化合价一定会改变;④生成盐和水的反应一定是中和反应;其中正确的个数是
A.1个 B.2个 C.3个 D.4个
2.向一定量硫酸和硫酸铜的混合溶液中,滴加氢氧化钠溶液,边滴边搅拌,反应过程中生成沉淀的质量与加入氢氧化钠溶液的质量变化如图所示。下列说法不正确的是
A.OP段发生了中和反应
B.Q点时,溶液中一定有三种离子
C.M点时,溶液中可能含有两种溶质
D.N点时,溶液中加入酚酞溶液,溶液呈红色
3.物质的性质很大程度上决定了物质的用途,下列对应关系不正确的是
选项 物质 性质 用途
A 一氧化碳 有毒 冶炼金属
B 活性炭 吸附性 作冰箱除味剂
C 生石灰 与水反应放热 自热饭盒
D 稀有气体 在通电时能发出不同颜色的光 制作霓虹灯
A.A B.B C.C D.D
4.类推是学习化学的重要方法之一,但盲目类推又可能得出错误结论。下列类推正确的是
A.H2SO4与HCl均是酸,H2SO4在水溶液中能电离出H+,则HCl在水溶液中也能电离出H+
B.锌和银均是金属,锌能与稀硫酸反应放出氢气,则银也能与稀硫酸反应放出氢气
C.溶液是均一、稳定的,则均一稳定的液体一定是溶液
D.能使石蕊变蓝的一定是碱溶液
5.推理是化学学习中常用的思维方法,下列推理正确的是
A.溶液具有均一、稳定的特征,则均一、稳定的物质一定是溶液
B.浓盐酸和浓硫酸在空气中敞口放置一段时间,溶质质量分数变小的原理相同
C.活泼金属与酸反应产生气体,与酸反应产生气体的物质不一定是活泼金属
D.向某溶液中滴加无色酚酞试液,酚酞试液不变色,说明该溶液一定显酸性
6.天宫课堂中,宇航员通过实验呈现了“奥运五环”,实验中使用了指示剂——溴百里酚蓝,溴百里酚蓝溶液在不同环境中的显色情况如表:
溶液 中性溶液 碱性溶液 酸性溶液
颜色 绿色 蓝色 黄色
下列溶液能使绿色溴百里酚蓝溶液变为黄色的是
A.氯化钠溶液 B.醋酸溶液 C.氢氧化钾溶液 D.蔗糖溶液
7.对下列事实的微观解释错误的是
选项 事实 解释
A 溶液具有均一性和稳定性 溶液中各种粒子都静止不动
B 固体溶于水时液体温度升高 溶质离子向水中扩散吸收的热量小于水合 过程放出的热量
C 溶液、溶液化学 性质存在差异 溶液中含有金属阳离子不同
D 盐酸的酸性比碳酸强 一定量的水溶液中,盐酸中含有的多
A.A B.B C.C D.D
8.做氧化铜与稀盐酸反应的实验,容器中溶液总质量随时间的变化曲线如图所示。下列说法错误的是
①该实验是将稀盐酸逐渐加到盛有氧化铜的容器中
②a点表示氧化铜与稀盐酸恰好完全反应
③a点和b点对应溶液中铜元素的质量不相等
④a点和b点对应溶液蒸发结晶后得到的固体成分不相同
A.②③ B.①②③ C.③④ D.②③④
9.下列应用中和反应的原理(用化学方程式表示)正确的是
A.高炉炼铁:Fe2O3+3CO=2Fe+3CO2
B.稀盐酸除铁锈:Fe2O3+6HCl=3FeCl2+3H2O
C.用硫酸处理印染厂的废水:H2SO4+Ca(OH)2=CaSO4+2H2O
D.用氢氧化钠溶液吸收SO2:2NaOH+SO2=Na2SO3+H2O
10.取四种植物的花瓣,分别放在研钵中,加入酒精研磨。各取少许,用稀酸或稀碱进行检验,结果如下表所示。不能做酸碱指示剂的花汁有
花的种类 花汁在酒精中的颜色 花汁在酸溶液中的颜色 花汁在碱溶液中的颜色
大红花 粉红色 橙色 绿色
玫瑰 粉红色 粉红色 绿色
万寿菊 黄色 黄色 黄色
雏菊 无色 无色 黄色
A.万寿菊 B.大红花 C.玫瑰 D.雏菊
11.一些食物近似pH如下表
食物 葡萄 牛奶 面汤 苹果汁
pH 4.0~4.4 6.3~6.6 7.6~8.0 2.9~3.3
则下列说法不正确的是
A.胃酸过多的人应少食葡萄 B.面汤属于酸性食品
C.葡萄和牛奶均为酸性食品 D.苹果汁酸性比牛奶强
12.下列能正确反映对应变化关系的图象是
A.向稀盐酸中加入少量氧化铜粉末
B.将生锈严重的铁钉加入到足量的稀硫酸中
C.将等质量的镁和锌分别加入到等质量、等浓度的过量的稀盐酸中
D.向一定量氯化铜溶液中不断加入铁粉
13.下列4个图象中,能正确反映对应变化关系的是( )
A B C D
向饱和石灰水中 加入少量CaO 定温下,向不饱和硝酸 钾溶液中加入硝酸钾 向一定量NaOH 溶 液中加入稀盐酸 向一定量镁粉和铜 粉的混合物中加 入硫酸铜溶液
A.A B.B C.C D.D
14.下列实验对应的图像正确的是
A.分别向足量的等质量的铁、锌中加入等质量、等浓度的稀盐酸 B.向 NaOH 溶液中逐滴加入稀盐酸至过量 C. KMnO4受热分解 D.NaOH 和NaCl固体分别溶于室温下足量的水中
A.A B.B C.C D.D
15.某校化学兴趣小组利用数字化传感器探究稀盐酸和氢氧化钠溶液的反应过程,测得烧杯中溶液的随滴加液体体积变化的曲线如图所示。下列说法正确的是
A.图中a点所示溶液中,含有的溶质是NaCl和NaOH
B.由a点到c点的 变化过程证明酸和碱发生了中和反应
C.向图中c点所示溶液中滴加无色酚酞,溶液不变色
D.该实验是将盐酸逐滴滴入到盛有氢氧化钠溶液的烧杯中
二、非选择题
16.化学与人类生活、生产活动息息相关,根据所学化学知识回答下列问题:
(1)2023 年 1 月 6 日,全省首批高品质夜间经济街区名单公布,南昌 699 夜市街区入选。街区内川味凉粉深受市民喜爱,川味凉粉的主料是绿豆淀粉,制作绿豆淀粉的步骤之一是用 80 目以上的筛子使淀粉乳与豆皮、豆渣分离,筛子的作用与实验室组装的过滤器中的 相同。
(2)街区内各式烧烤也深受市民喜爱,烧烤炉的材料主要是铁,烧烤炉的某些部位常涂有油漆,可以防止生锈,其原理是 ;
(3)装饰房屋的玻璃雕刻着美丽的花纹,带给我们美的享受。使用氢氟酸(HF)刻画玻璃,发生的主要反应是4HF+SiO2=X+2H2O,则 X 的化学式为 。
(4)使用时间较久的水壶中会出现水垢,要除去水垢可选用厨房调味品中的 。
(5)用如图所示装置进行电解水的实验, N 导管口产生的气体是 。M导管口和N导管口产生气体的质量比为 。电解水过程中常加入氢氧化钠,则电解后溶液的pH (填“增大”“减小”或“不变”)。
17.下表是几种家用清洁剂的功能和有效成分。
清洁剂 洁厕灵 彩漂液
功能 清除污垢,除异味 漂洗衣物,使色彩鲜艳
有效成分 盐酸(HCl) 过氧化氢
根据表中信息,回答下列问题。
(1)若大理石的污垢用洁厕灵清洗,主要现象是 。
(2)在盛有少量“彩漂液”的试管中,加少量二氧化锰,发生反应的化学方程式为 。
18.科学食用营养物质,可以保障人体健康。
(1)某同学的部分体液的pH如图所示。
①图中碱性最强的体液是 。
②该同学胃酸(主要成分为盐酸)过多,可服用胃舒平【主要成分为Al(OH)3】治疗,其原理是 (用化学方程式表示)。
(2)某84消毒液产品的部分说明如下表。
84消毒液 【产品特点】主要成分为次氯酸钠(NaClO),有效氯的质量分数为5.19%-6.9%。 【餐具消毒】用有效氯的质量分数为0.04%的消毒液浸泡,20min后用生活饮用水冲净。 【注意事项】①外用消毒剂,须稀释后使用。 ②不得将本产品与酸性产品(如洁厕类清洁产品)同时使用。
①次氯酸钠中氯元素的化合价为 ,次氯酸的化学式为 。
②据表信息,将有效氧的质量分数为6.0%的84消毒液与水按质量比为1: 进行稀释,即可用于餐具消毒。
③洁厕灵(主要成分为盐酸)与84消毒液混合会产生有毒的氯气(Cl2)。请将该反应的化学方程式补充完整:2HCl+NaClO= +Cl2↑+H2O。
19.有限的元素可以组成种类繁多的物质,请根据H、C、O、Cl、Fe、Cu元素回答问题:
(1)我国著名科学家、化学家侯德榜先生发明了侯式制碱法,其中一步是向反应液体中通入大量气体(约占空气体积0.03%)而生成NaHCO。该气体的化学式为: 。
(2)请写出一种常用作食品干燥剂的化学式 。
(3)请写出一种能够鉴别出铜和黄铜(铜锌合金)两种物质的化学式 。
(4)《天工开物》记载:以炉甘石(ZnCO3)…掺和赤铜矿(CuO)与木炭粉,高温炼制转色为黄铜(铜、锌合金)。请用化学方程式表示该反应的原理: 。
(5)甲、乙、丙是由上述部分元素组成的初中化学常见物质,它们之间有如图所示转化关系(部分反应物、生成物及反应条件已略去,“-”表示相邻一的两种物质能发生反应,“→”表示某一物质经一步反应可转化为另一种物质)。则下列判断错误的是______。(填字母序号)
A.甲、乙、丙可能都是单质 B.甲可能是碱
C.反应① 不可能是化合反应 D.丙不可能为氯化铜
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.B
2.C
3.A
4.A
5.C
6.B
7.A
8.C
9.D
10.A
11.B
12.A
13.A
14.B
15.B
16.(1)滤纸
(2)隔绝氧气和水
(3)SiF4
(4)食醋(合理即可)
(5) 氢气/H2 8:1 增大
17.(1)大理石表面有气泡冒出
(2)2H2O22H2O+O2↑
18.(1) 胰液
(2) +1 HClO 149 NaCl
19.(1)CO2
(2)Fe
(3)HCl
(4)
(5)B
答案第1页,共2页
答案第1页,共2页
同课章节目录
