第十单元酸和碱单元测试题(含答案)2023-2024学年九年级化学人教版下册
文档属性
| 名称 | 第十单元酸和碱单元测试题(含答案)2023-2024学年九年级化学人教版下册 |

|
|
| 格式 | docx | ||
| 文件大小 | 363.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-12-25 00:00:00 | ||
图片预览



文档简介
第十单元 酸和碱 单元测试题
一、单选题
1.下列说法不正确的是
A.二氧化碳能溶于水,也能与水发生反应
B.干冰可作制冷剂
C.某碱溶液加水稀释后,溶液的pH会变大
D.酒精溶解于水所得体积小于溶质与溶剂体积之和
2.“和谐”号动车保洁时先用洗车液清洗,然后用水冲洗至中性,最后洗车工人会用pH试纸检测是否清洗合格。下列关于pH试纸的说法正确的是
A.可以粗略测定溶液酸碱度
B.试纸使用前要用水先湿润
C.将试纸投入待测液中测定
D.若pH=7说明洗车液残留
3.下列有关实验操作正确的是
A.氢氧化钠沾到皮肤上先用大量水冲洗,再涂上盐酸
B.一氧化碳还原氧化铁的实验开始时,要先点燃酒精喷灯,再通入一氧化碳
C.检验氢气纯度,试管口向上移近火焰
D.测定食醋的酸碱度时,用玻璃棒蘸取待测液滴到pH试纸上,把试纸显示的颜色与标准比色卡比较
4.下列四个图像分别与选项中的操作相对应,其中合理的是
A.向一定量的盐酸和氯化钡混合溶液中滴加碳酸钠溶液
B.加热氯酸钾和二氧化锰的混合物制取氧气
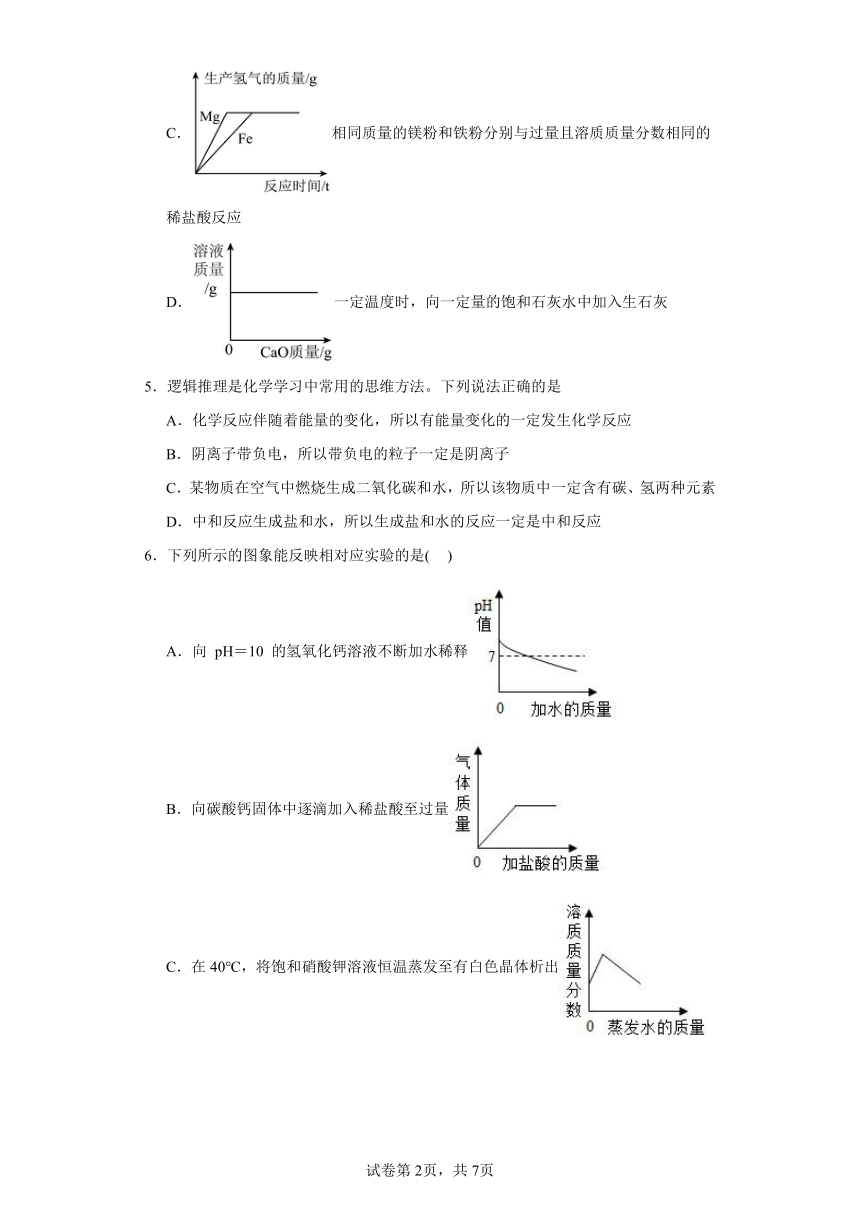
C.相同质量的镁粉和铁粉分别与过量且溶质质量分数相同的稀盐酸反应
D.一定温度时,向一定量的饱和石灰水中加入生石灰
5.逻辑推理是化学学习中常用的思维方法。下列说法正确的是
A.化学反应伴随着能量的变化,所以有能量变化的一定发生化学反应
B.阴离子带负电,所以带负电的粒子一定是阴离子
C.某物质在空气中燃烧生成二氧化碳和水,所以该物质中一定含有碳、氢两种元素
D.中和反应生成盐和水,所以生成盐和水的反应一定是中和反应
6.下列所示的图象能反映相对应实验的是( )
A.向 pH=10 的氢氧化钙溶液不断加水稀释
B.向碳酸钙固体中逐滴加入稀盐酸至过量
C.在40℃,将饱和硝酸钾溶液恒温蒸发至有白色晶体析出
D.将等质量的金属镁和锌分别和足量的稀硫酸混合
7.物质的性质不仅决定了它的用途,还决定了它的保存方法。固体氢氧化钠具有以下性质:
①有腐蚀性; ②易吸收水蒸气而潮解; ③易溶于水,溶解时放出热量; ④能与空气中的二氧化碳反应。 实验室中固体氢氧化钠必须密封保存的主要原因是( )
A.①② B.①③ C.②④ D.③④
8.除去下列物质中混有的少量杂质,所选用的试剂及操作方法不正确的是( )
选项 物质 杂质(少量) 试剂和操作方法
A 水蒸气 通过浓硫酸
B 稀盐酸 稀硫酸 加入过量溶液,过滤
C HCl气体 先通过NaOH溶液,再通过浓硫酸
D CO 先通过NaOH溶液,再通过浓硫酸
A.A B.B C.C D.D
9.用如图所示装置可以探究二氧化碳的制取和性质。下列关于该实验的叙述正确的是( )
A.浸有紫色石蕊试液的棉花会变蓝 B.可将稀盐酸换为稀硫酸
C.能验证二氧化碳的密度比空气大 D.上下移动粗铜丝能控制反应的发生和停止
10.下列有关硫酸的叙述中,不正确的是( )
A.硫酸溶液中,,,可以大量共存
B.硫酸和盐酸溶液中都含有,因此它们的化学性质相似
C.在稀释浓硫酸时,一定要把浓硫酸器壁慢慢注入水中,并不断搅拌
D.稀硫酸滴加到氢氧化钡溶液中,出现白色沉淀,即可说明复分解反应已经发生
11.向一定质量的CuSO4溶液中滴加NaOH溶液一段时间后,改为滴加稀盐酸,所得沉淀质量随加入试剂总体积的变化趋势,如图所示,下列有关说法不正确的是
A.b点时所加试剂一定是稀盐酸
B.加入试剂总体极为V1时,溶液中不存在NaOH
C.c点时溶液中的溶质都是盐
D.a点时溶液中一定不存在Cu2+
12.四种植物花汁在不同酸碱性下呈现的颜色如表所示.若要检测某溶液的酸碱性,最好选用( )
pH <7 =7 >7
玫瑰花汁 粉红 粉红 黄
万寿菊花汁 黄 黄 黄
大红花汁 橙 粉红 绿
万年青花汁 橙黄 浅绿 浅绿
A.玫瑰花汁 B.万寿菊花汁 C.大红花汁 D.万年青花汁
13.一些重要作物最适宜生长的土壤的pH范围如下:
作物 水稻 马铃薯 草莓 薄荷
pH 6~7 4.8~5.5 5~7.5 7~8
下列说法中正确的是( )
A.水稻和薄荷生长都适宜酸性土壤
B.草莓生长只适宜酸性土壤
C.马铃薯生长不适宜碱性土壤
D.以上作物都不适宜碱性土壤
14.为探究二氧化碳能否和水反应,用四朵石蕊溶液染成紫色的干燥小花完成下图四个实验。实验I、Ⅳ中小花变红,实验Ⅱ、Ⅲ中小花不变色。下列说法不正确的是( )
A.实验Ⅰ、Ⅱ说明醋酸可以使小花变红
B.实验Ⅲ说明二氧化碳不能使小花变红
C.实验Ⅱ、Ⅲ、Ⅳ说明二氧化碳能与水发生化学反应
D.上述实验说明二氧化碳和醋酸具有相似的化学性质
二、非选择题
15.化学兴趣小组的同学做中和反应实验时,将稀盐酸滴入氢氧化钠溶液中,看到有气泡产生。是不是拿错了药品?经检验确认没有拿错药品,而是氢氧化钠溶液变质了。小组同学另取未变质的氢氧化钠溶液继续实验,记录信息如下:
(1)氢氧化钠溶液变质的原因是 ;(用化学方程式表示)。
(2)图一中表示盐酸和氢氧化钠恰好反应的稀盐酸用量是 g。
(3)图二说明中和反应 (填“吸热”或“放热”)。
(4)由图三知中和反应的实质是 。
(5)氢氧化钠与盐酸反应的化学方程式 。
16.化学的学科特征让在原子、分子的水平上研究物成和创造物质。请从微观的角度回答下列问题。
(1)物质的结构决定性质。
①根据Na、Al的原子结构示意图可推知,金属Na、Al的化学性质不同的原因是
②CO和CO2化学性质不同的原因是 .
③稀盐酸和稀硫酸都可使紫色石蕊试剂变红,原因是 。
(2)下图是氢气在氧气中燃烧的微观示意图(图中“O”代表氢原子,“●“代表氧原子)。
①参加该化学反应的最小粒子是 ( 填微粒符号)。
②写出该反应的化学方程式 。
17.溶液酸碱度的表示法——pH
(1)溶液的酸碱性与pH
①pH>7,溶液呈 性;pH=7溶液,呈 性;pH<7溶液呈 性。
②pH越大 越强,pH越小 越强;pH升高加碱(或水),pH降低加酸(或水)。
(2)pH的测定:最简单的方法是使用
在白瓷板或玻璃片上放一小片 ,将 滴到试纸上,把试纸显示的颜色与 比较,可测出被测液的 。
注意:①不得直接将 试纸浸入 中。
②不得先用水将pH试纸 。
③用pH试纸测得的pH一般为 的整数。
④检验气体的酸碱性,可将试纸润湿再用。
(3)酸雨:正常雨水的pH约为 (因为溶有CO2),pH< 的雨水为酸雨。
18.亚硝酸钠(化学式为)是一种常用的防腐剂。亚硝酸钠是一种淡黄色或白色晶体,有咸味,易潮解,易溶于水,其水溶液呈碱性;在320℃时能分解产生氧化钠固体、一氧化氮气体和一种常见的助燃性气体。亚硝酸钠有毒性,能将人体血红蛋白中的﹢2价亚铁离子转化为﹢3价铁离子,使血红蛋白失去携氧能力,结合上述信息,完成下列实验探究:
(1)要测定亚硝酸钠溶液的酸碱度,可使用 。
(2)写出亚硝酸钠在320℃时分解的化学反应方程式: 。
(3)利用亚硝酸钠溶液进行如有图所示的实验,试管中可能产生的实验现象是 。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.C
2.A
3.D
4.A
5.C
6.B
7.C
8.B
9.D
10.A
11.D
12.C
13.C
14.D
15. 20 放热 或酸中的氢离子和碱中的氢氧根离子反应生成水分子
16. 钠元素与铝原子的最外层电子数不同 一氧化碳分子与二氧化碳分子结构不同 它们电离时产生的阳离子都是氢离子 H、O
17. 碱 中 酸 碱性 酸性 使用pH试纸 干燥的pH试纸 待测液 标准比色卡 pH值 pH 待测液 湿润 0-14 5.6 5.6
18. 试纸 溶液由浅绿色变为黄色
答案第1页,共2页
答案第1页,共2页
一、单选题
1.下列说法不正确的是
A.二氧化碳能溶于水,也能与水发生反应
B.干冰可作制冷剂
C.某碱溶液加水稀释后,溶液的pH会变大
D.酒精溶解于水所得体积小于溶质与溶剂体积之和
2.“和谐”号动车保洁时先用洗车液清洗,然后用水冲洗至中性,最后洗车工人会用pH试纸检测是否清洗合格。下列关于pH试纸的说法正确的是
A.可以粗略测定溶液酸碱度
B.试纸使用前要用水先湿润
C.将试纸投入待测液中测定
D.若pH=7说明洗车液残留
3.下列有关实验操作正确的是
A.氢氧化钠沾到皮肤上先用大量水冲洗,再涂上盐酸
B.一氧化碳还原氧化铁的实验开始时,要先点燃酒精喷灯,再通入一氧化碳
C.检验氢气纯度,试管口向上移近火焰
D.测定食醋的酸碱度时,用玻璃棒蘸取待测液滴到pH试纸上,把试纸显示的颜色与标准比色卡比较
4.下列四个图像分别与选项中的操作相对应,其中合理的是
A.向一定量的盐酸和氯化钡混合溶液中滴加碳酸钠溶液
B.加热氯酸钾和二氧化锰的混合物制取氧气
C.相同质量的镁粉和铁粉分别与过量且溶质质量分数相同的稀盐酸反应
D.一定温度时,向一定量的饱和石灰水中加入生石灰
5.逻辑推理是化学学习中常用的思维方法。下列说法正确的是
A.化学反应伴随着能量的变化,所以有能量变化的一定发生化学反应
B.阴离子带负电,所以带负电的粒子一定是阴离子
C.某物质在空气中燃烧生成二氧化碳和水,所以该物质中一定含有碳、氢两种元素
D.中和反应生成盐和水,所以生成盐和水的反应一定是中和反应
6.下列所示的图象能反映相对应实验的是( )
A.向 pH=10 的氢氧化钙溶液不断加水稀释
B.向碳酸钙固体中逐滴加入稀盐酸至过量
C.在40℃,将饱和硝酸钾溶液恒温蒸发至有白色晶体析出
D.将等质量的金属镁和锌分别和足量的稀硫酸混合
7.物质的性质不仅决定了它的用途,还决定了它的保存方法。固体氢氧化钠具有以下性质:
①有腐蚀性; ②易吸收水蒸气而潮解; ③易溶于水,溶解时放出热量; ④能与空气中的二氧化碳反应。 实验室中固体氢氧化钠必须密封保存的主要原因是( )
A.①② B.①③ C.②④ D.③④
8.除去下列物质中混有的少量杂质,所选用的试剂及操作方法不正确的是( )
选项 物质 杂质(少量) 试剂和操作方法
A 水蒸气 通过浓硫酸
B 稀盐酸 稀硫酸 加入过量溶液,过滤
C HCl气体 先通过NaOH溶液,再通过浓硫酸
D CO 先通过NaOH溶液,再通过浓硫酸
A.A B.B C.C D.D
9.用如图所示装置可以探究二氧化碳的制取和性质。下列关于该实验的叙述正确的是( )
A.浸有紫色石蕊试液的棉花会变蓝 B.可将稀盐酸换为稀硫酸
C.能验证二氧化碳的密度比空气大 D.上下移动粗铜丝能控制反应的发生和停止
10.下列有关硫酸的叙述中,不正确的是( )
A.硫酸溶液中,,,可以大量共存
B.硫酸和盐酸溶液中都含有,因此它们的化学性质相似
C.在稀释浓硫酸时,一定要把浓硫酸器壁慢慢注入水中,并不断搅拌
D.稀硫酸滴加到氢氧化钡溶液中,出现白色沉淀,即可说明复分解反应已经发生
11.向一定质量的CuSO4溶液中滴加NaOH溶液一段时间后,改为滴加稀盐酸,所得沉淀质量随加入试剂总体积的变化趋势,如图所示,下列有关说法不正确的是
A.b点时所加试剂一定是稀盐酸
B.加入试剂总体极为V1时,溶液中不存在NaOH
C.c点时溶液中的溶质都是盐
D.a点时溶液中一定不存在Cu2+
12.四种植物花汁在不同酸碱性下呈现的颜色如表所示.若要检测某溶液的酸碱性,最好选用( )
pH <7 =7 >7
玫瑰花汁 粉红 粉红 黄
万寿菊花汁 黄 黄 黄
大红花汁 橙 粉红 绿
万年青花汁 橙黄 浅绿 浅绿
A.玫瑰花汁 B.万寿菊花汁 C.大红花汁 D.万年青花汁
13.一些重要作物最适宜生长的土壤的pH范围如下:
作物 水稻 马铃薯 草莓 薄荷
pH 6~7 4.8~5.5 5~7.5 7~8
下列说法中正确的是( )
A.水稻和薄荷生长都适宜酸性土壤
B.草莓生长只适宜酸性土壤
C.马铃薯生长不适宜碱性土壤
D.以上作物都不适宜碱性土壤
14.为探究二氧化碳能否和水反应,用四朵石蕊溶液染成紫色的干燥小花完成下图四个实验。实验I、Ⅳ中小花变红,实验Ⅱ、Ⅲ中小花不变色。下列说法不正确的是( )
A.实验Ⅰ、Ⅱ说明醋酸可以使小花变红
B.实验Ⅲ说明二氧化碳不能使小花变红
C.实验Ⅱ、Ⅲ、Ⅳ说明二氧化碳能与水发生化学反应
D.上述实验说明二氧化碳和醋酸具有相似的化学性质
二、非选择题
15.化学兴趣小组的同学做中和反应实验时,将稀盐酸滴入氢氧化钠溶液中,看到有气泡产生。是不是拿错了药品?经检验确认没有拿错药品,而是氢氧化钠溶液变质了。小组同学另取未变质的氢氧化钠溶液继续实验,记录信息如下:
(1)氢氧化钠溶液变质的原因是 ;(用化学方程式表示)。
(2)图一中表示盐酸和氢氧化钠恰好反应的稀盐酸用量是 g。
(3)图二说明中和反应 (填“吸热”或“放热”)。
(4)由图三知中和反应的实质是 。
(5)氢氧化钠与盐酸反应的化学方程式 。
16.化学的学科特征让在原子、分子的水平上研究物成和创造物质。请从微观的角度回答下列问题。
(1)物质的结构决定性质。
①根据Na、Al的原子结构示意图可推知,金属Na、Al的化学性质不同的原因是
②CO和CO2化学性质不同的原因是 .
③稀盐酸和稀硫酸都可使紫色石蕊试剂变红,原因是 。
(2)下图是氢气在氧气中燃烧的微观示意图(图中“O”代表氢原子,“●“代表氧原子)。
①参加该化学反应的最小粒子是 ( 填微粒符号)。
②写出该反应的化学方程式 。
17.溶液酸碱度的表示法——pH
(1)溶液的酸碱性与pH
①pH>7,溶液呈 性;pH=7溶液,呈 性;pH<7溶液呈 性。
②pH越大 越强,pH越小 越强;pH升高加碱(或水),pH降低加酸(或水)。
(2)pH的测定:最简单的方法是使用
在白瓷板或玻璃片上放一小片 ,将 滴到试纸上,把试纸显示的颜色与 比较,可测出被测液的 。
注意:①不得直接将 试纸浸入 中。
②不得先用水将pH试纸 。
③用pH试纸测得的pH一般为 的整数。
④检验气体的酸碱性,可将试纸润湿再用。
(3)酸雨:正常雨水的pH约为 (因为溶有CO2),pH< 的雨水为酸雨。
18.亚硝酸钠(化学式为)是一种常用的防腐剂。亚硝酸钠是一种淡黄色或白色晶体,有咸味,易潮解,易溶于水,其水溶液呈碱性;在320℃时能分解产生氧化钠固体、一氧化氮气体和一种常见的助燃性气体。亚硝酸钠有毒性,能将人体血红蛋白中的﹢2价亚铁离子转化为﹢3价铁离子,使血红蛋白失去携氧能力,结合上述信息,完成下列实验探究:
(1)要测定亚硝酸钠溶液的酸碱度,可使用 。
(2)写出亚硝酸钠在320℃时分解的化学反应方程式: 。
(3)利用亚硝酸钠溶液进行如有图所示的实验,试管中可能产生的实验现象是 。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.C
2.A
3.D
4.A
5.C
6.B
7.C
8.B
9.D
10.A
11.D
12.C
13.C
14.D
15. 20 放热 或酸中的氢离子和碱中的氢氧根离子反应生成水分子
16. 钠元素与铝原子的最外层电子数不同 一氧化碳分子与二氧化碳分子结构不同 它们电离时产生的阳离子都是氢离子 H、O
17. 碱 中 酸 碱性 酸性 使用pH试纸 干燥的pH试纸 待测液 标准比色卡 pH值 pH 待测液 湿润 0-14 5.6 5.6
18. 试纸 溶液由浅绿色变为黄色
答案第1页,共2页
答案第1页,共2页
同课章节目录
