第八单元金属和金属材料 单元测试题(含答案)2023-2024学年九年级化学人教版下册
文档属性
| 名称 | 第八单元金属和金属材料 单元测试题(含答案)2023-2024学年九年级化学人教版下册 |

|
|
| 格式 | docx | ||
| 文件大小 | 507.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-12-25 00:00:00 | ||
图片预览



文档简介
第八单元 金属和金属材料 单元测试题
一、单选题
1.为验证铁、铜、银的金属活动性顺序,某同学设计了以下四组实验。下列说法错误的是
A.通过实验①、②,能验证金属活动性:Fe>Cu
B.通过实验①、②、③,能验证金属活动性:Fe>Cu>Ag
C.实验④中X为Cu,Y为FeSO4溶液,能验证金属活动性:Fe>Cu
D.实验④中X为Cu,Y为AgNO3溶液,能验证金属活动性:Cu>Ag
2.我市即将正式跨入高铁时代。高铁钢轨制造使用的是含锰钢,轨道铺设时每段钢轨的长度达1~2千米,从而大幅减少轨道借口数量。下列说法错误的是
A.制造钢轨的材料是铁的合金
B.钢轨制造时加入锰是为了增大硬度、增强韧性
C.在钢轨接口处涂上油或扣上帽,可以防止接口处锈蚀
D.钢轨热胀冷缩、歪曲变形是化学变化
3.一定条件下,H2S与O2反应前后各物质的质量如图(注意各物质起始质量)。下列说法不正确的是
A.x值为65
B.物质M中一定不含氧元素
C.该反应基本反应类型为置换反应
D.该反应中H2S与O2的化学计量数之比为1:2
4.金属R与HCl溶液反应的化学方程式为R+2HCl=RCl2+H2,则下列说法错误的是
A.该反应是置换反应 B.金属R可能是铝
C.金属R活动性比Cu强 D.该反应前后R的化合价发生了改变
5.用如图所示装置探究铜生锈的条件,一个月后发现铜丝未生锈。下列叙述错误的是
A.金属的腐蚀是金属从单质变成化合物的过程
B.在潮湿的空气中,铝比铁耐锈蚀
C.在有氧气和水的条件下,铜比铁易生锈
D.铜生锈可能与空气中的O2、H2O和CO2有关
6.金属材料对于促进生产发展、改善人类生活发挥了重大作用。下列有关金属材料的说法正确的是
A.所有金属都呈银白色
B.人类使用铝的年代早于铜、铁
C.多数合金的熔点高于它的成分金属
D.铝制品在常温下有良好的抗腐蚀性
7.已知某反应的微观示意图如图所示,则下列说法正确的是
A.反应物中甲、乙微粒个数比为1:1
B.该反应属于置换反应
C.反应生成丙与丁物质的质量比为11:6
D.该反应可以有效地减少温室效应
8.金属资源是不可再生的资源,利用与保护金属资源是现代公民的责任。下列有关金属资源利用与保护的叙述中不正确的是( )
A.大力开采稀有金属矿物,以保障金属材料的供应
B.提高废旧金属的回收利用率
C.采用多种有效防锈措施,可避免金属的锈蚀
D.用塑料代替金属制造管道和机器部件
9.托盘天平左右两边各放一只质量相等的烧杯,在两只烧杯中均加入等质量、等质量分数的稀硫酸,此时天平平衡,然后在左盘烧杯中加5g锌粒,在右盘烧杯中加5g铁粉,充分反应后两只烧杯底部均无固体剩余,此时天平
A.偏向右边 B.偏向左边 C.仍然平衡 D.无法判断
10.归纳推理是学习化学的一种重要的思维方法。下列归纳推理正确的是
A.蜡烛燃烧生成CO2和H2O,则蜡烛组成中一定含有碳、氢元素
B.铝表面会形成氧化铝保护层,则铁制品表面的铁锈也可起到保护作用
C.置换反应有单质生成,则有单质生成的反应一定是置换反应
D.催化剂在化学反应前后质量不变,则化学反应前后质量不变的物质一定是催化剂
11.有X、Y、Z三种金属,其中Y能与稀硫酸反应产生氢气,而X、Z不能与稀硫酸反应;将Z浸入X的盐溶液中,Z的表面有X析出。则X、Y、Z的金属活动性由强到弱的顺序是
A.X、Y、Z
B.Y、Z、X
C.Y、X、Z
D.Z、X、Y
12.某学习小组同学做完铁与稀硫酸反应实验后,将反应后的混合物M全部倒入盛有一小块铜锌合金的烧杯中,发现有大量气泡产生。待充分反应后过滤,得到滤液和滤渣。他们得出的现象或结论如下:①M中一定不含铁单质;②烧杯中溶液由浅绿色变成蓝色;③滤液中一定含有ZnSO4;④滤渣中可能含有三种金属单质;⑤滤液中可能含有两种金属离子。其中正确的个数有:
A.4个 B.3个 C.2个 D.1个
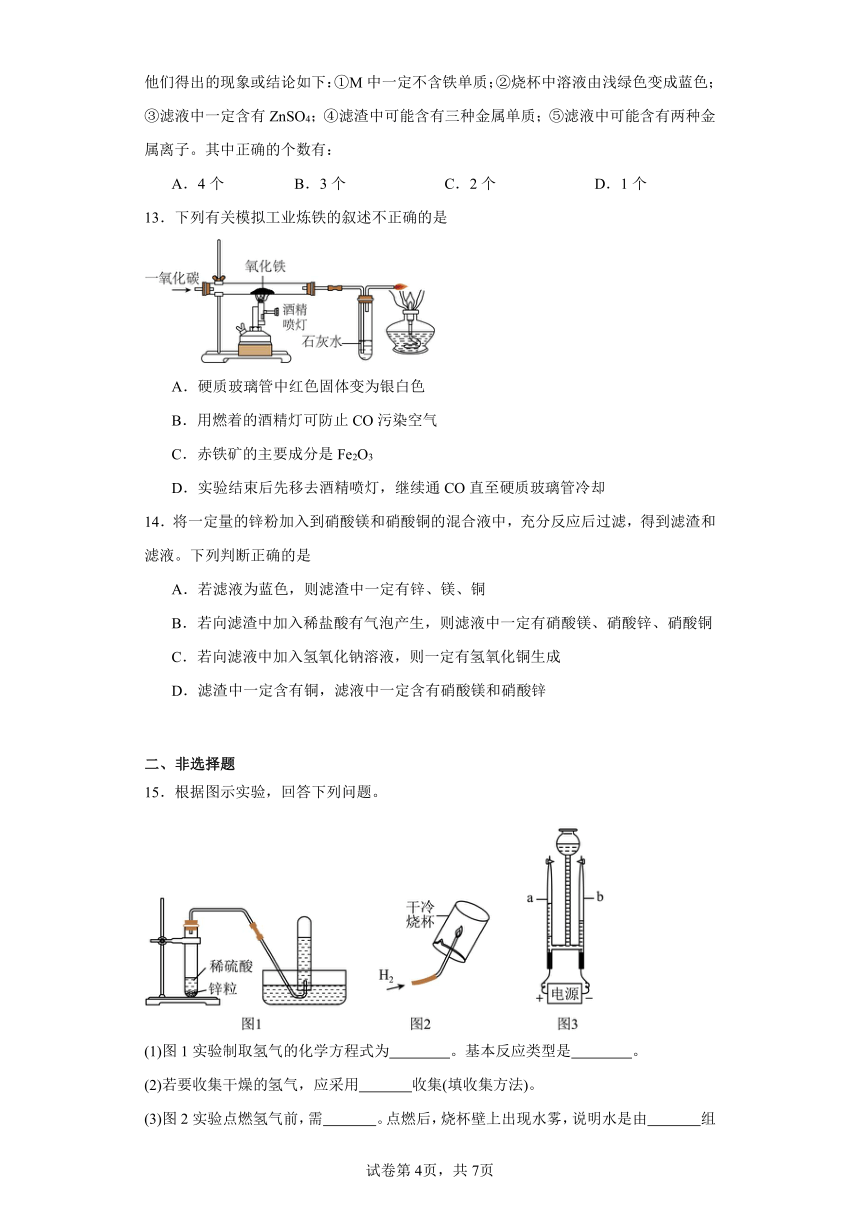
13.下列有关模拟工业炼铁的叙述不正确的是
A.硬质玻璃管中红色固体变为银白色
B.用燃着的酒精灯可防止CO污染空气
C.赤铁矿的主要成分是Fe2O3
D.实验结束后先移去酒精喷灯,继续通CO直至硬质玻璃管冷却
14.将一定量的锌粉加入到硝酸镁和硝酸铜的混合液中,充分反应后过滤,得到滤渣和滤液。下列判断正确的是
A.若滤液为蓝色,则滤渣中一定有锌、镁、铜
B.若向滤渣中加入稀盐酸有气泡产生,则滤液中一定有硝酸镁、硝酸锌、硝酸铜
C.若向滤液中加入氢氧化钠溶液,则一定有氢氧化铜生成
D.滤渣中一定含有铜,滤液中一定含有硝酸镁和硝酸锌
二、非选择题
15.根据图示实验,回答下列问题。
(1)图1实验制取氢气的化学方程式为 。基本反应类型是 。
(2)若要收集干燥的氢气,应采用 收集(填收集方法)。
(3)图2实验点燃氢气前,需 。点燃后,烧杯壁上出现水雾,说明水是由 组成。
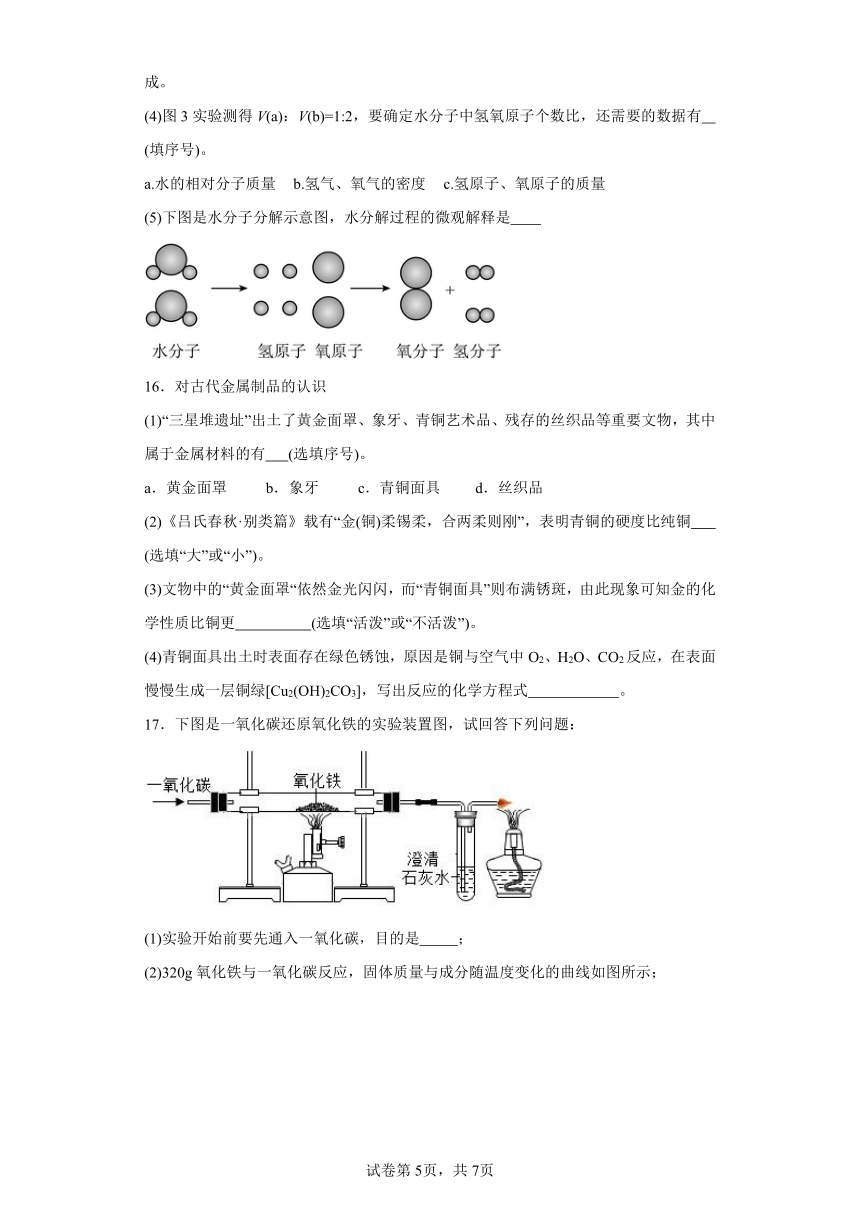
(4)图3实验测得V(a):V(b)=1:2,要确定水分子中氢氧原子个数比,还需要的数据有 (填序号)。
a.水的相对分子质量 b.氢气、氧气的密度 c.氢原子、氧原子的质量
(5)下图是水分子分解示意图,水分解过程的微观解释是
16.对古代金属制品的认识
(1)“三星堆遗址”出土了黄金面罩、象牙、青铜艺术品、残存的丝织品等重要文物,其中属于金属材料的有 (选填序号)。
a.黄金面罩 b.象牙 c.青铜面具 d.丝织品
(2)《吕氏春秋·别类篇》载有“金(铜)柔锡柔,合两柔则刚”,表明青铜的硬度比纯铜 (选填“大”或“小”)。
(3)文物中的“黄金面罩“依然金光闪闪,而“青铜面具”则布满锈斑,由此现象可知金的化学性质比铜更 (选填“活泼”或“不活泼”)。
(4)青铜面具出土时表面存在绿色锈蚀,原因是铜与空气中O2、H2O、CO2反应,在表面慢慢生成一层铜绿[Cu2(OH)2CO3],写出反应的化学方程式 。
17.下图是一氧化碳还原氧化铁的实验装置图,试回答下列问题:
(1)实验开始前要先通入一氧化碳,目的是 ;
(2)320g氧化铁与一氧化碳反应,固体质量与成分随温度变化的曲线如图所示;
①氧化铁在 ℃开始生成四氧化三铁。
②根据总反应方程式∶3CO+Fe2O32Fe+3CO2,求出图中x的值 (写出计算过程)。
(3)理论上相等质量的下列物质能得到铁质量最多的是 (填标号)。
A.Fe3O4 B.Fe2O3 C.FeCO3 D.FeO
18.金属从古至今在人类生活中都扮演着重要的角色。
(1)山西太钢集团生产“手撕钢”的工艺世界领先,“手撕钢”是一种厚度只有0.02毫米的不锈钢箔材料,钢材能够被轧压成“手斯钢”体现了金属材料的 性。
(2)要炼钢先炼铁。下图是某化学兴趣小组设计的模拟炼铁装置图。
装置A中直玻璃管内反应的化学方程式为 。虚线框内装置的作用是 。
(3)生活中为了防止铁制品生锈人们想了很多方法。为了防止厨房的菜刀生锈,一般可以采用 的方法。
(4)铝比铁活泼,但铝制品却比铁制品更耐腐蚀,原因是常温下 。
19.通过初中化学的学习,同学们掌握了一些基本的化学知识,初步形成了一些化学观念,具备了一定的化学科学素养。
(1)生活中常用来消毒,且又能使硬水软化的方法是 。
(2)房屋装修后,可在室内放一些活性炭来吸收装修材料释放出的甲醛、苯等有毒气体,这是利用活性炭的 性。
(3)市场上出售的加碘食盐“高钙牛奶”等食品,这里的“碘”“钙”是指 (选填“元素”“单质”“原子”)。
(4)2021年3月,三星堆遗址出土了金饼(如图所示),出土的金饼依然金光灿灿,从物质性质的角度解释其原因 ;金饼能加工成金链等首饰,说明金属具有物理性质是 。
(5)每到冬天,市场上便有一种“暖宝宝贴”出售,它是一个装有化学药品的小袋,袋中主要成分是铁粉。使用时,撕去它的保护膜贴在身体上,不久便会产生热量。其原因是:“暖宝宝贴”中的铁粉与 发生反应时放出热量。
(6)如图是一种家用环保型消毒液发生器,其中发生的主要反应是氯化钠和水在通电条件下反应生成氢氧化钠、氢气和氯气,该反应的化学方程式为 。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.B
2.D
3.D
4.B
5.C
6.D
7.C
8.A
9.B
10.A
11.B
12.A
13.A
14.D
15.(1) 置换反应
(2)向下排空气法
(3) 检验其纯度 氢元素和氧元素
(4)bc/cb
(5)每个水分子分解成2个氢原子和1个氧原子,2个氢原子结合成1个氢分子,2个原子结合成1个氧分子
16.(1)ac/ca
(2)大
(3)不活泼
(4)2Cu+O2+H2O+CO2=Cu2(OH)2CO3
17.(1)排尽装置内的空气,防止加热时发生爆炸
(2) 450 解:设最后生成铁的质量为x
x=224g
答: 最后生成铁,即x的值为224
(3)D
18.(1)延展
(2) 尾气处理
(3)使用后及时擦干
(4)铝和氧气反应生成致密的氧化铝薄膜
19.(1)煮沸
(2)吸附
(3)元素
(4) 金化学性质不活泼 延展性
(5)水和氧气
(6)2NaCl + 2H2O2NaOH+H2↑+Cl2↑
答案第1页,共2页
答案第1页,共2页
一、单选题
1.为验证铁、铜、银的金属活动性顺序,某同学设计了以下四组实验。下列说法错误的是
A.通过实验①、②,能验证金属活动性:Fe>Cu
B.通过实验①、②、③,能验证金属活动性:Fe>Cu>Ag
C.实验④中X为Cu,Y为FeSO4溶液,能验证金属活动性:Fe>Cu
D.实验④中X为Cu,Y为AgNO3溶液,能验证金属活动性:Cu>Ag
2.我市即将正式跨入高铁时代。高铁钢轨制造使用的是含锰钢,轨道铺设时每段钢轨的长度达1~2千米,从而大幅减少轨道借口数量。下列说法错误的是
A.制造钢轨的材料是铁的合金
B.钢轨制造时加入锰是为了增大硬度、增强韧性
C.在钢轨接口处涂上油或扣上帽,可以防止接口处锈蚀
D.钢轨热胀冷缩、歪曲变形是化学变化
3.一定条件下,H2S与O2反应前后各物质的质量如图(注意各物质起始质量)。下列说法不正确的是
A.x值为65
B.物质M中一定不含氧元素
C.该反应基本反应类型为置换反应
D.该反应中H2S与O2的化学计量数之比为1:2
4.金属R与HCl溶液反应的化学方程式为R+2HCl=RCl2+H2,则下列说法错误的是
A.该反应是置换反应 B.金属R可能是铝
C.金属R活动性比Cu强 D.该反应前后R的化合价发生了改变
5.用如图所示装置探究铜生锈的条件,一个月后发现铜丝未生锈。下列叙述错误的是
A.金属的腐蚀是金属从单质变成化合物的过程
B.在潮湿的空气中,铝比铁耐锈蚀
C.在有氧气和水的条件下,铜比铁易生锈
D.铜生锈可能与空气中的O2、H2O和CO2有关
6.金属材料对于促进生产发展、改善人类生活发挥了重大作用。下列有关金属材料的说法正确的是
A.所有金属都呈银白色
B.人类使用铝的年代早于铜、铁
C.多数合金的熔点高于它的成分金属
D.铝制品在常温下有良好的抗腐蚀性
7.已知某反应的微观示意图如图所示,则下列说法正确的是
A.反应物中甲、乙微粒个数比为1:1
B.该反应属于置换反应
C.反应生成丙与丁物质的质量比为11:6
D.该反应可以有效地减少温室效应
8.金属资源是不可再生的资源,利用与保护金属资源是现代公民的责任。下列有关金属资源利用与保护的叙述中不正确的是( )
A.大力开采稀有金属矿物,以保障金属材料的供应
B.提高废旧金属的回收利用率
C.采用多种有效防锈措施,可避免金属的锈蚀
D.用塑料代替金属制造管道和机器部件
9.托盘天平左右两边各放一只质量相等的烧杯,在两只烧杯中均加入等质量、等质量分数的稀硫酸,此时天平平衡,然后在左盘烧杯中加5g锌粒,在右盘烧杯中加5g铁粉,充分反应后两只烧杯底部均无固体剩余,此时天平
A.偏向右边 B.偏向左边 C.仍然平衡 D.无法判断
10.归纳推理是学习化学的一种重要的思维方法。下列归纳推理正确的是
A.蜡烛燃烧生成CO2和H2O,则蜡烛组成中一定含有碳、氢元素
B.铝表面会形成氧化铝保护层,则铁制品表面的铁锈也可起到保护作用
C.置换反应有单质生成,则有单质生成的反应一定是置换反应
D.催化剂在化学反应前后质量不变,则化学反应前后质量不变的物质一定是催化剂
11.有X、Y、Z三种金属,其中Y能与稀硫酸反应产生氢气,而X、Z不能与稀硫酸反应;将Z浸入X的盐溶液中,Z的表面有X析出。则X、Y、Z的金属活动性由强到弱的顺序是
A.X、Y、Z
B.Y、Z、X
C.Y、X、Z
D.Z、X、Y
12.某学习小组同学做完铁与稀硫酸反应实验后,将反应后的混合物M全部倒入盛有一小块铜锌合金的烧杯中,发现有大量气泡产生。待充分反应后过滤,得到滤液和滤渣。他们得出的现象或结论如下:①M中一定不含铁单质;②烧杯中溶液由浅绿色变成蓝色;③滤液中一定含有ZnSO4;④滤渣中可能含有三种金属单质;⑤滤液中可能含有两种金属离子。其中正确的个数有:
A.4个 B.3个 C.2个 D.1个
13.下列有关模拟工业炼铁的叙述不正确的是
A.硬质玻璃管中红色固体变为银白色
B.用燃着的酒精灯可防止CO污染空气
C.赤铁矿的主要成分是Fe2O3
D.实验结束后先移去酒精喷灯,继续通CO直至硬质玻璃管冷却
14.将一定量的锌粉加入到硝酸镁和硝酸铜的混合液中,充分反应后过滤,得到滤渣和滤液。下列判断正确的是
A.若滤液为蓝色,则滤渣中一定有锌、镁、铜
B.若向滤渣中加入稀盐酸有气泡产生,则滤液中一定有硝酸镁、硝酸锌、硝酸铜
C.若向滤液中加入氢氧化钠溶液,则一定有氢氧化铜生成
D.滤渣中一定含有铜,滤液中一定含有硝酸镁和硝酸锌
二、非选择题
15.根据图示实验,回答下列问题。
(1)图1实验制取氢气的化学方程式为 。基本反应类型是 。
(2)若要收集干燥的氢气,应采用 收集(填收集方法)。
(3)图2实验点燃氢气前,需 。点燃后,烧杯壁上出现水雾,说明水是由 组成。
(4)图3实验测得V(a):V(b)=1:2,要确定水分子中氢氧原子个数比,还需要的数据有 (填序号)。
a.水的相对分子质量 b.氢气、氧气的密度 c.氢原子、氧原子的质量
(5)下图是水分子分解示意图,水分解过程的微观解释是
16.对古代金属制品的认识
(1)“三星堆遗址”出土了黄金面罩、象牙、青铜艺术品、残存的丝织品等重要文物,其中属于金属材料的有 (选填序号)。
a.黄金面罩 b.象牙 c.青铜面具 d.丝织品
(2)《吕氏春秋·别类篇》载有“金(铜)柔锡柔,合两柔则刚”,表明青铜的硬度比纯铜 (选填“大”或“小”)。
(3)文物中的“黄金面罩“依然金光闪闪,而“青铜面具”则布满锈斑,由此现象可知金的化学性质比铜更 (选填“活泼”或“不活泼”)。
(4)青铜面具出土时表面存在绿色锈蚀,原因是铜与空气中O2、H2O、CO2反应,在表面慢慢生成一层铜绿[Cu2(OH)2CO3],写出反应的化学方程式 。
17.下图是一氧化碳还原氧化铁的实验装置图,试回答下列问题:
(1)实验开始前要先通入一氧化碳,目的是 ;
(2)320g氧化铁与一氧化碳反应,固体质量与成分随温度变化的曲线如图所示;
①氧化铁在 ℃开始生成四氧化三铁。
②根据总反应方程式∶3CO+Fe2O32Fe+3CO2,求出图中x的值 (写出计算过程)。
(3)理论上相等质量的下列物质能得到铁质量最多的是 (填标号)。
A.Fe3O4 B.Fe2O3 C.FeCO3 D.FeO
18.金属从古至今在人类生活中都扮演着重要的角色。
(1)山西太钢集团生产“手撕钢”的工艺世界领先,“手撕钢”是一种厚度只有0.02毫米的不锈钢箔材料,钢材能够被轧压成“手斯钢”体现了金属材料的 性。
(2)要炼钢先炼铁。下图是某化学兴趣小组设计的模拟炼铁装置图。
装置A中直玻璃管内反应的化学方程式为 。虚线框内装置的作用是 。
(3)生活中为了防止铁制品生锈人们想了很多方法。为了防止厨房的菜刀生锈,一般可以采用 的方法。
(4)铝比铁活泼,但铝制品却比铁制品更耐腐蚀,原因是常温下 。
19.通过初中化学的学习,同学们掌握了一些基本的化学知识,初步形成了一些化学观念,具备了一定的化学科学素养。
(1)生活中常用来消毒,且又能使硬水软化的方法是 。
(2)房屋装修后,可在室内放一些活性炭来吸收装修材料释放出的甲醛、苯等有毒气体,这是利用活性炭的 性。
(3)市场上出售的加碘食盐“高钙牛奶”等食品,这里的“碘”“钙”是指 (选填“元素”“单质”“原子”)。
(4)2021年3月,三星堆遗址出土了金饼(如图所示),出土的金饼依然金光灿灿,从物质性质的角度解释其原因 ;金饼能加工成金链等首饰,说明金属具有物理性质是 。
(5)每到冬天,市场上便有一种“暖宝宝贴”出售,它是一个装有化学药品的小袋,袋中主要成分是铁粉。使用时,撕去它的保护膜贴在身体上,不久便会产生热量。其原因是:“暖宝宝贴”中的铁粉与 发生反应时放出热量。
(6)如图是一种家用环保型消毒液发生器,其中发生的主要反应是氯化钠和水在通电条件下反应生成氢氧化钠、氢气和氯气,该反应的化学方程式为 。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.B
2.D
3.D
4.B
5.C
6.D
7.C
8.A
9.B
10.A
11.B
12.A
13.A
14.D
15.(1) 置换反应
(2)向下排空气法
(3) 检验其纯度 氢元素和氧元素
(4)bc/cb
(5)每个水分子分解成2个氢原子和1个氧原子,2个氢原子结合成1个氢分子,2个原子结合成1个氧分子
16.(1)ac/ca
(2)大
(3)不活泼
(4)2Cu+O2+H2O+CO2=Cu2(OH)2CO3
17.(1)排尽装置内的空气,防止加热时发生爆炸
(2) 450 解:设最后生成铁的质量为x
x=224g
答: 最后生成铁,即x的值为224
(3)D
18.(1)延展
(2) 尾气处理
(3)使用后及时擦干
(4)铝和氧气反应生成致密的氧化铝薄膜
19.(1)煮沸
(2)吸附
(3)元素
(4) 金化学性质不活泼 延展性
(5)水和氧气
(6)2NaCl + 2H2O2NaOH+H2↑+Cl2↑
答案第1页,共2页
答案第1页,共2页
同课章节目录
