第九单元溶液 单元测试卷(含答案)2023--2024学年九年级化学人教版下册
文档属性
| 名称 | 第九单元溶液 单元测试卷(含答案)2023--2024学年九年级化学人教版下册 |
|
|
| 格式 | docx | ||
| 文件大小 | 809.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-12-25 00:00:00 | ||
图片预览



文档简介
第九单元 溶液 单元测试卷
一、单选题
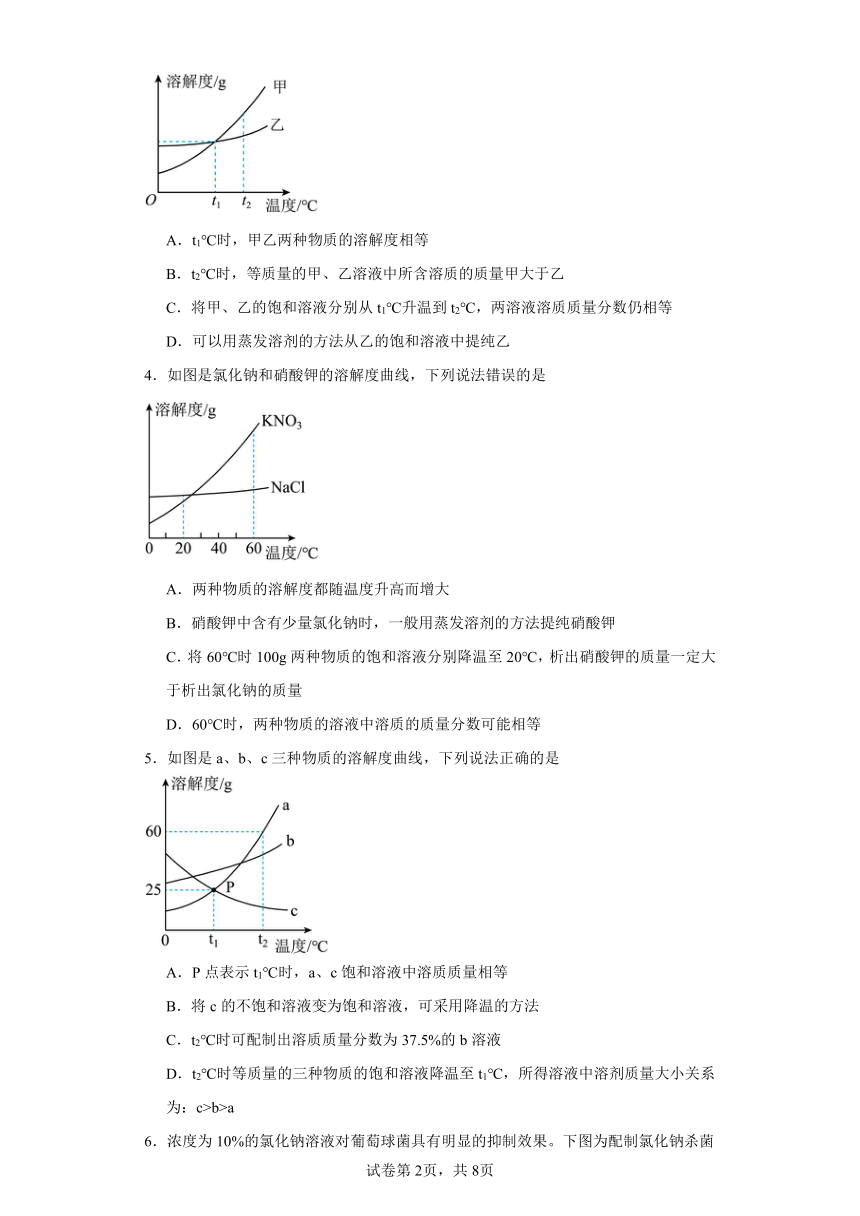
1.某化学兴趣小组用如图所示的装置来制取干燥的氧气,并测定H2O2溶液中溶质的质量分数。装置气密性良好,图I中的锥形瓶内装有二氧化锰,分液漏斗中盛有质量为m的H2O2溶液,干燥管内装有足量碱石灰(CaO和NaOH的混合物)。下列说法正确的是
A.将I分别与Ⅱ、Ⅲ、Ⅳ、V连接,均能达到实验目的
B.称量I反应前及完全反应冷却后的质量,可算出H2O2溶液中溶质的质量分数
C.若用Ⅳ收集,可将带火星的木条放置在b导管口处验满
D.若用V测量生成的体积,集气瓶上方原有的空气会使测量结果偏大
2.下列实验设计不能达到实验目的的是
选项 A B C D
实验设计
实验目的 探究呼出气体与空气中含量的差别 探究溶剂的性质对物质溶解性的影响 探究温度对分子运动快慢的影响 探究可燃物燃烧与温度达到可燃物的着火点有关
A.A B.B C.C D.D
3.如图是甲、乙两种固体物质(均不含结晶水)的溶解度曲线,下列说法错误的是
A.t1℃时,甲乙两种物质的溶解度相等
B.t2℃时,等质量的甲、乙溶液中所含溶质的质量甲大于乙
C.将甲、乙的饱和溶液分别从t1℃升温到t2℃,两溶液溶质质量分数仍相等
D.可以用蒸发溶剂的方法从乙的饱和溶液中提纯乙
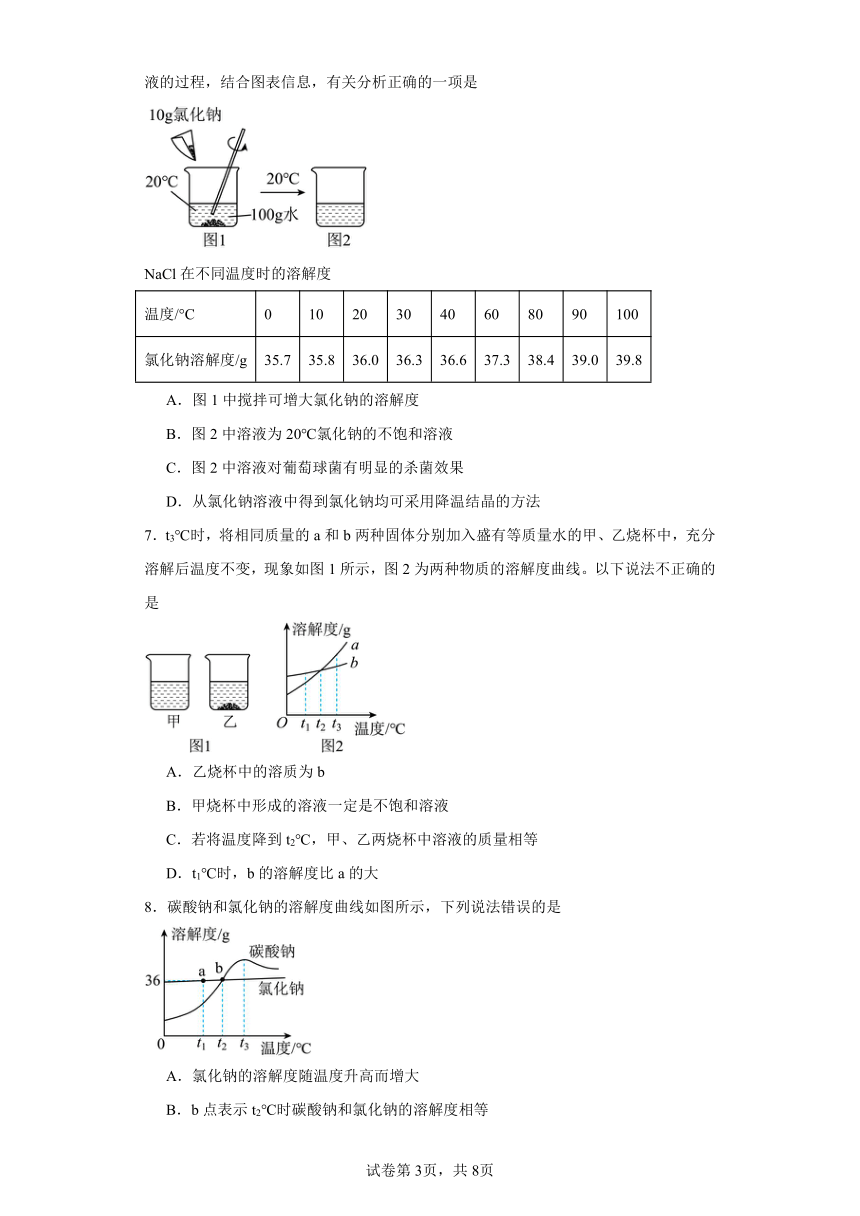
4.如图是氯化钠和硝酸钾的溶解度曲线,下列说法错误的是
A.两种物质的溶解度都随温度升高而增大
B.硝酸钾中含有少量氯化钠时,一般用蒸发溶剂的方法提纯硝酸钾
C.将60℃时100g两种物质的饱和溶液分别降温至20℃,析出硝酸钾的质量一定大于析出氯化钠的质量
D.60℃时,两种物质的溶液中溶质的质量分数可能相等
5.如图是a、b、c三种物质的溶解度曲线,下列说法正确的是
A.P点表示t1℃时,a、c饱和溶液中溶质质量相等
B.将c的不饱和溶液变为饱和溶液,可采用降温的方法
C.t2℃时可配制出溶质质量分数为37.5%的b溶液
D.t2℃时等质量的三种物质的饱和溶液降温至t1℃,所得溶液中溶剂质量大小关系为:c>b>a
6.浓度为10%的氯化钠溶液对葡萄球菌具有明显的抑制效果。下图为配制氯化钠杀菌液的过程,结合图表信息,有关分析正确的一项是
NaCl在不同温度时的溶解度
温度/°C 0 10 20 30 40 60 80 90 100
氯化钠溶解度/g 35.7 35.8 36.0 36.3 36.6 37.3 38.4 39.0 39.8
A.图1中搅拌可增大氯化钠的溶解度
B.图2中溶液为20℃氯化钠的不饱和溶液
C.图2中溶液对葡萄球菌有明显的杀菌效果
D.从氯化钠溶液中得到氯化钠均可采用降温结晶的方法
7.t3℃时,将相同质量的a和b两种固体分别加入盛有等质量水的甲、乙烧杯中,充分溶解后温度不变,现象如图1所示,图2为两种物质的溶解度曲线。以下说法不正确的是
A.乙烧杯中的溶质为b
B.甲烧杯中形成的溶液一定是不饱和溶液
C.若将温度降到t2℃,甲、乙两烧杯中溶液的质量相等
D.t1℃时,b的溶解度比a的大
8.碳酸钠和氯化钠的溶解度曲线如图所示,下列说法错误的是
A.氯化钠的溶解度随温度升高而增大
B.b点表示t2℃时碳酸钠和氯化钠的溶解度相等
C.t1℃时,将20g氯化钠放入50g水中,充分溶解后得到70g溶液
D.t3℃时,可通过升高温度的方法使接近饱和的碳酸钠溶液变为饱和溶液
9.下图是亮亮看到的NH4H2PO4和MgSO4溶解度曲线,下列说法正确的是:
A.搅拌,可以使溶解度变大
B.20℃时,在100g水中加33.7 gNH4H2PO4形成不饱和溶液
C.40℃时,NH4H2PO4的溶解度大于MgSO4的溶解度
D.NH4H2PO4溶液降温一定有晶体析出
10.配制一定质量分数的氯化钠溶液,下列操作会导致所配溶液的溶质质量分数偏小的是
①称取时,氯化钠放于右盘(使用了砝码和游码)
②所用砝码表面生锈
③溶解时烧杯内壁有水
④用量筒量取水时仰视读数
⑤将配制好的溶液装入试剂瓶,有少量洒出
A.①②④ B.①②③ C.①④⑤ D.①③④
11.如图是硝酸钾和氯化钾的溶解度曲线,下列说法不正确的是
A.小于时,氯化钾的溶解度比硝酸钾的大
B.时,两种物质的溶解度相等
C.时,向水中加入硝酸钾,得到饱和溶液
D.时,硝酸钾饱和溶液中溶质与溶液的质量比为11:21
12.如图为A、B、C三种固体物质的溶解度曲线,下列叙述中错误的是
A.时,50g水中加入25gB形成的溶液为饱和溶液
B.时,不能配制出溶质质量分数为25%的A溶液
C.B中混有少量A,应采用的提纯方法为蒸发溶剂结晶法
D.时,三种物质的溶液溶质质量分数由大到小的顺序为
13.如图是甲、乙两种物质的溶解度曲线。时,将甲和乙分别放入水中,充分搅拌,然后降温。下列说法正确的是
A.甲的溶解度大于乙的溶解度
B.时,两种溶液中溶质的质量分数相等
C.降温至时,乙溶液饱和,甲溶液不饱和
D.降温至时,两种物质的溶解度相等,甲溶液和乙溶液均饱和
14.硫酸钠、氯化钠的溶解度曲线如图所示,下列说法正确的是
A.硫酸钠的溶解度大于氯化钠的溶解度
B.20℃时,将40g氯化钠加入100g水中,充分搅拌后得到140g氯化钠溶液
C.40℃时,氯化钠溶液的溶质质量分数小于硫酸钠的溶质质量分数
D.将20℃的硫酸钠饱和溶液升温到50℃,溶质质量分数不变
二、非选择题
15.周末,小丽和爸爸妈妈一起乘坐CNG(压缩天然气)公共汽车,带上水果等礼物去乡下看望爷爷奶奶。
(1)小丽争着帮奶奶做家务,洗碗时用了洗洁精,碗洗得很干净,这是利用洗洁精对油污的 作用。
(2)妈妈给爷爷奶奶用肥皂洗衣服时,发现肥皂水中出现较多的浮渣,泡沫较少,这说明洗衣服所用的水是 (填“硬水”或“软水”)。
(3)乘坐CNG(压缩天然气)公共汽车出行,可以减少汽车尾气对空气的污染。在践行“低碳”生活的过程中,请写出一种你的做法 。
16.甲、乙、丙三种物质的溶解度曲线如图所示,请回答。
(1)t3℃时,甲的溶解度为 g。
(2)将丙的饱和溶液转化为不饱和溶液的一种方法是 。
(3)t1℃时,甲、乙的饱和溶液各100g,分别蒸发掉10g水,析出固体的质量:甲 乙(填“>”“<”或“=”)。
17.根据溶解度曲线及表中数据回答下列问题。
(1)如图中随着温度的变化溶解度变化较大的三种物质是 ,这类物质可以采取 的方法从溶液中获得晶体。
(2)如图中硝酸钠和硝酸钾两种物质的溶解度曲线有一个交点,此交点的含义是 。
(3)如表提供了硝酸钾固体在不同温度时的溶解度
温度/℃ 0 20 40 60 80
溶解度/g 13.3 31.6 63.9 110 169
①20℃时向100g水中加入40g硝酸钾,要使硝酸钾完全溶解,可以采取的措施是 。
②现有60℃时的硝酸钾饱和溶液210g,若降温至20℃析出硝酸钾晶体的质量是 g。
③表中对应的硝酸钾溶液溶质质量分数最大值为 (精确到0.1%)。
18.根据图中KNO3、NaCl的溶解度曲线,回答下列问题:
(1)40℃时,KNO3、NaCl两种物质的溶解度大小关系:KNO3 NaCl(填“>”“<”或“=”)。
(2)下列说法不正确的是 (填字母)。
A.t℃时,将45gKNO3固体放入50g水中充分溶解,所得溶液的质量为95g
B.NaCl溶液中含有少量KNO3,可以采用蒸发结晶的方法提纯NaCl
C.40℃时,将KNO3的饱和溶液降温至20℃,溶质的质量分数减小(不考虑水分损失)
(3)预使硝酸钾的不饱和溶液变为饱和溶液的方法是 (任意写一种)。
(4)同学们查阅NaCl的溶解度曲线后,欲配制20℃时100g溶质质量分数为10%的NaCl溶液。
已知配制溶液的步骤有:①溶解;②计算;③装瓶保存;④量取;⑤称量
I.上述步骤的正确顺序为 (填序号);
Ⅱ.溶解时玻璃棒的作用为 。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.B
2.A
3.B
4.B
5.D
6.B
7.B
8.C
9.C
10.D
11.C
12.D
13.B
14.D
15.(1)乳化
(2)硬水
(3)积极植树造林(或随手关闭用电器电源或一水多用)
16.(1)40
(2)加水(降低温度)
(3)<
17.(1) 硝酸钾/KNO3 降温结晶
(2)交点对应的温度下,硝酸钠和硝酸钾的溶解度相等
(3) 继续加水或升高温度 78.4
62.8%
18.(1)>
(2)A
(3)加硝酸钾(或恒温蒸发溶剂或降温)
(4) ②⑤④①③
搅拌,加快溶解速率
答案第1页,共2页
答案第1页,共2页
一、单选题
1.某化学兴趣小组用如图所示的装置来制取干燥的氧气,并测定H2O2溶液中溶质的质量分数。装置气密性良好,图I中的锥形瓶内装有二氧化锰,分液漏斗中盛有质量为m的H2O2溶液,干燥管内装有足量碱石灰(CaO和NaOH的混合物)。下列说法正确的是
A.将I分别与Ⅱ、Ⅲ、Ⅳ、V连接,均能达到实验目的
B.称量I反应前及完全反应冷却后的质量,可算出H2O2溶液中溶质的质量分数
C.若用Ⅳ收集,可将带火星的木条放置在b导管口处验满
D.若用V测量生成的体积,集气瓶上方原有的空气会使测量结果偏大
2.下列实验设计不能达到实验目的的是
选项 A B C D
实验设计
实验目的 探究呼出气体与空气中含量的差别 探究溶剂的性质对物质溶解性的影响 探究温度对分子运动快慢的影响 探究可燃物燃烧与温度达到可燃物的着火点有关
A.A B.B C.C D.D
3.如图是甲、乙两种固体物质(均不含结晶水)的溶解度曲线,下列说法错误的是
A.t1℃时,甲乙两种物质的溶解度相等
B.t2℃时,等质量的甲、乙溶液中所含溶质的质量甲大于乙
C.将甲、乙的饱和溶液分别从t1℃升温到t2℃,两溶液溶质质量分数仍相等
D.可以用蒸发溶剂的方法从乙的饱和溶液中提纯乙
4.如图是氯化钠和硝酸钾的溶解度曲线,下列说法错误的是
A.两种物质的溶解度都随温度升高而增大
B.硝酸钾中含有少量氯化钠时,一般用蒸发溶剂的方法提纯硝酸钾
C.将60℃时100g两种物质的饱和溶液分别降温至20℃,析出硝酸钾的质量一定大于析出氯化钠的质量
D.60℃时,两种物质的溶液中溶质的质量分数可能相等
5.如图是a、b、c三种物质的溶解度曲线,下列说法正确的是
A.P点表示t1℃时,a、c饱和溶液中溶质质量相等
B.将c的不饱和溶液变为饱和溶液,可采用降温的方法
C.t2℃时可配制出溶质质量分数为37.5%的b溶液
D.t2℃时等质量的三种物质的饱和溶液降温至t1℃,所得溶液中溶剂质量大小关系为:c>b>a
6.浓度为10%的氯化钠溶液对葡萄球菌具有明显的抑制效果。下图为配制氯化钠杀菌液的过程,结合图表信息,有关分析正确的一项是
NaCl在不同温度时的溶解度
温度/°C 0 10 20 30 40 60 80 90 100
氯化钠溶解度/g 35.7 35.8 36.0 36.3 36.6 37.3 38.4 39.0 39.8
A.图1中搅拌可增大氯化钠的溶解度
B.图2中溶液为20℃氯化钠的不饱和溶液
C.图2中溶液对葡萄球菌有明显的杀菌效果
D.从氯化钠溶液中得到氯化钠均可采用降温结晶的方法
7.t3℃时,将相同质量的a和b两种固体分别加入盛有等质量水的甲、乙烧杯中,充分溶解后温度不变,现象如图1所示,图2为两种物质的溶解度曲线。以下说法不正确的是
A.乙烧杯中的溶质为b
B.甲烧杯中形成的溶液一定是不饱和溶液
C.若将温度降到t2℃,甲、乙两烧杯中溶液的质量相等
D.t1℃时,b的溶解度比a的大
8.碳酸钠和氯化钠的溶解度曲线如图所示,下列说法错误的是
A.氯化钠的溶解度随温度升高而增大
B.b点表示t2℃时碳酸钠和氯化钠的溶解度相等
C.t1℃时,将20g氯化钠放入50g水中,充分溶解后得到70g溶液
D.t3℃时,可通过升高温度的方法使接近饱和的碳酸钠溶液变为饱和溶液
9.下图是亮亮看到的NH4H2PO4和MgSO4溶解度曲线,下列说法正确的是:
A.搅拌,可以使溶解度变大
B.20℃时,在100g水中加33.7 gNH4H2PO4形成不饱和溶液
C.40℃时,NH4H2PO4的溶解度大于MgSO4的溶解度
D.NH4H2PO4溶液降温一定有晶体析出
10.配制一定质量分数的氯化钠溶液,下列操作会导致所配溶液的溶质质量分数偏小的是
①称取时,氯化钠放于右盘(使用了砝码和游码)
②所用砝码表面生锈
③溶解时烧杯内壁有水
④用量筒量取水时仰视读数
⑤将配制好的溶液装入试剂瓶,有少量洒出
A.①②④ B.①②③ C.①④⑤ D.①③④
11.如图是硝酸钾和氯化钾的溶解度曲线,下列说法不正确的是
A.小于时,氯化钾的溶解度比硝酸钾的大
B.时,两种物质的溶解度相等
C.时,向水中加入硝酸钾,得到饱和溶液
D.时,硝酸钾饱和溶液中溶质与溶液的质量比为11:21
12.如图为A、B、C三种固体物质的溶解度曲线,下列叙述中错误的是
A.时,50g水中加入25gB形成的溶液为饱和溶液
B.时,不能配制出溶质质量分数为25%的A溶液
C.B中混有少量A,应采用的提纯方法为蒸发溶剂结晶法
D.时,三种物质的溶液溶质质量分数由大到小的顺序为
13.如图是甲、乙两种物质的溶解度曲线。时,将甲和乙分别放入水中,充分搅拌,然后降温。下列说法正确的是
A.甲的溶解度大于乙的溶解度
B.时,两种溶液中溶质的质量分数相等
C.降温至时,乙溶液饱和,甲溶液不饱和
D.降温至时,两种物质的溶解度相等,甲溶液和乙溶液均饱和
14.硫酸钠、氯化钠的溶解度曲线如图所示,下列说法正确的是
A.硫酸钠的溶解度大于氯化钠的溶解度
B.20℃时,将40g氯化钠加入100g水中,充分搅拌后得到140g氯化钠溶液
C.40℃时,氯化钠溶液的溶质质量分数小于硫酸钠的溶质质量分数
D.将20℃的硫酸钠饱和溶液升温到50℃,溶质质量分数不变
二、非选择题
15.周末,小丽和爸爸妈妈一起乘坐CNG(压缩天然气)公共汽车,带上水果等礼物去乡下看望爷爷奶奶。
(1)小丽争着帮奶奶做家务,洗碗时用了洗洁精,碗洗得很干净,这是利用洗洁精对油污的 作用。
(2)妈妈给爷爷奶奶用肥皂洗衣服时,发现肥皂水中出现较多的浮渣,泡沫较少,这说明洗衣服所用的水是 (填“硬水”或“软水”)。
(3)乘坐CNG(压缩天然气)公共汽车出行,可以减少汽车尾气对空气的污染。在践行“低碳”生活的过程中,请写出一种你的做法 。
16.甲、乙、丙三种物质的溶解度曲线如图所示,请回答。
(1)t3℃时,甲的溶解度为 g。
(2)将丙的饱和溶液转化为不饱和溶液的一种方法是 。
(3)t1℃时,甲、乙的饱和溶液各100g,分别蒸发掉10g水,析出固体的质量:甲 乙(填“>”“<”或“=”)。
17.根据溶解度曲线及表中数据回答下列问题。
(1)如图中随着温度的变化溶解度变化较大的三种物质是 ,这类物质可以采取 的方法从溶液中获得晶体。
(2)如图中硝酸钠和硝酸钾两种物质的溶解度曲线有一个交点,此交点的含义是 。
(3)如表提供了硝酸钾固体在不同温度时的溶解度
温度/℃ 0 20 40 60 80
溶解度/g 13.3 31.6 63.9 110 169
①20℃时向100g水中加入40g硝酸钾,要使硝酸钾完全溶解,可以采取的措施是 。
②现有60℃时的硝酸钾饱和溶液210g,若降温至20℃析出硝酸钾晶体的质量是 g。
③表中对应的硝酸钾溶液溶质质量分数最大值为 (精确到0.1%)。
18.根据图中KNO3、NaCl的溶解度曲线,回答下列问题:
(1)40℃时,KNO3、NaCl两种物质的溶解度大小关系:KNO3 NaCl(填“>”“<”或“=”)。
(2)下列说法不正确的是 (填字母)。
A.t℃时,将45gKNO3固体放入50g水中充分溶解,所得溶液的质量为95g
B.NaCl溶液中含有少量KNO3,可以采用蒸发结晶的方法提纯NaCl
C.40℃时,将KNO3的饱和溶液降温至20℃,溶质的质量分数减小(不考虑水分损失)
(3)预使硝酸钾的不饱和溶液变为饱和溶液的方法是 (任意写一种)。
(4)同学们查阅NaCl的溶解度曲线后,欲配制20℃时100g溶质质量分数为10%的NaCl溶液。
已知配制溶液的步骤有:①溶解;②计算;③装瓶保存;④量取;⑤称量
I.上述步骤的正确顺序为 (填序号);
Ⅱ.溶解时玻璃棒的作用为 。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.B
2.A
3.B
4.B
5.D
6.B
7.B
8.C
9.C
10.D
11.C
12.D
13.B
14.D
15.(1)乳化
(2)硬水
(3)积极植树造林(或随手关闭用电器电源或一水多用)
16.(1)40
(2)加水(降低温度)
(3)<
17.(1) 硝酸钾/KNO3 降温结晶
(2)交点对应的温度下,硝酸钠和硝酸钾的溶解度相等
(3) 继续加水或升高温度 78.4
62.8%
18.(1)>
(2)A
(3)加硝酸钾(或恒温蒸发溶剂或降温)
(4) ②⑤④①③
搅拌,加快溶解速率
答案第1页,共2页
答案第1页,共2页
同课章节目录
