第十一单元盐化肥单元同步测试(含答案)2023-2024学年九年级化学人教版下册
文档属性
| 名称 | 第十一单元盐化肥单元同步测试(含答案)2023-2024学年九年级化学人教版下册 |

|
|
| 格式 | docx | ||
| 文件大小 | 1.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-12-25 00:00:00 | ||
图片预览




文档简介
第十一单元 盐 化肥 单元同步测试
一、单选题
1.有一包均匀混合的Na2CO3和NaHCO3的固体粉末,为了测定其组成,小董同学称取不同质量的粉末样品溶于水,然后分别滴加相同浓度的稀盐酸100g,充分反应后记录生成CO2的质量与所取的混合固体质量关系如图所示。已知,向该混合物溶液滴加稀盐酸时,发生的化学反应分两步进行。第一步反应:。第二步反应:。根据图中信息,下列说法不正确的是
A.样品中碳酸钠的质量分数为55.8%
B.a点时所得溶液中的溶质为NaCl、Na2CO3、NaHCO3
C.14.25g样品中含NaHCO3的质量为6.3g
D.当固体样品质量为4.75g时,所取样品与100g稀盐酸恰好完全反应
2.甲、乙、丙均为初中化学常见的物质,它们之间相互关系如图所示(图中“—”表示相连的物质能相互反应,“→”表示一种物质可一步转化成另一种物质)。由此得出以下结论:
①甲、乙、丙必须含同种元素。
②图中所示关系均可通过置换反应实现。
③甲若是碱,丙只能是盐。
④丙若是氧化物,甲可以是单质或氧化物。
⑤甲、乙、丙可以是同一类别的物质(物质类别是指单质、氧化物、酸、碱、盐)。
其中正确的结论有
A.4个 B.3个 C.2个 D.1个
3.向一定质量和的混合溶液中逐滴加入溶质质量分数为10.0%的溶液。反应过程中加入的溶液的质量与产生沉淀或气体的质量关系如图所示,说法正确的是
A.图中段表示生成沉淀的过程 B.b点溶液中溶质有2种
C.x值为106.0 D.c点溶液的
4.实验室有四个药品橱,已存放如表药品,现新购进的纯碱,应将它存放在
药品橱 甲橱 乙橱 丙橱 丁橱
药品 盐酸 氢氧化钠 氯化钠 铜
A.甲橱 B.乙橱 C.丙橱 D.丁橱
5.实验室有失去标签的两瓶溶液,只知道二者为稀盐酸和稀硫酸,为区分哪个为稀盐酸,哪个为稀硫酸,请你选择一种药品将二者区分开
A.铁丝 B.氧化铜粉末 C.碳酸钠溶液 D.氯化钡溶液
6.工业上电解食盐(NaCl)溶液制取氢氧化钠(NaOH):。下列说法中不正确的是
A.NaCl可由海水蒸发、精制获得
B.点燃或加热H2前一定要检验其纯度
C.氯气(Cl2)可用于自来水生产中杀菌消毒
D.氢氧化钠易潮解,有腐蚀性,可直接在纸上称量
7.下列对实验现象的描述或实验操作正确的是
A.红磷在空气燃烧,生成五氧化二磷
B.电解水实验时,负极和正极产生气体的质量比为2:1
C.“铜绿”与盐酸混合,得到蓝绿色溶液
D.为加快过滤的速度,用玻璃棒在漏斗内不断搅拌
8.学习小组通过下列实验探究溶液的性质。
实验Ⅰ:把一根砂纸打磨过的Al丝浸入溶液中,一段时间后观察到Al丝表面出现红色物质。
实验Ⅱ:向溶液中滴加少量NaOH溶液,出现沉淀。
下列说法正确的是
A.实验Ⅰ中溶液颜色不变 B.实验Ⅰ说明Al的活动性比Cu的强
C.实验Ⅱ中只发生物理变化 D.实验Ⅱ中沉淀为CuO
9.下列实验操作或方法不能达到实验目的的是
选项 实验目的 实验操作或方法
A 除去氮气中混有的少量氧气 将气体通过灼热的铜网
B 除去KCl溶液中混有的少量CuCl2 加入氢氧化钠溶液至不再产生沉淀,过滤
C 鉴别过氧化氢溶液和水 取样,分别加入二氧化锰,观察是否产生气泡
D 鉴别化肥硫酸钾和硫酸铵 取样,分别加入熟石灰粉末混合研磨,闻气味
A.A B.B C.C D.D
10.除去下列物质中的杂质,所选用的试剂和操作方法都正确的
选项 物质 杂质 试剂 操作方法
A 铜 铁 过量的稀盐酸 溶解、过滤、洗涤、干燥
B 氯化铜溶液 氯化锌溶液 过量的锌 溶解、过滤
C 硫酸铜 铁 足量水 溶解、过滤、蒸发、结晶
D 生石灰 石灰石 无 高温煅烧
A.A B.B C.C D.D
11.下列叙述、对应的化学方程式、所属基本反应类型都正确的是
A.用稀硫酸洗去附着在试管壁上的铜: 置换反应
B.实验室制氢气: 分解反应
C.铝在空气中形成氧化膜: 化合反应
D.比较铜和银的活动性顺序: 置换反应
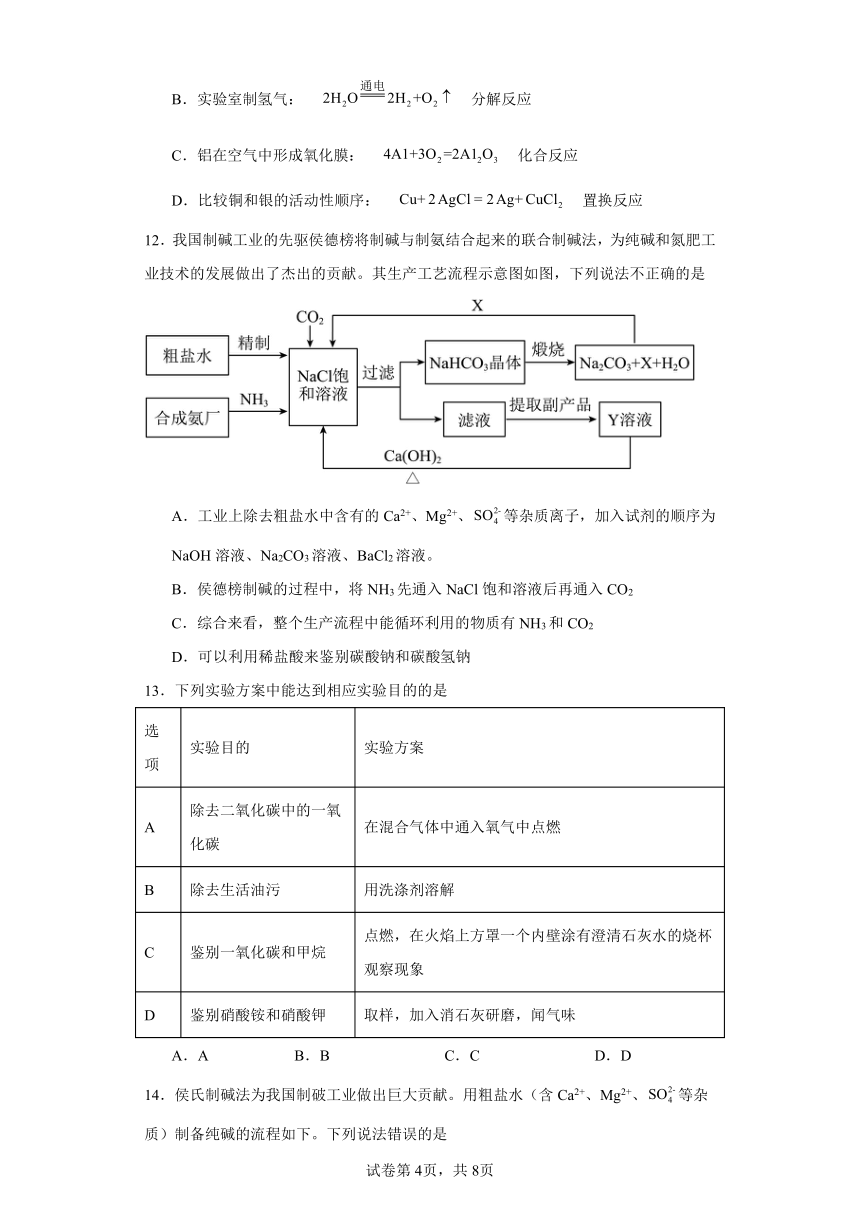
12.我国制碱工业的先驱侯德榜将制碱与制氨结合起来的联合制碱法,为纯碱和氮肥工业技术的发展做出了杰出的贡献。其生产工艺流程示意图如图,下列说法不正确的是
A.工业上除去粗盐水中含有的Ca2+、Mg2+、等杂质离子,加入试剂的顺序为NaOH溶液、Na2CO3溶液、BaCl2溶液。
B.侯德榜制碱的过程中,将NH3先通入NaCl饱和溶液后再通入CO2
C.综合来看,整个生产流程中能循环利用的物质有NH3和CO2
D.可以利用稀盐酸来鉴别碳酸钠和碳酸氢钠
13.下列实验方案中能达到相应实验目的的是
选项 实验目的 实验方案
A 除去二氧化碳中的一氧化碳 在混合气体中通入氧气中点燃
B 除去生活油污 用洗涤剂溶解
C 鉴别一氧化碳和甲烷 点燃,在火焰上方罩一个内壁涂有澄清石灰水的烧杯观察现象
D 鉴别硝酸铵和硝酸钾 取样,加入消石灰研磨,闻气味
A.A B.B C.C D.D
14.侯氏制碱法为我国制破工业做出巨大贡献。用粗盐水(含Ca2+、Mg2+、等杂质)制备纯碱的流程如下。下列说法错误的是
A.“精制” 除杂添加试剂的顺序为NaOH、Na2CO3、BaCl2
B.X为CO2,Y为NH3
C.相同条件下,溶解度:Na2CO3> NaHCO3,热稳定性:Na2CO3> NaHCO3
D.可以从母液中获取氮肥
二、非选择题
15.从玫瑰花瓣中提取的花青素(紫色)可制成酸碱指示剂,滴入到不同溶液中,颜色变化如下表,结合表中信息回答:
试剂 NaCl溶液 盐酸 溶液 溶液 NaOH溶液
颜色 紫 红 蓝 红 蓝
(1)溶液呈 (填“酸性”“碱性”或“中性”),用作化肥长期施用的结果是 ;
(2)向某无色溶液中滴入花青素,溶液变蓝色,则此溶液中一定不存在、、、、、离子中的 (填离子符号)。
16.我国冶炼金属的历史悠久,请根据所学知识回答下列问题。
(1)后母戊鼎是由青铜制作,青铜属于 (填“金属”或“合金”)。
(2)人类大规模使用金属的先后顺序跟 (填字母)关系最大。
a.地壳中金属元素的含量 b.金属的导电性 c.金属的活动性
(3)我国在春秋时期就开始了铁的冶炼,汉代出现了最早的炼铁高炉。如图是铁及其化合物的“价态一类别”二维图。高炉炼铁的反应原理为反应①~⑨中的 (填序号),利用CO的 性冶炼赭石(主要成分为Fe2O3)。其化学方程式为 。
(4)反应①~⑨中,其中既属于复分解反应,又属于中和反应的为 (填序号)。
(5)钛和钛合金是21世纪的重要的金属材料。工业上冶炼金属钛的原理是:在氩气环境和高温条件下,利用金属镁和TiCl4,反应生成氯化镁和金属钛,该反应的方程式为 。氩气作为保护气防止生成的金属钛被氧化,是因为氩气的化学性质 。
17.水是生命之源,也是我们化学实验室最常用的物质。
(1)水是一种重要的化学物质。
①下列有关水的说法正确的是 (填字母)。
A.过滤可以降低水的硬度
B.大量开采地下水可缓解水资源短缺
C.农业上以喷灌或滴灌的形式浇灌可节约用水
②下列各组固体物质能用水区分的是 (填字母)。
A.碳酸钙和碳酸钠 B.氯化钾和氯化钙 C.硝酸铵和氯化钠
③高铁酸钾(K2FeO4)是一种新型高效水处理消毒剂,高铁酸钾与水反应的化学方程式为:。请写出X的化学式 。
④用溶质质量分数为24%的氯化钠溶液和蒸馏水来配制300g溶质质量分数为16%的氯化钠溶液来选种,则需要蒸馏水的质量为 g。
(2)初中化学实验中经常用到水。
实验①采用排水法收集氧气,氧气从 端进入(填“a”或“b”):实验②集气瓶中的水换成烧碱溶液,也可以达到实验效果,这是因为 (用化学方程式表示)。实验③中根据 (填现象),说明铁生锈需要水。
18.我国对全世界宣布“碳中和”目标,彰显了大国的责任和担当。
(1)目前,人们使用的燃料大多来自化石燃料,化石燃料的大量使用,使大气中二氧化碳的含量持续上升,由此引发的环境问题是 。
(2)“碳中和”是指人为排放二氧化碳量与通过植树造林和人为碳捕集技术吸收二氧化碳量达到平衡。对于自然界中消耗二氧化碳的主要途径是 (写一条)。
(3)开发和利用新能源,有利于生态环境保护。氢氧燃料电池已得到广泛应用,在这种电池中,利用氢气作为能源的最大优点是 ;写出该反应的化学方程式 。
(4)化学家侯德榜在氨碱法的基础上创立“侯氏制碱法”,向滤出NaHCO3晶体后的NH4Cl溶液中加入NaCl粉末,析出NH4Cl。NH4Cl和NaCl两种物质的溶解度曲线如图所示。
①t1℃时,NH4Cl的溶解度 NaCl的溶解度。(填“大于”“等于”“小于”之一)
②t2℃时,NH4Cl的溶解度是 g。
③t2℃时,把50gNH4Cl加入100g水中,充分溶解,所得溶液的质量为 ,此溶液为 溶液(填“饱和”或“不饱和”之一)
④通过NaCl的溶解度曲线,可判断出海水“晒盐”是用 (填“蒸发结晶”“降温结晶”之一)的方法从海水中得到NaCl。
19.2023年春晚《满庭芳 国色》节目点燃了国人复古寻色的热潮。其中桃红、凝脂、湘叶、群青、沉香代表红、白、黄、青、黑传统五色。
(1)桃红:用银朱调合,银朱是硫黄与汞加热制成的硫化汞(HgS),反应过程中硫元素的化合价 (填“升高”、“降低”或“不变”)。
(2)群青:与石青颜色接近,石青的主要成分是Cu3(OH)2(CO3)2,将少量石青加入足量稀盐酸中,推测发生反应的现象为 。
拓展延伸:图2是硫酸氢钠在水中解离的微观示意图,向该溶液中滴加
(填化学式)溶液既能降低该溶液的酸性又能生成沉淀。
(3)凝脂:降低原料中含铁氧化物含量,实现从青瓷到凝脂似玉的白瓷。如图3为铁元素的价类二维图。
①a点表示物质的类别是 。
②“湘叶”代表黄色,图中代表的物质溶液呈黄色的是 (填字母);“沉香”代表黑色,e点代表的物质呈黑色,其化学式是 。
③b→a为工业炼铁原理,其化学方程式 。
④下列转化关系可以通过置换反应实现的是 (填字母)。
A.a→f B.b→d C.b→a D.d→c
试卷第2页,共2页
试卷第1页,共1页
参考答案:
1.B
2.C
3.C
4.C
5.D
6.D
7.C
8.B
9.B
10.A
11.C
12.A
13.D
14.A
15.(1) 酸性 使土壤酸化、板结
(2)、
16.(1)合金
(2)c
(3) ① 还原
(4)⑥⑧
(5)
稳定
17.(1) C AC/CA O2 100
(2) b A生锈C不生锈
18.(1)温室效应增强
(2)绿色植物的光合作用
(3) 燃烧产物为水,不污染环境
(4) 等于 48 148g 饱和 蒸发结晶
19.(1)降低
(2) 固体溶解,有气泡产生,溶液由无色变为蓝色 Ba(OH)2
(3) 单质 d FeO
AC/CA
答案第1页,共2页
答案第1页,共2页
一、单选题
1.有一包均匀混合的Na2CO3和NaHCO3的固体粉末,为了测定其组成,小董同学称取不同质量的粉末样品溶于水,然后分别滴加相同浓度的稀盐酸100g,充分反应后记录生成CO2的质量与所取的混合固体质量关系如图所示。已知,向该混合物溶液滴加稀盐酸时,发生的化学反应分两步进行。第一步反应:。第二步反应:。根据图中信息,下列说法不正确的是
A.样品中碳酸钠的质量分数为55.8%
B.a点时所得溶液中的溶质为NaCl、Na2CO3、NaHCO3
C.14.25g样品中含NaHCO3的质量为6.3g
D.当固体样品质量为4.75g时,所取样品与100g稀盐酸恰好完全反应
2.甲、乙、丙均为初中化学常见的物质,它们之间相互关系如图所示(图中“—”表示相连的物质能相互反应,“→”表示一种物质可一步转化成另一种物质)。由此得出以下结论:
①甲、乙、丙必须含同种元素。
②图中所示关系均可通过置换反应实现。
③甲若是碱,丙只能是盐。
④丙若是氧化物,甲可以是单质或氧化物。
⑤甲、乙、丙可以是同一类别的物质(物质类别是指单质、氧化物、酸、碱、盐)。
其中正确的结论有
A.4个 B.3个 C.2个 D.1个
3.向一定质量和的混合溶液中逐滴加入溶质质量分数为10.0%的溶液。反应过程中加入的溶液的质量与产生沉淀或气体的质量关系如图所示,说法正确的是
A.图中段表示生成沉淀的过程 B.b点溶液中溶质有2种
C.x值为106.0 D.c点溶液的
4.实验室有四个药品橱,已存放如表药品,现新购进的纯碱,应将它存放在
药品橱 甲橱 乙橱 丙橱 丁橱
药品 盐酸 氢氧化钠 氯化钠 铜
A.甲橱 B.乙橱 C.丙橱 D.丁橱
5.实验室有失去标签的两瓶溶液,只知道二者为稀盐酸和稀硫酸,为区分哪个为稀盐酸,哪个为稀硫酸,请你选择一种药品将二者区分开
A.铁丝 B.氧化铜粉末 C.碳酸钠溶液 D.氯化钡溶液
6.工业上电解食盐(NaCl)溶液制取氢氧化钠(NaOH):。下列说法中不正确的是
A.NaCl可由海水蒸发、精制获得
B.点燃或加热H2前一定要检验其纯度
C.氯气(Cl2)可用于自来水生产中杀菌消毒
D.氢氧化钠易潮解,有腐蚀性,可直接在纸上称量
7.下列对实验现象的描述或实验操作正确的是
A.红磷在空气燃烧,生成五氧化二磷
B.电解水实验时,负极和正极产生气体的质量比为2:1
C.“铜绿”与盐酸混合,得到蓝绿色溶液
D.为加快过滤的速度,用玻璃棒在漏斗内不断搅拌
8.学习小组通过下列实验探究溶液的性质。
实验Ⅰ:把一根砂纸打磨过的Al丝浸入溶液中,一段时间后观察到Al丝表面出现红色物质。
实验Ⅱ:向溶液中滴加少量NaOH溶液,出现沉淀。
下列说法正确的是
A.实验Ⅰ中溶液颜色不变 B.实验Ⅰ说明Al的活动性比Cu的强
C.实验Ⅱ中只发生物理变化 D.实验Ⅱ中沉淀为CuO
9.下列实验操作或方法不能达到实验目的的是
选项 实验目的 实验操作或方法
A 除去氮气中混有的少量氧气 将气体通过灼热的铜网
B 除去KCl溶液中混有的少量CuCl2 加入氢氧化钠溶液至不再产生沉淀,过滤
C 鉴别过氧化氢溶液和水 取样,分别加入二氧化锰,观察是否产生气泡
D 鉴别化肥硫酸钾和硫酸铵 取样,分别加入熟石灰粉末混合研磨,闻气味
A.A B.B C.C D.D
10.除去下列物质中的杂质,所选用的试剂和操作方法都正确的
选项 物质 杂质 试剂 操作方法
A 铜 铁 过量的稀盐酸 溶解、过滤、洗涤、干燥
B 氯化铜溶液 氯化锌溶液 过量的锌 溶解、过滤
C 硫酸铜 铁 足量水 溶解、过滤、蒸发、结晶
D 生石灰 石灰石 无 高温煅烧
A.A B.B C.C D.D
11.下列叙述、对应的化学方程式、所属基本反应类型都正确的是
A.用稀硫酸洗去附着在试管壁上的铜: 置换反应
B.实验室制氢气: 分解反应
C.铝在空气中形成氧化膜: 化合反应
D.比较铜和银的活动性顺序: 置换反应
12.我国制碱工业的先驱侯德榜将制碱与制氨结合起来的联合制碱法,为纯碱和氮肥工业技术的发展做出了杰出的贡献。其生产工艺流程示意图如图,下列说法不正确的是
A.工业上除去粗盐水中含有的Ca2+、Mg2+、等杂质离子,加入试剂的顺序为NaOH溶液、Na2CO3溶液、BaCl2溶液。
B.侯德榜制碱的过程中,将NH3先通入NaCl饱和溶液后再通入CO2
C.综合来看,整个生产流程中能循环利用的物质有NH3和CO2
D.可以利用稀盐酸来鉴别碳酸钠和碳酸氢钠
13.下列实验方案中能达到相应实验目的的是
选项 实验目的 实验方案
A 除去二氧化碳中的一氧化碳 在混合气体中通入氧气中点燃
B 除去生活油污 用洗涤剂溶解
C 鉴别一氧化碳和甲烷 点燃,在火焰上方罩一个内壁涂有澄清石灰水的烧杯观察现象
D 鉴别硝酸铵和硝酸钾 取样,加入消石灰研磨,闻气味
A.A B.B C.C D.D
14.侯氏制碱法为我国制破工业做出巨大贡献。用粗盐水(含Ca2+、Mg2+、等杂质)制备纯碱的流程如下。下列说法错误的是
A.“精制” 除杂添加试剂的顺序为NaOH、Na2CO3、BaCl2
B.X为CO2,Y为NH3
C.相同条件下,溶解度:Na2CO3> NaHCO3,热稳定性:Na2CO3> NaHCO3
D.可以从母液中获取氮肥
二、非选择题
15.从玫瑰花瓣中提取的花青素(紫色)可制成酸碱指示剂,滴入到不同溶液中,颜色变化如下表,结合表中信息回答:
试剂 NaCl溶液 盐酸 溶液 溶液 NaOH溶液
颜色 紫 红 蓝 红 蓝
(1)溶液呈 (填“酸性”“碱性”或“中性”),用作化肥长期施用的结果是 ;
(2)向某无色溶液中滴入花青素,溶液变蓝色,则此溶液中一定不存在、、、、、离子中的 (填离子符号)。
16.我国冶炼金属的历史悠久,请根据所学知识回答下列问题。
(1)后母戊鼎是由青铜制作,青铜属于 (填“金属”或“合金”)。
(2)人类大规模使用金属的先后顺序跟 (填字母)关系最大。
a.地壳中金属元素的含量 b.金属的导电性 c.金属的活动性
(3)我国在春秋时期就开始了铁的冶炼,汉代出现了最早的炼铁高炉。如图是铁及其化合物的“价态一类别”二维图。高炉炼铁的反应原理为反应①~⑨中的 (填序号),利用CO的 性冶炼赭石(主要成分为Fe2O3)。其化学方程式为 。
(4)反应①~⑨中,其中既属于复分解反应,又属于中和反应的为 (填序号)。
(5)钛和钛合金是21世纪的重要的金属材料。工业上冶炼金属钛的原理是:在氩气环境和高温条件下,利用金属镁和TiCl4,反应生成氯化镁和金属钛,该反应的方程式为 。氩气作为保护气防止生成的金属钛被氧化,是因为氩气的化学性质 。
17.水是生命之源,也是我们化学实验室最常用的物质。
(1)水是一种重要的化学物质。
①下列有关水的说法正确的是 (填字母)。
A.过滤可以降低水的硬度
B.大量开采地下水可缓解水资源短缺
C.农业上以喷灌或滴灌的形式浇灌可节约用水
②下列各组固体物质能用水区分的是 (填字母)。
A.碳酸钙和碳酸钠 B.氯化钾和氯化钙 C.硝酸铵和氯化钠
③高铁酸钾(K2FeO4)是一种新型高效水处理消毒剂,高铁酸钾与水反应的化学方程式为:。请写出X的化学式 。
④用溶质质量分数为24%的氯化钠溶液和蒸馏水来配制300g溶质质量分数为16%的氯化钠溶液来选种,则需要蒸馏水的质量为 g。
(2)初中化学实验中经常用到水。
实验①采用排水法收集氧气,氧气从 端进入(填“a”或“b”):实验②集气瓶中的水换成烧碱溶液,也可以达到实验效果,这是因为 (用化学方程式表示)。实验③中根据 (填现象),说明铁生锈需要水。
18.我国对全世界宣布“碳中和”目标,彰显了大国的责任和担当。
(1)目前,人们使用的燃料大多来自化石燃料,化石燃料的大量使用,使大气中二氧化碳的含量持续上升,由此引发的环境问题是 。
(2)“碳中和”是指人为排放二氧化碳量与通过植树造林和人为碳捕集技术吸收二氧化碳量达到平衡。对于自然界中消耗二氧化碳的主要途径是 (写一条)。
(3)开发和利用新能源,有利于生态环境保护。氢氧燃料电池已得到广泛应用,在这种电池中,利用氢气作为能源的最大优点是 ;写出该反应的化学方程式 。
(4)化学家侯德榜在氨碱法的基础上创立“侯氏制碱法”,向滤出NaHCO3晶体后的NH4Cl溶液中加入NaCl粉末,析出NH4Cl。NH4Cl和NaCl两种物质的溶解度曲线如图所示。
①t1℃时,NH4Cl的溶解度 NaCl的溶解度。(填“大于”“等于”“小于”之一)
②t2℃时,NH4Cl的溶解度是 g。
③t2℃时,把50gNH4Cl加入100g水中,充分溶解,所得溶液的质量为 ,此溶液为 溶液(填“饱和”或“不饱和”之一)
④通过NaCl的溶解度曲线,可判断出海水“晒盐”是用 (填“蒸发结晶”“降温结晶”之一)的方法从海水中得到NaCl。
19.2023年春晚《满庭芳 国色》节目点燃了国人复古寻色的热潮。其中桃红、凝脂、湘叶、群青、沉香代表红、白、黄、青、黑传统五色。
(1)桃红:用银朱调合,银朱是硫黄与汞加热制成的硫化汞(HgS),反应过程中硫元素的化合价 (填“升高”、“降低”或“不变”)。
(2)群青:与石青颜色接近,石青的主要成分是Cu3(OH)2(CO3)2,将少量石青加入足量稀盐酸中,推测发生反应的现象为 。
拓展延伸:图2是硫酸氢钠在水中解离的微观示意图,向该溶液中滴加
(填化学式)溶液既能降低该溶液的酸性又能生成沉淀。
(3)凝脂:降低原料中含铁氧化物含量,实现从青瓷到凝脂似玉的白瓷。如图3为铁元素的价类二维图。
①a点表示物质的类别是 。
②“湘叶”代表黄色,图中代表的物质溶液呈黄色的是 (填字母);“沉香”代表黑色,e点代表的物质呈黑色,其化学式是 。
③b→a为工业炼铁原理,其化学方程式 。
④下列转化关系可以通过置换反应实现的是 (填字母)。
A.a→f B.b→d C.b→a D.d→c
试卷第2页,共2页
试卷第1页,共1页
参考答案:
1.B
2.C
3.C
4.C
5.D
6.D
7.C
8.B
9.B
10.A
11.C
12.A
13.D
14.A
15.(1) 酸性 使土壤酸化、板结
(2)、
16.(1)合金
(2)c
(3) ① 还原
(4)⑥⑧
(5)
稳定
17.(1) C AC/CA O2 100
(2) b A生锈C不生锈
18.(1)温室效应增强
(2)绿色植物的光合作用
(3) 燃烧产物为水,不污染环境
(4) 等于 48 148g 饱和 蒸发结晶
19.(1)降低
(2) 固体溶解,有气泡产生,溶液由无色变为蓝色 Ba(OH)2
(3) 单质 d FeO
AC/CA
答案第1页,共2页
答案第1页,共2页
同课章节目录
