2024年高考化学选择题突破2:化学物质及其变化、阿伏加德罗常数的判断(含解析)
文档属性
| 名称 | 2024年高考化学选择题突破2:化学物质及其变化、阿伏加德罗常数的判断(含解析) |  | |
| 格式 | docx | ||
| 文件大小 | 344.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-12-28 22:41:43 | ||
图片预览



文档简介
选择题突破2 化学物质及其变化、阿伏加德罗常数的判断
【真题回顾】
命题角度1 化学物质及其变化
1.(2023·浙江1月选考)下列物质中属于耐高温酸性氧化物的是( )
A.CO2 B.SiO2
C.MgO D.Na2O
2.(2022·福建卷)福建多个科研机构经过长期联合研究发现,使用C60和改性的Cu基催化剂,可打通从合成气经草酸二甲酯常压催化加氢制备乙二醇的技术难关。下列说法正确的是( )
A.草酸属于无机物
B.C60与石墨互为同分异构体
C.Cu属于过渡元素
D.催化剂通过降低焓变加快反应速率
3.(2022·湖北卷)化学与生活密切相关,下列不涉及化学变化的是( )
A.加入明矾后泥水变澄清
B.北京冬奥会用水快速制冰
C.炖排骨汤时加点醋味道更鲜
D.切开的茄子放置后切面变色
命题角度2 阿伏加德罗常数的判断
4.(2023·全国甲卷)NA为阿伏加德罗常数的值。下列叙述正确的是( )
A.0.50 mol异丁烷分子中共价键的数目为6.5NA
B.标准状况下,2.24 L SO3中电子的数目为4.00NA
C.1.0 L pH=2的H2SO4溶液中H+的数目为0.02NA
D.1.0 L 1.0 mol·L-1的Na2CO3溶液中CO的数目为1.0NA
5.(2023·辽宁卷)我国古代四大发明之一黑火药的爆炸反应为:S+2KNO3+3C===K2S+N2↑+3CO2↑。设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.11.2 L CO2含π键数目为NA
B.每生成2.8 g N2转移电子数目为NA
C.0.1 mol KNO3晶体中含离子数目为0.2NA
D.1 L 0.1 mol·L-1 K2S溶液中含S2-数目为0.1NA
6.(2023·浙江6月选考)NA为阿伏加德罗常数的值,下列说法正确的是( )
A.4.4 g C2H4O中含有σ键数目最多为0.7NA
B.1.7 g H2O2中含有氧原子数为0.2NA
C.向1 L 0.1 mol/L CH3COOH溶液通氨气至中性,铵根离子数为0.1NA
D.标准状况下,11.2 L Cl2通入水中,溶液中氯离子数为0.5NA
【考点剖析】
微点1 化学物质及其变化
【典题精练】
1.(2023·衡水重点中学二模)中华文化博大精深、源远流长。下列文物主要是由金属材料制成的是( )
A.蚕丝琴弦 B.釉瓷棋子 C.猪鬃毛笔 D.宣纸画卷
2.(2022·浙江1月选考)下列物质对应的化学式不正确的是( )
A.氯仿:CHCl3 B.黄铜矿的主要成分:Cu2S
C.芒硝:Na2SO4·10H2O D.铝土矿的主要成分:Al2O3
3.(2023·德州模拟)下列物质分类正确的是( )
A.SO2、SiO2、NO2均为酸性氧化物
B.稀豆浆、硅酸、氯化铁溶液均为胶体
C.漂白粉、水玻璃、氨水均为混合物
D.Na2O2、Al2O3、Fe3O4均为碱性氧化物
【智能提升】
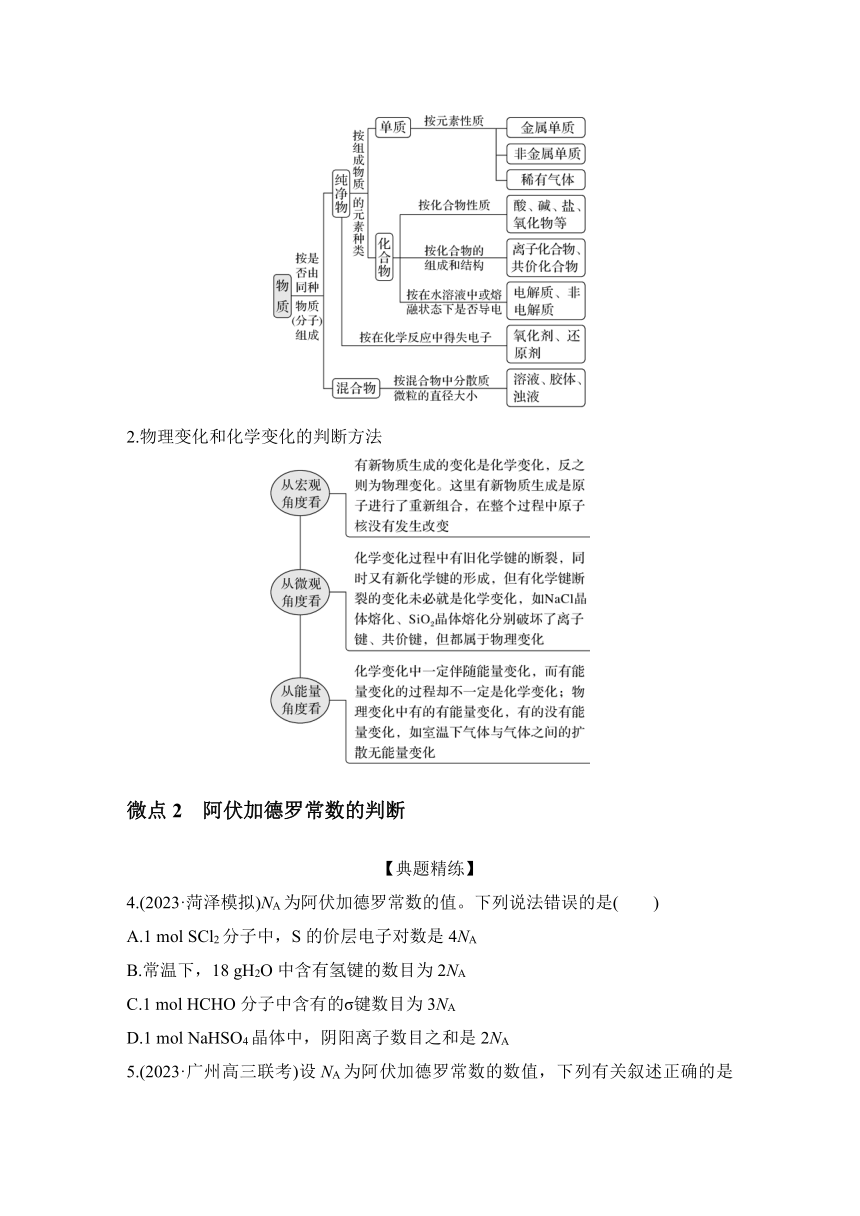
1.依据“标准”对物质进行分类
2.物理变化和化学变化的判断方法
微点2 阿伏加德罗常数的判断
【典题精练】
4.(2023·菏泽模拟)NA为阿伏加德罗常数的值。下列说法错误的是( )
A.1 mol SCl2分子中,S的价层电子对数是4NA
B.常温下,18 gH2O中含有氢键的数目为2NA
C.1 mol HCHO分子中含有的σ键数目为3NA
D.1 mol NaHSO4晶体中,阴阳离子数目之和是2NA
5.(2023·广州高三联考)设NA为阿伏加德罗常数的数值,下列有关叙述正确的是( )
A.25 ℃时,1 L pH=1的H2SO4溶液中含有的H+数为0.1NA
B.1 mol白磷(P4)分子中所含非极性共价键数为4NA
C.1 mol CH3COOC2H5在稀硫酸溶液中水解可得到乙醇分子数为NA
D.1.8 gH2O与CH2D2的混合物中所含中子数为NA
6.(2023·武汉调研)工业上制备高纯硅及反应SiHCl3+H2Si+3HCl。NA为阿伏加德罗常数的值。下列说法正确的是( )
A.2 g H2完全反应时转移的电子数为4NA
B.1 mol单晶硅中Si—Si键的数目为4NA
C.pH=1的HCl溶液中H+的数目为0.1NA
D.标准状况下,2.24 L SiHCl3的分子数为0.1NA
【智能提升】
1.阿伏加德罗常数常考陷阱总结
(1)忽视气体摩尔体积的适用条件、忽视物质的聚集状态。
如:标准状况下CCl4、CHCl3、CH2Cl2、苯、汽油、环己烷、SO3、NO2、HF不是气体。
(2)忽视原子结构中核素的计算关系。
如:D2O的中子数是10,NH的电子数是10,He是单原子分子等。
(3)没有正确理解物质的组成和微观结构。
如:NaCl是离子构成的,HCl是分子构成的。
(4)错记特殊物质中的化学键数目。
如:苯中无双键,1 mol金刚石中有2 mol C—C,1 mol SiO2中有4 mol Si—O。
(5)混淆某些氧化还原反应中电子转移的数目。Fe、Cu与氯气反应生成FeCl3、CuCl2,与硫反应生成FeS、Cu2S。Na2O2与H2O、CO2的反应是歧化反应,1 mol Na2O2反应转移1 mol电子。
(6)忽视可逆反应
常见的可逆反应有N2+H2、SO2+O2、H2+I2、NO2与N2O4的转化、PCl3+Cl2、Fe3++I-、Cl2+H2O、酯化反应等。
(7)忽视电解质溶液中因微粒的电离或水解造成微粒数目的变化。
常见的弱酸有CH3COOH、H2CO3、HClO、HF、H2S、H2SO3等。
易水解的离子有NH、Fe3+、CH3COO-、CO、ClO-、F-、SO等。
(8)忽视胶体粒子的组成。
胶体粒子是胶团,如1 mol FeCl3水解形成的Fe(OH)3胶体粒子数小于NA。
(9)忽视溶液的体积及溶剂水中的氧原子或氢原子。
2.混合物中微粒数目的计算技巧——求同存异
举例 判断正误 注意事项
①28 g乙烯和环丁烷(C4H8)的混合气体中含有的碳原子数为2NA √ a.注意整体和部分的关系; b.不同物质找相同,如:①②③的相同部分为最简式,分别为“CH2”“NO2”“O”;④中前者的相对分子质量为后者的2倍,铜原子数也为后者的2倍;⑤每摩尔物质中都含两摩尔“O”;⑥虽然都是水,但二者的相对分子质量不同,每个分子中所含中子数也不相同
②常温常压下,92 g NO2和N2O4的混合气体中含有的原子数为6NA √
③16 g O2和O3的混合气体中含有的O原子数为NA √
④8.0 g Cu2S和CuO的混合物中含有铜原子数为0.1NA √
⑤1 mol CO2和SO2的混合气体中含有的氧原子数为2NA √
⑥18 g H2O、D2O组成的物质中含有的质子数为10NA ×
参考答案
真题回顾
1.B [A项,二氧化碳和碱反应生成盐和水,是酸性氧化物,但为分子晶体,不耐高温,A错误;B项,SiO2能跟碱反应生成盐和水,所以是酸性氧化物,为共价晶体,耐高温,B正确;C项,MgO能跟酸反应生成盐和水,所以是碱性氧化物,C错误;D项,Na2O能跟酸反应生成盐和水,所以是碱性氧化物,D错误;故选B。]
2.C [A.草酸属于二元弱酸,即乙二酸,属于有机物,A错误;B.C60与石墨是碳元素的不同单质,互为同素异形体,B错误;C.Cu为ⅠB族,属于过渡元素,C正确;D.催化剂通过降低反应的活化能加快反应速率,反应焓变不变,D错误。]
3.B [明矾净水的原理为:Al3++3H2O??Al(OH)3+3H+,Al(OH)3胶体具有吸附性,可以使泥水变澄清,涉及化学变化,A错误;水和冰的分子式都是H2O,水快速制冰为物理变化,B正确;炖排骨汤时放点醋,可使骨头中的钙、磷、铁等矿物质溶解出来,营养值更价高。此外,醋还可以防止食物中的维生素被破坏,涉及化学变化,C错误;茄子中存在一类叫“酚氧化酶”的物质,它见到氧气之后,发生化学反应产生一些有色的物质。反应时间越长,颜色越深,D错误。]
4.A [A.异丁烷的结构式为,1 mol异丁烷分子含有13NA共价键,所以0.50 mol异丁烷分子中共价键的数目为6.5NA,A正确;B.在标准状况下SO3为固态,不能计算出2.24 L SO3物质的量,故无法求出其电子数目,B错误;C.pH=2的硫酸溶液中氢离子浓度为c(H+)=0.01 mol/L,则1.0 L pH=2的硫酸溶液中氢离子数目为0.01NA,C错误;D.Na2CO3属于强碱弱酸盐,在水溶液中CO会发生水解,所以1.0 L 1.0 mol/L的Na2CO3溶液中CO的数目小于1.0NA,D错误。]
5.C [A.CO2分子含有2个π键,题中没有说是标况条件下,气体摩尔体积未知,无法计算π键个数,A项错误;B.2.8 g N2的物质的量n== mol=0.1 mol,生成1 mol N2转移的电子数为12NA,则生成0.1 mol N2转移的电子数为1.2NA,B项错误;C.0.1 mol KNO3晶体含有离子为K+、NO,含有离子数目为0.2NA,C项正确;D.因为S2-水解使溶液中S2-的数目小于0.1NA,D项错误。]
6.A [A.1个C2H4O中含有6个σ键和1个π键(乙醛)或7个σ键(环氧乙烷),4.4 g C2H4O的物质的量为0.1 mol,则含有σ键数目最多为0.7NA,A正确;B.1.7 g H2O2的物质的量为=0.05 mol,则含有氧原子数为0.1NA,B不正确;C.向1 L 0.1 mol/L CH3COOH溶液通氨气至中性,溶液中存在电荷守恒关系:c(CH3COO-)+c(OH-)=c(NH)+c(H+),中性溶液c(OH-)=c(H+),则c(CH3COO-)=c(NH),再根据物料守恒:n(CH3COO-)+n(CH3COOH)=0.1 mol,得出铵根离子数小于0.1NA,C不正确;D.标准状况下,11.2 L Cl2的物质的量为0.5 mol,通入水中后只有一部分Cl2与水反应生成H+、Cl-和HClO,所以溶液中氯离子数不一定为0.5NA,D不正确。]
考点剖析
微点1
典题精练
1.A [磁州窑白底黑花瓶的主要成分是硅酸盐,属于无机物,B项不符合题意;象牙雕饰的主要成分是有机物,C项不符合题意;云锦龙袍的主要成分是丝绸织物,属于有机物,D项不符合题意。]
2.B [A项,氯仿是三氯甲烷的俗称,其化学式为CHCl3,故A正确;B项,黄铜矿的主要成分:CuFeS2,故B错误;C项,芒硝:Na2SO4·10H2O,故C正确;D项,铝土矿的主要成分:Al2O3,故D正确。]
3.C [二氧化氮与水反应生成硝酸和一氧化氮,不属于酸性氧化物,故A错误;硅酸属于纯净物,不是胶体,氯化铁溶液不是胶体,故B错误;Na2O2为过氧化物,Fe3O4不是碱性氧化物,Al2O3属于两性氧化物,故D错误。]
微点2
典题精练
4.B [A.一个SCl2分子中,S的孤电子对数是×(6-2×1)=2,硫氯单键是2,价层电子对数是4,所以1 mol SCl2分子中,S的价层电子对数是4NA,A正确;B.常温下,18 g H2O因是液态所以含有氢键的数目小于2NA,B错误;C.HCHO分子结构为,一个分子有3个σ键、1个π键,1 mol HCHO分子中含有的σ键数目为3NA,C正确;D.硫酸氢钠固体中存在钠离子和硫酸氢根离子,所以1 mol NaHSO4晶体中,阴阳离子数目之和是2NA,D正确。]
5.A [A.pH=1的硫酸溶液中氢离子浓度为0.1 mol/L,体积1 L,则含有的H+数为0.1NA,故A正确;B.P4分子为正四面体结构,1 mol白磷(P4)分子中所含非极性共价键数为6NA,故B错误;C.酯的水解为可逆反应,1 mol CH3COOC2H5水解生成的乙醇分子数小于NA,故C错误;D.1个H2O和1个CH2D2中均含8个中子,H2O和CH2D2的摩尔质量为18 g/mol,则1.8 g混合物为0.1 mol,含中子数为0.8NA,故D错误。]
6.A [2 g H2为1 mol,该反应中Si元素由+4价变为0价,故转移电子数为4NA,A项正确;单晶硅中1个Si原子形成4个Si—Si键,每个Si—Si键被2个Si原子共用,故1 mol单晶硅中Si—Si键的数目为2NA,B项错误;没有提供溶液体积,H+数目无法计算,C项错误;标准状况下SiHCl3为液体,2.24 L SiHCl3不为0.1 mol,所含分子数不为0.1NA,D项错误
【真题回顾】
命题角度1 化学物质及其变化
1.(2023·浙江1月选考)下列物质中属于耐高温酸性氧化物的是( )
A.CO2 B.SiO2
C.MgO D.Na2O
2.(2022·福建卷)福建多个科研机构经过长期联合研究发现,使用C60和改性的Cu基催化剂,可打通从合成气经草酸二甲酯常压催化加氢制备乙二醇的技术难关。下列说法正确的是( )
A.草酸属于无机物
B.C60与石墨互为同分异构体
C.Cu属于过渡元素
D.催化剂通过降低焓变加快反应速率
3.(2022·湖北卷)化学与生活密切相关,下列不涉及化学变化的是( )
A.加入明矾后泥水变澄清
B.北京冬奥会用水快速制冰
C.炖排骨汤时加点醋味道更鲜
D.切开的茄子放置后切面变色
命题角度2 阿伏加德罗常数的判断
4.(2023·全国甲卷)NA为阿伏加德罗常数的值。下列叙述正确的是( )
A.0.50 mol异丁烷分子中共价键的数目为6.5NA
B.标准状况下,2.24 L SO3中电子的数目为4.00NA
C.1.0 L pH=2的H2SO4溶液中H+的数目为0.02NA
D.1.0 L 1.0 mol·L-1的Na2CO3溶液中CO的数目为1.0NA
5.(2023·辽宁卷)我国古代四大发明之一黑火药的爆炸反应为:S+2KNO3+3C===K2S+N2↑+3CO2↑。设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.11.2 L CO2含π键数目为NA
B.每生成2.8 g N2转移电子数目为NA
C.0.1 mol KNO3晶体中含离子数目为0.2NA
D.1 L 0.1 mol·L-1 K2S溶液中含S2-数目为0.1NA
6.(2023·浙江6月选考)NA为阿伏加德罗常数的值,下列说法正确的是( )
A.4.4 g C2H4O中含有σ键数目最多为0.7NA
B.1.7 g H2O2中含有氧原子数为0.2NA
C.向1 L 0.1 mol/L CH3COOH溶液通氨气至中性,铵根离子数为0.1NA
D.标准状况下,11.2 L Cl2通入水中,溶液中氯离子数为0.5NA
【考点剖析】
微点1 化学物质及其变化
【典题精练】
1.(2023·衡水重点中学二模)中华文化博大精深、源远流长。下列文物主要是由金属材料制成的是( )
A.蚕丝琴弦 B.釉瓷棋子 C.猪鬃毛笔 D.宣纸画卷
2.(2022·浙江1月选考)下列物质对应的化学式不正确的是( )
A.氯仿:CHCl3 B.黄铜矿的主要成分:Cu2S
C.芒硝:Na2SO4·10H2O D.铝土矿的主要成分:Al2O3
3.(2023·德州模拟)下列物质分类正确的是( )
A.SO2、SiO2、NO2均为酸性氧化物
B.稀豆浆、硅酸、氯化铁溶液均为胶体
C.漂白粉、水玻璃、氨水均为混合物
D.Na2O2、Al2O3、Fe3O4均为碱性氧化物
【智能提升】
1.依据“标准”对物质进行分类
2.物理变化和化学变化的判断方法
微点2 阿伏加德罗常数的判断
【典题精练】
4.(2023·菏泽模拟)NA为阿伏加德罗常数的值。下列说法错误的是( )
A.1 mol SCl2分子中,S的价层电子对数是4NA
B.常温下,18 gH2O中含有氢键的数目为2NA
C.1 mol HCHO分子中含有的σ键数目为3NA
D.1 mol NaHSO4晶体中,阴阳离子数目之和是2NA
5.(2023·广州高三联考)设NA为阿伏加德罗常数的数值,下列有关叙述正确的是( )
A.25 ℃时,1 L pH=1的H2SO4溶液中含有的H+数为0.1NA
B.1 mol白磷(P4)分子中所含非极性共价键数为4NA
C.1 mol CH3COOC2H5在稀硫酸溶液中水解可得到乙醇分子数为NA
D.1.8 gH2O与CH2D2的混合物中所含中子数为NA
6.(2023·武汉调研)工业上制备高纯硅及反应SiHCl3+H2Si+3HCl。NA为阿伏加德罗常数的值。下列说法正确的是( )
A.2 g H2完全反应时转移的电子数为4NA
B.1 mol单晶硅中Si—Si键的数目为4NA
C.pH=1的HCl溶液中H+的数目为0.1NA
D.标准状况下,2.24 L SiHCl3的分子数为0.1NA
【智能提升】
1.阿伏加德罗常数常考陷阱总结
(1)忽视气体摩尔体积的适用条件、忽视物质的聚集状态。
如:标准状况下CCl4、CHCl3、CH2Cl2、苯、汽油、环己烷、SO3、NO2、HF不是气体。
(2)忽视原子结构中核素的计算关系。
如:D2O的中子数是10,NH的电子数是10,He是单原子分子等。
(3)没有正确理解物质的组成和微观结构。
如:NaCl是离子构成的,HCl是分子构成的。
(4)错记特殊物质中的化学键数目。
如:苯中无双键,1 mol金刚石中有2 mol C—C,1 mol SiO2中有4 mol Si—O。
(5)混淆某些氧化还原反应中电子转移的数目。Fe、Cu与氯气反应生成FeCl3、CuCl2,与硫反应生成FeS、Cu2S。Na2O2与H2O、CO2的反应是歧化反应,1 mol Na2O2反应转移1 mol电子。
(6)忽视可逆反应
常见的可逆反应有N2+H2、SO2+O2、H2+I2、NO2与N2O4的转化、PCl3+Cl2、Fe3++I-、Cl2+H2O、酯化反应等。
(7)忽视电解质溶液中因微粒的电离或水解造成微粒数目的变化。
常见的弱酸有CH3COOH、H2CO3、HClO、HF、H2S、H2SO3等。
易水解的离子有NH、Fe3+、CH3COO-、CO、ClO-、F-、SO等。
(8)忽视胶体粒子的组成。
胶体粒子是胶团,如1 mol FeCl3水解形成的Fe(OH)3胶体粒子数小于NA。
(9)忽视溶液的体积及溶剂水中的氧原子或氢原子。
2.混合物中微粒数目的计算技巧——求同存异
举例 判断正误 注意事项
①28 g乙烯和环丁烷(C4H8)的混合气体中含有的碳原子数为2NA √ a.注意整体和部分的关系; b.不同物质找相同,如:①②③的相同部分为最简式,分别为“CH2”“NO2”“O”;④中前者的相对分子质量为后者的2倍,铜原子数也为后者的2倍;⑤每摩尔物质中都含两摩尔“O”;⑥虽然都是水,但二者的相对分子质量不同,每个分子中所含中子数也不相同
②常温常压下,92 g NO2和N2O4的混合气体中含有的原子数为6NA √
③16 g O2和O3的混合气体中含有的O原子数为NA √
④8.0 g Cu2S和CuO的混合物中含有铜原子数为0.1NA √
⑤1 mol CO2和SO2的混合气体中含有的氧原子数为2NA √
⑥18 g H2O、D2O组成的物质中含有的质子数为10NA ×
参考答案
真题回顾
1.B [A项,二氧化碳和碱反应生成盐和水,是酸性氧化物,但为分子晶体,不耐高温,A错误;B项,SiO2能跟碱反应生成盐和水,所以是酸性氧化物,为共价晶体,耐高温,B正确;C项,MgO能跟酸反应生成盐和水,所以是碱性氧化物,C错误;D项,Na2O能跟酸反应生成盐和水,所以是碱性氧化物,D错误;故选B。]
2.C [A.草酸属于二元弱酸,即乙二酸,属于有机物,A错误;B.C60与石墨是碳元素的不同单质,互为同素异形体,B错误;C.Cu为ⅠB族,属于过渡元素,C正确;D.催化剂通过降低反应的活化能加快反应速率,反应焓变不变,D错误。]
3.B [明矾净水的原理为:Al3++3H2O??Al(OH)3+3H+,Al(OH)3胶体具有吸附性,可以使泥水变澄清,涉及化学变化,A错误;水和冰的分子式都是H2O,水快速制冰为物理变化,B正确;炖排骨汤时放点醋,可使骨头中的钙、磷、铁等矿物质溶解出来,营养值更价高。此外,醋还可以防止食物中的维生素被破坏,涉及化学变化,C错误;茄子中存在一类叫“酚氧化酶”的物质,它见到氧气之后,发生化学反应产生一些有色的物质。反应时间越长,颜色越深,D错误。]
4.A [A.异丁烷的结构式为,1 mol异丁烷分子含有13NA共价键,所以0.50 mol异丁烷分子中共价键的数目为6.5NA,A正确;B.在标准状况下SO3为固态,不能计算出2.24 L SO3物质的量,故无法求出其电子数目,B错误;C.pH=2的硫酸溶液中氢离子浓度为c(H+)=0.01 mol/L,则1.0 L pH=2的硫酸溶液中氢离子数目为0.01NA,C错误;D.Na2CO3属于强碱弱酸盐,在水溶液中CO会发生水解,所以1.0 L 1.0 mol/L的Na2CO3溶液中CO的数目小于1.0NA,D错误。]
5.C [A.CO2分子含有2个π键,题中没有说是标况条件下,气体摩尔体积未知,无法计算π键个数,A项错误;B.2.8 g N2的物质的量n== mol=0.1 mol,生成1 mol N2转移的电子数为12NA,则生成0.1 mol N2转移的电子数为1.2NA,B项错误;C.0.1 mol KNO3晶体含有离子为K+、NO,含有离子数目为0.2NA,C项正确;D.因为S2-水解使溶液中S2-的数目小于0.1NA,D项错误。]
6.A [A.1个C2H4O中含有6个σ键和1个π键(乙醛)或7个σ键(环氧乙烷),4.4 g C2H4O的物质的量为0.1 mol,则含有σ键数目最多为0.7NA,A正确;B.1.7 g H2O2的物质的量为=0.05 mol,则含有氧原子数为0.1NA,B不正确;C.向1 L 0.1 mol/L CH3COOH溶液通氨气至中性,溶液中存在电荷守恒关系:c(CH3COO-)+c(OH-)=c(NH)+c(H+),中性溶液c(OH-)=c(H+),则c(CH3COO-)=c(NH),再根据物料守恒:n(CH3COO-)+n(CH3COOH)=0.1 mol,得出铵根离子数小于0.1NA,C不正确;D.标准状况下,11.2 L Cl2的物质的量为0.5 mol,通入水中后只有一部分Cl2与水反应生成H+、Cl-和HClO,所以溶液中氯离子数不一定为0.5NA,D不正确。]
考点剖析
微点1
典题精练
1.A [磁州窑白底黑花瓶的主要成分是硅酸盐,属于无机物,B项不符合题意;象牙雕饰的主要成分是有机物,C项不符合题意;云锦龙袍的主要成分是丝绸织物,属于有机物,D项不符合题意。]
2.B [A项,氯仿是三氯甲烷的俗称,其化学式为CHCl3,故A正确;B项,黄铜矿的主要成分:CuFeS2,故B错误;C项,芒硝:Na2SO4·10H2O,故C正确;D项,铝土矿的主要成分:Al2O3,故D正确。]
3.C [二氧化氮与水反应生成硝酸和一氧化氮,不属于酸性氧化物,故A错误;硅酸属于纯净物,不是胶体,氯化铁溶液不是胶体,故B错误;Na2O2为过氧化物,Fe3O4不是碱性氧化物,Al2O3属于两性氧化物,故D错误。]
微点2
典题精练
4.B [A.一个SCl2分子中,S的孤电子对数是×(6-2×1)=2,硫氯单键是2,价层电子对数是4,所以1 mol SCl2分子中,S的价层电子对数是4NA,A正确;B.常温下,18 g H2O因是液态所以含有氢键的数目小于2NA,B错误;C.HCHO分子结构为,一个分子有3个σ键、1个π键,1 mol HCHO分子中含有的σ键数目为3NA,C正确;D.硫酸氢钠固体中存在钠离子和硫酸氢根离子,所以1 mol NaHSO4晶体中,阴阳离子数目之和是2NA,D正确。]
5.A [A.pH=1的硫酸溶液中氢离子浓度为0.1 mol/L,体积1 L,则含有的H+数为0.1NA,故A正确;B.P4分子为正四面体结构,1 mol白磷(P4)分子中所含非极性共价键数为6NA,故B错误;C.酯的水解为可逆反应,1 mol CH3COOC2H5水解生成的乙醇分子数小于NA,故C错误;D.1个H2O和1个CH2D2中均含8个中子,H2O和CH2D2的摩尔质量为18 g/mol,则1.8 g混合物为0.1 mol,含中子数为0.8NA,故D错误。]
6.A [2 g H2为1 mol,该反应中Si元素由+4价变为0价,故转移电子数为4NA,A项正确;单晶硅中1个Si原子形成4个Si—Si键,每个Si—Si键被2个Si原子共用,故1 mol单晶硅中Si—Si键的数目为2NA,B项错误;没有提供溶液体积,H+数目无法计算,C项错误;标准状况下SiHCl3为液体,2.24 L SiHCl3不为0.1 mol,所含分子数不为0.1NA,D项错误
同课章节目录
