2023—2024学年鲁教版(五四学制)化学九年级全一册第四单元 金属 期末复习(含答案)
文档属性
| 名称 | 2023—2024学年鲁教版(五四学制)化学九年级全一册第四单元 金属 期末复习(含答案) |  | |
| 格式 | doc | ||
| 文件大小 | 576.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-12-29 12:03:36 | ||
图片预览




文档简介
2023—2024学年鲁教版(五四学制)化学九年级全一册第四单元 金属 期末复习含答案
鲁教版(五四学制)第四单元 金属
一、选择题。
1、科学家发现一种新金属。根据右表信息推测其用途错误的是( )
熔点 2500℃
密度 3g/cm3
强度 与钢相似
导电性 良好
导热性 良好
抗腐蚀性 优异
A.用于焊接金属 B.制造航天飞机
C.制外科手术刀 D.用于通讯设备
2、下列实验现象描述正确的是( )
A.硫在氧气中燃烧,产生淡蓝色火焰
B.镁条在空气中燃烧,发出耀眼白光
C.铜片放入稀硫酸中,有气泡产生
D.一氧化碳还原氧化铁,固体粉末由黑色变为红色
3、下列说法中正确的是( )
A.废旧电池可以随意丢弃 B.铁矿石可以随意开采
C.被腐蚀的铁制品应该加以回收利用 D.铁丝在氧气中燃烧生成氧化铁
4、若金属锰(Mn)在金属活动性顺序中位于铝和锌之间,则下列反应不正确的是( )
A. Mn+H2SO4=MnSO4+H2↑ B. Mg+MnSO4=MgSO4+Mn
C. Fe+MnSO4=FeSO4+Mn D. Mn+CuSO4=MnSO4+Cu
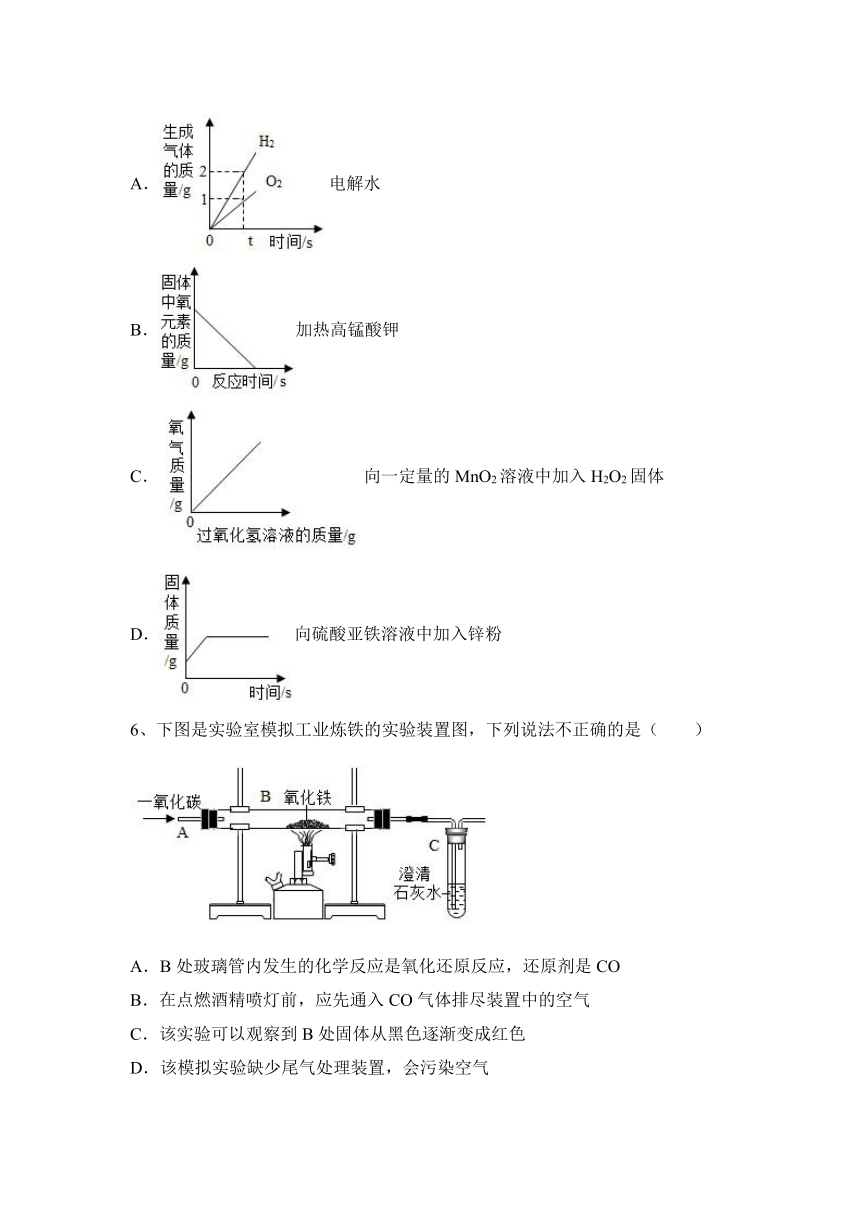
5、如图所示的四个图象,能正确反映对应变化关系的是( )
A.电解水
B.加热高锰酸钾
C.向一定量的MnO2溶液中加入H2O2固体D.向硫酸亚铁溶液中加入锌粉
6、下图是实验室模拟工业炼铁的实验装置图,下列说法不正确的是( )
A.B处玻璃管内发生的化学反应是氧化还原反应,还原剂是CO
B.在点燃酒精喷灯前,应先通入CO气体排尽装置中的空气
C.该实验可以观察到B处固体从黑色逐渐变成红色
D.该模拟实验缺少尾气处理装置,会污染空气
7、有X、Y、Z三种金属,把足量X放入Y(NO3)2和Z(NO3)2的混合溶液中,充分反应后过滤,滤渣中只有X、Z。据此判断这三种金属的活动性由强到弱的顺序为( )
A.Y>X>Z B.Y>Z>X C.X>Y>Z D.X>Z>Y
8、下列有关废旧金属回收的意义,说法错误的是( )
A.耗费大量人力物力,得不偿失
B.是保护金属资源的重要途径
C.可以减少废旧金属对环境的污染
D.可以节约宝贵的金属资源
9、如图所示对应关系正确的是( )
A.
一定量的MgSO4溶液中加入NaOH溶液,沉淀质量与加入NaOH溶液质量的关系
B.
相同质量的Mg、Fe分别与足量的同浓度稀硫酸反应,氢气的质量与反应时间的关系
C.
一定量的饱和石灰水中加入氧化钙,溶液中溶质质量与加入氧化钙质量的关系
D.
向氢氧化钠溶液中不断加水,溶液的pH与加入水的质量的关系
10、从废铜屑中得到较纯的铜,某探究小组设计方案如下,有关说法正确的是( )
A.X可以是Zn,但不能是Ag
B.若X是铁,第③步反应还会生成氯化铁
C.仅用第②③步操作也能达到实验目的
D.向第②步反应后的溶液中加入硝酸银溶液,若产生白色沉淀即证明稀盐酸过量
11、利用如图所示实验装置模拟工业炼铁。下列说法正确的是( )
A.实验时应先点燃酒精灯后通CO
B.充分加热,a处固体由黑色变为红色
C.b处可用澄清石灰水检验生成的CO2
D.可用NaOH溶液吸收尾气中的CO
12、从化学的角度对下列诗句、成语等进行解释,其中不正确的是( )
A.“遥知不是雪,为有暗香来”﹣﹣分子在不停地运动
B.“点石成金”﹣﹣化学反应改变了元素种类
C.“真金不怕火炼”﹣﹣金(Au)的化学性质不活泼
D.“釜底抽薪”(釜:烹煮食物的容器.薪:柴禾)﹣﹣破坏了燃烧的条件
13、下列环境中,铁钉表面最容易生锈的是( )
A.在稀盐酸中 B.在潮湿空气中
C.在干燥空气中 D.浸没在植物油中
14、X、Y、Z是金属活动性顺序表里的三种金属,它们在溶液中能发生如下反应:
①X+YSO4==XSO4+Y ②Y+2ZNO3=Y(NO3)2+2Z
③X+H2SO4==XSO4+H2↑ ④Z与H2SO4不发生反应
则三种金属的活动性满足( )
A. X>Y>Z B. Z>Y>X C. Y>Z>X D. X>Z>Y
15、国产大型客机C919于2017年5月5日在上海浦东国际机场首飞成功。C919大型客机的研制,使用了大量的铝锂合金、钛合金和复合材料等。下列有关说法错误的是( )
A.锂的密度应该比较小
B.金属铝质轻、耐腐蚀、延展性好
C.铝锂合金的硬度小,熔点高
D.钛合金是以钛为基础加入其他元素熔合而成的
16、下列关于金属材料的说法中,正确的是( )
A.生铁和钢是含碳量不同的两种铁合金
B.黄铜片(铜锌合金)比纯铜片硬度小
C.铁钉锈蚀主要是铁与空气中的氧气、二氧化碳发生了化学反应
D.铝制品在空气中耐腐蚀是因为铝不活泼
二、填空题。
17、“科技兴国、科技创新、不负嘱托!”习总书记来到哈尔滨为哈尔滨科技创新带来活力。哈工大学生设计制造的小卫星升空,哈工程大学研发的世界上速度最快的无人艇试航,石墨烯研发成功……都是哈尔滨的骄傲!
(1)利用火箭发射卫星,火箭使用肼(N2H4)作燃料,氧气作氧化剂,在一定条件下反应生成空气中含量最多的气体和一种常用来作溶剂的物质,同时放出巨大能量把火箭送入太空,该反应的化学方程式为: , 反应前后氧元素的化合价分别为 ,火箭升空过程中的能量转化为 →内能→ 。
(2)钛和钛合金是制造火箭、导弹、航天飞机的重要材料,主要利用了它们具有_______等性能(填字母)
A.熔点高、密度小、机械性能好
B.熔点低、硬度大、韧性好
C.密度大、耐磨、耐腐蚀
(3)石墨烯可被用于制造透明电极、液晶显示屏、触摸屏、有机光伏电池和有机发光二极管等,是由于石墨烯具有较高的 和透光性。
18、有X、Y、Z三种金属它们能发生如下反应:X放入Z的盐溶液中能得到Z,Y放入X的盐溶液中能得到X,Y放入Z的盐溶液中能得到Z,三种金属的活动性顺序由强到弱排列为 。
19、根据金属锈蚀的条件,防止金属生锈的方法可以是:
(1)保持金属制品(特别是钢铁)表面的洁净和____ 。
(2)在金属制品(特别是钢铁)表面涂上一层_____ ,如涂油、喷漆、覆盖搪瓷、塑料等;
(3)改变金属的_____ ,如加入铬、镍等制成不锈钢。
20、向铁粉和氧化铜的混合物中加入一定量的稀硫酸,微热,充分反应后过滤,向滤液中插入铁片,有气泡产生,则滤渣中一定含有________;氧化铜与稀硫酸反应的化学反应方程式为________ 。实验室用浓硫酸配制一定量的稀硫酸,正确操作是将________ ,并不断搅拌。
21、电池的变革。
(1)伏打电池(如图)食盐水中的溶质是_______(填化学式,下同);可用_______溶液比较电池中锌和银两种金属的活动性强弱。
(2)锌锰干电池(如图)其中能导电的非金属单质是_______(填化学式)。
(3)铅酸蓄电池工作原理为Pb+X+2H2SO4=2PbSO4+2H2O,则X的化学式为_______。
(4)燃料电池燃料在一定条件下与氧气反应,将_______能转化为电能。
(5)锂离子电池其电解液的溶剂常用碳酸乙烯酯(C3H4O3),碳酸乙烯酯完全燃烧的产物是____ 。
三、实验题。
22、铁合金是生产生活中使用最广泛的金属材料,但铁制品容易被腐蚀而在表面生成红褐色的铁锈。为探究铁制品锈蚀的条件,寻找防止铁制品锈蚀的方法,现进行如下实验:
步骤1:利用右图所示装置,将干燥的O2从导管a通入U形管(装置气密性良好,药品如图所示);待U形管内充满O2后,将导管a、b处的止水夹k1、k2夹紧。
步骤2:一段时间后,观察U形管内三处铁丝表面的变化情况。
回答下列问题:
(1)步骤1中,检验U形管内已充满O2的方法是________ 。
(2)步骤2中,观察到①处没有明显变化,说明铁制品锈蚀的条件之一是需要有_______(填化学式),②处可能观察到的现象是_______ ,③处没有明显变化,说明纯铁的抗腐蚀能力较____(填“强”或“弱”)。
(3)待U形管内有明显现象后,将b导管插入水中,打开止水夹k2,观察到_____现象,说明该条件下铁制品锈蚀过程消耗了O2。
(4)通过上述实验现象,请你提出一种防止铁制品锈蚀的方法(不包括制造纯铁):__________。
四、实验探究题。
23、金属材料的应用推动了社会发展。
I.被誉为“中国天眼”的FAST是目前世界上最大口径、最灵敏的射电望远镜,支撑它的角钢塔架中含有铁、铜、锰(Mn),现探究三种金属的活动性强弱。
【猜想】
(1)猜想1:Mn>Fe>Cu;猜想2:Fe>Cu>Mn;
猜想3:__________。猜想4:Cu>Fe>Mn:
猜想5:Cu>Mn>Fe:猜想6:Mn>Cu>Fe。
【实验】
【分析】
(2)实验过程中发现只有实验①无明显现象。由此可得出猜想__________(填序号)是正确的。
(3)实验③反应的化学方程式为__________ (生成物中锰元素显+2价)。
(4)通过实验现象及分析发现,不需要进行实验__________(选填写①②③④)就能够得出结论。
【拓展】
(5)已知金属锰和铁有相似的化学性质,能溶于稀酸,生成含有+2价金属离子的化合物。现将由5.5g金属锰、5.6g金属铁、6.4g金属铜组成的混合物放入一定量的稀硫酸中,充分反应后过滤得到固体12g,同时产生氢气的质量为_______g。
Ⅱ.实验室用金属铁制备新型多功能水处理剂高铁酸钾(K2FeO4)的流程如下:
(6)固体B中含有的物质是__________。
(7)反应③中沉淀D与H2O2发生化合反应,反应的化学方程式为__________ 。
五、计算类综合题。
24、化学实验小组同学为研究某公共场所铁制护栏锈蚀的程度,将12.8g已生锈的铁片,放入一定浓度的稀盐酸中充分反应,测得产生的气体质量与稀盐酸的质量关系如图所示(假设铁片除有Fe2O3外,不含其他杂质)。
(1)生成氢气的质量为______g;
(2)所用稀盐酸中溶质的质量分数为(写出计算过程)。
(3)该铁片中Fe2O3的质量______g,该铁制护栏锈蚀原因是铁与______反应,请你提出一条防止铁制护栏锈蚀合理措施______。
2023—2024学年鲁教版(五四学制)化学九年级全一册第四单元 金属 期末复习含答案
鲁教版(五四学制)第四单元 金属
一、选择题。
1、科学家发现一种新金属。根据右表信息推测其用途错误的是( )
熔点 2500℃
密度 3g/cm3
强度 与钢相似
导电性 良好
导热性 良好
抗腐蚀性 优异
A.用于焊接金属 B.制造航天飞机
C.制外科手术刀 D.用于通讯设备
【答案】A
2、下列实验现象描述正确的是( )
A.硫在氧气中燃烧,产生淡蓝色火焰
B.镁条在空气中燃烧,发出耀眼白光
C.铜片放入稀硫酸中,有气泡产生
D.一氧化碳还原氧化铁,固体粉末由黑色变为红色
【答案】B
3、下列说法中正确的是( )
A.废旧电池可以随意丢弃 B.铁矿石可以随意开采
C.被腐蚀的铁制品应该加以回收利用 D.铁丝在氧气中燃烧生成氧化铁
【答案】C
4、若金属锰(Mn)在金属活动性顺序中位于铝和锌之间,则下列反应不正确的是( )
A. Mn+H2SO4=MnSO4+H2↑ B. Mg+MnSO4=MgSO4+Mn
C. Fe+MnSO4=FeSO4+Mn D. Mn+CuSO4=MnSO4+Cu
【答案】C
5、如图所示的四个图象,能正确反映对应变化关系的是( )
A.电解水
B.加热高锰酸钾
C.向一定量的MnO2溶液中加入H2O2固体D.向硫酸亚铁溶液中加入锌粉
【答案】C
6、下图是实验室模拟工业炼铁的实验装置图,下列说法不正确的是( )
A.B处玻璃管内发生的化学反应是氧化还原反应,还原剂是CO
B.在点燃酒精喷灯前,应先通入CO气体排尽装置中的空气
C.该实验可以观察到B处固体从黑色逐渐变成红色
D.该模拟实验缺少尾气处理装置,会污染空气
【答案】C
7、有X、Y、Z三种金属,把足量X放入Y(NO3)2和Z(NO3)2的混合溶液中,充分反应后过滤,滤渣中只有X、Z。据此判断这三种金属的活动性由强到弱的顺序为( )
A.Y>X>Z B.Y>Z>X C.X>Y>Z D.X>Z>Y
【答案】A
8、下列有关废旧金属回收的意义,说法错误的是( )
A.耗费大量人力物力,得不偿失
B.是保护金属资源的重要途径
C.可以减少废旧金属对环境的污染
D.可以节约宝贵的金属资源
【答案】A
9、如图所示对应关系正确的是( )
A.
一定量的MgSO4溶液中加入NaOH溶液,沉淀质量与加入NaOH溶液质量的关系
B.
相同质量的Mg、Fe分别与足量的同浓度稀硫酸反应,氢气的质量与反应时间的关系
C.
一定量的饱和石灰水中加入氧化钙,溶液中溶质质量与加入氧化钙质量的关系
D.
向氢氧化钠溶液中不断加水,溶液的pH与加入水的质量的关系
【答案】A
10、从废铜屑中得到较纯的铜,某探究小组设计方案如下,有关说法正确的是( )
A.X可以是Zn,但不能是Ag
B.若X是铁,第③步反应还会生成氯化铁
C.仅用第②③步操作也能达到实验目的
D.向第②步反应后的溶液中加入硝酸银溶液,若产生白色沉淀即证明稀盐酸过量
【答案】A
11、利用如图所示实验装置模拟工业炼铁。下列说法正确的是( )
A.实验时应先点燃酒精灯后通CO
B.充分加热,a处固体由黑色变为红色
C.b处可用澄清石灰水检验生成的CO2
D.可用NaOH溶液吸收尾气中的CO
【答案】C
12、从化学的角度对下列诗句、成语等进行解释,其中不正确的是( )
A.“遥知不是雪,为有暗香来”﹣﹣分子在不停地运动
B.“点石成金”﹣﹣化学反应改变了元素种类
C.“真金不怕火炼”﹣﹣金(Au)的化学性质不活泼
D.“釜底抽薪”(釜:烹煮食物的容器.薪:柴禾)﹣﹣破坏了燃烧的条件
【答案】B
13、下列环境中,铁钉表面最容易生锈的是( )
A.在稀盐酸中 B.在潮湿空气中
C.在干燥空气中 D.浸没在植物油中
【答案】B
14、X、Y、Z是金属活动性顺序表里的三种金属,它们在溶液中能发生如下反应:
①X+YSO4==XSO4+Y ②Y+2ZNO3=Y(NO3)2+2Z
③X+H2SO4==XSO4+H2↑ ④Z与H2SO4不发生反应
则三种金属的活动性满足( )
A. X>Y>Z B. Z>Y>X C. Y>Z>X D. X>Z>Y
【答案】A
15、国产大型客机C919于2017年5月5日在上海浦东国际机场首飞成功。C919大型客机的研制,使用了大量的铝锂合金、钛合金和复合材料等。下列有关说法错误的是( )
A.锂的密度应该比较小
B.金属铝质轻、耐腐蚀、延展性好
C.铝锂合金的硬度小,熔点高
D.钛合金是以钛为基础加入其他元素熔合而成的
【答案】C
16、下列关于金属材料的说法中,正确的是( )
A.生铁和钢是含碳量不同的两种铁合金
B.黄铜片(铜锌合金)比纯铜片硬度小
C.铁钉锈蚀主要是铁与空气中的氧气、二氧化碳发生了化学反应
D.铝制品在空气中耐腐蚀是因为铝不活泼
【答案】A
二、填空题。
17、“科技兴国、科技创新、不负嘱托!”习总书记来到哈尔滨为哈尔滨科技创新带来活力。哈工大学生设计制造的小卫星升空,哈工程大学研发的世界上速度最快的无人艇试航,石墨烯研发成功……都是哈尔滨的骄傲!
(1)利用火箭发射卫星,火箭使用肼(N2H4)作燃料,氧气作氧化剂,在一定条件下反应生成空气中含量最多的气体和一种常用来作溶剂的物质,同时放出巨大能量把火箭送入太空,该反应的化学方程式为: , 反应前后氧元素的化合价分别为 ,火箭升空过程中的能量转化为 →内能→ 。
(2)钛和钛合金是制造火箭、导弹、航天飞机的重要材料,主要利用了它们具有_______等性能(填字母)
A.熔点高、密度小、机械性能好
B.熔点低、硬度大、韧性好
C.密度大、耐磨、耐腐蚀
(3)石墨烯可被用于制造透明电极、液晶显示屏、触摸屏、有机光伏电池和有机发光二极管等,是由于石墨烯具有较高的 和透光性。
【答案】(1)N2H4+O2 N2+2H2O;0价、-2价;化学能;机械能
(2)A (3)导电能力
18、有X、Y、Z三种金属它们能发生如下反应:X放入Z的盐溶液中能得到Z,Y放入X的盐溶液中能得到X,Y放入Z的盐溶液中能得到Z,三种金属的活动性顺序由强到弱排列为 。
【答案】Y>X>Z
19、根据金属锈蚀的条件,防止金属生锈的方法可以是:
(1)保持金属制品(特别是钢铁)表面的洁净和____ 。
(2)在金属制品(特别是钢铁)表面涂上一层_____ ,如涂油、喷漆、覆盖搪瓷、塑料等;
(3)改变金属的_____ ,如加入铬、镍等制成不锈钢。
【答案】 (1) 干燥 (2)保护层 (3)结构
20、向铁粉和氧化铜的混合物中加入一定量的稀硫酸,微热,充分反应后过滤,向滤液中插入铁片,有气泡产生,则滤渣中一定含有________;氧化铜与稀硫酸反应的化学反应方程式为________ 。实验室用浓硫酸配制一定量的稀硫酸,正确操作是将________ ,并不断搅拌。
【答案】铜;CuO+H2SO4=CuSO4+H2O;要把浓硫酸沿容器壁慢慢注入水中
21、电池的变革。
(1)伏打电池(如图)食盐水中的溶质是_______(填化学式,下同);可用_______溶液比较电池中锌和银两种金属的活动性强弱。
(2)锌锰干电池(如图)其中能导电的非金属单质是_______(填化学式)。
(3)铅酸蓄电池工作原理为Pb+X+2H2SO4=2PbSO4+2H2O,则X的化学式为_______。
(4)燃料电池燃料在一定条件下与氧气反应,将_______能转化为电能。
(5)锂离子电池其电解液的溶剂常用碳酸乙烯酯(C3H4O3),碳酸乙烯酯完全燃烧的产物是____ 。
【答案】(1) NaCl 盐酸 (2)C
(3)PbO2 (4)化学 (5)二氧化碳和水
三、实验题。
22、铁合金是生产生活中使用最广泛的金属材料,但铁制品容易被腐蚀而在表面生成红褐色的铁锈。为探究铁制品锈蚀的条件,寻找防止铁制品锈蚀的方法,现进行如下实验:
步骤1:利用右图所示装置,将干燥的O2从导管a通入U形管(装置气密性良好,药品如图所示);待U形管内充满O2后,将导管a、b处的止水夹k1、k2夹紧。
步骤2:一段时间后,观察U形管内三处铁丝表面的变化情况。
回答下列问题:
(1)步骤1中,检验U形管内已充满O2的方法是________ 。
(2)步骤2中,观察到①处没有明显变化,说明铁制品锈蚀的条件之一是需要有_______(填化学式),②处可能观察到的现象是_______ ,③处没有明显变化,说明纯铁的抗腐蚀能力较____(填“强”或“弱”)。
(3)待U形管内有明显现象后,将b导管插入水中,打开止水夹k2,观察到_____现象,说明该条件下铁制品锈蚀过程消耗了O2。
(4)通过上述实验现象,请你提出一种防止铁制品锈蚀的方法(不包括制造纯铁):__________。
【答案】(1) 在导管b处放一根带火星的木条,若木条复燃,则证明U形管内已充满O2
(2)H2O 产生较多红褐色的锈斑 强
(3) 水倒吸入U形管内 刷漆(涂油等合理即可)
四、实验探究题。
23、金属材料的应用推动了社会发展。
I.被誉为“中国天眼”的FAST是目前世界上最大口径、最灵敏的射电望远镜,支撑它的角钢塔架中含有铁、铜、锰(Mn),现探究三种金属的活动性强弱。
【猜想】
(1)猜想1:Mn>Fe>Cu;猜想2:Fe>Cu>Mn;
猜想3:__________。猜想4:Cu>Fe>Mn:
猜想5:Cu>Mn>Fe:猜想6:Mn>Cu>Fe。
【实验】
【分析】
(2)实验过程中发现只有实验①无明显现象。由此可得出猜想__________(填序号)是正确的。
(3)实验③反应的化学方程式为__________ (生成物中锰元素显+2价)。
(4)通过实验现象及分析发现,不需要进行实验__________(选填写①②③④)就能够得出结论。
【拓展】
(5)已知金属锰和铁有相似的化学性质,能溶于稀酸,生成含有+2价金属离子的化合物。现将由5.5g金属锰、5.6g金属铁、6.4g金属铜组成的混合物放入一定量的稀硫酸中,充分反应后过滤得到固体12g,同时产生氢气的质量为_______g。
Ⅱ.实验室用金属铁制备新型多功能水处理剂高铁酸钾(K2FeO4)的流程如下:
(6)固体B中含有的物质是__________。
(7)反应③中沉淀D与H2O2发生化合反应,反应的化学方程式为__________ 。
【答案】(1)Fe>Mn>Cu (2)1 (3)
(4)④ (5)0.2 (6)铜、铁 (7)H2O2+2Fe(OH)2=2Fe(OH)3
五、计算类综合题。
24、化学实验小组同学为研究某公共场所铁制护栏锈蚀的程度,将12.8g已生锈的铁片,放入一定浓度的稀盐酸中充分反应,测得产生的气体质量与稀盐酸的质量关系如图所示(假设铁片除有Fe2O3外,不含其他杂质)。
(1)生成氢气的质量为______g;
(2)所用稀盐酸中溶质的质量分数为(写出计算过程)。
(3)该铁片中Fe2O3的质量______g,该铁制护栏锈蚀原因是铁与______反应,请你提出一条防止铁制护栏锈蚀合理措施______。
【答案】(1)0.4
(2)生成氢气的质量为 0.4g;所用稀盐酸中溶质的质量分数为 14.6%。
(3)1.6g,水和氧气,喷漆。
鲁教版(五四学制)第四单元 金属
一、选择题。
1、科学家发现一种新金属。根据右表信息推测其用途错误的是( )
熔点 2500℃
密度 3g/cm3
强度 与钢相似
导电性 良好
导热性 良好
抗腐蚀性 优异
A.用于焊接金属 B.制造航天飞机
C.制外科手术刀 D.用于通讯设备
2、下列实验现象描述正确的是( )
A.硫在氧气中燃烧,产生淡蓝色火焰
B.镁条在空气中燃烧,发出耀眼白光
C.铜片放入稀硫酸中,有气泡产生
D.一氧化碳还原氧化铁,固体粉末由黑色变为红色
3、下列说法中正确的是( )
A.废旧电池可以随意丢弃 B.铁矿石可以随意开采
C.被腐蚀的铁制品应该加以回收利用 D.铁丝在氧气中燃烧生成氧化铁
4、若金属锰(Mn)在金属活动性顺序中位于铝和锌之间,则下列反应不正确的是( )
A. Mn+H2SO4=MnSO4+H2↑ B. Mg+MnSO4=MgSO4+Mn
C. Fe+MnSO4=FeSO4+Mn D. Mn+CuSO4=MnSO4+Cu
5、如图所示的四个图象,能正确反映对应变化关系的是( )
A.电解水
B.加热高锰酸钾
C.向一定量的MnO2溶液中加入H2O2固体D.向硫酸亚铁溶液中加入锌粉
6、下图是实验室模拟工业炼铁的实验装置图,下列说法不正确的是( )
A.B处玻璃管内发生的化学反应是氧化还原反应,还原剂是CO
B.在点燃酒精喷灯前,应先通入CO气体排尽装置中的空气
C.该实验可以观察到B处固体从黑色逐渐变成红色
D.该模拟实验缺少尾气处理装置,会污染空气
7、有X、Y、Z三种金属,把足量X放入Y(NO3)2和Z(NO3)2的混合溶液中,充分反应后过滤,滤渣中只有X、Z。据此判断这三种金属的活动性由强到弱的顺序为( )
A.Y>X>Z B.Y>Z>X C.X>Y>Z D.X>Z>Y
8、下列有关废旧金属回收的意义,说法错误的是( )
A.耗费大量人力物力,得不偿失
B.是保护金属资源的重要途径
C.可以减少废旧金属对环境的污染
D.可以节约宝贵的金属资源
9、如图所示对应关系正确的是( )
A.
一定量的MgSO4溶液中加入NaOH溶液,沉淀质量与加入NaOH溶液质量的关系
B.
相同质量的Mg、Fe分别与足量的同浓度稀硫酸反应,氢气的质量与反应时间的关系
C.
一定量的饱和石灰水中加入氧化钙,溶液中溶质质量与加入氧化钙质量的关系
D.
向氢氧化钠溶液中不断加水,溶液的pH与加入水的质量的关系
10、从废铜屑中得到较纯的铜,某探究小组设计方案如下,有关说法正确的是( )
A.X可以是Zn,但不能是Ag
B.若X是铁,第③步反应还会生成氯化铁
C.仅用第②③步操作也能达到实验目的
D.向第②步反应后的溶液中加入硝酸银溶液,若产生白色沉淀即证明稀盐酸过量
11、利用如图所示实验装置模拟工业炼铁。下列说法正确的是( )
A.实验时应先点燃酒精灯后通CO
B.充分加热,a处固体由黑色变为红色
C.b处可用澄清石灰水检验生成的CO2
D.可用NaOH溶液吸收尾气中的CO
12、从化学的角度对下列诗句、成语等进行解释,其中不正确的是( )
A.“遥知不是雪,为有暗香来”﹣﹣分子在不停地运动
B.“点石成金”﹣﹣化学反应改变了元素种类
C.“真金不怕火炼”﹣﹣金(Au)的化学性质不活泼
D.“釜底抽薪”(釜:烹煮食物的容器.薪:柴禾)﹣﹣破坏了燃烧的条件
13、下列环境中,铁钉表面最容易生锈的是( )
A.在稀盐酸中 B.在潮湿空气中
C.在干燥空气中 D.浸没在植物油中
14、X、Y、Z是金属活动性顺序表里的三种金属,它们在溶液中能发生如下反应:
①X+YSO4==XSO4+Y ②Y+2ZNO3=Y(NO3)2+2Z
③X+H2SO4==XSO4+H2↑ ④Z与H2SO4不发生反应
则三种金属的活动性满足( )
A. X>Y>Z B. Z>Y>X C. Y>Z>X D. X>Z>Y
15、国产大型客机C919于2017年5月5日在上海浦东国际机场首飞成功。C919大型客机的研制,使用了大量的铝锂合金、钛合金和复合材料等。下列有关说法错误的是( )
A.锂的密度应该比较小
B.金属铝质轻、耐腐蚀、延展性好
C.铝锂合金的硬度小,熔点高
D.钛合金是以钛为基础加入其他元素熔合而成的
16、下列关于金属材料的说法中,正确的是( )
A.生铁和钢是含碳量不同的两种铁合金
B.黄铜片(铜锌合金)比纯铜片硬度小
C.铁钉锈蚀主要是铁与空气中的氧气、二氧化碳发生了化学反应
D.铝制品在空气中耐腐蚀是因为铝不活泼
二、填空题。
17、“科技兴国、科技创新、不负嘱托!”习总书记来到哈尔滨为哈尔滨科技创新带来活力。哈工大学生设计制造的小卫星升空,哈工程大学研发的世界上速度最快的无人艇试航,石墨烯研发成功……都是哈尔滨的骄傲!
(1)利用火箭发射卫星,火箭使用肼(N2H4)作燃料,氧气作氧化剂,在一定条件下反应生成空气中含量最多的气体和一种常用来作溶剂的物质,同时放出巨大能量把火箭送入太空,该反应的化学方程式为: , 反应前后氧元素的化合价分别为 ,火箭升空过程中的能量转化为 →内能→ 。
(2)钛和钛合金是制造火箭、导弹、航天飞机的重要材料,主要利用了它们具有_______等性能(填字母)
A.熔点高、密度小、机械性能好
B.熔点低、硬度大、韧性好
C.密度大、耐磨、耐腐蚀
(3)石墨烯可被用于制造透明电极、液晶显示屏、触摸屏、有机光伏电池和有机发光二极管等,是由于石墨烯具有较高的 和透光性。
18、有X、Y、Z三种金属它们能发生如下反应:X放入Z的盐溶液中能得到Z,Y放入X的盐溶液中能得到X,Y放入Z的盐溶液中能得到Z,三种金属的活动性顺序由强到弱排列为 。
19、根据金属锈蚀的条件,防止金属生锈的方法可以是:
(1)保持金属制品(特别是钢铁)表面的洁净和____ 。
(2)在金属制品(特别是钢铁)表面涂上一层_____ ,如涂油、喷漆、覆盖搪瓷、塑料等;
(3)改变金属的_____ ,如加入铬、镍等制成不锈钢。
20、向铁粉和氧化铜的混合物中加入一定量的稀硫酸,微热,充分反应后过滤,向滤液中插入铁片,有气泡产生,则滤渣中一定含有________;氧化铜与稀硫酸反应的化学反应方程式为________ 。实验室用浓硫酸配制一定量的稀硫酸,正确操作是将________ ,并不断搅拌。
21、电池的变革。
(1)伏打电池(如图)食盐水中的溶质是_______(填化学式,下同);可用_______溶液比较电池中锌和银两种金属的活动性强弱。
(2)锌锰干电池(如图)其中能导电的非金属单质是_______(填化学式)。
(3)铅酸蓄电池工作原理为Pb+X+2H2SO4=2PbSO4+2H2O,则X的化学式为_______。
(4)燃料电池燃料在一定条件下与氧气反应,将_______能转化为电能。
(5)锂离子电池其电解液的溶剂常用碳酸乙烯酯(C3H4O3),碳酸乙烯酯完全燃烧的产物是____ 。
三、实验题。
22、铁合金是生产生活中使用最广泛的金属材料,但铁制品容易被腐蚀而在表面生成红褐色的铁锈。为探究铁制品锈蚀的条件,寻找防止铁制品锈蚀的方法,现进行如下实验:
步骤1:利用右图所示装置,将干燥的O2从导管a通入U形管(装置气密性良好,药品如图所示);待U形管内充满O2后,将导管a、b处的止水夹k1、k2夹紧。
步骤2:一段时间后,观察U形管内三处铁丝表面的变化情况。
回答下列问题:
(1)步骤1中,检验U形管内已充满O2的方法是________ 。
(2)步骤2中,观察到①处没有明显变化,说明铁制品锈蚀的条件之一是需要有_______(填化学式),②处可能观察到的现象是_______ ,③处没有明显变化,说明纯铁的抗腐蚀能力较____(填“强”或“弱”)。
(3)待U形管内有明显现象后,将b导管插入水中,打开止水夹k2,观察到_____现象,说明该条件下铁制品锈蚀过程消耗了O2。
(4)通过上述实验现象,请你提出一种防止铁制品锈蚀的方法(不包括制造纯铁):__________。
四、实验探究题。
23、金属材料的应用推动了社会发展。
I.被誉为“中国天眼”的FAST是目前世界上最大口径、最灵敏的射电望远镜,支撑它的角钢塔架中含有铁、铜、锰(Mn),现探究三种金属的活动性强弱。
【猜想】
(1)猜想1:Mn>Fe>Cu;猜想2:Fe>Cu>Mn;
猜想3:__________。猜想4:Cu>Fe>Mn:
猜想5:Cu>Mn>Fe:猜想6:Mn>Cu>Fe。
【实验】
【分析】
(2)实验过程中发现只有实验①无明显现象。由此可得出猜想__________(填序号)是正确的。
(3)实验③反应的化学方程式为__________ (生成物中锰元素显+2价)。
(4)通过实验现象及分析发现,不需要进行实验__________(选填写①②③④)就能够得出结论。
【拓展】
(5)已知金属锰和铁有相似的化学性质,能溶于稀酸,生成含有+2价金属离子的化合物。现将由5.5g金属锰、5.6g金属铁、6.4g金属铜组成的混合物放入一定量的稀硫酸中,充分反应后过滤得到固体12g,同时产生氢气的质量为_______g。
Ⅱ.实验室用金属铁制备新型多功能水处理剂高铁酸钾(K2FeO4)的流程如下:
(6)固体B中含有的物质是__________。
(7)反应③中沉淀D与H2O2发生化合反应,反应的化学方程式为__________ 。
五、计算类综合题。
24、化学实验小组同学为研究某公共场所铁制护栏锈蚀的程度,将12.8g已生锈的铁片,放入一定浓度的稀盐酸中充分反应,测得产生的气体质量与稀盐酸的质量关系如图所示(假设铁片除有Fe2O3外,不含其他杂质)。
(1)生成氢气的质量为______g;
(2)所用稀盐酸中溶质的质量分数为(写出计算过程)。
(3)该铁片中Fe2O3的质量______g,该铁制护栏锈蚀原因是铁与______反应,请你提出一条防止铁制护栏锈蚀合理措施______。
2023—2024学年鲁教版(五四学制)化学九年级全一册第四单元 金属 期末复习含答案
鲁教版(五四学制)第四单元 金属
一、选择题。
1、科学家发现一种新金属。根据右表信息推测其用途错误的是( )
熔点 2500℃
密度 3g/cm3
强度 与钢相似
导电性 良好
导热性 良好
抗腐蚀性 优异
A.用于焊接金属 B.制造航天飞机
C.制外科手术刀 D.用于通讯设备
【答案】A
2、下列实验现象描述正确的是( )
A.硫在氧气中燃烧,产生淡蓝色火焰
B.镁条在空气中燃烧,发出耀眼白光
C.铜片放入稀硫酸中,有气泡产生
D.一氧化碳还原氧化铁,固体粉末由黑色变为红色
【答案】B
3、下列说法中正确的是( )
A.废旧电池可以随意丢弃 B.铁矿石可以随意开采
C.被腐蚀的铁制品应该加以回收利用 D.铁丝在氧气中燃烧生成氧化铁
【答案】C
4、若金属锰(Mn)在金属活动性顺序中位于铝和锌之间,则下列反应不正确的是( )
A. Mn+H2SO4=MnSO4+H2↑ B. Mg+MnSO4=MgSO4+Mn
C. Fe+MnSO4=FeSO4+Mn D. Mn+CuSO4=MnSO4+Cu
【答案】C
5、如图所示的四个图象,能正确反映对应变化关系的是( )
A.电解水
B.加热高锰酸钾
C.向一定量的MnO2溶液中加入H2O2固体D.向硫酸亚铁溶液中加入锌粉
【答案】C
6、下图是实验室模拟工业炼铁的实验装置图,下列说法不正确的是( )
A.B处玻璃管内发生的化学反应是氧化还原反应,还原剂是CO
B.在点燃酒精喷灯前,应先通入CO气体排尽装置中的空气
C.该实验可以观察到B处固体从黑色逐渐变成红色
D.该模拟实验缺少尾气处理装置,会污染空气
【答案】C
7、有X、Y、Z三种金属,把足量X放入Y(NO3)2和Z(NO3)2的混合溶液中,充分反应后过滤,滤渣中只有X、Z。据此判断这三种金属的活动性由强到弱的顺序为( )
A.Y>X>Z B.Y>Z>X C.X>Y>Z D.X>Z>Y
【答案】A
8、下列有关废旧金属回收的意义,说法错误的是( )
A.耗费大量人力物力,得不偿失
B.是保护金属资源的重要途径
C.可以减少废旧金属对环境的污染
D.可以节约宝贵的金属资源
【答案】A
9、如图所示对应关系正确的是( )
A.
一定量的MgSO4溶液中加入NaOH溶液,沉淀质量与加入NaOH溶液质量的关系
B.
相同质量的Mg、Fe分别与足量的同浓度稀硫酸反应,氢气的质量与反应时间的关系
C.
一定量的饱和石灰水中加入氧化钙,溶液中溶质质量与加入氧化钙质量的关系
D.
向氢氧化钠溶液中不断加水,溶液的pH与加入水的质量的关系
【答案】A
10、从废铜屑中得到较纯的铜,某探究小组设计方案如下,有关说法正确的是( )
A.X可以是Zn,但不能是Ag
B.若X是铁,第③步反应还会生成氯化铁
C.仅用第②③步操作也能达到实验目的
D.向第②步反应后的溶液中加入硝酸银溶液,若产生白色沉淀即证明稀盐酸过量
【答案】A
11、利用如图所示实验装置模拟工业炼铁。下列说法正确的是( )
A.实验时应先点燃酒精灯后通CO
B.充分加热,a处固体由黑色变为红色
C.b处可用澄清石灰水检验生成的CO2
D.可用NaOH溶液吸收尾气中的CO
【答案】C
12、从化学的角度对下列诗句、成语等进行解释,其中不正确的是( )
A.“遥知不是雪,为有暗香来”﹣﹣分子在不停地运动
B.“点石成金”﹣﹣化学反应改变了元素种类
C.“真金不怕火炼”﹣﹣金(Au)的化学性质不活泼
D.“釜底抽薪”(釜:烹煮食物的容器.薪:柴禾)﹣﹣破坏了燃烧的条件
【答案】B
13、下列环境中,铁钉表面最容易生锈的是( )
A.在稀盐酸中 B.在潮湿空气中
C.在干燥空气中 D.浸没在植物油中
【答案】B
14、X、Y、Z是金属活动性顺序表里的三种金属,它们在溶液中能发生如下反应:
①X+YSO4==XSO4+Y ②Y+2ZNO3=Y(NO3)2+2Z
③X+H2SO4==XSO4+H2↑ ④Z与H2SO4不发生反应
则三种金属的活动性满足( )
A. X>Y>Z B. Z>Y>X C. Y>Z>X D. X>Z>Y
【答案】A
15、国产大型客机C919于2017年5月5日在上海浦东国际机场首飞成功。C919大型客机的研制,使用了大量的铝锂合金、钛合金和复合材料等。下列有关说法错误的是( )
A.锂的密度应该比较小
B.金属铝质轻、耐腐蚀、延展性好
C.铝锂合金的硬度小,熔点高
D.钛合金是以钛为基础加入其他元素熔合而成的
【答案】C
16、下列关于金属材料的说法中,正确的是( )
A.生铁和钢是含碳量不同的两种铁合金
B.黄铜片(铜锌合金)比纯铜片硬度小
C.铁钉锈蚀主要是铁与空气中的氧气、二氧化碳发生了化学反应
D.铝制品在空气中耐腐蚀是因为铝不活泼
【答案】A
二、填空题。
17、“科技兴国、科技创新、不负嘱托!”习总书记来到哈尔滨为哈尔滨科技创新带来活力。哈工大学生设计制造的小卫星升空,哈工程大学研发的世界上速度最快的无人艇试航,石墨烯研发成功……都是哈尔滨的骄傲!
(1)利用火箭发射卫星,火箭使用肼(N2H4)作燃料,氧气作氧化剂,在一定条件下反应生成空气中含量最多的气体和一种常用来作溶剂的物质,同时放出巨大能量把火箭送入太空,该反应的化学方程式为: , 反应前后氧元素的化合价分别为 ,火箭升空过程中的能量转化为 →内能→ 。
(2)钛和钛合金是制造火箭、导弹、航天飞机的重要材料,主要利用了它们具有_______等性能(填字母)
A.熔点高、密度小、机械性能好
B.熔点低、硬度大、韧性好
C.密度大、耐磨、耐腐蚀
(3)石墨烯可被用于制造透明电极、液晶显示屏、触摸屏、有机光伏电池和有机发光二极管等,是由于石墨烯具有较高的 和透光性。
【答案】(1)N2H4+O2 N2+2H2O;0价、-2价;化学能;机械能
(2)A (3)导电能力
18、有X、Y、Z三种金属它们能发生如下反应:X放入Z的盐溶液中能得到Z,Y放入X的盐溶液中能得到X,Y放入Z的盐溶液中能得到Z,三种金属的活动性顺序由强到弱排列为 。
【答案】Y>X>Z
19、根据金属锈蚀的条件,防止金属生锈的方法可以是:
(1)保持金属制品(特别是钢铁)表面的洁净和____ 。
(2)在金属制品(特别是钢铁)表面涂上一层_____ ,如涂油、喷漆、覆盖搪瓷、塑料等;
(3)改变金属的_____ ,如加入铬、镍等制成不锈钢。
【答案】 (1) 干燥 (2)保护层 (3)结构
20、向铁粉和氧化铜的混合物中加入一定量的稀硫酸,微热,充分反应后过滤,向滤液中插入铁片,有气泡产生,则滤渣中一定含有________;氧化铜与稀硫酸反应的化学反应方程式为________ 。实验室用浓硫酸配制一定量的稀硫酸,正确操作是将________ ,并不断搅拌。
【答案】铜;CuO+H2SO4=CuSO4+H2O;要把浓硫酸沿容器壁慢慢注入水中
21、电池的变革。
(1)伏打电池(如图)食盐水中的溶质是_______(填化学式,下同);可用_______溶液比较电池中锌和银两种金属的活动性强弱。
(2)锌锰干电池(如图)其中能导电的非金属单质是_______(填化学式)。
(3)铅酸蓄电池工作原理为Pb+X+2H2SO4=2PbSO4+2H2O,则X的化学式为_______。
(4)燃料电池燃料在一定条件下与氧气反应,将_______能转化为电能。
(5)锂离子电池其电解液的溶剂常用碳酸乙烯酯(C3H4O3),碳酸乙烯酯完全燃烧的产物是____ 。
【答案】(1) NaCl 盐酸 (2)C
(3)PbO2 (4)化学 (5)二氧化碳和水
三、实验题。
22、铁合金是生产生活中使用最广泛的金属材料,但铁制品容易被腐蚀而在表面生成红褐色的铁锈。为探究铁制品锈蚀的条件,寻找防止铁制品锈蚀的方法,现进行如下实验:
步骤1:利用右图所示装置,将干燥的O2从导管a通入U形管(装置气密性良好,药品如图所示);待U形管内充满O2后,将导管a、b处的止水夹k1、k2夹紧。
步骤2:一段时间后,观察U形管内三处铁丝表面的变化情况。
回答下列问题:
(1)步骤1中,检验U形管内已充满O2的方法是________ 。
(2)步骤2中,观察到①处没有明显变化,说明铁制品锈蚀的条件之一是需要有_______(填化学式),②处可能观察到的现象是_______ ,③处没有明显变化,说明纯铁的抗腐蚀能力较____(填“强”或“弱”)。
(3)待U形管内有明显现象后,将b导管插入水中,打开止水夹k2,观察到_____现象,说明该条件下铁制品锈蚀过程消耗了O2。
(4)通过上述实验现象,请你提出一种防止铁制品锈蚀的方法(不包括制造纯铁):__________。
【答案】(1) 在导管b处放一根带火星的木条,若木条复燃,则证明U形管内已充满O2
(2)H2O 产生较多红褐色的锈斑 强
(3) 水倒吸入U形管内 刷漆(涂油等合理即可)
四、实验探究题。
23、金属材料的应用推动了社会发展。
I.被誉为“中国天眼”的FAST是目前世界上最大口径、最灵敏的射电望远镜,支撑它的角钢塔架中含有铁、铜、锰(Mn),现探究三种金属的活动性强弱。
【猜想】
(1)猜想1:Mn>Fe>Cu;猜想2:Fe>Cu>Mn;
猜想3:__________。猜想4:Cu>Fe>Mn:
猜想5:Cu>Mn>Fe:猜想6:Mn>Cu>Fe。
【实验】
【分析】
(2)实验过程中发现只有实验①无明显现象。由此可得出猜想__________(填序号)是正确的。
(3)实验③反应的化学方程式为__________ (生成物中锰元素显+2价)。
(4)通过实验现象及分析发现,不需要进行实验__________(选填写①②③④)就能够得出结论。
【拓展】
(5)已知金属锰和铁有相似的化学性质,能溶于稀酸,生成含有+2价金属离子的化合物。现将由5.5g金属锰、5.6g金属铁、6.4g金属铜组成的混合物放入一定量的稀硫酸中,充分反应后过滤得到固体12g,同时产生氢气的质量为_______g。
Ⅱ.实验室用金属铁制备新型多功能水处理剂高铁酸钾(K2FeO4)的流程如下:
(6)固体B中含有的物质是__________。
(7)反应③中沉淀D与H2O2发生化合反应,反应的化学方程式为__________ 。
【答案】(1)Fe>Mn>Cu (2)1 (3)
(4)④ (5)0.2 (6)铜、铁 (7)H2O2+2Fe(OH)2=2Fe(OH)3
五、计算类综合题。
24、化学实验小组同学为研究某公共场所铁制护栏锈蚀的程度,将12.8g已生锈的铁片,放入一定浓度的稀盐酸中充分反应,测得产生的气体质量与稀盐酸的质量关系如图所示(假设铁片除有Fe2O3外,不含其他杂质)。
(1)生成氢气的质量为______g;
(2)所用稀盐酸中溶质的质量分数为(写出计算过程)。
(3)该铁片中Fe2O3的质量______g,该铁制护栏锈蚀原因是铁与______反应,请你提出一条防止铁制护栏锈蚀合理措施______。
【答案】(1)0.4
(2)生成氢气的质量为 0.4g;所用稀盐酸中溶质的质量分数为 14.6%。
(3)1.6g,水和氧气,喷漆。
同课章节目录
- 第一单元 溶液
- 1 溶液的形成
- 2 溶液组成的定量表示
- 3物质的溶解性
- 到实验室去:配制一定溶质质量分数的溶液
- 第二单元 常见的酸和碱
- 1 酸及其性质
- 2 碱及其性质
- 3 溶液的酸碱性
- 4 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 到图书馆去:分子变成离子
- 第三单元 海水中的化学
- 1 海洋化学资源
- 2 海水“晒盐”
- 3 海水“制碱”
- 到实验室去:粗盐中难溶性杂质的去除
- 第四单元 金属
- 1 常见的金属材料
- 2 金属的化学性质
- 3 钢铁的锈蚀与防护
- 到实验室去:探究金属的性质
- 第五单元 化学与健康
- 1 食物中的有机物
- 2 化学元素与人体健康
- 3 远离有毒物质
- 第六单元 化学与社会发展
- 1 化学与能源开发
- 2 化学与材料研制
- 3 化学与农业生产
- 4 化学与环境保护
