2024年化学中考复习专题5 金属活动性顺序的验证与探究 课件(共17张PPT)
文档属性
| 名称 | 2024年化学中考复习专题5 金属活动性顺序的验证与探究 课件(共17张PPT) |  | |
| 格式 | pptx | ||
| 文件大小 | 929.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-12-30 11:22:35 | ||
图片预览





文档简介
(共17张PPT)
中考复习专题5 金属活动性顺序的验证与探究
跟踪训练
2
1
典例串讲
典例串讲
一、金属活动性顺序的判断与验证依据
1. 金属活动性顺序:金属的位置越靠前,金属活动性越___。
2. 金属能否与酸反应:氢前金属能与稀酸反应,氢后金属不与稀酸反应。Cu与稀盐酸_______(填“反应”或“不反应”)。
3. 金属能否与金属盐溶液反应:将某金属(K、Ca、Na除外)放入另一金
属的盐溶液中,若该金属能将盐溶液中的金属置换出来,说明该金属的活动性___(填“强”或“弱”,后同)于该盐溶液中的金属,反之,则___于
该盐溶液中的金属。
强
不反应
强
弱
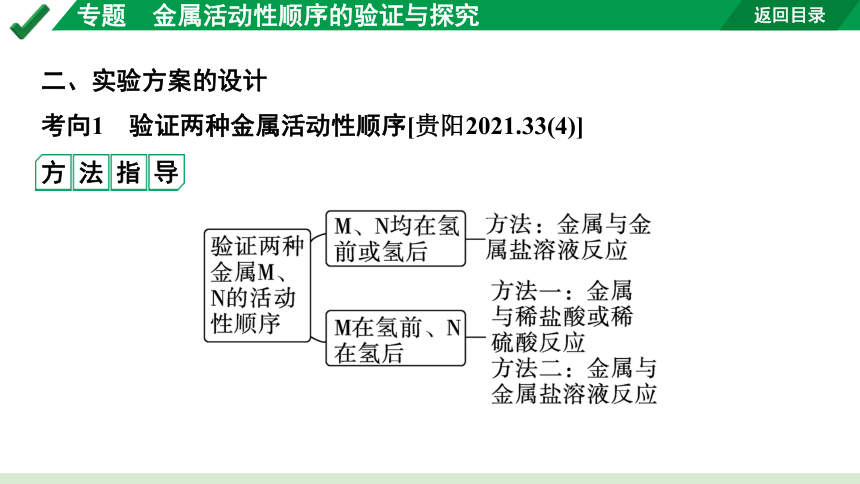
二、实验方案的设计
考向1 验证两种金属活动性顺序[贵阳2021.33(4)]
方法指导
例1 设计实验验证Fe、Cu的金属活动性顺序,完成下列实验报告。
思路 金属与金属盐溶液反应 金属与酸反应
方案 Ⅰ.将铁丝插入硫酸铜溶液中 Ⅱ.将铜丝插入________________溶液中 将铁丝和铜丝分别插入等体积、等浓度的稀盐酸中
现象 Ⅰ._______________________________________________; Ⅱ.无明显现象 ____________________________________________________________
FeSO4(或FeCl2等)
铁丝表面有红色固体析出,溶
液由蓝色变为浅绿色
铁丝表面有气泡产生,溶液由无色变为浅绿色;铜丝表面无明显现象
思路 金属与金属盐溶液反应 金属与酸反应
反应原理 ________________________ ______________________
结论 金属活动性顺序:_________________ Fe+CuSO4===FeSO4+Cu
Fe+2HCl===FeCl2+H2↑
Fe>Cu(或Cu<Fe)
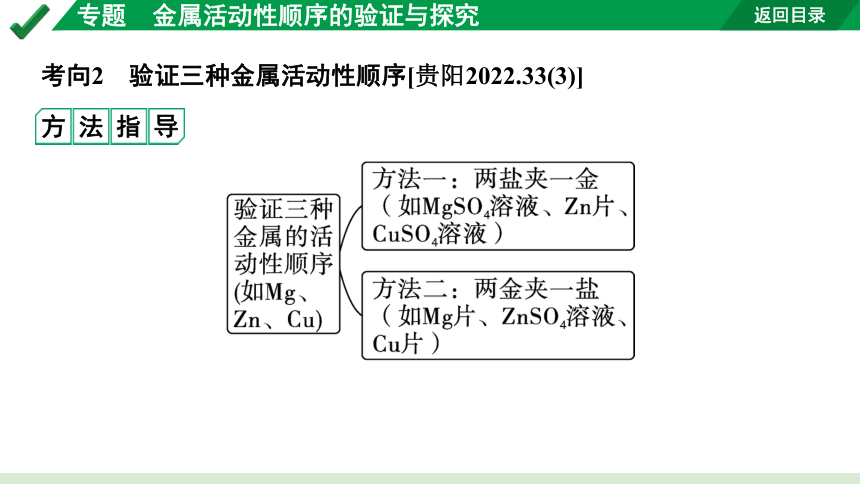
考向2 验证三种金属活动性顺序[贵阳2022.33(3)]
方法指导
思路 两金夹一盐 两盐夹一金
操作及试剂(均填名称) X为___, Y为___________
Z为___
现象 A中____________________ ___________________,B中___________ C中___________,D中_____
________________________________________
例2 设计实验验证Zn、Cu、Ag的金属活动性顺序,完成下列实验报告。
锌
硫酸铜溶液
铜
锌表面有红色固体析出,
溶液由蓝色变为无色
无明显现象
无明显现象
铜表面有银白色固体析出,溶液由无色变为蓝色
思路 两金夹一盐 两盐夹一金
操作及试剂(均填名称) X为___, Y为___________
Z为___
反应 原理 _______________________ ______________________________
结论 金属活动性顺序:___________________________ Zn+CuSO4===ZnSO4+Cu
Cu+2AgNO3=== 2Ag+Cu(NO3)2
Zn>Cu>Ag(或Ag<Cu<Zn)
锌
硫酸铜溶液
铜
【注意事项】①实验前,需用砂纸将金属打磨光亮,其目的是________
_____________________。
②做金属与酸反应的实验时,一般用稀盐酸或稀硫酸,不用浓盐酸、浓硫酸或硝酸。
除去金
属表面的氧化物和污物
跟踪训练
1. 现有X、Y、Z三种金属,已知:①X+YSO4===XSO4+Y
②Y+2ZNO3===Y(NO3)2+2Z ③Y+H2SO4不反应,则下列符合要求的X、Y、Z分别是( )
A. Fe、Cu、Ag
B. Mg、Fe、Ag
C. Zn、Fe、Cu
D. Mg、Zn、Cu
A
2. 同学们在实验室通过如图实验来验证铁、铜、银三种金属的活动性顺序,实验中金属均过量并充分反应。
(1)铜丝和铁丝一端可以被压成片状,说明金属具有_____性。
(2)步骤①中观察到的现象是______________________________________
_______,该实验设计的依据是___________________________________
_______。
延展
铜丝表面有银白色固体析出,溶液由无色变
为蓝色
三种金属的活动性由强到弱依次为铁、
铜、银
(3) [2022课标·作图]实验最后同学们欲画出步骤②反应前后溶液中离子组成示意图,请补全示意图。
3. 为验证铜、铁、锌的金属活动性顺序,小组同学设计如图1所示实验。
(1)试管B中发生反应的化学方程式为_________________________。
(2)为得出三种金属的活动性顺序,试管C中的甲、乙分别是___________
______________________________。
Zn+CuSO4===Cu+ZnSO4
铁片和硫酸铜溶液(或铜片和硫酸亚铁溶液等)
(3)如图2所示,在杠杆两端分别悬挂质量相等的铜球和锌球,此时杠杆平衡;然后将两个金属球分别浸没在稀硫酸和硫酸亚铁溶液中,一段时间后烧杯b中溶液质量_____(填“增大”“减小”或“不变”);实验结束后移走两烧杯,杠杆_____(填“能”或“不能”)保持平衡。
增大
不能
4. 小明同学了解到家用水龙头的材质是铜质镀铬。他想起在学习金属性质时用到的金属活动性顺序表中没有铬,于是和同学们对铬、铜、镁三种金属的活动性顺序进行了探究。
【查阅资料】CrSO4溶液呈蓝色。
【作出猜想】上述三种金属的活动性顺序是:
猜想一:Cr>Mg>Cu;
猜想二:Mg>Cr>Cu;
猜想三:_____________。
Mg>Cu>Cr
【进行实验】取两片大小、形状完全相同且已打磨好的铬片和铜片,进行下列实验:
实验编号 实验1 实验2
实验操作
实验现象 A试管中铬片表面有气泡出现,溶液变为蓝色;B试管中___________ 无明显现象
实验结论 猜想___正确 无明显现象
二
【交流讨论】(1)实验前打磨金属表面的目的是______________________
_______。
(2)实验1 A试管中发生反应的化学方程式
为_________________________。
【归纳总结】由上述实验得出比较金属活动性强弱的方法有:①_____
_______________________;②___________________________________。
【实验拓展】除了上述实验方案外,你还能设计的方案是____________
_____________________________________________________________。
除去金属表面的氧化物
和污物
Cr+H2SO4===CrSO4+H2↑
通过
金属与酸的反应现象判断
通过金属与金属盐溶液的反应现象判断
向两份等质量、等浓度的硫酸亚铬溶液中分别插入形状、大小相同的镁片和铜片
中考复习专题5 金属活动性顺序的验证与探究
跟踪训练
2
1
典例串讲
典例串讲
一、金属活动性顺序的判断与验证依据
1. 金属活动性顺序:金属的位置越靠前,金属活动性越___。
2. 金属能否与酸反应:氢前金属能与稀酸反应,氢后金属不与稀酸反应。Cu与稀盐酸_______(填“反应”或“不反应”)。
3. 金属能否与金属盐溶液反应:将某金属(K、Ca、Na除外)放入另一金
属的盐溶液中,若该金属能将盐溶液中的金属置换出来,说明该金属的活动性___(填“强”或“弱”,后同)于该盐溶液中的金属,反之,则___于
该盐溶液中的金属。
强
不反应
强
弱
二、实验方案的设计
考向1 验证两种金属活动性顺序[贵阳2021.33(4)]
方法指导
例1 设计实验验证Fe、Cu的金属活动性顺序,完成下列实验报告。
思路 金属与金属盐溶液反应 金属与酸反应
方案 Ⅰ.将铁丝插入硫酸铜溶液中 Ⅱ.将铜丝插入________________溶液中 将铁丝和铜丝分别插入等体积、等浓度的稀盐酸中
现象 Ⅰ._______________________________________________; Ⅱ.无明显现象 ____________________________________________________________
FeSO4(或FeCl2等)
铁丝表面有红色固体析出,溶
液由蓝色变为浅绿色
铁丝表面有气泡产生,溶液由无色变为浅绿色;铜丝表面无明显现象
思路 金属与金属盐溶液反应 金属与酸反应
反应原理 ________________________ ______________________
结论 金属活动性顺序:_________________ Fe+CuSO4===FeSO4+Cu
Fe+2HCl===FeCl2+H2↑
Fe>Cu(或Cu<Fe)
考向2 验证三种金属活动性顺序[贵阳2022.33(3)]
方法指导
思路 两金夹一盐 两盐夹一金
操作及试剂(均填名称) X为___, Y为___________
Z为___
现象 A中____________________ ___________________,B中___________ C中___________,D中_____
________________________________________
例2 设计实验验证Zn、Cu、Ag的金属活动性顺序,完成下列实验报告。
锌
硫酸铜溶液
铜
锌表面有红色固体析出,
溶液由蓝色变为无色
无明显现象
无明显现象
铜表面有银白色固体析出,溶液由无色变为蓝色
思路 两金夹一盐 两盐夹一金
操作及试剂(均填名称) X为___, Y为___________
Z为___
反应 原理 _______________________ ______________________________
结论 金属活动性顺序:___________________________ Zn+CuSO4===ZnSO4+Cu
Cu+2AgNO3=== 2Ag+Cu(NO3)2
Zn>Cu>Ag(或Ag<Cu<Zn)
锌
硫酸铜溶液
铜
【注意事项】①实验前,需用砂纸将金属打磨光亮,其目的是________
_____________________。
②做金属与酸反应的实验时,一般用稀盐酸或稀硫酸,不用浓盐酸、浓硫酸或硝酸。
除去金
属表面的氧化物和污物
跟踪训练
1. 现有X、Y、Z三种金属,已知:①X+YSO4===XSO4+Y
②Y+2ZNO3===Y(NO3)2+2Z ③Y+H2SO4不反应,则下列符合要求的X、Y、Z分别是( )
A. Fe、Cu、Ag
B. Mg、Fe、Ag
C. Zn、Fe、Cu
D. Mg、Zn、Cu
A
2. 同学们在实验室通过如图实验来验证铁、铜、银三种金属的活动性顺序,实验中金属均过量并充分反应。
(1)铜丝和铁丝一端可以被压成片状,说明金属具有_____性。
(2)步骤①中观察到的现象是______________________________________
_______,该实验设计的依据是___________________________________
_______。
延展
铜丝表面有银白色固体析出,溶液由无色变
为蓝色
三种金属的活动性由强到弱依次为铁、
铜、银
(3) [2022课标·作图]实验最后同学们欲画出步骤②反应前后溶液中离子组成示意图,请补全示意图。
3. 为验证铜、铁、锌的金属活动性顺序,小组同学设计如图1所示实验。
(1)试管B中发生反应的化学方程式为_________________________。
(2)为得出三种金属的活动性顺序,试管C中的甲、乙分别是___________
______________________________。
Zn+CuSO4===Cu+ZnSO4
铁片和硫酸铜溶液(或铜片和硫酸亚铁溶液等)
(3)如图2所示,在杠杆两端分别悬挂质量相等的铜球和锌球,此时杠杆平衡;然后将两个金属球分别浸没在稀硫酸和硫酸亚铁溶液中,一段时间后烧杯b中溶液质量_____(填“增大”“减小”或“不变”);实验结束后移走两烧杯,杠杆_____(填“能”或“不能”)保持平衡。
增大
不能
4. 小明同学了解到家用水龙头的材质是铜质镀铬。他想起在学习金属性质时用到的金属活动性顺序表中没有铬,于是和同学们对铬、铜、镁三种金属的活动性顺序进行了探究。
【查阅资料】CrSO4溶液呈蓝色。
【作出猜想】上述三种金属的活动性顺序是:
猜想一:Cr>Mg>Cu;
猜想二:Mg>Cr>Cu;
猜想三:_____________。
Mg>Cu>Cr
【进行实验】取两片大小、形状完全相同且已打磨好的铬片和铜片,进行下列实验:
实验编号 实验1 实验2
实验操作
实验现象 A试管中铬片表面有气泡出现,溶液变为蓝色;B试管中___________ 无明显现象
实验结论 猜想___正确 无明显现象
二
【交流讨论】(1)实验前打磨金属表面的目的是______________________
_______。
(2)实验1 A试管中发生反应的化学方程式
为_________________________。
【归纳总结】由上述实验得出比较金属活动性强弱的方法有:①_____
_______________________;②___________________________________。
【实验拓展】除了上述实验方案外,你还能设计的方案是____________
_____________________________________________________________。
除去金属表面的氧化物
和污物
Cr+H2SO4===CrSO4+H2↑
通过
金属与酸的反应现象判断
通过金属与金属盐溶液的反应现象判断
向两份等质量、等浓度的硫酸亚铬溶液中分别插入形状、大小相同的镁片和铜片
同课章节目录
