化学人教版(2019)选择性必修2 2.2.2杂化轨道(共27张ppt)
文档属性
| 名称 | 化学人教版(2019)选择性必修2 2.2.2杂化轨道(共27张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 24.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-12-30 00:00:00 | ||
图片预览




文档简介
(共27张PPT)
杂化轨道
新人教高中化学选择性必修2第二章第二节
授课教师 teacher 授课教师 teacher
微观理解杂化
建立分析分子结构的思维模型
教学目标
素养
请迅速填写下表
分子 σ键数 孤电子对数 价层电子对数 VSEPR模型 分子空间构型
CH4
【温故知新】
【温故知新】
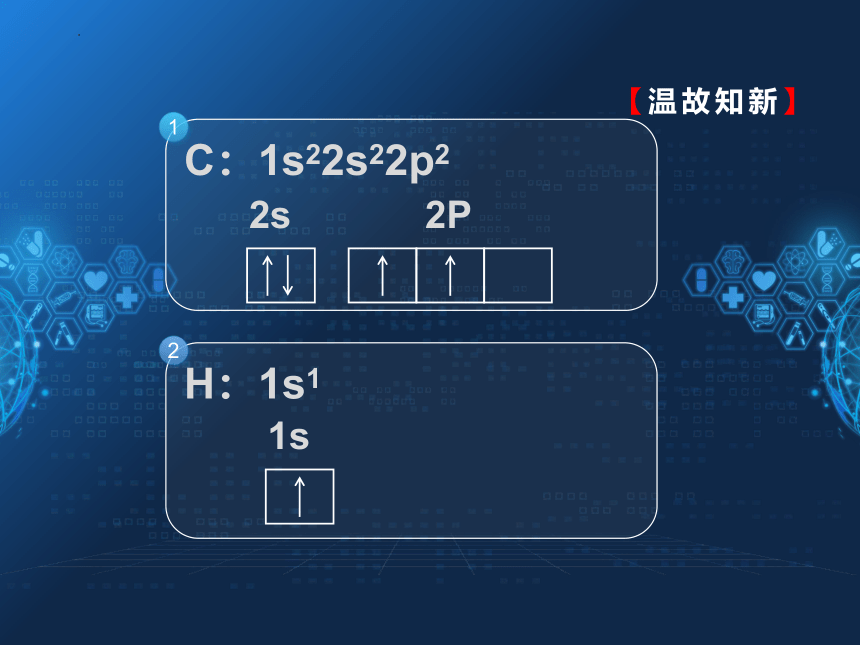
写出氢原子的核外电子排布式和轨道表示式
2
写出碳原子的核外电子排布式和轨道表示式
1
H:1s1
2
C:1s22s22p2
1
2s
2P
1s
【温故知新】
【温故知新】
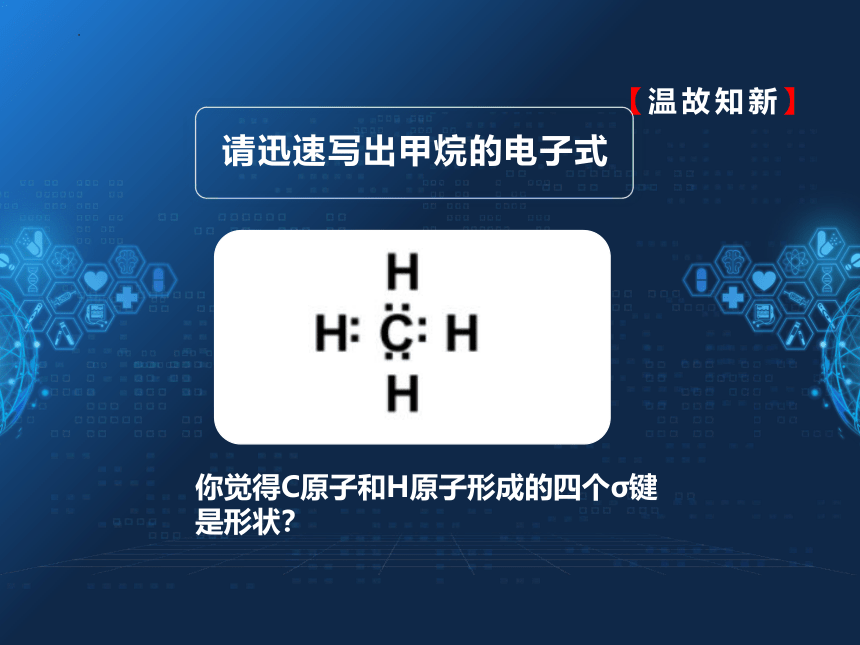
请迅速写出甲烷的电子式
你觉得C原子和H原子形成的四个σ键是形状?
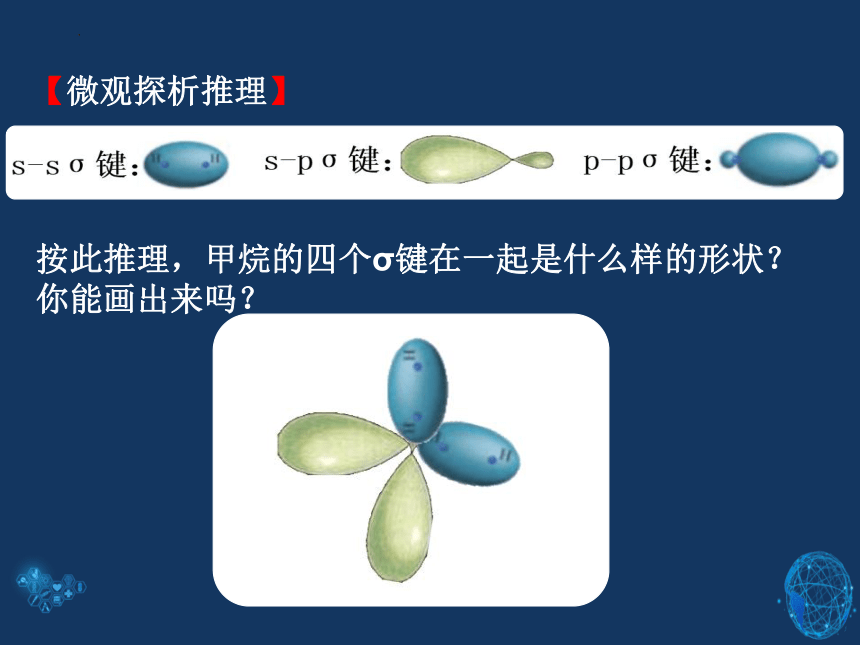
【微观探析推理】
按此推理,甲烷的四个σ键在一起是什么样的形状?你能画出来吗?
【微观探析推理】
正四面体,键角109°28′
四个键不一样,不是正四面体
推理错误!
哪是怎么回事呢?
【自主阅读归纳】
1、课本P47页第二段并自主归纳关键词
鲍林
C原子的1个2S和3个2P轨道混杂
轨道总数不变,能量相同,方向不同
SP3杂化
01
02
03
2、阅读课本P48页图2-15
【微观探析】
【微观探析】
2s
2P
C:1s22s22p2
基态
激发
2s
2P
激发态
杂化
SP3杂化轨道
【微观探析】
SP3杂化
【微观探析】
【微观探析】
【动画模拟】
【学生归纳】
【学生归纳】
【微观探析】
【VSEPR模型与杂化轨道理论的关联】
【VSEPR模型与杂化轨道理论的关联】
【自主归纳提升】
判断中心原子杂化轨道类型的方法?
(1)根据杂化轨道数目判断
杂化轨道数目=价层电子对数目=σ键电子对数目+中心原子的孤电子对数目,再由杂化轨道数目确定杂化轨道类型。
【自主归纳提升】
判断中心原子杂化轨道类型的方法?
(2)根据杂化轨道的空间分布判断
①若杂化轨道在空间的分布为正四面体或三角锥形,则中心原子发生sp3杂化。
②若杂化轨道在空间的分布呈平面三角形,则中心原子发生sp2杂化。
③若杂化轨道在空间的分布呈直线形,则中心原子发生sp杂化。
【自主归纳提升】
判断中心原子杂化轨道类型的方法?
(3)根据杂化轨道之间的夹角判断
①若杂化轨道之间的夹角为109°28′,则中心原子发生sp3杂化。
②若杂化轨道之间的夹角为120°,则中心原子发生sp2杂化。
③若杂化轨道之间的夹角为180°,则中心原子发生sp杂化。
【强化训练】
阅读课本P47第三自然段—P48页,结合图2-16,试着推理HCN的C原子杂化类型、空间结构和所有
共价键类型
【微观探究推理】
01
02
03
杂化轨道的理解
中心原子S轨道和P轨道杂化形成SP、SP2、SP3杂化
杂化轨道的特点
杂化后轨道不变,能量相同,方向不同,成键能力增强。杂化轨道在空间最小斥力,最大角度伸展。杂化轨道只用于形成σ键和容纳孤电子对。未参与杂化的轨道可形成π键。
杂化轨道与VSEPR模型的关联
杂化轨道数目=价层电子对数目=σ键电子对数目+中心原子的孤电子对数目
【课堂总结】
【课外作业】
制作分子空间结构模型,完成课本P50习题
杂化轨道
新人教高中化学选择性必修2第二章第二节
授课教师 teacher 授课教师 teacher
微观理解杂化
建立分析分子结构的思维模型
教学目标
素养
请迅速填写下表
分子 σ键数 孤电子对数 价层电子对数 VSEPR模型 分子空间构型
CH4
【温故知新】
【温故知新】
写出氢原子的核外电子排布式和轨道表示式
2
写出碳原子的核外电子排布式和轨道表示式
1
H:1s1
2
C:1s22s22p2
1
2s
2P
1s
【温故知新】
【温故知新】
请迅速写出甲烷的电子式
你觉得C原子和H原子形成的四个σ键是形状?
【微观探析推理】
按此推理,甲烷的四个σ键在一起是什么样的形状?你能画出来吗?
【微观探析推理】
正四面体,键角109°28′
四个键不一样,不是正四面体
推理错误!
哪是怎么回事呢?
【自主阅读归纳】
1、课本P47页第二段并自主归纳关键词
鲍林
C原子的1个2S和3个2P轨道混杂
轨道总数不变,能量相同,方向不同
SP3杂化
01
02
03
2、阅读课本P48页图2-15
【微观探析】
【微观探析】
2s
2P
C:1s22s22p2
基态
激发
2s
2P
激发态
杂化
SP3杂化轨道
【微观探析】
SP3杂化
【微观探析】
【微观探析】
【动画模拟】
【学生归纳】
【学生归纳】
【微观探析】
【VSEPR模型与杂化轨道理论的关联】
【VSEPR模型与杂化轨道理论的关联】
【自主归纳提升】
判断中心原子杂化轨道类型的方法?
(1)根据杂化轨道数目判断
杂化轨道数目=价层电子对数目=σ键电子对数目+中心原子的孤电子对数目,再由杂化轨道数目确定杂化轨道类型。
【自主归纳提升】
判断中心原子杂化轨道类型的方法?
(2)根据杂化轨道的空间分布判断
①若杂化轨道在空间的分布为正四面体或三角锥形,则中心原子发生sp3杂化。
②若杂化轨道在空间的分布呈平面三角形,则中心原子发生sp2杂化。
③若杂化轨道在空间的分布呈直线形,则中心原子发生sp杂化。
【自主归纳提升】
判断中心原子杂化轨道类型的方法?
(3)根据杂化轨道之间的夹角判断
①若杂化轨道之间的夹角为109°28′,则中心原子发生sp3杂化。
②若杂化轨道之间的夹角为120°,则中心原子发生sp2杂化。
③若杂化轨道之间的夹角为180°,则中心原子发生sp杂化。
【强化训练】
阅读课本P47第三自然段—P48页,结合图2-16,试着推理HCN的C原子杂化类型、空间结构和所有
共价键类型
【微观探究推理】
01
02
03
杂化轨道的理解
中心原子S轨道和P轨道杂化形成SP、SP2、SP3杂化
杂化轨道的特点
杂化后轨道不变,能量相同,方向不同,成键能力增强。杂化轨道在空间最小斥力,最大角度伸展。杂化轨道只用于形成σ键和容纳孤电子对。未参与杂化的轨道可形成π键。
杂化轨道与VSEPR模型的关联
杂化轨道数目=价层电子对数目=σ键电子对数目+中心原子的孤电子对数目
【课堂总结】
【课外作业】
制作分子空间结构模型,完成课本P50习题
