第五章 燃料 期末练习题(含答案)2023—2024学年科粤版(2012)化学九年级上册
文档属性
| 名称 | 第五章 燃料 期末练习题(含答案)2023—2024学年科粤版(2012)化学九年级上册 |

|
|
| 格式 | doc | ||
| 文件大小 | 950.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 科粤版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-12-30 00:00:00 | ||
图片预览



文档简介
第五章 燃料 期末练习题含答案2023—2024学年科粤版(2012)化学九年级上册
科粤版(2012)第五章 燃料
一、选择题。(16题)
1、长征5号运载火箭中采用了液氢﹣液氧发动机,关于选用液氢和液氧的说法中,不正确的是( )
A.与气态相比,液氢和液氧的分子间隔更小,节约空间
B.氢气、氧气经液化后,其化学性质没有发生改变
C.汽化后,产生的氢气和氧气都是可燃物
D.燃烧反应的产物是水,不会污染环境
2、“碳家族”的成员很多,用途很广。下列说法正确的是( )
A.石墨不具有导电性 B.C60单质是由碳原子直接构成的
C.活性炭具有吸附性 D.金刚石和石墨里碳原子的排列方式相同
3、成都以“碳达峰、碳中和”为目标,引领城市绿色低碳发展。下列做法利于实现此目标的是( )
A.石油炼制 B.太阳能发电 C.燃煤脱硫 D.酒精作燃料
4、逻辑推理是一种重要的化学思维方法,下列推理合理的是( )
A.单质由同种元素组成,则由同种元素组成的物质一定是单质
B.催化剂在反应前后质量不变,因此反应前后质量不变的物质一定是催化剂
C.点燃可燃性气体前需检验纯度,则点燃甲烷气体前需要验纯
D.同种元素的原子质子数相同,所以具有相同质子数的粒子一定是同种元素
5、“安全重于泰山”,下列有关说法正确的是( )
A.面粉厂周围不需要严禁烟火 B.天然气报警器应安装在灶台下方
C.冬季用炭火取暖需关闭门窗 D.档案失火用二氧化碳灭火器扑灭
6、我国发射的“天宫一号”目标飞行器和“神舟八号”飞船,实施了首次空间飞行器无人交会对接试验.“天宫一号”飞行器升空所用燃料之一为液氢.下列有关氢气的说法,你认为不正确的是( )
A.氢气是一种无色、无臭、难溶于水的气体
B.氢气在空气中燃烧时,产生淡蓝色火焰
C.氢气和液氢的化学性质不同
D.点燃用排水法收集的一试管氢气,若发出尖锐的爆鸣声,则表明氢气不纯
7、“见著之微,见微之著”是化学的思维方法。下图为金刚石、石墨、足球烯的结构示意图。下列说法正确的是( )
A.它们都是由原子直接构成的
B.构成它们的原子的种类和大小都不同
C.构成它们的原子种类相同,但原子的排列方式不同
D.只有石墨和足球烯能在氧气中燃烧,金刚石不能燃烧
8、下面是实验室制取二氧化碳和探究二氧化碳性质的实验,其中错误的是( )
A.图甲中装置a是长颈漏斗
B.图乙中用点燃的火柴放在集气瓶口来验满
C.图丙中二氧化碳使蜡烛火焰自上而下熄灭
D.图丁中将收集到的二氧化碳通入澄清石灰水会发现溶液变浑浊
9、下列不属于化石能源的是( )
A.煤 B.风能 C.石油 D.天然气
10、可用同一化学原理解释的现象是( )
①久置的石灰水,液面上出现一层硬壳状薄膜
②向澄清石灰水中,通过吸管不断吹入人体呼出的气体
③为了使石灰浆刷过的墙壁快点晾干,在室内生起一盆炭火开始时墙壁潮湿
④向紫色石蕊试液中通入CO2气体,试液变红
A.①②③ B.①②④ C.①③④ D.②③④
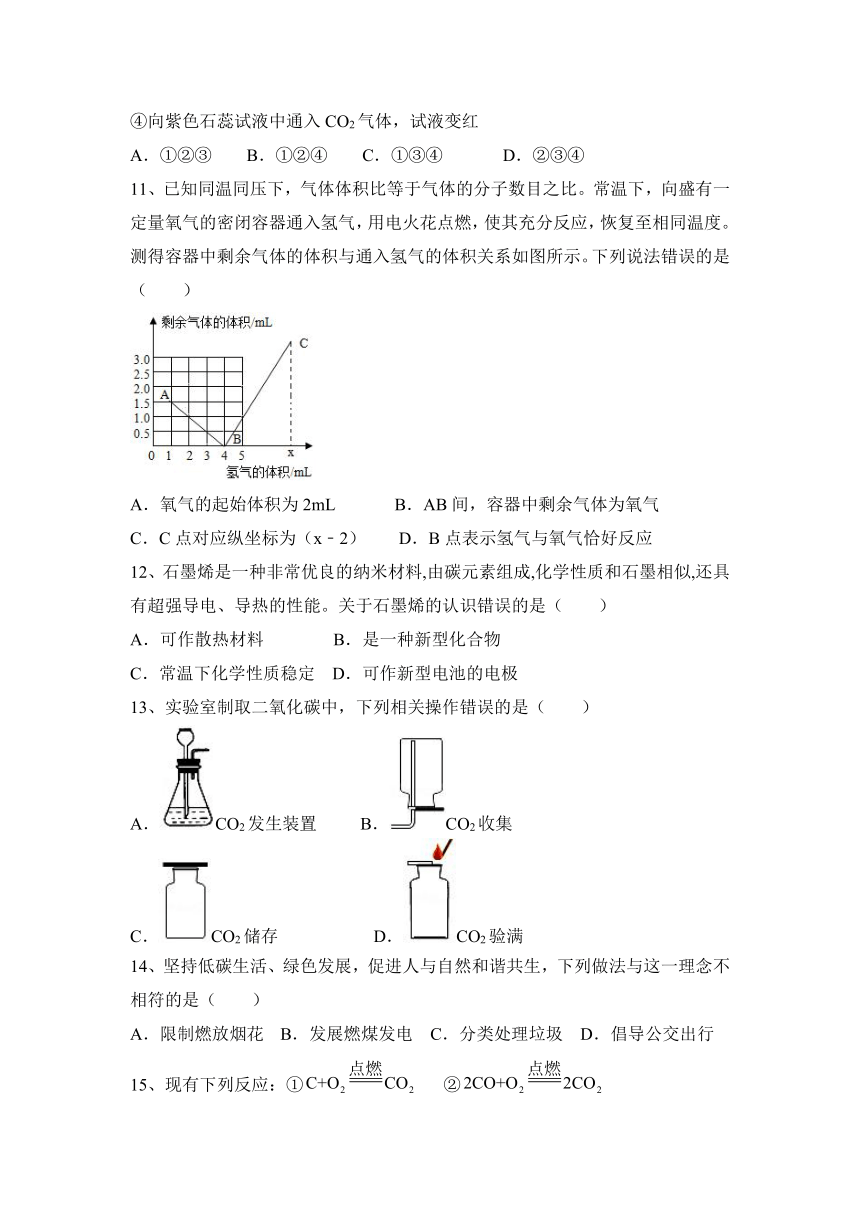
11、已知同温同压下,气体体积比等于气体的分子数目之比。常温下,向盛有一定量氧气的密闭容器通入氢气,用电火花点燃,使其充分反应,恢复至相同温度。测得容器中剩余气体的体积与通入氢气的体积关系如图所示。下列说法错误的是( )
A.氧气的起始体积为2mL B.AB间,容器中剩余气体为氧气
C.C点对应纵坐标为(x﹣2) D.B点表示氢气与氧气恰好反应
12、石墨烯是一种非常优良的纳米材料,由碳元素组成,化学性质和石墨相似,还具有超强导电、导热的性能。关于石墨烯的认识错误的是( )
A.可作散热材料 B.是一种新型化合物
C.常温下化学性质稳定 D.可作新型电池的电极
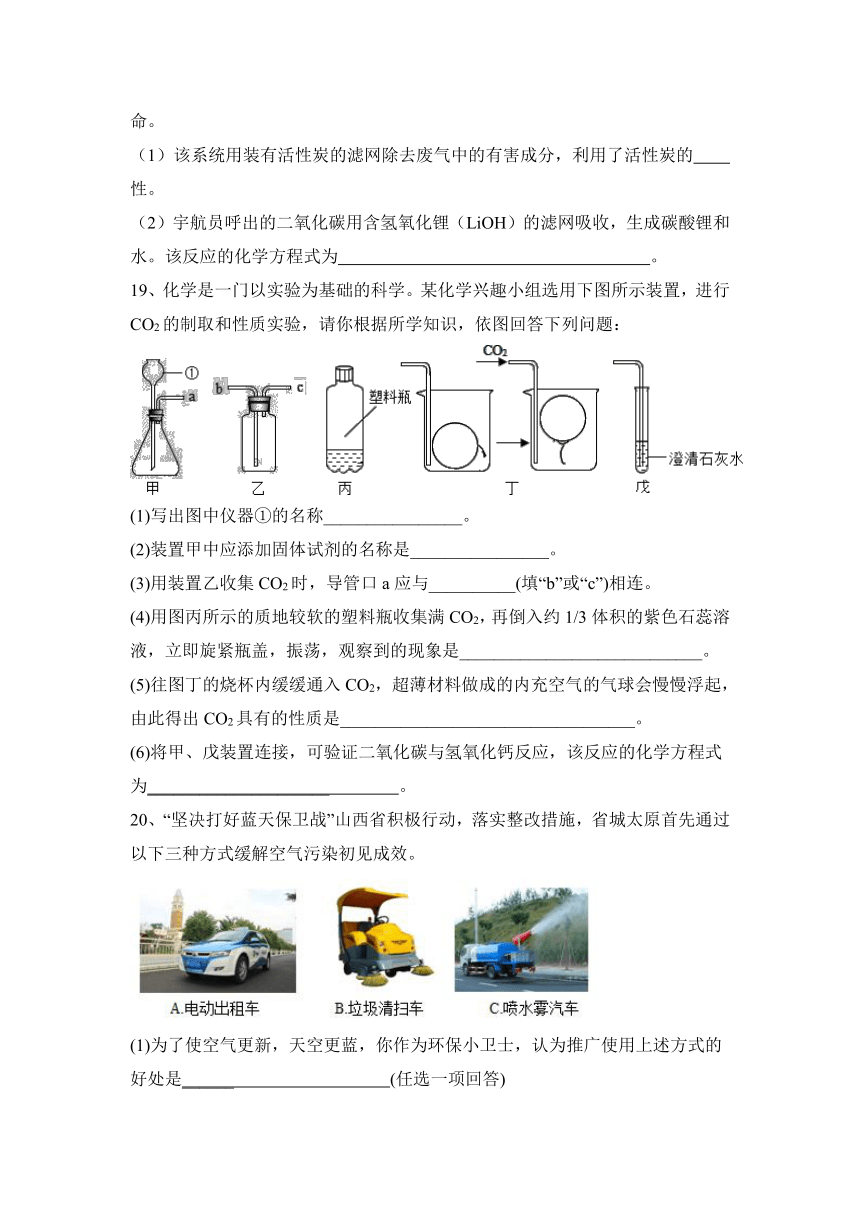
13、实验室制取二氧化碳中,下列相关操作错误的是( )
A.CO2发生装置 B.CO2收集
C.CO2储存 D.CO2验满
14、坚持低碳生活、绿色发展,促进人与自然和谐共生,下列做法与这一理念不相符的是( )
A.限制燃放烟花 B.发展燃煤发电 C.分类处理垃圾 D.倡导公交出行
15、现有下列反应:① ②
③④。
其中适用于实验室制取二氧化碳的是( )
A.①②③④ B.①③④ C.①④ D.④
16、2020年6月23日,我国“长三乙”火箭将第55颗北斗卫星送入预定轨道,完成北斗卫星导航系统的组网。该火箭第三级的推进剂为液氢和液氧组合,下列说法正确的是( )
A.氢气液化过程中,氢分子之间的间隔保持不变
B.分离液态空气得到液态氧气的过程中,氧分子静止不动
C.液氧变成气态氧时,放出热量
D.氢气与氧气反应放出热量为火发射提供了动力
二、填空题。
17、认真阅读下列材料,回答有关问题:
北京时间 2022 年 9 月 2 日 0 时 33 分,经过约 6 小时的出舱活动,神舟十四号航天员陈冬、刘洋、蔡旭哲密切协同,完成出舱活动期间全部既定任务,出舱活动取得圆满成功。航天员佩戴头盔的面窗两层之间充有高纯氮气,该氮气是通过分离液态空气法分离出氮气。航天员呼吸的氧气有三种来源:第一种主要是携带的纯氧氧气瓶,第二种是利用电解术的方式产生的氧气和氢气,氧气可以供宇航员呼吸,而氢气还可以作为燃料。第三种是利用固体氧气发生器产生的氧气。
(1)分离液态空气法分离出氮气的过程属于_________变化(填“物理”或“化学”)。
(2)利用电解水的方式产生的氧气和氢气的化学反应属于_________反应(填“化合”或“分解”)。
(3)氢气可以作为燃料,是利用氢气的_________性。
18、2022年6月5日,中国神舟十四号载人飞船成功发射。三位宇航员将在太空进行长达6个月的科学研究。宇航员舱外服的废气处理系统保障着宇航员的生命。
(1)该系统用装有活性炭的滤网除去废气中的有害成分,利用了活性炭的 性。
(2)宇航员呼出的二氧化碳用含氢氧化锂(LiOH)的滤网吸收,生成碳酸锂和水。该反应的化学方程式为 。
19、化学是一门以实验为基础的科学。某化学兴趣小组选用下图所示装置,进行CO2的制取和性质实验,请你根据所学知识,依图回答下列问题:
(1)写出图中仪器①的名称________________。
(2)装置甲中应添加固体试剂的名称是________________。
(3)用装置乙收集CO2时,导管口a应与__________(填“b”或“c”)相连。
(4)用图丙所示的质地较软的塑料瓶收集满CO2,再倒入约1/3体积的紫色石蕊溶液,立即旋紧瓶盖,振荡,观察到的现象是____________________________。
(5)往图丁的烧杯内缓缓通入CO2,超薄材料做成的内充空气的气球会慢慢浮起,由此得出CO2具有的性质是__________________________________。
(6)将甲、戊装置连接,可验证二氧化碳与氢氧化钙反应,该反应的化学方程式为_____________________ 。
20、“坚决打好蓝天保卫战”山西省积极行动,落实整改措施,省城太原首先通过以下三种方式缓解空气污染初见成效。
(1)为了使空气更新,天空更蓝,你作为环保小卫士,认为推广使用上述方式的好处是______ (任选一项回答)
(2)空气污染严重损害人体健康,影响作物生长,破坏生态平衡引起空气污染的有害气体种类很多,请举一例 _______________(用化学式表示)
(3)你认为改善空气质量的措施正确的是_____________
a.推广使用新能源
b.加强企业排污管理
c.雾霾多发天气,实行私家车限号出行。
21、(1)I、能源利用和环境保护是人类共同关注的问题。
化石燃料主要包括煤、 和天然气。
(2)化石燃料燃烧产生二氧化碳气体,经过绿色植物的光合作用生成淀粉,淀粉在人体内变成葡萄糖(C6H12O6),葡萄糖在酶的催化作用下发生缓慢氧化生成二氧化碳和水,同时放出能量,写出葡萄糖与氧气发生缓慢氧化反应的化学方程式: 。
(3)由上可知,减小温室效应的主要途径有:① ,② (写两条)。
(4)Ⅱ、化学与生活息息相关。根据所学知识回答下列问题:
为保证身体健康,在使用饮用水前,我们一般可以用 的方法降低水的硬度。
(5)在遇到紧急火灾时,我们常常会用水来扑灭,这其中的灭火原理是 。
(6)小朋友们将燃放的鞭炮扔到下水道的做法是危险的。有机物在密闭的环境里发酵可以产生沼气,沼气遇到明火有可能发生爆炸。沼气的主要成分是 。
(7)日常饮食要注意营养均衡,米饭、面条为我们身体提供了能量保障,其中包含的主要营养素是 。
三、推断题。
22、已知:A是相对分子质量最小的氧化物,D是最简单的有机物,也是天然气中最主要的成分。请分析A、B、C、D、E五种物质之间的变化关系,回答有关问题。
(1)请写出D、E的化学式D_________、E__________。
(2)请写出A→B+C的化学方程式:______________________;该反应的基本类型是_________。
四、综合应用题。
23、碳是形成化合物种类最多的元素,含碳物质是中学化学研究的重要内容.
(1)碳元素的化学性质与其原子的________ 关系密切。
(2)如图1为元素周期表中的一格,下列说法正确的是________(填标号).
A 碳元素属于非金属元素
B 碳原子核内质子数为6
C 碳元素的原子结构示意图为
D碳的相对原子质量为12.01g
(3)甲、乙、丙都是常见含有碳元素的物质,它们之间有如图所示的转化关系(部分物质和反应条件已略去),其中甲和丙都可以作燃料,乙和丙中所含的元素种类相同,乙能引起“温室效应”,则乙的化学式为:________,甲转化为丙的途径有多种,写出通过化合反应的方式,甲转化为丙的化学方程式为: ________ ,从微观的角度解释乙、丙性质有差异的原因是: ________ 。
(4)实验室用图3装置来制取二氧化碳,检查该装置的气密性的方法是:将该装置中导气管中的橡胶管用弹簧夹夹住,往长颈漏斗中注入水至液面高出漏斗颈的下端管口,若能观察到________ 现象,即可证明装置不漏气,实验室确定气体发生装置时应考虑的因素是________ 。
(5)称取12.5g石灰石(主要成份CaCO3,杂质不参加反应)放入烧杯中,向其中加入足量的稀盐酸,完全反应结束后放出4.4g气体,试计算石灰石中杂质的质量分数______。
五、科普阅读题。
24、阅读下列科普短文,回答问题。
2021年,考古学家利用碳-14断代法初步判定三星堆4号坑距今约3200至3000年。碳-14原子核中含6个质子与8个中子。生物死后体内的碳-14会不断衰变,碳-14原子核中1个中子变成1个质子,形成新的原子核。对比生物体内生前、死后碳-14的含量,可推算出其所属年代。
国家速滑馆利用CO2跨临界直冷制冰,就是将气态CO2通过加温加压形成超临界CO2流体(介于气态和液态之间的一种新的状态,兼有气体和液体的性质),后变为液态CO2,再变成气态完成制冰的过程。工业上可用CO2为原料合成燃料甲烷、甲醇(CH3OH),氮肥尿素等,合成尿素的反应:。
(1)碳-14原子核外电子数为_________,其衰变形成的新原子属于_________元素(填元素符号)。
(2)超临界CO2流体是______(填“纯净物”“混合物”)。液态CO2能用于制冰的原因是________ 。
(3)甲醇充分燃烧的产物为______________。
(4)合成尿素时,参与反应的CO2与NH3的质量比为__________。尿素含氮量高,其氮元素的质量分数为_________(保留小数点后一位)。
六、计算类综合应用题。
25、碳是重要的生命元素,碳及其化合物的综合利用使世界变得更加绚丽多彩。
Ⅰ碳的多样性
(1)金刚石和石墨的组成元素相同,碳原子的排列方式不同,导致_______。(填具体的物理性质)
(2)从石墨中分离出的单层石墨片(石墨烯)是目前人工制得的最薄材料,单层石墨片属于_______(填“单质”或“化合物”)。
Ⅱ“碳中和”的实现
“碳中和”是指一定时间内CO2的排放量与吸收量基本相当。CO2的捕集、利用是实现“碳中和”的重要途径。我国力争在2060年前实现“碳中和”,体现了中国对解决全球气候问题的大国担当。
(3)大气中CO2的过度排放会造成________的加剧。
(4)工业生产中产生的CO2经吸收剂处理可实现CO2的捕集。写出NaOH溶液吸收CO2生成NaHCO3的化学方程式:_______ 。
(5)“液态太阳燃料合成技术”如图1所示。
①从能源和环境角度说明该合成技术的优点:________ 。
②在合成工厂中,氢气与CO2在一定条件下反应转化为甲醇(CH3OH)和相对分子质量最小的氧化物。写出此反应的化学方程式:_______ 。
(6)CO2与H2在一定条件下转化为CH4(反应过程如图2所示,虚线处部分中间产物略去),可实现CO2的再利用。
①该反应中MgO的作用是_________。
②用该方法制取1t甲烷,则参与反应的二氧化碳的质量为多少?(写出计算过程)______。
第五章 燃料 期末练习题含答案2023—2024学年科粤版(2012)化学九年级上册
科粤版(2012)第五章 燃料
一、选择题。(16题)
1、长征5号运载火箭中采用了液氢﹣液氧发动机,关于选用液氢和液氧的说法中,不正确的是( )
A.与气态相比,液氢和液氧的分子间隔更小,节约空间
B.氢气、氧气经液化后,其化学性质没有发生改变
C.汽化后,产生的氢气和氧气都是可燃物
D.燃烧反应的产物是水,不会污染环境
【答案】C
2、“碳家族”的成员很多,用途很广。下列说法正确的是( )
A.石墨不具有导电性 B.C60单质是由碳原子直接构成的
C.活性炭具有吸附性 D.金刚石和石墨里碳原子的排列方式相同
【答案】C
3、成都以“碳达峰、碳中和”为目标,引领城市绿色低碳发展。下列做法利于实现此目标的是( )
A.石油炼制 B.太阳能发电 C.燃煤脱硫 D.酒精作燃料
【答案】B
4、逻辑推理是一种重要的化学思维方法,下列推理合理的是( )
A.单质由同种元素组成,则由同种元素组成的物质一定是单质
B.催化剂在反应前后质量不变,因此反应前后质量不变的物质一定是催化剂
C.点燃可燃性气体前需检验纯度,则点燃甲烷气体前需要验纯
D.同种元素的原子质子数相同,所以具有相同质子数的粒子一定是同种元素
【答案】C
5、“安全重于泰山”,下列有关说法正确的是( )
A.面粉厂周围不需要严禁烟火 B.天然气报警器应安装在灶台下方
C.冬季用炭火取暖需关闭门窗 D.档案失火用二氧化碳灭火器扑灭
【答案】D
6、我国发射的“天宫一号”目标飞行器和“神舟八号”飞船,实施了首次空间飞行器无人交会对接试验.“天宫一号”飞行器升空所用燃料之一为液氢.下列有关氢气的说法,你认为不正确的是( )
A.氢气是一种无色、无臭、难溶于水的气体
B.氢气在空气中燃烧时,产生淡蓝色火焰
C.氢气和液氢的化学性质不同
D.点燃用排水法收集的一试管氢气,若发出尖锐的爆鸣声,则表明氢气不纯
【答案】C
7、“见著之微,见微之著”是化学的思维方法。下图为金刚石、石墨、足球烯的结构示意图。下列说法正确的是( )
A.它们都是由原子直接构成的
B.构成它们的原子的种类和大小都不同
C.构成它们的原子种类相同,但原子的排列方式不同
D.只有石墨和足球烯能在氧气中燃烧,金刚石不能燃烧
【答案】C
8、下面是实验室制取二氧化碳和探究二氧化碳性质的实验,其中错误的是( )
A.图甲中装置a是长颈漏斗
B.图乙中用点燃的火柴放在集气瓶口来验满
C.图丙中二氧化碳使蜡烛火焰自上而下熄灭
D.图丁中将收集到的二氧化碳通入澄清石灰水会发现溶液变浑浊
【答案】C
9、下列不属于化石能源的是( )
A.煤 B.风能 C.石油 D.天然气
【答案】B
10、可用同一化学原理解释的现象是( )
①久置的石灰水,液面上出现一层硬壳状薄膜
②向澄清石灰水中,通过吸管不断吹入人体呼出的气体
③为了使石灰浆刷过的墙壁快点晾干,在室内生起一盆炭火开始时墙壁潮湿
④向紫色石蕊试液中通入CO2气体,试液变红
A.①②③ B.①②④ C.①③④ D.②③④
【答案】A
11、已知同温同压下,气体体积比等于气体的分子数目之比。常温下,向盛有一定量氧气的密闭容器通入氢气,用电火花点燃,使其充分反应,恢复至相同温度。测得容器中剩余气体的体积与通入氢气的体积关系如图所示。下列说法错误的是( )
A.氧气的起始体积为2mL B.AB间,容器中剩余气体为氧气
C.C点对应纵坐标为(x﹣2) D.B点表示氢气与氧气恰好反应
【答案】C
12、石墨烯是一种非常优良的纳米材料,由碳元素组成,化学性质和石墨相似,还具有超强导电、导热的性能。关于石墨烯的认识错误的是( )
A.可作散热材料 B.是一种新型化合物
C.常温下化学性质稳定 D.可作新型电池的电极
【答案】B
13、实验室制取二氧化碳中,下列相关操作错误的是( )
A.CO2发生装置 B.CO2收集
C.CO2储存 D.CO2验满
【答案】B
14、坚持低碳生活、绿色发展,促进人与自然和谐共生,下列做法与这一理念不相符的是( )
A.限制燃放烟花 B.发展燃煤发电 C.分类处理垃圾 D.倡导公交出行
【答案】B
15、现有下列反应:① ②
③④。
其中适用于实验室制取二氧化碳的是( )
A.①②③④ B.①③④ C.①④ D.④
【答案】D
16、2020年6月23日,我国“长三乙”火箭将第55颗北斗卫星送入预定轨道,完成北斗卫星导航系统的组网。该火箭第三级的推进剂为液氢和液氧组合,下列说法正确的是( )
A.氢气液化过程中,氢分子之间的间隔保持不变
B.分离液态空气得到液态氧气的过程中,氧分子静止不动
C.液氧变成气态氧时,放出热量
D.氢气与氧气反应放出热量为火发射提供了动力
【答案】D
二、填空题。
17、认真阅读下列材料,回答有关问题:
北京时间 2022 年 9 月 2 日 0 时 33 分,经过约 6 小时的出舱活动,神舟十四号航天员陈冬、刘洋、蔡旭哲密切协同,完成出舱活动期间全部既定任务,出舱活动取得圆满成功。航天员佩戴头盔的面窗两层之间充有高纯氮气,该氮气是通过分离液态空气法分离出氮气。航天员呼吸的氧气有三种来源:第一种主要是携带的纯氧氧气瓶,第二种是利用电解术的方式产生的氧气和氢气,氧气可以供宇航员呼吸,而氢气还可以作为燃料。第三种是利用固体氧气发生器产生的氧气。
(1)分离液态空气法分离出氮气的过程属于_________变化(填“物理”或“化学”)。
(2)利用电解水的方式产生的氧气和氢气的化学反应属于_________反应(填“化合”或“分解”)。
(3)氢气可以作为燃料,是利用氢气的_________性。
【答案】(1)物理 (2)分解 (3)可燃
18、2022年6月5日,中国神舟十四号载人飞船成功发射。三位宇航员将在太空进行长达6个月的科学研究。宇航员舱外服的废气处理系统保障着宇航员的生命。
(1)该系统用装有活性炭的滤网除去废气中的有害成分,利用了活性炭的 性。
(2)宇航员呼出的二氧化碳用含氢氧化锂(LiOH)的滤网吸收,生成碳酸锂和水。该反应的化学方程式为 。
【答案】(1)吸附; (2)CO2+2LiOH═Li2CO3+H2O。
19、化学是一门以实验为基础的科学。某化学兴趣小组选用下图所示装置,进行CO2的制取和性质实验,请你根据所学知识,依图回答下列问题:
(1)写出图中仪器①的名称________________。
(2)装置甲中应添加固体试剂的名称是________________。
(3)用装置乙收集CO2时,导管口a应与__________(填“b”或“c”)相连。
(4)用图丙所示的质地较软的塑料瓶收集满CO2,再倒入约1/3体积的紫色石蕊溶液,立即旋紧瓶盖,振荡,观察到的现象是____________________________。
(5)往图丁的烧杯内缓缓通入CO2,超薄材料做成的内充空气的气球会慢慢浮起,由此得出CO2具有的性质是__________________________________。
(6)将甲、戊装置连接,可验证二氧化碳与氢氧化钙反应,该反应的化学方程式为_____________________ 。
【答案】(1)长颈漏斗; (2)大理石等; (3)b;
(4)溶液变红色,塑料瓶变瘪;
(5)二氧化碳的密度比空气的大;
(6)Ca(OH)2+CO2=CaCO3↓+H2O。
20、“坚决打好蓝天保卫战”山西省积极行动,落实整改措施,省城太原首先通过以下三种方式缓解空气污染初见成效。
(1)为了使空气更新,天空更蓝,你作为环保小卫士,认为推广使用上述方式的好处是______ (任选一项回答)
(2)空气污染严重损害人体健康,影响作物生长,破坏生态平衡引起空气污染的有害气体种类很多,请举一例 _______________(用化学式表示)
(3)你认为改善空气质量的措施正确的是_____________
a.推广使用新能源
b.加强企业排污管理
c.雾霾多发天气,实行私家车限号出行。
【答案】减少化石燃料燃烧,减少空气污染(答案合理即可)
SO2(合理即可) abc
21、(1)I、能源利用和环境保护是人类共同关注的问题。
化石燃料主要包括煤、 和天然气。
(2)化石燃料燃烧产生二氧化碳气体,经过绿色植物的光合作用生成淀粉,淀粉在人体内变成葡萄糖(C6H12O6),葡萄糖在酶的催化作用下发生缓慢氧化生成二氧化碳和水,同时放出能量,写出葡萄糖与氧气发生缓慢氧化反应的化学方程式: 。
(3)由上可知,减小温室效应的主要途径有:① ,② (写两条)。
(4)Ⅱ、化学与生活息息相关。根据所学知识回答下列问题:
为保证身体健康,在使用饮用水前,我们一般可以用 的方法降低水的硬度。
(5)在遇到紧急火灾时,我们常常会用水来扑灭,这其中的灭火原理是 。
(6)小朋友们将燃放的鞭炮扔到下水道的做法是危险的。有机物在密闭的环境里发酵可以产生沼气,沼气遇到明火有可能发生爆炸。沼气的主要成分是 。
(7)日常饮食要注意营养均衡,米饭、面条为我们身体提供了能量保障,其中包含的主要营养素是 。
【答案】(1)石油
(2)C6H12O6+6O2===6CO2+6H2O
(3)骑自行车上学(合理即可);植树造林(合理即可)
(4)煮沸 (5)降低温度至可燃物的着火点以下
(6)甲烷/CH4 (7)糖类
三、推断题。
22、已知:A是相对分子质量最小的氧化物,D是最简单的有机物,也是天然气中最主要的成分。请分析A、B、C、D、E五种物质之间的变化关系,回答有关问题。
(1)请写出D、E的化学式D_________、E__________。
(2)请写出A→B+C的化学方程式:______________________;该反应的基本类型是_________。
【答案】CH4 CO2 2H2O2H2↑+ O2↑ 分解反应
四、综合应用题。
23、碳是形成化合物种类最多的元素,含碳物质是中学化学研究的重要内容.
(1)碳元素的化学性质与其原子的________ 关系密切。
(2)如图1为元素周期表中的一格,下列说法正确的是________(填标号).
A 碳元素属于非金属元素
B 碳原子核内质子数为6
C 碳元素的原子结构示意图为
D碳的相对原子质量为12.01g
(3)甲、乙、丙都是常见含有碳元素的物质,它们之间有如图所示的转化关系(部分物质和反应条件已略去),其中甲和丙都可以作燃料,乙和丙中所含的元素种类相同,乙能引起“温室效应”,则乙的化学式为:________,甲转化为丙的途径有多种,写出通过化合反应的方式,甲转化为丙的化学方程式为: ________ ,从微观的角度解释乙、丙性质有差异的原因是: ________ 。
(4)实验室用图3装置来制取二氧化碳,检查该装置的气密性的方法是:将该装置中导气管中的橡胶管用弹簧夹夹住,往长颈漏斗中注入水至液面高出漏斗颈的下端管口,若能观察到________ 现象,即可证明装置不漏气,实验室确定气体发生装置时应考虑的因素是________ 。
(5)称取12.5g石灰石(主要成份CaCO3,杂质不参加反应)放入烧杯中,向其中加入足量的稀盐酸,完全反应结束后放出4.4g气体,试计算石灰石中杂质的质量分数______。
【答案】(1)最外层电子数 (2)AB
(3)CO2 二氧化碳和一氧化碳的分子构成不同
(4)长颈漏斗和试管中出现液面差 反应物状态和反应条件 (5)20%
五、科普阅读题。
24、阅读下列科普短文,回答问题。
2021年,考古学家利用碳-14断代法初步判定三星堆4号坑距今约3200至3000年。碳-14原子核中含6个质子与8个中子。生物死后体内的碳-14会不断衰变,碳-14原子核中1个中子变成1个质子,形成新的原子核。对比生物体内生前、死后碳-14的含量,可推算出其所属年代。
国家速滑馆利用CO2跨临界直冷制冰,就是将气态CO2通过加温加压形成超临界CO2流体(介于气态和液态之间的一种新的状态,兼有气体和液体的性质),后变为液态CO2,再变成气态完成制冰的过程。工业上可用CO2为原料合成燃料甲烷、甲醇(CH3OH),氮肥尿素等,合成尿素的反应:。
(1)碳-14原子核外电子数为_________,其衰变形成的新原子属于_________元素(填元素符号)。
(2)超临界CO2流体是______(填“纯净物”“混合物”)。液态CO2能用于制冰的原因是________ 。
(3)甲醇充分燃烧的产物为______________。
(4)合成尿素时,参与反应的CO2与NH3的质量比为__________。尿素含氮量高,其氮元素的质量分数为_________(保留小数点后一位)。
【答案】(1) 6 N
(2) 纯净物 液态二氧化碳汽化吸热,能使周围温度降低
(3)二氧化碳和水 (4) 22:17 46.7%
六、计算类综合应用题。
25、碳是重要的生命元素,碳及其化合物的综合利用使世界变得更加绚丽多彩。
Ⅰ碳的多样性
(1)金刚石和石墨的组成元素相同,碳原子的排列方式不同,导致_______。(填具体的物理性质)
(2)从石墨中分离出的单层石墨片(石墨烯)是目前人工制得的最薄材料,单层石墨片属于_______(填“单质”或“化合物”)。
Ⅱ“碳中和”的实现
“碳中和”是指一定时间内CO2的排放量与吸收量基本相当。CO2的捕集、利用是实现“碳中和”的重要途径。我国力争在2060年前实现“碳中和”,体现了中国对解决全球气候问题的大国担当。
(3)大气中CO2的过度排放会造成________的加剧。
(4)工业生产中产生的CO2经吸收剂处理可实现CO2的捕集。写出NaOH溶液吸收CO2生成NaHCO3的化学方程式:_______ 。
(5)“液态太阳燃料合成技术”如图1所示。
①从能源和环境角度说明该合成技术的优点:________ 。
②在合成工厂中,氢气与CO2在一定条件下反应转化为甲醇(CH3OH)和相对分子质量最小的氧化物。写出此反应的化学方程式:_______ 。
(6)CO2与H2在一定条件下转化为CH4(反应过程如图2所示,虚线处部分中间产物略去),可实现CO2的再利用。
①该反应中MgO的作用是_________。
②用该方法制取1t甲烷,则参与反应的二氧化碳的质量为多少?(写出计算过程)______。
【答案】(1)金刚石硬度大,而石墨比较软(合理即可)
(2)单质 (3)温室效应 (4)
(5) 节约能源,有效缓解温室效应
(6) 催化作用 2.75t
设:参与反应的二氧化碳的质量为x
答:参与反应的二氧化碳的质量为2.75t。
科粤版(2012)第五章 燃料
一、选择题。(16题)
1、长征5号运载火箭中采用了液氢﹣液氧发动机,关于选用液氢和液氧的说法中,不正确的是( )
A.与气态相比,液氢和液氧的分子间隔更小,节约空间
B.氢气、氧气经液化后,其化学性质没有发生改变
C.汽化后,产生的氢气和氧气都是可燃物
D.燃烧反应的产物是水,不会污染环境
2、“碳家族”的成员很多,用途很广。下列说法正确的是( )
A.石墨不具有导电性 B.C60单质是由碳原子直接构成的
C.活性炭具有吸附性 D.金刚石和石墨里碳原子的排列方式相同
3、成都以“碳达峰、碳中和”为目标,引领城市绿色低碳发展。下列做法利于实现此目标的是( )
A.石油炼制 B.太阳能发电 C.燃煤脱硫 D.酒精作燃料
4、逻辑推理是一种重要的化学思维方法,下列推理合理的是( )
A.单质由同种元素组成,则由同种元素组成的物质一定是单质
B.催化剂在反应前后质量不变,因此反应前后质量不变的物质一定是催化剂
C.点燃可燃性气体前需检验纯度,则点燃甲烷气体前需要验纯
D.同种元素的原子质子数相同,所以具有相同质子数的粒子一定是同种元素
5、“安全重于泰山”,下列有关说法正确的是( )
A.面粉厂周围不需要严禁烟火 B.天然气报警器应安装在灶台下方
C.冬季用炭火取暖需关闭门窗 D.档案失火用二氧化碳灭火器扑灭
6、我国发射的“天宫一号”目标飞行器和“神舟八号”飞船,实施了首次空间飞行器无人交会对接试验.“天宫一号”飞行器升空所用燃料之一为液氢.下列有关氢气的说法,你认为不正确的是( )
A.氢气是一种无色、无臭、难溶于水的气体
B.氢气在空气中燃烧时,产生淡蓝色火焰
C.氢气和液氢的化学性质不同
D.点燃用排水法收集的一试管氢气,若发出尖锐的爆鸣声,则表明氢气不纯
7、“见著之微,见微之著”是化学的思维方法。下图为金刚石、石墨、足球烯的结构示意图。下列说法正确的是( )
A.它们都是由原子直接构成的
B.构成它们的原子的种类和大小都不同
C.构成它们的原子种类相同,但原子的排列方式不同
D.只有石墨和足球烯能在氧气中燃烧,金刚石不能燃烧
8、下面是实验室制取二氧化碳和探究二氧化碳性质的实验,其中错误的是( )
A.图甲中装置a是长颈漏斗
B.图乙中用点燃的火柴放在集气瓶口来验满
C.图丙中二氧化碳使蜡烛火焰自上而下熄灭
D.图丁中将收集到的二氧化碳通入澄清石灰水会发现溶液变浑浊
9、下列不属于化石能源的是( )
A.煤 B.风能 C.石油 D.天然气
10、可用同一化学原理解释的现象是( )
①久置的石灰水,液面上出现一层硬壳状薄膜
②向澄清石灰水中,通过吸管不断吹入人体呼出的气体
③为了使石灰浆刷过的墙壁快点晾干,在室内生起一盆炭火开始时墙壁潮湿
④向紫色石蕊试液中通入CO2气体,试液变红
A.①②③ B.①②④ C.①③④ D.②③④
11、已知同温同压下,气体体积比等于气体的分子数目之比。常温下,向盛有一定量氧气的密闭容器通入氢气,用电火花点燃,使其充分反应,恢复至相同温度。测得容器中剩余气体的体积与通入氢气的体积关系如图所示。下列说法错误的是( )
A.氧气的起始体积为2mL B.AB间,容器中剩余气体为氧气
C.C点对应纵坐标为(x﹣2) D.B点表示氢气与氧气恰好反应
12、石墨烯是一种非常优良的纳米材料,由碳元素组成,化学性质和石墨相似,还具有超强导电、导热的性能。关于石墨烯的认识错误的是( )
A.可作散热材料 B.是一种新型化合物
C.常温下化学性质稳定 D.可作新型电池的电极
13、实验室制取二氧化碳中,下列相关操作错误的是( )
A.CO2发生装置 B.CO2收集
C.CO2储存 D.CO2验满
14、坚持低碳生活、绿色发展,促进人与自然和谐共生,下列做法与这一理念不相符的是( )
A.限制燃放烟花 B.发展燃煤发电 C.分类处理垃圾 D.倡导公交出行
15、现有下列反应:① ②
③④。
其中适用于实验室制取二氧化碳的是( )
A.①②③④ B.①③④ C.①④ D.④
16、2020年6月23日,我国“长三乙”火箭将第55颗北斗卫星送入预定轨道,完成北斗卫星导航系统的组网。该火箭第三级的推进剂为液氢和液氧组合,下列说法正确的是( )
A.氢气液化过程中,氢分子之间的间隔保持不变
B.分离液态空气得到液态氧气的过程中,氧分子静止不动
C.液氧变成气态氧时,放出热量
D.氢气与氧气反应放出热量为火发射提供了动力
二、填空题。
17、认真阅读下列材料,回答有关问题:
北京时间 2022 年 9 月 2 日 0 时 33 分,经过约 6 小时的出舱活动,神舟十四号航天员陈冬、刘洋、蔡旭哲密切协同,完成出舱活动期间全部既定任务,出舱活动取得圆满成功。航天员佩戴头盔的面窗两层之间充有高纯氮气,该氮气是通过分离液态空气法分离出氮气。航天员呼吸的氧气有三种来源:第一种主要是携带的纯氧氧气瓶,第二种是利用电解术的方式产生的氧气和氢气,氧气可以供宇航员呼吸,而氢气还可以作为燃料。第三种是利用固体氧气发生器产生的氧气。
(1)分离液态空气法分离出氮气的过程属于_________变化(填“物理”或“化学”)。
(2)利用电解水的方式产生的氧气和氢气的化学反应属于_________反应(填“化合”或“分解”)。
(3)氢气可以作为燃料,是利用氢气的_________性。
18、2022年6月5日,中国神舟十四号载人飞船成功发射。三位宇航员将在太空进行长达6个月的科学研究。宇航员舱外服的废气处理系统保障着宇航员的生命。
(1)该系统用装有活性炭的滤网除去废气中的有害成分,利用了活性炭的 性。
(2)宇航员呼出的二氧化碳用含氢氧化锂(LiOH)的滤网吸收,生成碳酸锂和水。该反应的化学方程式为 。
19、化学是一门以实验为基础的科学。某化学兴趣小组选用下图所示装置,进行CO2的制取和性质实验,请你根据所学知识,依图回答下列问题:
(1)写出图中仪器①的名称________________。
(2)装置甲中应添加固体试剂的名称是________________。
(3)用装置乙收集CO2时,导管口a应与__________(填“b”或“c”)相连。
(4)用图丙所示的质地较软的塑料瓶收集满CO2,再倒入约1/3体积的紫色石蕊溶液,立即旋紧瓶盖,振荡,观察到的现象是____________________________。
(5)往图丁的烧杯内缓缓通入CO2,超薄材料做成的内充空气的气球会慢慢浮起,由此得出CO2具有的性质是__________________________________。
(6)将甲、戊装置连接,可验证二氧化碳与氢氧化钙反应,该反应的化学方程式为_____________________ 。
20、“坚决打好蓝天保卫战”山西省积极行动,落实整改措施,省城太原首先通过以下三种方式缓解空气污染初见成效。
(1)为了使空气更新,天空更蓝,你作为环保小卫士,认为推广使用上述方式的好处是______ (任选一项回答)
(2)空气污染严重损害人体健康,影响作物生长,破坏生态平衡引起空气污染的有害气体种类很多,请举一例 _______________(用化学式表示)
(3)你认为改善空气质量的措施正确的是_____________
a.推广使用新能源
b.加强企业排污管理
c.雾霾多发天气,实行私家车限号出行。
21、(1)I、能源利用和环境保护是人类共同关注的问题。
化石燃料主要包括煤、 和天然气。
(2)化石燃料燃烧产生二氧化碳气体,经过绿色植物的光合作用生成淀粉,淀粉在人体内变成葡萄糖(C6H12O6),葡萄糖在酶的催化作用下发生缓慢氧化生成二氧化碳和水,同时放出能量,写出葡萄糖与氧气发生缓慢氧化反应的化学方程式: 。
(3)由上可知,减小温室效应的主要途径有:① ,② (写两条)。
(4)Ⅱ、化学与生活息息相关。根据所学知识回答下列问题:
为保证身体健康,在使用饮用水前,我们一般可以用 的方法降低水的硬度。
(5)在遇到紧急火灾时,我们常常会用水来扑灭,这其中的灭火原理是 。
(6)小朋友们将燃放的鞭炮扔到下水道的做法是危险的。有机物在密闭的环境里发酵可以产生沼气,沼气遇到明火有可能发生爆炸。沼气的主要成分是 。
(7)日常饮食要注意营养均衡,米饭、面条为我们身体提供了能量保障,其中包含的主要营养素是 。
三、推断题。
22、已知:A是相对分子质量最小的氧化物,D是最简单的有机物,也是天然气中最主要的成分。请分析A、B、C、D、E五种物质之间的变化关系,回答有关问题。
(1)请写出D、E的化学式D_________、E__________。
(2)请写出A→B+C的化学方程式:______________________;该反应的基本类型是_________。
四、综合应用题。
23、碳是形成化合物种类最多的元素,含碳物质是中学化学研究的重要内容.
(1)碳元素的化学性质与其原子的________ 关系密切。
(2)如图1为元素周期表中的一格,下列说法正确的是________(填标号).
A 碳元素属于非金属元素
B 碳原子核内质子数为6
C 碳元素的原子结构示意图为
D碳的相对原子质量为12.01g
(3)甲、乙、丙都是常见含有碳元素的物质,它们之间有如图所示的转化关系(部分物质和反应条件已略去),其中甲和丙都可以作燃料,乙和丙中所含的元素种类相同,乙能引起“温室效应”,则乙的化学式为:________,甲转化为丙的途径有多种,写出通过化合反应的方式,甲转化为丙的化学方程式为: ________ ,从微观的角度解释乙、丙性质有差异的原因是: ________ 。
(4)实验室用图3装置来制取二氧化碳,检查该装置的气密性的方法是:将该装置中导气管中的橡胶管用弹簧夹夹住,往长颈漏斗中注入水至液面高出漏斗颈的下端管口,若能观察到________ 现象,即可证明装置不漏气,实验室确定气体发生装置时应考虑的因素是________ 。
(5)称取12.5g石灰石(主要成份CaCO3,杂质不参加反应)放入烧杯中,向其中加入足量的稀盐酸,完全反应结束后放出4.4g气体,试计算石灰石中杂质的质量分数______。
五、科普阅读题。
24、阅读下列科普短文,回答问题。
2021年,考古学家利用碳-14断代法初步判定三星堆4号坑距今约3200至3000年。碳-14原子核中含6个质子与8个中子。生物死后体内的碳-14会不断衰变,碳-14原子核中1个中子变成1个质子,形成新的原子核。对比生物体内生前、死后碳-14的含量,可推算出其所属年代。
国家速滑馆利用CO2跨临界直冷制冰,就是将气态CO2通过加温加压形成超临界CO2流体(介于气态和液态之间的一种新的状态,兼有气体和液体的性质),后变为液态CO2,再变成气态完成制冰的过程。工业上可用CO2为原料合成燃料甲烷、甲醇(CH3OH),氮肥尿素等,合成尿素的反应:。
(1)碳-14原子核外电子数为_________,其衰变形成的新原子属于_________元素(填元素符号)。
(2)超临界CO2流体是______(填“纯净物”“混合物”)。液态CO2能用于制冰的原因是________ 。
(3)甲醇充分燃烧的产物为______________。
(4)合成尿素时,参与反应的CO2与NH3的质量比为__________。尿素含氮量高,其氮元素的质量分数为_________(保留小数点后一位)。
六、计算类综合应用题。
25、碳是重要的生命元素,碳及其化合物的综合利用使世界变得更加绚丽多彩。
Ⅰ碳的多样性
(1)金刚石和石墨的组成元素相同,碳原子的排列方式不同,导致_______。(填具体的物理性质)
(2)从石墨中分离出的单层石墨片(石墨烯)是目前人工制得的最薄材料,单层石墨片属于_______(填“单质”或“化合物”)。
Ⅱ“碳中和”的实现
“碳中和”是指一定时间内CO2的排放量与吸收量基本相当。CO2的捕集、利用是实现“碳中和”的重要途径。我国力争在2060年前实现“碳中和”,体现了中国对解决全球气候问题的大国担当。
(3)大气中CO2的过度排放会造成________的加剧。
(4)工业生产中产生的CO2经吸收剂处理可实现CO2的捕集。写出NaOH溶液吸收CO2生成NaHCO3的化学方程式:_______ 。
(5)“液态太阳燃料合成技术”如图1所示。
①从能源和环境角度说明该合成技术的优点:________ 。
②在合成工厂中,氢气与CO2在一定条件下反应转化为甲醇(CH3OH)和相对分子质量最小的氧化物。写出此反应的化学方程式:_______ 。
(6)CO2与H2在一定条件下转化为CH4(反应过程如图2所示,虚线处部分中间产物略去),可实现CO2的再利用。
①该反应中MgO的作用是_________。
②用该方法制取1t甲烷,则参与反应的二氧化碳的质量为多少?(写出计算过程)______。
第五章 燃料 期末练习题含答案2023—2024学年科粤版(2012)化学九年级上册
科粤版(2012)第五章 燃料
一、选择题。(16题)
1、长征5号运载火箭中采用了液氢﹣液氧发动机,关于选用液氢和液氧的说法中,不正确的是( )
A.与气态相比,液氢和液氧的分子间隔更小,节约空间
B.氢气、氧气经液化后,其化学性质没有发生改变
C.汽化后,产生的氢气和氧气都是可燃物
D.燃烧反应的产物是水,不会污染环境
【答案】C
2、“碳家族”的成员很多,用途很广。下列说法正确的是( )
A.石墨不具有导电性 B.C60单质是由碳原子直接构成的
C.活性炭具有吸附性 D.金刚石和石墨里碳原子的排列方式相同
【答案】C
3、成都以“碳达峰、碳中和”为目标,引领城市绿色低碳发展。下列做法利于实现此目标的是( )
A.石油炼制 B.太阳能发电 C.燃煤脱硫 D.酒精作燃料
【答案】B
4、逻辑推理是一种重要的化学思维方法,下列推理合理的是( )
A.单质由同种元素组成,则由同种元素组成的物质一定是单质
B.催化剂在反应前后质量不变,因此反应前后质量不变的物质一定是催化剂
C.点燃可燃性气体前需检验纯度,则点燃甲烷气体前需要验纯
D.同种元素的原子质子数相同,所以具有相同质子数的粒子一定是同种元素
【答案】C
5、“安全重于泰山”,下列有关说法正确的是( )
A.面粉厂周围不需要严禁烟火 B.天然气报警器应安装在灶台下方
C.冬季用炭火取暖需关闭门窗 D.档案失火用二氧化碳灭火器扑灭
【答案】D
6、我国发射的“天宫一号”目标飞行器和“神舟八号”飞船,实施了首次空间飞行器无人交会对接试验.“天宫一号”飞行器升空所用燃料之一为液氢.下列有关氢气的说法,你认为不正确的是( )
A.氢气是一种无色、无臭、难溶于水的气体
B.氢气在空气中燃烧时,产生淡蓝色火焰
C.氢气和液氢的化学性质不同
D.点燃用排水法收集的一试管氢气,若发出尖锐的爆鸣声,则表明氢气不纯
【答案】C
7、“见著之微,见微之著”是化学的思维方法。下图为金刚石、石墨、足球烯的结构示意图。下列说法正确的是( )
A.它们都是由原子直接构成的
B.构成它们的原子的种类和大小都不同
C.构成它们的原子种类相同,但原子的排列方式不同
D.只有石墨和足球烯能在氧气中燃烧,金刚石不能燃烧
【答案】C
8、下面是实验室制取二氧化碳和探究二氧化碳性质的实验,其中错误的是( )
A.图甲中装置a是长颈漏斗
B.图乙中用点燃的火柴放在集气瓶口来验满
C.图丙中二氧化碳使蜡烛火焰自上而下熄灭
D.图丁中将收集到的二氧化碳通入澄清石灰水会发现溶液变浑浊
【答案】C
9、下列不属于化石能源的是( )
A.煤 B.风能 C.石油 D.天然气
【答案】B
10、可用同一化学原理解释的现象是( )
①久置的石灰水,液面上出现一层硬壳状薄膜
②向澄清石灰水中,通过吸管不断吹入人体呼出的气体
③为了使石灰浆刷过的墙壁快点晾干,在室内生起一盆炭火开始时墙壁潮湿
④向紫色石蕊试液中通入CO2气体,试液变红
A.①②③ B.①②④ C.①③④ D.②③④
【答案】A
11、已知同温同压下,气体体积比等于气体的分子数目之比。常温下,向盛有一定量氧气的密闭容器通入氢气,用电火花点燃,使其充分反应,恢复至相同温度。测得容器中剩余气体的体积与通入氢气的体积关系如图所示。下列说法错误的是( )
A.氧气的起始体积为2mL B.AB间,容器中剩余气体为氧气
C.C点对应纵坐标为(x﹣2) D.B点表示氢气与氧气恰好反应
【答案】C
12、石墨烯是一种非常优良的纳米材料,由碳元素组成,化学性质和石墨相似,还具有超强导电、导热的性能。关于石墨烯的认识错误的是( )
A.可作散热材料 B.是一种新型化合物
C.常温下化学性质稳定 D.可作新型电池的电极
【答案】B
13、实验室制取二氧化碳中,下列相关操作错误的是( )
A.CO2发生装置 B.CO2收集
C.CO2储存 D.CO2验满
【答案】B
14、坚持低碳生活、绿色发展,促进人与自然和谐共生,下列做法与这一理念不相符的是( )
A.限制燃放烟花 B.发展燃煤发电 C.分类处理垃圾 D.倡导公交出行
【答案】B
15、现有下列反应:① ②
③④。
其中适用于实验室制取二氧化碳的是( )
A.①②③④ B.①③④ C.①④ D.④
【答案】D
16、2020年6月23日,我国“长三乙”火箭将第55颗北斗卫星送入预定轨道,完成北斗卫星导航系统的组网。该火箭第三级的推进剂为液氢和液氧组合,下列说法正确的是( )
A.氢气液化过程中,氢分子之间的间隔保持不变
B.分离液态空气得到液态氧气的过程中,氧分子静止不动
C.液氧变成气态氧时,放出热量
D.氢气与氧气反应放出热量为火发射提供了动力
【答案】D
二、填空题。
17、认真阅读下列材料,回答有关问题:
北京时间 2022 年 9 月 2 日 0 时 33 分,经过约 6 小时的出舱活动,神舟十四号航天员陈冬、刘洋、蔡旭哲密切协同,完成出舱活动期间全部既定任务,出舱活动取得圆满成功。航天员佩戴头盔的面窗两层之间充有高纯氮气,该氮气是通过分离液态空气法分离出氮气。航天员呼吸的氧气有三种来源:第一种主要是携带的纯氧氧气瓶,第二种是利用电解术的方式产生的氧气和氢气,氧气可以供宇航员呼吸,而氢气还可以作为燃料。第三种是利用固体氧气发生器产生的氧气。
(1)分离液态空气法分离出氮气的过程属于_________变化(填“物理”或“化学”)。
(2)利用电解水的方式产生的氧气和氢气的化学反应属于_________反应(填“化合”或“分解”)。
(3)氢气可以作为燃料,是利用氢气的_________性。
【答案】(1)物理 (2)分解 (3)可燃
18、2022年6月5日,中国神舟十四号载人飞船成功发射。三位宇航员将在太空进行长达6个月的科学研究。宇航员舱外服的废气处理系统保障着宇航员的生命。
(1)该系统用装有活性炭的滤网除去废气中的有害成分,利用了活性炭的 性。
(2)宇航员呼出的二氧化碳用含氢氧化锂(LiOH)的滤网吸收,生成碳酸锂和水。该反应的化学方程式为 。
【答案】(1)吸附; (2)CO2+2LiOH═Li2CO3+H2O。
19、化学是一门以实验为基础的科学。某化学兴趣小组选用下图所示装置,进行CO2的制取和性质实验,请你根据所学知识,依图回答下列问题:
(1)写出图中仪器①的名称________________。
(2)装置甲中应添加固体试剂的名称是________________。
(3)用装置乙收集CO2时,导管口a应与__________(填“b”或“c”)相连。
(4)用图丙所示的质地较软的塑料瓶收集满CO2,再倒入约1/3体积的紫色石蕊溶液,立即旋紧瓶盖,振荡,观察到的现象是____________________________。
(5)往图丁的烧杯内缓缓通入CO2,超薄材料做成的内充空气的气球会慢慢浮起,由此得出CO2具有的性质是__________________________________。
(6)将甲、戊装置连接,可验证二氧化碳与氢氧化钙反应,该反应的化学方程式为_____________________ 。
【答案】(1)长颈漏斗; (2)大理石等; (3)b;
(4)溶液变红色,塑料瓶变瘪;
(5)二氧化碳的密度比空气的大;
(6)Ca(OH)2+CO2=CaCO3↓+H2O。
20、“坚决打好蓝天保卫战”山西省积极行动,落实整改措施,省城太原首先通过以下三种方式缓解空气污染初见成效。
(1)为了使空气更新,天空更蓝,你作为环保小卫士,认为推广使用上述方式的好处是______ (任选一项回答)
(2)空气污染严重损害人体健康,影响作物生长,破坏生态平衡引起空气污染的有害气体种类很多,请举一例 _______________(用化学式表示)
(3)你认为改善空气质量的措施正确的是_____________
a.推广使用新能源
b.加强企业排污管理
c.雾霾多发天气,实行私家车限号出行。
【答案】减少化石燃料燃烧,减少空气污染(答案合理即可)
SO2(合理即可) abc
21、(1)I、能源利用和环境保护是人类共同关注的问题。
化石燃料主要包括煤、 和天然气。
(2)化石燃料燃烧产生二氧化碳气体,经过绿色植物的光合作用生成淀粉,淀粉在人体内变成葡萄糖(C6H12O6),葡萄糖在酶的催化作用下发生缓慢氧化生成二氧化碳和水,同时放出能量,写出葡萄糖与氧气发生缓慢氧化反应的化学方程式: 。
(3)由上可知,减小温室效应的主要途径有:① ,② (写两条)。
(4)Ⅱ、化学与生活息息相关。根据所学知识回答下列问题:
为保证身体健康,在使用饮用水前,我们一般可以用 的方法降低水的硬度。
(5)在遇到紧急火灾时,我们常常会用水来扑灭,这其中的灭火原理是 。
(6)小朋友们将燃放的鞭炮扔到下水道的做法是危险的。有机物在密闭的环境里发酵可以产生沼气,沼气遇到明火有可能发生爆炸。沼气的主要成分是 。
(7)日常饮食要注意营养均衡,米饭、面条为我们身体提供了能量保障,其中包含的主要营养素是 。
【答案】(1)石油
(2)C6H12O6+6O2===6CO2+6H2O
(3)骑自行车上学(合理即可);植树造林(合理即可)
(4)煮沸 (5)降低温度至可燃物的着火点以下
(6)甲烷/CH4 (7)糖类
三、推断题。
22、已知:A是相对分子质量最小的氧化物,D是最简单的有机物,也是天然气中最主要的成分。请分析A、B、C、D、E五种物质之间的变化关系,回答有关问题。
(1)请写出D、E的化学式D_________、E__________。
(2)请写出A→B+C的化学方程式:______________________;该反应的基本类型是_________。
【答案】CH4 CO2 2H2O2H2↑+ O2↑ 分解反应
四、综合应用题。
23、碳是形成化合物种类最多的元素,含碳物质是中学化学研究的重要内容.
(1)碳元素的化学性质与其原子的________ 关系密切。
(2)如图1为元素周期表中的一格,下列说法正确的是________(填标号).
A 碳元素属于非金属元素
B 碳原子核内质子数为6
C 碳元素的原子结构示意图为
D碳的相对原子质量为12.01g
(3)甲、乙、丙都是常见含有碳元素的物质,它们之间有如图所示的转化关系(部分物质和反应条件已略去),其中甲和丙都可以作燃料,乙和丙中所含的元素种类相同,乙能引起“温室效应”,则乙的化学式为:________,甲转化为丙的途径有多种,写出通过化合反应的方式,甲转化为丙的化学方程式为: ________ ,从微观的角度解释乙、丙性质有差异的原因是: ________ 。
(4)实验室用图3装置来制取二氧化碳,检查该装置的气密性的方法是:将该装置中导气管中的橡胶管用弹簧夹夹住,往长颈漏斗中注入水至液面高出漏斗颈的下端管口,若能观察到________ 现象,即可证明装置不漏气,实验室确定气体发生装置时应考虑的因素是________ 。
(5)称取12.5g石灰石(主要成份CaCO3,杂质不参加反应)放入烧杯中,向其中加入足量的稀盐酸,完全反应结束后放出4.4g气体,试计算石灰石中杂质的质量分数______。
【答案】(1)最外层电子数 (2)AB
(3)CO2 二氧化碳和一氧化碳的分子构成不同
(4)长颈漏斗和试管中出现液面差 反应物状态和反应条件 (5)20%
五、科普阅读题。
24、阅读下列科普短文,回答问题。
2021年,考古学家利用碳-14断代法初步判定三星堆4号坑距今约3200至3000年。碳-14原子核中含6个质子与8个中子。生物死后体内的碳-14会不断衰变,碳-14原子核中1个中子变成1个质子,形成新的原子核。对比生物体内生前、死后碳-14的含量,可推算出其所属年代。
国家速滑馆利用CO2跨临界直冷制冰,就是将气态CO2通过加温加压形成超临界CO2流体(介于气态和液态之间的一种新的状态,兼有气体和液体的性质),后变为液态CO2,再变成气态完成制冰的过程。工业上可用CO2为原料合成燃料甲烷、甲醇(CH3OH),氮肥尿素等,合成尿素的反应:。
(1)碳-14原子核外电子数为_________,其衰变形成的新原子属于_________元素(填元素符号)。
(2)超临界CO2流体是______(填“纯净物”“混合物”)。液态CO2能用于制冰的原因是________ 。
(3)甲醇充分燃烧的产物为______________。
(4)合成尿素时,参与反应的CO2与NH3的质量比为__________。尿素含氮量高,其氮元素的质量分数为_________(保留小数点后一位)。
【答案】(1) 6 N
(2) 纯净物 液态二氧化碳汽化吸热,能使周围温度降低
(3)二氧化碳和水 (4) 22:17 46.7%
六、计算类综合应用题。
25、碳是重要的生命元素,碳及其化合物的综合利用使世界变得更加绚丽多彩。
Ⅰ碳的多样性
(1)金刚石和石墨的组成元素相同,碳原子的排列方式不同,导致_______。(填具体的物理性质)
(2)从石墨中分离出的单层石墨片(石墨烯)是目前人工制得的最薄材料,单层石墨片属于_______(填“单质”或“化合物”)。
Ⅱ“碳中和”的实现
“碳中和”是指一定时间内CO2的排放量与吸收量基本相当。CO2的捕集、利用是实现“碳中和”的重要途径。我国力争在2060年前实现“碳中和”,体现了中国对解决全球气候问题的大国担当。
(3)大气中CO2的过度排放会造成________的加剧。
(4)工业生产中产生的CO2经吸收剂处理可实现CO2的捕集。写出NaOH溶液吸收CO2生成NaHCO3的化学方程式:_______ 。
(5)“液态太阳燃料合成技术”如图1所示。
①从能源和环境角度说明该合成技术的优点:________ 。
②在合成工厂中,氢气与CO2在一定条件下反应转化为甲醇(CH3OH)和相对分子质量最小的氧化物。写出此反应的化学方程式:_______ 。
(6)CO2与H2在一定条件下转化为CH4(反应过程如图2所示,虚线处部分中间产物略去),可实现CO2的再利用。
①该反应中MgO的作用是_________。
②用该方法制取1t甲烷,则参与反应的二氧化碳的质量为多少?(写出计算过程)______。
【答案】(1)金刚石硬度大,而石墨比较软(合理即可)
(2)单质 (3)温室效应 (4)
(5) 节约能源,有效缓解温室效应
(6) 催化作用 2.75t
设:参与反应的二氧化碳的质量为x
答:参与反应的二氧化碳的质量为2.75t。
同课章节目录
- 第一章 大家都来学化学
- 1.1 身边的化学
- 1.2 化学实验室之旅
- 1.3 物质的变化
- 1.4 物质性质的探究
- 第二章 空气、物质的构成
- 2.1 空气的成分
- 2.2 构成物质的微粒(Ⅰ)——分子
- 2.3 构成物质的微粒(Ⅱ)——原子和离子
- 2.4 辨别物质的元素组成
- 第三章 维持生命之气——氧气
- 3.1 氧气的性质和用途
- 3.2 制取氧气
- 3.3 燃烧条件与灭火原理
- 3.4 物质构成的表示式
- 第四章 生命之源——水
- 4.1 我们的水资源
- 4.2 水的组成
- 4.3 质量守恒定律
- 4.4 化学方程式
- 第五章 燃料
- 5.1 洁净的燃料——氢气
- 5.2 组成燃料的主要元素——碳
- 5.3 二氧化碳的性质和制法
- 5.4 古生物的“遗产”——化石燃料
