第九单元溶液 单元同步卷(含答案) -2023-2024学年九年级化学人教版下册
文档属性
| 名称 | 第九单元溶液 单元同步卷(含答案) -2023-2024学年九年级化学人教版下册 |
|
|
| 格式 | docx | ||
| 文件大小 | 541.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-01-02 00:00:00 | ||
图片预览

文档简介
第九单元 溶液 单元同步卷
一、选择题
1.现有①氧化铜和稀盐酸 ②氢氧化钠和水 ③硝酸铵和水 ④镁和稀硫酸 ⑤锌和稀盐酸,五组物质。将各组中的两种物质在如图所示气密性良好的装置中相互混合,有气泡从水中逸出的是
A.③④⑤ B.①③⑤ C.②③④ D.②④⑤
2.向盛有硝酸钾的烧杯中加入水,充分溶解后现象如图所示,此时溶液温度为,下列说法正确的是
A.烧杯中的溶液总质量为
B.烧杯中的溶液为时硝酸钾饱和溶液,溶液的溶质质量分数为
C.若使烧杯中的固体全部溶解,则溶液的溶质质量分数一定增大
D.若使烧杯中的溶液变为不饱和溶液,则溶液的溶质质量分数可能增大
3.区分下列各组物质的方法均正确的是
选项 需区分的物质 方法一 方法二
A 硬水和蒸馏水 加肥皂水、振荡 品尝味道
B 硝酸钾饱和溶液和氯化钠饱和溶液 加入等质量的硝酸钾 升温观察
C 黄金和黄铜 加稀盐酸观察 加硝酸银溶液观察
D 铁粉和氧化铜 通入一氧化碳气体 用磁铁吸
A.A B.B C.C D.D
4.下列图像与对应的叙述相符合的是
A.在同一温度下,向饱和氯化钠溶液中加入固体氯化钠
B.将等质量的Mg、Fe分别与足量且溶质质量分数相同的稀硫酸反应
C.将水通电一段时间
D.向一定量氯化铜溶液中加入一定量铝
5.据甲、乙两种物质(不含结晶水)的溶解度曲线图像,下列说法中正确的是
A.甲物质的溶解度一定大于乙物质的溶解
B.30℃时,给甲乙的饱和溶液恒温蒸发等质量的水,析出晶体质量甲>乙
C.20℃时,甲溶液溶质质量分数等于乙溶液溶质质量分数
D.甲中含有少量乙,可以用蒸发结晶的方式提纯乙
6.“粗盐提纯”的实验内容和步骤如图,下列说法错误的是
A.本实验需查阅资料,了解食盐在室温时的溶解度
B.操作Ⅲ中,若未能充分溶解,则实验的产率将偏低
C.操作Ⅴ中,溶液中氯化钠的质量分数一定不变
D.将所得精盐放入饱和食盐水中,溶液质量会增大
7.在2023年东营市初中学业水平考试实验操作考试中有以下做法,正确的是
A.“配制溶质质量分数一定的溶液”实验,称量过程中多余的氯化钠固体放回原瓶
B.“二氧化碳的制取和性质”实验,反应后的废液直接倒入下水道
C.“探究温度对硝酸钾溶解能力的影响”实验,得到的溶液收集后再降温结晶出硝酸钾回收利用
D.“过氧化氢溶液制氧气”实验,加入过氧化氢溶液和二氧化锰后用酒精灯加热装置以提高反应速率
8.A、B、C三种物质的溶解度曲线如图所示。下列分析正确的是
A.t1℃时,A、C溶液中溶质的溶质质量分数相等
B.将t2℃的A、B饱和溶液降温至t1℃,A析出的晶体比B多
C.t2℃时,将30gA物质放入50g水中,充分溶解后,所得溶液溶质质量分数为33.3%。保持温度不变,向该溶液中再加入10g水充分搅拌,溶液的溶质质量分数将减小
D.将t2℃时,A、B、C三种物质的饱和溶液降温至t1℃,所得溶液的溶质质量分数由大到小是B>A>C
9.某同学对部分化学知识归纳如下,其中完全正确的是
A.化学巨匠与贡献 B.化学实验与安全
①卢瑟福发现原子的结构 ②道尔顿是原子之父 ③门捷列夫发现元素周期表 ①少量酒精失火立即用湿布盖灭 ②加热后的试管立即用水冲洗 ③点燃氢气前,应先检验气体的纯度
C.微粒构成物质 D.日常生活经验
①金刚石由碳原子构成 ②氧气由氧分子构成 ③氯化钠由钠离子和氯离子构成 ①区别硬水和软水—加入明矾振荡 ②区分白酒和白醋—闻气味 ③区分氢氧化钠和硝酸铵—加入水溶解测温度变化
A.A B.B C.C D.D
10.室温下,烧杯中装有200g NaCl溶液编号A;向烧杯中加入20g NaCl固体,充分搅拌后,尚有2g固体未溶解,此时的NaCl溶液为编号B;再向烧杯中加入20g水,固体全部溶解,此时的NaCl溶液为编号C.下列说法正确的是
A.A溶液是NaCl的饱和溶液 B.B溶液可能是NaCl的饱和溶液
C.C溶液是NaCl的饱和溶液 D.B溶液的溶质质量分数最大
11.如图是甲、乙两种固体物质(不含结晶水)的溶解度曲线,下列说法错误的是
A.乙物质属于易溶性物质
B.a1℃时,130g甲的饱和溶液中含有30g甲
C.a2℃时甲的溶解度大于乙的溶解度
D.a2℃时甲和乙的溶液分别蒸发等质量的水,析出的甲物质的质量一定大于乙物质的质量
12.如图为甲、乙两物质(均不含结晶水)的溶解度曲线,下列说法正确的是
A.20℃时,100g甲溶液中含甲物质的质量为25g
B.将甲物质从50℃降温到30℃时一定有晶体析出
C.20℃时,等质量甲、乙饱和溶液中含溶质的质量相等
D.将甲、乙两种物质的溶液分别从50℃降温至20℃时,溶液中溶质质量分数均为25%
13.甲、乙、丙三种物质在不同温度下的溶解度见下表:
下列有关说法正确的是
A.甲、乙、丙三种物质的溶解度大小顺序是甲>乙>丙
B.30℃时,三种物质的饱和溶液溶质质量分数是甲>乙>丙
C.甲、乙两物质溶解度相等的温度范围是30℃-60℃之间
D.使乙物质从一定温度下的饱和溶液中析出,一般采用降温结晶的方法
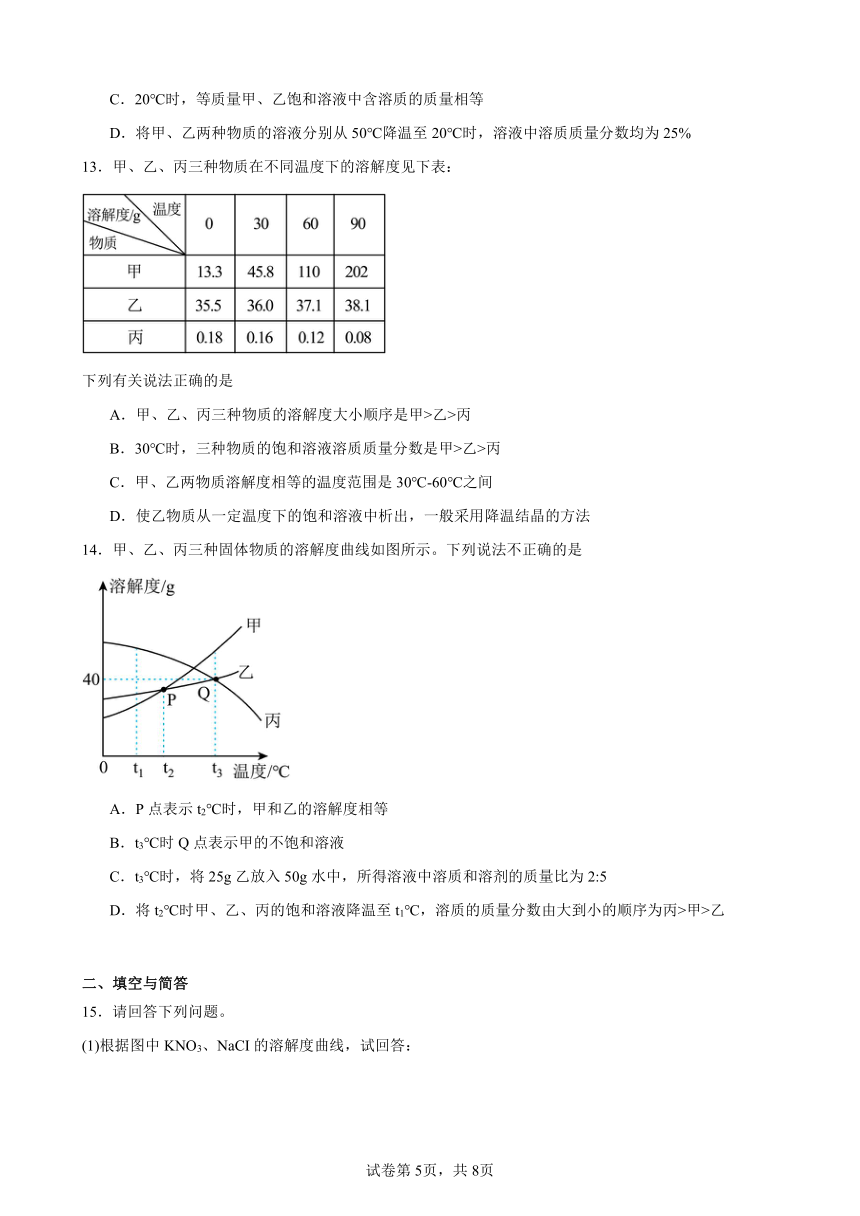
14.甲、乙、丙三种固体物质的溶解度曲线如图所示。下列说法不正确的是
A.P点表示t2℃时,甲和乙的溶解度相等
B.t3℃时Q点表示甲的不饱和溶液
C.t3℃时,将25g乙放入50g水中,所得溶液中溶质和溶剂的质量比为2:5
D.将t2℃时甲、乙、丙的饱和溶液降温至t1℃,溶质的质量分数由大到小的顺序为丙>甲>乙
二、填空与简答
15.请回答下列问题。
(1)根据图中KNO3、NaCI的溶解度曲线,试回答:
①40℃时,KNO3、NaCl两种物质的溶解度大小关系:KNO3 NaCl(填“<” “>”或“=”)。
②t℃时,将45gKNO3固体放入50g水中充分溶解,所得溶液的质量为 。
③在不改变溶液质量的情况下,要使一定量接近饱和的KNO3溶液变为饱和溶液的方法是 。
④NaCl溶液中含有少量KNO3,提纯NaCl的方法是 。
(2)回答下列问题:
①沙子是加油站常备灭火用品,其灭火原理是 。
②用汽油能除去衣服上的油污,其除油污的原理为 。
16.如图为A、B、C三种固体物质的溶解度曲线图(A、B、C析出晶体时均不含结晶水),根据曲线图回答下列题。
(1)t1℃时,溶解度最大的物质是 。
(2)若将M点处C的不饱和溶液变为饱和溶液,可以选择的方法是 (填序号)。
①降低温度 ②增加溶质 ③蒸发溶剂
(3)t2℃时,将等质量的A、B、C的饱和溶液都升温到t3℃,溶液中溶剂质量的大小关系是(忽略水的挥发) 。
(4)当A物质中混有少量B、C两种物质时,采用 的方法可以除去它们。
(5)将t2℃等质量的A、B、C三种物质的饱和溶液降温到t1℃,析出晶体最多的是 ,此时所得溶液中溶质质量分数由大到小的顺序是 。
17.下列数据是氯化钠和氯化钾固体在不同温度时的溶解度。
温度/℃ 0 20 40 60 80 100
溶解度/g NaCl 35.7 36.0 36.6 37.3 38.4 39.8
KCl 27.6 34.0 40.0 45.5 51.1 56.7
(1)在0~20℃时,KCl的溶解度 (填“>”或“<”)NaCl的溶解度;
(2)20℃时,向100g水中加入25g氯化钠,充分溶解后,得到的溶液为 (填“饱和”或“不饱和”)溶液,溶液中溶质质量分数为 ;
(3)20℃时,进行如下图所示的实验。
①A~E中,溶液中溶质质量分数相同的是 ;
②下列操作能使E溶液中溶质质量分数变小的是 (填字母序号)。
a.加入2g KCl b.加入100g 100℃的水 c.降温至40℃
18.合金
(1)生铁和钢是铁的两种合金,其中 的含碳量较高, 的含碳量较低。由于 不同,因此生铁和钢的性能有很大的区别。
(2)合金的特性:合金的硬度比组成它的纯金属的硬度 ;熔点比组成它的纯金属的熔点都 ;抗腐蚀性能 ,机械加工性能好。
(3)钛和钛合金被认为是21世纪的重要金属材料。可用于火箭、航天飞机、通讯 。
(4)“假黄金”黄铜是铜、锌合金,鉴别真假黄金可选用稀盐酸,“假黄金”遇到稀盐酸会有 的现象;也可通过加热的方法鉴别黄金,假黄金加热会 。
三、计算题
19.AgNO3溶液是实验室中的常用试剂。AgNO3的化学性质不稳定,在温度稍高或光照条件下可以发生反应:2AgNO32Ag+2NO2↑+O2↑ (假设气体全部逸出)。现有一瓶100g10%的AgNO3溶液,久置后(不考虑水分挥发),将瓶内物质过滤,得到固体1.08g和若干滤液。试计算:
(1)AgNO3中N和O的质量比为 。
(2)滤液中AgNO3的质量分数(结果精确到0.1%)。
20.过氧化氢消毒液能够杀灭细菌、真菌,包括破伤风杆菌、厌氧菌等,医疗上常用3%的过氧化氢溶液消毒。如图是学校实验室购买的过氧化氢溶液的标签,回答下列问题:
过氧化氢溶液
体积 500 mL
溶质质量分数 30%
有氧化性,接触皮肤后要立即用大量水冲洗
(1)从中取出10 mL,则溶液的溶质质量分数为 。
(2)欲配制溶质质量分数为3%的过氧化氢溶液200 g用于医用消毒,需要这种过氧化氢溶液的质量是多少克 需要加入水的质量为多少克 (写出解题过程)
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.D
2.D
3.C
4.A
5.B
6.C
7.C
8.D
9.C
10.D
11.D
12.C
13.B
14.D
15.(1) > 90g/90克 降温 蒸发结晶
(2) 隔绝氧气 汽油能溶解油污
16.(1)C
(2)②③
(3)B>A=C
(4)降温结晶
(5) A C>A=B
17.(1)<
(2) 不饱和 20%
(3) C和D bc
18.(1) 生铁 钢 含碳量
(2) 大 低 好
(3)船舶和化工等
(4) 产生气泡 变黑
19.(1)7:24
(2)解:设参加反应硝酸银的质量为x,生成二氧化氮的质量为y,生成氧气的质量为z。
x=1.7g y=0.46g z=0.16g
滤液中AgNO3的质量分数=×100%≈8.4%。
答:滤液中AgNO3的质量分数8.4%。
20.(1)30%
(2)解:设要这种过氧化氢溶液的质量为x;
解得x=20g
则需要加入水的质量是:
答:要30%过氧化氢溶液的质量为20g,需要加入水的质量是180g。
答案第1页,共2页
答案第1页,共2页
一、选择题
1.现有①氧化铜和稀盐酸 ②氢氧化钠和水 ③硝酸铵和水 ④镁和稀硫酸 ⑤锌和稀盐酸,五组物质。将各组中的两种物质在如图所示气密性良好的装置中相互混合,有气泡从水中逸出的是
A.③④⑤ B.①③⑤ C.②③④ D.②④⑤
2.向盛有硝酸钾的烧杯中加入水,充分溶解后现象如图所示,此时溶液温度为,下列说法正确的是
A.烧杯中的溶液总质量为
B.烧杯中的溶液为时硝酸钾饱和溶液,溶液的溶质质量分数为
C.若使烧杯中的固体全部溶解,则溶液的溶质质量分数一定增大
D.若使烧杯中的溶液变为不饱和溶液,则溶液的溶质质量分数可能增大
3.区分下列各组物质的方法均正确的是
选项 需区分的物质 方法一 方法二
A 硬水和蒸馏水 加肥皂水、振荡 品尝味道
B 硝酸钾饱和溶液和氯化钠饱和溶液 加入等质量的硝酸钾 升温观察
C 黄金和黄铜 加稀盐酸观察 加硝酸银溶液观察
D 铁粉和氧化铜 通入一氧化碳气体 用磁铁吸
A.A B.B C.C D.D
4.下列图像与对应的叙述相符合的是
A.在同一温度下,向饱和氯化钠溶液中加入固体氯化钠
B.将等质量的Mg、Fe分别与足量且溶质质量分数相同的稀硫酸反应
C.将水通电一段时间
D.向一定量氯化铜溶液中加入一定量铝
5.据甲、乙两种物质(不含结晶水)的溶解度曲线图像,下列说法中正确的是
A.甲物质的溶解度一定大于乙物质的溶解
B.30℃时,给甲乙的饱和溶液恒温蒸发等质量的水,析出晶体质量甲>乙
C.20℃时,甲溶液溶质质量分数等于乙溶液溶质质量分数
D.甲中含有少量乙,可以用蒸发结晶的方式提纯乙
6.“粗盐提纯”的实验内容和步骤如图,下列说法错误的是
A.本实验需查阅资料,了解食盐在室温时的溶解度
B.操作Ⅲ中,若未能充分溶解,则实验的产率将偏低
C.操作Ⅴ中,溶液中氯化钠的质量分数一定不变
D.将所得精盐放入饱和食盐水中,溶液质量会增大
7.在2023年东营市初中学业水平考试实验操作考试中有以下做法,正确的是
A.“配制溶质质量分数一定的溶液”实验,称量过程中多余的氯化钠固体放回原瓶
B.“二氧化碳的制取和性质”实验,反应后的废液直接倒入下水道
C.“探究温度对硝酸钾溶解能力的影响”实验,得到的溶液收集后再降温结晶出硝酸钾回收利用
D.“过氧化氢溶液制氧气”实验,加入过氧化氢溶液和二氧化锰后用酒精灯加热装置以提高反应速率
8.A、B、C三种物质的溶解度曲线如图所示。下列分析正确的是
A.t1℃时,A、C溶液中溶质的溶质质量分数相等
B.将t2℃的A、B饱和溶液降温至t1℃,A析出的晶体比B多
C.t2℃时,将30gA物质放入50g水中,充分溶解后,所得溶液溶质质量分数为33.3%。保持温度不变,向该溶液中再加入10g水充分搅拌,溶液的溶质质量分数将减小
D.将t2℃时,A、B、C三种物质的饱和溶液降温至t1℃,所得溶液的溶质质量分数由大到小是B>A>C
9.某同学对部分化学知识归纳如下,其中完全正确的是
A.化学巨匠与贡献 B.化学实验与安全
①卢瑟福发现原子的结构 ②道尔顿是原子之父 ③门捷列夫发现元素周期表 ①少量酒精失火立即用湿布盖灭 ②加热后的试管立即用水冲洗 ③点燃氢气前,应先检验气体的纯度
C.微粒构成物质 D.日常生活经验
①金刚石由碳原子构成 ②氧气由氧分子构成 ③氯化钠由钠离子和氯离子构成 ①区别硬水和软水—加入明矾振荡 ②区分白酒和白醋—闻气味 ③区分氢氧化钠和硝酸铵—加入水溶解测温度变化
A.A B.B C.C D.D
10.室温下,烧杯中装有200g NaCl溶液编号A;向烧杯中加入20g NaCl固体,充分搅拌后,尚有2g固体未溶解,此时的NaCl溶液为编号B;再向烧杯中加入20g水,固体全部溶解,此时的NaCl溶液为编号C.下列说法正确的是
A.A溶液是NaCl的饱和溶液 B.B溶液可能是NaCl的饱和溶液
C.C溶液是NaCl的饱和溶液 D.B溶液的溶质质量分数最大
11.如图是甲、乙两种固体物质(不含结晶水)的溶解度曲线,下列说法错误的是
A.乙物质属于易溶性物质
B.a1℃时,130g甲的饱和溶液中含有30g甲
C.a2℃时甲的溶解度大于乙的溶解度
D.a2℃时甲和乙的溶液分别蒸发等质量的水,析出的甲物质的质量一定大于乙物质的质量
12.如图为甲、乙两物质(均不含结晶水)的溶解度曲线,下列说法正确的是
A.20℃时,100g甲溶液中含甲物质的质量为25g
B.将甲物质从50℃降温到30℃时一定有晶体析出
C.20℃时,等质量甲、乙饱和溶液中含溶质的质量相等
D.将甲、乙两种物质的溶液分别从50℃降温至20℃时,溶液中溶质质量分数均为25%
13.甲、乙、丙三种物质在不同温度下的溶解度见下表:
下列有关说法正确的是
A.甲、乙、丙三种物质的溶解度大小顺序是甲>乙>丙
B.30℃时,三种物质的饱和溶液溶质质量分数是甲>乙>丙
C.甲、乙两物质溶解度相等的温度范围是30℃-60℃之间
D.使乙物质从一定温度下的饱和溶液中析出,一般采用降温结晶的方法
14.甲、乙、丙三种固体物质的溶解度曲线如图所示。下列说法不正确的是
A.P点表示t2℃时,甲和乙的溶解度相等
B.t3℃时Q点表示甲的不饱和溶液
C.t3℃时,将25g乙放入50g水中,所得溶液中溶质和溶剂的质量比为2:5
D.将t2℃时甲、乙、丙的饱和溶液降温至t1℃,溶质的质量分数由大到小的顺序为丙>甲>乙
二、填空与简答
15.请回答下列问题。
(1)根据图中KNO3、NaCI的溶解度曲线,试回答:
①40℃时,KNO3、NaCl两种物质的溶解度大小关系:KNO3 NaCl(填“<” “>”或“=”)。
②t℃时,将45gKNO3固体放入50g水中充分溶解,所得溶液的质量为 。
③在不改变溶液质量的情况下,要使一定量接近饱和的KNO3溶液变为饱和溶液的方法是 。
④NaCl溶液中含有少量KNO3,提纯NaCl的方法是 。
(2)回答下列问题:
①沙子是加油站常备灭火用品,其灭火原理是 。
②用汽油能除去衣服上的油污,其除油污的原理为 。
16.如图为A、B、C三种固体物质的溶解度曲线图(A、B、C析出晶体时均不含结晶水),根据曲线图回答下列题。
(1)t1℃时,溶解度最大的物质是 。
(2)若将M点处C的不饱和溶液变为饱和溶液,可以选择的方法是 (填序号)。
①降低温度 ②增加溶质 ③蒸发溶剂
(3)t2℃时,将等质量的A、B、C的饱和溶液都升温到t3℃,溶液中溶剂质量的大小关系是(忽略水的挥发) 。
(4)当A物质中混有少量B、C两种物质时,采用 的方法可以除去它们。
(5)将t2℃等质量的A、B、C三种物质的饱和溶液降温到t1℃,析出晶体最多的是 ,此时所得溶液中溶质质量分数由大到小的顺序是 。
17.下列数据是氯化钠和氯化钾固体在不同温度时的溶解度。
温度/℃ 0 20 40 60 80 100
溶解度/g NaCl 35.7 36.0 36.6 37.3 38.4 39.8
KCl 27.6 34.0 40.0 45.5 51.1 56.7
(1)在0~20℃时,KCl的溶解度 (填“>”或“<”)NaCl的溶解度;
(2)20℃时,向100g水中加入25g氯化钠,充分溶解后,得到的溶液为 (填“饱和”或“不饱和”)溶液,溶液中溶质质量分数为 ;
(3)20℃时,进行如下图所示的实验。
①A~E中,溶液中溶质质量分数相同的是 ;
②下列操作能使E溶液中溶质质量分数变小的是 (填字母序号)。
a.加入2g KCl b.加入100g 100℃的水 c.降温至40℃
18.合金
(1)生铁和钢是铁的两种合金,其中 的含碳量较高, 的含碳量较低。由于 不同,因此生铁和钢的性能有很大的区别。
(2)合金的特性:合金的硬度比组成它的纯金属的硬度 ;熔点比组成它的纯金属的熔点都 ;抗腐蚀性能 ,机械加工性能好。
(3)钛和钛合金被认为是21世纪的重要金属材料。可用于火箭、航天飞机、通讯 。
(4)“假黄金”黄铜是铜、锌合金,鉴别真假黄金可选用稀盐酸,“假黄金”遇到稀盐酸会有 的现象;也可通过加热的方法鉴别黄金,假黄金加热会 。
三、计算题
19.AgNO3溶液是实验室中的常用试剂。AgNO3的化学性质不稳定,在温度稍高或光照条件下可以发生反应:2AgNO32Ag+2NO2↑+O2↑ (假设气体全部逸出)。现有一瓶100g10%的AgNO3溶液,久置后(不考虑水分挥发),将瓶内物质过滤,得到固体1.08g和若干滤液。试计算:
(1)AgNO3中N和O的质量比为 。
(2)滤液中AgNO3的质量分数(结果精确到0.1%)。
20.过氧化氢消毒液能够杀灭细菌、真菌,包括破伤风杆菌、厌氧菌等,医疗上常用3%的过氧化氢溶液消毒。如图是学校实验室购买的过氧化氢溶液的标签,回答下列问题:
过氧化氢溶液
体积 500 mL
溶质质量分数 30%
有氧化性,接触皮肤后要立即用大量水冲洗
(1)从中取出10 mL,则溶液的溶质质量分数为 。
(2)欲配制溶质质量分数为3%的过氧化氢溶液200 g用于医用消毒,需要这种过氧化氢溶液的质量是多少克 需要加入水的质量为多少克 (写出解题过程)
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.D
2.D
3.C
4.A
5.B
6.C
7.C
8.D
9.C
10.D
11.D
12.C
13.B
14.D
15.(1) > 90g/90克 降温 蒸发结晶
(2) 隔绝氧气 汽油能溶解油污
16.(1)C
(2)②③
(3)B>A=C
(4)降温结晶
(5) A C>A=B
17.(1)<
(2) 不饱和 20%
(3) C和D bc
18.(1) 生铁 钢 含碳量
(2) 大 低 好
(3)船舶和化工等
(4) 产生气泡 变黑
19.(1)7:24
(2)解:设参加反应硝酸银的质量为x,生成二氧化氮的质量为y,生成氧气的质量为z。
x=1.7g y=0.46g z=0.16g
滤液中AgNO3的质量分数=×100%≈8.4%。
答:滤液中AgNO3的质量分数8.4%。
20.(1)30%
(2)解:设要这种过氧化氢溶液的质量为x;
解得x=20g
则需要加入水的质量是:
答:要30%过氧化氢溶液的质量为20g,需要加入水的质量是180g。
答案第1页,共2页
答案第1页,共2页
同课章节目录
