第九单元溶液单元训练题- --2023-2024学年九年级化学人教版下册(含答案)
文档属性
| 名称 | 第九单元溶液单元训练题- --2023-2024学年九年级化学人教版下册(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 923.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-01-03 00:00:00 | ||
图片预览


文档简介
第九单元 溶液 单元训练题
一、选择题
1.硝酸钾和氯化钠的溶解度曲线如图,下列说法正确的是
A.硝酸钾的溶解度比氯化钠的溶解度大
B.硝酸钾中含有少量氯化钠,常用蒸发结晶法提纯硝酸钾
C.60℃时,等质量的硝酸钾和氯化钠分别配成饱和溶液,所需水的质量:硝酸钾<氯化钠
D.将60℃时硝酸钾饱和溶液和氯化钠饱和溶液分别降温至10℃时,所得溶液的溶质质量分数:硝酸钾>氯化钠
2.NaCl和Na2CO3的溶解度曲线如图所示。下列说法正确的是
A.Na2CO3的溶解度比NaCl的溶解度大
B.10℃时,Na2CO3溶液中溶质与溶液的质量比为1∶10
C.20℃时,将120gNa2CO3溶液冷却到10℃可析出固体10g
D.Na2CO3中含有少量NaCl,可溶于适量热水再降温结晶提纯
3.下图为甲、乙两种物质(均不含结晶水)的溶解度曲线,下列说法正确的是( )
A.通过升温可以将甲的不饱和溶液变为饱和溶液
B.10℃时,甲溶液的溶质质量分数小于乙
C.甲、乙的不饱和溶液从30℃降温到20℃时,甲、乙都一定达到饱和
D.把溶质质量分数为10%的乙溶液从30℃降温到10℃其质量分数仍为10%
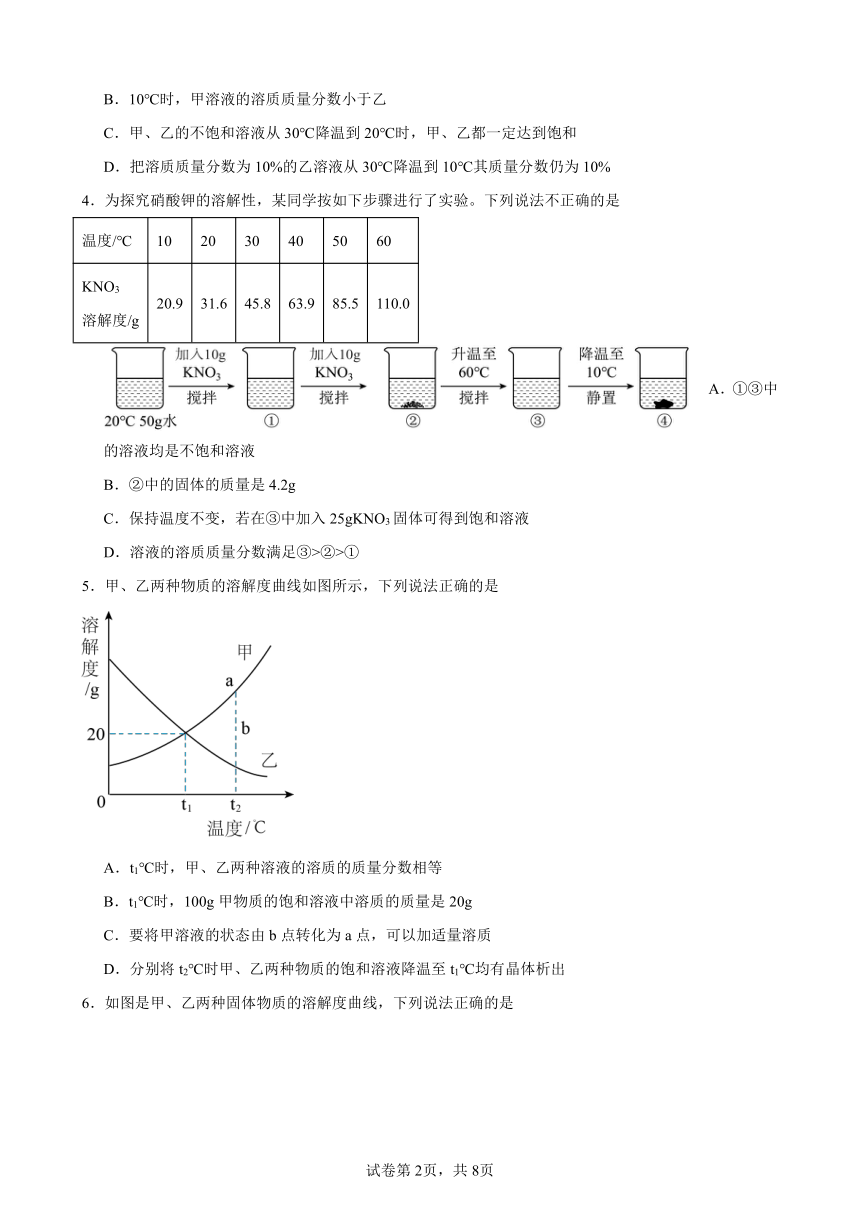
4.为探究硝酸钾的溶解性,某同学按如下步骤进行了实验。下列说法不正确的是
温度/℃ 10 20 30 40 50 60
KNO3 溶解度/g 20.9 31.6 45.8 63.9 85.5 110.0
A.①③中的溶液均是不饱和溶液
B.②中的固体的质量是4.2g
C.保持温度不变,若在③中加入25gKNO3固体可得到饱和溶液
D.溶液的溶质质量分数满足③>②>①
5.甲、乙两种物质的溶解度曲线如图所示,下列说法正确的是
A.t1℃时,甲、乙两种溶液的溶质的质量分数相等
B.t1℃时,100g甲物质的饱和溶液中溶质的质量是20g
C.要将甲溶液的状态由b点转化为a点,可以加适量溶质
D.分别将t2℃时甲、乙两种物质的饱和溶液降温至t1℃均有晶体析出
6.如图是甲、乙两种固体物质的溶解度曲线,下列说法正确的是
A.t1℃时,向50g水中加入20g甲得到70g溶液
B.t2℃时,等质量的甲、乙饱和溶液,溶质质量分数一定相等
C.将t3℃时甲、乙的饱和溶液降温至t1℃,析出晶体的质量甲一定大于乙
D.t3℃时,若将N点的甲溶液转变为M点的甲溶液,可采取增加溶剂的方法
7.下列实验设计不能达到实验目的的是
选项 A B C D
实验设计
实验目的 探究呼出气体与空气中含量的差别 探究溶剂的性质对物质溶解性的影响 探究温度对分子运动快慢的影响 探究可燃物燃烧与温度达到可燃物的着火点有关
A.A B.B C.C D.D
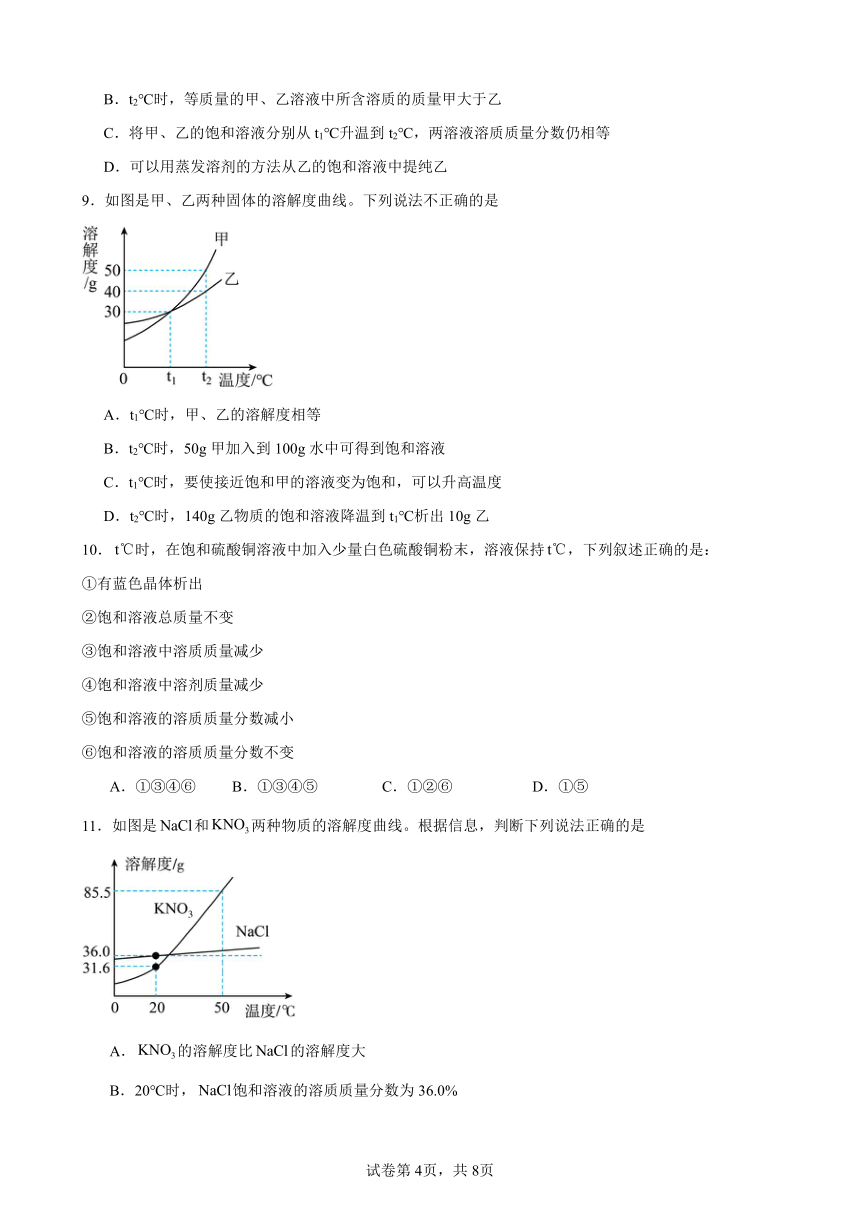
8.如图是甲、乙两种固体物质(均不含结晶水)的溶解度曲线,下列说法错误的是
A.t1℃时,甲乙两种物质的溶解度相等
B.t2℃时,等质量的甲、乙溶液中所含溶质的质量甲大于乙
C.将甲、乙的饱和溶液分别从t1℃升温到t2℃,两溶液溶质质量分数仍相等
D.可以用蒸发溶剂的方法从乙的饱和溶液中提纯乙
9.如图是甲、乙两种固体的溶解度曲线。下列说法不正确的是
A.t1℃时,甲、乙的溶解度相等
B.t2℃时,50g甲加入到100g水中可得到饱和溶液
C.t1℃时,要使接近饱和甲的溶液变为饱和,可以升高温度
D.t2℃时,140g乙物质的饱和溶液降温到t1℃析出10g乙
10.时,在饱和硫酸铜溶液中加入少量白色硫酸铜粉末,溶液保持,下列叙述正确的是:
①有蓝色晶体析出
②饱和溶液总质量不变
③饱和溶液中溶质质量减少
④饱和溶液中溶剂质量减少
⑤饱和溶液的溶质质量分数减小
⑥饱和溶液的溶质质量分数不变
A.①③④⑥ B.①③④⑤ C.①②⑥ D.①⑤
11.如图是和两种物质的溶解度曲线。根据信息,判断下列说法正确的是
A.的溶解度比的溶解度大
B.20℃时,饱和溶液的溶质质量分数为36.0%
C.50℃时,在水中充分溶解,形成饱和溶液
D.分别将50℃的、的饱和溶液降温至20℃,硝酸钾溶液析出的固体多
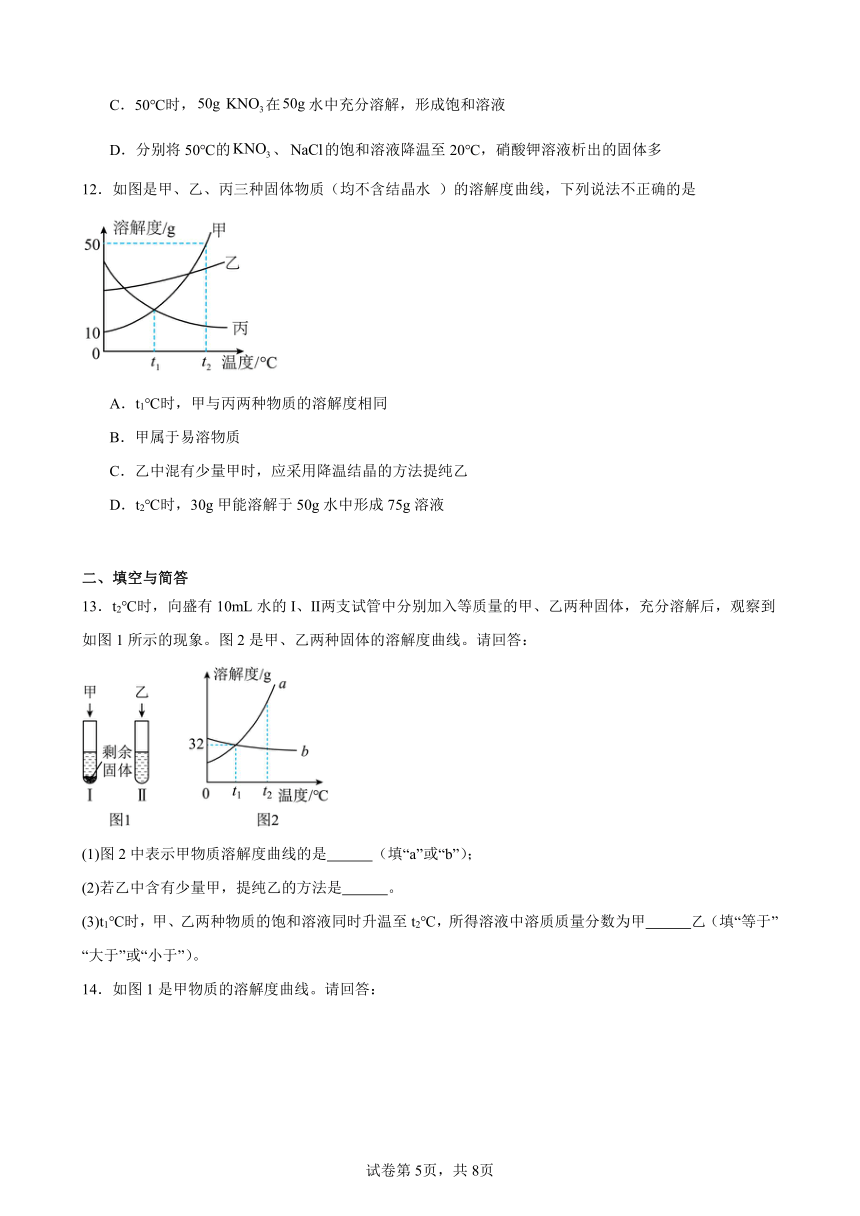
12.如图是甲、乙、丙三种固体物质(均不含结晶水 )的溶解度曲线,下列说法不正确的是
A.t1℃时,甲与丙两种物质的溶解度相同
B.甲属于易溶物质
C.乙中混有少量甲时,应采用降温结晶的方法提纯乙
D.t2℃时,30g甲能溶解于50g水中形成75g溶液
二、填空与简答
13.t2℃时,向盛有10mL水的I、Ⅱ两支试管中分别加入等质量的甲、乙两种固体,充分溶解后,观察到如图1所示的现象。图2是甲、乙两种固体的溶解度曲线。请回答:
(1)图2中表示甲物质溶解度曲线的是 (填“a”或“b”);
(2)若乙中含有少量甲,提纯乙的方法是 。
(3)t1℃时,甲、乙两种物质的饱和溶液同时升温至t2℃,所得溶液中溶质质量分数为甲 乙(填“等于” “大于”或“小于”)。
14.如图1是甲物质的溶解度曲线。请回答:
(1)为使图2试管中饱和甲溶液析出固体,可向烧杯中加入 (填“NH4NO3”或“NaCl”)固体。
(2)60℃时取210g甲溶液进行如下图操作:
①溶液属于 (填“饱和”或“不饱和”)溶液,其溶质质量分数为 。40℃时甲的溶解度为 g。
15.溶液在我们的日常生活和生产中有着广泛的用途。实验室配制一定溶质质量分数的氯化钠溶液的操作示意图如图所示:
(1)在常温下,小明按照图1实验操作配制一定溶质质量分数的甲溶液(甲完全溶解),其正确顺序为 (填序号)。操作③中玻璃棒的作用是 。将配制的甲溶液稀释为溶质质量分数为5%的溶液,需加水的质量是 g。
(2)图2为甲、乙、丙三种固体物质的溶解度曲线,请回答下列问题。
①图中A点的意义是: ;
②0℃时,甲、乙、丙三种固体物质的溶解度从大到小的顺序为 ;
③将t3℃时甲、乙、丙的饱和溶液降温至0℃,下列说法正确的是 。
A.t3℃时。甲、乙、丙的饱和溶液的溶质质量分数由大到小的顺序是甲>乙>丙
B.降温至t2℃时,甲溶液析出晶体的质量大于乙溶液析出晶体的质量
C.降温至t1℃时,甲、丙溶液的溶质质量分数相等
D.在降温过程中,甲、乙、丙三种溶液均为饱和溶液
E.在降温过程中,只有丙溶液的溶质质量分数不变
④图2中B点是用50g水配制成的甲溶液,现需将甲溶液由B点状态依次移至C点状态和A点状态,准确的操作是 。
16.溶液在生活、生产和科学研究中具有广泛的用途。
(1)厨房中有下列物质:①食盐 ②面粉 ③花生油 ④芝麻酱,将它们分别放入适量水中,充分搅拌,能够得到溶液的是 (填序号)。
(2)请根据氯化铵和硫酸钠的溶解度表及溶解度曲线回答下列问题:
温度/℃ 10 20 30 40 50 60
溶解度S/g 33.3 37.2 41.4 45.8 50.41 60.2
9.6 20.2 40.8 48.4 47.5 47.0
①根据上述溶解度表判断图1中硫酸钠的溶解度曲线是 (填“甲”或“乙”)
②20℃时,向80g水中加入20g氯化铵和20g硫酸钠,搅拌,充分溶解后,溶液中溶质氯化铵的质量分数为 (精确至0.1%)。
③下列说法错误的是 (填序号)。
A.将甲、乙的饱和溶液从降温到,溶质的质量分数都变小
B.将甲、乙溶液的d点状态变成c点状态,可加入适量溶质甲、乙或恒温蒸发适量溶剂
C.温度从降到,过滤,可将乙溶液的c点状态变成a点状态
D.将甲、乙溶液的a点状态变成c点状态,所加溶质质量相等
(3)某实验小组进行粗盐提纯并利用制得的精盐配制溶液,请回答下列问题。
①操作I中玻璃棒的作用是 ,操作Ⅱ的名称为 。
②若的产率偏低,则可能的原因是 (写一个即可)。
三、计算题
17.为了测定黄铜(铜、锌合金)的组成,某研究性学习小组称取该样品10g,向其中逐滴加入9.8%的稀硫酸至刚好不再产生气体为止。反应过程中生成的气体与所用硫酸溶液的质量关系如图所示。试计算:
(1)样品中铜的质量分数;
(2)反应后所得溶液质量。
18.工业上用NO生产HNO3过程中的物质转化关系如图所示
(1)HNO3中氮氧元素的质量比 。
(2)反应①中,参加反应的NO与O2的分子数之比为 。
(3)小组同学在老师的指导下,用工业生产的浓硝酸配制100g17%的稀硝酸。
①用68%的浓硝酸配制100g质量分数为17%的稀硝酸,需加水 g。
②将配制好的稀硝酸转移到试剂瓶中,贴上标签,标签上必须注明的是 。
A.100g B.17% C.稀硝酸
(4)已知该流程中总的化学方程式为4NO+3O2 +2H2O=4HNO3
当一氧化氮的转化率(×100%)为60%时,理论上1.0吨一氧化氮与足量氧气和水蒸气反应生成硝酸的总质量是多少吨?(请将计算过程写到答题卡上)
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.C
2.D
3.D
4.C
5.C
6.B
7.A
8.B
9.C
10.A
11.C
12.C
13.(1)b
(2)降温结晶/冷却热饱和溶液
(3)小于
14.(1)NH4NO3
(2) 不饱和 50% 45.8
15.(1) ②⑤①④③ 加快溶解速率 150
(2) t1℃时,甲、丙两物质的溶解度相等 丙>乙>甲 AE/EA t3℃时,加入甲物质,使溶液由B状态移至C状态;将溶液由t3℃降温至t1℃,使溶液由C状态移至A状态,过滤
16.(1)①
(2) 甲 17.2% AD/DA
(3) 搅拌,加速溶解 过滤 溶解时加入的水过少或过滤时有滤液溅出(其他合理即可)
17.(1)解:设生成0.10g氢气,需要参加反应的锌的质量为x,参加反应的硫酸质量为y,
解得x=3.25g
解得y=4.9g
则样品中铜的质量分数为
答:样品中铜的质量分数为67.5%。
(2)反应所消耗的硫酸溶液质量为
则反应后所得溶液质量为3.25g+50g-0.10g=53.15g
答:反应后所得溶液质量为53.15g。
18.(1)14:48/7:24
(2)2:1
(3) 75 BC
(4)解:设理论上1.0吨一氧化氮与足量氧气和水蒸气反应生成硝酸的总质量是x
x=1.26t
答:理论上1.0吨一氧化氮与足量氧气和水蒸气反应生成硝酸的总质量是1.26t。
答案第1页,共2页
答案第1页,共2页
一、选择题
1.硝酸钾和氯化钠的溶解度曲线如图,下列说法正确的是
A.硝酸钾的溶解度比氯化钠的溶解度大
B.硝酸钾中含有少量氯化钠,常用蒸发结晶法提纯硝酸钾
C.60℃时,等质量的硝酸钾和氯化钠分别配成饱和溶液,所需水的质量:硝酸钾<氯化钠
D.将60℃时硝酸钾饱和溶液和氯化钠饱和溶液分别降温至10℃时,所得溶液的溶质质量分数:硝酸钾>氯化钠
2.NaCl和Na2CO3的溶解度曲线如图所示。下列说法正确的是
A.Na2CO3的溶解度比NaCl的溶解度大
B.10℃时,Na2CO3溶液中溶质与溶液的质量比为1∶10
C.20℃时,将120gNa2CO3溶液冷却到10℃可析出固体10g
D.Na2CO3中含有少量NaCl,可溶于适量热水再降温结晶提纯
3.下图为甲、乙两种物质(均不含结晶水)的溶解度曲线,下列说法正确的是( )
A.通过升温可以将甲的不饱和溶液变为饱和溶液
B.10℃时,甲溶液的溶质质量分数小于乙
C.甲、乙的不饱和溶液从30℃降温到20℃时,甲、乙都一定达到饱和
D.把溶质质量分数为10%的乙溶液从30℃降温到10℃其质量分数仍为10%
4.为探究硝酸钾的溶解性,某同学按如下步骤进行了实验。下列说法不正确的是
温度/℃ 10 20 30 40 50 60
KNO3 溶解度/g 20.9 31.6 45.8 63.9 85.5 110.0
A.①③中的溶液均是不饱和溶液
B.②中的固体的质量是4.2g
C.保持温度不变,若在③中加入25gKNO3固体可得到饱和溶液
D.溶液的溶质质量分数满足③>②>①
5.甲、乙两种物质的溶解度曲线如图所示,下列说法正确的是
A.t1℃时,甲、乙两种溶液的溶质的质量分数相等
B.t1℃时,100g甲物质的饱和溶液中溶质的质量是20g
C.要将甲溶液的状态由b点转化为a点,可以加适量溶质
D.分别将t2℃时甲、乙两种物质的饱和溶液降温至t1℃均有晶体析出
6.如图是甲、乙两种固体物质的溶解度曲线,下列说法正确的是
A.t1℃时,向50g水中加入20g甲得到70g溶液
B.t2℃时,等质量的甲、乙饱和溶液,溶质质量分数一定相等
C.将t3℃时甲、乙的饱和溶液降温至t1℃,析出晶体的质量甲一定大于乙
D.t3℃时,若将N点的甲溶液转变为M点的甲溶液,可采取增加溶剂的方法
7.下列实验设计不能达到实验目的的是
选项 A B C D
实验设计
实验目的 探究呼出气体与空气中含量的差别 探究溶剂的性质对物质溶解性的影响 探究温度对分子运动快慢的影响 探究可燃物燃烧与温度达到可燃物的着火点有关
A.A B.B C.C D.D
8.如图是甲、乙两种固体物质(均不含结晶水)的溶解度曲线,下列说法错误的是
A.t1℃时,甲乙两种物质的溶解度相等
B.t2℃时,等质量的甲、乙溶液中所含溶质的质量甲大于乙
C.将甲、乙的饱和溶液分别从t1℃升温到t2℃,两溶液溶质质量分数仍相等
D.可以用蒸发溶剂的方法从乙的饱和溶液中提纯乙
9.如图是甲、乙两种固体的溶解度曲线。下列说法不正确的是
A.t1℃时,甲、乙的溶解度相等
B.t2℃时,50g甲加入到100g水中可得到饱和溶液
C.t1℃时,要使接近饱和甲的溶液变为饱和,可以升高温度
D.t2℃时,140g乙物质的饱和溶液降温到t1℃析出10g乙
10.时,在饱和硫酸铜溶液中加入少量白色硫酸铜粉末,溶液保持,下列叙述正确的是:
①有蓝色晶体析出
②饱和溶液总质量不变
③饱和溶液中溶质质量减少
④饱和溶液中溶剂质量减少
⑤饱和溶液的溶质质量分数减小
⑥饱和溶液的溶质质量分数不变
A.①③④⑥ B.①③④⑤ C.①②⑥ D.①⑤
11.如图是和两种物质的溶解度曲线。根据信息,判断下列说法正确的是
A.的溶解度比的溶解度大
B.20℃时,饱和溶液的溶质质量分数为36.0%
C.50℃时,在水中充分溶解,形成饱和溶液
D.分别将50℃的、的饱和溶液降温至20℃,硝酸钾溶液析出的固体多
12.如图是甲、乙、丙三种固体物质(均不含结晶水 )的溶解度曲线,下列说法不正确的是
A.t1℃时,甲与丙两种物质的溶解度相同
B.甲属于易溶物质
C.乙中混有少量甲时,应采用降温结晶的方法提纯乙
D.t2℃时,30g甲能溶解于50g水中形成75g溶液
二、填空与简答
13.t2℃时,向盛有10mL水的I、Ⅱ两支试管中分别加入等质量的甲、乙两种固体,充分溶解后,观察到如图1所示的现象。图2是甲、乙两种固体的溶解度曲线。请回答:
(1)图2中表示甲物质溶解度曲线的是 (填“a”或“b”);
(2)若乙中含有少量甲,提纯乙的方法是 。
(3)t1℃时,甲、乙两种物质的饱和溶液同时升温至t2℃,所得溶液中溶质质量分数为甲 乙(填“等于” “大于”或“小于”)。
14.如图1是甲物质的溶解度曲线。请回答:
(1)为使图2试管中饱和甲溶液析出固体,可向烧杯中加入 (填“NH4NO3”或“NaCl”)固体。
(2)60℃时取210g甲溶液进行如下图操作:
①溶液属于 (填“饱和”或“不饱和”)溶液,其溶质质量分数为 。40℃时甲的溶解度为 g。
15.溶液在我们的日常生活和生产中有着广泛的用途。实验室配制一定溶质质量分数的氯化钠溶液的操作示意图如图所示:
(1)在常温下,小明按照图1实验操作配制一定溶质质量分数的甲溶液(甲完全溶解),其正确顺序为 (填序号)。操作③中玻璃棒的作用是 。将配制的甲溶液稀释为溶质质量分数为5%的溶液,需加水的质量是 g。
(2)图2为甲、乙、丙三种固体物质的溶解度曲线,请回答下列问题。
①图中A点的意义是: ;
②0℃时,甲、乙、丙三种固体物质的溶解度从大到小的顺序为 ;
③将t3℃时甲、乙、丙的饱和溶液降温至0℃,下列说法正确的是 。
A.t3℃时。甲、乙、丙的饱和溶液的溶质质量分数由大到小的顺序是甲>乙>丙
B.降温至t2℃时,甲溶液析出晶体的质量大于乙溶液析出晶体的质量
C.降温至t1℃时,甲、丙溶液的溶质质量分数相等
D.在降温过程中,甲、乙、丙三种溶液均为饱和溶液
E.在降温过程中,只有丙溶液的溶质质量分数不变
④图2中B点是用50g水配制成的甲溶液,现需将甲溶液由B点状态依次移至C点状态和A点状态,准确的操作是 。
16.溶液在生活、生产和科学研究中具有广泛的用途。
(1)厨房中有下列物质:①食盐 ②面粉 ③花生油 ④芝麻酱,将它们分别放入适量水中,充分搅拌,能够得到溶液的是 (填序号)。
(2)请根据氯化铵和硫酸钠的溶解度表及溶解度曲线回答下列问题:
温度/℃ 10 20 30 40 50 60
溶解度S/g 33.3 37.2 41.4 45.8 50.41 60.2
9.6 20.2 40.8 48.4 47.5 47.0
①根据上述溶解度表判断图1中硫酸钠的溶解度曲线是 (填“甲”或“乙”)
②20℃时,向80g水中加入20g氯化铵和20g硫酸钠,搅拌,充分溶解后,溶液中溶质氯化铵的质量分数为 (精确至0.1%)。
③下列说法错误的是 (填序号)。
A.将甲、乙的饱和溶液从降温到,溶质的质量分数都变小
B.将甲、乙溶液的d点状态变成c点状态,可加入适量溶质甲、乙或恒温蒸发适量溶剂
C.温度从降到,过滤,可将乙溶液的c点状态变成a点状态
D.将甲、乙溶液的a点状态变成c点状态,所加溶质质量相等
(3)某实验小组进行粗盐提纯并利用制得的精盐配制溶液,请回答下列问题。
①操作I中玻璃棒的作用是 ,操作Ⅱ的名称为 。
②若的产率偏低,则可能的原因是 (写一个即可)。
三、计算题
17.为了测定黄铜(铜、锌合金)的组成,某研究性学习小组称取该样品10g,向其中逐滴加入9.8%的稀硫酸至刚好不再产生气体为止。反应过程中生成的气体与所用硫酸溶液的质量关系如图所示。试计算:
(1)样品中铜的质量分数;
(2)反应后所得溶液质量。
18.工业上用NO生产HNO3过程中的物质转化关系如图所示
(1)HNO3中氮氧元素的质量比 。
(2)反应①中,参加反应的NO与O2的分子数之比为 。
(3)小组同学在老师的指导下,用工业生产的浓硝酸配制100g17%的稀硝酸。
①用68%的浓硝酸配制100g质量分数为17%的稀硝酸,需加水 g。
②将配制好的稀硝酸转移到试剂瓶中,贴上标签,标签上必须注明的是 。
A.100g B.17% C.稀硝酸
(4)已知该流程中总的化学方程式为4NO+3O2 +2H2O=4HNO3
当一氧化氮的转化率(×100%)为60%时,理论上1.0吨一氧化氮与足量氧气和水蒸气反应生成硝酸的总质量是多少吨?(请将计算过程写到答题卡上)
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.C
2.D
3.D
4.C
5.C
6.B
7.A
8.B
9.C
10.A
11.C
12.C
13.(1)b
(2)降温结晶/冷却热饱和溶液
(3)小于
14.(1)NH4NO3
(2) 不饱和 50% 45.8
15.(1) ②⑤①④③ 加快溶解速率 150
(2) t1℃时,甲、丙两物质的溶解度相等 丙>乙>甲 AE/EA t3℃时,加入甲物质,使溶液由B状态移至C状态;将溶液由t3℃降温至t1℃,使溶液由C状态移至A状态,过滤
16.(1)①
(2) 甲 17.2% AD/DA
(3) 搅拌,加速溶解 过滤 溶解时加入的水过少或过滤时有滤液溅出(其他合理即可)
17.(1)解:设生成0.10g氢气,需要参加反应的锌的质量为x,参加反应的硫酸质量为y,
解得x=3.25g
解得y=4.9g
则样品中铜的质量分数为
答:样品中铜的质量分数为67.5%。
(2)反应所消耗的硫酸溶液质量为
则反应后所得溶液质量为3.25g+50g-0.10g=53.15g
答:反应后所得溶液质量为53.15g。
18.(1)14:48/7:24
(2)2:1
(3) 75 BC
(4)解:设理论上1.0吨一氧化氮与足量氧气和水蒸气反应生成硝酸的总质量是x
x=1.26t
答:理论上1.0吨一氧化氮与足量氧气和水蒸气反应生成硝酸的总质量是1.26t。
答案第1页,共2页
答案第1页,共2页
同课章节目录
