2.2. 1 活泼的金属单质--钠 (表格式)教学设计 2023-2024学年高一上学期化学人教版(2019)必修第一册
文档属性
| 名称 | 2.2. 1 活泼的金属单质--钠 (表格式)教学设计 2023-2024学年高一上学期化学人教版(2019)必修第一册 |
|
|
| 格式 | docx | ||
| 文件大小 | 38.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-01-03 00:00:00 | ||
图片预览


文档简介
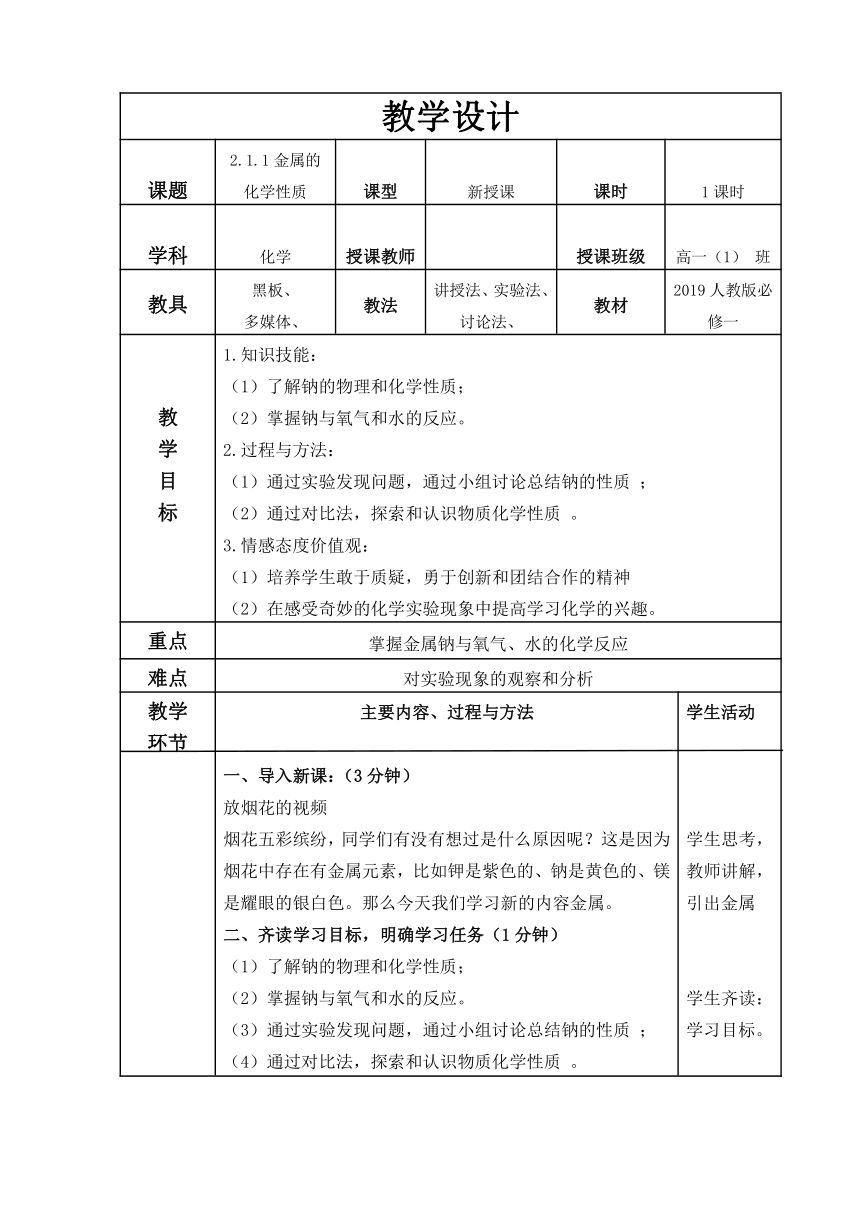
教学设计
课题 2.1.1金属的化学性质 课型 新授课 课时 1课时
学科 化学 授课教师 授课班级 高一(1) 班
教具 黑板、 多媒体、 教法 讲授法、实验法、讨论法、 教材 2019人教版必修一
教 学 目 标 1.知识技能: (1)了解钠的物理和化学性质; (2)掌握钠与氧气和水的反应。 2.过程与方法: (1)通过实验发现问题,通过小组讨论总结钠的性质 ; (2)通过对比法,探索和认识物质化学性质 。 3.情感态度价值观: (1)培养学生敢于质疑,勇于创新和团结合作的精神 (2)在感受奇妙的化学实验现象中提高学习化学的兴趣。
重点 掌握金属钠与氧气、水的化学反应
难点 对实验现象的观察和分析
教学 环节 主要内容、过程与方法 一、导入新课:(3分钟) 放烟花的视频 烟花五彩缤纷,同学们有没有想过是什么原因呢?这是因为烟花中存在有金属元素,比如钾是紫色的、钠是黄色的、镁是耀眼的银白色。那么今天我们学习新的内容金属。 二、齐读学习目标,明确学习任务(1分钟) (1)了解钠的物理和化学性质; (2)掌握钠与氧气和水的反应。 (3)通过实验发现问题,通过小组讨论总结钠的性质 ; (4)通过对比法,探索和认识物质化学性质 。 三、讲授新课(29分钟) (一)回顾旧知识(7分钟) 多媒体上展示图片 同学们思考:金属有哪些共同的物理性质? 学生与教师一起回忆、总结:除汞以外都是有金属光泽的固体、不透明、易导热、易导电,有延展性。 过渡:同学们还记得金属共同的物理性质,那还记得它的化学性质吗? 同学们思考:根据图片上的实验,请同学们回忆金属共同的化学性质并写出相关的化学反应方程式。 请同学们上黑板写出图片上的化学反应方程式 教师点评并简单讲解方程式内容(出现错误,及时纠正) 同时总结金属的化学通性 过渡:同学们都听说过“真金不怕火炼”,这是指黄金,即使在高温下也不与氧气发生反应。而有些金属在空气(或氧气)中剧烈反应,那么接下来我们学习这样的金属----钠 (二)讲授新课(22分钟) 一、金属与非金属 实验一: (1)用镊子从煤油中取出钠后用滤纸吸干煤油,用小刀切割钠,立即观察钠断面的颜色。 (2)一段时间后观察钠断面的颜色变化。 多媒体上给出相关的图片,请同学们观察实验现象并回答问题 请同学们根据实验一,归纳总结金属钠的物理性质,以及金属钠变暗的原因(用方程式表示) 1.钠的物理性质 色态:银白色固体 硬度:小 密度:大于煤油小于水 导电性、导热性 钠的化学性质 与氧气反应 常温下:4Na+O2==2Na2O 过渡:金属钠常温下在生成氧化钠,那么加热会生成什么呢?请同学们观察实验二,归纳总结。 实验二: 将一小块金属钠放在坩埚里,加热,有什么现象? 实验现象:钠受热后,与氧气剧烈反应,火焰呈黄色,生成的固体呈淡黄色。 加热时:2Na+O2==Na2O2(淡黄色) 过渡:金属钠太活泼了,位于元素周期表的三位,它不仅能与氧气反应,也能与水发生剧烈的反应,请同学们观看实验视频。 实验三: 1、在水中滴入酚酞试液 2、将一小块钠用滤纸吸干煤油后投入水中,观察现象 同学们注意观察现象:① 浮还是沉?② 钠的状态 ③ 运动还是静止?④ 有无声响?⑤ 溶液颜色变化? 小组讨论:根据实验中的现象,分组合作,讨论现象出现的原因,给大家4分钟的时间。 提问小组讨论结果:浮----比水的密度小 熔----反应放热、熔点低 游----反应剧烈、气体生成 响----有气体生成 红----有NaOH生成(滴加酚酞) 提问:金属钠溶于水中,发生了什么反应? 与水反应 2Na+2H2O==2NaOH+H2↑ 拓展思考:将Na投入CuSO4溶液中将会看到什么现象?生成物是什么?请根据所学知识写出其反应方程式。 现象:Na浮在液面上,熔化成小球,四处游动,发出“嘶嘶” 的响声,最后消失,同时生成蓝色絮状沉淀。 2Na+2H2O==2NaOH+H2↑ 四、课堂小结(2分钟) 1.钠的物理性质 2钠的化学性质 (1)与氧气反应 (2)与水反应 五、巩固练习(4分钟) PPT练习题 六、作业(1分钟) 将Na投入FeCl3溶液中将会看到什么现象? 生成物是什么? 请根据所学知识写出其反应方程式。 3.1金属的化学性质 一、金属与非金属的反应 1.钠的物理性质:银白色固体、质软、硬度小、密度比水小、 有导电性、导热性 2.钠的化学性质 (1)与氧气反应 4Na+O2==2Na2O 2Na+O2==Na2O2(淡黄色) (2)与水反应 2Na+2H2O==2NaOH+H2↑ 现象:浮、熔、游、响、红 学生活动 学生思考,教师讲解,引出金属 学生齐读:学习目标。 学生思考问题并回答,教师讲解相关性质 学生上黑板写出化学反应方程式,出现错误的地方及时纠正 学生们观看实验一的图片,归纳总结,金属钠的物理性质以及金属钠变暗的原因(用反应方程式你表示) 请同学们观察实验二图片,思考此时生成了什么? 观看实验三视频进行小组讨论。 小组代表回答问题 学生继续思考,此时金属钠与水反应生成了什么?方程式如何书写? 如果钠投入硫酸铜溶液中,有什么现象?为什么? 学生与教师一起进行小结 学生做题,教师讲解
课题 2.1.1金属的化学性质 课型 新授课 课时 1课时
学科 化学 授课教师 授课班级 高一(1) 班
教具 黑板、 多媒体、 教法 讲授法、实验法、讨论法、 教材 2019人教版必修一
教 学 目 标 1.知识技能: (1)了解钠的物理和化学性质; (2)掌握钠与氧气和水的反应。 2.过程与方法: (1)通过实验发现问题,通过小组讨论总结钠的性质 ; (2)通过对比法,探索和认识物质化学性质 。 3.情感态度价值观: (1)培养学生敢于质疑,勇于创新和团结合作的精神 (2)在感受奇妙的化学实验现象中提高学习化学的兴趣。
重点 掌握金属钠与氧气、水的化学反应
难点 对实验现象的观察和分析
教学 环节 主要内容、过程与方法 一、导入新课:(3分钟) 放烟花的视频 烟花五彩缤纷,同学们有没有想过是什么原因呢?这是因为烟花中存在有金属元素,比如钾是紫色的、钠是黄色的、镁是耀眼的银白色。那么今天我们学习新的内容金属。 二、齐读学习目标,明确学习任务(1分钟) (1)了解钠的物理和化学性质; (2)掌握钠与氧气和水的反应。 (3)通过实验发现问题,通过小组讨论总结钠的性质 ; (4)通过对比法,探索和认识物质化学性质 。 三、讲授新课(29分钟) (一)回顾旧知识(7分钟) 多媒体上展示图片 同学们思考:金属有哪些共同的物理性质? 学生与教师一起回忆、总结:除汞以外都是有金属光泽的固体、不透明、易导热、易导电,有延展性。 过渡:同学们还记得金属共同的物理性质,那还记得它的化学性质吗? 同学们思考:根据图片上的实验,请同学们回忆金属共同的化学性质并写出相关的化学反应方程式。 请同学们上黑板写出图片上的化学反应方程式 教师点评并简单讲解方程式内容(出现错误,及时纠正) 同时总结金属的化学通性 过渡:同学们都听说过“真金不怕火炼”,这是指黄金,即使在高温下也不与氧气发生反应。而有些金属在空气(或氧气)中剧烈反应,那么接下来我们学习这样的金属----钠 (二)讲授新课(22分钟) 一、金属与非金属 实验一: (1)用镊子从煤油中取出钠后用滤纸吸干煤油,用小刀切割钠,立即观察钠断面的颜色。 (2)一段时间后观察钠断面的颜色变化。 多媒体上给出相关的图片,请同学们观察实验现象并回答问题 请同学们根据实验一,归纳总结金属钠的物理性质,以及金属钠变暗的原因(用方程式表示) 1.钠的物理性质 色态:银白色固体 硬度:小 密度:大于煤油小于水 导电性、导热性 钠的化学性质 与氧气反应 常温下:4Na+O2==2Na2O 过渡:金属钠常温下在生成氧化钠,那么加热会生成什么呢?请同学们观察实验二,归纳总结。 实验二: 将一小块金属钠放在坩埚里,加热,有什么现象? 实验现象:钠受热后,与氧气剧烈反应,火焰呈黄色,生成的固体呈淡黄色。 加热时:2Na+O2==Na2O2(淡黄色) 过渡:金属钠太活泼了,位于元素周期表的三位,它不仅能与氧气反应,也能与水发生剧烈的反应,请同学们观看实验视频。 实验三: 1、在水中滴入酚酞试液 2、将一小块钠用滤纸吸干煤油后投入水中,观察现象 同学们注意观察现象:① 浮还是沉?② 钠的状态 ③ 运动还是静止?④ 有无声响?⑤ 溶液颜色变化? 小组讨论:根据实验中的现象,分组合作,讨论现象出现的原因,给大家4分钟的时间。 提问小组讨论结果:浮----比水的密度小 熔----反应放热、熔点低 游----反应剧烈、气体生成 响----有气体生成 红----有NaOH生成(滴加酚酞) 提问:金属钠溶于水中,发生了什么反应? 与水反应 2Na+2H2O==2NaOH+H2↑ 拓展思考:将Na投入CuSO4溶液中将会看到什么现象?生成物是什么?请根据所学知识写出其反应方程式。 现象:Na浮在液面上,熔化成小球,四处游动,发出“嘶嘶” 的响声,最后消失,同时生成蓝色絮状沉淀。 2Na+2H2O==2NaOH+H2↑ 四、课堂小结(2分钟) 1.钠的物理性质 2钠的化学性质 (1)与氧气反应 (2)与水反应 五、巩固练习(4分钟) PPT练习题 六、作业(1分钟) 将Na投入FeCl3溶液中将会看到什么现象? 生成物是什么? 请根据所学知识写出其反应方程式。 3.1金属的化学性质 一、金属与非金属的反应 1.钠的物理性质:银白色固体、质软、硬度小、密度比水小、 有导电性、导热性 2.钠的化学性质 (1)与氧气反应 4Na+O2==2Na2O 2Na+O2==Na2O2(淡黄色) (2)与水反应 2Na+2H2O==2NaOH+H2↑ 现象:浮、熔、游、响、红 学生活动 学生思考,教师讲解,引出金属 学生齐读:学习目标。 学生思考问题并回答,教师讲解相关性质 学生上黑板写出化学反应方程式,出现错误的地方及时纠正 学生们观看实验一的图片,归纳总结,金属钠的物理性质以及金属钠变暗的原因(用反应方程式你表示) 请同学们观察实验二图片,思考此时生成了什么? 观看实验三视频进行小组讨论。 小组代表回答问题 学生继续思考,此时金属钠与水反应生成了什么?方程式如何书写? 如果钠投入硫酸铜溶液中,有什么现象?为什么? 学生与教师一起进行小结 学生做题,教师讲解
