湖南省株洲市重点中学2023-2024学年高一上学期期中考试化学试题(含答案)
文档属性
| 名称 | 湖南省株洲市重点中学2023-2024学年高一上学期期中考试化学试题(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 383.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-01-03 00:00:00 | ||
图片预览


文档简介
株洲市二中2023年下学期高一年级期中考试试卷
化学试题
时量:60分钟分值:100分
可能用到的相对原子质量:H~1 He~4 C~12 N~14 O~16 S~32 Ca~40 Cu~64
一、选择题(本题包括18小题,每小题3分,共54分。在每小题给出的四个选项中,只有一项是符合题目要求的)
1.“月光如流水一般,静静地泻在这一片叶子和花上。薄薄的青雾浮起在荷塘里。叶子和花仿佛在牛乳中洗过一样;又像笼着轻纱的梦。”——朱自清《荷塘月色》。月光穿过薄雾形成的缕缕光束主要是因为( )
A.分子的运动 B.丁达尔效应 C.作者在梦境 D.荷叶上露珠的反光
2.化学实验中具有安全意识是重要的科学素养。下列实验操作不正确的是( )
A.大量氯气泄漏时,迅速离开现场并尽量顺风往低处跑
B.金属钠着火时,立即用干燥的沙土覆盖
C.不慎洒出的酒精在桌上着火时,立即用湿毛巾盖灭
D.闻氯气时,用手在瓶口轻轻扇动,使极少量的氯气飘进鼻孔
3.化学与生活密切相关,下列物质与其用途不符合的是( )
A B C D
物质 NaCl Na2CO3 Na2O2 NaClO
用途 做调味品 做膨松剂 做供氧剂 做消毒剂
A.A B.B C.C D.D
4.下列各组均为两种化合物溶于水时电离出的离子,其中由酸电离的是( )
A.、、 B.、、
C.、、 D.、、
5.符合如图中阴影部分的物质是( )
A. B. C. D.NaCl
6.碱溶液中都含有,因此不同的碱表现出一些共同的性质。下列关于性质的描述中,不属于碱的共同性质的是( )
A.能与CO2反应生成水 B.能与盐酸反应生成水
C.能使酚酞溶液变红色 D.能与Na2CO3溶液反应生成CaCO3沉淀
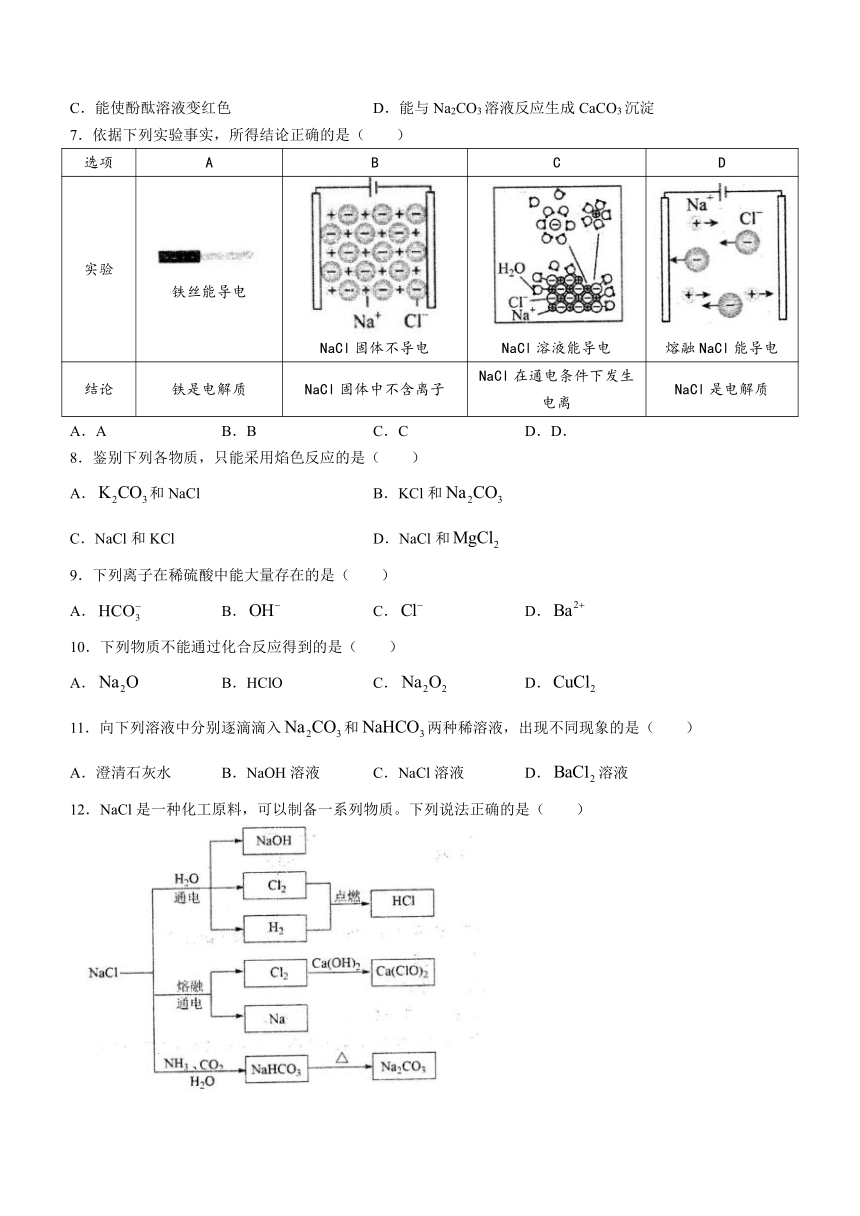
7.依据下列实验事实,所得结论正确的是( )
选项 A B C D
实验 铁丝能导电 NaCl固体不导电 NaCl溶液能导电 熔融NaCl能导电
结论 铁是电解质 NaCl固体中不含离子 NaCl在通电条件下发生电离 NaCl是电解质
A.A B.B C.C D.D.
8.鉴别下列各物质,只能采用焰色反应的是( )
A.和NaCl B.KCl和
C.NaCl和KCl D.NaCl和
9.下列离子在稀硫酸中能大量存在的是( )
A. B. C. D.
10.下列物质不能通过化合反应得到的是( )
A. B.HClO C. D.
11.向下列溶液中分别逐滴滴入和两种稀溶液,出现不同现象的是( )
A.澄清石灰水 B.NaOH溶液 C.NaCl溶液 D.溶液
12.NaCl是一种化工原料,可以制备一系列物质。下列说法正确的是( )
A.25℃,在水中的溶解度比的大
B.石灰乳与的反应中,既是氧化剂,又是还原剂
C.常温下干燥的能用钢瓶贮存,所以不与铁反应
D.图中所示转化反应都是氧化还原反应
13.科学家开发出一种低成本光伏材料—蜂窝状石墨烯。生产原理是:(石墨烯)下列说法错误的是( )
A.该反应中氧化剂与还原剂的质量之比为1:1
B.和都属于电解质
C.是氧化剂,属于碱性氧化物
D.石墨烯是还原产物
14.若1gCO2中含有x个原子,则阿伏加德罗常数可表示为( )
A. B. C. D.
15.在2L 0.5mol/LH2SO4溶液中,下列数据正确的是( )
A.的数目为 B.S原子的物质的量为1mol
C. D.0原子的摩尔质量为16g
16.下列描述对应的离子方程式书写正确的是( )
A.小苏打可用于治疗胃酸过多:
B.NaCl溶液与硝酸银溶液混合:
C.溶于水:
D.软锰矿与浓盐酸反应制氯气:(浓)
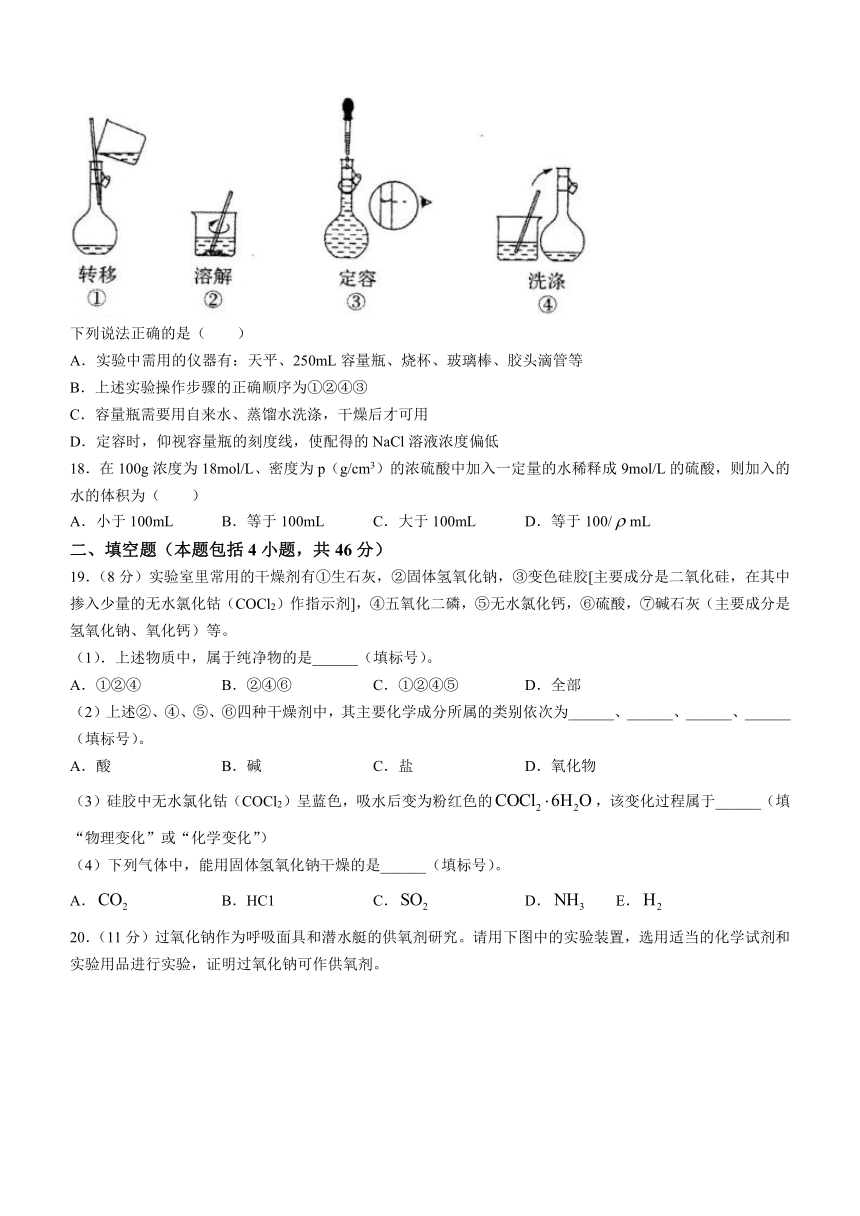
17.配制500 mL 0.100 的NaCl溶液,部分实验操作示意图如下:
下列说法正确的是( )
A.实验中需用的仪器有:天平、250mL容量瓶、烧杯、玻璃棒、胶头滴管等
B.上述实验操作步骤的正确顺序为①②④③
C.容量瓶需要用自来水、蒸馏水洗涤,干燥后才可用
D.定容时,仰视容量瓶的刻度线,使配得的NaCl溶液浓度偏低
18.在100g浓度为18mol/L、密度为p(g/cm3)的浓硫酸中加入一定量的水稀释成9mol/L的硫酸,则加入的水的体积为( )
A.小于100mL B.等于100mL C.大于100mL D.等于100/mL
二、填空题(本题包括4小题,共46分)
19.(8分)实验室里常用的干燥剂有①生石灰,②固体氢氧化钠,③变色硅胶[主要成分是二氧化硅,在其中掺入少量的无水氯化钴(COCl2)作指示剂],④五氧化二磷,⑤无水氯化钙,⑥硫酸,⑦碱石灰(主要成分是氢氧化钠、氧化钙)等。
(1).上述物质中,属于纯净物的是______(填标号)。
A.①②④ B.②④⑥ C.①②④⑤ D.全部
(2)上述②、④、⑤、⑥四种干燥剂中,其主要化学成分所属的类别依次为______、______、______、______(填标号)。
A.酸 B.碱 C.盐 D.氧化物
(3)硅胶中无水氯化钴(COCl2)呈蓝色,吸水后变为粉红色的,该变化过程属于______(填“物理变化”或“化学变化”)
(4)下列气体中,能用固体氢氧化钠干燥的是______(填标号)。
A. B.HC1 C. D. E.
20.(11分)过氧化钠作为呼吸面具和潜水艇的供氧剂研究。请用下图中的实验装置,选用适当的化学试剂和实验用品进行实验,证明过氧化钠可作供氧剂。
A是制取CO2的装置。
(1)B中加入的试剂,下列合理的是______(填序号)。
A.NaOH溶液 B.饱和食盐水 C.溶液 D.饱和溶液
(2)C中加入的试剂是______(填化学式),其中发生的化学反应有______。
(3)D中加入的试剂是______,其目的是______。
21.(14分)研究氯气的水溶液。某同学将黄绿色的氯水密闭放置一段时间后,发现氯水的颜色变浅。
【提出猜想】
(1)甲同学猜测是氯气与水发生反应生成了新物质。画出了如下微观示意图。请在下图中画出产物2的微观示意图。
【实验验证】
甲同学依据猜想,进行了如下3个实验,请将实验报告补充完整。
序号 实验操作 实验现象 实验结论
实验1 向氯水中加入硝酸酸化的硝酸银溶液 ______。 氯水中存在。
实验2 向氯水中加入打磨过的镁条 镁条表面明显有气泡产生 氯水中存在______。
实验3 向氯水中滴加紫色石蕊溶液 溶液颜色很快褪去,最终混合液呈很浅的黄色。 氯水中存在具有漂白性的物质。
(2)实验1中的实验现象是______。
(3)实验2中的实验结论是氯水中存在______。
【提出新问题】
(4)实验3中溶液颜色褪去的原因是什么?甲同学分析氯水的成分,认为不可能是氯水中的HC1或H2O导致的,判断可能是______导致,或氯气与水反应的另一产物导致。
【设计实验】
(5)甲同学设计了如下装置并实施实验。(气体发生装置及尾气处理装置略)。观察到B中的有色布条不褪色,而C中的有色布条褪色。
由此得出结论:___________________________。
【解释分析】
(6)氯气与水发生了反应,其中产物______(填化学式)具有漂白性。
【实验思考】
(7)氯气有毒。上述实验中,尾气可用稍过量溶液吸收,也生成具有漂白性的强氧化性盐。写出生成该盐的离子方程式:______________________。
22.(13分)化学应用分析。
(1)火药是中国的四大发明之一。黑火药在发生爆炸时,发生如下反应:
。其中氧化剂的是______(填化学式)。
(2)中国古代著作中有“银针验毒”的记录,其原理为:
,则X的化学式是______,其中H2S在该反应中______(填标号)。
A.作氧化剂 B.作还原剂
C.既是氧化剂又是还原剂 D.既不是氧化剂又不是还原剂
(3)波尔多液是一种保护性杀菌剂,因首先在法国波尔多大量使用而得名。某化学课外小组按照以下流程制备了波尔多液。
i.将铜屑放入稀硫酸中,加热并不断鼓入空气,在氧气作用下便生成硫酸铜,蒸发浓缩结晶即可以得到胆矾。写出生成硫酸铜的化学方程式_____________________。
ii.将胆矾与生石灰、水按质量比依次为1:0.56:100混合配制成无机铜杀菌剂波尔多液。
①此波尔多液中离子和离子的物质的量比为______(最简整数比)。
②波尔多液有效成分的化学式可表示为,
此种配比中,当时,则y=______。
化学参考答案
1.D 7.A 13.A
2.A 8.C 14.B
3.C 9.D 15.C
4.C 10.A 16.B
5.D 11.D 17.D
6.C 12.B 18.B
19.
(1)
(2)第二周期第VA族
(3)
(4)
(5)弱于
(6)CH4
(7)(高温)
20.(1)SiO2(2)漏斗 玻璃棒 KSCN溶液
(3)①1 14 8 15 2 16H+
②③5:3
(4)
21.(1)分液漏斗
(2)使沉淀与氧气充分接触
(3)
(4)
(5)瓶内空气中、溶液中O2含量均降低,沉淀颜色改变
(6)防止FeSO4溶液氧化;制备过程中防止与氧气接触(7)AC
化学试题
时量:60分钟分值:100分
可能用到的相对原子质量:H~1 He~4 C~12 N~14 O~16 S~32 Ca~40 Cu~64
一、选择题(本题包括18小题,每小题3分,共54分。在每小题给出的四个选项中,只有一项是符合题目要求的)
1.“月光如流水一般,静静地泻在这一片叶子和花上。薄薄的青雾浮起在荷塘里。叶子和花仿佛在牛乳中洗过一样;又像笼着轻纱的梦。”——朱自清《荷塘月色》。月光穿过薄雾形成的缕缕光束主要是因为( )
A.分子的运动 B.丁达尔效应 C.作者在梦境 D.荷叶上露珠的反光
2.化学实验中具有安全意识是重要的科学素养。下列实验操作不正确的是( )
A.大量氯气泄漏时,迅速离开现场并尽量顺风往低处跑
B.金属钠着火时,立即用干燥的沙土覆盖
C.不慎洒出的酒精在桌上着火时,立即用湿毛巾盖灭
D.闻氯气时,用手在瓶口轻轻扇动,使极少量的氯气飘进鼻孔
3.化学与生活密切相关,下列物质与其用途不符合的是( )
A B C D
物质 NaCl Na2CO3 Na2O2 NaClO
用途 做调味品 做膨松剂 做供氧剂 做消毒剂
A.A B.B C.C D.D
4.下列各组均为两种化合物溶于水时电离出的离子,其中由酸电离的是( )
A.、、 B.、、
C.、、 D.、、
5.符合如图中阴影部分的物质是( )
A. B. C. D.NaCl
6.碱溶液中都含有,因此不同的碱表现出一些共同的性质。下列关于性质的描述中,不属于碱的共同性质的是( )
A.能与CO2反应生成水 B.能与盐酸反应生成水
C.能使酚酞溶液变红色 D.能与Na2CO3溶液反应生成CaCO3沉淀
7.依据下列实验事实,所得结论正确的是( )
选项 A B C D
实验 铁丝能导电 NaCl固体不导电 NaCl溶液能导电 熔融NaCl能导电
结论 铁是电解质 NaCl固体中不含离子 NaCl在通电条件下发生电离 NaCl是电解质
A.A B.B C.C D.D.
8.鉴别下列各物质,只能采用焰色反应的是( )
A.和NaCl B.KCl和
C.NaCl和KCl D.NaCl和
9.下列离子在稀硫酸中能大量存在的是( )
A. B. C. D.
10.下列物质不能通过化合反应得到的是( )
A. B.HClO C. D.
11.向下列溶液中分别逐滴滴入和两种稀溶液,出现不同现象的是( )
A.澄清石灰水 B.NaOH溶液 C.NaCl溶液 D.溶液
12.NaCl是一种化工原料,可以制备一系列物质。下列说法正确的是( )
A.25℃,在水中的溶解度比的大
B.石灰乳与的反应中,既是氧化剂,又是还原剂
C.常温下干燥的能用钢瓶贮存,所以不与铁反应
D.图中所示转化反应都是氧化还原反应
13.科学家开发出一种低成本光伏材料—蜂窝状石墨烯。生产原理是:(石墨烯)下列说法错误的是( )
A.该反应中氧化剂与还原剂的质量之比为1:1
B.和都属于电解质
C.是氧化剂,属于碱性氧化物
D.石墨烯是还原产物
14.若1gCO2中含有x个原子,则阿伏加德罗常数可表示为( )
A. B. C. D.
15.在2L 0.5mol/LH2SO4溶液中,下列数据正确的是( )
A.的数目为 B.S原子的物质的量为1mol
C. D.0原子的摩尔质量为16g
16.下列描述对应的离子方程式书写正确的是( )
A.小苏打可用于治疗胃酸过多:
B.NaCl溶液与硝酸银溶液混合:
C.溶于水:
D.软锰矿与浓盐酸反应制氯气:(浓)
17.配制500 mL 0.100 的NaCl溶液,部分实验操作示意图如下:
下列说法正确的是( )
A.实验中需用的仪器有:天平、250mL容量瓶、烧杯、玻璃棒、胶头滴管等
B.上述实验操作步骤的正确顺序为①②④③
C.容量瓶需要用自来水、蒸馏水洗涤,干燥后才可用
D.定容时,仰视容量瓶的刻度线,使配得的NaCl溶液浓度偏低
18.在100g浓度为18mol/L、密度为p(g/cm3)的浓硫酸中加入一定量的水稀释成9mol/L的硫酸,则加入的水的体积为( )
A.小于100mL B.等于100mL C.大于100mL D.等于100/mL
二、填空题(本题包括4小题,共46分)
19.(8分)实验室里常用的干燥剂有①生石灰,②固体氢氧化钠,③变色硅胶[主要成分是二氧化硅,在其中掺入少量的无水氯化钴(COCl2)作指示剂],④五氧化二磷,⑤无水氯化钙,⑥硫酸,⑦碱石灰(主要成分是氢氧化钠、氧化钙)等。
(1).上述物质中,属于纯净物的是______(填标号)。
A.①②④ B.②④⑥ C.①②④⑤ D.全部
(2)上述②、④、⑤、⑥四种干燥剂中,其主要化学成分所属的类别依次为______、______、______、______(填标号)。
A.酸 B.碱 C.盐 D.氧化物
(3)硅胶中无水氯化钴(COCl2)呈蓝色,吸水后变为粉红色的,该变化过程属于______(填“物理变化”或“化学变化”)
(4)下列气体中,能用固体氢氧化钠干燥的是______(填标号)。
A. B.HC1 C. D. E.
20.(11分)过氧化钠作为呼吸面具和潜水艇的供氧剂研究。请用下图中的实验装置,选用适当的化学试剂和实验用品进行实验,证明过氧化钠可作供氧剂。
A是制取CO2的装置。
(1)B中加入的试剂,下列合理的是______(填序号)。
A.NaOH溶液 B.饱和食盐水 C.溶液 D.饱和溶液
(2)C中加入的试剂是______(填化学式),其中发生的化学反应有______。
(3)D中加入的试剂是______,其目的是______。
21.(14分)研究氯气的水溶液。某同学将黄绿色的氯水密闭放置一段时间后,发现氯水的颜色变浅。
【提出猜想】
(1)甲同学猜测是氯气与水发生反应生成了新物质。画出了如下微观示意图。请在下图中画出产物2的微观示意图。
【实验验证】
甲同学依据猜想,进行了如下3个实验,请将实验报告补充完整。
序号 实验操作 实验现象 实验结论
实验1 向氯水中加入硝酸酸化的硝酸银溶液 ______。 氯水中存在。
实验2 向氯水中加入打磨过的镁条 镁条表面明显有气泡产生 氯水中存在______。
实验3 向氯水中滴加紫色石蕊溶液 溶液颜色很快褪去,最终混合液呈很浅的黄色。 氯水中存在具有漂白性的物质。
(2)实验1中的实验现象是______。
(3)实验2中的实验结论是氯水中存在______。
【提出新问题】
(4)实验3中溶液颜色褪去的原因是什么?甲同学分析氯水的成分,认为不可能是氯水中的HC1或H2O导致的,判断可能是______导致,或氯气与水反应的另一产物导致。
【设计实验】
(5)甲同学设计了如下装置并实施实验。(气体发生装置及尾气处理装置略)。观察到B中的有色布条不褪色,而C中的有色布条褪色。
由此得出结论:___________________________。
【解释分析】
(6)氯气与水发生了反应,其中产物______(填化学式)具有漂白性。
【实验思考】
(7)氯气有毒。上述实验中,尾气可用稍过量溶液吸收,也生成具有漂白性的强氧化性盐。写出生成该盐的离子方程式:______________________。
22.(13分)化学应用分析。
(1)火药是中国的四大发明之一。黑火药在发生爆炸时,发生如下反应:
。其中氧化剂的是______(填化学式)。
(2)中国古代著作中有“银针验毒”的记录,其原理为:
,则X的化学式是______,其中H2S在该反应中______(填标号)。
A.作氧化剂 B.作还原剂
C.既是氧化剂又是还原剂 D.既不是氧化剂又不是还原剂
(3)波尔多液是一种保护性杀菌剂,因首先在法国波尔多大量使用而得名。某化学课外小组按照以下流程制备了波尔多液。
i.将铜屑放入稀硫酸中,加热并不断鼓入空气,在氧气作用下便生成硫酸铜,蒸发浓缩结晶即可以得到胆矾。写出生成硫酸铜的化学方程式_____________________。
ii.将胆矾与生石灰、水按质量比依次为1:0.56:100混合配制成无机铜杀菌剂波尔多液。
①此波尔多液中离子和离子的物质的量比为______(最简整数比)。
②波尔多液有效成分的化学式可表示为,
此种配比中,当时,则y=______。
化学参考答案
1.D 7.A 13.A
2.A 8.C 14.B
3.C 9.D 15.C
4.C 10.A 16.B
5.D 11.D 17.D
6.C 12.B 18.B
19.
(1)
(2)第二周期第VA族
(3)
(4)
(5)弱于
(6)CH4
(7)(高温)
20.(1)SiO2(2)漏斗 玻璃棒 KSCN溶液
(3)①1 14 8 15 2 16H+
②③5:3
(4)
21.(1)分液漏斗
(2)使沉淀与氧气充分接触
(3)
(4)
(5)瓶内空气中、溶液中O2含量均降低,沉淀颜色改变
(6)防止FeSO4溶液氧化;制备过程中防止与氧气接触(7)AC
同课章节目录
